Professional Documents
Culture Documents
Bab IV Hasil Dan Pembahasan Viskositas
Uploaded by
Ferah FranciskaCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Bab IV Hasil Dan Pembahasan Viskositas
Uploaded by
Ferah FranciskaCopyright:
Available Formats
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Percobaan
Tabel 4.1 Data Hasil Percobaan
Sampel
Konsentrasi
(%)
Suhu
(
o
C)
Massa
Jenis
(gr/ml)
Viskositas
Teori
(cP)
Viskositas
Praktek
(cP)
Persen
Ralat
(%)
Aquadest 100
15 0,98 1,141 - -
30 0,96 0,836 - -
60 0,96 0,549 - -
Aseton
20
15 0,95 2,200 1,646 25
30 0,96 1,717 1,012 41
60 0,95 0,900 0,589 34
40
15 0,90 1,400 1,597 14
30 0,91 1,140 1,014 11
60 0,91 0,700 0,596 14
Kecap
Kental
Manis
(ABC)
20
15 1,094 - 1,7 -
30 1,0784 - 1,174 -
60 1,0784 - 0,683 -
40
15 1,24 - 2,344 -
30 1,1532 - 1,438 -
60 1,1536 - 0,839 -
4.2 Pembahasan
4.2.1 Pengaruh Temperatur Terhadap Viskositas
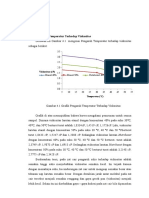
Gambar 4.1 Grafik Pengaruh Temperatur Terhadap Viskositas
Grafik di atas menunjukkan bahwa kurva menunjukan penurunan
untuk semua sampel. Viskositas aseton 20% pada suhu 15
o
C, 30
o
C dan 60
o
C adalah 1,18 cP, 1,07 cP dan 0,85 cP. Viskositas aseton 40% pada suhu 15
o
C, 30
o
C dan 60
o
C adalah 1,27 cP, 1,23 cP dan 1,15 cP. Viskositas kecap
kental manis (ABC) 20% pada suhu 15
o
C, 30
o
C dan 60
o
C adalah 1,94 cP,
1,86 cP dan 1,72 cP. Viskositas kecap kental manis (ABC) 40% pada suhu 15
o
C, 30
o
C dan 60
o
C adalah 3,77 cP, 3,69 cP dan 3,52 cP.
Berdasarkan teori, viskositas dari suatu cairan akan menurun dengan
meningkatnya temperatur. Hal ini disebabkan karena adanyagerakan partikel-
partikel cairan yang semakin cepat apabila suhuditingkatkan dan menurun
kekentalannya (Citra, 2009).
Secara matematis ditulis sebagai berikut
q
P V = n R T
0
0.5
1
1.5
2
2.5
3
3.5
4
15 30 60 75
V
i
s
k
o
s
i
t
a
s
(
c
P
)
Temperatur (
o
C)
Aseton 20%
Aseton 40%
Kecap Kental Manis
(ABC) 20%
Kecap Kental Manis
(ABC) 40%
=
P r
4
t
8 V l
q
dimana: t = waktu T = temperatur
q = viskositas R = konstanta gas
V = volume l = panjang pipa
= konstanta n = mol
(Yazid, 2005).
Maka dari grafik diatas dapat disimpulkan hasil percobaan untuk
semua sampel sesuai dengan teori yang menyatakan bahwa viskositas
berbanding terbalik dengan temperatur.
4.2.2 Pengaruh Konsentrasi Terhadap Viskositas
Gambar 4.2 Grafik Pengaruh Konsentrasi Terhadap Viskositas
Grafik di atas menunjukkan bahwa kurva menunjukkan penurunan
untuk aseton 30
o
C, 60
o
C, dan kecap kental manis (ABC) 15
o
C, 30
o
C, 60
o
C
sedangkan mengalami kenaikan untuk aseton 15
o
C. Viskositas aston dengan
suhu 15
o
C pada konsentrasi 20%, 30% dan 40% adalah 1,18 cP, 1,23 cP dan
1,28 cP. Viskositas aseton dengan suhu 30
o
C pada konsentrasi 20%, 30%
dan 40% adalah 1,9 cP, 1,85 cP dan 1,8 cP. Viskositas aseton dengan suhu 60
o
C pada konsentrasi 20%, 30% dan 40% adalah 0,42 cP, 0,4 cP dan 0,38 cP.
0
0.5
1
1.5
2
2.5
3
3.5
4
0.2 0.3 0.4 0.5
V
i
s
k
o
s
i
t
a
s
(
c
P
)
Konsentrasi (%)
Aseton 15oC
Aseton 30oC
Aseton 60oC
Kecap Kental Manis
(ABC) 15oC
Kecap Kental Manis
(ABC) 30oC
Kecap Kental Manis
(ABC) 60oC
Aseton 15
o
C
Aseton 30
o
C
Aseton 60
o
C
Kecap Kental Manis
(ABC) 15
o
C
Kecap Kental Manis
(ABC) 60
o
C
Kecap Kental Manis
(ABC) 60
o
C
=
n R T r
4
t
8 V l
Viskositas kecap kental manis (ABC) dengan suhu 15
o
C pada konsentrasi
20%, 30% dan 40% adalah 3,7 cP, 3,45 cP dan 3,2 cP. Viskositas kecap
kental manis (ABC) dengan suhu 30
o
C pada konsentrasi 20%, 30% dan 40%
adalah 3,61 cP, 2,97 cP dan 2,65 cP. Viskositas kecap kental manis (ABC)
dengan suhu 60
o
C pada konsentrasi 20%, 30% dan 40% adalah 2,03 cP, 1,81
cP dan 1,59 cP.
Berdasarkan teori, larutan yang konsentrasinya tinggi, Viskositas
berbanding lurus dengan konsentrasi larutan. Suatu larutan dengan
konsentrasi tinggi akan memiliki viskositas yang tinggi pula, karena
konsentrasi larutan menyatakan banyaknya partikel zat yang terlarut
tiapsatuan volume. Semakin banyak partikel yang terlarut, gesekan
antarpartikel semakin tinggi dan viskositasnya semakin tinggi pula (Citra,
2009).
Secara matematis dapat ditulis sebagai berikut:
vl 8
t r gh
=
dimana :
Mr
10.%.
M =
10.%
M.Mr
=
sehingga menjadi : =
dimana:
= densitas t = waktu L = panjang pipa
g = percepatan gravitasi r = jari-jari pipa Mr = berat molekul
h = beda ketinggian V = volume = konstanta
= koefisien viskositas
Berdasarkan penjelasan diatas, terlihat bahwa hasil yang diperoleh
dari praktek pada sampel aseton pada konsentrasi 20%, 30% dan 40% sesuai
dengan teori sedangkan pada sampel kecap kental manis (ABC) dengan
konsentrasi 20%, 30% dan 40% menyimpang dengan teori. Penyimpangan
pada sampel kecap kental manis (ABC) mungkin disebabkan karena :
1. Adanya sampel yang terkontaminasi dengan zat lain yang terdapat dalam
viskosimeter.
2. Sulitnya mempertahankan suhu yang konstan.
4.2.3 Pengaruh Berat Molekul Terhadap Viskositas Regresi
Gambar 4.3 Grafik Pengaruh Berat Molekul Terhadap Viskositas
Pada gambar 4.3 menunjukkan bahwa kurva secara umum
menunjukan penurunan. Dimana berat molekul aseton pada konsentrasi 20%,
30% dan 40% berturut-turut adalah 26 gr/mol, 30 gr/mol dan 34 gr/mol dan
viskositas aseton pada 15
o
C viskositasnya sebesar 1.395 cP untuk BM 26
gr/mol, kemudian viskositasnya sebesar 1,225 cP untuk BM 30 gr/mol dan
1,579 cP untuk BM 34 gr/mol. Viskositas aseton pada 30
o
C viskositasnya
sebesar 1,7 cP untuk BM 26 gr/mol, kemudian viskositasnya sebesar 1,85 cP
untuk BM 30 gr/mol dan 2 cP untuk BM 34 gr/mol. Viskositas aseton pada
60
o
C viskositasnya sebesar 2,37 cP untuk BM 26 gr/mol, kemudian
viskositasnya sebesar 2,34 cP untuk BM 30 gr/mol dan 2,32 cP untuk BM 34
gr/mol
Berdasarkan teori, viskositas berbanding lurus dengan berat molekul
solute, karena dengan adanya solute yang berat akan menghambat atau
0.000
0.500
1.000
1.500
2.000
2.500
26 30 34 38
V
i
s
k
o
s
i
t
a
s
(
c
P
)
Berat Molekul (gr/mol)
Aseton 15oC
Aseton 30oC
Aseton 60oC
Aseton 15
o
C
Aseton 30
o
C
Aseton 60
o
C
memberi beban yang berat pada cairan sehingga akan menaikkan
viskositasnya (Citra, 2009).
Secara matematis ditulis sebagai berikut :
[] = kM
[] = k
o
|
.
|
\
|
MR
gr
dimana:
[] = viskositas intrinsik Mr = berat molekul
k = konstanta pelarut M = konsentrasi zat
= konstanta
Berdasarkan penjelasan diatas, terlihat bahwa hasil yang diperoleh
dari praktek pada semua sampel adalah tidak sesuai dengan teori.
Penyimpangan pada sampel mungkin disebabkan karena :
1. Adanya sampel yang terkontaminasi dengan zat lain yang terdapat dalam
viskosimeter.
2. Sulitnya mempertahankan suhu yang konstan.
4.2.4 Pengaruh Densitas Terhadap Viskositas Praktek
Gambar 4.4 Grafik Pengaruh Densitas Terhadap Viskositas Praktek
0
0.5
1
1.5
2
2.5
0 0,5 1
V
i
s
k
o
s
i
t
a
s
(
c
P
)
Densitas (g/ml)
Aseton 20%
Aseton 40%
Kecap Kental Manis
(ABC) 20%
Kecap Kental Manis
(ABC) 40%
Berdasarkan grafik di atas menunjukkan bahwa kurva menunjukan
kenaikan. Dimana viskositas larutan aseton 20% pada suhu 15 C dengan
densitas 0.9876 gr/ml dengan viskositas sebesar 1,646 cP, pada suhu 30 C
didapatkan densitas sebesar 0,9984 gr/ml dan viskositas sebesar 1,012 cP,
dan pada suhu 60 C didapatkan densitas sebesar 0,986 gr/ml dengan
viskositas 0,589 cP. Viskositas larutan aseton 40% pada suhu 15 C dengan
densitas 0.9344 gr/ml dengan viskositas sebesar 1,597 cP, pada suhu 30 C
didapatkan densitas sebesar 0,948 gr/ml dan viskositas sebesar 1,014 cP,
dan pada suhu 60 C didapatkan densitas sebesar 0,9416 gr/ml dengan
viskositas 0,596 cP. Untuk viskositas larutan kecap kental manis (ABC) 20%
pada suhu 15 C dengan densitas 1,094 gr/ml dengan viskositas sebesar 1,7
cP, pada suhu 30 C didapatkan densitas sebesar 1,0784 gr/ml dan viskositas
sebesar 1,174 cP, dan pada suhu 60 C didapatkan densitas sebesar 1,0784
gr/ml dengan viskositas 0,683 cP. Viskositas larutan kecap kental manis
(ABC) 40% pada suhu 15 C dengan densitas 1,2476 gr/ml dengan
viskositas sebesar 2,344 cP, pada suhu 30 C didapatkan densitas sebesar
1,1532 gr/ml dan viskositas sebesar 1,438 cP, dan pada suhu 60 C
didapatkan densitas sebesar 1,1536 gr/ml dengan viskositas 0,839 cP.
Berdasarkan teori, nilai viskositas sebanding dengan nilai densitas
suatu cairan. Jadi, bila densitas suatu cairan tinggi, maka viskositas cairan
tersebut juga akan meningkat (Citra, 2009).
Secara sistematis dapat ditulis sebagai berikut:
q
Rdv 2
Re =
di mana: R = jari-jari pipa,
v = kecepatan alir rata-rata,
q = viskositas,
d = diameter pipa.
Re = Bilangan Reynolds
Maka dari grafik diatas dapat disimpulkan hasil percobaan pada
semua sampel sesuai dengan teori yang menyatakan bahwa viskositas
sebanding dengan nilai densitas suatu cairan kecuali pada sampel kecap
kental manis (ABC) 40% pada suhu 15
o
C. Penyimpangan pada sampel
mungkin disebabkan karena :
1. Adanya sampel yang terkontaminasi dengan zat lain yang terdapat dalam
viskosimeter.
2. Sulitnya mempertahankan suhu yang konstan.
You might also like
- Bab 4 ViskositasDocument7 pagesBab 4 ViskositasPelegia SamiraNo ratings yet
- Laporan Viskositas Sebagai Fungsi SuhuDocument22 pagesLaporan Viskositas Sebagai Fungsi SuhuYusiana YusiNo ratings yet
- Laporan Viskositas Dan RheologiDocument11 pagesLaporan Viskositas Dan RheologiAnita Anggriani100% (1)
- Bab Iv Kurva KelarutanDocument18 pagesBab Iv Kurva KelarutanHalimaSiregarNo ratings yet
- B-2 AyuDocument14 pagesB-2 AyuAyu ZakiaNo ratings yet
- Laporan Kimfis RefraktometriDocument10 pagesLaporan Kimfis RefraktometriNDSNo ratings yet
- Praktikum IiDocument7 pagesPraktikum IiDhikaJessNo ratings yet
- 2 RefraktometriDocument7 pages2 RefraktometriAlmaNo ratings yet
- Percobaan B2Document14 pagesPercobaan B2Dede MulyamanNo ratings yet
- Laporan Praktikum DaringDocument9 pagesLaporan Praktikum DaringNURFITRIA MUTMAINNAHNo ratings yet
- Fisik 6Document5 pagesFisik 6Putri Pah Kumala DewiNo ratings yet
- Laporan Penentuan Bobot JenisDocument14 pagesLaporan Penentuan Bobot JenisAmelia ZahridaNo ratings yet
- Laporan Praktikum Kimia Fisika IIDocument24 pagesLaporan Praktikum Kimia Fisika IISanty Athifah ZakiyahNo ratings yet
- Mini Riset. Nur Atika. PSF 23ADocument9 pagesMini Riset. Nur Atika. PSF 23Atikaaa25.3No ratings yet
- 2 REFRAKTOMETRI FixDocument10 pages2 REFRAKTOMETRI Fixhamidah ashraNo ratings yet
- Laporan Hasil Titrasi Asam Lemah Ch3cooh Dengan Basa Kuat Naoh 1Document6 pagesLaporan Hasil Titrasi Asam Lemah Ch3cooh Dengan Basa Kuat Naoh 1Dhedhe Lestari'thaNo ratings yet
- Diagram TernerDocument11 pagesDiagram TernerAl KahfiNo ratings yet
- MakalaDocument21 pagesMakalaOpieNo ratings yet
- Laporan ViskositasDocument15 pagesLaporan ViskositasfixdilNo ratings yet
- Marisa Nurlita (1601024) - Penetapan Kadar Zat Secara KCKTDocument10 pagesMarisa Nurlita (1601024) - Penetapan Kadar Zat Secara KCKTMarisa NurlitaNo ratings yet
- Laporan Praktikum Analisis TerapanDocument13 pagesLaporan Praktikum Analisis TerapanYossy AyuliansariNo ratings yet
- Titrasi KonduktometriDocument11 pagesTitrasi KonduktometriprisantiuniNo ratings yet
- Ni Luh Putu Agustina Putri 1713081015 Uas Praktikum BiokimiaDocument10 pagesNi Luh Putu Agustina Putri 1713081015 Uas Praktikum BiokimiaPutrik AgustinaNo ratings yet
- Percobaan B2Document8 pagesPercobaan B2Elvina Laksmi KhairunisaNo ratings yet
- Laporan Praktikum Instrumentasi Kelompok 3Document9 pagesLaporan Praktikum Instrumentasi Kelompok 3Tasha AsyariNo ratings yet
- Penetapan Kadar Asam AsetatDocument4 pagesPenetapan Kadar Asam AsetatAndi AnugrahNo ratings yet
- Tes Awal Titrasi Formal-I Made Yoga Santika Putra-1813081017Document7 pagesTes Awal Titrasi Formal-I Made Yoga Santika Putra-1813081017DekyogaNo ratings yet
- PK 2 Spektrofotometri UVDocument29 pagesPK 2 Spektrofotometri UVlupu rinaNo ratings yet
- Laporan PotensiometriDocument11 pagesLaporan PotensiometriMayang BerlianaNo ratings yet
- I Wayan Seniarta - 192211101113 - Farmasi PraktisDocument10 pagesI Wayan Seniarta - 192211101113 - Farmasi PraktisWayan SeniartaNo ratings yet
- Laporan Praktikum KIMIADocument12 pagesLaporan Praktikum KIMIA29Armeisia Daun RaraNo ratings yet
- Modul Kimia Kelas XiiDocument38 pagesModul Kimia Kelas XiiIlhamsya Nurghaly AldrianNo ratings yet
- VISKOSITASDocument11 pagesVISKOSITASsabilNo ratings yet
- Laporan Praktikum Ai Perc. 5Document7 pagesLaporan Praktikum Ai Perc. 5Siti ChotimahNo ratings yet
- Pemba Has AnDocument7 pagesPemba Has AnNatasha LaurentiaNo ratings yet
- Analisis Kuantitatif Metode Volumetrik (Argentometri) - Tiara Sophia Ananda (2111102415047)Document14 pagesAnalisis Kuantitatif Metode Volumetrik (Argentometri) - Tiara Sophia Ananda (2111102415047)Tiara Sophia AnandaNo ratings yet
- Viskositas Sebagai Fungsi SuhuDocument17 pagesViskositas Sebagai Fungsi SuhushafiraNo ratings yet
- Penentuan Keasaman Pada SusuDocument5 pagesPenentuan Keasaman Pada SusuFirmaning NurNo ratings yet
- B2 - Kelarutan Sebagai Fungsi SuhuDocument12 pagesB2 - Kelarutan Sebagai Fungsi Suhu016 Cica Siti NurjanahNo ratings yet
- Refraktometri NayaDocument13 pagesRefraktometri NayaAinayya AnnihayahNo ratings yet
- Praktikum 2 - Penurunan KesadahanDocument8 pagesPraktikum 2 - Penurunan KesadahanDhea Shofi RachmaditaNo ratings yet
- Laporan Praktikum ViskosimetriDocument16 pagesLaporan Praktikum ViskosimetriQurrotaA'yunNo ratings yet
- Percobaan 3 Penetapan Konsentrasi Sulfat Didalam Larutan K2SO4 Secara Turbidimetri Dengan Alat Spektronik 20Document16 pagesPercobaan 3 Penetapan Konsentrasi Sulfat Didalam Larutan K2SO4 Secara Turbidimetri Dengan Alat Spektronik 20SitiNurAzizah A.TNo ratings yet
- Titrasi Asam-BasaDocument6 pagesTitrasi Asam-BasaElisna Jayanti100% (1)
- Laporan Praktikum Fisika FarmasiDocument6 pagesLaporan Praktikum Fisika FarmasiAttahiraNo ratings yet
- Soal Dan Jawaban Quiz 1 & Quiz 2 PBIKDocument6 pagesSoal Dan Jawaban Quiz 1 & Quiz 2 PBIKAzri Nurafif ArsyaddilaNo ratings yet
- 5 Spektro Vis PDFDocument32 pages5 Spektro Vis PDFRoms KitchenNo ratings yet
- PO 7 KIMIA - ALC Indonesia (WWW - Defantri.com)Document10 pagesPO 7 KIMIA - ALC Indonesia (WWW - Defantri.com)Stephen PramatyaNo ratings yet
- RefraktometriDocument13 pagesRefraktometriNuril Mega MusfitaNo ratings yet
- Laporan Praktikum B-2Document13 pagesLaporan Praktikum B-2fry voni stekyNo ratings yet
- SPEKTRO GENESYS20.nntikDocument13 pagesSPEKTRO GENESYS20.nntikAditya RachmanNo ratings yet
- Kesetimbangan FasaDocument2 pagesKesetimbangan Fasachelsea_fc43No ratings yet
- Uts Material Maju Pak PirimDocument14 pagesUts Material Maju Pak Pirimrizqya laramadhanaNo ratings yet
- Laporan Hasil Praktikum Farmasi FisikaDocument27 pagesLaporan Hasil Praktikum Farmasi FisikaCahyadi SuratmanNo ratings yet
- Pembahasan AlkalimetriDocument5 pagesPembahasan AlkalimetriJesicha Dwi FitriaNo ratings yet
- Laprak Asam CukaDocument9 pagesLaprak Asam CukaSeila MaliyaNo ratings yet
- 4 VolumetriDocument55 pages4 VolumetriIndah Wulan AdjahNo ratings yet