Professional Documents
Culture Documents
Hierro
Uploaded by
Griffin EpgCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Hierro
Uploaded by
Griffin EpgCopyright:
Available Formats
Hierro
Hierro
Manganeso
Hierro Cobalto
26
Fe
Tabla completa Tabla ampliada
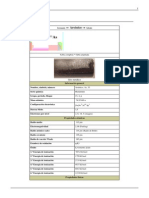
Metlico brillante con un tono grisceo
Informacin general Nombre, smbolo, nmero Serie qumica Grupo, perodo, bloque Masa atmica Configuracin electrnica Dureza Mohs Electrones por nivel Hierro, Fe, 26 Metales de transicin 8, 4, d 55,845u [Ar]3d 4s 4,0 2, 8, 14, 2 (imagen) Propiedades atmicas Radio medio Electronegatividad Radio atmico (calc) Radio covalente Radio de van der Waals Estado(s) de oxidacin xido 1. Energa de ionizacin 2. Energa de ionizacin 3. Energa de ionizacin 4. Energa de ionizacin 140pm 1,83 (Pauling) 155.8pm (Radio de Bohr) 126pm Sin datospm 2, 3 Anftero 762,5kJ/mol 1561,9kJ/mol 2957kJ/mol 5290kJ/mol Propiedades fsicas Estado ordinario Densidad Slido (ferromagntico) 7874 kg/m3, 7,87 g/cm3kg/m3
6 2
Hierro
2
Punto de fusin Punto de ebullicin Entalpa de vaporizacin Entalpa de fusin Presin de vapor 1808K (1535C) 3023K (2750C) 349,6kJ/mol 13,8kJ/mol 7,05 Pa a 1808 K Varios Estructura cristalina N CAS N EINECS Calor especfico Conductividad elctrica Conductividad trmica Resistencia mxima Mdulo elstico Velocidad del sonido Cbica centrada en el cuerpo 7439-89-6 231-096-4 440J/(Kkg) 9,9310 S/m 80,2W/(Km) 540MPa 200GPa 4910m/s a 293,15K (20C) Istopos ms estables Artculo principal: Istopos del hierro Ed iso
54 55 56 57 58 59 60 6
[1]
AN
Periodo MD MeV
PD
Fe 5,845% Fe Sinttico Fe 91,72% Fe 2,119% Fe 0,282%
Estable con 28 neutrones 2,73 a 0,231
55
Mn
Estable con 30 neutrones Estable con 31 neutrones Estable con 32 neutrones 1,565 3,978
59 60
Fe Sinttico 44,503 d Fe Sinttico 1,5106 a
Co Co
Valores en el SI y condiciones normales de presin y temperatura, salvo que se indique lo contrario.
Hierro
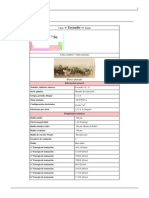
El hierro o fierro (en muchos pases hispanohablantes se prefiere esta segunda forma)[2] es un elemento qumico de nmero atmico 26 situado en el grupo 8, periodo 4 de la tabla peridica de los elementos. Su smbolo es Fe (del latn frrum) y tiene una masa atmica de 55,6u. Este metal de transicin es el cuarto elemento ms abundante en la corteza terrestre, representando un 5% y, entre los metales, slo el aluminio es ms abundante. Estructura de un puente en hierro. El ncleo de la Tierra est formado principalmente por hierro y nquel, generando al moverse un campo magntico. Ha sido histricamente muy importante, y un perodo de la historia recibe el nombre de Edad de Hierro. En cosmologa, es un metal muy especial, pues es el metal ms pesado que puede producir la fusin en el ncleo de estrellas masivas; los elementos ms pesados que el hierro solo pueden crearse en supernovas..
Caractersticas principales
Es un metal maleable, de color gris plateado y presenta propiedades magnticas; es ferromagntico a temperatura ambiente y presin atmosfrica. Es extremadamente duro y denso. Se encuentra en la naturaleza formando parte de numerosos minerales, entre ellos muchos xidos, y raramente se encuentra libre. Para obtener hierro en estado elemental, los xidos se reducen con carbono y luego es sometido a un proceso de refinado para eliminar las impurezas presentes.
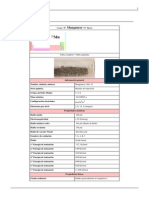
Hierro puro
Es el elemento ms pesado que se produce exotrmicamente por fusin, y el ms ligero que se produce a travs de una fisin, debido a que su ncleo tiene la ms alta energa de enlace por nuclen (energa necesaria para separar del ncleo un neutrn o un protn); por lo tanto, el ncleo ms estable es el del hierro-56 (con 30 neutrones). Presenta diferentes formas estructurales dependiendo de la temperatura y presin. A presin atmosfrica: Hierro-: estable hasta los 911C. El sistema cristalino es una red cbica centrada en el cuerpo (bcc). Hierro-: 911C - 1392C; presenta una red cbica centrada en las caras (fcc). Hierro-: 1392C - 1539C; vuelve a presentar una red cbica centrada en el cuerpo. Hierro-: Puede estabilizarse a altas presiones, presenta estructura hexagonal compacta (hcp).
Aplicaciones
El hierro es el metal duro ms usado, con el 95% en peso de la produccin mundial de metal. El hierro puro (pureza a partir de 99,5%) no tiene demasiadas aplicaciones, salvo excepciones para utilizar su potencial magntico. El hierro tiene su gran aplicacin para formar los productos siderrgicos, utilizando ste como elemento matriz para alojar otros elementos aleantes tanto metlicos como no metlicos, que confieren distintas propiedades al material. Se considera que una aleacin de hierro es acero si contiene menos de un 2,1% de carbono; si el porcentaje es mayor, recibe el nombre de fundicin. El acero es indispensable debido a su bajo precio y tenacidad, especialmente en automviles, barcos y componentes estructurales de edificios.
Hierro Las aleaciones frreas presentan una gran variedad de propiedades mecnicas dependiendo de su composicin o el tratamiento que se haya llevado a cabo.
Aceros
Los aceros son aleaciones frreas con un contenido mximo de carbono del 2%, el cual puede estar como aleante de insercin en la ferrita y austenita y formando carburo de hierro. Algunas aleaciones no son ferromagnticas. ste puede tener otros aleantes e impurezas. Dependiendo de su contenido en carbono se clasifican en los siguientes tipos: Acero bajo en carbono: menos del 0,25% de C en peso. Son blandos pero dctiles. Se utilizan en vehculos, tuberas, elementos estructurales, etctera. Tambin existen los aceros de alta resistencia y baja aleacin, que contienen otros elementos aleados hasta un 10% en peso; tienen una mayor resistencia mecnica y pueden ser trabajados fcilmente. Acero medio en carbono: entre 0,25% y 0,6% de C en peso. Para mejorar sus propiedades son tratados trmicamente. Son ms resistentes que los aceros bajos en carbono, pero menos dctiles; se emplean en piezas de ingeniera que requieren una alta resistencia mecnica y al desgaste. Acero alto en carbono: entre 0,60% y 1,4% de C en peso. Son an ms resistentes, pero tambin menos dctiles. Se aaden otros elementos para que formen carburos, por ejemplo, con wolframio se forma el carburo de wolframio, WC; estos carburos son muy duros. Estos aceros se emplean principalmente en herramientas. Aceros aleados: Con los aceros no aleados, o al carbono, es imposible satisfacer las demandas de la industria actual. Para conseguir determinadas caractersticas de resiliencia, resistencia al desgaste, dureza y resistencia a determinadas temperaturas deberemos recurrir a estos. Mediante la accin de uno o varios elementos de aleacin en porcentajes adecuados se introducen modificaciones qumicas y estructurales que afectan a la temlabilidad, caractersticas mecnicas, resistencia a oxidacin y otras propiedades. La clasificacin ms tcnica y correcta para los aceros al carbono (sin alear) segn su contenido en carbono: Los aceros hipoeutectoides, cuyo contenido en carbono oscila entre 0.02% y 0,8%. Los aceros eutectoides cuyo contenido en carbono es de 0,8%. Los aceros hipereutectoides con contenidos en carbono de 0,8% a 2%. Aceros inoxidables: uno de los inconvenientes del hierro es que se oxida con facilidad. Aadiendo un 12% de cromo se considera acero inoxidable, debido a que este aleante crea una capa de xido de cromo superficial que protege al acero de la corrosin o formacin de xidos de hierro. Tambin puede tener otro tipo de aleantes como el nquel para impedir la formacin de carburos de cromo, los cuales aportan fragilidad y potencian la oxidacin intergranular. El uso ms extenso del hierro es para la obtencin de aceros estructurales; tambin se producen grandes cantidades de hierro fundido y de hierro forjado. Entre otros usos del hierro y de sus compuestos se tienen la fabricacin de imanes, tintes (tintas, papel para heliogrficas, pigmentos pulidores) y abrasivos (colctar).
Fundiciones
El hierro es obtenido en el alto horno mediante la conversin de los minerales en hierro lquido, a travs de su reduccin con coque; se separan con piedra caliza, los componentes indeseables, como fsforo, azufre, y manganeso. Los gases de los altos hornos son fuentes importantes de partculas y contienen monxido de carbono. La escoria del alto horno es formada al reaccionar la piedra caliza con los otros componentes y los silicatos que contienen los minerales. Se enfra la escoria en agua, y esto puede producir monxido de carbono y sulfuro de hidrgeno. Los desechos lquidos de la produccin de hierro se originan en el lavado de gases de escape y enfriamiento de la escoria. A menudo, estas aguas servidas poseen altas concentraciones de slidos suspendidos y pueden contener una amplia gama de compuestos orgnicos (fenoles y cresoles), amonaco, compuestos de arsnico y sulfuros.
Hierro Cuando el contenido en carbono es superior a un 2.43% en peso, la aleacin se denomina fundicin. Este carbono puede encontrarse disuelto, formando cementita o en forma libre. Son muy duras y frgiles. Hay distintos tipos de fundiciones: Gris Blanca Atruchada Maleable americana Maleable europea Esferoidal o dctil Vermicular
Sus caractersticas varan de un tipo a otra; segn el tipo se utilizan para distintas aplicaciones: en motores, vlvulas, engranajes, etc. Por otra parte, los xidos de hierro tienen variadas aplicaciones: en pinturas, obtencin de hierro, la magnetita (Fe3O4) y el xido de hierro (III) (Fe2O3) en aplicaciones magnticas, etc. El hidrxido de hierro (III) (Fe(OH)3) se utiliza en radioqumica para concentrar los actnidos mediante co-precipitacin.
Historia
Se tienen indicios de uso del hierro, cuatro milenios antes de Cristo, por parte de los sumerios y egipcios. En el segundo y tercer milenio, antes de Cristo, van apareciendo cada vez ms objetos de hierro (que se distingue del hierro procedente de meteoritos por la ausencia de nquel) en Mesopotamia, Anatolia y Egipto. Sin embargo, su uso parece ser ceremonial, siendo un metal muy caro, ms que el oro. Algunas fuentes sugieren que tal vez se obtuviera como subproducto de la obtencin de cobre. Entre 1600a.C. y 1200a.C. va aumentando su uso en Oriente Medio, pero no sustituye al predominante uso del bronce. Entre los siglos XIIa.C. y Xa.C. se produce una rpida transicin en Oriente Medio desde las armas de bronce a las de hierro. Esta rpida transicin tal vez fuera debida a la falta de estao, antes que a una mejora en la tecnologa en el trabajo del hierro. A este periodo, que se produjo en diferentes fechas segn el lugar, se denomina Edad de Hierro, sustituyendo a la Edad de Bronce. En Grecia comenz a emplearse en torno al ao 1000a.C. y no lleg a Europa occidental hasta el siglo VIIa.C. La sustitucin del bronce por el hierro fue paulatina, pues era difcil fabricar piezas de hierro: localizar el mineral, luego fundirlo a temperaturas altas para finalmente forjarlo. En Europa Central, surgi en el siglo IXa.C. la cultura de Hallstatt (sustituyendo a la cultura de los campos de urnas, que se denomina primera Edad de Hierro, pues coincide con la introduccin de este metal. Hacia el 450a.C. se desarroll la cultura de La Tne, tambin denominada segunda Edad de Hierro. El hierro se usa en herramientas, armas y joyera, aunque siguen encontrndose objetos de bronce. Junto con esta transicin del bronce al hierro se descubri el proceso de carburizacin, consistente en aadir carbono al hierro. El hierro se obtena como una mezcla de hierro y escoria, con algo de carbono o carburos, y era forjado, quitando la escoria y oxidando el carbono, creando as el producto ya con una forma. Este hierro forjado tena un contenido en carbono muy bajo y no se poda endurecer fcilmente al enfriarlo en agua. Se observ que se poda obtener un producto mucho ms duro calentando la pieza de hierro forjado en un lecho de carbn vegetal, para entonces sumergirlo en agua o aceite. El producto resultante, que tena una superficie de acero, era ms duro y menos frgil que el bronce, al que comenz a reemplazar. En China el primer hierro que se utiliz tambin proceda de meteoritos, habindose encontrado objetos de hierro forjado en el noroeste, cerca de Xinjiang, del siglo VIIIa.C. El procedimiento era el mismo que el utilizado en Oriente Medio y Europa. En los ltimos aos de la Dinasta Zhou (550a.C.) se consigue obtener hierro colado (producto de la fusin del arrabio). El mineral encontrado all presenta un alto contenido en fsforo, con lo que funde
Hierro a temperaturas menores que en Europa y otros sitios. Sin embargo durante bastante tiempo, hasta la Dinasta Qing (hacia 221a.C.), no tuvo una gran repercusin. El hierro colado tard ms en Europa, pues no se consegua la temperatura suficiente. Algunas de las primeras muestras de hierro colado se han encontrado en Suecia, en Lapphyttan y Vinarhyttan, del 1150 a 1350. En la Edad Media, y hasta finales del siglo XIX, muchos pases europeos empleaban como mtodo siderrgico la farga catalana. Se obtena hierro y acero bajo en carbono empleando carbn vegetal y el mineral de hierro. Este sistema estaba ya implantado en el siglo XV, y se conseguan alcanzar hasta unos 1200C. Este procedimiento fue sustituido por el empleado en los altos hornos. En un principio se usaba carbn vegetal para la obtencin de hierro como fuente de calor y como agente reductor. En el siglo XVIII, en Inglaterra, comenz a escasear y hacerse ms caro el carbn vegetal, y esto hizo que comenzara a utilizarse coque, un combustible fsil, como alternativa. Fue utilizado por primera vez por Abraham Darby, a principios del siglo XVIII, que construy en Coalbrookdale un alto horno. Asimismo, el coque se emple como fuente de energa en la Revolucin industrial. En este periodo la demanda de hierro fue cada vez mayor, por ejemplo para su aplicacin en ferrocarriles. El alto horno fue evolucionando a lo largo de los aos. Henry Cort, en 1784, aplic nuevas tcnicas que mejoraron la produccin. En 1826 el alemn Friedrich Harkot construye un alto horno sin mampostera para humos. Hacia finales del siglo XVIII y comienzos del XIX se comenz a emplear ampliamente el hierro como elemento estructural (en puentes, edificios, etc). Entre 1776 a 1779 se construye el primer puente de fundicin de hierro, construido por John Wilkinson y Abraham Darby. En Inglaterra se emplea por primera vez en la construccin de edificios, por Mathew Boulton y James Watt, a principios del siglo XIX. Tambin son conocidas otras obras de ese siglo, por ejemplo el Palacio de Cristal construido para la Exposicin Universal de 1851 en Londres, del arquitecto Joseph Paxton, que tiene un armazn de hierro, o la Torre Eiffel, en Pars, construida en 1889 para la Exposicin Universal, en donde se utilizaron miles de toneladas de hierro..
Abundancia y obtencin
El hierro es el metal de transicin ms abundante en la corteza terrestre, y cuarto de todos los elementos. Tambin existe en el Universo, habindose encontrado meteoritos que lo contienen. Es el principal metal que compone el ncleo de la Tierra hasta con un 70%. Se encuentra formando parte de numerosos minerales, entre los que destacan la hematites (Fe2O3), la magnetita (Fe3O4), la limonita (FeO (OH)), la siderita (FeCO3), la pirita (FeS2), la ilmenita (FeTiO3), etctera. Se puede obtener hierro a partir de los xidos con ms o menos impurezas. Muchos de los minerales de hierro son xidos, y los que no, se pueden oxidar para obtener los correspondientes xidos. La reduccin de los xidos para obtener hierro se lleva a cabo en un horno denominado comnmente alto horno . En l se aaden los minerales de hierro en presencia de coque y carbonato de calcio, CaCO3, que acta como escorificante. Los gases sufren una serie de reacciones; el carbono puede reaccionar con el oxgeno para formar dixido de carbono: C + O2 CO2 A su vez el dixido de carbono puede reducirse para dar monxido de carbono: CO2 + C 2CO Aunque tambin se puede dar el proceso contrario al oxidarse el monxido con oxgeno para volver a dar dixido de carbono: 2CO + O2 2CO2
Hierro El proceso de oxidacin de coque con oxgeno libera energa y se utiliza para calentar (llegndose hasta unos 1900C en la parte inferior del horno). En primer lugar los xidos de hierro pueden reducirse, parcial o totalmente, con el monxido de carbono, CO; por ejemplo: Fe3O4 + CO 3FeO + CO2 FeO + CO Fe + CO2 Despus, conforme se baja en el horno y la temperatura aumenta, reaccionan con el coque (carbono en su mayor parte), reducindose los xidos. Por ejemplo: Fe3O4 + C 3FeO + CO El carbonato de calcio (caliza) se descompone: CaCO3 CaO + CO2 Y el dixido de carbono es reducido con el coque a monxido de carbono como se ha visto antes. Ms abajo se producen procesos de carburacin: 3Fe + 2CO Fe3C + CO2 Finalmente se produce la combustin y desulfuracin (eliminacin de azufre) mediante la entrada de aire. Y por ltimo se separan dos fracciones: la escoria y el arrabio: hierro fundido, que es la materia prima que luego se emplea en la industria. El arrabio suele contener bastantes impurezas no deseables, y es necesario someterlo a un proceso de afino en hornos llamados convertidores. En 2000 los cinco mayores productores de hierro eran China, Brasil, Australia, Rusia e India, con el 70% de la produccin mundial. Actualmente el mayor yacimiento de Hierro del mundo se encuentra en la regin de "El Mutn", en el departamento de Santa Cruz, Bolivia; dicho yacimiento cuenta con entre 40.000 y 42.000 millones de toneladas aprox. (40% de la reserva mundial) para explotar.[citarequerida]
Compuestos
Los estados de oxidacin ms comunes son +2 y +3. Los xidos de hierro ms conocidos son el xido de hierro (II) (FeO), el xido de hierro (III), Fe2O3, y el xido mixto Fe3O4. Forma asimismo numerosas sales y complejos en estos estados de oxidacin. El hexacianoferrato (II) de hierro (III), usado en pinturas, se ha denominado azul de Prusia o azul de Turnbull; se pensaba que eran sustancias diferentes. Se conocen compuestos en el estado de oxidacin +4, +5 y +6, pero son poco comunes, y en el caso del +5, no est bien caracterizado. El ferrato de potasio (K2FeO4), en el que el hierro est en estado de oxidacin +6, se emplea como oxidante. El estado de oxidacin +4 se encuentra en unos pocos compuestos y tambin en algunos procesos enzimticos. Varios compuestos de hierro exhiben estados de oxidacin extraos, como el tetracarbonilferrato disdico.[3] , Na2[Fe(CO)4], que atendiendo a su frmula emprica el hierro posee estado de oxidacin -2 (el monxido de carbono que aparece como ligando no posee carga), que surge de la reaccin del pentacarbonilhierro con sodio. El Fe3C se conoce como cementita, que contiene un 6,67 % en carbono, al hierro se le conoce como ferrita, y a la mezcla de ferrita y cementita, perlita o ledeburita dependiendo del contenido en carbono. La austenita es una solucin slida intersticial de carbono en hierro (Gamma).
Hierro
Metabolismo del hierro
Aunque solo existe en pequeas cantidades en los seres vivos, el hierro ha asumido un papel vital en el crecimiento y en la supervivencia de los mismos y es necesario no slo para lograr una adecuada oxigenacin tisular sino tambin para el metabolismo de la mayor parte de las clulas. En la actualidad con un incremento en el oxgeno atmosfrico el hierro se encuentra en el medio ambiente casi exclusivamente en forma oxidada ( ferrica Fe3+) y en esta forma es poco utilizable. En los adultos sanos el hierro corporal total es de unos 2 a 4 gramos ( 2,5 gramos en 71 kg de peso en la mujer 35 mg/kg) (a 4 gramos en 80kg o 50 mg/kg en los varones). Se encuentra distribuido en dos formas: 70% como hierro funcional (2,8 de 4 gramos): Eritrocitos (65%). Tisular: mioglobinas (4%). Enzimas dependientes del hierro (hem y no hem): 1% Estas son enzimas esenciales para la funcin de las mitocondrias y que controlan la oxidacin intracelular (citocromos, oxidasas del citrocromo, catalasas, peroxidasas). Transferrina (0,1%), la cual se encuentra normalmente saturada en 1/3 con hierro. La mayor atencin con relacin a este tipo de hierro se ha enfocado hacia el eritrn, ya que su estatus de hierro puede ser fcilmente medible y constituye la principal fraccin del hierro corporal. 30% como hierro de depsito (1 g): Ferritina (2/3): Principal forma de depsito del hierro en los tejidos. Hemosiderina (1/3). Hemoglobina: Transporta el oxgeno a las clulas. Transferrina: Transporta el hierro a travs del plasma.
Estudios recientes de disponibilidad del hierro de los alimentos han demostrado que el hierro del hem es bien absorbido, pero el hierro no hem se absorbe en general muy pobremente y este ltimo, es el hierro que predomina en la dieta de gran cantidad de gente en el mundo.[citarequerida] Hem: Como hemoglobina y mioglobina, presente principalmente en la carne y derivados. No hem. La absorcin del hierro hem no es afectada por ningn factor; ni diettico, ni de secrecin gastrointestinal. Se absorbe tal cual dentro del anillo porfirnico. El hierro es liberado dentro de las clulas de la mucosa por la HEM oxigenasa, enzima que abunda en las clulas intestinales del duodeno. Las absorcin del hierro no hem, por el contrario se encuentra afectada por una gran contidad de factores dietticos y de secrecin gastrointestinal que se analizarn posteriormente. El hierro procedente de la dieta, especialmente el "no hem", es hierro frrico y debe ser convertido en hierro ferroso a nivel gstrico antes que ocurra su absorcin en esta forma (hierro ferroso) a nivel duodenal principalmente. Otros factores, independientes de la dieta que pueden influir en la absorcin del hierro son: El tamao del depsito de hierro que indica el estado de reserva de hierro de un individuo. Este es el principal mecanismo de control. Se encuentra influenciado por los depsitos de hierro y por lo tanto, por las necesidades corporales. As, reservas aumentadas de hierro disminuyen su absorcin. En este punto el factor ms importante que influye en la absorcin del hierro es el contenido de hierro en las clulas de la mucosa intestinal (ferritina local). Es el llamado Bloqueo mucoso de Granick. La eritropoyesis en la mdula sea: que es un estado dinmico de consumo o no de hierro corporal. As, decae la absorcin del hierro cuando disminuye la eritropoyesis.
Hierro La absorcin del hierro en forma ferrosa tiene lugar en el duodeno y en el yeyuno superior, y requiere de un mecanismo activo que necesita energa. El hierro se une a glucoprotenas de superficie (o receptores especficos de la mucosa intestinal para el hierro), situadas en el borde en cepillo de las clulas intestinales. Luego se dirige al retculo endoplasmtico rugoso y a los ribosomas libres (donde forma ferritina) y posteriormente a los vasos de la lmina propia. Como puede deducirse, la absorcin del hierro es regulada por la mucosa intestinal, lo que impide que reservas excesivas de hierro se acumulen. La absorcin del hierro depende tambin de la cantidad de esta protena. El hierro se encuentra en prcticamente todos los seres vivos y cumple numerosas y variadas funciones. Hay distintas protenas que contienen el grupo hemo, que consiste en el ligando porfirina con un tomo de hierro. Algunos ejemplos: La hemoglobina y la mioglobina; la primera transporta oxgeno, O2, y la segunda, lo almacena. Los citocromos; los citocromos c catalizan la reduccin de oxgeno a agua. Los citocromos P450 catalizan la oxidacin de compuestos hidrofbicos, como frmacos o drogas, para que puedan ser excretados, y participan en la sntesis de distintas molculas. Las peroxidasas y catalasas catalizan la oxidacin de perxidos, H2O2, que son txicos.
Ejemplo de centro de una protena de Fe/S (ferredoxina) Las protenas de hierro/azufre (Fe/S) participan en procesos de transferencia de electrones. Tambin se puede encontrar protenas en donde tomos de hierro se enlazan entre s a travs de enlaces puente de oxgeno. Se denominan protenas Fe-O-Fe. Algunos ejemplos: Las bacterias metanotrficas, que emplean el metano, CH4, como fuente de energa y de carbono, usan protenas de este tipo, llamadas monooxigenasas, para catalizar la oxidacin de este metano. La hemeritrina transporta oxgeno en algunos organismos marinos. Algunas ribonucletido reductasas contienen hierro. Catalizan la formacin de desoxinucletidos. Los animales para transportar el hierro dentro del cuerpo emplean unas protenas llamadas transferrinas. Para almacenarlo, emplean la ferritina y la hemosiderina. El hierro entra en el organismo al ser absorbido en el intestino delgado y es transportado o almacenado por esas protenas. La mayor parte del hierro se reutiliza y muy poco se excreta. Tanto el exceso como el defecto de hierro, pueden provocar problemas en el organismo. El envenamiento por hierro ocurre debido a la ingesta exagerada de est (como suplemento en el tratamiento de anemias). La hemocromatosis corresponde a una enfermedad de origen gentico, en la cual ocurre una excesiva absorcin del hierro, el cual se deposita en el hgado, causando disfuncin de ste y eventualmente llegando a la cirrosis heptica. En las transfusiones de sangre, se emplean ligandos que forman con el hierro complejos de una alta estabilidad para evitar que quede demasiado hierro libre. Estos ligandos se conocen como siderforos. Muchos microorganismos emplean estos siderforos para captar el hierro que necesitan. Tambin se pueden emplear como antibiticos, pues no dejan hierro libre disponible.
Hierro
10
Istopos
El hierro tiene cuatro istopos estables naturales: 54Fe, 56Fe, 57Fe y 58Fe, Las abundancias relativas en las que se encuentran en la naturaleza son de aproximadamente: 54Fe (5,8%), 56Fe (91,7%), 57Fe (2,2%) y 58Fe (0,3%).
Precauciones
La siderosis es el depsito de hierro en los tejidos.El hierro en exceso es txico. El hierro reacciona con perxido y produce radicales libres; la reaccin ms importante es: Fe2+ + H2O2 Fe3+ + OH- + OH Cuando el hierro se encuentra dentro de unos niveles normales, los mecanismos antioxidantes del organismo pueden controlar este proceso. La dosis letal de hierro en un nio de 2 aos es de unos 3.1 g puede provocar un envenenamiento importante. El hierro en exceso se acumula en el hgado y provoca daos en este rgano.
Referencias
[1] http:/ / toolserver. org/ ~magnus/ cas. php?language=en& cas=7439-89-6& title= [2] Joan Corominas: Breve diccionario Etimolgico de la lengua castellana. 3 edicin, 1987. Ed. Gredos, Madrid. [3] (http:/ / en. wikipedia. org/ wiki/ Disodium_tetracarbonylferrate), Tetracarbonilferrato disdico en la Wikipedia inglesa.
Enlaces externos
Wikimedia Commons alberga contenido multimedia sobre HierroCommons. Wikcionario tiene definiciones para Hierro.Wikcionario Precios histricos del mineral de hierro, de acuerdo al FMI (http://www.indexmundi.com/es/ precios-de-mercado/?mercancia=mineral-de-hierro&meses=300) El hierro en aguas (http://www.xtec.net/~gjimene2/llicencia/students/bscw.gmd.de_bscw_bscw. cgi_d32809203-3_______Fe_final.html) Alto horno (http://www.coiim.es/enla/Industria/horno_alto.htm) WebElements.com - Iron (http://www.webelements.com/webelements/elements/text/Fe/index.html) EnvironmentalChemistry.com - Iron (http://environmentalchemistry.com/yogi/periodic/Fe.html) It's Elemental - Iron (http://education.jlab.org/itselemental/ele026.html) Los lamos National Laboratory - Iron (http://periodic.lanl.gov/elements/26.html) La farga catalana (en cataln) La Qumica de Referencia - Hierro (http://www.chemistry-reference.com/pdictable/q_elements. asp?language=es&Symbol=Fe) Cientficos vuelven el hierro transparente (http://www.abc.es/20120208/ciencia/ abci-cientificos-vuelven-hierro-transparente-201202081338.html)
Fuentes y contribuyentes del artculo
11
Fuentes y contribuyentes del artculo
Hierro Fuente: http://es.wikipedia.org/w/index.php?oldid=70331555 Contribuyentes: .Sergio, Adrixadrix, Adrruiz, Aepedraza, Aikurn, Alberto22598, Alchemist-hp, Aleator, Alelapenya, Alexav8, Alhen, Aloneibar, Alvaro qc, Andreasmperu, Antur, Arbeyu, Armonizador, Atayde13, Aulacopalpus256, BF14, Baiji, Bakasurvivor, Balderai, Banfield, Begueta250, Bernard, BlackBeast, Bonnot, BuenaGente, Dangelin5, Danielba894, Danielsan2099, David0811, Demin23, Der Knstler, DerKrieger, Dermot, Diamondland, Diegusjaimes, Dreitmen, Eduardosalg, Edub, El tiu Cancho, Ellinik, Er Komandante, Esp1986, Ezed0, Fede0428, Felipealvarez, Ferbr1, Fev, Filumestre, Floripaint, Foundling, FrancoGG, Gesvilsur, Gins90, Gogiva, Greek, HUB, Halfdrag, Hispa, Hprmedina, Huevos, Humberto, Ialad, Idiazabal26, Igna, Ikertza, Irvr, J.M.Domingo, JMCC1, Javierito92, Jkbw, Jmartipp, Joelfriky, Jonas Scrub, Jorge 2701, Jorge c2010, JorgeGG, Joseaperez, Joselarrucea, Josell2, Jsanchezes, Julie, Jurock, Kizar, KnightRider, Konas, Kouriquitaka, Kuanto, Laura Fiorucci, Leonpolanco, Limbo@MX, Lobo, Lucien leGrey, Luis Villodas, Mafores, Magister Mathematicae, Mansoncc, ManuelGR, Manuelt15, Marcelo, MarcoAurelio, Matdrodes, Mecamtico, Mel 23, Miss Manzana, Mister, Moriel, Mortadelo2005, Mowsseep, Mrteverett, Murphy era un optimista, Netito777, Nicholasraul, Nicholaus, Ninovolador, Nioger, Onixqwert, Ortisa, Osado, P. S. F. Freitas, Paintman, Pepealo 11, Petruss, PhJ, Pico pal q lee 2.0, Pipekane, Prietoquilmes, ProfesorFavalli, Purodha, Plux, Qoan, Rafael Soriano, Raulshc, Remux, Retama, Ricardo daniel estrada moreno, Ricardogpn, Rikardo gs, Roberto Fiadone, Rosarinagazo, RoyFocker, Rubpe19, Sanbec, Sasandres, Savh, Smrolando, Sms, SpeedyGonzalez, StormBringer, SuperBraulio13, Tafol, Tano4595, Technopat, Template namespace initialisation script, Tirithel, Tortillovsky, Triku, Truor, Txo, UA31, Ucevista, Untipopancho, Untrozo, Urdangaray, Utach, Vale210, Vic Fede, Vitamine, Vubo, Waka Waka, Wilfredor, Xvazquez, Yodigo, Yrithinnd, Zerabat, Zore, Zufs, 531 ediciones annimas
Fuentes de imagen, Licencias y contribuyentes
Archivo:Lattice body centered cubic.svg Fuente: http://es.wikipedia.org/w/index.php?title=Archivo:Lattice_body_centered_cubic.svg Licencia: desconocido Contribuyentes: Original uploader was Baszoetekouw at en.wikipedia Archivo:Capa electrnica 026 Hierro.svg Fuente: http://es.wikipedia.org/w/index.php?title=Archivo:Capa_electrnica_026_Hierro.svg Licencia: Creative Commons Attribution-Sharealike 3.0 Contribuyentes: Electron_shell_026_Iron.svg: Pumbaa (original work by Greg Robson) derivative work: Kizar Archivo:Fe,26.jpg Fuente: http://es.wikipedia.org/w/index.php?title=Archivo:Fe,26.jpg Licencia: GNU Free Documentation License Contribuyentes: User:RTC Archivo:The viaduct La Polvorilla, Salta Argentina.jpg Fuente: http://es.wikipedia.org/w/index.php?title=Archivo:The_viaduct_La_Polvorilla,_Salta_Argentina.jpg Licencia: Creative Commons Attribution 2.0 Contribuyentes: Ezarate, FlickreviewR, Gabo2012, JuTa, 3 ediciones annimas Archivo:Iron_electrolytic_and_1cm3_cube.jpg Fuente: http://es.wikipedia.org/w/index.php?title=Archivo:Iron_electrolytic_and_1cm3_cube.jpg Licencia: Free Art License Contribuyentes: Alchemist-hp (talk) ( www.pse-mendelejew.de) Archivo:Ferredoxina_4Fe-4S.png Fuente: http://es.wikipedia.org/w/index.php?title=Archivo:Ferredoxina_4Fe-4S.png Licencia: GNU Free Documentation License Contribuyentes: Original uploader was Untrozo at es.wikipedia Archivo:Commons-logo.svg Fuente: http://es.wikipedia.org/w/index.php?title=Archivo:Commons-logo.svg Licencia: logo Contribuyentes: SVG version was created by User:Grunt and cleaned up by 3247, based on the earlier PNG version, created by Reidab. Archivo:Wiktionary-logo-es.png Fuente: http://es.wikipedia.org/w/index.php?title=Archivo:Wiktionary-logo-es.png Licencia: logo Contribuyentes: es:Usuario:Pybalo
Licencia
Creative Commons Attribution-Share Alike 3.0 //creativecommons.org/licenses/by-sa/3.0/
You might also like
- Retratos y FigurasDocument165 pagesRetratos y FigurasgretagamondesNo ratings yet
- Robert OppenheimerDocument14 pagesRobert Oppenheimerkvg69No ratings yet
- Los Cuatros Fundamentos de La Atención-Anapanasatti SuttaDocument129 pagesLos Cuatros Fundamentos de La Atención-Anapanasatti SuttaPilates Fit In100% (2)
- Cultura Libre - LAWRENCE LESSIGDocument375 pagesCultura Libre - LAWRENCE LESSIGalfredovpangueNo ratings yet
- GermanioDocument6 pagesGermanioGriffin EpgNo ratings yet
- Cultura Libre - LAWRENCE LESSIGDocument375 pagesCultura Libre - LAWRENCE LESSIGalfredovpangueNo ratings yet
- Cultura Libre - LAWRENCE LESSIGDocument375 pagesCultura Libre - LAWRENCE LESSIGalfredovpangueNo ratings yet
- Cultura Libre - LAWRENCE LESSIGDocument375 pagesCultura Libre - LAWRENCE LESSIGalfredovpangueNo ratings yet
- Cultura Libre - LAWRENCE LESSIGDocument375 pagesCultura Libre - LAWRENCE LESSIGalfredovpangueNo ratings yet
- Vs CopyrightDocument99 pagesVs CopyrightGerar Muz100% (1)
- ArsénicoDocument8 pagesArsénicoGriffin EpgNo ratings yet
- HidrógenoDocument12 pagesHidrógenoGriffin EpgNo ratings yet
- CromoDocument7 pagesCromoGriffin EpgNo ratings yet
- CobreDocument33 pagesCobreGriffin EpgNo ratings yet
- GalioDocument5 pagesGalioGriffin EpgNo ratings yet
- CloroDocument7 pagesCloroGriffin EpgNo ratings yet
- CincDocument11 pagesCincGriffin EpgNo ratings yet
- NíquelDocument6 pagesNíquelGriffin EpgNo ratings yet
- PotasioDocument8 pagesPotasioGriffin EpgNo ratings yet
- ManganesoDocument6 pagesManganesoGriffin EpgNo ratings yet
- Van AdioDocument10 pagesVan AdioGriffin EpgNo ratings yet
- Cobalt oDocument9 pagesCobalt oGriffin EpgNo ratings yet
- TitanioDocument15 pagesTitanioGriffin EpgNo ratings yet
- ArgónDocument4 pagesArgónRodny LópezNo ratings yet
- EscandioDocument5 pagesEscandioGriffin Epg100% (1)
- AzufreDocument7 pagesAzufreGriffin EpgNo ratings yet
- CalcioDocument7 pagesCalcioGriffin EpgNo ratings yet
- FósforoDocument5 pagesFósforoGriffin EpgNo ratings yet
- Si LicioDocument8 pagesSi LicioWalter LemusNo ratings yet
- Penman-MonteithDocument8 pagesPenman-MonteithFreddy Vargas RiveraNo ratings yet
- Modelo Humanista ExistencialDocument29 pagesModelo Humanista ExistencialJuan Jose ZarazuaNo ratings yet
- Act3 Fabricio NoriegaDocument3 pagesAct3 Fabricio NoriegaFabricio NoriegaNo ratings yet
- ShockDocument34 pagesShockNorma Beatriz CenturionNo ratings yet
- Qué Es La QuímicaDocument6 pagesQué Es La QuímicaLuis VillanuevaNo ratings yet
- Consorcio Salud Amarilis: Valorizacion de Ioarr #04Document96 pagesConsorcio Salud Amarilis: Valorizacion de Ioarr #04DANIEL MALLQUI DIAZNo ratings yet
- Anexo A - Marco TeóricoDocument5 pagesAnexo A - Marco TeóricoManuela Cuervo ArangoNo ratings yet
- Análisis de confiabilidad de un sistema estructural mediante simulación Monte Carlo y método Rackwitz-FiesslerDocument18 pagesAnálisis de confiabilidad de un sistema estructural mediante simulación Monte Carlo y método Rackwitz-FiesslermchaindlNo ratings yet
- Proyecto Investigacion de Mercados Parte 1Document38 pagesProyecto Investigacion de Mercados Parte 1Jhonatan Carvajal QuiñonesNo ratings yet
- Serie BlancaDocument14 pagesSerie BlancaTon SalmonNo ratings yet
- ENCUESTA PizzeriaDocument2 pagesENCUESTA PizzeriaChristian Lazo Quispe85% (13)
- HDS Chile Clorox® Disinfecting Mist Multi-Surface-Eucalyptus Pepermint-Lemongrass MandarinDocument7 pagesHDS Chile Clorox® Disinfecting Mist Multi-Surface-Eucalyptus Pepermint-Lemongrass MandarinEvelyn OrellanaNo ratings yet
- Rehabilitación Del Servicio de Agua Del Sector de Riego Almapampa Garlero, Distrito de Huarmey, Provincia de Huarmey, Departamento de AncashDocument2 pagesRehabilitación Del Servicio de Agua Del Sector de Riego Almapampa Garlero, Distrito de Huarmey, Provincia de Huarmey, Departamento de AncashJHON WILLYNo ratings yet
- 1-COL-PB-LAPAZ-009 Ejecución de Dovelas en VoladizosDocument34 pages1-COL-PB-LAPAZ-009 Ejecución de Dovelas en VoladizosCormedes copaso100% (1)
- Según La Organización Mundial de La SaludDocument1 pageSegún La Organización Mundial de La SaludMilene VillacortaNo ratings yet
- HUAWEI Y7a Gu A de Inicio R Pido - (PPA-LX3, EMUI10.1.1 - 01, Es-Us)Document18 pagesHUAWEI Y7a Gu A de Inicio R Pido - (PPA-LX3, EMUI10.1.1 - 01, Es-Us)Ce Ga Bo100% (1)
- Ensayo Carbohidratos 1Document6 pagesEnsayo Carbohidratos 1AndrESNo ratings yet
- Enfermedad de PagetDocument47 pagesEnfermedad de PagetJesús Ruiz PovedaNo ratings yet
- Módulo 4 - Lineamientos para La Planificación Dietética Nutricional PDFDocument24 pagesMódulo 4 - Lineamientos para La Planificación Dietética Nutricional PDFNeisser Arquimedes Alegria ChavezNo ratings yet
- Informe Final Piloto Cocinas Mejoradas Sartimbama 23 02 2015Document5 pagesInforme Final Piloto Cocinas Mejoradas Sartimbama 23 02 2015Richard VegaNo ratings yet
- Programa de Capacitaciòn 2006 SURATEPDocument6 pagesPrograma de Capacitaciòn 2006 SURATEPfadesaNo ratings yet
- Enfermedades NeurodegenerativasDocument6 pagesEnfermedades NeurodegenerativasNaida Kamila Garay MachucaNo ratings yet
- Porque El Agua Del Mar Se EvaporaDocument1 pagePorque El Agua Del Mar Se EvaporaBenjaminNo ratings yet
- Sistema Nervioso Periférico. Plexo Braquial y LumbosacroDocument9 pagesSistema Nervioso Periférico. Plexo Braquial y LumbosacroJulio César Amarilla100% (1)
- TesisDocument87 pagesTesisGuillermoNo ratings yet
- Guia de Arquitectura - Colsanitas-IIIADocument5 pagesGuia de Arquitectura - Colsanitas-IIIAKaren PérezNo ratings yet
- F29-Anverso: XX - XXX.XXX-XDocument15 pagesF29-Anverso: XX - XXX.XXX-Xaudicon2011No ratings yet
- Los-Ácidos-Nucleicos-Martes 22-09 - 4to-Grado-de-SecundariaDocument4 pagesLos-Ácidos-Nucleicos-Martes 22-09 - 4to-Grado-de-SecundariaYuri Ramos100% (1)
- Ética Profesional en El Uso de Las Pruebas PsicométricasDocument2 pagesÉtica Profesional en El Uso de Las Pruebas PsicométricasAlan VenebraNo ratings yet
- Sunafil DenunciaDocument15 pagesSunafil DenunciaAnonymous lq5ndptvm0% (1)