Professional Documents
Culture Documents
98 565
Uploaded by
hizballah27Original Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
98 565
Uploaded by
hizballah27Copyright:
Available Formats
Pédiatrie
B 258
Dystrophie musculaire
de Duchenne
Syndrome de l’X fragile
Épidémiologie, génétique, diagnostic
Dr Stéphane PINSON, Pr Henri PLAUCHU
Service de génétique, Hospices civils de Lyon, 1, place de l’Hôpital, 69288 Lyon cedex 02.
UFR, Rth Laennec, Université Claude-Bernard, Lyon I.
DYSTROPHIE MUSCULAIRE lité et une trophicité normales. Il apprend à marcher sans
DE DUCHENNE retard caractéristique mais lorsqu’il se relève de la posi-
tion accroupie, il doit s’appuyer sur ses genoux pour se
redresser : c’est le signe de Gowers. Il trébuche fréquem-
Points Forts à comprendre ment et il garde toujours un appui pour monter les marches
d’escaliers, une à une. L’examen clinique est pauvre et ne
révèle que des masses musculaires diminuées et un peu
• Cette maladie décrite par Duchenne de Boulogne fibreuses à la palpation méticuleuse de l’enfant. La signi-
à la fin du siècle dernier correspond ficative pseudo-hypertrophie des mollets apparaît plus tar-
à la génopathie musculaire la plus fréquente. divement. Lorsque l’on évoque la maladie, la forte éléva-
• Elle ne touche que les garçons et appartient, tion des créatines-kinases musculaires (de 20 à 100 fois les
avec l’X fragile et l’hémophilie, aux trois maladies valeurs normales) oriente fortement vers le diagnostic.
génétiques liées au sexe les plus fréquentes. L’électromyogramme permet de confirmer une atteinte
• Cette dystrophie musculaire est progressivement myogène. La biopsie musculaire n’apporte que des élé-
évolutive vers la mort avant l’âge adulte. ments indirects de diagnostic de dystrophie musculaire
(atrophie myogène, nécrose, fibrose lipoïdique). L’utilisa-
tion d’anticorps spécifiques anti-dystrophine permet d’être
affirmatif et d’établir un pronostic grave.
Épidémiologie
Dans la dystrophie de Duchenne, on ne retrouve pas de
L’incidence de la maladie est de l’ordre de 1/3 500 à marquage par les anticorps puisque la dystrophie est tota-
1/4 500 garçons nés vivants. La fréquence de cette maladie lement absente de la fibre musculaire, son évolution va se
étant stable depuis plus de 30 ans alors que les hommes poursuivre inéluctablement vers l’insuffisance musculaire
malades ne deviennent jamais pères de famille, il faut donc des ceintures, avec des variations d’un garçon à l’autre. Les
admettre un taux de mutation élevé pour expliquer le main- rétractions tendineuses achiléennes mettent les pieds en
tien du stock de gènes délétés d’une population. L’appari- équinisme, un flessum de hanche s’installe et l’enfant prend
tion d’une mutation de novo est en cause pour un tiers des ainsi une démarche dandinante « en canard » sur la pointe
cas sporadiques. Les mères de ces enfants sont déjà conduc- des pieds, avec une lordose pour rétablir l’équilibre fragile.
trices de la mutation dans deux tiers des cas et sont le plus L’atrophie musculaire des quadriceps précipite, en géné-
souvent asymptomatiques. Les formes familiales, avec ral, l’enfant vers le fauteuil roulant entre 8 et 12 ans. Cette
atteinte de plusieurs enfants, ne concernent que 20 à 30 % immobilisation accélère l’installation de rétractions irré-
des enfants malades, car l’atteinte réduite aux garçons et ductibles des membres inférieurs. Le risque d’une scoliose
les petites fratries limitent l’extériorisation familiale. La très évolutive est important, et peut être aggravé par une
myopathie de Duchenne est une maladie génétique réces- obésité intercurrente. La scolarisation devient probléma-
sive liée au sexe ne touchant que des garçons apparentés tique, d’autant que l’on retrouve des difficultés intellec-
de façon matrilinéaire dans une même famille. tuelles chez un tiers des garçons. La prise en charge de ces
patients, psychologiquement lourde, demeure principale-
Génétique ment symptomatique comprenant la kinésithérapie pour
L’examen clinique des malades à la naissance ne montre lutter contre les rétractions, le traitement précoce chirur-
aucune anomalie apparente : le garçon présente une mobi- gical de la scoliose et la prévention des troubles trophiques
LA REVUE DU PRATICIEN (Paris) 565
1998, 48
DY S T R O P H I E M U S C U L A I R E D E D U C H E N N E - S Y N D R O M E D E L’ X F R A G I L E
et vasomoteurs. Elle n’empêche pas son extension à la cein- 1. Diagnostic moléculaire
ture scapulaire qui réduit l’usage des membres supérieurs Les méthodes d’étude directe sont entreprises, après un
du jeune adolescent. C’est l’atteinte du muscle cardiaque simple prélèvement sanguin, sur l’ADN lymphocytaire du
et des muscles respiratoires qui met en jeu le pronostic vital garçon atteint, et après consentement éclairé des parents.
nécessitant une prise en charge nocturne puis permanente Les macrodélétions sont recherchées par PCR et Southern
de l’insuffisance respiratoire. blot et maintenant à l’aide des microsatellites. Il est envi-
Pour les mères conductrices, l’inactivation de l’X porteur sageable de chercher une délétion chez un fœtus masculin
de la mutation n’étant jamais totale (courbe de Gauss), il dans une famille sans garçon atteint survivant. Ce résultat
est possible de retrouver chez ces femmes vectrices une est toujours limité puisque l’on ne retrouve une mutation
fibrose du mollet, une petite faiblesse musculaire ou une de type délétion que dans 65 % des cas. Mais la recherche
augmentation discrète de leur CK (1,5 à 10 fois la normale) de mutations ponctuelles et des microdélétions n’est pas
qui doit être considérée comme un indice du statut de trans- actuellement l’objet d’une détection accessible aux clini-
mettrice. Les femmes conductrices ont un risque de 1 sur ciens.
2 de transmettre la maladie à leurs futurs garçons.
Le gène responsable a été localisé sur le bras court de l’X, 2. Diagnostic des conductrices
en Xp21 et a été dénommé DYS en raison de la dystrophie Lorsqu’un garçon est atteint de façon sporadique dans la
qu’entraîne son altération. Il comprend 2,3 millions de famille, il s’agit d’une mutation « de novo », une fois sur
paires de bases, soit 1 % du chromosome X et presque trois. Dans l’autre situation, la mère est conductrice. Si
1 p. 1000 du génome. C’est le plus grand gène humain aucune délétion n’est trouvée chez le garçon, il n’est pas
connu actuellement. Il se compose de 76 exons et est trans- possible de conclure sur la réalité du caractère conducteur
crit en un ARN de seulement 14 000 bases. L’étude de la de la mère. Devant une forme familiale, une étude molé-
transcription de ce gène a aussi montré qu’il existe un épis- culaire indirecte permet, selon la structure familiale, d’éta-
sage différentiel entraînant la coexistence dans une même blir le statut des femmes potentiellement conductrices de
cellule de nombreuses versions de la dystrophine. Leurs la famille qui le demandent. On identifie l’haplotype de
lieux d’action éventuellement spécifiques expliqueraient l’X porteur du gène muté en comparant les haplotypes de
les différentes manifestations cliniques, et l’atteinte men- l’X chez les sujets malades et les sujets sains de cette
tale. famille. C’est l’étude de la transmission de l’X « patholo-
Différents types de mutations responsables de la maladie gique » dans la famille qui permettra de reconnaître indi-
ont été décrits. Une grande délétion intragénique de plu- rectement les vectrices parmi les conductrices possibles.
sieurs milliers de paires de bases est retrouvée chez 65 % Si une délétion était trouvée chez un garçon malade, l’étude
des patients. Celle-ci survient essentiellement en certains directe, sur les deux X de sa mère, de la région de la délé-
« points chauds » du gène facilitant sa recherche. Les autres tion permet parfois de reconnaître directement les conduc-
mutations du gène (35 %) correspondent à des duplications trices. Une consultation de conseil génétique est indispen-
ou délétions partielles, des microdélétions de quelques sable, avant le début des investigations, afin d’expliquer les
bases ou des mutations ponctuelles. L’apparition des muta- difficultés et les limites de ces examens, et de recueillir la
tions entraîne deux types d’anomalies : soit elles font appa- participation des sujets informatifs de la famille et leur
raître un codon stop qui interrompt la synthèse de la pro- consentement. La transmission des résultats de l’étude
téine, soit elles décalent le cadre de lecture (duplication ou familiale s’accompagnera de l’explication de la notion de
délétion d’un nombre de bases différent de 3 ou d’un mul- crossing-over dont la survenue modifie la fiabilité des ana-
tiple) et entraînent une perturbation importante de la pro- lyses. Le diagnostic prénatal, s’il est demandé, devra être
téine qui est rapidement dégradée. organisé dans les meilleures conditions pour tous.
La protéine codée, appelée dystrophine, est présente nor- 3. Diagnostic prénatal
malement en très faible quantité dans le muscle, mais fait
partie des protéines indispensables du cytosquelette des Sa réalisation dépend de toute la démarche familiale
myocytes. Son rôle est capital dans l’attachement des fila- décrite, avant la grossesse, afin que les parents possèdent
ments d’actine des fibres musculaires à la membrane cyto- toutes les informations nécessaires. Si un diagnostic pré-
plasmique. La recherche directe des mutations ponctuelles natal est demandé sans qu’une étude familiale ne soit pos-
reste encore du domaine théorique. Mais l’étude haploty- sible (garçon malade décédé) ou n’ait été faite, il n’y a pas
pique des chromosomes X bénéficie de l’existence de nom- d’étude directe fiable possible chez le fœtus masculin
breux polymorphismes intra- et juxtagéniques permettant attendu, contrairement à l’hémophilie ou à l’X fragile. La
d’utiliser une batterie de sondes microsatellites adaptées à recherche d’une macrodélétion possible, réalisable sur la
chaque situation familiale (voir : pour approfondir / 1). notion d’antécédent très précis, se révèle trop hasardeuse.
Elle est cependant la seule façon d’aider à conserver une
grossesse remise en cause par la décision des parents devant
le risque existant.
Diagnostic
4. Diagnostic différentiel
Le diagnostic positif de la maladie est avant tout clinico- Devant un jeune garçon hypotonique et ayant un taux de
biologique. créatine kinase élevé, il faut écarter le diagnostic de myo-
566 LA REVUE DU PRATICIEN (Paris)
1998, 48
Pédiatrie
pathie congénitale et penser à une dystrophie musculaire
congénitale à l’aide surtout de la biopsie. Devant un ado- • Comme pour toute maladie liée à l’X,
lescent qui n’évolue pas gravement comme une myopathie l’établissement de l’haplotype des X
de Duchenne, selon les investigations paracliniques, il fau- par les marqueurs moléculaires permet une étude
dra penser à une forme allélique de Becker (faible fixation indirecte des familles. Les données informatives
des anticorps anti-DYS sur le muscle et mutation-délétion peuvent permettre l’identification du caractère
ne compromettant pas la totalité de la fonction du gène conducteur de femmes en âge de procréer.
DYS). ■ • La survenue sporadique de la dystrophie
musculaire de Duchenne chez un garçon pose
la question d’une récurrence familiale puisque
la mère est conductrice avec une probabilité
de 2 sur 3.
• Les familles touchées ne peuvent bénéficier d’un
Points Forts à retenir diagnostic prénatal que si l’étude en génétique
moléculaire est réalisée et est informative.
• Le conseil génétique est l’acte médical
• La dystrophie musculaire de Duchenne est une responsable de l’étude familiale, de la transmission
myopathie sévère des ceintures touchant le jeune des résultats expliqués, de l’écoute de la demande
garçon et évoluant vers la mort précoce de diagnostic prénatal par un couple et de son
par l’atteinte cardiorespiratoire. éventuelle mise en place avec suivi et soutien.
• La dystrophie musculaire de Duchenne est une
maladie fréquente à transmission récessive liée
à l’X. Le gène DYS responsable est altéré 65 fois
POUR EN SAVOIR PLUS
sur 100 par une grande délétion identifiable. Eberhard Passarge. Atlas de poche de Génétique. Paris :
Médecine-Sciences Flammarion, 1995.
Le reste des mutations correspond à des lésions
moléculaires plus petites qui restent méconnues. Kaplan JC, Delpech M. Biologie moléculaire et médecine,
2e édition. Paris : Médecine-Sciences Flammarion, 1993 :
Aucun diagnostic direct n’est alors disponible. 386-404.
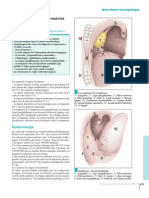
SYNDROME DE L’X FRAGILE Sémiologie clinique
Classiquement, la définition du syndrome repose sur une
triade de signes cliniques qui ne sont ni spécifiques, ni
Points Forts à comprendre constants.
1. Retard mental et signes neuropsychiques
• Le syndrome de l’X fragile est défini • La déficience intellectuelle est pratiquement constante
par un retard mental lié au chromosome X, mais de gravité variable allant de l’intelligence subnormale
s’accompagnant parfois d’un morphotype à la débilité profonde, souvent associée à des troubles du
particulier et d’une macro-orchidie. langage.
• La découverte au locus de l’X fragile • Les troubles psychiatriques sont caractérisés par des
d’un nouveau type de mutation dite instable troubles du comportement : instabilité psychomotrice ou
a permis de localiser le gène en cause : FMR1 « autisme » retrouvé chez la moitié des enfants de moins
(Fragile X Mental Retardation). de 30 mois.
• Les signes neurologiques sont définis par un retard psy-
chomoteur avec hypotonie, retard d’acquisition de la sta-
tion assise et difficulté à la marche. Mais il peut n’appa-
raître qu’à l’entrée en milieu scolaire. Une comitialité est
Épidémiologie retrouvée dans 20 % des cas, parfois maligne.
La maladie de l’X fragile a une incidence estimée à envi-
ron 1/4 000 chez les hommes ; elle est aussi responsable de 2. Syndrome dysmorphique de la face
retard mental léger à modéré chez la femme avec une inci- et du crâne
dence estimée à 1/7 000. On peut donc estimer à environ Il permet d’évoquer le diagnostic en donnant à ces sujets
10 000 le nombre de patients atteints en France. Cette mala- un « air de famille » : un visage allongé (front haut, hypo-
die correspond à la forme de retard mental héréditaire la plasie de l’étage moyen) associé à des lèvres épaisses et de
plus fréquente en France. grandes oreilles mal ourlées.
LA REVUE DU PRATICIEN (Paris) 567
1998, 48
DY S T R O P H I E M U S C U L A I R E D E D U C H E N N E - S Y N D R O M E D E L’ X F R A G I L E
3. Macro-orchidie post-pubertaire nière éventualité n’est pas obligatoire mais semble surve-
Elle s’observe dans 80 % des cas. Elle est généralement nir avec une probabilité dépendant de la taille de la pré-
importante, supérieure à 30 mL et isolée, sans anomalie mutation. Plus la taille de la prémutation portée par la mère
endocrine. Des signes de dysplasie du tissu conjonctif peu- est importante, plus le risque d’avoir un enfant avec une
vent s’associer (hernies). mutation complète est grand (une prémutation de grande
taille, 90 CGG et plus par exemple, entraîne un risque de
• Femmes conductrices transformation en mutation complète supérieur à 50 % pour
Elles ont un morphotype normal mais 40 à 60 % d’entre chaque grossesse avec l’X pathologique).
elles ont un retard mental, léger, dominé par un retard 3. Retard mental léger avec site fragile FRAX-E
du langage. Un second site fragile, beaucoup plus rare, FRAX-E a été
récemment décrit chez des familles avec un retard mental
Génétique de l’X fragile léger. Il est localisé au même endroit (Xq27.3) et présente
le même biais maternel de transmission de l’expansion. Il
La fragilité caractéristique de l’X fut individualisée grâce
est caractérisé par l’existence d’une expansion identique
à l’analyse du caryotype en milieu révélateur pauvre en
au niveau d’un gène voisin récemment identifié : FMR2.
acide folique. Le site fragile « FRAX-A » est localisé en
Le retard mental est modéré et les filles en général, ne sont
Xq27.3.
pas atteintes.
1. Défaut moléculaire
Il correspond à l’amplification anormale d’une séquence Diagnostic de l’X fragile
instable de trinucléotides CGG localisés dans le premier La découverte de la mutation responsable du syndrome X
exon (non traduit) du gène FMR 1 entraînant l’inactivation fragile a modifié le conseil génétique permettant le dia-
de ce gène. Ce gène code une protéine cytoplasmique asso- gnostic de la maladie, la détection des personnes à risque
ciée aux ribosomes pouvant lier des ARN. Elle pourrait de la transmettre et le diagnostic prénatal en l’absence de
jouer un rôle dans la régulation de la traduction de certains traitement. On utilise, actuellement, l’analyse de l’ADN
ARN messagers. Ce nouveau type de mutation instable per- afin de faire le diagnostic (prélèvement de sang périphé-
met d’expliquer le mode inhabituel de transmission, avec rique, de villosités choriales ou de cellules amniotiques).
augmentation du risque de développer la maladie au cours Deux stratégies complémentaires peuvent être utilisées :
des générations successives dans une même famille (phé- l’analyse directe de la mutation et l’analyse indirecte par
nomène d’anticipation). La taille de l’amplification étude de la transmission de marqueurs polymorphiques liés
influence l’expression phénotypique. L’amplification évo- au locus X fragile. L’analyse indirecte est nécessaire pour
lue différemment selon le sexe du parent transmetteur. Chez l’interprétation fine du résultat d’analyse directe, particu-
le sujet normal, la répétition est polymorphique (n = 6 à 50 lièrement en cas de contamination maternelle d’un prélè-
CGG). Les mutations complètes correspondent à des vement de fœtus féminin (voir : pour approfondir / 1).
expansions importantes allant de 230 à plus de 1 000 CGG 1. Analyse directe
et sont associées à une méthylation anormale de la répéti- • La technique de Southern-Blot permet la mise en évi-
tion CGG et des séquences d’ADN environnantes. Ces phé- dence des mutations et prémutations par analyse de la
nomènes entraînent un retard mental chez 100 % des migration de l’ADN après l’action d’enzymes de restric-
hommes, et 40 à 60 % des femmes hétérozygotes. Les pré- tion. Elle permet de connaître la taille de l’expansion et son
mutations sont des expansions intermédiaires (60 à envi- état de méthylation, mais cette méthylation est absente au
ron 200 CGG) non méthylées. Elles n’entraînent pas la terme gestationnel habituel d’un prélèvement sur villosi-
maladie mais semblent la « préparer ». Elles sont retrou- tés choriales. Les allèles normaux et les petites prémuta-
vées chez les hommes « sains » transmetteurs et chez la tions peuvent être analysés par amplification génique
majorité des femmes vectrices sans retard mental. On (PCR) de la zone où se trouve la mutation. Cela permet
remarquera la difficulté d’interprétation des zones inter- d’exclure la présence d’une mutation complète par la détec-
médiaires pour lesquelles les connaissances restent incer- tion de l’allèle maternel normal chez un fœtus masculin,
taines (de 50 à 60 CGG et de 200 à 230). ou de voir une hétérozygotie chez un fœtus féminin (la
2. Transmission connaissance des allèles des parents est indispensable).
L’expression de l’anomalie dépend de l’origine parentale 2. Analyse indirecte
de la transmission. Elle repose sur la notion de coségrégation entre le gène
• Quand le père transmet la séquence, elle est peu modi- muté et des marqueurs génétiques polymorphiques (micro-
fiée. Un homme normal transmetteur, donc porteur d’une satellites) situés au voisinage du locus morbide de l’X fra-
prémutation, la transmet, inchangée, à toutes ses filles nais- gile (entourant les répétitions CGG). Il s’agit d’une
sant vectrices. Le risque d’avoir des enfants atteints n’ap- méthode fiable si la famille est informative, nécessitant peu
paraîtra qu’à la génération suivante. d’ADN, et donnant des résultats rapides. Elle permet de
• Quand la mère transmet la séquence, on assiste généra- pister le chromosome X muté maternel et de rassurer rapi-
lement à une augmentation du nombre de répétitions, soit dement quand le fœtus a hérité de l’haplotype maternel
par augmentation de la taille de la prémutation, soit en pas- sain. De rares crossing-over sont possibles expliquant un
sant d’une prémutation à une mutation complète. Cette der- faux résultat qui doit être vérifié par analyse directe. ■
568 LA REVUE DU PRATICIEN (Paris)
1998, 48
Pédiatrie
Points Forts à retenir • Cette situation très conflictuelle de la médecine et l’évolution socio-
médicale depuis la loi sur l’interruption volontaire de grossesse de 1975,
ont conduit à une « anti-médecine », le diagnostic prénatal, quand il
conduit à une interruption de grossesse. Celle-ci est alors faite dans le but
La possiblité d’un diagnostic fiable pour l’X de soulager les parents d’une grande souffrance, mais au détriment d’une
fragile est à mettre au service des familles pour vie, c’est une décision éthiquement difficile qui doit être prise directe-
éviter une récurrence en attendant une thérapie ment avec chaque couple.
efficace. Cela oblige à penser à ce diagnostic • Ce diagnostic ne peut pas être une fin en soi mais n’est qu’une étape
temporaire en attendant le succès de la thérapie génique. Comme tout
devant un retard mental, en particulier chez le défaut génétique « constitutionnel » dû à l’anomalie d’une protéine struc-
garçon, et a fortiori devant une forme familiale. turelle, l’espoir thérapeutique repose sur l’utilisation du gène normal,
comme « médicament ». Chaque traitement génétique nécessite l’élabo-
ration d’un vecteur adapté au gène transféré et à son fonctionnement ulté-
rieur. L’immense taille du gène DYS constitue un obstacle majeur à son
intégration dans un vecteur et à son transport vers les cellules atteintes.
POUR APPROFONDIR
POUR EN SAVOIR PLUS
1 / Conseil génétique Cossée M, Moutou C, Biancalana V et al. Le syndrome X
fragile est encore méconnu : efficacité du diagnostic
• La loi de bioéthique du 29 juillet 1994 rend obligatoire la consultation moléculaire chez les proposants avec retard mental. Arch
du conseil génétique avant tout acte de diagnostic prénatal. Pediatr 1997 ; 4 : 227-36.
• Elle exige qu’une information adaptée à chaque cas et comprenant une Forestier F, Schorderet DF. Diagnostics prénatals et bio-
logie moléculaire. Éditions Médicales Internationales,
explication des risques et des limites de chaque examen proposé soit déli- 1997.
vrée au préalable. Mandel JL, Biancalana V. Diagnostic anténatal du syn-
• Et elle oblige, de la part du médecin, de recueillir un consentement écrit drome X fragile. Chapitre 5.
du patient pour lequel est entreprise une étude génétique spécifique. Romana SP, Gérard B. Indications de l’analyse des chro-
mosomes et de l’ADN pour le diagnostic des maladies
• Comme c’est souvent le cas pour les maladies génétiques, les progrès génétiques. Nouvelle question de l’internat, numéro 261.
réalisés dans la connaissance du gène apportent actuellement des possi- Rev Prat (Paris) 1997 ; 47 : 1241-52.
bilités diagnostiques avant de déboucher sur une solution thérapeutique.
LA REVUE DU PRATICIEN (Paris) 569
1998, 48
You might also like
- 98 999Document4 pages98 999hizballah27No ratings yet
- 98 1011Document7 pages98 1011hizballah27100% (1)
- 98 1003Document7 pages98 1003hizballah27No ratings yet
- 98 905Document4 pages98 905hizballah27No ratings yet
- 98 987Document3 pages98 987hizballah27No ratings yet
- Antagonistes Des Récepteurs H Et Inhibiteurs de La Pompe À ProtonsDocument6 pagesAntagonistes Des Récepteurs H Et Inhibiteurs de La Pompe À Protonshizballah27No ratings yet
- 98 909Document3 pages98 909hizballah27No ratings yet
- 98 991Document7 pages98 991hizballah27No ratings yet
- 98 887Document5 pages98 887hizballah27100% (1)
- 98 919Document5 pages98 919hizballah27No ratings yet
- 98 899Document6 pages98 899hizballah27No ratings yet
- 98 689Document5 pages98 689hizballah27No ratings yet
- 98 881Document5 pages98 881hizballah27No ratings yet
- 98 913Document6 pages98 913hizballah27No ratings yet
- 98 805Document5 pages98 805hizballah27No ratings yet
- 98 802Document3 pages98 802hizballah27No ratings yet
- 98 875Document5 pages98 875hizballah27No ratings yet
- 98 765Document5 pages98 765hizballah27No ratings yet
- 98 781Document5 pages98 781hizballah27No ratings yet
- 98 787Document10 pages98 787hizballah27No ratings yet
- 98 667Document4 pages98 667hizballah27No ratings yet
- 98 679Document6 pages98 679hizballah27No ratings yet
- 98 771Document6 pages98 771hizballah27100% (1)
- 98 797Document5 pages98 797hizballah27No ratings yet
- 98 685Document3 pages98 685hizballah27No ratings yet
- 98 671Document4 pages98 671hizballah27No ratings yet
- 98 657Document3 pages98 657hizballah27No ratings yet
- 98 653Document4 pages98 653hizballah27No ratings yet
- Lipothymie, Syncope Et Perte de Connaissance Brève: Orientation DiagnostiqueDocument4 pagesLipothymie, Syncope Et Perte de Connaissance Brève: Orientation Diagnostiquehizballah27100% (1)
- 98 661Document6 pages98 661hizballah27No ratings yet
- 14 - Hémorragies Digestives HautesDocument3 pages14 - Hémorragies Digestives Hautesrazorghot1No ratings yet
- Muskelstimulering BEURER EMS TENS EM49 Manual - Part17Document3 pagesMuskelstimulering BEURER EMS TENS EM49 Manual - Part17nilsNo ratings yet
- Kiné PassivDocument25 pagesKiné PassivSelem Moussa100% (2)
- ABLS ESP 2014 VF29Sept2014Document130 pagesABLS ESP 2014 VF29Sept2014Brenda SilvestreNo ratings yet
- Prévention Drogues Et DépendancesDocument5 pagesPrévention Drogues Et DépendancesmecherguiNo ratings yet
- Notice Tirlor 10mg Comp B 20Document1 pageNotice Tirlor 10mg Comp B 20hawaceNo ratings yet
- Vitamine B12 Anti Cancer Coment en Obtenir NaturellementDocument2 pagesVitamine B12 Anti Cancer Coment en Obtenir Naturellementzakaria zakoNo ratings yet
- Annie Anzieu12Document169 pagesAnnie Anzieu12Frans TassignyNo ratings yet
- Les Troubles Du Rythme Et de La Conduction CardiaqueDocument53 pagesLes Troubles Du Rythme Et de La Conduction CardiaqueBMA-medecine100% (8)
- 2016-5 DESC PAP ALR Main - Doigts 2ème PartieDocument21 pages2016-5 DESC PAP ALR Main - Doigts 2ème PartieProfesseur Christian DumontierNo ratings yet
- Vocabulaire de La PreventionDocument29 pagesVocabulaire de La PreventionMame Médoune Dieuguène100% (3)
- Anomalies Du Cycle MenstruelDocument46 pagesAnomalies Du Cycle MenstruelIdiAmadouNo ratings yet
- Exploration de L'insightDocument34 pagesExploration de L'insightTheviolonistNo ratings yet
- 2008 Questionnaire SDIALOR - Instrument de Mesure de La Satisfaction Des Patients en Dialyse SDIALOR - A Dialysis Patient Satisfaction QuestionnaireDocument12 pages2008 Questionnaire SDIALOR - Instrument de Mesure de La Satisfaction Des Patients en Dialyse SDIALOR - A Dialysis Patient Satisfaction QuestionnaireMedgen GrupoNo ratings yet
- Chirurgie de La CataracteDocument2 pagesChirurgie de La CataracteFoued DelleliNo ratings yet