Professional Documents
Culture Documents
Manual de Prácticas de Química Orgánica I: - Miguel Ángel García Sánchez
Uploaded by
Florencia RenteríaOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Manual de Prácticas de Química Orgánica I: - Miguel Ángel García Sánchez
Uploaded by
Florencia RenteríaCopyright:
Available Formats
Manual de prcticas de
qumica orgnica I
Miguel ngel Garca Snchez
UNIVERSIDAD AUTONOMA METROPOLITANA
UNIDAD IZTAPALAPA
Casa abierta al tiempo
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Miguel ngel Garca Snchez
naci en la ciudad de Mxico el
25 de marzo de 1965. Es
egresado de la Universidad
Autnoma Metropolitana,
donde obtuvo el ttulo de
qumico en el ao de 1990.
Culmin estudios de maestra en
Qumica (Inorgnica) en 1993 y actualmente est
prximo a presentar su tesis de doctorado en la
misma institucin. Ha sido profesor en la UAM-I
desde 1990 y profesor de la FES-Zaragoza de la
UNAM de 1992 a 1996. En ambas instituciones ha
impartido diversos cursos de ramas de la qumica.
Es autor de tres artculos de investigacin
publicados en revistas internacionales. Actualmente
realiza investigacin sobre sntesis, caracterizacin,
propiedades y aplicabilidad de macrociclos
orgnicos, as como sobre su incorporacin en redes
inorgnicas por el mtodo sol gel. Ha presentado
ms de treinta trabajos de investigacin en
congresos nacionales e internacionales. Es profesor
de tiempo completo en el rea de Qumica
Inorgnica del Departamento de Qumica de la
UAM-Iztapalapa. Durante toda su formacin ha
sido alumno del Profesor Distinguido Dr. Antonio
Campero Celis.
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de
qumica orgnica I
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
^ UNIVERSIDAD AUTNOMA METROPOLITANA
Casa abierta al tiempo
Dr. Luis Mier y Tern Casanueva
Rector General
Dr. Ricardo Sols Rosales
Secretario General
UNIDAD IZTAPALAPA
Dr. Jos Lema Labadie
Rector
Mtro. Javier Rodrguez Lagunas
Secretario
Dr. Gerardo Saucedo Castaeda
Director de la Divisin de Ciencias Biolgicas y de la Salud
Dr. Alberto Rojas Hernndez
Jefe del Departamento de Qumica
Mtro. Daniel Toledo Beltrn
Coordinador de Extensin Universitaria
Ma. del Rosario Hoyos Alea
Jefa de la Seccin de Produccin Editorial
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de
qumica orgnica I
M. Q. Miguel ngel Garca Snchez
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Primera impresin: 2002
UNIVERSIDAD AUTNOMA METROPOLITANA
UNIDAD ETAPALAPA
Av. San Rafael Atlixco No. 186 Col. Vicentina
Iztapalapa, 09340, Mxico, D.F.
ISBN: 970-31-0052-X
Impreso y hecho en Mxico / Printed in Mxico
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
ndice
Prlogo 9
Dedicatoria 11
Prctica 1: Normas de seguridad 13
Prctica 2: Identificacin de grupos funcionales orgnicos 21
Prctica 3: Aislamiento de limoneno de naranjas 35
Prctica 4: Aislamiento de la cafena a partir del T o el caf 41
Prctica 5: Extraccin y recristalizacin de un frmaco 45
Prctica 6: Cromatografa I: en capa fina 53
Prctica 7: Cromatografa II: en columna 59
Prctica 8: Isomera cis-trans: isomerizacin del cido
maleico a fumrico 67
Prctica 9: Reacciones de sustitucin nucleoflica (S
N
):
sntesis de los cloruros de -butilo y tert-butilo 71
Prctica 10: Espectroscopia en la regin del infrarrojo 77
Anexo A: Espectros infrarrojos 91
Anexo B: Material de vidrio y equipo de laboratorio 99
Anexo C: Montaje de dispositivos experimentales 109
Anexo D: Sustancias peligrosas 115
Formato de reporte 118
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Prlogo
El siguiente conjunto de experiencias de laboratorio constituye el resultado de una
cuidadosa eleccin entre muchas posibles. Cada prctica fue primero probada por
el autor y posteriormente con los alumnos en varios trimestres. El orden presentado
es muy cercano al programa de la materia Qumica Orgnica I de la Divisin de
Ciencias Bsicas e Ingeniera de laUAM-Iztapalapa, pero puede muy bien adaptarse
a otros programas, incluso de otras instituciones. Aunque la observacin podra
resultar excesiva de acuerdo con el criterio de algunos colegas, nos hemos dado
cuenta de que las carencias formativas de los alumnos que por primera vez asisten
a un laboratorio de este tipo son muchas y van en aumento. Es por ello que hemos
incluido el mayor nmero posible de herramientas que guen a nuestros estudiantes
de una manera slida, segura y amena en su formacin como qumicos.
Debemos mencionar que las experiencias aqu vertidas se han adaptado de
diversas fuentes. Aproximadamente la mitad de las mismas pueden muy bien
realizarse en el mbito de lo que se ha dado en llamar micromtodos. Por otra
parte, en el presente manual queremos mostrar que la qumica tiene una presencia
muchas veces inadvertida en mltiples mbitos de la vida diaria. Nuestra intencin
es que en este primer encuentro de nuestros alumnos con un laboratorio de Qumica
Orgnica sea motivador, formativo y en lo posible correctivo pues, al parecer, en
el nivel de bachillerato se le ha relegado.
Se ha procurado presentar cada prctica con una introduccin suficiente como
para evitar al alumno una intil prdida de tiempo; consideramos que por la
naturaleza del curso es mejor invertir ese tiempo en el entrenamiento y en el
despertar de la intuicin de qumico. Al final del conjunto de prcticas presentamos
una serie de anexos que pueden utilizarse para conocer el material empleado, el
montaje de los sistemas de operaciones ms comunes y un anexo de espectros en
la regin del infrarrojo. Estos anexos pueden o no utilizarse, pero, segn nuestra
experiencia, el usuario puede adaptarlos a sus necesidades. As mismo, al final
presentamos un formato que los alumnos pueden aprovechar para presentar sus
reportes de las prcticas de manera ms completa y concreta.
Si este manual presenta errores y defectos, estoy en la mejor disposicin de
realizar las correcciones pertinentes y aceptar todos los comentarios tendientes a
su enriquecimiento.
Por ltimo, deseo a los futuros usuarios del presente manual un
"Feliz encuentro con la qumica".
Miguel A. Garca Snchez
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Dedicatoria
El presente trabajo esta dedicado a mis maestros y compaeros del Departamento
de Qumica de la UAM-Iztapalapa, entre los cuales, con mucho orgullo, cuento a
mis mejores amigos. Les doy las gracias por mostrar con su ejemplo la belleza de
nuestra profesin y por no permitir que termine el sueo de nuestra nacin, pues
Yo aseguro
que el sembrador de sueos
cosechar algn da
frutos que huelen a horizonte
y que saben a infinito.
Miguel ngel Garca Snchez
Mayo de 2002
11
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Prctica 1
NORMAS DE SEGURIDAD
OBJETIVO
a) El alumno conocer y aprender el reglamento interno, y reconocer que su
acatamiento har ms seguro su trabajo en todo laboratorio de qumica.
b) El alumno conocer las principales causas de incendios y explosiones.
c) El alumno estudiar el pequeo anexo de primeros auxilios.
INTRODUCCIN
Debido a los riesgos que implica la manipulacin cotidiana de sustancias perju-
diciales al organismo humano, el qumico debe siempre comportarse respetuoso
de los peligros inherentes a su actividad, y ejercer las mayores precauciones. Es
igualmente importante que conozca el dao que estas sustancias, mal tratadas o
mal desechadas, pueden ocasionar a sus semejantes y al ecosistema.
Por lo anterior, consideramos que es indispensable que todo profesional de la
qumica y de carreras afines conozca e interprete adecuadamente el reglamento
bsico al que debe ajustarse su comportamiento. El respeto de dicho reglamen-
to lo ayudar a preservar su salud e integridad fsica, lo sensibilizar sobre el
hecho de que su labor conlleva un riesgo para sus semejantes y su medio ambiente,
y le permitir desarrollar el sentido crtico necesario para enfrentar aquellas
situaciones imprevistas para las que este reglamento no es suficiente.
Sugerimos que este reglamento se lea y analice cuidadosamente antes de iniciar
cualquier actividad en el laboratorio de Qumica Orgnica.
1. Reglamento bsico
A continuacin se presenta una serie de reglas bsicas que deben seguirse en el
laboratorio de Qumica Orgnica.
13
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
Conocer bien las propiedades fsicas, qumicas y toxicolgicas de las
sustancias que se van a utilizar.
Nunca trabajar solo en el laboratorio.
Usar siempre bata.
Usar lentes protectores y guantes cuando sea necesario.
Manipular el equipo caliente con guantes de asbesto o pinzas, para evitar
quemaduras.
Mantener libre de objetos innecesarios la zona de trabajo.
Nunca perder de vista los reactivos y el sistema con que se est trabajando.
No comer, fumar o jugar dentro del laboratorio.
Utilizar todo el material de laboratorio limpio y seco.
Nunca pipetear los reactivos lquidos con la boca.
Nunca devolver al envase original los remanentes de reactivos no utilizados.
Lavarse bien las manos al final de cada sesin de laboratorio.
Antes de usar un reactivo, verificar los datos anotados en la etiqueta y
consultar sus propiedades fsicas, qumicas y toxicolgicas para manejarlo
adecuadamente.
Nunca probar el sabor u olor de ningn producto, a menos que sea estric-
tamente necesario y seguro.
Para oler una sustancia, sta no debe ponerse directamente debajo de la
nariz; por el contrario, se mueve la mano sobre ella para percibir su aroma
sin peligro.
Los productos qumicos nunca se tocan directamente con las manos,
especialmente aquellos que, adems de su toxicidad, pueden producir
quemaduras graves. Todo manejo se har mediante esptulas.
Todo compuesto voltil o que desprenda humos o vapores txicos deber
manejarse en las campanas o permanecer en un lugar ventilado.
Si se derrama cido sobre la mesa, se debe recoger inmediatamente y lavar
la superficie con agua varias veces.
No debe mirarse dentro de un tubo o matraz que contenga una reaccin o
sustancia que se est calentando.
Las soluciones concentradas de lcalis o cidos deben neutralizarse antes
de ser desechadas por el desage.
No se deben tirar por la tarja lquidos inflamables, irritables o lacrimgenos.
Cuando utilice cidos, hgalo en la campana de extraccin y siempre pro-
tegido con guantes y lentes de seguridad.
Para preparar una solucin diluida de cido se debe aadir, lentamente, con
agitacin y con enfriamiento externo, el cido al agua, nunca el agua sobre
el cido ya que la reaccin es muy exotrmica y puede proyectarse
violentamente.
14
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Normas de seguridad
Antes de poner a calentar lquidos, stos deben estar bien mezclados (si son
miscibles; en caso contrario, al hervir el de menor punto de ebullicin puede
proyectarse o explotar. Los de bajo punto de ebullicin no se deben calentar
nunca en recipientes de cuello corto).
En una destilacin no se deben obstruir los condensadores ni los tubos de
evacuacin.
2. Incendios
Las razones ms comunes de incendio son:
Hacer hervir un disolvente voltil o inflamable con un mechero y sin un
condensador.
Mantenerlo cerca de alguna fuente de calor o chispa.
Arrojar reactivos y los desechos de reacciones exotrmicas u organome-
tlicas en la tarja.
Mezclar sustancias que al reaccionar generan vapores o gases inflamables.
No respetar las condiciones de almacenamiento de reactivos inestables,
voltiles o que pueden reaccionar violentamente con: temperatura, agua,
cidos, bases, agentes oxidantes, reductores o compuestos de elementos
pesados.
Las precauciones que se deben de tomar son las siguientes:
Conocer bien la toxicidad de cada reactivo y las precauciones de necesarias
al usarlo.
Evitar el uso de mecheros; en su lugar se usarn baos de agua, parrillas de
calentamiento o canastillas.
Ser muy cuidadoso al utilizar disolventes inflamables y voltiles
Conocer la temperatura de ignicin espontnea de las sustancias.
3. Explosiones
Las explosiones pueden ocurrir en las siguientes situaciones:
Una reaccin exotrmica no controlable (que provoca explosin y fuego).
Una explosin de residuos de perxidos al concentrar soluciones etreas a
sequedad.
15
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
Una explosin por calentamiento, secado, destilacin o golpe de compuestos
inestables.
Mezclar sustancias incompatibles que generan vapores o gases inflamables
o explosivos.
Para evitar explosiones, una regla esencial es conocer las condiciones de
almacenamiento y uso de cada sustancia.
4. Primeros auxilios
En caso de incendio, aljese rpidamente y permita que su asesor lo apague
con el extinguidor que debe haber en el laboratorio. Si esto ya no es posible,
salga rpidamente del laboratorio. Si el fuego afecta ya a algn compaero,
trate de quitarle las prendas que se estn consumiendo y retrelo de la zona
del siniestro.
En caso de explosin, salga inmediatamente del laboratorio y, si le es po-
sible, ayude a sus compaeros afectados. Avise al resto del personal de
laboratorio para que presten auxilio.
Si se salpica la piel con cidos, lvese inmediatamente con agua abundante
y apliqese una disolucin de bicarbonato sdico.
Si una sustancia lo salpica sobre los ojos, enjuagese inmediatamente con
el lavaojos o bien con agua abundante y despus con una solucin de brax
(que debe existir en el botiqun del laboratorio). Si persisten las molestias,
consulte al mdico.
Cuando se ingiere un cido fuerte, se puede neutralizar con melox o su
equivalente.
Cuando se ingiere una base se neutraliza con jugo de naranja o de uva, o
con vinagre.
Cuando se haya ingerido una sustancia venenosa o txica y sea necesario
provocar vmito, utilice un esmtico.
Emtico: es una mezcla de sustancias que sirven para producir el vmito y
liberar al estmago del veneno. Algunos emticos son:
Agua con mostaza: se agrega una cucharadita de t de mostaza a un vaso de
agua caliente. Se administra una cuarta parte del contenido.
Agua salada: se disuelven dos cucharaditas de sal en agua caliente y se
toma la dilucin a intervalos de un minuto hasta suministrar ms o menos
cuatro vasos.
Agua con jabn: se agita un pedazo de jabn en agua caliente.
16
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Normas de seguridad
Nota: Los emticos no deben administrarse nunca cuando el paciente est:
a) Inconsciente o con convulsiones
b) Incapacitado para deglutir
c) Lastimado por haber tragado un veneno corrosivo
Para neutralizar el efecto de una sustancia venenosa o txica, debe adminis-
trarse un antdoto.
Antdoto: es una sustancia que se suministra para hacer inofensivo un veneno o
para retardar su accin.
Antdoto universal: esta mezcla se prepara con dos partes de carbn activado,
una de xido de magnesio y una de cido tnico. Se homogeniza totalmente y se
guarda en seco. Para administrar se disuelven 15 g en medio vaso de agua caliente.
Si es necesario, se practica un lavado estomacal.
Cuando la piel haya estado en contacto con una sustancia venenosa o haya
sufrido alguna quemadura, despus de lavar la zona afectada aplique un
emoliente.
Emoliente; sirve para quitar el dolor de los tejidos y membranas inflamadas, por
ejemplo la clara de huevo, la leche y el agua de cebada. Se administra despus
de eliminar el veneno.
5. Botiqun de primeros auxilios
El botiqun de primeros auxilios debe existir en todo laboratorio de qumica y
debe contener:
Material de curacin
gasas
apositos
torundas
hisopos
tela adhesiva
Instrumental
tijeras de punta
pinza de diseccin sin dientes
jeringas de varios tamaos
17
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
un torniquete
vendas
Antispticos
alcohol
agua oxigenada
merthiolate
benzal
violeta de genciana
vinagre
bicarbonato de sodio
cido brico (brax)
melox
CUESTIONARIO
1. Describa brevemente las normas bsicas de conducta que se deben observar
en todo laboratorio.
2. Antes de manipular una sustancia, qu es lo que debe conocer de ella?
3. Cules son las causas ms frecuentes de incendio en un laboratorio de
qumica?
4. Qu son un antdoto y un emtico?
5. Si un compaero ha ingerido una sustancia corrosiva y sta le ha afectado la
garganta, la trquea, etc., por qu no debe provocarle el vmito?
6. Cmo se prepara el antdoto universal?
BIBLIOGRAFA
1. E. R. Plunkett. 1978. Manual de toxicologa industrial. Enciclopedia de la
Qumica Industrial. Espaa, Urmo.
2. R C. Lu. 1991. Basic Toxicology. 2
a
ed. USA, Taylor and Francis.
3. Instructivo sobre el funcionamiento interno y operativo para regular el
uso de los servicios e instalaciones de los laboratorios de docencia. UAM-
Iztapalapa, Aprobado por el Consejo Acadmico en su sesin 133. Mxico,
UAM-Iztapalapa.
18
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Normas de seguridad
4. R. S. Stricoff y D. B. Walters. 1995. Handbook ofLaboratory Health and
Safety. New York, John Wiley & Sons.
5. R. J. Lewis. 1996. Hazardous Chemicals Desk Reference, New York, Van
Nostrand Reinhold.
6. R. E. Lenga (ed.). 1998. The Sigma-Aldrich Library of Chemical Safety
Data. Milwaukee, WI, Sigma-Aldrich.
7. Merck. 1996. The Merkndex, 12
a
ed. Rahway, NJ, S. Budavari.
19
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Prctica 2
IDENTIFICACIN DE GRUPOS
FUNCIONALES ORGNICOS
OBJETIVO
El alumno aprender a identificar los grupos funcionales que se encuentran en
compuestos orgnicos de origen natural o sinttico mediante pruebas a la gota.
INTRODUCCIN
El comportamiento qumico y fsico de una molcula orgnica se debe principal-
mente a la presencia en su estructura de uno o varios grupos, funciones o familias
qumicas. Los grupos funcionales son agrupaciones constantes de tomos, en dis-
posicin espacial y conectividad, que por tal regularidad confieren propiedades
fsicas y qumicas muy similares a la estructura que las posee. En qumica orgnica
los grupos funcionales ms importantes son los que se muestran en la tabla 2.1.
21
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
TABLA2.1 PRINCIPALES FUNCIONES ORGNICAS DE ACUERDO
CON SU PRIORIDAD Y SU REACTIVIDAD
Grupo funcional
Sales de amonio,
fosfonio
sulfonio
Acido carboxlico
Anhdrido
Esteres
Halogenuro de acilo
Amida
Nitrito
Aldehido
Cetona
Alcohol
Mercaptano
Amina
ter
Sulfuro
Alqueno
Alquino
Halogenuro de alquilo
Nitro
Alcano
Agrupamiento
caracterstico
R
4
N
+
R
4
P
+
R
3
s
+
R-COOH
R-CO-O-CO-R'
R-CO-O-R
1
R-CO-X
R-CO-NR
1
V
R-CN
R-CHO
R-CO-R'
R"
R-C-OH
k
R
1
R-C-SH
R"
R-N-R
1
R"
R-O-R
1
R-S-R
1
C=C
O=C
R-X
R-NO
2
C-C
Ejemplo
(CH
3
)
3
NH*: trimetilamonio
(C
6
H
5
)
4
PH*: trifenilfosfonio
(CH
3
CH
2
)
3
S
+
: trietilsulfonio
CH
3
COOH: cido actico
CH
3
CO-O-COCH
3
: anhdrido actico
CH
3
CO-O-C
2
H
5
: acetato de etilo
CH
3
CH
2
COCI: cloruro de propanolo
HCO-NH
2
: formamida
CH
3
(CH
2
)
2
. CN: butanonitrilo
CH
3
CH
2
-CHO: propanal
CH
3
-CO-CH
3
: acetona
CH
3
CH
2
.OH:etanol
CH
3
CH
2
.SH: etanotiol
CH
3
(CH
2
)
6
.NH
2
: hexanamina
(CH
3
CH
2
)
2
O: ter etlico
(CH
3
CH
2
)
2
S: sulfuro de dietilo
CH
3
.CH=CH
2
:1-propeno
CH
3
.CsCH:1-propino
CH
3
.CH
2
.Br: bromuro de etilo
C
6
H
5
.NO
2
: nitrobenceno
CH
3
(CH
2
)
6
.CH
3
: n-octano
Nota: Los grupos R, R
1
y R" representan cualquier grupo alquilo o arilo, y X representa un ha-
lgeno (F, Cl, Br o I).
22
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Identificacin de grupos funcionales orgnicos
La mayora de estos grupos funcionales se presentan en las molculas de origen
natural. Algunas de stas, por ejemplo los halogenuros de acilo, por su reactividad
son poco frecuentes en la naturaleza y se utilizan ms como intermediarios en
sntesis orgnica.
Las propiedades fsicas y qumicas de una molcula sencilla estn determinadas
por la presencia de alguno de estos agrupamientos, pero en la mayora de las
molculas ms tiles, naturales o sintticas existen varios de estos agrupamientos.
En tal caso las propiedades fsicas y qumicas de la molcula son el resultado del
comportamiento combinado y de la distribucin espacial de las funciones qumicas
presentes en ella.
Para un profesional de la qumica es muy importante averiguar qu grupos
funcionales posee una molcula, ya que de ello depender en ocasiones el poder
predecir sus propiedades o explicar su comportamiento en un proceso qumico o
fsico.
CLASIFICACIN DE UNA MOLCULA EN
UN GRUPO FUNCIONAL
La tcnica descrita ms adelante permitir al alumno clasificar una molcula
desconocida dentro de una familia orgnica mediante pruebas a la gota con diversos
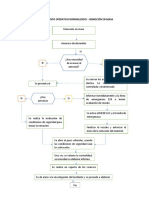
reactivos colorimtricos (Fig. 2.1) Tales pruebas aprovechan las propiedades
qumicas ms notorias; por ejemplo los cidos carboxlicos, disueltos en agua,
generan un exceso de iones H
3
O
+
y las aminas un exceso de iones OH~. Estos iones
pueden detectarse midiendo el pH, mediante papel indicador o utilizando una
disolucin indicadora sencilla o medianamente elaborada como el llamado
indicador universal, el cual manifiesta un color que depende del pH de la disolucin
analizada.
Con un cido, el indicador universal vira a color rojo y con una base, a color
verde azulado. Si al agregar unas gotas del indicador la mezcla no cambia su color
amarillo, la molcula analizada no es ni cido ni base. Para clasificar una molcula
con tales caractersticas se utiliza KMnO
4
, un agente oxidante neutro. Con este
reactivo se detectan los grupos fcilmente oxidables de la molcula. Cuando tal
oxidacin ocurre, la disolucin de KMnO
4
, inicialmente de color violeta oscuro,
se torna de color amarillo claro o incolora y se observa la precipitacin de dixido
de manganeso, MnO
2
. Algunos de los grupos oxidables son a) los aldehidos, que
al reaccionar producen cidos carboxlicos, y b) los alquenos, que inicialmente
se transforman en dioles que por oxidaciones posteriores producen dos molculas
carboxlicas, RCOR" y RCOR".
23
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
Molcula problema
i
Adicionar el indicador universal
i
Color rojo Color amarillo Verde o azul
oscuro
cido carboxlico alcano, alqueno, alcohol amina
aldehido o cetona
Adicionar KMnO
4
neutro
Caf oscuro
alqueno o aldehido
i
Adicionar reactivo de Tollens
i
Espejo plateado
aldehido
No reacciona
alcano, alcohol o cetona
i
Adicionar dinitrofenilhidrazina
I i
No reacciona No reacciona Amarillo-anaranjado
alcano alcano o alcohol cetona
i
Adicionar sodio metlico
i i
Burbujeo
alcohol
No reacciona
alcano
Figura 2.1 Ruta recomendada para la clasificacin de una molcula desconocida en
un grupo funcional orgnico.
a) Con un aldehido
R-CHO + KMnO
4
(ac)
violeta oscuro
->R-co-cr
incoloro
MnO
2
+
caf oscuro
KOH
24
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Identificacin de grupos funcionales orgnicos
b) Con un alqueno
R
f
R" R
f
R"
II II [O]
R-C=C-R
llf
+ KMnO
4(ac)
-> R-CC-R"
f
+ MnO
2
+ KOH -> RCOR" + R'COR
1
"
OH OH
violeta oscuro incoloro caf oscuro
Los alcanos, alcoholes y cetonas no se oxidan con la disolucin neutra de
permanganato de potasio y deben identificarse de otra forma.
c) Con un reactivo de Tollens
Para distinguir entre un alqueno y un aldehido se utiliza el reactivo de Tollens,
que al reaccionar con un aldehido provoca la reduccin de la plata, lo cual
se detecta por la formacin de una pelcula plateada o espejo de plata en el
recipiente de prueba.
R-CHO + Ag(NH
3
)
2
+
R-CO-O- + Ag + 2NH
3
espejo de plata
d) Cetonas e hidrazinas
Las cetonas reaccionan con las hirazinas, por ejemplo con la 2, 4- dini-
tro fenilhidrazina, (NO
2
)
2
C
6
H
3
-NH-NH
2
, para formar hidrazonas que suelen
ser compuestos muy coloridos por la presencia del grupo C=N- en su
estructura.
R-CO-R
1
+ (NO
2
)
2
C
6
H
3
_NH-NH
2
> (NO
2
)
2
C
6
H
3
_N-N=C-R
I I
H R
f
e) Reaccin de alcoholes con sodio metlico
Para distinguir los alquenos de los alcoholes puede recurrirse a una pequea
propiedad de las molculas que poseen grupos OH. Los alcoholes, al igual
que el agua, reaccionan con el sodio metlico (y con el litio) para dar un
25
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
alcxido de sodio (o de litio) e hidrgeno gaseoso. En consecuencia, los
alcoholes se detectan por el burbujeo del hidrgeno generado al reaccionar
con el sodio metlico.
2R0H + 2Na(s) >2R-0Na
+
+ H
2
(g)
Finalmente, debemos decir que como los alcanos no reaccionan tampoco con
el sodio metlico, puede utilizarse esta ltima reaccin para distinguir entre un
alcano y un alcohol.
MATERIAL DE VIDRIO
12 tubos de ensaye pequeos c/ tapn
2 vasos de precipitado de 50 mi
2 pipetas Pasteur
1 pipeta graduada de 5 mi
1 propipeta
2 matraces aforados de 100 mi
2 matraces aforados de 50 mi
1 matraz Erlenmeyer de 50 mi
1 varilla de vidrio
Nota: Si desconoce alguna pieza de vidrio o equipo de laboratorio, puede revisar
el anexo B de material de vidrio y equipo de laboratorio.
EQUIPO DE LABORATORIO
1 esptula
1 gradilla para tubos de ensaye
SUSTANCIAS
n-heptano (un alcano)
ciclohexeno (un alqueno)
etanol o n-butanol (alcoholes)
26
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Identificacin de grupos funcionales orgnicos
propionaldehdo o butiraldehdo (aldehidos)
acetona o 2-butanona (cetonas)
cido actico o cido propinico (cidos qarboxlicos)
dietilamina (aminas)
permanganato de potasio, KMnO
4
nitrato de plata, AgNO
3
hidrxido de sodio, NaOH
hidrxido de amonio, NH
4
OH
etanol,C
2
H
5
OH
cido sulfrico, H
2
SO
4
cido ntrico, HNO
3
2,4-dinitrofenilhidrazina
sodio metlico, Na
fenolftalena
rojo de metilo
azul de bromotimol
amarillo de metilo
azul de timol
EXPERIMENTACIN
Se numeran 10 tubos de ensaye pequeos y se colocan en ellos las sustancias en la
cantidad indicada en la tabla 2.2.
Adems de la siguiente lista de sustancias pueden analizarse dos sustancias
problema, que bien pueden ser muestras de las anteriores prcticas o muestras
proporcionadas por el asesor del alumno. Las llamaremos molcula problema 1
(MP1) y molcula problema 2 (MP2).
27
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
TABLA 2.2 SUSTANCIAS RECOMENDADAS PARA ANALIZARSE Y
CANTIDADES SUGERIDAS
Tubo No.
1
2
3
4
5
6
7
8
9
10
Sustancia
cido actico o propinico
Agua destilada
Dietilamina
Propionaldehdo o butiraldehdo
Ciclohexeno
Propionaldehdo o butiraldehdo
Ciclohexeno
Acetona
Etanol
n-heptano
Volumen/gotas I
10
10
10
10
10
2
2
10
20
20
Una vez hecho esto, proceda a realizar las pruebas que a continuacin se indican.
A) Se adicionan 10 gotas de agua destilada a los tubos 1-3, se mezcla per-
fectamente y se agrega una gota del indicador universal.
Recurdese que:
Si la disolucin se torna roja, hay un cido carboxlico presente.
Si la disolucin se torna azul-verdosa, hay una sustancia bsica presente,
muy probablemente una amina.
Si la disolucin se torna amarillo-verdosa o amarillo-anaranjada, la di-
solucin es neutra y puede tratarse de un alcano, un alqueno, un aldehido,
una cetona o un alcohol. Si ste es el caso, proceda a la siguiente etapa.
B) Se agregan 10 gotas de agua destilada y 5 gotas de disolucin 0.02M de
KMnO
4
a los tubos 4 y 5. Se agita suavemente cada tubo por aproximadamente
un minuto.
Si despus de este tiempo se observa la formacin de un precipitado
color caf (MnO
2
), se trata de un aldehido o de un alqueno.
Si no ocurre cambio de color y la mezcla permanece de color violeta
oscuro, ello indica que no ocurri reaccin y que se trata de un alcano,
un alcohol o una cetona.
28
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Identificacin de grupos funcionales orgnicos
C) Se agregan 2.0 mi de reactivo de Tollens a los tubos 6 y 7, se agita suavemente
por dos minutos y se deja reposar por otros 5 minutos.
Si se observa la formacin de una capa de precipitado, el espejo de
plata, se trata de un aldehido.
Si no se observa precipitado alguno, se trata de un alqueno.
D) Se agregan 2.0 mi de disolucin de 2,4-dinitrofenilhidrazina (precaucin:
es txica) al tubo 8, se agita vigorosamente y se deja reposar por dos minutos.
Si no se forma de inmediato un precipitado, deber dejarse reposar hasta 15
minutos.
Si se observa la formacin de un slido amarillo-anaranjado, la reaccin
ha ocurrido y se trata de una cetona.
Si no se observa precipitado alguno (ignore la turbidez), la reaccin no
ha ocurrido y se trata de un alcano o de un alcohol.
Nota: a) Lo recomendable es agregar una o dos gotas del aldehido o la cetona que
se va a estudiar a 2 mi de etanol al 95% y agregar esta mezcla a 3 mi de la di-
solucin de 2,4-dinitrofenilhidrazina. b) Si se hace reaccionar un aldehido con la
2,4-dinitrofenilhidrazina, puede producir una coloracin amarillo anaranjada y
confundirse con una cetona; sin embargo, puede distinguirse entre ambos mediante
la reaccin del permanganato de potasio.
E) Se agrega a los tubos 9 y 10 una pequea pieza de sodio metlico (precaucin;
el sodio metlico debe manejarse con cuidado y alejarse del agua). Agtese
suavemente por unos 15 segundos y obsrvese si ocurre alguna reaccin.
Si el sodio metlico se disuelve y hay burbujeo, se trata de un alcohol.
Si no se observa reaccin alguna, se trata de un alcano.
F) Se determina qu grupo funcional hay en las muestras MP1 y MP2 siguiendo
el esquema mostrado antes. Para ello, se puede repetir lo hecho en las etapas
A a E, teniendo cuidado de que en esta ltima etapa, al trabajar con so-
dio metlico, no disuelva las sustancias en agua o disolventes prticos
(con hidrgenos liberables), ya que reaccionar vigorosamente y podra
incendiarse.
Para concluir sobre el grupo funcional de estas dos especies se pueden realizar
otras pruebas, como la determinacin del punto de fusin, la medicin del ndice
de refraccin, el olor, el color, la espectroscopia IR, UV-Visible, etctera.
29
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
PREPARACIONES
Indicador universal
Para preparar el indicador universal se disuelven en 200 mi de etanol 50 mg de
fenolftalena, 100 mg de rojo de metilo, 150 mg de amarillo de metilo, 200 mg de
azul de bromotimol y 250 mg de azul de timol. Una vez que se obtiene una disolucin
de color rojo oscuro, se adiciona gota a gota (aproximadamente entre 20 y 25
gotas) una disolucin 1M de NaOH hasta que la disolucin sea de un color amarillo
oscuro. Cuando esto haya ocurrido, se afora a 250 mi con alcohol etlico y se agita
con fuerza para mezclar perfectamente. La disolucin se cubre y se guarda en un
lugar fresco. Este indicador universal manifiesta un color que depende fuertemente
del pH de la disolucin en que se adicione (Tabla 2.3).
TABLA 2.3 COLOR DE LA DISOLUCIN EN QUE SE ADICIONA EL
INDICADOR UNIVERSAL, DEPENDIENDO DEL PH DE LA
DISOLUCIN
pH
2
4
6
8
10
12
Color
Rojo
Anaranjado
Amarillo
Verde
Azul
Violeta
Preparacin del reactivo de Tollens
El reactivo de Tollens debe prepararse antes de usarse, y no debe almacenarse ya
que se descompone con rapidez, formndose un precipitado que es un poderoso
explosivo. Si no ocurre ninguna reaccin en fro, la disolucin deber calentarse
suavemente. Para preparar el reactivo de Tollens puede procederse de dos maneras:
30
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Identificacin de grupos funcionales orgnicos
Procedimiento por gotas
Se vierten 30 gotas de AgNO
3
al 5% en un tubo de ensaye limpio y se agregan 2
gotas de disolucin al 5% de NaOH. Se observar la formacin de un precipitado
de color caf oscuro (Ag^). A continuacin se agregan, agitando siempre, las
gotas suficientes de NH
3
al 5% para disolver el precipitado de Ag ^ y para que la
disolucin se vuelva transparente (se requieren aproximadamente 20 gotas). La di-
solucin incolora obtenida contiene el ion Ag(NH
3
)
2
+
.
Procedimiento en mililitros
En un matraz de 50 mi se vierten 25 mi de una disolucin al 5% de AgNO
3
y se
aaden gota a gota 0.5 mi de una disolucin al 10% de NaOH. Se observar la for-
macin de un precipitado color caf oscuro. A continuacin se agrega gota a gota
una disolucin de NH
3
al 5%, agitando constantemente y hasta que se disuelva el
xido de plata formado (de 15 a 20 mi). Para obtener un reactivo sensible es
necesario evitar un exceso de hidrxido de amonio.
Nota: a) El reactivo de Tollens se desecha neutralizndolo en HNO
3
diluido,
b) La difenilamina, las acilonas, las aminas aromticas, el p-nftol y
algunos fenoles dan positiva la prueba de Tollens. Tambin se ha
encontrado que las p-alcxi y p-dialquilaminocetonas reducen la
plata del ion Ag(NH
3
)
2
+
.
Preparacin de la disolucin de hidrazina
Con fenilhidrazina o p-nitrofenilhidrazina: a 5 mi de agua se adicionan 0.5 mi de
fenilhidrazina y se agrega gota a gota cido actico para disolver la hidrazina.
Con 2,4-dinitrofenilhidrazina: se disuelven 1.5 g de 2,4-dinitrofenilhidrazina
en 7.5 mi de cido sulfrico concentrado y se aaden, agitando, a 10 mi de agua y
35 mi de etanol al 95%. Se mezcla perfectamente y se filtra para eliminar los
slidos no disueltos.
Nota: La mayora de los aldehidos y las cetonas producen dinitrofenilhidrazonas,
que son slidos insolubles. Al principio el slido puede ser aceitoso y, al reposar,
volverse cristalino. Sin embargo, algunas cetonas producen hidrazonas que son
31
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
aceites; por ejemplo, la metil-n-octilcetona, la di-n-amilcetona y sustancias
similares no producen dinitrofenilhidrazonas slidas.
Algunos derivados del alcohol allico pueden ser oxidados por la disolucin
de 2,4-dinitrofenilhidrazina y producir aldehidos o cetonas que darn positiva
esta prueba. Por ejemplo, se han obtenido las 2,4-dinitrofenilhidrazonas de los
derivados carbonlicos del alcohol cinamlico, del 4-fenil-3-buten-2-ol y de la
vitamina A en rendimientos que van del 10 al 25%. Lo mismo ocurre con el
benzidrol, que al transformarse en benzofenona da positiva la prueba. Tambin
puede ocurrir que un alcohol se encuentre contaminado con el aldehido o la cetona
que se genera por oxidacin con el aire, dando positiva la prueba.
Las dinitrofenilhidrazonas de aldehidos o cetonas en las que el grupo carbonilo no
est conjugado con otro grupo funcional, son amarillas. Si el grupo carbonilo se
encuentra junto a un doble enlace carbono-carbono o junto a un anillo bencnico,
desplaza hacia el mximo de absorcin al visible (al anaranjado); esto se descu-
bre fcilmente realizando un anlisis por espectroscopia de UV-Visible. Entonces
puede decirse que una dinitrofenilhidrazona amarilla no est conjugada. Esto debe
tomarse con precaucin ya que, por ejemplo, la 2,4-dinitrofenilhidrazina no disuelta
es de color rojo-anaranjado.
CUESTIONARIO
1. Investigue la estructura de cada una de las sustancias de la tabla 2.2.
2. El indicador universal slo puede mostrar el carcter cido-base de una
sustancia; es posible utilizarlo para distinguir un derivado de un cido
carboxlico o de aminas secundarias y terciarias?
3. Un alquino se oxida con permanganato de potasio?
4. Si una molcula posee tanto grupos carbonlicos (aldehidos y cetonas) como
carboxlicos, puede utilizarse una fenilhidrazina para identificarlos?
5. Qu ventaja tendr utilizar 2,4-dinitrofenilhidrazina en lugar de fenil-
hidrazina?
6. Si una sustancia dio positiva la prueba de 2,4-dinitrofenilhidrazina, pero se
tiene duda de si se trata de un aldehido o de una cetona, de qu manera
resolvera usted la incgnita?
7. Qu se obtendra si en lugar de un aldehido o una cetona, se analiza un
cido carboxlico o un ster con 2,4-dinitrofenilhidrazina?Qu productos
se obtienen?
8. Por qu no debe utilizarse agua o disolventes prticos al trabaj ar con sodio
metlico?
32
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Identificacin de grupos funcionales orgnicos
BIBLIOGRAFA
1. E. Boschmann y N. Wells. 1990. Chemistry in Action. A Laboratory Manual
for General Organic and Biological Chemistry. New York, McGraw-HiU.
2. J. Chem. Educ. 25, 258 (1948).
3. L. R. Shriner, R. C. Fucson y D. Y. Curtin. 1991. Identificacin sistemtica
de compuestos orgnicos. Mxico, Limusa, pp. 142,164,192.
4. Leonard y Gelfand, J. Am. Chem. Soc, 77,3272 (1955).
33
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Prctica 3
AISLAMIENTO DE LIMONENO DE
NARANJAS
OBJETIVO
El alumno realizar la extraccin de limoneno a partir de cascaras de naranja
mediante un disolvente, lo purificar por destilacin y comprobar que en su
estructura existen dobles enlaces carbono-carbono.
INTRODUCCIN
El limoneno (Fig. 3.1a) pertenece a una clase de compuestos qumicos conocidos
como terpenos.
Los terpenos tienen como unidad bsica la del isopreno o 2-metil-l ,3-butadieno
(Fig. 3.1b). El limoneno se encuentra en muchos aceites esenciales, por ejemplo
en: limones, naranjas, limas, bergamota y alcaravea. Los terpenos son una familia
que se presenta en forma muy variada en muchas plantas. Por ej emplo el geraniol,
la mentona, el menteno, lpineno, etc., son aceites esenciales que se encuentran
en los geranios, la menta y el rbol de pino respectivamente. El limoneno posee un
carbono quiral, por lo que las formas (+) o (-) se presentan de manera natural. Sin
embargo, los rboles de naranja producen slo uno de dichos enantimeros. El
alcanfor es un terpeno que puede separarse de la esencia de manzanilla (Matricaria
camomilla), y puede reducirse para obtener el isoborneol y el borneol que se
utiliza en la esencia de lavanda. Por otro lado, el terpeno llamado canfeno puede
extraerse del romero y su forma levgira se presenta en el citronelal o en la
valeriana.
35
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
CH
2
= C- CH = CH
2
(a) (b)
Figura 3.1 a) Estructura del limoneno, b) estructura del isopreno.
MATERIAL DE VIDRIO
1 matraz redondo de tres bocas y de 500 mi
1 condensador
1 junta en Y para destilacin
1 tapn de vidrio
1 adaptador curvo para destilacin
1 matraz Erlermeyer de 50 mi
1 embudo de adicin
1 embudo de separacin
EQUIPO DE LABORATORIO
3 soportes universales
3 pinzas con nuez.
1 restato
1 manta de calentamiento
1 parrilla
1 cuchillo de cocina
1 refractmetro de Abbe (ver Figs. C 9 y C 10 del anexo C )
Nota: Si desconoce alguna pieza de vidrio o equipo de laboratorio, puede revisar
el anexo B de material de vidrio y equipo de laboratorio.
36
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Aislamiento de limoneno de naranjas
SUSTANCIAS Y REACTIVOS
La cascara de tres naranjas
Agua destilada
Pentano (o ter)
Sulfato de sodio anhidro, Na
2
SO
4
Permanganato de potasio, KMnO
4
PROCEDIMIENTO
Con un cuchillo de cocina se quita la cascara a tres naranjas, con todo y la pulpa
blanca que lleva adherida, cuidando de no presionar o tocar demasiado la cascara
para evitar la prdida del aceite esencial. Con ella se prepara un picadillo o, si se
puede, un pur en un matraz redondo de tres bocas y de 500 mi. En la boca central
se ensambla un aparato de destilacin (ver la Fig. C 3 del anexo C); en la boca
lateral se coloca un embudo para adicionar agua. Se utiliza un matraz Erlenmeyer
para colectar el destilado.
Se adiciona agua al pur y se calienta procurando que la ebullicin no sea muy
violenta y que el nivel de lquido en el interior del matraz se mantenga constante
durante el proceso de destilacin. Debe destilarse tan rpido como sea posible,
de manera que se colecten 150-200 mi de lquido turbio o aceitoso.
El pur del matraz se desecha y el destilado se enfra. El destilado se transfiere
a un embudo de separacin y se adicionan 5-10 mi de pentano (o bien ter), se
agita vigorosamente y se deja reposar para que las capas se separen. La disolucin
de pentano se coloca en un pequeo matraz Erlermeyer y se seca con sulfato de
sodio anhidro. La disolucin se filtra o decanta en un recipiente previamente pesado
y el pentano se evapora con un bao de vapor. Se pesa nuevamente el matraz con
el limoneno, se mide el volumen y se determina su ndice de refraccin.
ANLISIS
Para comprobar la presencia de los dobles enlaces del limoneno, puede realizarse
una pequea prueba con disolucin de bromo. Para ello se vierten 0,5 mi de
tetrahidrofixrano en un tubo de ensaye, se adicionan dos o tres gotas de la sustancia
por analizar y se mezcla hasta disolver. Se agrega gota a gota una solucin al 2%
de bromo lquido en tetracloruro de carbono. Una prueba de la existencia de dobles
o triples enlaces es positiva cuando la solucin se vuelve incolora. El color rojo-
caf del bromo desaparece cuando se adiciona a un compuesto con doble enlace
C=C, ya que se forma un compuesto hidrohalogenado que generalmente es
37
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
transparente. Aclaramos que tal procedimiento no se puede utilizar cuando existen
sistemas conjugados.
Otra alternativa es realizar una prueba con disolucin acuosa de KMnO
4
. La
disolucin violeta de permanganato de potasio se vuelve de color caf claro o
incolora debido a que se oxidan y rompen los dobles enlaces C=C.
Es posible obtener el espectro IR del limoneno y compararlo con el espectro
IR-18delanexoA.
CUESTIONARIO
1. Cuntas unidades de isopreno intervienen para formar el limoneno?
Identifquelas.
2. Existen 14 posibles ismeros para la misma frmula, C
10
H
16
, que difieren
en la posicin de los dobles enlaces; dibuje sus estructuras.
3. El limoneno es una molcula polar o no polar?
4. Identifique el centro quiral del limoneno.
5. Durante la separacin del limoneno a partir de su disolucin acuosa, qu
capa lo contiene, la superior o la inferior? Por qu?
6. El punto de ebullicin del limoneno es de 177C; entonces, por qu es
posible separarlo de las cascaras del ctrico por destilacin con agua?
7. Investigue la estructura del canfeno y sugiera un posible mtodo para extraer
el canfeno del romero.
8. La vitamina A es tambin un terpeno que puede separarse con hexano de las
zanahorias y de las espinacas. Cul es su estructura? Cuntas unidades de
isopreno la forman?
BIBLIOGRAFA
1. Clarke F. Most. Jr. 1988. Experimental Organic Chemistry. USA, John Wiley
& Sons.
2. D. L. Pavia, G. M. Lampman y G. S. Kriz, Jr. 1982. Organic Laboratory
Techniques. 2
a
ed. New York, Saunders, p. 163.
3. H. A. Strobel. 1982. Instrumentacin qumica. I
a
ed. Mxico, Limusa.
38
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Aislamiento de limoneno de naranjas
4. H. Murillo. 1970. Tratado elemental de qumica. Mxico, ECLALSA,
p. 280.
5. J. R. Dyer. 1965. Applications ofAbsortion Spectroscopy of Organic Com-
pounds. USA, Prentice Hall.
6. D. H. Williams y I. Fleming. 1986. Spectroscopic Methods in Organic Che-
mistry. 4
a
ed. UK, McGraw-Hill.
7. R. M. Silverstein y F. X. Webster. 1998. Spectrometric Identification of
Organic Compounds. 6
a
ed. New York, John Wiley & Sons.
8. Aldrich Chemical. 1997. The Aldrich Library ofFT-IR Spectra. 2
a
ed.
Milwaukee,WI,USA.
39
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Prctica 4
AISLAMIENTO DE CAFENA A PARTIR
DEL T O EL CAF
OBJETIVO
a) El alumno aislar la cafena a partir del t, usando disolucin de carbonato
de sodio, neutralizacin y extraccin con diclorometano.
b) El alumno identificar los grupos funcionales existentes en la estructura de
la cafena.
INTRODUCCIN
La cafena es uno de los derivados ms importantes de la xantina (un alcaloide).
Su concentracin en una variedad de t, incluyendo el t negro y el t verde, de-
pende de las condiciones climticas y topogrficas de su desarrollo y de los m-
todos de procesamiento.
Se ha encontrado que su concentracin vara de un 2.0 a un 4.0%; l t negro de
China contiene 2.6 a 3.6%, el de Brasil 2.2 a 2.9% y el turco 2.1 a 4.6%.
La cafena fue aislada por primera vez por Friese [1] de las semillas de Genipa
americana (2.25%) y por Sthenhouse [2] de los granos de caf. La cafena es un
estimulante del sistema nervioso central y produce efectos miocrdicos y diurticos,
as como el relajamiento del pequeo msculo de los bronquios; se trata de un
diurtico menos potente que la teobromina.
MATERIAL DE VIDRIO
1 dedo fro (Fig. B 5e del anexo B)
1 vaso de precipitado de 250 mi
1 probeta graduada de 100 mi
41
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
1 parrilla de calentamiento
1 matraz aforado de 250 mi
1 matraz Kitazato
1 embudo Buchner
1 embudo de separacin
1 varilla de vidrio
EQUIPO DE LABORATORIO
1 soporte universal con anillo
1 pinza de tres dedos con nuez
1 balanza
1 parrilla
1 manta de calentamiento
1 restato
1 esptula
SUSTANCIAS
cido sulfrico, H
2
SO
4
Diclorometano, CH
2
C1
2
Carbonato de sodio, Na
2
CO
3
Celita
T negro
PROCEDIMIENTO
En un vaso de precipitado de 250 mi, se colocan 10 g de hojas de t molidas en
2.5 g de carbonato de sodio y 50 mi de agua. La mezcla es calentada hasta ebullicin
por 20 minutos, agregando ocasionalmente ms agua para mantener constante el
volumen de la mezcla. La disolucin caliente se filtra y neutraliza mediante la
adicin de una disolucin de cido sulfrico al 10%.
La disolucin neutra es entonces filtrada en un tamiz de celita (la cual se coloca
en un embudo Buchner con papel filtro) y lavada con 10 mi de diclorometano. El
filtrado de dos fases se lleva a un embudo de separacin. La fase orgnica es
separada y la acuosa extrada dos veces con porciones de 20 mi de diclorometano
cada una. Las tres extracciones de diclorometano se combinan y el disolvente se
42
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Aislamiento de cafena a partir del t o el caf
evapora. La cafena cruda se puede recristalizar en la menor cantidad de acetona o
agua calientes.
Si se dispone de un dedo fro es posible obtener cristales muy puros de cafena
por sublimacin. Los cristales de la cafena tienen forma en agujas (de 0.25 g
aproximadamente) y tienen un punto de fusin de 235C.
Nota: Tenga la precaucin de realizar las extracciones con diclorometano en un
lugar perfectamente ventilado y lejos de cualquier flama o fuente de calentamiento
pues es muy voltil.
PRUEBAS
Se colocan unos cuantos cristales de cafena y 3 gotas de cido ntrico en un disco
pequeo de porcelana y se calienta para evaporar el liquido. Se agregan dos gotas
de hidrxido de amonio. Si la mezcla se torna violeta, se ha confirmado la presen-
cia de cafena.
De ser posible, obtngase el espectro infrarrojo de la cafena y comprese con
el espectro IR-9 del anexo A, buscando en especial las bandas sealadas en la ta-
bla 4.1.
Tambin puede obtenerse el espectro en la regin del ultravioleta visible, UV-
Vis. La cafena, disuelta en agua, presenta una seal de mxima absorbancia en
278 nm, caracterstica de las purinas y que se desplaza a mayores longitudes de
onda debido a los sustituyentes presentes.
TABLA 4.1 LAS PRINCIPALES SEALES DEL ESPECTRO IR DE LA
CAFENA (VER ESPECTRO IR-19 EN EL ANEXO A)
Seal/crrr
1
3134
2850
1705
1660
1604,1548,1440
1470,1358
1230,1197,1020
740
Grupo
C-H
N-CH
3
C=O
C=C
CH
3
C-N
C-H
Movimiento
alargamiento
alargamiento
alargamiento
alargamiento
sistema de pirimidina
flexin
alargamiento
deformacin
43
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
CUESTIONARIO
1. Investigue la estructura de la cafena e identifique en ella los grupos
funcionales que la forman.
2. Qu efecto del carbonato de sodio permite que la separacin de la cafena
sea eficiente?
3. Por qu se agrega la solucin de H
2
SO
4
a la mezcla de carbonato y t
caliente?
4. A qu atribuye usted el color violeta en la prueba de murexida con cafena?
BIBLIOGRAFA
1. F.W. Freise. Pharm. Zentr, 704, 76 (1935).
2. J. Stenhouse. Ann. 244,89 (1954).
3. Silverstein, R. M., Webster, F., Clayton, G., Bassler y T. C. Morrill. 1998.
Spectrometric Identification ofOrganic Compounds. 6
a
ed. John Wiley &
Sons, New York, 1998.
4. J. R. Dyer. 1995. Applications ofAbsortion Spectroscopy ofOrganic Com-
pounds. USA, Prentice Hall.
5. D. H. Williams e I. Fleming. 1986. Spectroscopic Methods in Organic Che-
mistry. 4
a
ed. UK, McGraw-Hill.
6. Aldrich Chemical. 1997. The Aldrich Library ofFT-IR Spectra. 2
a
ed.
Milwaukee,WI,USA.
44
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Prctica 5
EXTRACCIN Y RECRISTALIZACIN DE
UN FRMACO
OBJETIVOS
a) El alumno realizar la extraccin del cido acetilsaliclico (analgsico),
principio activo de varias preparaciones farmacolgicas.
b) El alumno realizar una purificacin del cido acetilsaliclico mediante
recristalizacin de dicho compuesto.
c) El alumno comprobar que en la estructura del compuesto existe el grupo
funcional cido carboxlico mediante pruebas a la gota o por espectrosco-
pia IR.
INTRODUCCIN
Las sustancias qumicas puras se caracterizan por ciertas constantes fsicas (punto
de fusin, punto de ebullicin, densidad, rotacin ptica, ndice de refraccin,
etc.) que nos permiten evaluar la pureza. La recristalizacin es uno de los mejores
mtodos fsicos para purificar compuestos slidos a temperatura ambiente.
Un compuesto slido puede recristalizarse a partir de su solucin saturada y
caliente, en un disolvente en el que a temperatura ambiente es poco o medianamente
soluble. La tcnica se basa en el hecho de que el exceso de soluto forma ncleos
cristalinos que crecen al enfriarse la disolucin, dejando la mayor parte de sus
impurezas en el disolvente. Como regla general, una sustancia es ms soluble en
aquellos disolventes cuya estructura se le parezca ms. Para que un disolvente se
considere adecuado para la recristalizacin, debe cumplir los siguientes requisitos:
a) Que el compuesto por cristalizar sea poco soluble en l a baj as temperaturas,
pero muy soluble a temperatura elevada.
b) Que no reaccione con el soluto.
45
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
c) Que sea lo suficientemente voltil para que resulte fcil eliminarlo de los
cristales filtrados.
d) Que las impurezas sean mucho ms solubles en fro que el soluto, para que
no lo recontaminen.
Para encontrar el disolvente adecuado para una recristalizacin, se recomienda
ensayarla con varios disolventes. Para ello es importante tener presentes algunas
de las propiedades de los ms utilizados, los cuales se muestran en la tabla 5.1.
TABLA 5.1 ALGUNOS DE LOS DISOLVENTES MS UTILIZADOS
PARA RECRISTALIZACIONES, ORDENADOS PRINCIPALMENTE POR
SUS CONSTANTES DIELCTRICAS
Disolvente
Formamida
Agua
Dimetilsulfxido
N,N-dimetlformamida
Acetonitrilo
Nitrobenceno
Metanol
Etanol
Acetona
n-propanol
sopropanol
Piridina
Diclorometano
Tetrahidrofurano
Acetato de etilo
Cloroformo
ter
Disulfuro de carbono
o-xileno
Frmula
HCONH,
H
2
O
(CH
3
)
2
SO
CH
3
CON(CH
3
)
2
CH
3
CN
C
6
H
5
NO
2
CH
3
0H
C
2
H
6
OH
(CH
3
)
2
CO
n-C
3
H
7
OH
teo-C
3
H
7
OH
C
6
H
5
N
CH
2
CI
2
C
4
H
8
O
CH
3
-COO.C
2
H
5
CHCI
3
(C
2
H
5
)
2
O
CS
2
o-C
6
H
5
.(CH
3
)
2
(c)
193
100.0
189.0
153
81.6
210.9
64+
78.1
56.1
97.8
82.5
115.5
40.1
65.4
77.2
61.3
34.6
46.3
144.4
P,
fe)
2.55
0.0
18.6
-61.0
-45.7
5.7
.-987
-116.0
-95.0
-127
-85.8
-41.8
-96.7
<0
-84.0
-63.5
-116.0
-111.6
-25.0
Constante
dilctrica
109.50
78.5
47.6(23)
36.70
36.20
34.6
32.60
24.30
20.70
19.7
18.3
12.3
8.9
7.39
6.02
4.70
4.22
2.64
2.57(20)
Miscibilidad
en agua
+
+
+
+
+
+
+
+
+
+
+
+
-
-
-
-
-
-
-
46
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Extraccin y recristalizacin de un frmaco
Tolueno
Benceno
Tetracloruro de carbono
Dioxano
n-hexano
ter de petrleo
C
6
H
5
CH
3
C
6
H
6
CCI
4
C
4
H
8
O
2
n-C
6
H
14
C
5
H
1 2
y C
6
H
1 4
110.6
80.2
76.8
101.5
69.0
35-65
-95.0
5,5
-22.8
11.7
-94.3
<0
2.38
2.27
2.23
2.21
1.9
-
-
-
-
-
-
MATERIAL DE VIDRIO
2 matraces Erlermeyer de 50 mi
2 vasos de precipitado de 50 mi
2 vasos de precipitado de 100 mi
1 embudo de separacin de 125 mi
1 probeta de 25 mi
1 pipeta Pasteur
1 matraz Kitazato de 250 mi
1 embudo Buchner
1 mortero con pistilo
1 cristalizador
1 agitador de vidrio
EQUIPO DE LABORATORIO
1 soporte universal
2 pinzas de tres dedos con nuez
1 parrilla
1 esptula
1 agitador magntico mediano
1 anillo pequeo
1 piceta con agua destilada
1 papel pH
1 papel filtro
47
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
REACTIVOS
Cloroformo, CHC1
3
Diclorometano, CH
2
C1
2
Hexano, n-C
6
H
14
ter de petrleo, C
5
H
12
y C
6
H
14
Acetato de etilo, CH
3
-COO.C
2
H
5
Etanol,C
2
H
5
OH
Metanol,CH
3
OH
Hidrxido de sodio, NaOH
cido clorhdrico, HC1
Hielo
PROCEDIMIENTO
Se coloca 1 g de tabletas (que contengan cido acetilsaliclico o acetaminofn),
previamente pulverizadas, en un matraz Erlermeyer de 50 mi. Se adicionan 25 mi
de diclorometano y se agita hasta disolver lo ms posible el slido. Se separa,
filtrando por gravedad y en un papel previamente pesado, el slido insoluble y se
deja secar, para posteriormente evaluar la composicin porcentual del frmaco.
El lquido filtrado se colecta en un vaso de precipitado de 50 mi y se transfiere a
un embudo de separacin; el vaso de precipitado se lava con 5 mi de diclorometano
y ste se vierte tambin en el embudo. Se adicionan 10 mi de una solucin de
NaOH 1M, se tapa el embudo y se agita varias veces, liberando la presin en cada
agitacin. El embudo se deja reposar sobre un anillo para permitir que las fases se
separen. La fase acuosa se colecta en un vaso de precipitado de 100 mi y el
proceso de extraccin se repite otras dos veces. La fase orgnica, de diclorometano,
se guarda en un matraz Erlenmeyer de 100 mi.
Se adiciona a la fase acuosa una solucin 6 M de HC1 (aproximadamente 10 mi)
hasta que el pH sea menor o igual a 2, procurando agitar constantemente durante el
proceso. La mezcla se enfra en un bao de hielo, hasta que ya no aparezca ms
precipitado. Los cristales se filtran y secan lo ms posible en un embudo Buchner
y en papel previamente pesado.
El diclorometano de la fase orgnica se evapora en un bao caliente. Sobre la
base de los pesos de los slidos separados, se calcula la composicin porcentual
aproximada del frmaco.
Con la mitad del cido acetilsaliclico obtenido, se procede a realizar pruebas
de solubilidad, en fro y en caliente, en tubos de ensaye pequeos y con las canti-
dades y disolventes sealados en la tabla 5.2.
48
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Extraccin y recristalizacin de un frmaco
TABLA 5.2 PRUEBAS DE SOLUBILIDAD RECOMENDADAS PARA LA
RECRISTALIZACIN DEL CIDO ACETILSALICLICO
Tubo
1
2
3
4
5
6
Disolvente
hexano
ter de petrleo
cloroformo
acetato de etilo
etanol
metanol
Muestra
(mg)
25
25
25
25
25
25
Volumen
(mi)
1.0
1.0
1.0
1.0
1.0
1.0
Solubilidad
en fro
Solubilidad
en caliente
Nota: En caso de que ninguno de los disolventes propuestos cumpla con los
requisitos arriba sealados, puede realizarse una recristalizacin por par de
disolventes utilizando una mezcla de dos de ellos. Recuerde que en este caso uno
de dichos disolventes debe solubilizar a la sustancia problema, en caliente, y el
otro no disolverla en fro.
Una vez encontrado el disolvente o la mezcla adecuada, se procede a recristalizar
la mitad del cido acetilsaliclico extrado del frmaco. Si se observa que la so-
lucin es colorida, puede agregarse un poco de carbn activado y filtrar en caliente
para eliminar los contaminantes que originan dicho color.
Para recristalizar se disuelve el cido acetilsalcilico en la menor cantidad de
solvente caliente, se evapora hasta el 70% del volumen original y se deja enfriar,
primero hasta temperatura ambiente y despus en hielo. Una vez formados los
cristales, se filtran por succin en un papel previamente pesado y se dejan secar
completamente. Una vez secos, se determina el punto de fusin de los cristales
puros e impuros, se compara su color y forma y si es posible se obtiene el espectro
IR del cido recristalizado (comprelo con el espectro IR-20 del anexo A). Asi-
mismo, con el indicador universal se comprueba que efectivamente la sustancia
recristalizada tiene carcter cido.
OPCIONAL
El cido saliclico puede obtenerse a partir de la aspirina calentando a reflujo,
en agua, y agregando un poco de cido actico. Posteriormente se deja enfriar y se
49
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
filtra el slido formado. Esta sustancia se recristaliza en ter de petrleo (a 40-
60C), obtenindose as cristales en forma de agujas que son cido saliclico
puro, el cual se descompone a 128-135C.
CUESTIONARIO
1. Por qu una sustancia se vuelve ms soluble en un disolvente al aumentar
la temperatura?
2. En la tabla 5.1, los disolventes se ordenaron por el valor decreciente de su
constante dielctrica. En esa tabla, cul es el disolvente ms polar y cul
el menos polar?
3. Investigue la estructura del cido acetilsaliclico y la del acetaminofn.
4. Qu es un analgsico? Qu es un excipiente?
5. Cmo puede obtenerse cido acetilsaliclico a partir de cido saliclico?
6. En el presente experimento, para qu se agrega la solucin de NaOH?
7. Qu funcin cumple la adicin de HC1 a la fase acuosa?
8. Es posible predecir, basndose slo en la estructura de una sustancia, el
tipo de disolvente que puede servir para disolverla y recristalizarla? Se
cumple esto con el cido acetilsaliclico?
BIBLIOGRAFA
1. A. I. Vogel. 1989. Textbook ofPractical Orgnic Chemistry. 5
a
ed. London
Longman Scientific & Technical.
2. J. W. Zubrick. 1992. The Organic Chem lab Survival Manual New York,
John Wiley and Sons.
3. L.A. Kirk. 1978. Enciclopedia de tecnologa qumica. Tomo XI. 3
a
ed.
USA, John Wiley & Sons, p. 424.
4. David C. Eaton. 1989. Laboratory Investigations in Organic Chemistry,
USA, McGraw-Hill.
5. J.A. Landgrabe. 1993. Theory and Practice in Organic Laboratory. 4
a
ed.
Brooks/Cale Calif, USA.
50
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Extraccin y recristalizacin de un frmaco
6. R. M. Silverstein y F. X. Webster. 1998. Spectrometric Identification of
Organic Compounds. 6
a
ed. New York, John Wiley and Sons.
7. Aldrich Chemical. 1997. lite Aldrich Library of FT-IR Spectra. 2
a
ed.
Milwaukee,WI,USA.
51
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Prctica 6
CROMATOGRAFA I:
EN CAPA FINA
OBJETIVO
El alumno comprender el principio de la cromatografa y utilizar sus diversas
posibilidades para la purificacin e identificacin de compuestos orgnicos.
INTRODUCCIN
La cromatografa es la tcnica que permite separar sustancias de diferente color
mediante la distribucin desigual de stas entre dos fases, un adsorbente y un me-
dio de arrastre. En qumica orgnica se utilizan tres tipos de cromatografa: cro-
matografa en capa fina (ccf), cromatografa en columna (ce) y cromatografa de
gas-lquido (cgl). Para separaciones ms especializadas existe la cromatografa
de alta presin de lquidos (cap), la cromatografa de permeacin en gel (cpg) y
la cromatografa de intercambio inico (cii).
Todos los tipos de cromatografa dependen de la distribucin de sustancias
entre dos fases. Estas dos fases son el slido adsorbente y el eluyente, que es la
fase lquida o gaseosa que atraviesa el slido. El slido adsorbe y retiene ms
fuertemente los compuestos ms polares que se encuentran en el lquido; debido a
ello, los menos polares son arrastrados por el eluyente y separados. Al ser retenidas
con mayor fuerza, las sustancias ms polares permanecern ms tiempo dentro del
slido y para extraerlas se necesitar un mayor volumen de lquido.
La adsorcin y desorcin de una sustancia de una superficie slida es lo que se
llama adsorcin cromatogrfica. Esta adsorcin es posible por la existencia de
una fase slida con un lquido estacionario y un segundo lquido que lo atraviesa.
Las sustancias con diferente polaridad se separan o reparten entre estos dos lquidos
en forma desigual; esto es lo que se llama particin cromatogrfica. La adsorcin
y la particin cromatogrfica se encuentran en un equilibrio dinmico en el cual el
soluto se mueve lentamente a travs de un medio adsorbente en la direccin en que
53
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
fluye el lquido. Si en el solvente existe una mezcla de compuestos, stos se
separarn debido a sus diferentes adsortividades y a las distintas velocidades con
que atraviesan el medio adsorbente.
CROMATOGRAFA EN CAPA FINA
Con la cromatografa en capa fina se puede determinar de manera rpida y eficiente
el nmero de componentes de una mezcla, e incluso se puede establecer si dos
sustancias son idnticas o poseen diferente estructura. Esta tcnica es utilizable
slo si los slidos analizados no son voltiles.
Como su nombre lo indica, la cromatografa en capa fina requiere el uso de una
pelcula delgada de adsorbente (de entre 0.10 mm y 0.25 mmm de espesor) soportada
sobre vidrio o plstico.
Debido a la necesidad de realizar experimentos reproducibles, las placas para
cromatografa en capa fina se fabrican con un espesor fijo de adsorbente y se
montan en vidrio, plstico* (polister resistente) o placa de aluminio, y son de
tamao estndar: 2.5 x 6.7 cm. Asimismo, pueden cortarse piezas de este tamao
a partir de placas de 20 x 20 cm, que tambin son comerciales. En el mercado
pueden conseguirse incluso placas para cromatografa con indicador fluorescen-
te, la cual es recomendable para el estudio de compuestos no coloridos pero
fluorescentes.
En la cromatografa de capa fina son comunes tres tipos de medios adsorbentes:
la almina, el gel de slice y la celulosa. Cada una de estas sustancias se utiliza
como un polvo activo finamente pulverizado. Se dice que un adsorbente se ha
activado cuando se le calienta para eliminar el agua que ha adsorbido. La almina
y el gel de slice se utilizan para analizar una gama muy grande de compuestos
orgnicos polares y no polares. La almina es ms polar que el gel de slice, y por
lo tanto retiene ms fuertemente a las sustancias que adsorbe. La celulosa es utilizada
para estudiar compuestos orgnicos muy polares o solubles en agua, razn por la
cual es un medio ms verstil. La celulosa puede adsorber hasta un 20% en peso
de agua.
Si no se dispone de cualquiera de estos productos, se pueden fabricar placas de
pelcula delgada con portaobjetos de vidrio, como se indica en el anexo.
El adsorbente ms popular en este caso es el gel de slice G o cido silcico.
ste no es ms que slica hidratada (SiO
2
. x H
2
O) con aproximadamente un 10%
de yeso (CaSO
4
.1/ 2H
2
O). La slica GF es slica hidratada con yeso y un indicador
fluorescente.
El adsorbente se pega fuertemente si se usa alcohol polivinlico.
54
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Cromatografa I: en capa fina
Para preparar la placa de cromatografa se puede utilizar uno de varios
disolventes, pero el cloroformo es el ms recomendable. La adicin de metanol al
cloroformo hace que el yeso se una ms fuertemente al vidrio.
Nota: Si la placa que se va a utilizar es muy vieja, se puede activar calentndola a
100C por 30 minutos.
MATERIAL DE VIDRIO
1 vaso de precipitado de 100 mi
1 vidrio de reloj
1 pipeta Pasteur
1 jarra para revelado de placas cromatogrficas (Fig. B 2h del anexo B)
EQUIPO DE LABORATORIO
Lmpara UV porttil
REACTIVOS
Almina, A1
2
O
3
Gel de slice, SiO
2
- xH
2
O
Metanol, CH
3
OH
Cloroformo, CHC1
3
ter dietlico, (CH
3
CH
2
)
2
O
Etanol,CH
3
CH
2
OH
Azul de bromotimol
/?-nitrofenol
Fibra de vidrio
Arena para cromatografa o sulfato de sodio anhidro, Na
2
SO
4
Placa para cromatografa en capa fina o 3 portaobjetos
PROCEDIMIENTO
Se aplica una pequea cantidad de mezcla problema (que puede ser una mezcla de
azul de bromotimol y p-nitrofenol, mezcla de tinta china o estracto de pasto o
55
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
betabel) cerca de la parte inferior de la pelcula adsorbente* (digamos a 10 mm).
La pelcula se coloca en un recipiente con tapa en el cual se ha vertido un mnimo
de disolvente (5 a 10 mm). Debe tenerse cuidado de que la zona donde se aplic la
mezcla problema no quede sumergida en el disolvente. El disolvente arrastra por
ascenso capilar los distintos componentes de la mezcla, los cuales ascienden por
la pelcula adsorbente segn su menor polaridad.
Se deja que el lquido ascienda hasta que ya no se observe desplazamiento
alguno del frente de lquido. Despus de ocurrido esto, la pelcula se deja secar y
se procede a examinarla.
Una vez seca la pelcula, se podrn notar zonas ms coloridas en las cuales se
han ubicado los diferentes componentes de la mezcla. Si no es posible observarlos
claramente, puede revelarse la pelcula, colocndola unos momentos en un
recipiente que contiene unos cristalitos de yodo, los cuales, al sublimar, realzarn
aquellas zonas donde las sustancias se han estancado. Tambin puede iluminarse
la placa con una lmpara UV (hay que tener cuidado de no observar la luz
directamente) para observar aquellas sustancias que no son coloridas pero son
fluorescentes.
Recurdese que mientras ms fuerte sea la interaccin entre una sustancia y el
slido adsorbente, ste se mover ms lentamente en dicha sustancia. Es decir que
un disolvente arrastrar ms rpidamente las sustancias no polares. Es posible
que las sustancias polares se desplacen lentamente o que no sean arrastradas por
el disolvente.
En condiciones definidas de trabajo, una sustancia dada puede desplazarse una
distancia relativa (d
s
) respecto al frente del disolvente utilizado (dj). La razn
entre estas distancias se llama cociente de arrastre o grado de arrastre (R
f
):
R
f
= d/d,
El valor de R
f
es una propiedad fisicoqumica de cada sustancia y depende de su
estructura. Para calcular R
f
slo debern medirse las distancias recorridas por el
frente del lquido y por los distintos componentes de la mezcla.
La cromatografa en capa fina permite estimar qu tan bueno es un disolvente
para utilizarse en cromatografa en columna. Un disolvente puede utilizarse como
eluyente de algn componente de una mezcla cuando provoca un Rf del orden de
0.3 o mayor. La cromatografa en capa fina tambin permite analizar el nmero de
componentes de una fraccin salida de una cromatografa en columna, siempre y
cuando se disponga de un buen agente revelador.
* La mezcla problema puede ser una mezcla de azul de bromotimol y p-nitrofenol, una mezcla
de tintas, o extracto de pasto o betabel.
56
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Cromatografa I: en capa fina
FABRICACIN DE PLACA CROMATOGRAFICA
a) Lave bien con jabn y agua los portaobjetos de vidrio y squelos.
b) Prepare una suspensin de 40 g de gel de slice G en 100 mi de una mezcla
2:1 (en volumen) de cloroformo y metanol, y agtela por un minuto o hasta
que obtenga una mezcla homognea.
c) Coloque cara a cara dos portaobjetos y sumrjalos en la suspensin, hasta
que slo 1 cm quede fuera.
d) Extraiga lenta y uniformemente los portaobjetos de la mezcla, permitiendo
que el disolvente se evapore lentamente para que no se formen grietas. Des-
pus de que el disolvente se ha evaporado, separe los dos portaobjetos y
djelos secar unos minutos.
Frente de
disolvente
1 cm
(a) (b)
Figura 1 a) Montaje de una prueba de cromatografa en pelcula delgada; b) placa de
pelcula delgada con dos muestras a diferente distancia de arrastre ds.
57
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
CUESTIONARIO
1. Explique lo que entiende por cromatografa y diga cuntas clases de
cromatografa conoce.
2. Cul es la utilidad inmediata de la cromatografa en capa fina?
3. Cmo escogera el disolvente ms adecuado para utilizarlo como eluyente?
4. Qu es la adsorcin cromatogrfica? Qu diferencia existe entre adsorcin
y absorcin?
BIBLIOGRAFA
1. J. R. Mohring y D. C. Neckers. 1979. Laboratory Experiments in Organic
Chemistry. 3
a
ed. New York, D. Van Nostrand.
2. Shellard, EJ. Quantitative paper and Thin Layer Cromatography, Aca-
demic Press, New York, 1968.
3. Stahl E. Thin Layer Chromatography, a Laboratory Handbook, 2
a
ed.
Spring-Verlag, New York, 1969.
4. Stock R., Rice C. B.I. Chromatographic Methods, Halsted Press of John
Wiley & Sons, New York, 1959.
5. Zweig G., Whitaker, J.R. Paper Chromatography andElectrophoresis, Vol.
I and II, Academic Press, New York, 1969.
58
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Prctica 7
CROMATOGRAFA II: EN COLUMNA
OBJETIVO
El alumno entender el principio de la cromatografa y utilizar sus diversas posibilidades
para la purificacin e identificacin de compuestos orgnicos.
INTRODUCCIN
La cromatografa en capa fina y en columna son dos ejemplos de cromatografa de
adsorcin. En ambos casos los slidos adsorbentes utilizados son los mismos,
pero en la cromatografa en columna el tamao de los granos de adsorbente es
considerablemente mayor.
En la cromatografa en columna se utilizan principalmente dos medios ab-
sorbentes: el xido de aluminio, A1
2
O
3
, y el gel de slice, SiO
2
x H
2
O. La almina se
utiliza principalmente para separar compuestos medianamente o no polares y el gel de
slice para separar compuestos orgnicos polares.
La almina para cromatografa se encuentra disponible como un polvo fino y
puede ser: acida (pH = 4), neutra (pH = 7) y bsica (pH = 10). La almina activada
es aquella que se ha sometido a un tratamiento trmico para eliminar su contenido
de agua, lo cual le confiere capacidades adsorbentes muy importantes. Una almina
activada de grado I (segn el sistema de clasificacin de Brockman) es aquella
que se ha calentado a 400-450C y hasta que ya no pierde ms agua. La almi-
na que ha adsorbido un 3% de agua se denomina de grado II, la que ha adsorbido
6% es la de grado III, y las de grados IV y V son aquellas que contienen un 10% y
un 15% de agua respectivamente.
El grado de adsorcin de una sustancia en la almina depende sobre todo de las
fuerzas de atraccin (fuerzas de Van der Walls, interacciones dipolo-dipolo, en-
laces puente de hidrgeno y coordinaciones) entre la sustancia y la superficie
adsorbente.
59
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
Las sustancias orgnicas polares, como los cidos carboxlicos, las aminas, los
polioles, etc., se adsorben tan fuertemente en la almina que para separarlos de
ella y extraerlos es necesario utilizar disolventes muy polares.
El gel de slice por lo general se utiliza como un soporte slido del agua, por lo
cual los compuestos en ella separados se reparten entre el agua fuertemente unida
a la superficie de gel de slice y el disolvente eluyente. Por tanto, la eficiencia de
la separacin depende de la solubilidad relativa de los compuestos entre el agua
y el lquido eluyente. El gel de slice comercial contiene por lo general de 10 a
20% de agua adsorbida y se utiliza sin necesidad de activarlo por calentamiento.
ELUYENTES
En cromatografa, los lquidos utilizados para separar los compuestos adsorbidos
en la columna de cromatografa deben ser progresivamente ms polares. Los
compuestos polares son fuertemente adsorbidos por la superficie del xido metlico,
y para separarlos (eluirlos) y extraerlos de la columna es necesario utilizar
disolventes ms polares. Por el contrario, los compuestos no polares se unen con
menos fuerza al slido adsorbente y son separados ms fcilmente por disolventes
no polares.
La velocidad con la cual una sustancia es separada puede controlarse cambiando
la polaridad del disolvente o el grado de actividad del slido adsorbente. Por
ejemplo, si una sustancia es eluida con rapidez pero su separacin respecto de
posibles contaminantes es poco eficiente, se recomienda utilizar un adsorbente
ms fuerte o bien utilizar un disolvente menos polar. Por el contrario, si la
purificacin es eficiente pero muy lenta, se recomienda cambiar el adsorbente por
uno menos activo.
La siguiente serie es el orden recomendado de lquidos eluyentes por probar, y
va del menos al ms poderoso:
Alcanos (ter de petrleo, hexano, ciclohexano)<CCl
4
<tolueno<CH
2
Cl
2
<ter
dietlico< CHCl
3
<acetona<acetato de etilo<etanol<metanol (consulte la constante
dielctrica de estas sustancias en la Tabla 5.1 de la Prctica 5).
DIMENSIONES DE LA COLUMNA
Tenga en cuenta que una columna ms larga y delgada adsorber ms tenazmente
los compuestos que una corta y ancha. Una razn de 8:1 a 10:1 entre la altura y el
dimetro de la columna es lo recomendable.
60
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Cromatografa II: en columna
Por otro lado, es recomendable utilizar de 20 a 30 veces ms de slido adsorbente
que de mezcla problema, aunque puede ser una cantidad mayor si la separacin es
poco eficiente.
Por ejemplo: si se desea separar 10 gramos de muestra problema en una bure-
ta de 3.4 cm, lo recomendable son 250 g de almina (la almina tiene una densidad
de aproximadamente 1 g/cm
3
) y la columna tendr una altura de aproximadamen-
te 27 cm.
La altura de la columna puede calcularse con facilidad (el volumen de un cilin-
dro = 7ir
2
h), o en su caso el dimetro ms adecuado.
Por ejemplo, si se van a utilizar 20 g de almina y el tubo de vidrio tiene un
dimetro de 1.5 cm, la columna tendr una altura de 11 cm.
El gel de slice tiene una densidad de 0.3 g/cm
3
, mucho menor que la almina,
es por ello que al trabajar con esta sustancia es necesario utilizar columnas ms
anchas.
Por lo general, para construir una columna de cromatografa se utilizan piezas
de vidrio que en su parte inferior poseen una llave para controlar la salida del
lquido eluyente.
Al construir una columna de cromatografa se debe tener cuidado ya que la
existencia de imperfecciones, burbujas de aire atrapadas o fisuras provocar una
separacin deficiente de las muestras.
MATERIAL DE VIDRIO
1 bureta de 25 mi o una columna de vidrio con llave
3 matraces Erlenmeyer de 125 mi
1 vaso de precipitado de 100 mi
1 vaso de precipitado de 50 mi
1 embudo de cuello largo
1 pipeta graduada de 5 mi
1 propipeta
EQUIPO DE LABORATORIO
1 soporte universal
1 pinza para bureta (Fig. B 4c del anexo B)
61
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
REACTIVOS
Almina, A1
2
O
3
Gel de slice, SiO
2
xH
2
O
Placa para cromatografa en capa fina
Fibra de vidrio
Arena para cromatografa
Hexano, C
6
H
14
Metanol,CH
3
OH
Cloroformo, CHC1
3
ter dietlico, (CH
3
CH
2
)
2
O
Etanol, CH
3
CH
2
OH
Diclorometano, CH
2
C1
2
Tolueno, C
6
H
5
CH
3
Acetona, CH
3
COCH
3
Acetato de etilo, CH
3
COOCH
2
CH
3
Azul de bromotimol
/7-nitrofenol
PROCEDIMIENTO
A) Montaje de la columna (Fig. 7.1)
1. Se coloca y fija la columna de vidrio en posicin vertical, mediante las
pinzas para ello creadas, cuidando de no apretar en exceso.
2. Se llena la columna con lquido eluyente que se planee usar, o bien con el de
menor polaridad, hasta aproximadamente la mitad.
3. Se coloca un retn en la parte inferior interna de la columna, utilizando un
trozo de fibra de vidrio. Debe tenerse cuidado de que no queden burbujas
de aire atrapadas.
4. A continuacin, se cubre con una capa de entre 5 y 10 mm de arena blanca
(aunque puede utilizarse sulfato de sodio anhidro).
5. Se agrega lentamente el slido adsorbente por la parte superior de la columna,
cuidando que caiga de manera uniforme en el fondo de sta. Este paso se
lleva a cabo lentamente para que la columna formada sea firme pero no
apretada y permita el paso del disolvente.
6. Unos pequeos golpes a los lados de la columna permiten obtener una columna
uniforme, horizontal y sin burbujas atrapadas. Si se observan canales o
muchas burbujas atrapadas, es mejor extraer el disolvente y rehacer la
columna.
62
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Cromatografa II: en columna
7. Una vez agregado todo el adsorbente, se adiciona una capa de 5 mm de
arena blanca para proteger la capa de adsorbente.
8. Se elimina el lquido eluyente en exceso, cuidando que su nivel nunca sea
inferior a la capa superior de arena.
Nota: a) Si se va a utilizar un disolvente ms polar que el tetracloruro de car-
bono, se recomienda mezclar el slido adsorbente en dicho disolvente
y despus adicio-narlo a la columna, para evitar la presencia de bur-
bujas de aire atrapadas y que el lquido se evapore, seque la columna
y la arruine.
b) Si se construye una columna de gel de slice, sta debe adicionarse a
la columna lo ms lentamente que se pueda ya que contiene mucho
ms aire que la almina.
tt) Fibra de vidrio o algodn
Figura 7.1 Montaje de una columna de cromatografa.
63
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
B)Elusin
Prepare una disolucin de la mezcla problema, lo ms concentrada posible (en no
ms de 5 mi del lquido eluyente). Antes de adicionar la disolucin problema, por
la parte superior de la columna, cercirese de que el nivel de lquido no se encuentre
muy por arriba de la capa de arena, pues un exceso de disolvente provocar una
mezcla y una separacin deficiente de sus componentes.
Si la muestra problema no se disuelve en el disolvente de la columna, puede
agregarse una pequea cantidad de un disolvente ms polar para disolverla.
A continuacin se abre la llave de la columna para permitir la salida del eluyente
hasta que su nivel superior quede al ras de la capa de arena. Para iniciar la se-
paracin se agrega ms disolvente y se abre nuevamente la llave de flujo, evitando
siempre que la columna se seque.
Si el disolvente utilizado no favorece la separacin, se agrega otro de mayor
polaridad. La separacin se considera eficiente cuando el flujo de disolvente
provoca la formacin de bandas fcilmente distinguibles y separadas en el tramo
de columna.
Recolecte cada banda de color que sale de la columna en un matraz bien
etiquetado para su posterior manipulacin.
Si un primer disolvente no arrastra fraccin alguna, se pueden agregar mezclas
de concentracin creciente de otro disolvente, de distinta polaridad (disueltas en
el primero), para evitar que el calentamiento provocado por una mezcla abrupta
de disolventes con polaridades muy diferentes fracture la columna.
El tiempo ptimo de salida del eluyente es de aproximadamente 2 ml/7 min, ya
que un flujo ms grande no permite que el equilibrio de adsorcin ocurra
correctamente.
Cuando los componentes de una mezcla problema no son coloridos, puede
utilizarse una lmpara UV para detectarlas. Si aun de esta forma no son observables,
se deber realizar una recoleccin en matraces pequeos y numerados, los cuales se
analizarn por espectroscopia UV-Visible u otra tcnica para poder combinar
aquellos que contienen una nica y misma fraccin. Si no se detecta componente
alguno de la mezcla, ser necesario cambiar de eluyente.
C) Purificacin
Para obtener los distintos componentes de la mezcla problema en forma pura, se
eliminan los disolventes por destilacin en un evaporador rotatorio.
Si alguno o algunos de los componentes de la mezcla fueran muy difciles de
extraer, puede recurrirse a la cromatografa en columna seca. Esta seudotcnica
64
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Cromatografa II: en columna
consiste en permitir la separacin de los componentes de la mezcla en la columna
aunque no se extraigan, eliminar lo ms posible de eluyente, extraer el slido
adsorbente y cortar en rodajas las distintas fracciones observadas. Despus se
lava cada rodaja con el o los disolventes que logren separar cada sustancia del
slido adsorbente, y por ltimo se evaporan todos los disolventes.
Nota: Si no se desea separar mezclas de productos naturales, puede prepararse
una mezcla problema de entre las siguientes:
a) 1 mg de azul de bromotimol y 1 mg de p-nitrofenol, eluyendo con metanol.
b) 50 mg de p-nitroanilina y 70 mg de o-nitroanilina, eluyendo con benceno
(aunque no es recomendable) sobre almina grado IV.
c) Una mezcla 1:1:1 de benzofenona, difenilmetanol y difenilo, eluyendo con
ter de petrleo, benceno y ter (en ese orden) sobre almina grado IV.
Estas tres sustancias incoloras se recolectan en matraces de hasta 25 mi,
para posteriormente analizarse por cromatografa en capa fina u otra tcnica.
CUESTIONARIO
1. La almina y el gel de slice son los nicos slidos adsorbentes que se
pueden utilizar en cromatografa?
2. Si al realizar una separacin cromatogrfica en columna de gel de slice
llena con cloroformo ningn componente se puede separar, qu hara usted
para separar los distintos componentes?
3. Si trabajara con compuestos que no son coloridos ni fluorescentes, de qu
otra manera podra realizar una separacin exitosa?
4. Si realiza una separacin con una columna de almina usando cloroformo
como eluyente, en qu orden salen el ter dietlico, el p-nitrotolueno, el
benceno y el cloroetano, que tienen los momentos dipolares (x 10
18
): 1.0,
4.5,0.0 y 2.0 respectivamente?
BIBLIOGRAFA
1. Determann H, Gel Chromatography, a Laboratory Handbook, 2
a
ed. Spring-
Verlag, New York, 1969.
65
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
2. Fischer, L. Introduccin a la Cromatografa en Gel, Editorial el Manual
Moderno, S.A. Mxico, 1975.
3. J. R. Mohring y D. C. Neekers. 1979. Laboratory Experiments in Organic
Chemistry. 3
a
ed. New York, D. Van Nostrand.
4. Stock, R., Rice C.B.L Chromatographic Methods, Halsted Press of John
Wiley & Sons, New York, 1959.
66
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Prctica 8
ISOMERA CIS-TRANS: ISOMERIZACION
DEL CIDO MALEICO A FUMRICO
OBJETIVO
El alumno comprender el concepto de isomera, en particular el de isomera cis-
trans, al realizar la transformacin del ismero cis del cido 2-butenodiico (cido
maleico) al ismero trans, o cido fumrico, y observar sus formas cristalinas y
sus diferentes puntos de fusin.
INTRODUCCIN
Dos sustancias son ismeros cuando poseen la misma frmula molecular pero di-
fieren en la conectividad o en la disposicin espacial sus tomos.
Los cidos maleico y fumrico pueden obtenerse a partir del cido mlico, ya
que ste se deshidrata en presencia de medio cido, formndose el carbocatin
intermediario. Cuando el proceso se realiza a baja temperatura los grupos carboxilo
(-COOH) se repelen mutuamente; en consecuencia, el enlace a gira de tal modo
que al formarse el doble enlace estos grupos quedan ubicados en lados opuestos
del enlace n, obtenindose el cido fumrico (ismero trans). Cuando la reaccin
se realiza a mayor temperatura, los grupos carboxilo pueden vencer la mutua
repulsin y al formarse el doble enlace tales grupos quedan ubicados del mismo
lado del doble enlace TC, obtenindose as el cido maleico (ismero cis).
67
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
HOOC COOH
a | TI |
HOOC-CH-CH-COOH > HOOC-CHCH-COOH ->HC=CH + H
+
II I +
H OH H
cido mlico 1 cido maleico
HOOC (ismero cis)
I n
HC=CH +H
+
COOH
cido fumrico
(ismero trans)
Debido a que en la estructura del cido maleico los grupos qarboxilo se localizan
uno frente al otro es muy fcil que reaccionen, producindose entonces el anhdrido
maleico. Esta propiedad permite diferenciar y separar al cido maleico del fu-
mrico. En nuestro experimento se parte precisamente del anhdrido maleico que
se hidroliza fcilmente para dar el cido maleico, bastante soluble en agua y que tie-
ne un bajo punto de fiisin (130C). Por otra parte, el doble enlace del cido
maleico puede hidratarse fcilmente con cido clorhdrico que lo isomeriza en
cido fumrico, muy insoluble y de punto de fusin elevado (ms de 220C).
MATERIAL
2 vasos de precipitado de 50 mi
2 tubos de ensaye medianos
2 tubos de ensaye pequeos
1 embudo Buchner
1 matraz Kitazato
EQUIPO DE LABORATORIO
1 esptula
1 parrilla de calentamiento
1 bscula
1 aparato de Fisher-Johns (Fig. C 11 del anexo C)
68
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Isomera cis-trans: Isomerizacin del cido maleico a fumrico
SUSTANCIAS
Anhdrido maleico, C
4
H
4
O
3
cido clorhdrico, HC1
Permanganato de potasio, KMnO
4
Bromo, Br
2
(de preferencia disolucin al 1%)
Agua destilada
PROCEDIMIENTO
PRUEBA
Se disuelven 2.5 g de anhdrido maleico en 5 mi de agua destilada. Hecho esto, se
calienta hasta fundir el anhdrido maleico y a continuacin se agrega un poco de
agua para disolver el cido maleico formado. La solucin se enfra y se filtra en
un embudo Buchner. El slido filtrado se seca, y se determina su punto de fusin
(P
f
= 130.5C) con el aparato de Fisher-Johns.
Al lquido filtrado se le adiciona un poco de cido clorhdrico concentrado
(entre 1.5 y 2 mi es suficiente), se calienta suavemente hasta que d la solucin
empiecen a separarse los cristales de cido fumrico, lo cual ocurre al calentar
durante 5 a 10 min. Se deja enfriar la mezcla, se filtra el slido, se seca, se pesa y
se determina su punto de fusin (mayor de 220C).
En dos tubos de ensaye pequeos se colocan unos 10 mg de cido maleico y cido
fumrico y se observa qu pasa al agregar a cada tubo 1 mi de solucin acuosa de
bromo al 1%. La prueba se repite con solucin de permanganato de potasio.
Para comprobar que las sustancias obtenidas son cidos carboxlicos, se utiliza
un indicador universal como el de la prctica 2.
Nota: Se recomienda que la disolucin al 1% de bromo sea preparada por el pro-
fesor en un lugar ventilado y se utilicen guantes y lentes de proteccin.
69
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
CUESTIONARIO
1. Defina el concepto de isomera. Describa los tipos de isomera ms frecuentes
en qumica orgnica.
2. A qu se debe la mayor solubilidad del cido maleico en agua?
3. Por qu el cido fumrico hierve a mayor temperatura?
4. Describa el mecanismo de reaccin de la transformacin de cido maleico
a fumrico.
5. En la anterior experiencia, el cido clorhdrico es un reactivo o un cata-
lizador?
6. Suponga una mezcla slida problema que entre sus componentes tiene al
cido fumrico; cmo lo separara del resto de los componentes?
BIBLIOGRAFA
1. H. Murillo. 1970. Tratado elemental de qumica orgnica. 10
a
ed. Mxico,
ECLALSA,p.241.
2. R.T. Morrison y R.N. Boyd. 1992. Qumica orgnica. 5
a
ed. Mxico, Adisson-
Wesley Iberoamrica.
3. S. H. Pine. 1993. Qumica orgnica, 2
a
ed. Mxico, Me Graw-Hill.
4. X. A. Domnguez. 1989. Experimentos de qumica orgnica. Mxico,
Limusa,p. 75.
70
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Prctica 9
REACCIONES DE SUSTITUCIN
NUCLEOFLICA (SN): SNTESIS DE LOS
CLORUROS DE A7-BUTILO Y ferf-BUTILO
OBJETIVO
a) El alumno sintetizar los cloruros de -butilo y ter-butilo a partir de los
alcoholes respectivos.
b) El alumno comprender que estos compuestos se obtienen mediante reac-
ciones de sustitucin nucleoflica (S
N
).
c) El alumno evaluar la importancia del efecto estrico en la obtencin de los
productos, as como la formacin del intermediario ms estable.
REACCIONES
Para realizar un anlisis del efecto estrico, es recomendable elegir las experiencias
a y c que se presentan a continuacin. Ahora bien, puede compararse el poder
nuclefilo del ion cloruro y el ion bromuro realizando las experiencias a y b. Si el
profesor considera muy tediosas y largas estas experiencias, puede sugerir solamente
la experiencia a para ilustrar una reaccin de sustitucin nucleoflica.
ZnCl,
a) CH
3
CH
2
CH
2
CH
2
_OH + HC1
2 4
b) CH
3
CH
2
CH
2
CH
2
_OH + NaBr * CH
3
CH
2
CH
2
CH
2
3r
c) (CH
3
)
3
C-OH + HC1 (CH
3
)
3
C-C1
71
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
MATERIAL DE VIDRIO
1 juego de qumica conjuntas 19/22
3 matraces Erlenmeyer de 25 mi
1 vaso de precipitado de 50 mi
1 matraz Kitazato de 100 mi
1 pipeta graduada de 5 mi
EQUIPO DE LABORATORIO
2 soportes universales
3 pinzas de tres dedos c/ nuez
1 anillo de hierro para soporte universal
1 parrilla
1 restato
1 manta de calentamiento
1 termmetro
1 esptula
1 propipeta
REACTIVOS
Alcohol n-butlico, n-C
4
H
9
_OH
Alcohol tert-butilico t- C4H
9
_OH
cido clorhdrico, HC1
cido sulfrico, H
2
SO
4
Cloruro de cinc, ZnCl
2
Bicarbonato de sodio, NaHCO
3
Sulfato de sodio anhidro, Na
2
SO
4
Bromuro de sodio, NaBr
PROCEDIMIENTO
A) Sntesis de cloruro de tert-butilo:
Se mezclan 2.5 g de alcohol tert-butilico y 10 mi de cido clorhdrico concentrado
en un pequeo vaso de precipitado de 50 mi (mezclar en la campana). La mezcla
72
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Reacciones de sustitucin nucleofilica (S
N
): Sntesis de los cloruros de n-butilo y ert-buto
se transfiere a un embudo de separacin pequeo y se deja reposar por 40 minutos,
procurando agitar de vez en cuando. Se deja reposar, hasta que se formen dos
fases, y entonces se elimina la fase acuosa. La fase orgnica se lava con 5 mi de
agua destilada y dos veces con 5 mi con disolucin al 5% de bicarbonato de sodio
(precaucin: la mezcla de bicarbonato de sodio con el medio cido provoca la
formacin de CO
2
; debe aliviarse la presin generada en cada extraccin). El pro-
ducto se vierte en un matraz Erlenmeyer de 25 mi y se seca con suficiente sulfato
de sodio anhidro. El lquido se transfiere a otro matraz Erlenmeyer, seco y pre-
viamente pesado. El cloruro de ter-butilo puede purificarse destilando a 49-
51C. El rendimiento esperado es del 90%.
B) Sntesis de bromuro de butilo:
Se colocan 2.5 g de bromuro de sodio, 3 mi de agua y 1.9 mi de alcohol n-butlico
en un matraz redondo de 50 mi. La mezcla se enfra en agua con hielo y se adiciona
lentamente 2.1 de cido sulfrico concentrado, sin dejar de agitar. Se coloca un
refrigerante sobre el matraz redondo y se calienta la mezcla a reflujo por 30 minutos.
Se deja enfriar lentamente para que la reaccin termine. Con el mismo condensador,
se monta ahora un sistema de destilacin y se recibe la fraccin que hierve a
115C. Se detiene la destilacin cuando ya no se observa la salida de gotas de
sustancia insoluble en el agua (se recomienda realizar pequeas pruebas a la gota
en tubos de ensaye). Un incremento en el punto de ebullicin se debe a la ebullicin
del bromuro de n-butilo y agua que contiene cantidades crecientes de cido
sulfrico. El destilado se transfiere a un embudo de separacin y se lava con 5 mi
de agua destilada. Si se observa una coloracin rosada, debida a trazas de bromo,
se debern agregar unos granos de bisulfito de sodio y agitar varias veces para
que la coloracin desaparezca o disminuya. Se separa el bromuro de butilo, la
capa inferior de lquido, y se vuelve a lavar con 2 mi de cido sulfrico concentrado
fro, se agita vigorosamente por 5 minutos y se deja reposar para que se separen
las capas. Despus de aproximadamente 5 minutos se separa la capa de bromuro
(ahora ser la capa superior, pues el cido sulfrico concentrado tiene una densidad
de 1.84 gr/ml y el bromuro una densidad de 1.275 g/ml) y se lava con 2.0 mi de
una disolucin al 5% de NaOH. El bromuro de butilo turbio se seca con un poco
de sulfato de sodio anhidro y la mezcla se calienta ligeramente hasta que se torna
transparente. Se decanta el lquido y se transfiere a un matraz redondo seco y
limpio para que destile el bromuro de butilo a 99-103C. El volumen de lquido
obtenido se pesa y se mide (aproximadamente 1.9-2.3 g, 42-50% de rendimiento).
De ser posible, obtngase el espectro IR del compuesto.
73
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
NOTAS
C) Sntesis de cloruro de butilo
En un matraz redondo se colocan 5 g (6.2 mi) de n-butanol, 11 mi de cido
clorhdrico concentrado y 18.4 g de cloruro de zinc anhidro. Se adapta un
condensador al matraz redondo para mantener un reflujo por dos horas, con agita-
cin constante. Para evitar que escapen vapores de cido clorhdrico, se adapta
una junta a la parte superior del condensador para que los vapores se hagan
burbujear en un matraz pequeo con agua.
Transcurridas las dos horas de reflujo, se modifica el sistema y se monta un
sistema de destilacin para obtener su producto, el cual hierve a 115C. Se separa
la fraccin superior del destilado, se mide su volumen y se transfiere a otro matraz
redondo. Se agrega el mismo volumen de cido sulfrico concentrado y se calienta
a reflujo por aproximadamente 30 minutos. Entonces se destila el producto, el
cual hierve a 76-79 C. El compuesto se transfiere a un embudo de separacin y se
lava con 6 mi de agua destilada, 2.5 mi de una disolucin al 5% de hidrxido de
sodio y por ltimo con otros 6 mi de agua destilada. Se procede a secar con
suficiente sulfato de sodio anhidro. Si se desea purificar ms, puede volverse a
destilar a 75-78 C. El volumen de lquido obtenido se pesa y se mide (rendimiento
de 60 a 65%) para calcular el rendimiento. De ser posible, obtngase el espectro
IR del cloruro de tert-butilo (espectro IR-21 en el anexo A).
Se utiliza cido sulfrico concentrado para remover impurezas de alto punto de
ebullicin que no pueden separarse por simple destilacin.
Se recomienda utilizar sulfato de sodio anhidro como desecante, ya que el cloruro
de calcio anhidro podra provocar la eliminacin del cloruro en el producto en
caso de que la mezcla an sea acida.
CUESTIONARIO
1. Cul es el mecanismo de reaccin en cada caso?
2. Qu otros productos se pueden formar?
3. Qu efecto tiene en la reaccin el utilizar un alcohol primario en lugar de
uno terciario?
4. En el mecanismo planteado, qu carbn es ms estable; uno primario, uno
secundario o uno terciario?
5. Para sintetizar cloruro de butilo es necesario calentar y para obtener el
cloruro de tert-butilo no. Por qu?
74
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Reacciones de sustitucin nucleoflica (S
N
): Sntesis de los cloruros de -butilo y tert-butilo
6. Con cul alcohol se obtiene mayor rendimiento de producto? Por qu?
7. Basndose en los rendimientos arriba indicados de bromuro de butilo y
cloruro de butilo, explique: cul es el nuclefilo ms poderoso, el cloro o
el bromo? Qu reaccin ocurrir con mayor rapidez y por qu?
BIBLIOGRAFA
1. A. I. Vogel. 1989. Textbook ofPractical Organic Chemistry. 5
a
ed. London,
Longman Scientific & Technical, p. 383.
2. L. F. Fieser. 1968. Organic Experimente. 2
a
ed. USA, D. C. Heath and
Company, p. 79.
3. M. Fieser y L.F. Fieser. 1974. Organic Synthesis. Vol. 1. New York, John
Wiley& Sons, p. 441.
4. R. K. Stevens y J. A. Hodgenson, Modern Classics in Analitical Chemistry.
Vo\2
9
Am. Chem. Soc, 205, 2 (1976).
5. L.A. Kirk. Enciclopedia de tecnologa qumica. Tomo XI, 3
a
ed. USA, John
Wiley&Sons.
75
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Prctica 10
ESPECTROSCOPIA EN LA REGIN DEL
INFRARROJO
OBJETIVOS
a) El alumno comprender el principio bsico de la espectroscopia, en par-
ticular la espectroscopia en la regin del infrarrojo (IR).
b) El alumno aprender a identificar las seales tpicas de los grupos
funcionales ms comunes en qumica orgnica.
c) El alumno obtendr los espectros IR de sustancias slidas y lquidas,
analizar las seales ms importantes y propondr estructuras para los
espectros obtenidos.
INTRODUCCIN
El espectro electromagntico est constituido por una amplia gama de regiones
entre las que destacan (Tabla 10.1): luz visible (Vis), regin del ultravioleta (UV),
regin del infrarrojo (IR), regin de los rayos X, regin de las microondas, regin
de las ondas de radio, etc. La radiacin electromagntica puede describirse por su
longitud, que es la distancia de un ciclo completo de la onda (A,, letra griega
larnda), o por su frecuencia (v, letra griega nu), que es el nmero de ciclos de la
onda que pasan por un punto por unidad de tiempo, por lo general el segundo.
77
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
TABLA 10.1 PRINCIPALES REGIONES EN QUE SE DIVIDE EL
ESPECTRO ELECTROMAGNTICO Y EFECTO QUE PROVOCA
CADA ZONA AL INCIDIR SOBRE LA MATERIA
Regin
Rayos gamma
Rayos X
Ultravioleta (UV)
Visible (Vis)
Infrarrojo (IR)
Microondas
Ondas de Radio
Ondas de Radio
Mm)
<10-10
10-M0-
10
4 x 10-
7
- 10-
8
8x 10~
7
- 4 x 10-
8
10-
4
-2.5 x 10*
10"
2
-10"
4
10"
2
10
Energa
KJ/mol
> 10
6
10
4
- 10
6
10
3
- 10
4
10
2
- 10
3
1-50
0.01 a 1
0.01
10"
5
Efecto
Transiciones nucleares
Transiciones de electrones
internos
Prdida de electrones de
valencia
Transiciones electrnicas
Vibraciones moleculares
Rotaciones moleculares
Resonancia del espn del
electrn (RSE*)
Resonancia del espn
nuclear (RMN**)
* ESR = Resonancia del espn del electrn. **RMN = Resonancia magntica nuclear.
La regin de la luz visible constituye una pequea parte del espectro global (de
3.8 x 10"
5
cm a 7.8 x 10~
5
cm de longitud de onda) y est limitada por las regiones
del infrarrojo y del ultravioleta.
Cuando una sustancia se expone a radiacin electromagntica, absorbe energa
de ciertas longitudes de ondas pero deja pasar otras. Cul radiacin es absorbida
y cul no depende tanto de la estructura del compuesto como de la longitud de on-
da de la radiacin. Si el material se expone a radiacin de un intervalo de energa,
o lo que es lo mismo un intervalo de longitudes de onda, y se determina cules
longitudes de onda absorbe y cules no y en qu grado, se dice que se obtiene su
espectro de absorcin en dicha regin.
Al absorber la molcula energa proveniente de la radiacin que incide en ella,
se dice que pasa a un estado excitado; en consecuencia, debe disipar de algn
modo dicha energa para volver a su estado inicial o basal. Para disipar el excedente
de energa la molcula puede incrementar la amplitud de sus movimientos, haciendo
que los enlaces se alarguen, se flexionen o giren. Otras formas en que la molcula
78
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Espectroscopia en la regin del infrarrojo
reacciona a la absorcin de energa pueden dar como resultado un cambio en la
forma y tamao de su nube de electrones, e incluso la prdida o aceptacin de
electrones, la emisin de fotones, etctera.
ESPECTROSCOPIA IR DE MOLCULAS ORGNICAS
La regin de infrarrojo (IR) de espectro electromagntico cubre el intervalo que
queda justo por debajo del visible (7.8 x 10~
5
cm) hasta aproximadamente
10~
2
cm, pero slo la porcin central, que va de 2.5 x 10"
3
cm hasta los 2.5 x
10 ^ cm, se utiliza para identificar y cuantificar compuestos orgnicos, inorgnicos
u organometlicos.
Por conveniencia, las longitudes de ondas en la regin del IR suelen expresarse
en micrmetros: 1 |um = 10 ~
3
cm, y las frecuencias en funcin del nmero de onda
(v en cm"
1
), que es simplemente el recproco de la longitud de onda expresada en
centmetros.
La energa de que normalmente dispone una molcula provoca que los tomos
que la forman oscilen y vibren y que los enlaces que los unen se estiren y flexionen.
Todos estos movimientos combinados dan como resultado varios tipos de mo-
vimientos relativos, algunos de los cuales son los abajo expuestos:
Alargamiento Alargamiento Flexin Flexin fuera
simtrico asimtrico en el plano del plano
Figura 10.1 Algunos de los movimientos ms comunes que provoca la radiacin
infrarroja en una molcula tetradrica.
Una molcula efecta cada uno de estos movimientos a frecuencias especficas
y que corresponden a niveles que le son accesibles. Los enlaces interatmicos
suelen representarse como si tuvieran una longitud fija, pero la verdad es que los
valores dados son en realidad un promedio porque los enlaces se encuentran en
79
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
continuo movimiento, ya sea que se estiren y flexionen, se alarguen o contraigan.
Por ejemplo, un enlace C-H tpico que mide como promedio 1.10 oscilar a una
frecuencia especfica. Un enlace en particular de una molcula absorber energa
de la radiacin electromagntica incidente si las frecuencias de sta y de la
vibracin son iguales.
En otras palabras, cada frecuencia de la luz absorbida por la molcula
corresponde a la vibracin de un enlace especifico; as, puede verse en su espectro
IR qu tipo de vibraciones moleculares presenta una muestra en particular. Estas
frecuencias a las que ocurre un determinado movimiento de cierta agrupacin
particular de tomos en una molcula han sido perfectamente determinadas y
tabuladas.
INTERPRETACIN DE UN ESPECTRO INFRARROJO
La interpretacin completa de un espectro infrarrojo es difcil, en virtud de que la
mayora de las molculas orgnicas estn formadas por gran cantidad de tomos,
cuyos movimientos relativos y combinados dan origen a cientos de seales en su
espectro IR (estiramientos, flexiones, etc.). Esta complejidad resulta valiosa porque
el espectro de cada sustancia sirve como huella digital inconfundible de un
compuesto especifico. Por tal motivo, la regin del infrarrojo que queda por debajo
de los 1800 cnr
1
se denomina regin de las huellas dactilares.
Para la determinacin de estructuras, la gran cantidad de absorciones que suelen
presentarse en la mayora de los espectros hace difcil la interpretacin correcta.
Sin embargo, no es necesaria la interpretacin completa de un espectro IR para
obtener informacin valiosa de los grupos funcionales presentes, la posible
estructura de la molcula o la pureza de la misma. En la tabla 10.2 se muestran las
zonas donde se localizan las absorciones de los grupos funcionales ms comunes
en el IR, y en el anexo A de espectros IR se puede observar la mayora de las
seales a que hacemos referencia en dicha tabla.
Al analizar un espectro IR es conveniente considerar las zonas en que aparecen
las seales principales (Fig. 10.2), ya que ello nos orientar sobre la posible
identidad del compuesto.
80
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Espectroscopia en la regin del infrarrojo
Enlaces con
hidrgeno
Triples enlaces Dobles enlaces Regin de las flexiones
Enlaces
simples
Ncleos de
masa
moderada
Enlaces
simples
Ncleos
pesados
4000 2700 2000 1600
frecuencia (v, en cm~
1
)
1000 300
Figura 10.2 Esquema de las distintas regiones en que se puede dividir un espectro
infrarrojo.
TABLA 10.2 ABSORCIONES EN LA REGIN DEL IR DE LOS
GRUPOS FUNCIONALES ORGNICOS MS COMUNES
(CONSLTENSE LOS ESPECTROS IR DEL ANEXO A)
Grupo funcional
Alcanos y grupos alquilos
CH
C H (aldehdico)
Alquenos
C=C-H
C=C-
Alquinos
C=C-H
C=C-
Compuestos aromticos
CH
C=C-(aromtico)
Posicin de la banda
v/(cirr
1
)
2850-2960
1350-1470
2720
3020-3080,
675-1000 (f)
1640-1680
3300
2100-2260
610-700 (f)
3000-3100
675-870
1500-1600
Intensidad de la banda
(u. a.)
Media a alta
Media
Pequea y aguda
Media
Media
Media
Alta
Media
Pequea
Media
Media
Alta
81
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
Grupo funcional
Halogenuros de alquilo
CCI
CBr
Cl
Alcoholes, fenoles
O H (monmero)
0 H (puentes de hidrgeno)
CO
teres, Ac. carboxlicos,
esteres, amidas
CO
Aminas
NH
CN
Compuestos carboxlicos;
aldehidos, cetonas, cidos
carboxlicos y sus derivados
C=O
cidos carboxlicos
OH
Nitritos
CN
Nitro
NO
2
Posicin de la banda
(cm-
1
)
750
650
500
3610-3640
3200-3600
1050-1150
1080-1300
3300-3500
1180-1360
1690-1760
3500-3100
2210-2260
1540-1560
1345-1385
Intensidad de la banda
(u. a.)
Media
Media
Media
Alta y aguda
Alta y ancha
Media
Media
Media
Media
Alta
Alta y muy ancha
Media
Alta
82
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Espectroscopia en la regin del infrarrojo
Grupo funcional
Compuestos sulfo
C=S
S=Ode
Sulfxidos
Sulfonas
Sulfitos
Cloruros de sulfonilo
Sulfonamidas
cidos sulfnicos
Enlaces a hidrgeno
Si-H
Ge-H
P-H
As-H
S-H
Se-H
F-H
Cl-H
Br-I
I-H
Otros grupos
O-NO2 (nitratos)
O-NO (nitritos)
C-NO (comp. nitrosos)
N=N (Diazo)
N=C=N (diimidas)
- N
3
(azidas)
C=N
S-0
P-0
Se-0
B-O
B-F
N-F
Br-Br
Posicin de la banda
(cm-
1
)
1050-1200
1030-1070
1140-1160
1300-1350
1150-1230
1350-1430
1185-1165
1340-1370
1140-1180
1150-1210
1030-1060
650
2150
2100
2300
2200
2600
2300
4100
3000
2650
2300
1600-1650
1650-1680
1500-1600
1575-1630
2130-1155
1650
500-600
500-600
400-450
600-650
1400
1070
800
Intensidad de la banda
(u. a.)
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Media
Baja
Baja
Baja
Media
Media
Baja
83
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
SEALES CARACTERSTICAS DE LOS PRINCIPALES GRUPOS
FUNCIONALES
Para aclarar cualquier duda, consltense los espectros referidos en el anexo A de
espectros IR.
a) Alanos (Espectro IR-1):
Su espectro se caracteriza por presentar seales agudas e intensas en dos
regiones principales: 2850-2960 cnr
1
, asignadas a las vibraciones de los
enlaces C-H; y 1350-1470 cnr
1
, asignadas a las vibraciones de los grupos
metilo.
b) Alquenos (Espectro IR-2):
Su espectro se caracteriza por presentar seales agudas e intensas en tres
regiones principales: 3020 a 3080 cnr
1
, asignadas a vibraciones de los
enlaces C-H; 1640 a 1680 cnr
1
, asignadas a vibraciones del grupo C=C; y
650 a 1000 cnr
1
, asignadas a las flexiones del alqueno. Debemos mencionar
que cuando existe un doble enlace en un extremo de la cadena, se presentan
seales a 720 y 1465 cnr
1
correspondientes a vibraciones del grupo
metileno.
c) Alquinos
Su espectro se caracteriza por presentar seales agudas e intensas en tres
regiones principales: 3300 cm-1, asignadas a vibraciones de los enlaces
C-H; una seal pequea debida al triple enlace, entre 2100 y 2260 cnr
1
; y
finalmente flexiones de la cadena en la regin de 610 a 700 cnr
1
.
d) Compuestos aromticos (Espectro IR-4):
Su espectro suele ser muy rico en seales muy agudas en tres regiones
principales: 3000 a 3100 cnr
1
, asignadas a vibraciones de los enlaces C-H;
1500 a 1600, debido a los dobles enlaces conjugados; y finalmente una
serie de seales agudas y de intensidad media entre 675 y 870 cnr
1
debidas
a las flexiones del anillo aromtico.
Para el caso particular de los derivados del benceno se puede saber si se
trata de un compuesto mono, di, tri o poli-sustituido analizando las pequeas
bandas que aparecen en el intervalo de los 1670 a 2000 cnr
1
.
e) Alcoholes (Espectro IR-5):
La seal del grupo funcional O-H de los alcoholes es fcil de distinguir en
el espectro IR ya que usualmente es ancha e intensa, de 3300 a 3600 cnr
1
.
84
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Espectroscopia en la regin del infrarrojo
Al mismo tiempo, hay que observar una banda en el intervalo de 1050 a
1150 cnr
1
, que se debe a la vibracin C-O.
f) Aminas (Espectro IR-7):
El grupo funcional N-H de las aminas se distingue por una absorcin
caracterstica en el intervalo de 3300 a 3500 cnr
1
, mucho ms aguda y
menos intensa que la de los alcoholes, y por una seal en 1180 - 1360 cnr
1
asignada a la vibracin del enlace C-N.
g) teres (Espectro IR-8):
Se caracterizan principalmente por una seal de intensidad media cerca de
los 1100 cnr
1
atribuida al enlace C-O.
h) Cetonas (Espectros IR-9 e IR-10)
El espectro IR de las cetonas se caracteriza por la seal que origina su
grupo funcional C=O y aparece en el intervalo de 1690 a 1760 cnr
1
. Adems,
tiene que aparecer una seal en el intervalo de 1050 a 1150 cnr
1
, que se
debe a la vibracin C-O.
i) Aldehidos (Espectro IR-11):
Deben aparecer las mismas seales que se observan para las cetonas; sin
embargo, se observa adems una tercera banda cerca de los 2720 cnr
1
que
se atribuye al hidrgeno aldehdico.
j) cidos carboxlicos (Espectro IR-12):
El espectro IR de los cidos carboxlicos se caracteriza por tres seales
principales: la mayor es una seal ancha e intensa que comnmente se observa
superpuesta a las seales C-H (3000 cnr
1
); asignada a la vibracin OH,
aparece en el intervalo de 3100 a 3500 cnr
1
. La segunda seal es aguda e
intensa y se atribuye al grupo C=O; aparece en el intervalo 1690 a 1760 cnr
1
.
Por ltimo, se observa una seal en el intervalo de los 1080-1300 cnr
1
que
se atribuye al enlace C-O.
k) Derivados de cidos carboxlicos: amidas, ster, etc. (Espectros IR-13 a
IR-16):
Sus espectros se caracterizan por las seales del grupo carboxilo (1690 a
1760 cnr
1
) y del enlace C-O (1080-1300 cnr
1
), pero sin la seal del OH
del cido carboxlico. En su lugar aparecern vibraciones y flexiones del
tipo C-O, C-N, C-X (X = halgeno), N-H, etc., ya incluidas en la tabla
10.2.
85
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
1) Nitrilos (Espectro IR-17):
Su espectro se caracteriza por una seal pequea pero aguda en los 2210 a
2260 cnr
1
debida al triple enlace carbono-nitrgeno.
EQUIPO DE LABORATORIO
2 vasos de precipitado de 25 mi
2 tubos de ensaye de 5 mi con tapn
1 esptula
1 mortero de gata (por grupo)
1 pastilladora para muestras de IR
1 prensa (por grupo)
Celda de NaCl para espectroscopia IR de lquidos (ver Fig. C 8 en el anexo C)
APARATO DE FT-IR
SUSTANCIAS (las ms posibles entre las siguientes):
Pentano o hexano
Ciclohexeno
Etanol, propanol, terbutanol o butanol
Propanaldehdo o butiraldehdo
Acetona o 2-butanona
cido actico, propinico o butrico
ter etlico
Formamida
N,N-dimetilformamida
Acetato de isoamilo
Urea
Anilina o fenol
Tolueno o xileno
Muestra problema 1, MP1
Muestra problema 2, MP2
Bromuro de potasio seco, KBr
EXPERIMENTACIN
Para la realizacin de esta prctica recomendamos que previamente se tenga una
seccin de principios bsicos de espectroscopia en la regin del IR y se analicen
ejemplos de espectros de las principales familias orgnicas.
86
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Espectroscopia en la regin del infrarrojo
1. Asigne a cada eqipo alguna de las muestras problema, MP1* o MP2*, y reparta
segn el nmero de equipos que formen el grupo, las sustancias siguientes:
a) pentano o hexano
b) ciclohexeno
c) etanol, propanol, tert-butanol o butanol
d) propanaldehdo o butiraldehdo
e) acetona o 2-butanona
f) cido butrico
g) ter etlico
h) anilina
i) tolueno o xileno.
j) Muestra problema 1, MP1 y Muestra problema 2, MP2.
2. Que cada alumno obtenga el espectro de las muestras en pastilla de bromuro
de potasio o bien en celdas de cloruro de sodio, segn se trate de muestras
slidas o lquidas respectivamente (Fig. C 8 del anexo C).
3. Que cada equipo localice en los espectros obtenidos las seales
caractersticas de la sustancia que se le asign y la compare con lo obtenido
por los otros equipos.
4. Finalmente, es conveniente realizar una sesin audiovisual para discutir las
similitudes y diferencias observadas entre los espectros de las sustancias
analizadas y concluir sobre la identidad de las sustancias MP1 y MP2.
CUESTIONARIO
1. Qu es la espectroscopia?
2. En qu intervalo de frecuencias se localiza la regin del infrarrojo que
sirve para analizar compuestos orgnicos?
3. Qu es el nmero de onda?En qu unidades se expresa?
4. Qu es un espectro?
5. Qu efecto tiene la radiacin infrarroja en las molculas?
6. La espectroscopia en el IR permite identificar plenamente la identidad de
cualquier sustancia? Por qu?
7. Cmo distinguira usted si un espectro corresponde a
a) un alcohol y un ter?
b) un cido carboxlico y un ster?
c) un aldehido o una cetona?
d) un compuesto aromtico de uno que no lo es?
* MP1 y MP2 pueden ser sustancias cuya identidad conozca el profesor o bien muestras de
los compuestos obtenidos durante el curso.
87
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
BIBLIOGRAFA
1. R. T. Morrison y R. N. Boyd. 1990. Qumica orgnica. 5
a
ed. Mxico,
Addison-Wesley Iberoamrica.
2. J. R. Dyer. 1965. Applications ofAbsortion Spectroscopy ofOrganic Com-
pounds. USA, Prentice Hall.
3. D. H. Williams e I. Fleming. 1986. Spectroscopic Methods in Organic
Chemistry. 4
a
ed. UK, McGraw-Hill.
4. R. M. Silverstein y R X. Webster. 1998. Spectrometric Identification of
Organic Compounds. 6
a
ed. New York, John Wiley and Sons.
5. Aldrich Chemical. 1997.The Aldrich Library of FT-IR Spectra. 2
a
ed.
Milwaukee,WI,USA.
88
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
ANEXOS
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Anexo A
ESPECTROS INFRARROJOS
Butano
4AQ
Nmero de onda
Espectro IR-1: de butano
Nmero de onda
Espectro IR-2: de 1-buteno
Nmero de onda
Espectro IR-3: de bromobutano
91
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
IOO
Benceno
ooo 5*5 5o 40O0 9OO0
2000
Nmero de onda
Espectro IR-4: de benceno
9OO
Butano!
2000 fOOO
Nmero de onda
Espectro IR-5: de butanol
450
I-Butonotiol
4000 3OOO 2000 fOOO
Nmero de onda
Espectro IR-6: de butanodiol
4S0
92
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Anexo A: Espectros infrarrojos
4000 ooo
Nmero de onda
1000
Espectro IR-7: de butilamina
100
ter etlico
4OOO 3000 20O0 1000
Nmero de onda
Espectro IR-8: de ter etlico
490
100
Acetona
4000 StOOO
Nmero de onda
Espectro IR-9: de acetona
450
93
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
100
2-Bu+enona
4000 3000 tooo
Nmero de onda
Espectro IR-10: de 2-butanona
Butiroldehido
Nmero de onda
Espectro IR-11: de butanal
450
IOO
Acido buTlrico
2000 1000
Nmero de onda
450
Espectro IR-12: de cido butanoico
94
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Anexo A: Espectros infrarrojos
100
Cloruro dttHJtonoilo
4OOO 3OQ0
Nmero de onda
Espectro IR-13: de cloruro de butanoilo
490
00
Butiroto de metilo
4OOO
2000 1000
Nmero de onda
Espectro IR-14: de butirato de metilo
eoo
6Q0 430
BuTanomkta
Nmero de onda
Espectro IR-15: de butanamida
450
95
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
Anhdrido butrico
100
C=>
tooo woo
Nmero de onda
Espectro IR-16: de anhdrido butrico
Butironitrilo
100 r-r
Nmero de onda
Espectro IR-17: de butironitrilo
moneno
JOO
40O0 3000 ^000
Nmero de onda
Espectro IR-18: de limoneno
96
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Anexo A: Espectros infrarrojos
IOO
Cofeina
Espectro IR-19: de cafena
IOO
Acido ocetilsolicrijco
4OOO 3OOO
Nmero de onda
Espectro IR-20: de cido acetil saliclico
IOO
Cloruro de tertbutilo
Nmero de onda
Espectro IR-21: de cloruro de tert-butilo
97
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Anexo B
MATERIAL DE VIDRIO Y EQUIPO DE
LABORATORIO
(a)
(c)
(b)
Figura B 1 a) Bao caliente o "bao Mara ", b) bomba de vaco porttil c) cuba
hidroneumatica, d) gradilla, e) tringulo de porcelana, j) malla de asbesto y
g) mecheros de Bunsen.
99
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
Figura B 2 a) Soporte universal, b) cucharilla de ignicin, c) esptulas, d) escobillas,
e) tripi de hierro, f) guantes de asbesto, g) guantes resistentes a cidos, h) jarra de
revelado de placas cromatogrficas, i) desecador, j) desecador con adaptador para vaco.
100
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Anexo B: Material de vidrio y equipo de laboratorio
(a) (b) (c)
(f)
(h)
(i)
Figura B 3 o) Picetas, b) goteros, c) embudos cnicos, d) cpsula de porcelana, e) crisol,
j) mortero con pistilo, g) cristalizador, h) caja de Petri, i) vidrio de reloj.
101
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
(d)
Figura B 4 a) Pinzas con nuez, b) pinzas de tres dedos con nuez, c) pinzas dobles para
bureta, d) pinzas para crisol, e) pinzas para cpsula de porcelana, j) pinzas para tubo de
ensaye, g) pinzas revestidas para vaso de precipitado.
102
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Anexo B: Material de vidrio y equipo de laboratorio
\J
Figura B 5 a) Vasos de precipitado, b) tubo de ensaye, c) probeta graduada,
d) picnmetro, e) dispositivo de sublimacin o
t(
dedofro",j) tubos para desecador,
g) adaptador para termmetro, h) tubo de Thiele, i) embudo Bchner de porcelana,
j) embudos Bchner con disco poroso.
103
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
(b) (c)
Figura Bl a) Termmetro, b) bureta, c) pipeta graduada, d) pipeta volumtrica,
e) micropipeta automtica.
^
^
(a) (b) (c)
(e) (f)
Figura B 7 aj Columna para cromatografa, b) columna Vigreaux, c) columna Snyder,
d) columna de bulbos Kugeirohr, e) condensador Liebing con camisa interna,
f) condensador Allihn o de rosario, g) condensador de Graham o de serpentn,
h) condensador Friedrichs.
104
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Anexo B: Material de vidrio y equipo de laboratorio
(g)
Figura B 8 a) Adaptador para destilacin Claisen, b) conector en "Y" para
destilacin, c) adaptador en "Y" para destilacin y con adaptador para termmetro,
d) adaptador para destilacin curvo de 105, e) adaptador curvo (105) para
destilacin a vaco, j) adaptador recto para destilacin a vaco, g) junta Dean Stark.
105
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
Figura B 9 a) Embudo de separacin, b) matraz aforado, c) matraz Erlenmeyer,
d) matraz Kitazato, e) matraces redondos con fondo plano, f) matraces redondos,
g) matraz redondo de cuello largo sin junta esmerilada, h) matraz de tres bocas de
250 mi, i) matraz de tres bocas de 500 mi.
106
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Anexo B: Material de vidrio y equipo de laboratorio
(a) (b) (c) (d) (e)
Q
M
Tsf
n
cu
/
(f) (g) (h) (i) (j) (k) (1) (m)
Figura B 10 Equipo bsico de micromtodos: a) Matraz Erlenmeyer, b) viales,
c) matraz redondo, d) junta Ciis en, e) adaptador para destilacin a vaco,
f) condensador de aire para reflujo, g) agitador magntico, h) jeringa, i) cristalizador
de Craig,j) tubo colector de muestras de cromatografa de gases, k) condensador de
aire, 1) destilador de Hickman simple, m) destilador de Hickman con adaptacin
lateral, n) condensadores, ) tubo de seguridad para burbujeo de gases,
o) tubo conectorpara desecador.
107
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Anexo C
MONTAJE DE DISPOSITIVOS
EXPERIMENTALES
Figura C 1 Sistema de destilacin simple.
Figura C 2 Sistema de destilacin fraccionada con columna Vireaux; sta puede
sustituirse con un condensador Liebing empacado con fibra de vidrio.
109
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
Figura C 3 Sistema de destilacin simple con adicin lateral en matraz de tres bocas.
Figura C 4 Sistema de destilacin simple en matraz de dos bocas, con llave par a flujo
de atmsfera inerte y conexin a vaco.
110
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Anexo C: Montaje de dispositivos experimentales
Figura C 5 Sistema de destilacin por arrastre de vapor en matraz de tres bocas.
Figura C 6 Filtrado simple en papel y b) filtrado a vaco en embudo Buchnery
matraz Kitazato.
111
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
-coa:
(a) (b) (c)
Figura C 7 Sistema de reflujo simple, b) sistema de reflujo con desecador, c) sistema
de reflujo con desecador y embudo de adicin en matraz de tres bocas.
Soporte
frontal
Cristales
de NaCI
Guia de
ventana
Soporte
posterior
Figura C 8 Portaceldas de NaClpara espectroscopia IR con muestras lquidas.
112
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Anexo C: Montaje de dispositivos experimentales
Ocular
Ajuste del
prisma de
Amici
Recirculacin
de agua
Prisma
porta-muestra
Lmpara
Termmetro
Tornillo de
ajuste
burdo
Tornillo de
ajuste fino
Brazo
extensor de
la lmpara
Interruptor
para
lectura
Figura C 9 Refractmetro deAbbe.
113
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
Por abajo
(b)
Figura C 10 Lecturas en el refractmetro deAbbe: a) Ajuste por arriba, b) ajuste por
abajo, c) ajuste ideal, d) lectura del valor del ndice de refraccin.
Control de
^voltaje
Interruptor
Lmpara
Ocular
Muestra
Placa
calefactora
Figura C 11 Aparato de Fisher-Johns para medir el punto de fusin.
114
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Anexo D
SUSTANCIAS PELIGROSAS
SUSTANCIAS PELIGROSAS MS COMUNES
Sustancia Riesgo Mtodo de eliminacin
2-aminofenol:
C
6
H
4
(OH)NH
2
Sales de
aminobenceno
y sales de anilina:
C
6
H
5
NH
2
HC
Compuestos de bario
Bromo, Br
2
Cromatos y
dicromatos:
K
2
Cr0
4
, Na
2
Cr
2
O
7>
etc.
Cianuros:
KCN, NaCN, etc.
Ocasiona dermatitis y es
txico si se ingiere
Polvos txicos
Todas las sales solubles
de bario deben
considerarse muy txicas
Causa quemaduras graves
Es muy corrosivo e irritante
de la piel y el sistema
respiratorio
El polvo irrita los ojos y el
sistema respiratorio
La exposicin prolongada
de la piel puede ocasionar
ulceras. Al contacto con
materia orgnica
(combustible) puede
provocar incendios
Txicos por ingestin
Txicos por inhalacin del
gas HCN (producido por la
acidificacin de las sales).
Se absorben por la piel
Diluya en gran cantidad de agua
y deschelo
Al usarlos evite el contacto con
los ojos y la piel
Puede diluirse con abundante
agua y desecharse
Diluya y elimine con abundante
agua. Los sulfates pueden
eliminarse en la forma normal
en que se eliminan los slidos
Evite respirar sus vapores;
trate con disolucin de
carbonato de sdico, mezcle
y elimine con abundante agua
Diluya con abundante agua
hasta formar una suspensin
y elimnela
Coloque cuidadosamente los
slidos en un recipiente,
disuelva en agua y neutralice
con solucin de clorato de sodio,
dejando reposar un da, al cabo
del cual pueden eliminarse
115
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
Sustancia
Fluoruros:
KF
Formalina
(solucin de metal)
cido frmico:
HCOOH
Fenol:
C
6
H
5
OH
Metales de alcalinos:
Li, Na, K, etc.
Cloruro de aluminio:
AICI3
Riesgo
Txicos si se ingieren, su
polvo irrita la piel, los ojos
y el sistema respiratorio
Txico por inhalacin 0 al
Tragar. Irrita la piel, los ojos
y el aparato respiratorio
Causa quemaduras e irrita
a piel, los ojos y el sistema
respiratorio
Txico por ingestin, se
absorbe por la piel.
Ocasiona quemaduras y
dao grave en los ojos
Al contacto con el agua
reaccionan violentamente
produciendo hidrgeno,
que puede incendiarse
violentamente
Reacciona violentamente
con el agua, produciendo
HCI gaseoso que ocasiona
desde irritacin hasta
quemaduras graves de la
piel, los ojos y el sistema
respiratorio
Mtodo de eliminacin
Evite el contacto y diluya y
elimine con abundante agua
Aljelo de toda fuente posible de
Ignicin. Evite todo contacto,
diluya y elimnelo con agua.
Ventile bien la zona afectada
y trtela con carbonato de sodio
Lave bien con abundante agua y
trate con carbonato de sodio
Evite todo contacto,
mezcle con arena y qumelo
en lugar seguro
Na: neutralice lentamente con
pequeas cantidades de etanol
en una campana de extraccin
y lejos de cualquier flama.
Al cesar la reaccin, se diluye
con agua y se elimina.
K: es ms reactivo. Por ello debe
primero dispersarse en glicerol,
para que reaccione lentamente.
Ya disuelto se agrega etanol y al
terminar toda reaccin, se diluye
y elimina con abundante agua
Mezcle con arena, diluya
pequeas cantidades de la
mezcla en un gran volumen
de agua y elimnelo
116
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Anexo D: Sustancias peligrosas
Sustancia
xidos y perxidos:
HA
cido clorhdrico:
HCI
cido ntrico
HNO
3
cido sulfrico:
H
2
SO
4
Hidrxido de amonio:
NH
4
OH
Oxalatos
Agua regia: consiste
en 4 partes de HCI
(conc
+ 1 parte de HNO
3
Riesgo
Los xidos y perxidos de
metales alcalinos reaccionan
vigorosamente con el agua,
formando soluciones
alcalinas y un aerosol del
hidrxido metlico en el aire
Vapor nocivo, causa
quemaduras graves en piel,
ojos y sistema respiratorio
Causa quemaduras e
irritacin. Agente oxidante
muy fuerte que puede
producir xidos de nitrgeno
muy txicos
Causa quemaduras graves y
reacciona vigorosamente con
el agua
Causa quemaduras graves;
es muy corrosivo e irritante
de la piel y el sistema
respiratorio
Txicos
Los riesgos de los cidos,
ms la posibilidad de
formacin de vapor de
cloruro de nitrosilio
Mtodo de eliminacin
Se lava y desecha con
abundante agua
Evite todo contacto e
inhalacin de sus vapores.
Diluya con grandes
cantidades de agua.
Neutralice con carbonato
sdico y lave con abundante
agua
Evite el contacto y la
inhalacin. Diluya con
abundante agua y
neutralice con carbonato
sdico
Evite el contacto 0 la
inhalacin. Diluya con
abundante agua y
espolvoree carbonato
sdico sobre cualquier
derrame
Evite el contacto y la
inhalacin. Diluya con
abundante agua
Diluya con agua y elimine
Trtela como al HCI
(conc}
117
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Anexo D: Sustancias peligrosas
REPORTE
LABORATORIO DE QUMICA ORGNICA I
Alumno: Equipo:
Prctica No:
Fecha:
Nombre:
Objetivos:
1. Reaccin o reacciones:
2. Introduccin:
119
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
3. Sustancias peligrosas: Precauciones recomendadas:
4. Experimentacin y observaciones:
120
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Anexo D: Sustancias peligrosas
5. Resultados:
Peso o volumen
del o los productos:
Frmula:
Estado:
P.M. (g/mol):
Estructura:
Color:
Otros:
Otras pruebas
PfoPeb(C):
Dato bibliogrfico:
Datos espectroscopicos:
Clculos:
121
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
6. Discusin:
7. Conclusiones:
Notas y sugerencias:
8.-Bibliografa:
Nota: Si requiere ms espacio, anexe las hojas necesarias.
122
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Manual de prcticas de qumica orgnica I
se termin de imprimir en noviembre del 2002
en la Seccin de Impresiones y Diseo Grfico de la UAM-I.
La edicin consta de 500 ejemplares.
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
Aunque el avance tecnolgico en computacin ha permitido resolver y predecir eventos cada vez
ms complejos de la naturaleza, ciencias como la qumica seguirn siendo bsicamente
experimentales. Sin embargo, parece ser que la importancia de la experimentacin como fuente
directa de conocimientos est siendo olvidada en los niveles que preceden a la universidad. Esto ha
provocado en ocasiones que los cursos de qumica en este nivel sean un primer encuentro
desagradable y complejo para muchos de nuestros estudiantes, no solo con la qumica sino con
otras ciencias. El presente Manual de Prcticas de Qumica Orgnica /pretende ser un encuentro
conciliador, formativo y, en la medida de lo posible, una segunda oportunidad que ratifique la
vocacin de aquellos que contemplaron la qumica como su posible proyecto de vida. Hemos incluido
aqu el material y equipo de laboratorio indispensable para trabajar en la escala tradicional o
microescala, las operaciones bsicas de extraccin y purificacin y las tcnicas suficientes de
caracterizacin, que van desde sencillas pruebas a la gota hasta la espectroscopia, que para este
manual se limita a la espectroscopia en la regin del infrarrojo.
ISBN:170-31-0052-X
7 8 9 7 0 3 9 100521
DERECHOS RESERVADOS 2004, Universidad Autnoma Metropolitana (Mxico). Prohibida la reproduccin de esta obra as como la distribucin y venta fuera del mbito de la UAM. E-libro Bibliomedia Bibliomedia@mail.com
You might also like
- Plan de Contingencias FormatoDocument16 pagesPlan de Contingencias FormatoAndrea JimenezNo ratings yet
- Primeros AuxiliosDocument29 pagesPrimeros AuxiliosCARLOSNo ratings yet
- Primeros Auxilios - QuemadurasDocument10 pagesPrimeros Auxilios - QuemadurasEVELYNNo ratings yet
- Pro - Pro.006 - Relleno y CompactacionDocument13 pagesPro - Pro.006 - Relleno y CompactacionEnma Glaribel Pezo EscalanteNo ratings yet
- Agrupación PON'sDocument17 pagesAgrupación PON'sLady Maritza Reina UribeNo ratings yet
- Msds Sigmacover 350 Base LDocument20 pagesMsds Sigmacover 350 Base LTania TixeNo ratings yet
- FT-SGI-GRUPECSAC-001 (Inspeccion de Botiquín de Primeros Auxilios en Planta)Document1 pageFT-SGI-GRUPECSAC-001 (Inspeccion de Botiquín de Primeros Auxilios en Planta)Andre MestasNo ratings yet
- PE-MACO-FERT-P21 Procedimiento para Instalación de Cuellos MuertosDocument19 pagesPE-MACO-FERT-P21 Procedimiento para Instalación de Cuellos MuertosJoao Galarza EleraNo ratings yet
- Av 7 CamillajeDocument14 pagesAv 7 CamillajeStivy Sarmiento Bolaño75% (4)
- Especificaciones Técnicas Puerto RicoDocument63 pagesEspecificaciones Técnicas Puerto Ricovladimir sauneNo ratings yet
- Plan de Atencion A EmergenciaDocument16 pagesPlan de Atencion A Emergenciamartin estradaNo ratings yet
- SDS Aceite de Motor Fuera de Borda Tc-w3 LubrimaticDocument4 pagesSDS Aceite de Motor Fuera de Borda Tc-w3 LubrimaticJulio PerezNo ratings yet
- Ficha de Datos de Seguridad de La Vinaza M - 3kDocument6 pagesFicha de Datos de Seguridad de La Vinaza M - 3klucenyagroNo ratings yet
- Msds Bismutato de Sodio WinklerDocument5 pagesMsds Bismutato de Sodio WinklerPatrícia HashimotoNo ratings yet
- Lección # 1 Sobre Primeros AuxiliosDocument13 pagesLección # 1 Sobre Primeros AuxiliosLuis Guzman100% (1)
- Los Peligros Dentro Del HogarDocument6 pagesLos Peligros Dentro Del HogarporfirioNo ratings yet
- Sanidad en Campaña Tarea 3Document8 pagesSanidad en Campaña Tarea 3Fernando SoteloNo ratings yet
- Semana A01Document17 pagesSemana A01Elizabeth Palomino de la CruzNo ratings yet
- Primeros AuxiliosDocument15 pagesPrimeros AuxiliosBuenaventura Jose Huamani TalaveranoNo ratings yet
- Procedimiento de Caso de Emergencia en Trabajo CalienteDocument2 pagesProcedimiento de Caso de Emergencia en Trabajo CalientelauraNo ratings yet
- Temas de SeguridadDocument31 pagesTemas de SeguridadGerman Cruz MallquiNo ratings yet
- Primeros Auxilios Nivel IDocument2 pagesPrimeros Auxilios Nivel ILucero Guillén BuñuelosNo ratings yet
- Plan de Seguridad ContingenciaDocument25 pagesPlan de Seguridad ContingenciaMarcelo Miranda SandovalNo ratings yet
- UT 2 Valoración Inicial de La Asistencia en EmergenciasDocument10 pagesUT 2 Valoración Inicial de La Asistencia en EmergenciasDiego DelgadoNo ratings yet
- Plan de Contingencia ColegioDocument33 pagesPlan de Contingencia ColegioGutiérrez Mendoza D GiselNo ratings yet
- Beatriz PeñaDocument6 pagesBeatriz PeñaBeatriz PeñaNo ratings yet
- CI 2021 Generalidades de Primeros Auxilios y RCPDocument15 pagesCI 2021 Generalidades de Primeros Auxilios y RCPCarla PatriciaNo ratings yet
- Clase 17 y 18 de Julio Primeros AuxiliosDocument54 pagesClase 17 y 18 de Julio Primeros AuxiliosHector HuisaNo ratings yet
- Dialogos de Seguridad - Áreas de Mantenimiento - Operaciones - EstabloDocument100 pagesDialogos de Seguridad - Áreas de Mantenimiento - Operaciones - Establoines C. TNo ratings yet
- Rep 8Document9 pagesRep 8MONSERRATH CARRETERO URIBENo ratings yet