Professional Documents
Culture Documents
Makalah Asam Asetat
Uploaded by
Widya FiqraOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Makalah Asam Asetat
Uploaded by
Widya FiqraCopyright:
Available Formats
1
PENDAHULUAN
I.1. Sejarah Proses
Cuka telah dikenal manusia sejak dahulu kala. Dahulu kala cuka dihasilkan
oleh berbagai bakteri penghasil asam asetat, dan asam asetat merupakan hasil
samping dari pembuatan bir atau anggur.
Penggunaan asam asetat sebagai pereaksi kimia juga sudah dimulai sejak
lama. Pada abad ke-3 Sebelum Masehi, Filsuf Yunani kuno Theophrastos
menjelaskan bahwa cuka bereaksi dengan logam-logam membentuk berbagai zat
warna, misalnya timbal putih (timbal karbonat), dan verdigris , yaitu suatu zat hijau
campuran dari garam-garam tembaga dan mengandung tembaga (II) asetat. Bangsa
Romawi menghasilkan sapa , sebuah sirup yang amat manis, dengan mendidihkan
anggur yang sudah asam. Sapa mengandung timbal asetat, suatu zat manis yang
disebut juga gula timbal dan gula Saturnus. Akhirnya hal ini berlanjut kepada
peracunan dengan timbal yang dilakukan oleh para pejabat Romawi.
Pada abad ke-8, ilmuwan Persia Jabir Ibnu Hayyan menghasilkan asam asetat
pekat dari cuka melalui distilasi. Pada masa renaisans, asam asetat glasial dihasilkan
dari distilasi kering logam asetat. Pada abad ke-16 ahli alkimia Jerman Andreas
Libavius menjelaskan prosedur tersebut, dan membandingkan asam asetat glasial
yang dihasilkan terhadap cuka. Ternyata asam asetat glasial memiliki banyak
perbedaan sifat dengan larutan asam asetat dalam air, sehingga banyak ahli kimia
yang mempercayai bahwa keduanya sebenarnya adalah dua zat yang berbeda. Ahli
kimia Prancis Pierre Adet akhirnya membuktikan bahwa kedua zat ini sebenarnya
sama.
Pada 1847 kimiawan Jerman Hermann Kolbe mensintesis asam asetat dari zat
anorganik untuk pertama kalinya. Reaksi kimia yang dilakukan adalah klorinasi
karbon disulfida menjadi karbon tetraklorida, diikuti dengan pirolisis menjadi
tetrakloroetilena dan klorinasi dalam air menjadi asam trikloroasetat, dan akhirnya
reduksi melalui elektrolisis menjadi asam asetat.
Sejak 1910 kebanyakan asam asetat dihasilkan dari cairan piroligneous yang
diperoleh dari distilasi kayu. Cairan ini direaksikan dengan kalsium hidroksida
2
menghasilkan kalsium asetat yang kemudian diasamkan dengan asam sulfat
menghasilkan asam asetat.
Sekarang ini, asam asetat diproduksi baik secara sintetis maupun secara
fermentasi bakteri. Produksi asam asetat melalui fermentasi hanya mencapai sekitar
10% dari produksi dunia utamanya produksi cuka makanan. Aturan menetapkan
bahwa cuka yang digunakan dalam makanan harus berasal dari proses biologis
karena lebih aman bagi kesehatan.
Pembuatan asam asetat sintesis dalam skala industri lebih sering menggunakan
metode karbonilasi methanol. Ada dua macam proses pembuatan asam asetat dalam
pabrik yakni proses monsanto dan proses cativa. Proses monsanto menggunakan
katalis kompleks Rhodium (cis[Rh(CO)
2
I
2
]
), sedangkan proses cativa
menggunakan katalis iridium ([Ir(CO)
2
I
2
]
) yang didukung oleh ruthenium.
I.2. Spesifikasi Bahan Baku
I.2.1. Methanol
Metanol, juga dikenal sebagai metil alkohol, wood alcohol atau spiritus, adalah
senyawa kimia dengan rumus kimia CH
3
OH. Ia merupakan bentuk alkohol paling
sederhana. Pada "keadaan atmosfer" ia berbentuk cairan yang ringan, mudah
menguap, tidak berwarna, mudah terbakar, dan beracun dengan bau yang khas
(berbau lebih ringan daripada etanol). Metanol digunakan sebagai bahan baku
pembuatan asam asetat dengan metode karbonilasi methanol.
Metanol diproduksi secara alami oleh metabolisme anaerobik oleh bakteri.
Hasil proses tersebut adalah uap metanol (dalam jumlah kecil) di udara. Setelah
beberapa hari, uap metanol tersebut akan teroksidasi oleh oksigen dengan bantuan
sinar matahari menjadi karbon dioksida dan air.
Methanol
3
Nama IUPAC
Methanol
Nama lain
hydroxymethane
methyl alcohol
methyl hydrate
wood alcohol
carbinol
Sifat
Rumus molekul CH
3
OH
Massa molar 32.04 g/mol
Penampilan colorless liquid
Densitas 0.7918 g/cm, liquid
Titik leleh 97 C, -142.9 F (176 K)
Titik didih 64.7 C, 148.4 F (337.8 K)
Kelarutan dalam air Fully miscible
Keasaman (pK
a
) ~ 15.5
Viskositas 0.59 mPa s at 20 C
Momen dipol 1.69 D (gas)
Bahaya
Klasifikasi EU Flammable (F)
Toxic (T)
Titik nyala 11 C
I.2.2. Iodida
Peran iodida adalah hanya untuk mempromosikan konversi methanol menjadi
metil iodide:
MaOH + HI MeI + H
2
O
4
Setelah metil iodida telah terbentuk maka diteruskan ke reaktor katalis. Siklus
katalitik dimulai dengan penambahan oksidatif metil iodida ke dalam [Rh(CO)
2
I
2
]
-
sehingga terbentuk kompleks [MeRh(CO)I
3
]
-
I.2.3. Rhodium (cis[Rh(CO)
2
I
2
]
)
Rhodium (cis[Rh(CO)
2
I
2
]
) berperan sebagai katalis dalam proses
pembuatan asam asetat dalam skala industri. Katalis ini sangat aktif sehingga akan
memberikan reaksi dan distribusi produk yang baik. Struktur katalis kompleks
Rhodium (cis[Rh(CO)
2
I
2
]
)
dapat dilihat seperti gambar berikut:
I.2.4. Iridium ([Ir(CO)
2
I
2
]
)
Iridium ([Ir(CO)
2
I
2
]
) berperan sebagai katalis dalam proses pembuatan asam
asetat dalam skala industri.Penggunaan iridium memungkinkan penggunaan air lebih
sedikit dalam campuran reaksi. Struktur katalis kompleks Ir[(CO)
2
I
2]
dapat dilihat
seperti gambar berikut:
I.3. Spesifikasi Produk
Asam asetat yang jelas, cairan tak berwarna dengan rumus kimia C
2
H
4
O
2.
Memiliki titik leleh 62,06F (16.7C) dan mendidih pada 244,4F (118C), kerapatan
1,049g/mL pada 25
o
C dan flash point 39
0
C. Dalam konsentrasi tinggi,asam asetat
bersifat korosif, memiliki bau tajam dan dapat menyebabkan luka bakar pada kulit.
Atom hidrogen (H) pada gugus karboksil (COOH) dalam asam karboksilat
seperti asam asetat dapat dilepaskan sebagai ion H
+
(proton), sehingga memberikan
sifat asam. Asam asetat adalah asam lemah monoprotik dengan nilai pK
a
=4.8. Basa
5
konjugasinya adalah asetat (CH
3
COO
). Sebuah larutan 1.0 M asam asetat (kira-kira
sama dengan konsentrasi pada cuka rumah) memiliki pH sekitar 2.4.
Struktur kristal asam asetat menunjukkan bahwa molekul-molekul asam asetat
berpasangan membentuk dimer yang dihubungkan oleh ikatan hidrogen. Dimer juga
dapat dideteksi pada uap bersuhu 120C. Dimer juga terjadi pada larutan encer di
dalam pelarut tak-berikatan-hidrogen, dan kadang-kadang pada cairan asam asetat
murni Dimer dirusak dengan adanya pelarut berikatan hidrogen (misalnya air).
Entalpi disosiasi dimer tersebut diperkirakan 65.066.0 kJ/mol, entropi disosiasi
sekitar 154157 J mol
1
K
1
.
Asam asetat bersifat korosif terhadap banyak logam seperti besi, magnesium,
dan seng, membentuk gas hidrogen dan garam-garam asetat (disebut logam asetat).
Logam asetat juga dapat diperoleh dengan reaksi asam asetat dengan suatu basa.
Contohnya adalah soda kue (Natrium bikarbonat) bereaksi dengan cuka. Hampir
semua garam asetat larut dengan baik dalam air. Contoh reaksi pembentukan garam
asetat:
Mg(s) + 2 CH
3
COOH(aq) (CH
3
COO)
2
Mg(aq) + H
2
(g)
NaHCO
3
(s) + CH
3
COOH(aq) CH
3
COONa(aq) + CO
2
(g) + H
2
O(l)
Asam asetat mengalami reaksi-reaksi asam karboksilat, misalnya menghasilkan
garam asetat bila bereaksi dengan alkali, menghasilkan logam etanoat bila bereaksi
dengan logam, dan menghasilkan logam etanoat, air dan karbondioksida bila
bereaksi dengan garam karbonat atau bikarbonat. Reaksi organik yang paling
terkenal dari asam asetat adalah pembentukan etanol melalui reduksi, pembentukan
turunan asam karboksilat seperti asetil klorida atau anhidrida asetat melalui substitusi
nukleofilik.
Nama sistematis : Asam etanoat, Asam asetat
Nama alternatif : Asam metanakarboksilat
Asetil hidroksida : (AcOH)
Hidrogen asetat : (HAc) Asam cuka
Rumus molekul : CH3COOH
Massa molar : 60.05 g/mol
6
Densitas dan fase : 1.049 g cm
3
, cairan 1.266 g cm
3
, padatan
Titik lebur : 16.5 C (289.6 0.5 K) (61.6 F)
Titik didih : 118.1 C (391.2 0.6 K) (244.5 F)
Penampilan : Cairan tak berwarna atau kristal
Keasaman (pKa) : 4.76 pada 25C
I.4. Kegunaan Asam Asetat
Asam asetat digunakan sebagai pereaksi kimia untuk menghasilkan berbagai
senyawa kimia. Sebagian besar (40-45%) dari asam asetat dunia digunakan sebagai
bahan untuk memproduksi monomer vinil asetat (vinyl acetate monomer, VAM).
Selain itu asam asetat juga digunakan dalam produksi anhidrida asetat dan juga ester.
Penggunaan asam asetat lainnya, termasuk penggunaan dalam cuka relatif kecil.
7
RANCANGAN PROSES
II.1. Reaksi / mekanisme reaksi
Teknologi pembuatan asam asetat mungkin yang paling beragam dari
pembuatan semua bahan kimia organik industri. Ada beberapa teknik yang
digunakan dalam pembuatan asam asetat, diantaranya ialah; karbonilasi methanol,
sintesis gas metan, oksidasi asetaldehida, oksidasi etilena, oksidasi alkana, oksidatif
fermentasi, dan anaerob fermentasi. Karbonilisasi methanol merupakan teknik yang
umum digunakan dalam industri asam asetat dan menjadi teknik penghasil asam
asetat lebih dari 65% dari kapasitas global. Dari asam asetat yang diproduksi oleh
industri kimia, 75% diantaranya diproduksi melalui karbonilasi metanol. Sisanya
dihasilkan melalui metode-metode alternatif.
1. Karbonilisasi methanol
Kebanyakan asam asetat murni dihasilkan melalui karbonilasi. Dalam reaksi
ini, metanol dan karbon monoksida bereaksi menghasilkan asam asetat
CH
3
OH + CO CH
3
COOH
Proses ini melibatkan iodometana sebagai zat antara, dimana reaksi itu sendiri
terjadi dalam tiga tahap dengan katalis logam kompleks pada tahap kedua.
(1) CH
3
OH + HI CH
3
I + H
2
O
(2) CH
3
I + CO CH
3
COI
(3) CH
3
COI + H
2
O CH
3
COOH + HI
Ada dua macam proses pembuatan asam asetat dengan metode karbonilisasi
methanol yakni proses monsanto dan proses cativa. Proses monsanto menggunakan
katalis kompleks Rhodium (cis[Rh(CO)
2
I
2
]
), sedangkan proses cativa
menggunakan katalis iridium ([Ir(CO)
2
I
2
]
) yang didukung oleh ruthenium.
II.2.Kondisi Operasi Proses Monsanto
Metode ini pertama kali dikembangkan oleh pabrik Perusahaan Monsanto di
Texas City. Keunggulan dari metode ini ialah dapat dijalankan pada tekanan yang
rendah. Bahan dasar dari pembuatan asam asetat menggunakan metode ini ialah
methanol. Prinsip pembuatannya ialah methanol direaksikan dengan gas CO
menghasilkan asam asetat difasilitasi katalis rhodium. Sebelumnya pembuatan asam
asetat dengan teknik BASF dapat dilakukan dengan menggunakan katalis
8
iodinepromoted kobalt, namun kurang efektif dalam hal biaya karena katalis ini
bekerja pada tekanan tinggi yakni sekitar 7.500 lb/in
2
. Sedangkan katalis rhodium
bekerja pada tekanan antara 200 - 1800 lb/in
2
. Katalis rhodium menghasilkan asam
asetat sampai 99 % sedangkan katalis iodinepromoted kobalt hanya sekitar 90 %
saja. Mekanisme kerja proses monsanto berjalan dengan beberapa tahap,
1. Siklus katalitik konversi metanol menjadi metiliodida
CH
3
OH + HI CH
3
I + H
2
O
2. Penambahan katalis Rh (I) kompleks (d
8
segi empat planar) ke dalam metil iodida
menghasilkan struktur baru koordinat 6 alkil rhodium (III) kompleks (d
6
). CH
3
I +
[Rh-kompleks]
Mekanisme Reaksi Katalis
Katalis Carbonylation terdiri dari dua komponen utama yaitu rhodium
kompleks yang larut dan iodida promotor. Hampir setiap sumber Rh dan I
-
akan
bekerja dalam reaksi ini karena akan dikonversi menjadi katalis [Rh (CO)
2
I
2
]
-
di
bawah kondisi reaksi. Struktur katalis [Rh(CO)
2
I
2
]
-
dapat dilihat seperti gambar
berikut.
Katalis ini sangat aktif sehingga akan memberikan reaksi dan distribusi produk
yang baik. Skema pembuatan dalam pabrik dapat dilihat seperti pada gambar berikut:
9
Proses yang terjadi ialah; pertama methanol dimasukkan dalam tangki reaktor
dan direaksikan dengan HI. Peran iodida adalah hanya untuk mempromosikan
konversi methanol menjadi metil iodide:
MaOH + HI MeI + H
2
O
Setelah metil iodida telah terbentuk maka diteruskan ke reaktor katalis. Siklus
katalitik dimulai dengan penambahan oksidatif metil iodida ke dalam [Rh(CO)
2
I
2
]
-
sehingga terbentuk kompleks [MeRh(CO)I
3
]
-
(Gambar 2). Kemudian dengan cepat
CO pindah berikatan dengan CH
3
membentuk kompleks seperti pada gambar 3.
Setelah itu direaksikan dengan karbon monoksida, dimana gas CO berkoordinasi
sebagai ligan dalam kompleks Rh, menjadi rhodium-alkil kemudian membentuk
ikatan menjadi kompleks asil-rhodium (III) (Gambar 4). Dengan terbentuknya
kompleks pada gambar 4 maka gugus CH
3
COI mudah lepas. Kompleks ini kemudian
direduksi menghasilkan asetil iodide dan katalis rhodium yang terpisah. Ditangki ini
bekerja suhu 150
0
C-200
0
C dan tekanan 30 atm- 60 atm. Asetil iodida yang terbentuk
kemudian dihidrolisis dengan H
2
O menghasilkan CH
3
COOH dan HI.
Dimana HI yang terbentuk dapat digunakan lagi untuk mengkonversi methanol
menjadi MeI yang akan masuk dalam proses reaksi dan melanjutkan siklus.
Sedangkan asam asetat yang dihasilkan masuk dalam tangki pemurinian untuk
dipisahkan dari pengotor yang mungkin ada seperti asam propionate. Pemurnian
dilakukan dengan cara destilasi. Mekanisme reaksinya dapat dilihat pada gambar
berikut:
10
Gambar 5 The major unit comprising a commercial-scale Monsanto methanol
operating plant, which uses a rhodium-based catalyst
II.3. Kondisi Operasi Proses Cativa
Proses Cativa adalah metode lain untuk produksi asam asetat oleh
carbonylation dari metanol . Teknologi ini mirip dengan proses Monsanto hanya
berbeda dalam penggunaan katalis. Proses ini didasarkan pada iridium yang
mengandung katalis seperti kompleks Ir[(CO)
2
I
2]
.
Proses ini pertama kali
dikembangkan oleh BP Chemicals dan lisensi oleh BP Plc. Pada awalnya kajian
11
Monsanto telah menunjukkan bahwa iridium kurang aktif dari rhodium untuk proses
carbonylation metanol. Namun penelitian selanjutnya menunjukkan bahwa katalis
iridium bisa dipromosikan dengan bantuan ruthenium. Kombinasi ini menghasilkan
sebuah katalis yang lebih unggul daripada sistem berbasis rhodium. Penggunaan
iridium memungkinkan penggunaan air lebih sedikit dalam campuran reaksi. Dengan
demikian dapat mengurangi jumlah kolom pengeringan yang diperlukan, mengurangi
produk samping dan menekan gas air reaksi bergeser. Selain itu, proses ini
memungkinkan loading katalis yang lebih tinggi. Dibandingkan dengan proses
Monsanto, proses Cativa menghasilkan asam propionat sangat kecil dalam produk.
Struktur katalis kompleks Ir[(CO)
2
I
2]
dapat dilihat seperti gambar beriktut:
Proses reaksi dalam tangki dapat digambarkan dalam diagram berikut ini:
Pertama methanol direaksikan dengan asam iodide menghasilkan Metil Iodida.
Setelah itu, metal iodida masuk dalam tangki reaktor bereaksi sengan katalis
kompleks iridium (gambar 1) membentuk [Ir(CO)
2
I
3
CH
3
]
-
(gambar 2), setelah
terbentuk struktur ini dengan cepat direaksikan dengan gas CO sehingga I
-
akan
keluar dari kompleks digantikan CO sehingga terbentuk kompleks baru [Ir(CO)
3
I]
12
(gambar 3), struktuir ini kurang stabil sehingga untuk menstabilkan CO di mutasi
berikatan dengan CH
3
(gambar 4). Gugus CH
3
CO pada kompleks mudah lepas,
sehingga dengan adanya ion I
-
di sekitar kompleks menyebabkan gugus CH
3
CO
lepas dari kompleks dan bereaksi dengan I
-
membentuk CH
3
COI. Senyawa CH
3
COI
ini kemudian dihidrolisis menghasilkan asam asetat (CH
3
COOH) dan asam halida
(HI). Dimana HI yang terbentuk ini ditarik lagi masuk dalam siklus bereaksi dengan
methanol membentuk Metil Iodida yang akan bereaksi lagi dengan katalis. Asam
asetat yang terbentuk belum murni. Untuk memisahkan asam asetat dari pengotor
maka dilakukan destilasi. Mekanisme pembuatan asam asetat dalam pabrik dengan
proses Cativa dapat dipresentasikan seperti berikut ini.
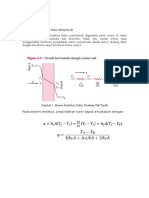
II.4. Tinjauan Thermodinamika dan Kinetika dari proses produksi asam asetat
dengan metode Monsato dan metode Cativa:
1) Tinjauan Thermodinamika:
CH
3
OH + CO CH
3
COOH
( )
o Karena
bernilai negatif, maka dapat diketahui reaksi bersifat eksotermis.
13
o Sesuai dengan tinjauan Thermodinamika, pada reaksi eksotermis jika tekanan
diperkecil maka reaksi akan berjalan ke arah reaktan (koefisien besar). Oleh
karena itu tekanan harus diperbesar agar reaksi berjalan ke kanan.
o Jika suhu dinaikkan maka reaksi akan berjalan ke arah reaktan, oleh karena itu
suhu operasi harus diturunkan agar reaksi berjalan ke arah produk.
2) Tinjauan Kinetika:
Sesuai dengan hukum Arrhenius:
k = konstanta kecepatan reaksi
A = frekuensi faktor tumbukan
E = energi aktivasi dari reaksi
R = konstanta gas ideal
= 1.98 cal/gm-mol.
o
K
= 1.98 Btu/lb-mol.
o
R
= 82.06 cm
3
.atm/gm-mol.
o
K
T = suhu reaksi
Sesuai hukum Arrhenius maka semakin tinggi suhu operasi maka semakin
besar nilai konstanta kecepatan reaksi
Semakin besar nilai konstanta kecepatan reaksi, maka semakin cepat laju
reaksinya sehingga semakin banyak produk yang dihasilkan
Sesuai dengan persamaan laju reaksi di atas, semakin besar konsentrasi reaktan
maka semakin cepat laju reaksi pembentukan produk.
a. Pemilihan Reaktor :
Jika jenis reaktor yang dipilih Batch
o Semakin besar volume reaktan dalam reaktor maka semakin kecil laju
kecepatan reaksi pembentukan produk. Secara molekular semakin besar
14
volume reaktan dalam reaktor maka jarak antar molekul satu dengan yang lain
akan semakin jauh sehingga frekuensi tumbukan antar reaktan akan semakin
kecil.
Jika jenis reaktor yang dipilih Continue stirred tank reactor (CSTR)
Overall
( )
()
Neraca Komponen
Q
1
C
A0
Q
2
C
A
C
C
C
B
C
D
15
o Dari persamaan di atas dapat diketahui bahwa semakin besar volume reaktor
maka laju pembentukan produk akan semakin kecil. Namun penggunaan
reaktor CSTR lebih efektif daripada reaktor batch, karena pada reaktor CSTR
produk akan secara kontinyu dihasilkan sehingga akan mengurangi waktu
tinggal reaktan dalam reaktor.
o Waktu tinggal reaktan dalam reaktor yang terlalu lama dapat mengurangi hasil
produksi suatu pabrik atau industri sehingga akan kurang menguntungkan bagi
suatu industri.
16
PENUTUP
1. Kesimpulan
1. Bahan dasar dari pembuatan asam asetat menggunakan metode monsato ialah
methanol. Prinsip pembuatannya ialah methanol direaksikan dengan gas CO
menghasilkan asam asetat difasilitasi katalis rhodium. Katalis rhodium
bekerja pada tekanan antara 200 - 1800 lb/in
2
.
2. Proses Cativa adalah metode lain untuk produksi asam asetat oleh
carbonylation dari metanol . Teknologi ini mirip dengan proses Monsanto
hanya berbeda dalam penggunaan katalis. Proses ini didasarkan pada iridium
yang mengandung katalis seperti kompleks Ir[(CO)
2
I
2]
.
3. Reaksi pembuatan asam asetat adalah reaksi eksotermis karena
bernilai
negatif.
4. Pada penggunaan reaktor batch dan kontinyu semakin besar volume maka
kecepatan reaksi pembentukan produknya akan semakin kecil.
5. Penggunaan reaktor CSTR lebih efektif daripada reaktor batch, karena pada
reaktor CSTR produk akan secara kontinyu dihasilkan sehingga akan
mengurangi waktu tinggal reaktan dalam reaktor.
6. Waktu tinggal reaktan dalam reaktor yang terlalu lama dapat mengurangi
hasil produksi suatu pabrik atau industri sehingga akan kurang
menguntungkan bagi suatu industri.
2. Saran
1. Proses produksi asam asetat sebaiknya dilakukan pada tekanan besar dan
suhu rendah.
2. Industri asam asetat akan lebih baik jika menggunakan reactor CSTR.
17
Daftar Pustaka
Jones Jone H., The Cativa Process For The Manufacture Plant Of Acetic Acid
Iridium Catalyst Improves Productivity In An Established Industrial Process.
BP Chemicals Ltd., Hull Research &Technology Centre, Salt End, Hull HU12
8DS, U.K
Li Xuebing and Enrique Iglesia. The Synthesis of Acetic Acid from Ethane, Ethene,
or Ethanol on Mo-V-Nb Oxide. Department of Chemical Engineering,
University of California, Berkeley, CA 94720, USA
Roth J. F. The Production of Acetic Acid Rhodium Catalysed Carbonylation Of
Methanol. Monsanto Co., St. Louis, Missouri
Shakhashiri. 2008. Acetic Acid & Acetic Anhydride. General Chemistry.
You might also like
- Paper Katalis Fischer TropschDocument12 pagesPaper Katalis Fischer TropschTriyana DefiNo ratings yet
- Analisis Alat Penukar Kalor Tipe Shell and Tube Dan Aplikasi Perhitungan Dengan MicrosoftDocument19 pagesAnalisis Alat Penukar Kalor Tipe Shell and Tube Dan Aplikasi Perhitungan Dengan MicrosoftarayeuukNo ratings yet
- Ammonia PlantDocument11 pagesAmmonia PlantSyariful Maliki NejstaršíNo ratings yet
- Pabrik BTX dari NaftaDocument48 pagesPabrik BTX dari NaftaLiona Margarita100% (1)
- Perancangan Pabrik MethanolDocument208 pagesPerancangan Pabrik MethanolHilman Billie JoeNo ratings yet
- Kel.5 Polimerisasi Skala IndustriDocument24 pagesKel.5 Polimerisasi Skala IndustriArifah JoharNo ratings yet
- Produksi Bersih Urea BaruDocument12 pagesProduksi Bersih Urea BaruAfrina NuratikaNo ratings yet
- EKSTRAKSI SUPERKRITISDocument12 pagesEKSTRAKSI SUPERKRITISNurul Maziyah100% (1)
- Formalin dan AplikasinyaDocument9 pagesFormalin dan AplikasinyaArrizal BuditamaNo ratings yet
- CO2 RemovalDocument12 pagesCO2 RemovalArdhyn GBNo ratings yet
- Surat Rekomendasi Kuliah Kerja Praktek 2Document1 pageSurat Rekomendasi Kuliah Kerja Praktek 2Dendha Dhonie Dwi PutraNo ratings yet
- Laporan 4C Kelompok 1 TRP Angkatan 2016Document97 pagesLaporan 4C Kelompok 1 TRP Angkatan 2016Revika WulandariNo ratings yet
- AIK (Makalah Distilasi)Document10 pagesAIK (Makalah Distilasi)Citra Kusuma ParahitaNo ratings yet
- Prob 8 Dan Prob 9Document9 pagesProb 8 Dan Prob 9Daning Kinanti SutamaNo ratings yet
- Distilasi Metode Mc. Cabe - ThieleDocument26 pagesDistilasi Metode Mc. Cabe - ThieleDian RestiNo ratings yet
- CabaiDocument45 pagesCabaiademadridNo ratings yet
- Destilasi Packing PDFDocument14 pagesDestilasi Packing PDFLuluk MalikNo ratings yet
- AMONIADocument26 pagesAMONIAisrayandiNo ratings yet
- Kerja Vacuum Pan CristallizerDocument1 pageKerja Vacuum Pan CristallizerMeyse Linda Susanti Teknik KimiaNo ratings yet
- NMEDocument20 pagesNMEAzhmed ZikryNo ratings yet
- HHV Dan LHVDocument7 pagesHHV Dan LHVyohanes100% (1)
- Training Jaya BayaDocument106 pagesTraining Jaya BayaismatNo ratings yet
- REAKTOR CSTRDocument22 pagesREAKTOR CSTRDian Remarthin GirsangNo ratings yet
- Proses Pembuatan Metilen KloridaDocument6 pagesProses Pembuatan Metilen KloridaAry OctavianiNo ratings yet
- Satuan Proses 1 11Document17 pagesSatuan Proses 1 11sriNo ratings yet
- HETP MbudddDocument30 pagesHETP MbudddDanu BratakusumaNo ratings yet
- PEMISAHANDocument25 pagesPEMISAHANDeborah Basa LumbanrajaNo ratings yet
- KOMPOSIT LAMINATEDocument46 pagesKOMPOSIT LAMINATEMuhammad FaridNo ratings yet
- Pemilihan Fluid PackageDocument8 pagesPemilihan Fluid PackagefebriNo ratings yet
- OPTIMASI WWCDocument26 pagesOPTIMASI WWCfiraNo ratings yet
- Shell-and-Tube Heat Exchanger DesignDocument87 pagesShell-and-Tube Heat Exchanger DesignFadhila UlfaNo ratings yet
- Pemurnian As - Stearin Di Pabrik Oleokimia PT. Flora SwtitkindoDocument8 pagesPemurnian As - Stearin Di Pabrik Oleokimia PT. Flora SwtitkindoAnonymous qIimoyNo ratings yet
- Fluid-Fluid Reactor DesignDocument19 pagesFluid-Fluid Reactor DesignFaghi Davi SNo ratings yet
- Bioadsorben DR Kulit Pisang RajaDocument33 pagesBioadsorben DR Kulit Pisang RajaNunie Puji LestariNo ratings yet
- Laporan PKL Yuliasari RevDocument73 pagesLaporan PKL Yuliasari Revirmayulianty100% (1)
- Pengoperasian Separator Di Lapangan PPSDM MigasDocument3 pagesPengoperasian Separator Di Lapangan PPSDM MigasGerald RahanraNo ratings yet
- Perancangan Pabrik Vinyl Acetate Monomer Dari EthyleneDocument16 pagesPerancangan Pabrik Vinyl Acetate Monomer Dari EthyleneLazuardi Hanif 19No ratings yet
- Modul Praktikum TransesterifikasiDocument13 pagesModul Praktikum Transesterifikasianastasia natalisaNo ratings yet
- Distilasi Kolom dengan Perubahan Konsentrasi UmpanDocument4 pagesDistilasi Kolom dengan Perubahan Konsentrasi UmpanDevita UtamiNo ratings yet
- Zat Pengotor Dalam AirDocument20 pagesZat Pengotor Dalam AirisnainiNo ratings yet
- Kimia Makalah HCLDocument7 pagesKimia Makalah HCLFarenayla AesyaNo ratings yet
- DMT Pabrik RancanganDocument443 pagesDMT Pabrik Rancanganjakarta 48No ratings yet
- HidrodesulfurisasiDocument6 pagesHidrodesulfurisasiAnisatul AzizahNo ratings yet
- CrackingDocument10 pagesCrackinghayati_nufus_1No ratings yet
- Cara Membuat Nata de Coco Menggunakan Air Kelapa dan Starter Acetobacter XylinumDocument7 pagesCara Membuat Nata de Coco Menggunakan Air Kelapa dan Starter Acetobacter XylinumDeliza DonaNo ratings yet
- KompositDocument15 pagesKompositWidya BestariNo ratings yet
- Makalah PK No 1Document4 pagesMakalah PK No 1MeidinaSekarNadistiNo ratings yet
- DHDT Proses dan KomponenDocument28 pagesDHDT Proses dan KomponenMayFifthNo ratings yet
- Asam Asetat ProsesDocument41 pagesAsam Asetat ProsesNiar R Sofiana0% (1)
- Makalah Industri Asam Asetat KLP 6 Pik 3Document18 pagesMakalah Industri Asam Asetat KLP 6 Pik 3Andi Sauqi UlviahNo ratings yet
- Asam Asetat Ke SiswaDocument19 pagesAsam Asetat Ke SiswaAnita RatnasariNo ratings yet
- As WadDocument9 pagesAs Wadsepul05No ratings yet
- Kimia Dasar ASAM CUKADocument22 pagesKimia Dasar ASAM CUKARachael SchneiderNo ratings yet
- 21-Industri Asam AsetatDocument90 pages21-Industri Asam AsetatBESTY LOVIANDANo ratings yet
- Pembuatan Asam KARBOKSILATDocument6 pagesPembuatan Asam KARBOKSILATTommy Injani0% (1)
- PEMBAHASAN PROSES PEMBUATAN ASAM ASETATDocument11 pagesPEMBAHASAN PROSES PEMBUATAN ASAM ASETATIskandar ZulkarnainNo ratings yet
- Pembuatan Asam Asetat Skala LaboratoriumDocument27 pagesPembuatan Asam Asetat Skala Laboratoriumatas warsiNo ratings yet
- Pigmen Warna PolimerDocument2 pagesPigmen Warna PolimerNia Sasria IdrisNo ratings yet
- Struktur OrganisasiDocument3 pagesStruktur OrganisasiNia Sasria IdrisNo ratings yet
- Ikatan HydrogenDocument1 pageIkatan HydrogenNia Sasria IdrisNo ratings yet
- Atiek Soemiati-UiDocument8 pagesAtiek Soemiati-Uiika21_chemistNo ratings yet
- Alcanivorax BorkumensisDocument1 pageAlcanivorax BorkumensisNia Sasria IdrisNo ratings yet
- LipidDocument1 pageLipidNia Sasria IdrisNo ratings yet
- Struktur Molekul ProteinDocument11 pagesStruktur Molekul ProteinNia Sasria IdrisNo ratings yet
- Formulir Pendaftaran Siswa BaruDocument1 pageFormulir Pendaftaran Siswa BaruNia Sasria IdrisNo ratings yet
- Jadwal Kegiatan Pelatihan Audit Energi SD Insan Mulia SurabayaDocument1 pageJadwal Kegiatan Pelatihan Audit Energi SD Insan Mulia SurabayaNia Sasria IdrisNo ratings yet
- CONTOH TANAHDocument63 pagesCONTOH TANAHNur CimootzNo ratings yet
- Metabolisme Mikroba LautDocument12 pagesMetabolisme Mikroba LautNia Sasria IdrisNo ratings yet
- Prak. Instrumen Oleh Nia SasriaDocument1 pagePrak. Instrumen Oleh Nia SasriaNia Sasria IdrisNo ratings yet
- KELOMPOK ElektronikaDocument3 pagesKELOMPOK ElektronikaNia Sasria IdrisNo ratings yet
- PROTEINDocument3 pagesPROTEINNia Sasria IdrisNo ratings yet
- Bio LeachingDocument1 pageBio LeachingNia Sasria IdrisNo ratings yet
- LipidDocument1 pageLipidNia Sasria IdrisNo ratings yet
- Cover ProposalDocument2 pagesCover ProposalNia Sasria IdrisNo ratings yet
- Prak. Instrumen Besi Oleh Nia SasriaDocument4 pagesPrak. Instrumen Besi Oleh Nia SasriaNia Sasria IdrisNo ratings yet
- Soal KimfisDocument1 pageSoal KimfisNia Sasria IdrisNo ratings yet
- Organik BenzoinDocument3 pagesOrganik BenzoinNia Sasria IdrisNo ratings yet
- Form - Pendaftaran Genap 2013 - 2014Document18 pagesForm - Pendaftaran Genap 2013 - 2014Nia Sasria IdrisNo ratings yet
- Cover PKMP NikelDocument1 pageCover PKMP NikelNia Sasria IdrisNo ratings yet
- RPP Ikatan Kimia 1 (4 JP)Document7 pagesRPP Ikatan Kimia 1 (4 JP)Nia Sasria IdrisNo ratings yet
- Surat Izin Penelitian Dan Bon AlatDocument3 pagesSurat Izin Penelitian Dan Bon AlatNia Sasria IdrisNo ratings yet
- Cover PKMP NiDocument3 pagesCover PKMP NiNia Sasria IdrisNo ratings yet
- Tracer Study Dan Hasil Evaluasi PenggunaDocument2 pagesTracer Study Dan Hasil Evaluasi PenggunaNia Sasria IdrisNo ratings yet
- Data Awal Pra s2 (2) - 2Document1 pageData Awal Pra s2 (2) - 2Nia Sasria IdrisNo ratings yet
- Bio LeachingDocument1 pageBio LeachingNia Sasria IdrisNo ratings yet
- 2714201009-Abstract IdDocument2 pages2714201009-Abstract IdNia Sasria IdrisNo ratings yet
- Cover ProposalDocument2 pagesCover ProposalNia Sasria IdrisNo ratings yet