Professional Documents
Culture Documents
Buku Anorganik
Uploaded by
ainiaturOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Buku Anorganik
Uploaded by
ainiaturCopyright:
Available Formats
Laboratorium Dasar Universitas Trunojoyo 1
ACARA I
PENGENALAN PERALATAN dan BAHAN
1. Tujuan Instruksional Khusus
Pada akhir praktikum nahasiswa diharapkan dapat menjelaskan tentang :
a. Alat-alat kimia dan cara pemakaiannya
b. Karakteristik bahan-bahan kimia
2. Dasar Teori
Yang harus diperhatikan :
Mengenal alat, bahan kimia serta cara pemakaian alat tersebut merupakan
yang sangat penting dalam aktivitas praktikum
Kemurnian bahan kimia, terutama dalam analisa, penting guna memperoleh
ketelitian semaksimal mungkin.
Setiap membuka tutup botol bahan kimia, harus segera ditutup kembali untuk
menghindari kontaminasi dan dehidrasi dan segera kembalikan ketempatnya
semula
Banyak bahan kimia yang harus ditangani dengan hati-hati karena sifatnya
yang berbahaya atau beracun
3. Bahan dan Alat
3.1. Bahan
a. AgNO3
b. HCl
c. H2SO4
d. NaOH
e. Indikakator PP
f. Indikator MO
g. KMO4
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 2
3.2. Alat
a. Gelas arloji
b. Timbangan analitik
c. Labu ukur
d. Pipet volume
e. Pipet ukur
f. Beaker glass
g. Buret
h. Erlenmeyer
i. Corong
j. Crus porselin
k. Mortar
4. Prosedur Percobaan
a. Siapkan beberapa peralatan
b. Gambar alat-alat tersebut
c. Tulis spesifikasi dan fungsinya
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 3
LEMBAR KERJA
Nama Mahasiswa : ……………………………. Pembimbing : …………………..
NRP : ……………………………. Paraf …………………..
Judul Praktikum : Pengenalan Alat dan Bahan
Tanggal : ……………………………..
Hasil Pengamatan :
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 4
ACARA II
SIFAT ASAM DAN BASA SENYAWA
1. Tujuan Instruksional Khusus
Pada akhir praktikum mahasiswa diharapkan dapat menjelaskan tentang :
a. Sifat-sifat asam dan basa senyawa
b. Perbedaan tingkat keasaman antara alkohol alifatis dan alkohol aromatis
c. Struktur senyawa asam dan basa
d. Struktur senyawa asam dan basa berdasarkan struktur elektron.
2. Dasar Teori
Sifat asam dan basa suatu senyawa dapat diuji dengan kertas lakmus. Jika
kertas lakmus biru oleh sesuatu zat diubah menjadi merah, maka zat tersebut
bersifat asam. Jika kertas lakmus merah diubah menjadi biru, maka zat tersebut
adalah basa atau bersifat basa.
Sifat asam maupun basa bisa diterangkan dengan tiga teori asam basa
menurut :
1. Arrehenius
2. Bronsted – Lowry
3. Lewis
Sedangkan kekuatan asam dan basa daopat diukur dengan pH paper universil
atau dengan pH meter.
3. Bahan dan Alat
3.1. Bahan
a. Larutan A
b. Larutan B
c. Larutan C
d. Larutan D
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 5
3.2. Alat
a. pH paper universil
4. Prosedur Percobaan
a. Ambil 4 buah pH paper universal & 4 buah kertas lakmus
b. Masukkan kedalam masing-masing larutan.
c. Amati perubahan yang terjadi.
d. Ulangi sekali lagi dan catat hasilnya
e. Bandingkan hasil dari pH paper Universil & Kertas lakmus
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 6
LEMBAR KERJA
Nama Mahasiswa : ……………………………. Pembimbing : …………………..
NRP : ……………………………. Paraf …………………..
Judul Praktikum : Sifat Asam dan Basa Senyawa
Tanggal : ……………………………..
Hasil Pengamatan :
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 7
ACARA III
ACIDIMETRI/ ALKALIMETRI
1. Tujuan Instruksional Khusus
Pada akhir praktikum mahasiswa diharapkan dapat memahami dan menjelaskan
hal-hal sebagai berikut :
a. Menentukan kadar Asam Asetat
b. Menentukan kadar Asam Sulfat
c. Menentukan kadar air dalam Soda Kristal & menentukan kadar HCl
d. Menentukan kadar amoniak dalam larutan
2. Dasar Teori
Pada titrasi asidi alkalimetri dibagi menjadi 2 bagian yaitu :
1. Asidimetri
Titrasi dengan menggunakan larutan standart asam yang digunakan untuk
menentukan basa.
Larutan standart asam yang biasa digunakan adalah HCl, asam cuka, asam,
oksalat dan asam borate
2. Alkalimetri
Titrasi ini merupakan kebalikan dari asidimetri dimana larutan standart yang
digunakan untuk menentukan asam.
Disini dipakai larutan standart NaOH.
III.1. Standarisasi Larutan Baku Asam Asetat dengan NaOH
3. Bahan dan Alat
3.1. Bahan
a. Asam Asetat
b. Indikator PP
c. NaOH 0,1 N
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 8
3.2. Alat
a. Pipet volume
b. Erlenmeyer
c. Pipet tetes
d. Buret
e. Corong
4. Prosedur Percobaan
a. Ambil beberapa ml larutan asam asetat 0,1 N (minta ukuran volume larutan
pada asisten) dengan menggunakan pipet, masukkan dalam erlenmeyer.
b. Tambahkan 2-3 tetes indikator pp atau tymol blue.
c. Titrasi larutan ini dengan NaOH 0,1 N sampai terjadi perubahan warna dari
tidak berwarna menjadi kerosa muda untuk indikator pp, sedangkan tymol
blue menjadi biru.
d. Amati sehingga terjadi suatu perubahan warna dan hentikan penitrasian.
e. Ulangi percobaan sekali lagi dan catat volume penitrasi, kemudian rata-rata
hasilnya.
f. Hitung kadar asam asetat (gram/100 ml)
Catatan :
100 NNaOH x VNaOH x BMAsam Asetat
Kadar Asam Asetat = x
V Asam Asetat 1000
Pembacaan Buret I II
Akhir Titrasi ……… ml ……… ml
Awal Tirasi ……… ml ……… ml
Volume Larutan CH3COOH ……… ml ……… ml
……. + …….
Volume rata-rata Penitir = ml
2
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 9
LEMBAR KERJA
Nama Mahasiswa : ……………………………. Pembimbing : …………………..
NRP : ……………………………. Paraf …………………..
Judul Praktikum : Standarisasi Larutan Baku Asam Asetat dengan NaOH
Tanggal : ……………………………..
Hasil Pengamatan :
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 10
III.2. Standarisasi Larutan Baku Asam Sulfat dengan NaOH
3. Bahan dan Alat
3.1. Bahan
a. Asam Sulfat
b. Indikator PP
c. NaOH 0.1N
3.2. Alat
a. Pipet volume
b. Erlenmeyer
c. Pipet tetes
d. Buret
e. Corong
4. Prosedur Percobaan
a. Pipetlah beberapa ml larutan asam sulfat, masukkan kedalam Erlenmeyer
b. Kemudian tambahkan indikator pp sebanyak 5 tetes
c. Titrasi larutan ini dengan NaOH 0.1N
d. Amati sehingga terjadi perubahan warna dan hentikan penitrasian
e. Ulangi percobaan sekali lagi dan catat volume penitrasi, kemudian rata-rata
hasilnya
f. Hitung kadar Asam Sulfat (gram/100 ml)
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 11
LEMBAR KERJA
Nama Mahasiswa : ……………………………. Pembimbing : …………………..
NRP : ……………………………. Paraf …………………..
Judul Praktikum : Standarisasi Larutan Baku Asam Sulfat dengan NaOH
Tanggal : ……………………………..
Hasil Pengamatan :
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 12
III.3. Standarisasi Larutan Baku Amoniak dengan HCl
3. Bahan dan Alat
3.1. Bahan
a. Amoniak
b. Indikator Metil Merah
c. HCl 0.1N
3.2. Alat
a. Pipet volume
b. Erlenmeyer
c. Pipet tetes
d. Buret
e. Corong
4. Prosedur Percobaan
a. Pipetlah 10 ml larutan yang diperlukan, masukkan kedalam Erlenmeyer
b. Tambahkan 40 ml aquades
c. Tambahkan 3 tetes indikator Metil Merah
d. Titrasi larutan ini dengan HCl 0.1N
e. Amati sehingga terjadi perubahan warna dari kuning menjadi merah dan
hentikan penitrasian
f. Ulangi percobaan sekali lagi dan catat volume penitrasi, kemudian rata-rata
hasilnya
g. Hitunglah kadar amoniak (gram/100 ml)
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 13
LEMBAR KERJA
Nama Mahasiswa : ……………………………. Pembimbing : …………………..
NRP : ……………………………. Paraf …………………..
Judul Praktikum : Standarisasi Larutan Baku Amoniak dengan HCl
Tanggal : ……………………………..
Hasil Pengamatan :
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 14
III.4. Standarisasi Larutan Baku HCl dengan Borax
Keuntungan standarisasi dengan Borax daripada yang lain adalah :
Borax mempunyai sifat anhygropic (tidak mudah menyerap air)
Dalam temperatur kamar, endapan pointnya jelas dengan metyl merah
2H+ + B4O7 + 5H2O → 4H3BO3 + Na2+
1 grl Na2B4O7 = 2 grek Na2B4O7
3. Bahan dan Alat
3.1. Bahan
a. Larutan Borax
b. HCl
c. Indikator MO
3.2. Alat
a. Pipet volume
b. Erlenmeyer
c. Pipet tetes
d. Buret
e. Corong
4. Prosedur Percobaan
a. Pipetlah beberapa ml larutan borax, masukkan kedalam Erlenmeyer
b. Tambahkan beberapa tetes indikator MO
c. Titrasi larutan borax yang telah diberi indikator dalam Erlenmeyer dengan
larutan baku HCl yang berada dalam buret secara perlahan-lahan dengan
dikocok hingga warna berubah dari kuning menjadi merah muda
d. Setelah warna menjadi merah muda, hentikan penitasian
e. Ulangi percobaan sekali lagi dan catat volume titrasi, kemudian rata-rata
hasilnya
f. Hitung kadar HCl (gram/100 ml)
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 15
LEMBAR KERJA
Nama Mahasiswa : ……………………………. Pembimbing : …………………..
NRP : ……………………………. Paraf …………………..
Judul Praktikum : Standarisasi Larutan Baku HCl dengan Borax
Tanggal : ……………………………..
Hasil Pengamatan :
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 16
PERCOBAAN IV
KECEPATAN REAKSI
1. Tujuan Instruksional Khusus
Mahasiswa diharapkan mampu :
a. Mengetahui pengaruh konsentrasi terhadap kecepatan reaksi
b. Mengetahui pengaruh suhu terhadap kecepatan reaksi.
2. Dasar Teori
Perubahan-perubahan dalam suatu reaksi kimia dan kecepatan reaksi dapat
dijelaskan dengan teori kinetika kesetimbangan kimia. Mekanisme reaksi kimia
menerangkan melalui langkah-langkah manakah suatu zat pereaksi berubah
menjadi hasil reaksi. Kecepatan reaksi menerangkan seberapa cepat reaksi
berlangsung. Kecepatan reaksi kimia biasanya didefinisikan sebagai perubahan
konsentrasi zat yang ikut serta dalam reaksi tersebut per satuan waktu, misal
untuk reaksi :
A+B P
Persamaan kecepatan reaksi dapat dituliskan :
d[A] d[B] d[P]
r = - =- =-
dt dt dt
Persamaan ini menunjukkan bahwa kecepatn reaksi berbanding lurus dengan
konsentrasi dan berbanding terbalik dengan waktu.
Dari berbagai percobaan ternyata bahwa kecepatan reaksi tidak selalu
merupakan fungsi linier dari konsentrasi zat pereaksi. Untuk reaksi di atas, dapat
dinyatakan secara empiris dalam persamaan :
r = k [A]p[B]q
P dan q merupakan orde reaksi (tingkat reaksi), (p+q) adalah tingkat reaksi total
untuk reaksi tersebut. Andaikan suatu reaksi mempunyai orde n, maka kecepatan
reaksi akan sebanding dengan [konsentrasi]n dan berbanding terbalik dengan
waktu t :
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 17
r ≅ [C ] n C = konsentrasi n = orde reaksi
1
r ≅ t = waktu
t
1 n
Sehingga jika dibuat grafik [C ] versus
, maka akan diperoleh grafik
t
berupa garis lurus. Dengan demikian tingkat reaksi suatu reaksi kimia dapat
n
1
ditentukan dengan membuat grafik [C ] versus
t
Tingkat reaksi Penetuan tingkat reaksi dengan membuat grafik
1 [C ] 1 vs 1/t
2 [C ] 2 vs 1/t
3 [C ] 3 vs 1/t
Kecepatan reaksi dapat diukur dari laju terbentuknya hasil reaksi, misalnya reaksi
antara Na2S2O3 dan H2SO4 dapat diukur dari laju pembentukan S yang
mengakibatkan kekeruhan larutan :
Na+S2O3 + H2SO4 Na+SO3 + SO2(g) + S(s) + H2O
3. Bahan dan Alat
3.1. Bahan
a. Na2S2O3 0,2 N ; 0,4 N ; 0,6 N ; 0,8 N ;1 N
b. H2SO4 0,2 N ; 0,4 N ; 0,6 N ; 0,8 N ; 1 N
c. Aquades
3.2. Alat
a. Rak tabung reaksi
b. Tabung reaksi
c. Beaker glass
d. Stopwatch/jam tangan
e. Gelas pengaduk
f. Gelas ukur
g. Thermometer
h. Penjepit kayu
i. Pipet tetes
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 18
4. Prosedur Percobaan
IV.1. Hubungan antara kecepatan reaksi dengan konsentrasi H2SO4
a. Isilah 5 tabung reaksi, masing-masing dengan 5 ml Na2S2O3 0,2 N dan
letakkan di rak.
b. Isikan pada tabung pertama 5 ml H2SO4 0,2 N dan aduklah dengan baik
sampai timbul kekeruhan .
c. Catat waktu terbentuknya kekeruhan.
d. Ulangi percobaan di atas untuk tabung reaksi berikutnya dengan konsentrasi
H2SO4 0,4 N ; 0,6 N ; 0,8 N ; 1N
e. Buatlah kurva antara 1/t terhadap konsentrasi H2SO4.
IV.2. Hubungan antara kecepatan reaksi dengan konsentrasi Na2S2O3
a. Isilah 5 tabung reaksi, masing-masing dengan 5 ml H2SO4 0,2 N dan letakkan
di rak.
b. Isikan pada tabung pertama 5 ml Na2S2O3 0,2 N dan aduklah dengan baik
sampai timbul kekeruhan .
c. Catat waktu terbentuknya kekeruhan.
d. Ulangi percobaan di atas untuk tabung reaksi berikutnya dengan konsentrasi
Na2S2O3 0,4 N ; 0,6 N ; 0,8 N ; 1N
e. Buatlah kurva antara 1/t terhadap konsentrasi Na2S2O3.
IV.3. Hubungan antara kecepatan reaksi dengan suhu
a. Isilah 5 tabung reaksi, masing-masing dengan 5 ml Na2S2O3 0,2 N dan
letakkan di rak.
b. Catat suhunya. Ini adalah suhu awal reaksi
c. Isikan pada tabung pertama 5 ml H2SO4 0,2 N dan aduklah dengan baik
sampai timbul kekeruhan. Catat waktu terbentuknya kekeruhan.
d. Catat suhunya. Ini adalah suhu awal reaksi.
e. Ulangi percobaan tersebut untuk suhu zat pereaksi 35, 40, 45, dan 50oC
(Catatan : pemanasan zat pereaksi dimulai dengan suhu yang lebih tinggi,
gunakan penangas air)
f. Buatlah kurva antara 1/t terhadap suhu pereaksi.
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 19
LEMBAR KERJA
Nama Mahasiswa : …………………………… Pembimbing : ………………
NRP : …………………………… Paraf : ………………
Judul Praktikum : Kecepatan Reaksi
Tanggal : ……………………………
Hasil Pengamatan :
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 20
PERCOBAAN V
PERMANGANOMETRI
1. Tujuan Instruksional Khusus
Pada akhir titrasi mahasiswa diharapkan dapat memahami dan mengerti
prinsip dasar Permanganometri
- Menghitung kadar calium
2. Dasar Teori
Cara ini berdasarkan oksidasi oleh ion permanganat. Karena itu selain
disebut permanganometri, berdasarkan oksidasi juga disebut oksidimetri.
Oksidimetri dapat dilakukan dalam suasana asam, basa maupun netral.
Dalam lingkungan asam KMnO4 bereaksi
MnO- + 8H+ + 5e- → Mn2+ + 4H2O
Dalam lingkungan netral
MnO- + 2H2O + 3e- → MnO + 4OH-
Dalam lingkungan basa
MnO- + e- → MnO2-
3. Bahan dan Alat
3.1. Bahan
a. K2Cr2O7 .2H2O
b. Larutan baku KMnO4 0,1 N
c. Larutan H2SO4 4N
d. Aquadest
3.2. Alat
a. Gelas arloji
b. Labu ukur 250 ml
c. Buret
d. Timbangan analitik
e. Pipet volume
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 21
4. Prosedur Percobaan
a. Timbang 0,3 grK2Cr2O7. 2H2O dalam gelas arloji.
b. Larutkan dengan aquadest dalam labu ukur 50 ml sampai batas, kocok dengan
sempurna.
c. Pipet 25 ml, masukkan ke dal;am erlenmeyer dan tambahkan H2SO4 4 N
d. Kocok dengan baik, lalu panaskan pai mendidih, kocok lagi kemudian dititrasi
dengan larutan KMnO4
e. Titik akhir tercapai, bila warna pink berubah menjadi tak berwarna.
f. Ulangi percobaan sekali lagi dan hasilnya dirata-rata.
Catatan :
MK2Cr2O7.2H2O (dalam mg) x 2
Kadar K2Cr2O7. 2H2O =
BM K2Cr2O7.2H2O x VKMnO4
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 22
LEMBAR KERJA
Nama Mahasiswa : …………………………… Pembimbing : ………………
NRP : …………………………… Paraf : ………………
Judul Praktikum : Permanganometri
Tanggal : ……………………………
Hasil Pengamatan :
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 23
PERCOBAAN VI
IODOMETRI
1. Tujuan Instruksional Khusus
Diharapkan mahasiswa mampu :
- Memakai prinsip dasar Iodometri
- Menentukan atau menghitung Iod dalam larutan aktif Chlor
2. Dasar Teori
Dasar dari cara iodometri adalah reaksi keseimbangan dari iodom dan iodida.
Normal potensial reduksi dari system reversible adalah
I2 + 2e → 2I- …………………..0.5354 volt
Dengan demikian
1 grol I2 = 2 grek I2
Titrasi iodometri ada 2 cara yaitu :
1. Cara Langsung
Menurut cara ini suatu zat reduksi dititrasi langsung oleh iodom
Misal pada titrasi Na2S2O3 oleh I2
2. Cara Tak Langsung
Dalam hal ini ion iododa sebagai pereduksi diubah menjadi iodium-iodium
yang terbentuk dititrasi dengan larutan standart Na2S2O3. Jadi cara ini
digunakan untuk menentukan zat pengoksidasi.
Misal pada penentuan suatu zat oksidator ini (H2O2). Pada oksidator ini
ditambahkan larutan KI dan asam sehingga akan terbentuk iodium yang
kemudian dititrasi dengan larutan.
Na2S2O3 . H2O2 + KI + 2HCl → I2 + 2 KCl +2H2O
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 24
VI.1. Pembakuan Larutan Natrium Thiosulfat dengan Larutan
Baku KIO3
3. Bahan dan Alat
3.1. Bahan
a. KIO3 kristal
b. Aquadest
c. KI
d. H2SO4 1 N
e. Larutan baku Na2S2O3
f. Indikator amylum
3.2. Alat
a. Gelas arloji
b. Erlenmeyer
c. Corong
d. Pipet
e. Neraca analitik
f. Buret
g. Labu takar
4. Prosedur Percobaan
a. Timbang 0.2 gram KIO3 kristal pada gelas arloji yang telah ditimbang
b. Masukkan dalam labu ukur 50 ml melalui corong bilas
c. Campurkan dengan aquades sampai tanda batas
d. Pipet 25 ml larutan KIO3, masukkan dalam Erlenmeyer
e. Tambahkan 2 gram KI yang bebas dari iodat dan 10 ml H2SO4 1N
f. Titrasi dengan larutan Na2S2O3 yang akan ditentukan normalitasnya
g. Bila warna kuning iodium menjadi pucat hentikan titrasi dan tambahkan 4 ml
indikator amilum . Teruskan titrasi hingga warna menjadi hilang
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 25
h. Ulangi percobaan sekali lagi dengan volume larutan KIO3 tetap dan hasilnya
dirata-rata.
Rumus yang dipakai :
100
Kadar KIO3 = x NNa2S2O3 x VNa2S2O3 x BMKIO3
VKIO3
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 26
LEMBAR KERJA
Nama Mahasiswa : …………………………… Pembimbing : ………………
NRP : …………………………… Paraf : ………………
Judul Praktikum : Pembakuan Larutan Natrium Thiosulfat dengan KIO3
Tanggal : ……………………………
Hasil Pengamatan :
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 27
VI.2. Penentuan Chlor Aktif dalam Kapur Chlor
3. Bahan dan Alat
3.1. Bahan
a. Kapur Chlor
b. Aquades
c. Kristal KI
d. Asam Asetat 4 N
e. Indikator thiosulfat
3.2. Alat
a. Timbangan analitik
b. Gelas arloji
c. Mortar
d. Pipet volume
e. Erlenmeyer
f. Pipet tetes
g. Buret
4. Prosedur Percobaan
a. Timbanglah dengan tepat 300 mg kapur chlor
b. Masukkan kedalam Erlenmeyer
c. Tambahkan 50 ml aquades, 1 gram kristal KI yang telah dihaluskan terlebih
dahulu dan tambahkan 20 ml asam asetat 4 N
d. Tutuplah labu tersebut, diamkan selama 2 menit dengan sebentar-sebentar
dikocok, lalu titrasikan secepatnya dengan thiosulfat
e. Indikator ditambahkan sesudah larutan terlihat berwarna kuning muda
f. Tentukan kadar chlor aktif dalam kapur chlor tersebut.
g. Ulangi percobaan sekali lagi dan hasilnya dirata-rata
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 28
LEMBAR KERJA
Nama Mahasiswa : …………………………… Pembimbing : ………………
NRP : …………………………… Paraf : ………………
Judul Praktikum : Penentuan Chlor Aktif dalam Kapur Chlor
Tanggal : ……………………………
Hasil Pengamatan :
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 29
PERCOBAAN VII
GRAVIMETRI
1. Tujuan Instruksional Khusus
Diharapkan mahasiswa mampu :
a. Menghitung air hidrat
b. Menentukan x dalam BaCl2 x H2O
2. Dasar Teori
Penentuan Kwantitatif suatu zat dengan cara pengendapan diikuti isolasi dan
penimbangan endapan dinamakan analisa gravimetric.
3. Bahan dan Alat
3.1. Bahan
a. BaCl2 x H2O
3.2. Alat
a. Crus Porselin
b. Eksikator
c. Timbangan amalitik
d. Oven
4. Prosedur Percobaan
a. Panaskan crus porselin beberapa menit, dinginkan dalam eksikator dan
timbang sesudah 30 menit
b. Masukkan kedalam crus tersebut 1 –1.5 gram BaCl2 x H2O
c. Panaskan selama 10 menit. Dinginkan dalam eksikator dan timbang lagi
d. Ulangi pemijaran agar diperoleh berat yang konstan
e. Ulangi percobaan sekali lagi dan hasilnya dirata-rata
Rumus yang dipakai :
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 30
Berat crus porselin + BaCl2 x H2O kering = ………………. gr
Berat crus porselin kosong = ………………. gr
Berat BaCl2 x H2O kering = ………………. gr
Berat BaCl2 x H2O basah = ………………. gr
Berat BaCl2 x H2O kering = ………………. gr
Jumlah air yang hilang = ………………. Gr
Massa x H2O = Massa BaCl2 x H2O
BM xH2O BM BaCl2 x H2O
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 31
LEMBAR KERJA
Nama Mahasiswa : …………………………… Pembimbing : ………………
NRP : …………………………… Paraf : ………………
Judul Praktikum : Gravimetri
Tanggal : ……………………………
Hasil Pengamatan :
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 32
TATA TERTIB DI LABORATORIUM
1. Mahasiswa harus datang di Laboratorium 10 menit sebelum praktikum dimulai.
2. Sebelum melaksanakan praktikum mahasiswa diwajibkan mempelajari materi
yang akan dipraktikumkan.
3. Mahasiswa harus mengikuti semua kegiatan praktikum yang diselenggarakan di
laboratorium.
4. Pada waktu praktikum mahasiswa diharuskan memakai baju praktikum/ Jas Lab
5. Jika akan meninggalkan Laboratorium sebelum waktunya selesai, mahasiswa
diwajibkan minta ijin terlebih dahulu kepada asisten yang bertugas
6. Mahasiswa bertanggung jawab atas alat-alat atau bahan-bahan yang digunakan
di dalam praktikum.
7. Waktu praktikum mahasiswa harus bekerja dengan tenang dan penuh tanggung
jawab, dilarang bersendau gurau, ribut, main, merokok dan makan ataupun
minum di Laboratorium.
8. Mahasiswa dilarang melakukan percobaan atau mencoba-coba dengan bahan-
bahan kimia di Laboratorium tanpa seijin asisten yang bertugas.
9. Bila ada kesulitan atau kecelakaan harus segera lapor pada asisten yang
bertugas.
10. Bila mahasiswa memecahkan ataupun merusakkan barang-barang/ alat-alat
Laboratorium diharuskan mengganti dengan barang yang sama.
11. Selesai melakukan praktikum setiap mahasiswa diharuskan membuat laporan
sementara.
12. Seminggu setelah laporan sementara, mahasiswa harus menyerahkan laporan
resmi dari percobaan yang telah dilakukan. Keterlambatan pengumpulan
laporan dikenai sangsi pengurangan nilai 2,5% perhari.
13. Sebelum melaksanakan praktikum mahasiswa diwajibkan mempelajari materi
yang akan dipraktikumkan.
14. Penanggung jawab Laboratorium/ Asisten berwenang untuk mengambil
tindakan, jika ada mahasiswa yang melanggar peraturan tata tertib di atas.
15. Pelanggaran terhadap tata tertib ini dikenakan sanksi sebagai berikiut :
a. Peringatan atas pelanggaran yang dilakukan.
b. Tidak diijinkan mengikuti praktikum.
Petunjuk Praktikum Kimia Anorganik
Laboratorium Dasar Universitas Trunojoyo 33
DAFTAR ISI
Acara I : Pengenalan Peralatan dan Bahan ………………………….. 1
Acara II : Sifat Asam dan Basa Senyawa …………………………….. 4
Acara III : Acidimetri/Alkalimetri
III.1. Standarisasi Lart. Baku Asam Asetat dengan NaOH … 7
III.2. Standarisasi Lart. Baku Asam Sulfat dengan NaOH … 10
III.3. Standarisasi Lart. Baku Amoniak dengan HCl ………. 12
III.4. Standarisasi Lart. Baku HCl dengan Borax ………….. 14
Acara IV : Kecepatan Reaksi
IV.1. Hub. kecepatan reaksi dengan konsentrasi H2SO4 …… 18
IV.2. Hub. Kecepatan reaksi dengan konsentrasi Na2S2O3 ... 18
IV.3. Hub. Antara kecepatan reaksi dengan suhu ………….. 18
Acara V : Permanganometri …………………………………………… 20
Acara VI : Iodometri
VI.1. Pembakuan Larutan Na2S2O3 dengan KIO3 …………. 24
VI.2. Penentuan Chlor Aktif salam Kapur Chlor ………….. 27
Acara VII : Gravimetri ………………………………………………….. 29
Petunjuk Praktikum Kimia Anorganik
You might also like
- Buku Biokimia PDFDocument29 pagesBuku Biokimia PDFdonordarah93100% (1)
- Petunjuk Praktikum Kimia Dasar IIDocument67 pagesPetunjuk Praktikum Kimia Dasar IIOktaviaIntanSianturiNo ratings yet
- Parasetamol Deteksi 40Document12 pagesParasetamol Deteksi 40YUYUNSENTOSANo ratings yet
- Ujian Akhir Semester Ganjil SMK Bhakti Putra Bangsa Purworejo Tahun Pelajaran 2017/2018Document7 pagesUjian Akhir Semester Ganjil SMK Bhakti Putra Bangsa Purworejo Tahun Pelajaran 2017/2018Novydita RiscaNo ratings yet
- LKM Percobaan 3 Asam BasaDocument7 pagesLKM Percobaan 3 Asam BasaBrian FebriantoNo ratings yet
- Analisis KromatografiDocument36 pagesAnalisis KromatografiAriantoNo ratings yet
- DETEKSIDocument30 pagesDETEKSIShela SaidNo ratings yet
- Penuntun Praktikum Kimia AnalitikDocument31 pagesPenuntun Praktikum Kimia AnalitikDwi HeniantariNo ratings yet
- LAPORAN PRAKTIKUM ANALISIS POTENSIOMETRI Catatan MahasiswaDocument5 pagesLAPORAN PRAKTIKUM ANALISIS POTENSIOMETRI Catatan MahasiswaLinda Faiqotul HimmahNo ratings yet
- KadarDocument4 pagesKadarLi LiNo ratings yet
- Kimia Analitik IDocument21 pagesKimia Analitik Ivilda roudha ningrumNo ratings yet
- Kartu Soal Ujian Praktik 2016Document3 pagesKartu Soal Ujian Praktik 2016Anonymous vGkPvADMNo ratings yet
- Unit. 2 TitrimetriDocument13 pagesUnit. 2 TitrimetrirabiantiNo ratings yet
- PRAKTIKUM KIMIA LINGKUNGANDocument39 pagesPRAKTIKUM KIMIA LINGKUNGANWelltina WelltinaNo ratings yet
- Standarisasi Asam KloridaDocument7 pagesStandarisasi Asam KloridaHindun FauziahNo ratings yet
- Modul Praktikum Kimia Organik FIXDocument31 pagesModul Praktikum Kimia Organik FIXwiwin kusuma dewiNo ratings yet
- Sophia Az-Zahro S - 104221015 - Keasaman Dalam Air Dengan Titrimetrik DanDocument13 pagesSophia Az-Zahro S - 104221015 - Keasaman Dalam Air Dengan Titrimetrik DanfiaNo ratings yet
- LKS XI Titrasi P2Document2 pagesLKS XI Titrasi P2dian anggreniNo ratings yet
- Panduan Praktikum Kimia Klinik 3Document34 pagesPanduan Praktikum Kimia Klinik 3Fredy MayorNo ratings yet
- Laporan Prak - Analisi HPLCDocument15 pagesLaporan Prak - Analisi HPLCElva DevyantiNo ratings yet
- Siska Dwi W - 104221009 - Modul 5-6Document13 pagesSiska Dwi W - 104221009 - Modul 5-6Siska Dwi WahyuniNo ratings yet
- Konsep Analisis Kuantitatif Dan Pengukuran PHDocument11 pagesKonsep Analisis Kuantitatif Dan Pengukuran PHSilvyera HeryantiNo ratings yet
- Manual Praktikum Kimia Dasar PDFDocument64 pagesManual Praktikum Kimia Dasar PDFImam BaehaqiNo ratings yet
- Alat Kimia DasarDocument18 pagesAlat Kimia DasarKAFIANA DAMAYANTINo ratings yet
- Kimia Farmasi AnalisisDocument25 pagesKimia Farmasi AnalisisItsuka TenmaNo ratings yet
- SNI 19-7117.6-2005 (Amonia Indophenol - Emisi)Document14 pagesSNI 19-7117.6-2005 (Amonia Indophenol - Emisi)Andri Fachrur RozieNo ratings yet
- Methyl Orange dan FenolphtaleinDocument6 pagesMethyl Orange dan FenolphtaleinNicky ArwitaNo ratings yet
- ANALITIK KIMIADocument7 pagesANALITIK KIMIAMuhammad RafiNo ratings yet
- Makalah Aplikasi Analisis AirDocument52 pagesMakalah Aplikasi Analisis AirArrovi Septian100% (3)
- KIMIA ANALISISDocument10 pagesKIMIA ANALISISElida NadiaNo ratings yet
- Percobaan 4. Analisis Kuantitatif (Titrasi Asam Basa Dan Gravimetri)Document22 pagesPercobaan 4. Analisis Kuantitatif (Titrasi Asam Basa Dan Gravimetri)Cinderi Maura Restu100% (2)
- Laporan Resmi PDTKDocument34 pagesLaporan Resmi PDTKlatifanurul080No ratings yet
- Buku PraktikumDocument52 pagesBuku PraktikumadindaNo ratings yet
- Analisa Kadar Natrium BenzoatDocument2 pagesAnalisa Kadar Natrium BenzoatTarmi ZeeNo ratings yet
- Kel 2 KromotografiDocument8 pagesKel 2 KromotografiChandraNo ratings yet
- Teknik Dan Metode Kimia Analis Kuantitatif KonvensionalDocument132 pagesTeknik Dan Metode Kimia Analis Kuantitatif Konvensionalvenus_asihNo ratings yet
- Hasil DiskusiDocument6 pagesHasil DiskusiNur Muthmainna SNo ratings yet
- I - Kamis Pagi - Spektrofotometri Anorganik PDFDocument41 pagesI - Kamis Pagi - Spektrofotometri Anorganik PDFDeariska Dahlan100% (1)
- Jepretan Layar 2022-08-22 Pada 8.37.54 PMDocument16 pagesJepretan Layar 2022-08-22 Pada 8.37.54 PMmanasye tangguNo ratings yet
- Laporan Praktikum BiokimiaDocument21 pagesLaporan Praktikum BiokimiaIbnu Fajar50% (2)
- Laporan PotensiometriDocument34 pagesLaporan PotensiometriPutri EprianiNo ratings yet
- Analisis FarmasiDocument11 pagesAnalisis FarmasiMareta Nur AisyahNo ratings yet
- FOR-LABORATORY-REPORTDocument10 pagesFOR-LABORATORY-REPORTDwi AndikaNo ratings yet
- Analisis Kuantitatif FeCl3.6H2O dengan Metode GravimetriDocument11 pagesAnalisis Kuantitatif FeCl3.6H2O dengan Metode Gravimetrisiti hidraNo ratings yet
- PenuntunPrak Kimia 2020Document52 pagesPenuntunPrak Kimia 2020adindaNo ratings yet
- Praktikum Larutan PenyanggaDocument2 pagesPraktikum Larutan PenyanggaMaroh ImuetzNo ratings yet
- Tugas Kimia Analitik TPS 1A-1BDocument2 pagesTugas Kimia Analitik TPS 1A-1BKHOCENG OYENNo ratings yet
- Petunjuk Praktikum Kimia Analitik III (2010)Document20 pagesPetunjuk Praktikum Kimia Analitik III (2010)Yudi Prika NugrohoNo ratings yet
- Kriteria Perencanaan Desain Bak Ekualisasi Dan AerasiDocument8 pagesKriteria Perencanaan Desain Bak Ekualisasi Dan AerasiAde YusufNo ratings yet
- Bab 1 Makalah Bu Puji InsulinDocument20 pagesBab 1 Makalah Bu Puji InsulinYudha Setyo PratamaNo ratings yet
- Teknik Analisis DataDocument1 pageTeknik Analisis DataYudha Setyo PratamaNo ratings yet
- Naskah Drama NasionalDocument2 pagesNaskah Drama NasionalYudha Setyo Pratama100% (1)
- Drama Ovj Ala Kelompok 2Document4 pagesDrama Ovj Ala Kelompok 2Yudha Setyo PratamaNo ratings yet
- Kekurangan Dan Kelebihan MultimediaDocument3 pagesKekurangan Dan Kelebihan MultimediaYudha Setyo Pratama100% (1)
- AMPIBI Sosialisasi Kemahasiswaan 18 Des 2011Document1 pageAMPIBI Sosialisasi Kemahasiswaan 18 Des 2011Yudha Setyo PratamaNo ratings yet
- Fakta UnikDocument3 pagesFakta UnikYudha Setyo PratamaNo ratings yet
- Buku Ekologi TumbuhanDocument2 pagesBuku Ekologi TumbuhanYudha Setyo PratamaNo ratings yet
- Makalah Pembelajaran Audio VisualDocument11 pagesMakalah Pembelajaran Audio VisualYudha Setyo PratamaNo ratings yet
- Rekapitulasi PajakDocument1 pageRekapitulasi PajakYudha Setyo PratamaNo ratings yet
- Pengaruh Air Kelapa MudaDocument2 pagesPengaruh Air Kelapa MudaYudha Setyo PratamaNo ratings yet
- AMPIBI Sosialisasi Kemahasiswaan 18 Des 2011Document1 pageAMPIBI Sosialisasi Kemahasiswaan 18 Des 2011Yudha Setyo PratamaNo ratings yet
- Bunga Putri Kel 2Document1 pageBunga Putri Kel 2Yudha Setyo PratamaNo ratings yet
- Bacaan Doa Bersama PernikahanDocument28 pagesBacaan Doa Bersama Pernikahanalvia sheera arifin60% (5)
- Bab 1 (08308141034)Document9 pagesBab 1 (08308141034)Yudha Setyo PratamaNo ratings yet
- Bab 1 (08308141034)Document9 pagesBab 1 (08308141034)Yudha Setyo PratamaNo ratings yet
- Bab 1 (08308141034)Document9 pagesBab 1 (08308141034)Yudha Setyo PratamaNo ratings yet
- Bacaan Doa Bersama PernikahanDocument28 pagesBacaan Doa Bersama Pernikahanalvia sheera arifin60% (5)
- ANALISIS E.COLIDocument7 pagesANALISIS E.COLIYunita ManurungNo ratings yet
- Bab 1 (08308141034)Document9 pagesBab 1 (08308141034)Yudha Setyo PratamaNo ratings yet
- Resum StrukturDocument6 pagesResum StrukturYudha Setyo PratamaNo ratings yet
- Hendro WahjonoDocument66 pagesHendro WahjonosanbowoNo ratings yet
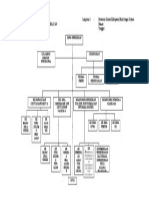
- Bagan Struktur OrganisasiDocument1 pageBagan Struktur OrganisasiYudha Setyo PratamaNo ratings yet
- Tupoksi Dinas PendidikanDocument20 pagesTupoksi Dinas PendidikanYudha Setyo PratamaNo ratings yet
- Resum StrukturDocument6 pagesResum StrukturYudha Setyo PratamaNo ratings yet
- Nutrisi N Kuliah MediaDocument55 pagesNutrisi N Kuliah MediaYudha Setyo PratamaNo ratings yet
- Bagan Struktur OrganisasiDocument1 pageBagan Struktur OrganisasiYudha Setyo PratamaNo ratings yet
- Resum StrukturDocument6 pagesResum StrukturYudha Setyo PratamaNo ratings yet
- Resum StrukturDocument6 pagesResum StrukturYudha Setyo PratamaNo ratings yet
- Tugas 1 ProfesiDocument3 pagesTugas 1 ProfesiYudha Setyo PratamaNo ratings yet