Professional Documents
Culture Documents
2 Ecuaciones de Estado
Uploaded by
Beto CordovaCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
2 Ecuaciones de Estado
Uploaded by
Beto CordovaCopyright:
Available Formats
Ingeniera Qumica - Univ.
Valladolid
Tema 2 - Ecuaciones de Estado
Tema 2 :
Ecuaciones de Estado
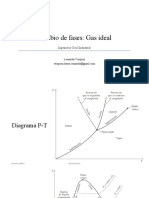
Ecuacin de estado de los Gases Ideales. Factor de compresibilidad y correlaciones. Ecuaciones Cbicas: Evolucin de la EOS de van der Waals: Compuestos puros. Funciones alfa y factor acntrico. Densidades de lquidos *. PSAT de substancias polares *. SRK (Soave-Redlich-Kwong). PR (Peng-Robinson). PRSV y t-PR (Pneloux) *. Funciones alfa (I) y (II) *. Otras ecuaciones de estado: Ecuacin del Virial. BWR (Benedict-Webb-Rubin) *. Lee-Kesler *. Reglas de mezcla: Reglas clsicas. Parmetros de interaccin binaria. Reglas EoS-GEX *. Aplicabilidad de las EoS:
* En el tema adicional 2b
Adecuacin de EoS. Regiones crticas *.
Termodinmica Aplicada 2005/06
p.1
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
GAS IDEAL
Solo describe el comportamiento V , no L ni L+V : una sola raiz en V (P = RT/V) Ms empleada, y con mejores resultados de lo que puede parecer para: Condiciones ambiente Puros y mezclas Ligeros: Aire, N2, O2, H2, He, CO2 (error< 1%) Ecuacin del virial sin trminos de interaccin molecular
Boyle + Gay-Lussac
pV = RT
Factor de compresibilidad Z=1 Precisin: Hasta algunos bar; ms precisa cuanto ms lejos de la linea de saturacin. Agua P <0.1 bar P. Crtico error < 0.1 % error ~ 100 % Comportamiento de gas real con P 0
Termodinmica Aplicada 2005/06
p.2
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
FACTOR DE COMPRESIBILIDAD
Medida de la desviacin del comportamiento de Gas Ideal. Z = PV/RT VREAL/VIDEAL Estudio de las desviaciones Correlacin con TR y PR
Ley de los estados correspondientes (2 parmetros): Todos los gases se comportan de igual manera en las mismas condiciones reducidas.
Termodinmica Aplicada 2005/06
p.3
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
Gas Ideal para: PR<<1 (Presiones muy bajas) TR > 2 (Temp. muy altas excepto PR>>1) Desviaciones mximas cerca del Punto Crtico
Termodinmica Aplicada 2005/06 p.4
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
CORRELACIONES GENERALIZADAS PARA Z (1)
Z=
pV RT
V =Z
RT = ZV id p
Pitzer; Nelson y Obert; Lydersen Para fluidos simples.
Termodinmica Aplicada 2005/06
p.5
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
ECUACIONES CBICAS
Ecuaciones cbicas en el volumen [P=f(T,V,V2,V3) o Z=f(T,V,V2,V3)] : Las mas simples que pueden representar {L+V}. 3 raices del V para cada (P,T) : Dos raices significativas en la zona de dos fases. Una sola raiz significativa en las zonas monofsicas. No excesivamente costosas numricamente. Suficientemente precisas para el diseo (algunas). P Raices lquido y vapor van der Waals (1873) SRK (Soave-Redlich-Kwong , 1949, 1972) PR (Peng-Robinson , 1976) Mltiples derivaciones
Raiz no significativa V
Termodinmica Aplicada 2005/06 p.6
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
ECUACIN DE VAN DER WAALS
Modificacin G.I.
(1873, Nobel de Fsica en 1910) Parmetro de atraccin molecular
a p + 2 ( V b ) = RT V
Formas polinmicas:
RT 2 a ab V 3 b + V + V =0 p p p ap abp 2 bp Z3 + 1 Z 2 + Z =0 2 3 ( ) ( ) RT RT RT
Parmetro de repulsin o covolumen
T > TC 1 raiz real, 2 imag (gas) T < TC P 1 raiz real (l v), 2 imag P 3 raices reales (l + v)
Parmetros: en el punto crtico, inflexin horizontal:
2p p =0 = 2 V TC V TC
Forma reducida:
3 (3 Vr 1) = 8 Tr pr + V 2 r
27 R 2TC2 2 a = 3 pCVC = 64 pC V RTC 8 pCVC b = C = R= RG .I . 3 8 pC 3TC
Validez: - moderadamente bien gases no polares y mal cerca de saturacin. - solo aproximadamente {L+V} mal presin de saturacin (eq. entre fases). - mal cerca del P.C. Zc:[vdW:0375, HF:012, H2O:0229, HC027, G.Nobles:0286-0311]
Termodinmica Aplicada 2005/06 p.7
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
PRESIN DE VAPOR O DE SATURACIN
Mediante una ecuacin de estado (van der Waals) P
f Liq = f Vap Liq = Vap
Una raiz real
3 raices
Psat
ln = (Z 1)
p 0
dp p
V Coeficiente de fugacidad mediante la ec. de van der Waals:
ln = Z 1 b b b 2a a ln Z 1 = ln Z 1 V V V b RTV RTV
(Z
Liq
Liq ; Z Vap Vap
)
PInicial )
Procedimiento de clculo:
T , PInicial Z
Liq
;Z
Vap
Liq
Vap
Liq
Vap
PSig
Liq = PInicial Vap
hasta que
(P
Sig
Termodinmica Aplicada 2005/06
p.8
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
MEJORA DE LA PRESIN DE SATURACIN: FUNCIN ALFA
Improvement of the van der Waals Equation of State Se corrige a con un factor
p=
Soave, G., Chem. Eng. Sci. 39, pp 357-369, 1984
(T), dependiente de la temperatura:
27 R 2TC2 64 pC
Nomenclatura artculo: (T ) a(TR ) ; ac a(Tc )
(T ) ac RT V b V2
donde ac =
A partir de una serie de PSat conocidas en funcin de T:
T(K) 149,98 179,98 212,65 249,98 272,65 319,98 379,98
(T) TR P(bar) 0,3527 0,2318 E-5 1,7539 0,4233 0,3369 E-2 1,6348 0,5001 0,4834 E-1 1,5230 0,5879 0,3915 1,4091 0,6412 1,0136 1,3467 0,7525 4,5747 1,2280 0,8937 17,3888 1,0966 PSat para el n-butano
m 0,7987 0,7974 0,7995 0,8019 0,8054 0,8160 0,8635
Correlacionando los valores:
(T ) = 1 + m 1 TR
donde m = 0.8004 (a dim .)
))
Generalizando (para una amplia base de datos de presiones de saturacin):
(T ) = 1 + m 1 TR
))
m = 0.4998 + 1.5928 0.19563 2 + 0.025 3 donde factor acntrico de Pitzer
( vlida para 0 1 )
Aplicable (suficientemente precisa para diseo) a substancias no polares y poco polares.
Termodinmica Aplicada 2005/06 p.9
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
FACTOR ACNTRICO DE PITZER
(1955)
Z no es una funcin exclusiva de Tr y Pr ; es necesaria ms informacin.
= 1 log10 (PRSat )T
= 0.7
Medida de la acentricidad (no-esfericidad) de la molcula. Aporta informacin valiosa sobre condiciones de saturacin (equilibrio entre fases). Disponibilidad, determinacin experimental y clculo sencillos, pues: Para muchas substancias, Tr = 0.7 es prxima al punto normal de ebullicin. Para gases simples (Ar,Kr,..) (PR,SAT) Pitzer: Este tercer parmetro es necesario porque la fuerza intermolecular en molculas complejas es la suma de las interacciones entre las diferentes partes de las molculas no solo entre sus centros- de ah que se sugiera el nombre de factor acntrico. Ley de los estados correspondientes (3 parmetros): Todos los gases que presenten el mismo factor acntrico se comportan de igual manera en las mismas condiciones reducidas.
Termodinmica Aplicada 2005/06 p.10
Tr =0.7
= 0.1
=0
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
REDLICH-KWONG (RK)
a V b ) = RT p+ 1/ 2 ( V (V + b)T
3
SOAVE-REDLICH-KWONG (SRK)
a p + V (V + b ) (V b) = RT RT V3 p R 2TC2 a = 0.427480 Pc RTc b = 0.086640 Pc
R 2TC2.5 a 0.427480 = Pc b = 0.086640 RTc Pc
RT 2 a / T 1/ 2 bRT pb 2 ab V =0 V V + p pT 1/ 2 p pr ap A = R 2T 2.5 = 0.427480 T 2.5 r Z 3 Z 2 + ( A B B 2 ) Z AB = 0 p bp B = = 0.086640 r RT Tr
2 a bRT pb 2 ab V =0 V + p p
Z 3 Z 2 + A B B 2 Z AB = 0
= 1 + m( ) (1 Tr1 / 2 )
PENG-ROBINSON (PR)
a (V b ) = RT + p V (V + b ) + b(V b ) 2 2 R TC RTc a = 0.45724 b = 0.07780 Pc Pc m( ) = 0.37464 + 1.54226 0.26992 2
Hidrgeno = 1.202 exp( 0.30288Tr )
m( ) = 0.48508 + 1.55171 0.15613 2
pr A = 0.427480 T 2 r B = 0.086640 pr Tr
Z 3 (1 B ) Z 2 + ( A 3B 2 2 B ) Z ( AB B 2 B 3 ) = 0 A = 0.45724 B = 0.07780
pr
Tr2 pr Tr
= 1 + m( ) (1 Tr1 / 2 )
Representan muy bien la fase vapor y aceptablemente la lquida.
Termodinmica Aplicada 2005/06 p.11
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
FUNCIONES ALFA (I)
f(T,); introducida por Soave para SRK; usada por PR. Mejora la correlacin de la presiones de vapor de puros
(T , ) = 1 + m( ) (1 Tr1 / 2 )
PR original:
m( ) = 0.37464 + 1.54226 0.26992 2
SRK original:
m( ) = 0.48508 + 1.55171 0.15613 2 , Hidrgeno = 1.202 exp( 0.30288Tr )
Para las ecuaciones t-PR, PRSV, PR-BM, RKS-BM y SR Vase Tema 2b.
Termodinmica Aplicada 2005/06
p.12
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
ECUACIN DEL VIRIAL
Deducible mediante la mecnica estadstica
Z = pV B C D = 1 + + 2 + 3 + � = 1 + B' P + C' P 2 + D' 3 + � RT V V V ,,
B' = B RT ,, C' = C B2 ( RT )2
B,C dependen slo de T y la naturaleza de la substancia (para puros). B,B segundos coef. del virial. Interaccin de 2 molculas, C,C terceros 3 molculas ... Se usa truncada:
Z =
pV B BP = 1+ = 1+ RT V RT
(slo fase gas-vapor, no 3 raices)
Con B experimentales (abundantes compilaciones) o predichos: No polares Correlacin de Abbot:
RTC B= P C (0 ) ( 1) B + B
Polares Correlacin de Hayden-OConell: B = f(PC,TC, momento dipolar, radio de giro) Representa la asociacin qumica en fase vapor Truncada tras B: vlida para P
0.422 (0 ) = 0.0832 1.6 B TR B( 1) = 0.139 0.172 TR4.2
P T PC = TR C ,, tras C: hasta 50 bar , T<TC 2 TC 2
Reglas de mezcla exactas muy usada para diseo de destilacin y absorcin a bajas P.
Termodinmica Aplicada 2005/06
p.13
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
REGLAS DE MEZCLA CLSICAS
Reglas de combinacin : ai , a j aij , a ji ; bi , b j bij , b ji Reglas de mezcla :
n n
aij , a ji a ; bij , b ji b
n
Reglas de Kay (pseudocomponente, 2 versiones):
PC = yi PCi ; TC = yi TCi ; = yi i
i =1 i =1 i =1
PC =
Z c RTC ; Z C , TC yVC Kay VC
Ecuacin del Virial:
B=
y y B
i j i j
ij
Bii = Bi Bij = B ji
Coeficientes cruzados
Ecuciones Cbicas:
a= b=
x x a
i j i j
ij
,,
aii = ai ,,
,,
aij =
ai a j + b j ) = 2
x i x j bij = bij = b ji i j Volumen trasladado t =
Termodinmica Aplicada 2005/06
bij =
i i
(b
xb
i i
xt
i
p.14
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
PARMETROS DE INTERACCIN BINARIA (PIB)
1PVDW: Coeficientes cruzados mejorados
aij = (1 kij ) ai a j a=
Parametro de Interaccin Binaria
ij
x x (1 k )
i j i j
ai a j
2PVDW: 2 parmetros ajustables:
kij = K ij xi + K ji x j
SR (Schwartzentruber-Renon) y otras. Dependencia importante de la T => no se puede extrapolar con confianza. (Mathias-Klotz:) el ajuste multipropiedad (Psat, h, Cp) mejora grandemente la precisin de las EoS; especialmente cuando se va a usar para calcular simultneamente varias propiedades. Ajuste de parmetros: en general, minimizacin con funciones objetivo compuestas.
Termodinmica Aplicada 2005/06
p.15
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
PARMETROS DE INTERACCIN BINARIA (APLICACIN I)
1PVDW : Bien para slo hidrocarburos Regular para gases inorgnicos. C1+C4 CO2+C3
Comparado con VDW1Fluid (sin PIBs)
Termodinmica Aplicada 2005/06
p.16
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
PARMETROS DE INTERACCIN BINARIA (APLICACIN II)
1PVDW: ... Inutilizable en desviaciones importantes (alcohol-alcano). C5+EtOH C3+MeOH H2O+2-C3OH
PIB ajustado para cada T
Falso split
Falso split
Termodinmica Aplicada 2005/06
p.17
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
PARMETROS DE INTERACCIN BINARIA (APLICACIN III)
2PVDW: Mejor, pero dependencia importante de la T. C5+EtOH C3+MeOH H2O+2-C3OH
Sigue mostrando falso split PIB ajustado para cada T 2PVDW (
Termodinmica Aplicada 2005/06
Desaparece falso split )
p.18
) y 1PVDW(
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
APLICABILIDAD DE EoS
Utilizables en la actualidad para: Clculo de propiedades volumtricas y termodinmicas de compuestos puros y todo tipo de mezclas, a excepcin de las que se asocian. Localizacin de fases: escisiones lquidos, slidos, supercrticos (G-G). Todo tipo de equilibrio VLE, LLE, GLE, VLLE, SLE, an con fuertes desviaciones de la idealidad. Problemas (y reas de desarrollo): Componentes asociados/reactivos. Temperaturas sub-ambientales y criognicas. Regiones crticas. Consistencia en amplios intervalos (sub y supercrticos): CrossOver. Consistencia en propiedades volumtricas y termodinmicas . Ausencia de datos experimentales (ms correlacin que prediccin en el sentido EoS). Reglas de mezcla, en especial para mezclas (cond+supercrit) y polmeros. Cbicas (las ms frecuentemente utilizadas): SRK PR (y variedades) aproximadamente iguales. Mayor diferencia en funciones alfa y reglas de mezcla. Parmetros de interaccin binaria (1 2) ajustados para la tarea concreta. Tendencias mecnica estadstica (SAFT) o derivados de PHCT (Pertub.Hard.Chain.Theory): SAFT: correlacin de densidades lquidas y PSAT aprox. 1'5% error.
Termodinmica Aplicada 2005/06 p.19
Ingeniera Qumica - Univ. Valladolid
Tema 2 - Ecuaciones de Estado
ADECUACIN DE EoS
Cbicas: SRK mejor (un poco) en general. PR mejor mezclas HC (Ind. petrolfera). Mejor en las regiones crticas (PRSV). Funciones alfa: Boston-Mathias para T>Tc . Mathias-Copeman para PSAT con mucha curvatura. SR para amplio intervalo de uso. BWR: Si hay parmetros, y se requiere precisin. Sistemas criognicos.(Tambin PRSV2). LKP: no polares y se requiere precisin en entalpas/entropas. Alta presin: No polares (Ind. petrolfera) Buena representacin PSAT de los puros esencial. PIB esenciales. Sistemas agua-HC: SRK y PR, ajustando aii para PSAT del agua. Mejores resultados PR, sobre todo para K-values y solubilidad de agua en la fase HC (mejor que al revs). Polares: Reglas EoS-GEX, sobre todo Michelsen (admite supercrticos).
Termodinmica Aplicada 2005/06 p.20
You might also like
- 2 Ecuaciones de EstadoDocument20 pages2 Ecuaciones de EstadoSergiosanchez0712No ratings yet
- Termo TablasDocument19 pagesTermo TablasIvan galarza avilaNo ratings yet
- 05-Clase Termo - Gases Reales Correlaciones y Tablas de Vapor 201027Document56 pages05-Clase Termo - Gases Reales Correlaciones y Tablas de Vapor 201027Carlos SandovalNo ratings yet
- Presentacion de Ecuaciones-De-EstadoDocument14 pagesPresentacion de Ecuaciones-De-EstadoDamiano PantaleoNo ratings yet
- Ecuaciones de Estado Cúbicas v2Document2 pagesEcuaciones de Estado Cúbicas v2CARLOTA MORALES LEÓNNo ratings yet
- Ecuaciones de Estado y Factores CruzadosDocument21 pagesEcuaciones de Estado y Factores CruzadosJosé Luis LMNo ratings yet
- Integración IV: Propiedades termodinámicasDocument73 pagesIntegración IV: Propiedades termodinámicasZule GalvánNo ratings yet
- Comportamiento PVT de los gases reales y desviaciones de la idealidadDocument30 pagesComportamiento PVT de los gases reales y desviaciones de la idealidadSteven Azañedo AranaNo ratings yet
- Semana 3Document20 pagesSemana 3Leonardo Lozano CallacaNo ratings yet
- Clase I - Segunda ParteDocument28 pagesClase I - Segunda ParteJuan Manuel AldereteNo ratings yet
- Clase Nc2ba011Document15 pagesClase Nc2ba011Gabriel BustosNo ratings yet
- 03 CaracterizacionDocument53 pages03 CaracterizacionDavid Guzman BlancoNo ratings yet
- 1.2 Gases RealesDocument36 pages1.2 Gases RealesElizabeth Vivar RojasNo ratings yet
- Term II Clase 2 2017Document28 pagesTerm II Clase 2 2017Cid Lord ChocoNo ratings yet
- Mezcla gases reales fisicoquímica ingeniería alimentosDocument34 pagesMezcla gases reales fisicoquímica ingeniería alimentosjose zeaNo ratings yet
- 1.2 Gases RealesDocument55 pages1.2 Gases RealesLuis CONDORI SOTO100% (1)
- Ecuaciones de EstadoDocument34 pagesEcuaciones de Estadomariacamy07No ratings yet
- Termo Clase 5Document21 pagesTermo Clase 5carlaytbpremium carlaNo ratings yet
- Termo 4 - EOS, PRIMERA LEY Y PROPIEDADESDocument65 pagesTermo 4 - EOS, PRIMERA LEY Y PROPIEDADESMiguel Angel Rubiano GuevaraNo ratings yet
- Clase 1 Unidad 3Document15 pagesClase 1 Unidad 3Liga ChilenaNo ratings yet
- 1.2 Gases Reales - AnotacionesDocument39 pages1.2 Gases Reales - AnotacionesBea EgNo ratings yet
- Equilibrio Entre FasesDocument40 pagesEquilibrio Entre Fasesraymon6666No ratings yet
- Semana 6 - Transferencia de Masa y ADocument60 pagesSemana 6 - Transferencia de Masa y ABrisa J. Rojas GutierrezNo ratings yet
- Formulario Limpio PDFDocument22 pagesFormulario Limpio PDFVidal TxusNo ratings yet
- PRESENTACION PROPIEDADES DE LOS GASES PresentaciónDocument21 pagesPRESENTACION PROPIEDADES DE LOS GASES PresentaciónCarmelo HernandezNo ratings yet
- Separata de Gases RealesDocument6 pagesSeparata de Gases Realesluis DQNo ratings yet
- Gases Reales-Fuerzas Intermoleculares PDFDocument34 pagesGases Reales-Fuerzas Intermoleculares PDFdamiánNo ratings yet
- Termodinámica gases realesDocument21 pagesTermodinámica gases realesJEFFERSON FERNANDO ESTRADA ALCOSERNo ratings yet
- Presentación de PowerPointDocument29 pagesPresentación de PowerPointSicomoseaRamiresNo ratings yet
- Universidad Nacional Autónoma de MéxicoDocument2 pagesUniversidad Nacional Autónoma de MéxicoFERNo ratings yet
- Ecuaciones de estado para gases ideales y realesDocument52 pagesEcuaciones de estado para gases ideales y realesVicente RiffoNo ratings yet
- Sección 04Document11 pagesSección 04AlejandroCalleRuizNo ratings yet
- Tema 2 - 2Document32 pagesTema 2 - 2Norberto IglesiasNo ratings yet
- 15-Estado GaseosoDocument12 pages15-Estado Gaseosoblas.snblasNo ratings yet
- Gases Reales - USILDocument29 pagesGases Reales - USILjoseNo ratings yet
- Q - R5 - Cinética Química - Equilibrio Químico - ElectroquímicaDocument7 pagesQ - R5 - Cinética Química - Equilibrio Químico - Electroquímicamaria fernanda gonzales cabreraNo ratings yet
- Archivo 2021711204941Document15 pagesArchivo 2021711204941Yeliver RamónNo ratings yet
- 3 GasesDocument21 pages3 GasesLEINER GAMBOA VALDEZNo ratings yet
- Gases Reales-Ec Van Der WaalsDocument27 pagesGases Reales-Ec Van Der WaalsVanessa TrujilloNo ratings yet
- T 3 A. Gases RealesDocument27 pagesT 3 A. Gases RealesTatiana ZorrillaNo ratings yet
- SESION 2 - UCV - PDF - VDocument57 pagesSESION 2 - UCV - PDF - V5F Barraza ArianaNo ratings yet
- Clase 1 - Gases RealesDocument27 pagesClase 1 - Gases RealesAlen NievesNo ratings yet
- Gases RealesDocument17 pagesGases RealesGustavo Espinoza Rivera100% (2)
- Practica N°1 - Ley de Boyle 22Document14 pagesPractica N°1 - Ley de Boyle 22Max BarzolaNo ratings yet
- Marco - Normativo.legal - Uncp Reglamento - AcademicoDocument62 pagesMarco - Normativo.legal - Uncp Reglamento - AcademicoSaul QUISPE VARGASNo ratings yet
- Capitulo1 PDFDocument121 pagesCapitulo1 PDFariel edison duran limaNo ratings yet
- 053 BCD 2018 II Gas Ideal RealDocument61 pages053 BCD 2018 II Gas Ideal RealJasmin Yanina Solis SantiagoNo ratings yet
- Ecuaciones de estado para gases ideales y realesDocument63 pagesEcuaciones de estado para gases ideales y realesCallejas Palominos Eduardo0% (1)
- Archivo Ecuaciones de Estado para Gases Ideales RealesDocument7 pagesArchivo Ecuaciones de Estado para Gases Ideales RealesSez BvNo ratings yet
- EOS (Ecuaciones de EstadoDocument38 pagesEOS (Ecuaciones de EstadoJussef Fuentes QuinteroNo ratings yet
- Ecuación de estado Redlich-Kwong para CO2Document9 pagesEcuación de estado Redlich-Kwong para CO2FERNANDA JESUS YANEZ ERIZANo ratings yet
- Gases Reales2Document42 pagesGases Reales2Iván Zelaya HuertaNo ratings yet
- CCEE - Tema 7 - GasesDocument24 pagesCCEE - Tema 7 - GasesDavid GarcíaNo ratings yet
- Ingeniería química. Soluciones a los problemas del tomo IFrom EverandIngeniería química. Soluciones a los problemas del tomo INo ratings yet
- Termodinámica clásica. Protocolos experimentales sobre primera y segunda leyes, y sobre potenciales selectosFrom EverandTermodinámica clásica. Protocolos experimentales sobre primera y segunda leyes, y sobre potenciales selectosNo ratings yet
- Construcción de Modelos Estáticos 3D de Yacimientos de HidrocarburosDocument1 pageConstrucción de Modelos Estáticos 3D de Yacimientos de HidrocarburosEuler CauchiNo ratings yet
- Formation Damage TOPDocument177 pagesFormation Damage TOPAntonio Subero RuizNo ratings yet
- Capitulo 1... Flujo de FluidosDocument40 pagesCapitulo 1... Flujo de FluidosHamilton Morales MirandaNo ratings yet
- Diagnostico Peru 1990 2000Document59 pagesDiagnostico Peru 1990 2000Jazmine Zoar Panaifo VillafanaNo ratings yet
- Modelo kárstico GorbeaDocument29 pagesModelo kárstico GorbeaEuler CauchiNo ratings yet
- Modelo Sedimentologico 2008Document10 pagesModelo Sedimentologico 2008Euler CauchiNo ratings yet
- Verbos para Proyectos de InvestigaciónDocument3 pagesVerbos para Proyectos de Investigaciónisanico90% (146)
- TUTORIAL Cómo Importar Una Biblia A E-Sword Usando Biblos, 1.Document8 pagesTUTORIAL Cómo Importar Una Biblia A E-Sword Usando Biblos, 1.Euler CauchiNo ratings yet
- Estimacion de ViscosidadesDocument25 pagesEstimacion de ViscosidadesAlejandro Briceño57% (7)
- Tabla Pesos y MedidasDocument1 pageTabla Pesos y MedidasEuler CauchiNo ratings yet
- Importancia de La Anisotropia en La Caracterizacion de Yacimientos de Hidrocarburos y en La Optimizacion Del Recobro FinalDocument130 pagesImportancia de La Anisotropia en La Caracterizacion de Yacimientos de Hidrocarburos y en La Optimizacion Del Recobro FinalEuler CauchiNo ratings yet
- Inversión en Infraestructura Del TransporteDocument19 pagesInversión en Infraestructura Del TransporteEuler CauchiNo ratings yet
- Situación Del Mercado Laboral en Lima Metropolitana: Resumen EjecutivoDocument51 pagesSituación Del Mercado Laboral en Lima Metropolitana: Resumen EjecutivoPablo MateusNo ratings yet
- Ecuaciones de EstadoDocument13 pagesEcuaciones de EstadoEuler CauchiNo ratings yet
- TEMA2 - Ecuaciones de EstadoDocument13 pagesTEMA2 - Ecuaciones de Estadorey-gMNo ratings yet
- Elam - Filacion, Nombre, CaracteresDocument13 pagesElam - Filacion, Nombre, CaracteresMilton Teodosio Ramirez MolinaresNo ratings yet
- Gas Natural GeneralidadesDocument12 pagesGas Natural GeneralidadesEuler CauchiNo ratings yet
- Caracterizacion de YacimientoDocument20 pagesCaracterizacion de Yacimientosimonramos23100% (3)
- Tabla de Vapor Del AntoineDocument2 pagesTabla de Vapor Del Antoineldpt9467% (3)
- Definiciones de ProyectoDocument3 pagesDefiniciones de ProyectoEuler CauchiNo ratings yet
- Imbibicion y DrenajeDocument17 pagesImbibicion y DrenajeJonathan Guano100% (3)
- ANTOINEDocument3 pagesANTOINEEuler CauchiNo ratings yet
- Tabla de Vapor Del AntoineDocument2 pagesTabla de Vapor Del Antoineldpt9467% (3)
- Trin7es DesbloqueadoDocument15 pagesTrin7es DesbloqueadoAngel ChávezNo ratings yet
- Campos Maduros Ypf2Document14 pagesCampos Maduros Ypf2contradictorio_alexNo ratings yet
- Gas Natural GeneralidadesDocument12 pagesGas Natural GeneralidadesEuler CauchiNo ratings yet
- Campos Maduros Ypf2Document14 pagesCampos Maduros Ypf2contradictorio_alexNo ratings yet
- Use of Pressure Transient TestingDocument130 pagesUse of Pressure Transient TestingYarisol Rivera ChàvezNo ratings yet
- Importancia de La Anisotropia en La Caracterizacion de Yacimientos de Hidrocarburos y en La Optimizacion Del Recobro FinalDocument130 pagesImportancia de La Anisotropia en La Caracterizacion de Yacimientos de Hidrocarburos y en La Optimizacion Del Recobro FinalEuler CauchiNo ratings yet
- Propiedades Areologicas Del Fluido PDFDocument30 pagesPropiedades Areologicas Del Fluido PDFnoeNo ratings yet
- 1er Lab de Mec de FluidosDocument7 pages1er Lab de Mec de FluidosHernán LAQUI MAMANINo ratings yet
- Tablas TD1 P2019Document56 pagesTablas TD1 P2019Alvaro AguileraNo ratings yet
- Adobe Scan 22 Nov. 2022Document25 pagesAdobe Scan 22 Nov. 2022mike2.0wasNo ratings yet
- Metereologia General - Tema 4 - Análisis de Presión AtmosféricaDocument23 pagesMetereologia General - Tema 4 - Análisis de Presión AtmosféricaRafael Alejandro Herrera HerreraNo ratings yet
- Tabla - Leyes de Los GasesDocument3 pagesTabla - Leyes de Los GasesAlexandra MarleneNo ratings yet
- Termo Ejer U2Document3 pagesTermo Ejer U2Bryan CorreaNo ratings yet
- Pseudo PresionnnDocument10 pagesPseudo PresionnnaitaNo ratings yet
- Vallejos Chavez Bani Susi - Solucionario Primera EvaluaciónDocument4 pagesVallejos Chavez Bani Susi - Solucionario Primera EvaluaciónEdison Marcial Aliaga LozanoNo ratings yet
- Perdidas por fricción en tuberíasDocument10 pagesPerdidas por fricción en tuberíasDiego TorresNo ratings yet
- Ejercicios de las leyes de los gases y clasificación de compresoresDocument5 pagesEjercicios de las leyes de los gases y clasificación de compresoresCristhian Mucha Fabian100% (1)
- Propiedades de La Sustancia Pura y Diagrama, Gas Ideal, Análisis de Masa y EnergíaDocument9 pagesPropiedades de La Sustancia Pura y Diagrama, Gas Ideal, Análisis de Masa y EnergíaJhony Alfonso Atiaga VelasteguiNo ratings yet
- Métodos Licuefacción de GasesDocument5 pagesMétodos Licuefacción de GasesDavidNarvaezNo ratings yet
- 1 Serie de ProblemasDocument2 pages1 Serie de Problemaspollo_10No ratings yet
- Práctica de Laboratorio No. 6 - VirtualDocument14 pagesPráctica de Laboratorio No. 6 - VirtualJulian AndrewNo ratings yet
- Memoria de CalculoDocument8 pagesMemoria de CalculoRolin PazNo ratings yet
- Informe Química - GasesDocument14 pagesInforme Química - GasesDieloz Sanchez0% (1)
- Estado GaseosoDocument15 pagesEstado GaseosojoseNo ratings yet
- Documento 179Document3 pagesDocumento 179Oscar Palacios HuicocheaNo ratings yet
- Mezcla de Gases IdealesDocument21 pagesMezcla de Gases IdealesGiovanni RodriguezNo ratings yet
- Propiedades Del Gas NaturalDocument60 pagesPropiedades Del Gas NaturalHoracio RodriguezNo ratings yet
- Química General: Gases IdealesDocument4 pagesQuímica General: Gases IdealesEmiliano PicconiNo ratings yet
- Ley de Dalton de Las Presiones ParcialesDocument2 pagesLey de Dalton de Las Presiones ParcialesPedro Casullo100% (2)
- Flujo de FluidosDocument21 pagesFlujo de FluidosoriannyNo ratings yet
- Calor LatenteDocument9 pagesCalor LatenteEvelyn Calderón MartínezNo ratings yet
- Bitacora 3 PmoDocument1 pageBitacora 3 PmoPamela MuñozNo ratings yet
- Anexo 1 - Tarea 3Document15 pagesAnexo 1 - Tarea 3yeimy bautistaNo ratings yet
- Reacción de Sodio Metálico Con AguaDocument8 pagesReacción de Sodio Metálico Con AguaCristhian GutierrezNo ratings yet
- Tema 2 Fisica y Quimica Santillana 3ºesoDocument14 pagesTema 2 Fisica y Quimica Santillana 3ºesosenecamovil50% (4)
- Guia de Demostracion de CavitacionDocument5 pagesGuia de Demostracion de CavitacionTomy Yannick QcNo ratings yet