Professional Documents
Culture Documents
Arderea Combustibililor Cap 9
Uploaded by
Ionescu FlorinOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Arderea Combustibililor Cap 9
Uploaded by
Ionescu FlorinCopyright:
Available Formats
BTT II, cap 9, Arderea Combustibililor
CAP. 9 ARDEREA COMBUSTIBILILOR
(SINTEZA)
Procedeele utilizate pentru obinerea cldurii prin metode convenionale se bazeaz, n
principal, pe transformarea energiei legate chimic de combustibili n energie termic. Dintre
combustibili cel mai des se folosesc crbunii, hidrocarburile lichide obinute din petrol i gaze
combustibile care pot fi: gaze naturale, gaze de sonda sau gaze obinute n urma unor procese
tehnologice (exemplu gazul de furnal, gazul de apa, etc.). Biomasa solid se trateaz ca un
combustibil solid. Biocombustibili obinui din diverse plante care sunt de tip alcooli sau
uleiuri se tratez ca i ceilali combustbili lichizi.
Transformarea energiei chimice n cldura, denumit i ardere sau proces de combustie,
are loc n urma reaciilor exoterme de oxidare rapid a elementlor oxidabile coninute n
combustibil.
Arderea se studiaza din doua puncte de vedere: termodinamic i cinetic.
Din punct de vedere termodinamic, procesul de ardere este tratat global, n sensul
evalurii energiei reactanilor i a produselor finale, fr a se lua n considerare mecanismul
cinetic i produsele intermediare de ardere. Purttorul de energie termic rezultat n urma
procesului de ardere este constituit din gazele de ardere evacuate la o temperatur care
depinde de natura combustibilului, perfeciunea procesului i modul de desfurare a arderii.
Din punct de vedere cinetic, procesul de ardere pune n evidenta mecanismul polistadial
de realizare a procesului i rolul radicalilor activi n propagarea frontului de flacara.
8.1. Compoziia combustibililor
Compoziia combustibililor pune n eviden elementele care iau parte la procesul de
ardere i care formeaza masa combustibila i elementele care nu iau parte la acest proces care
formeaza balastul. Compoziia combustibililor este dat prin analiza chimica elementar
definit fie prin elementele primare, fie prin compuii stabili care-i alcatuiesc.
n cazul combustibililor solizi i lichizi analiza chimic elementar se exprim prin
participaia masica a elementelor primare, fie procentual fie raportat la 1 kg de combustibil.
n general, elementele chimice din care este format un combustibil solid sau lichid sunt:
carbonul C, hidrogenul H, sulful S, azotul N, oxigenul O, umiditatea W; precum i cenua A.
n cazul n care participaia elementelor este dat procentual, analiza chimica elementar a
combustibilului este:
C + H + S + N + O + W + A = 100 [%] (9.1)
n cazul n care participaia masic a componenilor este raportat la 1 kg de combustibil,
simbolurile lor se scriu cu litere mici:
c + h + s + n + o + w + a = 1 kg comb. (9.2)
La combustibilii gazoi analiza elementar indic participaiile volumice procentuale
raportate la 1 m
3
N
de combustibil gazos. Un combustibil gazos este format n principal din:
hidrogen H
2
, oxid de carbon CO, metan CH
4
, hidrocarburi detipul C
m
H
n
, oxigen O
2
, azot N
2
,
etc. Umiditatea combustibilului gazos este data separat i se exprima n kg/m
3
N
combustibil
gazos uscat. Aceasta umiditate se noteaza cu d [kg/m
3
N
cb.g.us]
n consecin, compoziia unui combustibil gazos la starea uscat exprimat n procente
volumice este:
Prof. Alex. Chisacof
an univ. 2007/2008
9 - 1
BTT II, cap 9, Arderea Combustibililor
H
2
+ CO + CH
4
+ C
m
H
n
+ H
2
S + O
2
+ CO
2
+ N
2
= 100 [%] (9.3)
respectiv n participaii volumice raportate la 1 m
3
N
de combustibil gazos (n acest caz
simbolurile elementelor se scriu cu litere mici), rezult:
h
4
+ c
m
h
n
+ h
2
s+ o
2
+ n
2
= 1 m
3
N
c. g. (9.4)
2
+ co + ch
Atunci cnd se ine seama i de umiditatea combustribilului, umiditatea d se nmulete
cu volumul specific al vaporilor de ap v
n
=1/
n
=22,414/18,016=1,244 m
3
N
/kg vap, iar pentru
umiditatea d exprimata n g/m
3
N
cb.g.us , participaia volumic de vapori de ap, raportat la
stare uscat este:
W = H
2
O = d 10
-3
v
N
100 = d 10
-3
1,244 100 = 0,1244 d [%] (9.5)
Prin adugarea acestui procent volumic la compoziia gazului combustibil dat de relaia
(9.3) se obine:
H
2
+ CO + CH
4
+ C
m
H
n
+ H
2
S + O
2
+ CO
2
+ N
2
+1,244d= 100 + 0,1244d
Compoziia corespunztoare a combustibilului gazos umed este:
H
2
um
+CO
um
+CH
4
um
+C
m
H
n
um
+H
2
S
um
+O
2
um
+CO
2
um
+N
2
um
+W
um
=100[%] (9.6)
Umiditatea raportat la starea umed este:
d ,
d , W
um
1244 0 100
100
1244 0
+
= [%] (9.7)
Determinarea componenilor combustibilului gazos raportai la starea umed se face prin
nmulirea participaiei procentuale volumice raportat la starea uscat, cu coeficientul K, dat
de expresia:
d 0,1244 100
100
K
+
= (9.8)
Deci, se obine: H
2
um
= KH
2
, CO
2
um
=KCO
2
, etc, sau H
2
um
= KH
2
, CO
2
um
=KCO
2
etc,
pentru cazul cnd raportarea participaiei volumice se face la 1 m
3
N
de combustibil gazos
umed.
La combustibilii solizi sau lichizi componenii care oxideaz (ard) sunt carbonul C,
hidrogenul H i sulful S, iar la combustibilii gazoi elementele combustibile sunt: hidrogenul
H
2
, oxidul de carbon CO, metanul CH
4
, hidrocarburile C
m
H
n
i hidrogenul sulfurat H
2
S.
8.2. Efectul termic al reaciilor chimice de ardere. Puterea calorific
Aplicarea primului principiu al termodinamicii la reaciile chimice permite aprecierea
efectului termic al unei reacii, iar pentru cazul desfasurarii lor la presiune constant, funcia
caracteristic a sistemului este entalpia de reacie
r
H. Daca se considera o reacie de forma:
1
A
1
+
2
A
2
+ ...
1
A
1
+
2
A
2
+ ... (9.9)
Prof. Alex. Chisacof
an univ. 2007/2008
9 - 2
BTT II, cap 9, Arderea Combustibililor
unde
1
,
2
... ,
1
,
2
... reprezint coeficienii stoechiometrici ai componenilor ce intra n
reacie (reactanii A
1
, A
2
...), respectiv a produselor care rezult din reacie (A
1
, A
2
...).
Variaia de entalpie, numit i entalpie de reacie, este dat de diferena ntre suma
entalpiilor produselor de reacie i suma entaliilor reactanilor, toate msurate la aceeai
presiune i temperatur, i are expresia:
(9.10)
reactanti
produsi
|
|
.
|
\
|
|
.
|
\
|
=
j
r
j
j
'
i
r
i
'
i
r
H H H
n care
r
H
i
i
r
H
j
sunt entalpiile de reacie ale produilor de reacie, respectiv a reactanilor
care intr n reacie. Starea standard de referin pentru calculul entalpiei de reacie este
presiunea atmosferica (760 mmHg) i temperatura de 25C (293,15 K).
Reaciile chimice se pot desfura fie cu absorbie de cldur, aa cum este cazul
reaciilor endoterme (
r
H>0), fie cu degajare de cldur, cazul reaciilor exoterme (
r
H<0).
Puterea calorificreprezinta cldura care o degaj la arderea complet a unitii de
cantitate de combustibil n condiii normale (standard). n cazul combustibililor solizi i
lichizi puterea calorifica se exprim n kJ/kg, iar pentru combustibilii gazosi n kJ/m
3
N
.
n gazele rezultate n urma arderii se gasesc vapori de apa provenii din oxidarea
hidrogenului, a hidrogenului sulfurat i a hidrocarburilor precum i din umiditatea de
compoziie a combustibilului sau a aerului necesar arderii. Datorit temperaturii ridicate la
care se evacueaza gazele, umiditatea se afla n stare gazoas (vapori). Pentru vaporizare s-a
consumat o parte din cldura de reacie. n funcie de starea de agregare la care se evcueaz
umiditatea se deosebesc doua tipuri de putere calorific:
- putere calorific superioara (Q
s
sau H
s
), determinat pentru cazul n care apa din
compoziia iniial a combustibilui, precum i apa format prin reacie este evacuat n
stare lichid, n kJ/kg sau kJ/m
3
N
;
- putere calorifica inferioar (Q
i
sau H
i
), determinat pentru cazul n care apa din
compoziia iniial a combustibilui, precum i apa format prin reacie este evacuat n
stare lichida stare de vapori, n kJ/kg sau kJ/m
3
N
.
Relaia dintre cele dou tipuri de puteri calorifice este:
(
|
.
|
\
|
+ =
kg
kJ
W H
Q Q
s i
100 100
9 2510 (9.11)
(
|
.
|
\
|
+ =
kg
kJ
W H
H H
s i
100 100
9 2510 (9.11)
n care 2510 kJ/kg vap reprezint cldura de vaporizare a apei la presiunea punctului
triplu, iar
100 100
9
W H
+ reprezint cantitatea de ap provenit din oxidarea hidrogenului i din
umiditatea combustibilului, n kJ/kg.
Puterea calorifica a combustibilului este data de suma cldurii degajate n urma oxidrii
componenilor combustibili. La hidrogen se face ipoteza ca oxigenul de constituie nu
participa la ardere, ci rmne legat cu o parte din hidrogenul din compoziie. Astfel, dac
combustibilul conine O/100 kg O
2
/kg
comb
cantitatea de hidrogen corespunztoare este
O/(8100) kg H
2
/kg
comb
, deci, cantitatea disponibil de hidrogen este:
100 8 100
O H
[kgH
2
/kg
comb
].
Prof. Alex. Chisacof
an univ. 2007/2008
9 - 3
BTT II, cap 9, Arderea Combustibililor
Tnnd seama de valorile cldurii de reacie pentru elementele combustibile, puterea
calorific inferioar a combustibililor solizi i lichizi se determin cu relaia:
(
+ |
.
|
\
|
+ = =
kg
kJ
100
2510
100
9250
8 100
1
120120
100
33900
W S O
H
C
Q H
i i
(9.12)
iar pentru combustibilii gazoi se utilizeaz relaia:
(
+ + + +
+ + + + = =
3
N
2 2 2 6 2
4 2 4 2
m
kJ
100
23400
100
56920
100
63730
100
60020
100
35910
100
10800
100
12720
S H
...
H C H C
H C CH H CO
Q H
i i
(9.13)
Atunci cand puterea calorica se raporteaza la combustibilul gazos umed puterea calorific
este:
( )
(
+
=
us . g . c m
kJ
51 2
1244 0 100
100
3
N
d , Q
d ,
Q
i
um
i
(9.14)
n cazul amestecurilor de combustibili, puterea calorific se stabilete n funcie de
participaia masic sau volumic astfel:
- pentru combustibilii solizi sau lichizi:
Q
i
= g
i
Q
i,i
[kJ/kg cb] (9.15)
- pentru combustibilii gazoi:
Q
i
= r
i
Q
i,i
[kJ/m
3
N
c.g.us] (9.16)
- pentru un amestec de combustibili lichizi, solizi i gazoi
Q
i
= Q
il,s
+ n Q
ig
[kJ/kg] (9.17)
n care : g
i
participaia masic a combustibilului i, n amestec, n %/100;
r
i
- participatia volumica a combustibilului i, n amestec, n %/100;
Q
i l,s
puterea calorica a combustibilului solid sau lichid, n kJ/kg;
Q
i g
puterea calorica a combustibilului gazos, n kJ/m
3
N
;
n cantitatea de combustibil gazos introdus pentru arderea unitii de cantitate de
combustibil lichid sau solid, n m
3
N
/kg
cb
.
8.3 Calculul arderii (oxidrii) combustibililor
Calculul arderii are ca scop determinare cantitaii de aer necesara desfurrii reaciilor
chimice de oxidare (ardere) precum i a volumului i compoziiei gazelor rezultate n urma
arderii. n continuare se va considera cazul aerului uscat (fr umiditatea x [kg
vap
/kg
a us
], de
obicei se ia x = 10 g
vap
/kg
a us
)
8.3.1. Arderea combustibililor solizi i lichizi
Prof. Alex. Chisacof
an univ. 2007/2008
9 - 4
BTT II, cap 9, Arderea Combustibililor
n cazul combustibililor solizi sau lichizi, compoziia lor este dat n procente masice.
Astfel 1 kg de combustibil se exprima sub forma:
kg comb kg umid
W
kg cenusa
A
kg O
O
kg N
N
kg S
S
kg H
H
kg C
C
1
100 100 100
100 100 100 100
2
2 2
= + + +
+ + + +
(9.18)
Elementele care formeaza masa combustibil sunt C, H, S, iar reaciile chimice de
oxidare sunt:
C - pentru carbon
C + O
2
= CO
2
1 kmol C + 1 kmol O
2
= 1 kmol CO
2
12 kg C + 22,414 m
3
N
O
2
= 22,414 m
3
N
CO
2
2
3
2
3
12
414 22
12
414 22
CO m
,
O m
,
kg C
N N
= + 1
iar pentru
100
C
kg C rezult:
2
3
2
3
12
414 22
100 12
414 22
100 100
CO m
, C
O m
,
C
kg C
C
N N
= +
- la arderea hidrogenului H:
H
2
+
2
1
O
2
= H
2
O
1 kmol H
2
+
2
1
kmol O
2
= 1 kmol H
2
O
vap
2 kg H
2
+
2
414 , 22
m
3
N
O
2
= 22,414 m
3
N
H
2
O
vap
vap N N
O H m
,
O m
,
kg H
2
3
2
3
2
2
414 22
4
414 22
= + 1
iar pentru
100
H
kg H
2
rezult:
vap N N
O H m
, H
O m
,
H
kg H
H
2
3
2
3
2
2
414 22
100 4
414 22
100 100
= + (9.20)
- la arderea sulfului S
S + O
2
= SO
2
1 kmol S + 1 kmol O
2
= 1 kmol SO
2
Prof. Alex. Chisacof
an univ. 2007/2008
9 - 5
BTT II, cap 9, Arderea Combustibililor
32 kg S + 22,414 m
3
N
O
2
= 22,414 m
3
N
SO
2
2
3
2
3
32
414 22
32
414 22
SO m
,
O m
,
kg S
N N
= + 1
iar pentru
100
S
kg S rezult:
2
3
2
3
32
414 22
100 32
414 22
100 100
SO m
, S
O m
,
S
kg S
S
N N
= + (9.21)
a) Aerul necesar arderii
Din reaciile de oxidare de mai sus, pentru arderea completa a unui kg de combustibil,
este necesara cantitatea de oxigen, dat de expresia:
| |
cb 2
3
N min 2
/kg O m
32 32 4 12 100
414 22
O S H C ,
O
,
(
+ + = (9.22)
sau
| |
cb 2
3
N min 2
/kg O m
32 4
8
12 100
414 22
2
S
O
H-
C ,
V O
o
O ,
(
(
(
(
+ + = = (9.22)
Oxigenul necesar arderii este luat, n majoritatea cazurilor, din aerul atmosferic. n aerul
uscat oxigenul reprezint 21% (participaie volumic sau molar), iar azotul 79% volumice. n
consecin, volumul de aer necesar arderii unui kg de combustibil este:
(
=
cb kg
us a m
21 0
3
N min 2 0
,
O
V
,
a
(9.23)
Arderea complet cu aerul minim necesar presupune realizarea unui amestec combustibil
omogen, lucru greu de realizat n instalaiile sau spaiile de combustie. Pentru asigurarea unui
proces complet de ardere se introduce o cantitate de aer mai mare dect cantitatea teoretic.
Deci, cantitatea de aer real necesar arderii este:
(
= =
cb kg
aer m
3
N
V V ; V V
0
um a, um a,
0
a a
(9.24)
unde este coeficientul de exces de aer i are valori supraunitare. Funcie de natura
combustibilului, a tipului instalaiei sau a spaiului de ardere, pentru coeficientul de exces de
aer sunt recomandate urmtoarele valori orientative :
- pentru combustibili lichizi = 1,05 1,2
- pentru combustibili solizi = 1,05 1,4
- pentru combustibilii gazoi = 1,02 1,15
b) Compoziia i volumul gazelor rezultate din ardere
Prof. Alex. Chisacof
an univ. 2007/2008
9 - 6
BTT II, cap 9, Arderea Combustibililor
n urma arderii combustibilului se obin produsele de ardere sub forma de gaze de
ardere i cenu (stare solid). Gazele de ardere se obin din ecuaiile de ardere (9.19 8.21)
i ele sunt compuse din:
bioxid de carbon,
(
=
cb kg
CO m
100 12
414 , 22
2
3
N
2
C
V
CO
(9.25)
bioxid de sulf
(
=
cb kg
SO m
100 32
414 , 22
2
3
N
2
S
SO
V (9.26)
vapori de ap
W , H ,
V
O H
100 18
414 22
100 2
414 22
2
+ = (9.27)
azot
(
+ =
cb kg
N m
79 0
100 28
414 22
2
3
N 0 0
2
V ,
N ,
V
a N
(9.28)
aer n exces
( )
(
=
cb kg
aer m
1
3
N 0
V V
a
ex
a
(9.29)
Volumul teoretic de gaze de ardere uscate este:
(
+ + =
cb kg
us g m
3
N 0 0
2 2 2
V V V V
N SO CO g,us
(9.30)
Volumul teoretic de gaze arse umede:
(
+ = + + + =
cb kg
um g m
3
N 0 0 0
2 2 2 2 2
V V V V V V V
O H g,us O H N SO CO g
(9.31)
Volumul real de gaze de ardere uscate:
( )
(
+ = + =
cb kg
s u g m
1
3
N 0 0 0
V V V V V
ex
a g,us a g,us g,us
(9.32)
Volumul real de gaze de ardere la starea umed:
(
+ = + =
cb kg
um g m
1
3
N 0 0 0
)V ( V V V V
a g
ex
a g g
(9.33)
Acest volum de gaze de ardere se mai poate exprima i n funcie de compoziia
elementar a gazelor (obinut prin analiz):
Prof. Alex. Chisacof
an univ. 2007/2008
9 - 7
BTT II, cap 9, Arderea Combustibililor
(
+ + + + =
cb kg
um g m
3
N
2 2 2 2 2
V V V V V V
O H O N SO CO g
(9.34)
n care V
CO2
i V
SO2
au expresiile date anterior. Ceilali componeni devin:
( )
(
+ = + =
cb kg
N m
28
414 22
100
79 0 1 79 0
2
3
N 0 0 0
2 2
, N
V , V , V V
a a N N
(9.35)
( )
(
= =
kg cb
O m
V , V , V
N ex
a a O
2
3
0
21 0 1 21 0
2
(9.36)
(
=
cb kg
vap O H m
2
3
N 0
2 2
V V
O H O H
(9.37)
n acest caz volumul de gaze de ardere uscate este:
(
+ + + =
cb kg
s u g m
3
N
,
2 2 2 2
V V V V V
O N SO CO us g
(9.40)
8.3.2. Arderea combustibililor gazoi
n cazul combustibililor gazoi compoziia este dat n procente volumice. Astfel 1 m
3
N
de combustibil gazos la starea uscat se exprima sub forma:
cb m N m
N
CO m
CO
O m
O
S H m
S H
H C m
H C
CH m
CH
CO m
CO
H m
H
N N N N
N n m N
n m
N N N
3
2
3 2
2
3 2
2
3 2
2
3 2 3
4
3 4 3
2
3 2
1
100 100 100
100 100 100 100 100
= + + +
+ + + + +
(9.41)
Elementele combustibile sunt H
2
, CO, CH
4
, C
m
H
n
, H
2
S, iar reaciile chimice de oxidare
sunt:
- arderea hidrogenului
H
2
+
2
1
O
2
= H
2
O (a)
1 kmol H
2
+
2
1
kmol O
2
= 1 kmol H
2
O (b)
22,414 m
3
N
H
2
+
2
414 , 22
m
3
N
O
2
= 22,414 m
3
N
H
2
O (c)
O H m
,
O m
,
H m
N N N 2
3
2
3
2
3
2
414 22
4
414 22
1 = + (d)
iar pentru cantitatea volumic de
100
2
H
m
3
N
H
2
rezult:
Prof. Alex. Chisacof
an univ. 2007/2008
9 - 8
BTT II, cap 9, Arderea Combustibililor
O H m
, H
O m
,
H
H m
H
N N N 2
3 2
2
3 2
2
3 2
2
414 22
100 4
414 22
100 100
= + (9.42)
Se constat c valorile coeficienilor stoichiometrici de la reacia chimic de oxidare (a)
se regsesesc la reacia cantitativ (d). n consecin, pentru ceilali componeni se vor utiliza
ecuaiile (a) i (d).
n mod similar se obin i ecuaiile de ardere pentru ceilali componeni combustibili.
Astfel:
CO rezulta: - pentru
CO +
2
1
O
2
= CO
2
1 m
3
N
CO +
2
1
m
3
N
O
2
= 1 m
3
N
CO
2
2
3
2
3 3
100 100 2
1
100
CO m
CO
O m
CO
CO m
CO
N N N
= + (9.43)
- pentru metan CH
4
rezult:
-
CH
= CO
2
+ 2 H
2
O
4
+ 2O
2
1 m
3
N
CH
4
+ 2 m
3
N
O
2
= 1 m
3
N
CO
2
+ 2 m
3
N
H
2
O
O H m
CH
CO m
CH
O m
CH
CH m
CH
N N N N 2
3 4
2
3 4
2
3 4
4
3 4
100
2
100 100
2
100
+ = + (9.44)
- pentru o hidrocarbura de tipul C
m
H
n
rezult:
C
m
H
n
+ |
.
|
\
+
4
n
m
|
O
2
+
2
n
H
2
O
2
= m CO
1 m
3
N
C
m
H
n
+
|
.
|
\
+
4
n
m
|
m = m m
3
N
CO
2
+
2
n
m
3
N
H
2
O
3
N
O
2
O H m
H C n
CO m
H C
m
O m
n
m
H C
H C m
H C
N
n m
N
n m
N
n m
n m N
n m
2
3
2
3
2
3 3
100 2 100
4 100
2
100
+
= |
.
|
\
|
+ +
(9.45)
- pentru hidrogen sulfurat H
2
S se obine:
H
2
S +
2
3
O
2
= SO
2
+ H
2
O
1 m
3
N
H
2
S +
2
3
m
3
N
O
2
= 1 m
3
N
SO
2
+ 1 m
3
N
H
2
O
O H m
S H
SO m
S H
O m
S H
S H m
S H
N N N N 2
3 2
2
3 2
2
3 2
2
3 2
100 100 100 2
3
100
+ = + (9.46)
Prof. Alex. Chisacof
an univ. 2007/2008
9 - 9
BTT II, cap 9, Arderea Combustibililor
a) Aerul de ardere necesar
Din reaciile de mai sus, pentru arderea completa a unui m
3
N
de combustibil, rezult
cantitatea de oxigen necesar:
(
+
|
.
|
\
|
+ + + + = =
. g . c m
m
2
3
4
2
2 2 100
1
3
N
3
N
2 2 4
2
min 2
2
O S H H C
n
m CH
CO H
V O
n m
o
O ,
(9.47)
Aerul minim necesar arderii teoretice este:
(
=
. g . c m
er a m
21 0
3
N
3
N min 2 0
,
O
V
,
a
(9.48)
Iar pentru un coeficient de exces de aer , aerul necesar arderii este:
V
a
= V
a
0
; V = V
0
a,um
(
. g . c m
er a m
3
N
3
N
(9.49)
a,um
b) Compoziia i volumul de gaze de ardere
n urma oxidrii complete a componentelor combustibile din gaz se obin gaze de ardere
compuse din:
- bioxid de carbon
(
+ + + =
. g . c m
CO m
100 100 100 100
3
N
2
3
N 2 4
2
CO H C
m
CH CO
n m
CO
V (9.50)
- bioxid de sulf
(
=
. g . c m
SO m
100
3
N
2
3
N 2
2
S H
V
SO
(9.51)
- vapori de apa,
(
+ + =
. g . c m
O H m
100 100 2 100
2
3
N
2
3
N 2 4 0
2
S H H C N CH
V
n m
O H
(9.52)
- azot
(
+ =
. g . c m
N m
100
79 , 0
3
N
2
3
N 2 0 0
2
N
V V
a N
(9.53)
- aer n exces
V
ex
a
=(-1) V
a
0
;
(
. g . c m
aer m
3
N
3
N
(9.54)
Volumul teoretic de gaze de ardere uscate:
Prof. Alex. Chisacof
an univ. 2007/2008
9 - 10
BTT II, cap 9, Arderea Combustibililor
(
+ + =
us . g . c m
us . g m
3
N
3
N 0 0
2 2 2
V V V V
N SO CO g,us
(9.55)
Volumul teoretic de gaze de ardere umede:
(
+ + + =
us . g . c m
um . g m
3
N
3
N 0 0 0
2 2 2 2
V V V V V
O H N SO CO g
(9.56)
Volumul real de gaze arse uscate:
V
g,us
= V
g,us
0
+ ( 1 ) V
a
0
(
us . g . c m
um . g m
3
N
3
N
(9.57)
Volumul real de gaze de ardere umede:
V
g
= V
g
O
+ V
a
ex
= V
g
o
+ ( 1 ) V
a
o
(
us . g . c m
um . g m
3
N
3
N
(9.58)
Volumul de gaze de ardere se mai poate exprima i n funcie de compoziia
elementar a gazelor (obinuta prin analiz):
V
g
= V
CO SO2
+ V
N2
+ V
O H O 2
(
us . g . c m
um . g m
3
N
3
N
(9.59)
2
+ V
2
+ V
n care V
CO2
i V
SO2
au expresiile prezentate anterior, iar ceilali componeni sunt:
V
N2
= V
N2
0
+ 0,79 ( 1 ) V
a
0
= 0,79 V
a
0
+ N
2
/100
(
us . g . c m
N m
3
N
2
3
N
(9.60)
V
O2
= 0,21 ( 1) V
a
0
= 0,21 V
a
ex
(
us . g . c m
O m
3
N
2
3
N
(9.61)
V
H2O
= V
H O 2
0
+0,00161 x ( 1) V
a
0
(
(
us . g . c m
O H m
3
N
vap 2
3
N
(9.62)
Volumul de gaze arse uscate este n acest caz:
V
g,us
= V
CO SO2
+ V
N2
+ V
O2
(
us . g . c m
us . g m
3
N
3
N
(9.63)
2
+ V
n care participaiile volumice de CO
2
, SO
2
, O
2
, N
2
se obin cu ajutorul analizoarelor de
gaze.
Prof. Alex. Chisacof
an univ. 2007/2008
9 - 11
BTT II, cap 9, Arderea Combustibililor
9. 4 Diagrama H-T. Temperatura de ardere
a) Diagrama H-T reprezint legtura grafic intre entalpia gazelor rezultat n urma
arderii unitii de cantitate de combustibil. Entalpia gazelor de ardere corespunztoare unei
temperaturi T este:
H
g
= H
g
0
+ H
a
ex
(
. g . cb m
kJ
;
l s, cb kg
kJ
3
N
(9.64)
n care H
g
o
reprezint entalpia gazelor de ardere rezultat n urma arderii cu aerul minim
necesar:
( )
(
=
+ + + =
= + + + =
= + + + =
3
N
,
0
0
0
2
0
m
kJ
;
kg
kJ
2 2 2 2 2 2 2 2
2 2 2 2 2 2 2 2
2 2 2
T C V
) T C V C V C V C (V
T C V T C V T C V T C V
H HN H H H
ga
i pm i
O pm,H O H pm,N N pm,SO SO pm,CO CO
O pm,H O H pm,N N pm,SO SO pm,CO CO
O H SO CO g
(9.65)
iar H
a
ex
reprezint entalpia aerului n exces care se gsete n gazele de ardere:
H
a
ex
= V
a
ex
C
pm,a
T = ( 1) V
a
0
C
pm,a
T
(
3
N
m
kJ
;
kg
kJ
(9.66)
C
pm,i
reprezint cldura specifica medie la presiune constanta ntre temperatur de referin 0
i o temperatur curent T, a componenilor din gazele de ardere, n kJ/m
3
N
K.
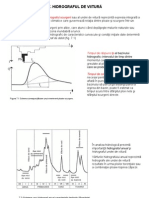
Considernd o anumit valoare pentru excesul de aer pentru diferite temperaturi T se
obin curbele de entalpie a gazelor de ardere (fig. 9.1). Diagrama H-T se obine prin puncte
fiind construit pe intervalul de temperatura, de exemplu 0 2500 C, cu pasul T=100 K.
Utilitatea diagramei const n posibilitatea de stabilire a temperaturii de ardere, a
disponibilului de cldur coninut n gazele de ardere funcie de temperatura la o anumit
seciune a echipamentului termic.
H
g
=1,2 =1,1
=1
H
g
o
Fig. 9.1 Diagrama H-T
H
g
T
t T
g
T
Prof. Alex. Chisacof
an univ. 2007/2008
9 - 12
BTT II, cap 9, Arderea Combustibililor
b) Temperatura de ardere (temperatura gazelor de ardere)
Temperatura teoretic de ardere T
t
reprezint temperatura gazelor rezultate ntr-un
proces complet de ardere cu aerul teoretic necesar arderii (=1), n condiiile n care ntreaga
cantitate de cldur este preluat de gazele de ardere. Considerand temperatura
combustibilului T
cb
, puterea calorific inferioar a combustibilului H
i
, temperatura aerului
care intr n procesul de ardere T
a
, expresia bilanului termic al procesului de ardere pentru
unitatea de cantitate de combustibil este:
( )T C V T C V H H T C V h
i pm
o
i t g pm g g i a pm,a a cb
= = = + +
, ,
0 0 0
(
3
N
m
kJ
;
kg
kJ
(9.67)
n care : h
cb
entalpia unitii de cantitate de combustibil sau entalpia sensibila a
combustibilului, h
cb
= 1 c
cb
T
cb
[kJ/kg cb] pentru combustibilul solid sau lichid, respectiv
h
cb
=C
pm,cb
T
cb
[kJ/m
3
N
cg] pentru combustibilul gazos; V
a
0
volumul minim de aer necesar
arderii, n m
3
N
/kg cb sau m
3
N
/ m
3
N
cg; C
pm,a
cldura specific medie la presiune constanta a
aerului la intrare n reacia de oxidare la temperatura T
a
, n kJ/m
3
N
K; H
i
puterea calorific
inferioar a combustibilului, n kJ/kg cb sau kJ/ m
3
N
cg; V
g
0
volumul de gaze de ardere
rezultat n urma arderii teoretice, n m
3
N
/kg cb, m
3
N
/ m
3
N
cg, C
pm,g
cldura specific medie la
presiune constant a gazelor de ardere la temperatura T
t
, kJ/m
3
N
K; V
i
0
volumul de
component i din gazele de ardere rezultat n urma arderii teoretice. Cu aceste elemente
temperatura teoretic de ardere rezult:
| | C
,
0
,
0
,
0
,
0
o
C V
H T C V h
C V
H T C V h
T
i pm i
i a a pm a cb
g pm g
i a a pm a cb
t
+ +
=
+ +
= (9.68)
Temperatura teoretic de ardere se poate determina i grafic din fig. 9.1, pe baza entalpiei
teoretice a gazelor de ardere H
g
0
(rel. 9.67).
Pentru stabilirea temperaturii reale de ardere T
g
n expresia bilanului termic se vor lua n
considerare att pierderile de cldur din spaiul de ardere, ct i pierderile de cldur datorate
arderii incomplete a combustibilului, precum i acelea datorate evacurii unor reziduuri solide
rezultate din ardere (cenua i zgura). Aceste pierderi se pun n eviden prin randamentul
spaiului de ardere (al focarului)
f
, ele fiind raportate la puterea calorifica inferioar a
combustibilului. De asemenea, o parte din cldur este transmis prin radiaie, n timpul
procesului de ardere, de la flacra la materialul din focar i ctre pereii acestuia. Aceast
cldur radiat se exprim procentual n funcie de puterea calorific inferioar a
combustibilului Q
r
= H
i
[kJ/kg cb; kJ/m
3
N
cb], n care este cota din puterea calorific
inferioar a combustibilului transmis prin radiaie (valorii orientative 0,3 0,5). Ecuaia de
bilan termic a focarului (fig. 9.2) pentru unitatea de cantitate de combustibil este:
h
cb
+H
i
+ H
a
=(1-
f
)H
i
+ Q
r
+ H
g
(
3
N
m
kJ
;
kg
kJ
(9.69)
n care:
- h
cb
reprezint cldura (entalpia) sensibil a combustibilului la intrarea n focar:
h
cb
=c
pm,cb
T
cb
, n [kJ/kg cb]; h
cb
=C
pm,cb
T
cb
[kJ/m
3
N
cb] (9.70)
- H
a
entalpia sensibil a aerului necesar arderii care intr cu temperatura T
a
Prof. Alex. Chisacof
an univ. 2007/2008
9 - 13
BTT II, cap 9, Arderea Combustibililor
H
a
= V
a
C
pm,a
T
a
= V
a
0
C
pm,a
T
a
(
3
N
m
kJ
;
kg
kJ
(9.71)
Q
r
(1-
f
) H
i
h
cb
+H
i
H
g
H
a
Fig. 9.2 Bilanul termic al unui spaiu de ardere
- Q
r
cldura cedat prin radiaie de ctre flacr materialelor i suprafeelor reci:
Q
r
= H
i
(9.72)
- H
g
entalpia sensibil a gazelor de ardere, care prsesc focarul cu temperatura T
g
:
H
g
= V
g
C
pm,g
T
g
(
3
N
m
kJ
;
kg
kJ
(9.73)
-
f
randamentul focarului ( al spaiului de ardere) se determin cu expresia:
( )
100
q q q q 100
ex rez
m
in
ch
in
f
+ + +
= (9.74)
n aceast expresie mrimile au urmatoarele semnificatii: cldura pierdut prin arderea
chimica incompleta a combustibilului, cldur care este pus n eviden de existena n
gazele de ardere a unor gaze combustibile (CO, CH
ch
in
q
4
, alte hidrocarburi, H
2
, etc), gaze rezultate
i datorita disociaiei gazelor de ardere, precum i a funinginii, =(03)%; pierderea
de cldur provenita din arderea incompleta din cauze mecanice, ea fiind caracteristica
combustibililor solizi, =(15)%; q
ch
in
q
m
in
q
m
in
q
rez
pierderea de cldur datorat evacuarii reziduurilor
solide din focar la temperatur ridicat (de exemplu zgura se evacueaz la 500900C),
q
rez
=(0,53)%; q
ex
cldura pierdut prin pereii focarului i trasferat ctre mediul exterior,
q
ex
=(0,53)%. n aceste condiii randamentul focarului are valori de 0,850,98.
Inlocuind relaiile de mai sus n ecuaia de bilan (9.69) se obine:
c +H
i
+ V
a
0
C
pm,a
T
a
=(1-
f
)H
i
+ H
i
+ V
g
C
pm,g
T
g
(9.75)
pm,cb
T
cb
de unde rezult temperatura real a gazelor de ardere:
Prof. Alex. Chisacof
an univ. 2007/2008
9 - 14
BTT II, cap 9, Arderea Combustibililor
Prof. Alex. Chisacof
an univ. 2007/2008
9 - 15
( )
| | C
0
o
C V
H T C V T c
T
pm,g g
i f a pm,a a cb pm,cb
g
+ +
= (9.76)
Volumul gazelor de ardere este:
(
+ + + + =
cb , m sau kg
m
3
N
3
N 0
V V V V V V
ex
a N O H SO CO g
2 2 2 2
(9.77)
Cldura specific medie a gazelor de ardere la presiune constant ntre zero i
temperatura de ardere T
g
este dat de relaia pentru amestecuri de gaze:
K] [kJ/m
3
N a pm a N pm N O H pm O H SO pm SO CO pm CO g pm,
C r C r C r C r C r C
2 2 2 2 2 2 2 2
+ + + + = (9.78)
n care participaiile volumice ale gazelor componente sunt:
g
ex
a,
a
g
0
N
N
g
O H
O H
g
SO
SO
g
CO
CO
V
V
r ;
V
V
r ;
V
V
r ;
V
V
r ;
V
V
r
2
2
2
2
2
2
2
2
= = = = = (9.79)
Tinnd seama de relaiile (9.78) i (9.79) expresia produsului :
( )
(
+ + + + =
K cb , m sau kg
kJ
3
N
2 2 2 2 2 2 2 2
a pm a N pm N O H pm O H SO pm SO CO pm CO g pm,g
C V C V C V C V C V V C
(9.87)
Observaia 1. n calculele practice se alege o valoare a temperaturii gazelor de ardere,
valoare cu care se calculeaz caldurile specifice medii ale gazelor componente. Cu aceste
calduri specifice se determin o valoare a temperaturii gazelor de ardere T
g
. Dac aceast
valoare este diferit cu 20 K de valoarea la care s-au calculat cldurile specifice, se impune
noua valoare T
g
pentru calculul a caldurilor specifice i se recalculeaza temperatura T
g
.
Iteraia se face pn cnd temperatura obinuta este n limita a 20 K fa de aceea la care s-au
calculat cldurile specifice.
Observaia 2. Temperatura real de ardere se mai poate determina i din diagrama H-T,
atunci cnd se cunoate entalpia gazelor H
g
i coeficientul de exces de aer la care a avut loc
arderea. Pe de alt parte, dac se cunoate temperatura gazelor de ardere i coeficientul de
exces de aer se poate evalua entalpia gazelor de ardere H
g
(fig. 9.1).
You might also like
- ArdereaDocument37 pagesArdereaVlad GrigoreNo ratings yet
- Instalatii Cu Turbine Cu AburDocument6 pagesInstalatii Cu Turbine Cu AburSzekely Sarolta100% (4)
- Calculul Termic Al Unei Instalatii Cu Turbina Cu AburDocument11 pagesCalculul Termic Al Unei Instalatii Cu Turbina Cu AburCosmin Rachieru100% (1)
- Echipamente de Transfer Termic Si Utilaje PCDocument466 pagesEchipamente de Transfer Termic Si Utilaje PCLeonard Braun100% (2)
- Alimentarea Cu Caldura A Unui OrasDocument19 pagesAlimentarea Cu Caldura A Unui OrasRazvan Niculae0% (1)
- Energetica - Schimbatoare de Caldura PDFDocument245 pagesEnergetica - Schimbatoare de Caldura PDFEmil Catalin Schiopu100% (1)
- Calculul Consumului de AburDocument10 pagesCalculul Consumului de AburAlisa ManoloiuNo ratings yet
- Instalatii Frigorifice - Principiul de FunctionareDocument19 pagesInstalatii Frigorifice - Principiul de FunctionaresimNo ratings yet
- Transfer Global de CalduraDocument101 pagesTransfer Global de CaldurakingdiamondNo ratings yet
- Motoare Termice-Sisteme de CogenerareDocument70 pagesMotoare Termice-Sisteme de CogenerarePopa Mihai100% (4)
- Cap 5 TurbineDocument52 pagesCap 5 TurbineCristina Maria Sandu100% (1)
- Piroliza RefDocument40 pagesPiroliza RefAdriana RîbuNo ratings yet
- Generatoare Cu Abur Si TurbineDocument6 pagesGeneratoare Cu Abur Si TurbineSergiu Constantin100% (1)
- Bazele Transferului de Caldura PDFDocument258 pagesBazele Transferului de Caldura PDFLeo CrisuNo ratings yet
- Dimensionarea Unei TurbineDocument45 pagesDimensionarea Unei TurbineDenisTrifan0% (1)
- 14 Vapori: VaporiiDocument17 pages14 Vapori: VaporiiSqueezy Channel50% (2)
- Lucrare Licenta Ionela Maghiran CU Nume ModificatDocument37 pagesLucrare Licenta Ionela Maghiran CU Nume Modificatandrei andreiNo ratings yet
- Proiect BenzenDocument38 pagesProiect BenzenAlexandra BuzeaNo ratings yet
- Caracteristici Tehnice Ale Turbinei DSL 50Document19 pagesCaracteristici Tehnice Ale Turbinei DSL 50Narcis PedrosNo ratings yet
- PTQ Proiect RalucaDocument23 pagesPTQ Proiect RalucaradugNo ratings yet
- Instalatii FrigorificeDocument79 pagesInstalatii FrigorificeSergiu100% (2)
- TERMODINAMICA LUCRARE DE AN - копияDocument15 pagesTERMODINAMICA LUCRARE DE AN - копияDavid CotetNo ratings yet
- Proiect Densitate MotorinaDocument29 pagesProiect Densitate MotorinaAlex Zamficu100% (2)
- Termotehnica Curs 6 - 11Document35 pagesTermotehnica Curs 6 - 11Anonymous kAxPF8v100% (3)
- Schimbatoare de Caldura ReferatDocument33 pagesSchimbatoare de Caldura ReferatIuliu Damian100% (1)
- Generatoare de AburDocument20 pagesGeneratoare de AburDumitru Podgorneak67% (3)
- Evacuarea Zgurii Si CenusiiDocument11 pagesEvacuarea Zgurii Si CenusiibosoiroNo ratings yet
- Moduri de Transfer Al CălduriiDocument70 pagesModuri de Transfer Al CălduriiSebastian BuduNo ratings yet
- Proiect - Aerul ConditionatDocument45 pagesProiect - Aerul ConditionatMarius-Iulian Munteanu75% (4)
- Schimbator de CalduraDocument8 pagesSchimbator de CaldurabumboncikNo ratings yet
- CANDU TrigaDocument89 pagesCANDU Trigaandycs14100% (4)
- Centralele Termoelectrice Cu Abur CTEDocument36 pagesCentralele Termoelectrice Cu Abur CTEDaniel BodeaNo ratings yet
- Schimbator de Caldura TubularDocument15 pagesSchimbator de Caldura TubularAndrei RohlicekNo ratings yet
- Puterea CaloricaDocument19 pagesPuterea CaloricaMihail Prescura100% (2)
- Proiect Cazane AburDocument19 pagesProiect Cazane AburfusuiocNo ratings yet
- Combustibili PetrolieriDocument39 pagesCombustibili PetrolieriIoana Andreea Repede100% (2)
- Turbine Cu GazDocument14 pagesTurbine Cu GazAlexandra Iorga100% (1)
- Pile de CombustieDocument27 pagesPile de CombustieIonuţ FloreaNo ratings yet
- Proiectare Instalatie Racire. Simulare Ansys - Vanghele IancuDocument23 pagesProiectare Instalatie Racire. Simulare Ansys - Vanghele Iancu万荣扬库No ratings yet
- Instalaţii Frigorifice Cu Comprimare Mecanică de Vapori Într-O TreaptaDocument18 pagesInstalaţii Frigorifice Cu Comprimare Mecanică de Vapori Într-O Treaptav vNo ratings yet
- Caiet PracticaDocument13 pagesCaiet Practicacerruti5No ratings yet
- Exploatarea Instalatiilor de Încalzire IDocument25 pagesExploatarea Instalatiilor de Încalzire IIulia Patruica0% (1)
- Bilant TermicDocument4 pagesBilant TermicAdriana NechitaNo ratings yet
- Cuptoare IndustrialeDocument15 pagesCuptoare IndustrialeTudor VasilachiNo ratings yet
- Schimbatoare de CalduraDocument25 pagesSchimbatoare de Calduramariussyz100% (2)
- Referate MariusDocument3 pagesReferate Mariusliliana100% (1)
- 2.ard CBLDocument30 pages2.ard CBLRadu M.No ratings yet
- Gatag 1Document8 pagesGatag 1Meca CosminNo ratings yet
- ARDEREADocument12 pagesARDEREAIasmina ClaudiaNo ratings yet
- Lectia11 Reactiile Exoterme Si Endoterme Entalpia de Reactie Legea Lui Hess PDFDocument3 pagesLectia11 Reactiile Exoterme Si Endoterme Entalpia de Reactie Legea Lui Hess PDFivan turcan100% (1)
- 3,4,5, Arederea CombustibililorDocument17 pages3,4,5, Arederea Combustibililorjoy shareNo ratings yet
- Teoria CombustieiDocument5 pagesTeoria Combustieiytriu39No ratings yet
- Notiuni de Termochimie PDFDocument11 pagesNotiuni de Termochimie PDFGiaconiaNo ratings yet
- PACE CursDocument100 pagesPACE CursAndreea CostacheNo ratings yet
- Noţiuni de TermochimieDocument4 pagesNoţiuni de TermochimieCostinNo ratings yet
- Termodinamica 2Document6 pagesTermodinamica 2CosminNo ratings yet
- ArdereaDocument40 pagesArdereaIon Morari100% (6)
- Căldura de DizolvareDocument2 pagesCăldura de DizolvareAndrei PrisacariuNo ratings yet
- Tema 6.Document18 pagesTema 6.CuffNo ratings yet
- Apa grea: O școală a cercetării științifice și tehnologice românești, o paradigmă în sensul lui KuhnFrom EverandApa grea: O școală a cercetării științifice și tehnologice românești, o paradigmă în sensul lui KuhnNo ratings yet
- Curs 3 Metode - EITDocument15 pagesCurs 3 Metode - EITGmd28No ratings yet
- David R. Montgomery - Țărână. Cum Se Fac Praf Civilizațiile - TEI - ColorDocument248 pagesDavid R. Montgomery - Țărână. Cum Se Fac Praf Civilizațiile - TEI - ColorTei Traduceri Ecologice Independente100% (4)
- Sepp Holzer - Permacultura. Ghid Practic Pentru Agricultura La Scara Mica - TEI - v. ColorDocument236 pagesSepp Holzer - Permacultura. Ghid Practic Pentru Agricultura La Scara Mica - TEI - v. ColorTei Traduceri Ecologice Independente97% (29)
- Clasificare Schimbatoarelor de CalduraDocument17 pagesClasificare Schimbatoarelor de CalduralilboteNo ratings yet
- Curs RegeneratoareDocument10 pagesCurs RegeneratoarelilboteNo ratings yet
- Curs 3 MASINI HIDRAULICEDocument27 pagesCurs 3 MASINI HIDRAULICEGmd28100% (1)
- Introducere - Masini HidrauliceDocument35 pagesIntroducere - Masini HidrauliceGmd28100% (1)
- Curs 4 MASINI HIDRAULICEDocument20 pagesCurs 4 MASINI HIDRAULICEGmd28100% (1)
- Recuperatoare de CalduraDocument6 pagesRecuperatoare de Calduralilbote100% (1)
- Curs 1 MASINI HIDRAULICEDocument51 pagesCurs 1 MASINI HIDRAULICEGmd28100% (2)
- Hidrograful UnitarDocument12 pagesHidrograful UnitarGmd28No ratings yet
- Curs 2 MASINI HIDRAULICEDocument28 pagesCurs 2 MASINI HIDRAULICEGmd28100% (1)
- Curs 10 Indici Calitate EITDocument4 pagesCurs 10 Indici Calitate EITGmd28No ratings yet
- Curs 7 SCTT EITDocument10 pagesCurs 7 SCTT EITGmd28No ratings yet
- Curs 5 SCP - EITDocument9 pagesCurs 5 SCP - EITGmd28No ratings yet
- Hidrologie - INTR ĂRILE ÎN SISTEMUL HIDROLOGICDocument8 pagesHidrologie - INTR ĂRILE ÎN SISTEMUL HIDROLOGICGmd28100% (1)
- Schimb TubulareDocument15 pagesSchimb TubulareAlin BeșaNo ratings yet
- 8 Prezentare - RecuperatoareDocument6 pages8 Prezentare - RecuperatoareCiocarda AndreeaNo ratings yet
- Rosia MontanaDocument11 pagesRosia MontanaGmd28No ratings yet
- Hidrologie - INFILTRAŢIADocument8 pagesHidrologie - INFILTRAŢIAGmd28No ratings yet
- HidrologieDocument7 pagesHidrologieGmd28100% (1)
- Hidrologie - EVAPOTRANSPIRAŢIADocument10 pagesHidrologie - EVAPOTRANSPIRAŢIAGmd28No ratings yet
- Hidrologie Si MeteorologieDocument29 pagesHidrologie Si MeteorologieGmd28100% (1)
- Lectia 11 Transfer de Căldură Si MasaDocument18 pagesLectia 11 Transfer de Căldură Si MasaGmd28No ratings yet
- Lectia 12 Transfer de Căldură Si MasaDocument22 pagesLectia 12 Transfer de Căldură Si MasaGmd28No ratings yet
- Lectia 10 Transfer de Căldură Si MasaDocument28 pagesLectia 10 Transfer de Căldură Si MasaGmd28No ratings yet
- Lectia 8Document24 pagesLectia 8Bucur StefanNo ratings yet
- Lectia 9Document34 pagesLectia 9Bucur StefanNo ratings yet
- Lectia 7 Transfer de Căldură Si MasaDocument7 pagesLectia 7 Transfer de Căldură Si MasaGmd28No ratings yet