Professional Documents
Culture Documents
Redução Carbotérmica Dos Óxidos de Manganês e de Ferro
Uploaded by
Celi GomesCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Redução Carbotérmica Dos Óxidos de Manganês e de Ferro
Uploaded by
Celi GomesCopyright:
Available Formats
49
6
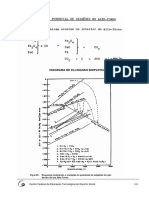
Reduo carbotrmica dos xidos de mangans e de ferro
Segundo Rosenqvist
(29)
, um grande nmero de metais se produzem a partir
de matrias primas em forma de xidos, como o caso do ferro, do mangans, do
cromo, etc. S os xidos dos metais mais nobres podem se converter em metal,
mediante uma simples decomposio trmica, como o caso do xido de prata
Ag2O.
A grande maioria dos xidos se decompem por meio de um agente redutor.
PUC-Rio - Certificao Digital N 0321309/CA
Este pode ser carbono, monxido de carbono ou hidrognio ou, em casos
especiais outro metal, o qual tenha uma maior afinidade pelo oxignio. O carbono,
monxido de carbono e o hidrognio so os agentes redutores de maior
importncia industrial e econmica que podem ser produzidos a partir de matrias
primas como o carvo, o petrleo e o gs natural.
6.1.
O processo de fabricao do ferro mangans alto carbono
A metalurgia do mangans muito similar metalurgia do ferro exceto ao
que se refere a maiores temperaturas, por volta de 1200C, o que se precisa para
a reduo de xidos de mangans. Ferro mangans padro ou comumente
chamado de ferro mangans alto carbono (FeMnAC) a liga mais usada. Ela
contm mais de 76% de mangans e aproximadamente 7% de carbono. Esta liga
pode ser produzida em alto forno ou em forno eltrico (1).
A indstria do ao tambm requer ligas de mangans com baixo teor de
carbono. Por muito tempo estas ligas de ferro mangans mdio carbono e ferro
mangans baixo carbono, foram produzidas por processos silicotrmicos,
envolvendo a reao de slico-mangans e minrio de mangans. Este minrio de
mangans reduzido ao estado de MnO por aquecimento (1).
50
O ferro-mangans pode ser produzido em alto forno ou em forno eltrico a
arco, a partir de minrios contendo xidos de mangans e de ferro
(5)
, j que o
minrio de mangans contm sempre xidos de ferro e o ferro incorpora-se na
fase metlica, isto porque o mangans menos nobre que o ferro, ento o teor de
ferro na liga estar determinado pela quantidade de ferro no minrio
(29)
. Est
comprovado que o minrio precisa ter pelo menos uma relao de percentagem
em peso Mn / Fe de 6 para assegurar uma boa recuperao de mangans
(5)
Minrios de baixos teores e com uma relao Mn / Fe de aproximadamente 4 e
relativamente alto teor de slica, usado pela Thermit Alloys Limited para
produzir ferro-mangans com um teor limitado de mangans (5).
Morimoto et al.
(53)
, no seu trabalho sobre a Construo de um Forno de
Cuba para Fuso de Ferro-mangans, fez um esboo do forno e uma comparao
PUC-Rio - Certificao Digital N 0321309/CA
com o alto forno de reduo de minrios de ferro. O Forno de Cuba tm um
volume interno de 398 m3 e uma capacidade de produo de 270 ton/dia de FeMn
AC. O autor indica que para produzir uma tonelada de ferro-mangans usando o
forno eltrico, so requeridos 2400 KWh de energia eltrica e cerca de 360 kg de
coque; mas com o forno de cuba, os requerimentos so cerca de 200 KWh e 1500
kg de coque. A tabela 6 mostra os principais dados de operao do forno de
fuso.
Tabela 1 - Principais especificaes de operao do Forno de Cuba para Fuso de
Ferro-mangans (53).
Item
Especificaes
Volume interno
398 m3
Produo
230 ton/dia
Volume de ar
450 Nm3/min
Enriquecimento de oxignio
7-8 %
Temperatura de exploso
860C
Contedo de Mn no metal
74,5 %
Consumo de coque
1500 Kg/ton
Produtividade
0,58 t/m3 .dia
51
Volume de escoria
580 kg/ton
Volume do gs de topo
4890 Nm3/ton
A seguir, sero descritas algumas caractersticas do forno de fuso de ferromangans em comparao com o alto forno para a produo de ferro gusa:
a) Alto consumo de coque
A maior diferena entre a fabricao de ferro gusa e FeMn est em que o Fe
pode ser produzido atravs da reduo indireta de FeO pelo gs CO, enquanto que
a reduo indireta de MnO pelo CO(g) no ocorre, entretanto o Mn produzido
somente atravs da reduo direta pelo C.
PUC-Rio - Certificao Digital N 0321309/CA
Conseqentemente, a eficincia de utilizao do CO no forno de cuba
menor e o calor latente e o calor sensvel do gs do topo tornam-se muito elevado.
Alm disso, o consumo de energia para a reduo de mangans maior que para a
reduo de ferro.
Esses fatos fazem que o consumo de combustvel e de coque no forno de
fuso, aumentem em torno de 1200 a 1500 kg/ton na fabricao de FeMn,
entretanto ocorre um aumento de 450 para 500 kg/ton na fabricao de ferro gusa.
b) Baixa Produtividade
A produtividade de ferro gusa 1,8 a 2,2 ton/m3.dia. Porm a produtividade
de ferro-mangans cai para 0,58 a 0,68 ton/m3.dia porque na fuso de ferromangans a taxa de coque alta e o consumo unitrio de gs gerado no forno
tambm alto, devido alta combusto do coque na frente das ventaneiras.
52
SF
CO/CO2
7-9
400 600C
~900C
BF
CO/CO2
~1
~ 150C
~ 300C
Reduo at
MnO
pelo gs CO
PUC-Rio - Certificao Digital N 0321309/CA
Reduo de
FeO pelo
CO(g)
Reduo de
MnO
pelo Carbono
(altamente
Endotrmica)
2400 2600C
Reduo de
FeO
pelo Carbono
2300
860C
26-28 % O2
1200C
21 % O2
escria
Fe Mn metal
escria
Fe metlico
Figura 1 - Comparao de reaes metalrgicas entre o Forno de Cuba para Fuso de
ferro-mangans e o Alto Forno para ferro gusa (53).
c) Alta temperatura do gs do topo
A alta temperatura do gs do topo devido reduo de MnO2 e Mn2O3
pelo CO(g) os quais tm reao exotrmica significante, ocorre na parte superior
do forno e adicionalmente, por causa do alto consumo de coque, a temperatura do
gs do topo eleva-se de 400 a 600C comparados com os aproximados 150C do
alto forno para fabricao de ferro gusa. A temperatura do gs do topo
controlada de 300 a 350C por jato de gua para a proteo da unidade.
d) Alta Taxa de Poeira
53
A taxa de poeira (poeira seca mais poeira mida) na fuso no forno de fuso
100 kg/ton ou mais, comparado com cerca de 20 kg/t no alto forno para ferro
gusa, pelas seguintes razes:
* Minrio de mangans freqentemente desenvolve trincas trmicas e gera
muito p.
* Desde que a temperatura da zona de combusto e a temperatura interna so
altas, ento finos de poeira, como a slica (SiO2), esto aptos para ser gerados
em frente das ventaneiras.
* O volume do gs do topo gerado no forno grande devido alto consumo
de coque, alta temperatura do gs do topo, tambm ao volume aparente de
PUC-Rio - Certificao Digital N 0321309/CA
gs e a velocidade de fluxo de gs aumenta no topo.
e) Alta Temperatura Terica de Chama (TFT) na zona de combusto
Como o mangans tem uma forte afinidade pelo oxignio, ento xidos de
mangans apresentam dificuldade para se reduzir. Conseqentemente a
Temperatura Terica de Chama, a qual melhora o rendimento do mangans,
ajustado de 2400C a 2600C. Para fins de comparao, a TFT do alto forno para
ferro gusa est cerca de 2300C. Desde que a temperatura da chama to baixo da
ordem de 860C, a TFT mantida e controlada por enriquecimento de oxignio.
f) Elevado lcalis
Desde que o minrio de mangans contm mais lcalis que o minrio de
ferro e a taxa de coque trs vezes mais alta que a usada no alto forno para ferro
gusa, o consumo de K2O carregado dentro do forno cerca de doze vezes mais
alta que a do alto forno e, mesmo usando um coeficiente de produtividade, este
forno de fuso requer quatro vezes tanto quanto K2O que no alto forno. O K2O
no somente corroi o refratrio do forno, mas tambm se adere ao sistema de
lavagem de gases, prejudicando o mesmo (53).
54
Hoje em dia, a fuso em forno eltrico a arco mais comum que a fuso em
alto forno. O forno eltrico a arco muito flexvel e pode ser usado para produzir
qualquer tipo de ferro-mangans ou silico-mangans, econmica para
capacidade de produo pequena. Neste forno possvel obter altas recuperaes
a partir de minrios de baixa qualidade, alm disso, o consumo de coque muito
menor que em alto forno. Assim, o principal problema da fuso em forno eltrico
a arco o alto custo da eletricidade (5).
Devido maior temperatura de reduo, o forno eltrico torna-se mais
competitivo frente ao alto forno na medida que aumenta a estabilidade do xido
que vai ser reduzido. Isto se mostra na tabela 7, na qual comparam-se alguns
dados para a fuso do ferro gusa e ferro-mangans em alto forno e forno eltrico,
PUC-Rio - Certificao Digital N 0321309/CA
respectivamente (29).
Tabela 2 - Comparao de consumos de coque e KWh, na produo de ferro gusa e
ferro-mangans em alto forno e forno eltrico, segundo Rosenqvist (29).
Ferro gusa
Alto Forno
Ferro-mangans 80 %
Forno
Alto Forno
Forno Eltrico
Eltrico
Kg de coque /
550
380
1500
400
---
2000
---
2600
ton
KWh / ton
Kg
de
0,085
0,42
coque/KWh
Pode-se ver na tabela 7 que para o mesmo preo de coque, a usina de ferromangans capaz de pagar at cinco vezes mais por kilowatt-hora que a usina de
ferro gusa.
As ferro-ligas de mangans so usualmente produzidas em fornos de fuso
eltricos a arco, usando reduo carbotrmica de minrios de mangans, sinter e
coque metalrgico (6,9,10), pode tambm ser feito com ou sem a adio de fluxo de
55
cal, o qual conhecido como um processo bsico ou um processo de menos fluxo
de cal, respectivamente (6).
A produo carbotrmica da liga de ferro-mangans em forno eltrico a arco
caracterizada pela perda de 20 a 40 % de mangans na escoria e na poeira. O
mangans perdido na escoria est na forma de xidos e tambm na forma
metlica, o metal retido na escoria (6).
Alm disso, o alto custo da energia eltrica e questes ambientais
associadas com a produo de coque metalrgico e minrios sinterizados, fazem
com que se esteja a procura de tecnologias alternativas
(9)
. Segundo Kamei et al.
(12)
, a produo de ferro-mangans alto carbono na industria japonesa, tem um
consumo de eletricidade que est por volta de 7300 MJ /t, isso incrementa o custo
PUC-Rio - Certificao Digital N 0321309/CA
de produo somado ao alto custo da eletricidade no Japo. Com isso o ferromangans japons tinha menos competitividade no mercado internacional,
conseqentemente o mtodo de produo de ferro-mangans alto carbono
usando forno eltrico a arco, teve que ser bem investigado (12).
Anacleto et al.
(9)
, indica que a pr-reduo de minrios de mangans pode
ser uma rota atrativa para incrementar a eficincia de produo de ferromangans.
6.1.1.
O processo no forno eltrico a arco
O esquema geral da reduo dos minrios de mangans na produo de
ligas de mangans em forno eltrico a arco, pode ser apresentado na seguinte
seqncia (17):
- Primeiro, xidos de ferro e de mangans so reduzidos para FexO e MnO
pelo CO(g), isto acontece ainda no estado slido.
- A fase metlica comea com a reduo de FexO para Fe, provavelmente
tambm em estado slido.
56
- Esse processo acompanhado pela dissoluo de carbono no ferro e
formao de carbeto de ferro.
- Carbono do coque, de outros materiais carbonceos e da fase metlica
reduzem minrio de mangans a elevadas temperaturas com formao de
mistura de carbetos.
Limitaes em diferentes estgios da reduo de minrios de mangans
dependem do tipo de minrio e tipo de redutor, tamanho de matria prima e de
PUC-Rio - Certificao Digital N 0321309/CA
outros parmetros (17).
Figura 2 - Forno eltrico fechado arco submerso para fuso de ferro-mangans,
modificado da Clark and Martin (5).
A descrio do forno eltrico a arco feito por Vandertaay et al.
(5)
, indica
que um forno circular fixo com trs eletrodos Soderberg de 1.5 a 2 metros de
dimetro e geralmente desenhado para 20 45 MW, embora haja fornos
desenhados at 110 MW. Cada eletrodo cercado por trs rampas carregando
material, mas h somente um lugar para a sada de gases. O forno formado por
57
blocos de carbono que contm a liga fundida e a escria durante a fuso, os gases
de sada so captados no topo do forno. O esquema do forno eltrico a arco
modificado da Clark and Martins apresentada na figura 9.
H dois possveis mtodos de fuso usando forno eltrico a arco. O processo
de escoria pobre, que tem como alvo a mxima recuperao de mangans na
liga e produzir uma escoria descartvel contendo 15 20% Mn e o outro processo
chamado de escoria rica em mangans que produz uma escoria contendo 3040% de Mn a qual torna-se como alimentao no processo de fuso do silicomangans (5,35).
O processo de escoria rica em mangans favorvel porque requer baixo
consumo de energia, permite acrescentar a produtividade no forno, reduz o
PUC-Rio - Certificao Digital N 0321309/CA
consumo de coque na fuso de silico-mangans, opera a baixas temperaturas,
abaixa as perdas de mangans por vaporizao e diminui o problema da poluio
(5)
.
Enfatizando o descrito acima, os autores Andrade de Castro e Santos (2,35),
desenvolveram um estudo utilizando os dados de operao de fornos eltricos de
reduo fechados que operam no Brasil na produo de FeMnAC, estabelecendo
uma correlao entre as perdas de mangans na escoria e nos gases,
especificamente para saber qual deveria ser a porcentagem de MnO na escoria,
quando utilizando-se os processos de escoria pobre e de escoria rica (2).
Esses autores chegaram s seguintes concluses (2,35):
A) No caso de processos em simples estgio, ou seja, produo de
FeMnAC com escoria pobre, a porcentagem tima de MnO na escoria
deve estar entre 15 20 %.
B) No processo de produo de FeMnAC em duplo estgio, com escoria
rica e pobre, as porcentagens de MnO na escoria deveria estar entre 30
40%.
Alm disso, eles ratificam que o processo em duplo estgio, com produo
de FeMnAC e FeSiMn o que conduz a uma taxa de recuperao mxima,
58
ao lado de permitir operar-se no primeiro forno com escria cida e
portanto com menor carregamento de fundentes carbonticos, quer na
sinterizao ou forno.
O processo com escria pobre embora possa parecer pouco atrativo, dever
ser melhor estudado atravs do emprego das poeiras recuperadas nas
instalaes de depurao dos gases, bem como dos fundentes carbonticos
ou cal na instalao de sinterizao o que eliminaria em grande parte os
inconvenientes principais desta alternativa.
6.2.
Termodinmica da reduo carbotrmica de xidos de mangans
PUC-Rio - Certificao Digital N 0321309/CA
A termodinmica fornece mtodos para prever o equilbrio das reaes
qumicas acuradamente e, muitas vezes, sem necessidade de apelar para a
experincia. Mas importante lembrar que a termodinmica lida com funes de
estado (aquelas propriedades cuja variao independe do modo como o sistema
sofreu transformaes) e como independe do processo, no pode dar informaes
sobre a velocidade das reaes. Tais informaes s podem ser obtidas pela
cintica (29,47).
Para um processo que ocorre a temperatura constante (uma reao
qumica, por exemplo):
G = H T.S
eq.(1)
Onde:
G: variao de energia livre
H: variao de entalpia
S: variao de entropia
Quando
uma
determinada
reao
qumica
pode
se
processar
simultaneamente nos dois sentidos, h um momento em que o sistema parece
estacionrio, para uma presso e temperatura determinadas. Em outras palavras,
59
um estado de equilbrio foi atingido e, como sabemos, um estado de equilbrio
dinmico, sendo o estado estacionrio apenas aparente, pois as reaes se
processam em direes opostas com a mesma velocidade. No estado de equilbrio,
o sistema contm uma certa quantidade de reagentes e de produtos. Muitas
reaes qumicas so aparentemente completas, mas na realidade, a reao inversa
tem lugar com uma intensidade to pequena que as propores dos reagentes esto
alm dos limites de determinao pelos meios comuns (47).
A termodinmica estabeleceu a seguinte relao fundamental:
G = G + RT ln J
eq.(2)
onde:
PUC-Rio - Certificao Digital N 0321309/CA
G: variao de energia livre de Gibb, (em calorias da reao).
G: variao de energia livre padro da reao.
R: constante universal dos gases ideais (1,987 cal/mol.K)
T: temperatura absoluta, (K).
J: quociente reacional.
A segunda lei da termodinmica forneceu o critrio fundamental de
equilbrio nos sistemas em reao:
No equilbrio: G = 0.
Mais ainda, atravs da segunda lei demonstra-se que os sistemas tendem a
reagir na direo de um mnimo de energia livre.
O grande significado da eq. (2) o fato de que ela proporciona um meio de
determinar se uma reao particular termodinamicamente possvel ou no, sob
determinadas condies. Dito em outras palavras, permite saber a qualquer
momento, se o processo est ou no no equilbrio, e ainda, se no est, indica em
qual direo ele tende a caminhar.
60
Para que uma reao seja espontnea, G temperatura e presso
constantes deve ser negativo.
Se a temperatura (sempre mantida constante) e as presses parciais dos
gases envolvidos na reao qumica so tais que o sistema est em equilbrio,
ento G = 0, portanto J = K, obtemos:
G = - RT lnK
eq.(3)
Onde:
K: constante de equilbrio
Se um elemento forma vrios xidos com o oxignio, a estabilidade do
oxido inferior de suma importncia no processo gradual de reduo (caso do Fe
PUC-Rio - Certificao Digital N 0321309/CA
e do M, por exemplo). Os xidos inferiores so mais estveis que os superiores, e
so por tanto mais difceis de reduzir. Logo a obteno de um metal depender da
estabilidade de seu oxido inferior (47).
O diagrama u O2 x T permite no somente caracterizar a estabilidade dos
vrios xidos, mas tambm determinar a possibilidade de se usar vrios elementos
como agentes redutores.
No caso particular das ferro-ligas a caracterstica essencial que a reduo
dos xidos realizada na presena de ferro e seus xidos, o que facilita
consideravelmente o processo de reduo. Isto pode ser explicado pelas seguintes
razes (47):
a) Os xidos de ferro so muito mais facilmente reduzidos do que os outros,
do que resulta condies mais favorveis de G do sistema.
b) Ao dissolver os elementos reduzidos, o ferro abaixa as atividades
respectivas, facilitando a reduo.
61
c) Dissolvendo o elemento reduzido, o ferro o remove da rea da reao,
impedindo assim o desenvolvimento de reaes secundarias (oxidao),
bem como a volatilizao do elemento.
d) Em geral, o ferro-liga tem ponto de fuso inferior ao do elemento de liga
quando puro. Resulta que a produo de ferro-liga conduzida numa
temperatura inferior aquela que seria necessria para a obteno do
elemento puro.
Isso explica porque se prefere utilizar em siderurgia os ferro-ligas no lugar
dos elementos de liga puros.
Como os minrios de mangans sempre contm xidos de ferro e o ferro
incorpora-se na fase metlica (29). Estes teores de ferro esto variando entre 1,5 %
PUC-Rio - Certificao Digital N 0321309/CA
e 2,5 %, ademais o ferro reduzido simultaneamente com o mangans. O produto
deste processo chamado de ligas Fe Mn.
As ligas Fe-Mn fabricadas tm em mdia teores de mangans entre 66% e
78% e os teores de ferro variando entre 13% e 19 %. Por conseguinte, no estudo
da reduo do minrio de mangans e em especial dos aglomerados autoredutores, temos que levar em conta os processos de reduo destes metais e suas
interaes (30).
O conhecimento termodinmico do sistema Mn-C muito importante para
melhorar o processo de produo de ferro-mangans (13).
Segundo os relatos de Anacleto, Ostrovski e Ganguly
(9)
, os xidos de
mangans e os minrios de mangans em estado slido, so reduzidos por coque,
hidrognio ou monxido de carbono, somente at MnO. Isso pode ser visto no
diagrama de estabilidade da figura 10.
62
PUC-Rio - Certificao Digital N 0321309/CA
Figura 3 - Diagrama de estabilidade para o sistema Mn-O-C a 1000C (9).
Pode se ver na figura acima, que em temperaturas nas quais o minrio de
mangans slido (abaixo de 1200C), so necessrios baixas presses parciais
de oxignio (PO2) para a reduo de MnO a mangans metlico ou a carbeto de
mangans, tais condies, no sentido prtico no so atingidos usando carbono
slido, hidrognio ou monxido de carbono (9).
O mangans pode ter estados de oxidao entre Mn+3 e Mn+7, sendo que os
estados de oxidao mais conhecidos so Mn+4 e Mn+2. O estado de oxidao dos
principais minrios o Mn+4 e o estado de oxidao dos principais compostos
qumicos de mangans o Mn+2.
O aquecimento em condies controladas (decomposio destes xidos ao
ar) dos xidos de mangans pode lev-los a nveis de oxidao mais baixos (30):
Sendo as reaes de dissociao as seguintes:
4 MnO2
2 Mn2O3 + O2
eq.(4)
6 Mn2O3
4 Mn3O4 + O2
eq.(5)
63
2 Mn3O4
2 MnO
6 MnO + O2
eq.(6)
2 Mn + O2
eq.(7)
PUC-Rio - Certificao Digital N 0321309/CA
As variaes de energia livre para estas reaes de dissociao so (36):
G4 = 40185 51,28 T
cal / mol O2
eq.(8)
G5 = 44204 - 36,89 T
cal / mol O2
eq.(9)
G6 = 104844 55,46 T
cal / mol O2
eq.(10)
G7 = 186742 36,65 T
cal / mol O2
eq.(11)
No caso do ferro, ele apresenta as seguintes etapas de decomposio:
6 Fe2O3
4 Fe3O4 + O2
eq.(12)
2 Fe3O4
6 FeO + O2
eq.(13)
2 FeO
2 Fe + O2
eq.(14)
As variaes de energia livre para estas reaes de dissociao so (36):
G12 = 114287 65,93 T cal / mol CO2
eq.(15)
G13 = 158969 54,89 T cal / mol CO2
eq.(16)
G14 = 126645 30,90 T
eq.(17)
cal / mol CO2
64
Para se gerar um diagrama de Predominncia de Fases na qual possam-se
ver as condies nas quais os xidos de mangans e de ferro atingiro a fase
metlica, consideramos tambm a reao seguinte:
2 CO2
2 CO + O2
eq.(18)
Com variao de energia livre padro de:
G18 = - 134923 + 40,93 T cal / mol O2
eq.(19)
Ento, considerando agora as reaes de (4) a (7) com seus dados
termodinmicos de (8) a (11) e as reaes de (12) a (14) com seus respectivos
dados termodinmicos de (15) a (17) e tambm a reao (18) e a eq.(19), alm
atividades iguais a 1, conseguimos levantar o diagrama da figura 11.
Diagrama de Estabilidade: Presso parcial de O2 em equilibrio com xidos puros
de Mn e Fe. Presso=1 atm
a) 4MnO2 = 2Mn2O3 + O2
0
b) 6Mn2O3 = 4Mn3O4 + O2
-5
c) 2Mn3O4 = 6MnO + O2
-10
Log P O2 ( atm )
PUC-Rio - Certificao Digital N 0321309/CA
disso, consideramos puros o carbono, os xidos e os metais, ou seja, com
d) 2MnO = 2 Mn + O2
-15
-20
e) 6Fe2O3 = 4Fe3O4 + O2
-25
f ) 2Fe3O4 = 6FeO + O2
-30
g) 2 FeO = 2 Fe + O2
-35
h) 2CO + O2 = 2 CO2
-40
673
873
1073
1273
1473
1673
T ( K)
Figura 4 - Presso parcial de oxignio em equilbrio com xidos puros de mangans e de
ferro. Presso total de 1 atm.
65
Observando-se esta figura, e fazendo uma anlise na temperatura de
1250C, pode se determinar que a presso parcial de O2 em equilbrio com a
decomposio do FeO da ordem de 10 -12 atm e para a decomposio do MnO
da ordem de 10-18 atm. Como a presso parcial de O2 em equilbrio no sistema CCO-CO2 nesta temperatura da ordem de 10-16 atm, neste caso, conclumos que
possvel ocorrer reduo do ferro e impossvel a obteno de Mn metlico puro,
isso para atividades unitrias de C, Fe, Mn e seus xidos.
A termodinmica da reduo de xidos de mangans e de ferro pelo
carbono, pode ter uma compreenso melhor com referncia no Diagrama de
Ellingham (5,21).
Como mencionado no trabalho de Welham (21), o diagrama de Ellingham
PUC-Rio - Certificao Digital N 0321309/CA
para o sistema Mn-O-C, calculado para uma presso total de 1 atm. e apresentado
na figura embaixo, indica que o MnO2 pode espontaneamente se reduzir sob
aquecimento em temperaturas maiores a 510 C e o Mn2O3 formado pode tambm
se reduzir sob aquecimento a temperaturas maiores a 915C, gerando Mn3O4. A
perda de oxignio durante o aquecimento da Pirolusita (MnO2) foi observado
previamente a 500C e para Mn2O3 a 900C pelo Stobbe et al (31).
A reduo de MnO pelo carbono a presso atmosfrica somente factvel
em temperaturas maiores a 1410C
(21,34)
. Welham
(21)
, tambm acrescenta
comentrios e indica que este fato explica o uso do alumnio como redutor de
minrios de ferro e mangans na produo de ferro-mangans.
Dando continuidade ao trabalho de Welham (21), referente temperatura de
reduo de MnO pelo carbono, o autor acrescenta que esta temperatura mnima
pode ser baixada pela diminuio da presso no curso da reduo, mas isso no
acontece na prtica e o autor no considera esse fato no seu trabalho. A figura 12
tambm indica que o MnO e o CO2 esto em equilbrio de fases esperado num
sistema a 25C.
PUC-Rio - Certificao Digital N 0321309/CA
66
Figura 5 - Diagrama de Ellingham para o sistema Mn-O-C, para 1 atm de presso total
(21)
Reforando o dito por Welham
(21)
, Vanderstaay et al.
(5)
indicam que o
mangans se apresenta na forma de quatro xidos, onde o xido primrio MnO2
o maior constituinte dos minrios de mangans. Ademais indica que acima de
1000C, o MnO2 e Mn2O3 so dissociados termicamente para Mn3O4. Este xido
prontamente reduzido por qualquer carbono ou mistura de gs com PCO/ PCO2 = 1
para MnO, levando em considerao que a reduo de Fe3O4 para FeO requer
qualquer carbono ou mistura de gs com maior quantidade de CO (g) (5).
A composio de equilbrio termodinmico de uma mistura de MnO2 e
carbono tambm foi estudado por Welham (21) e apresentado na figura 13, onde
mostra a provvel composio de equilbrio para MnO2 reagindo com quantidades
incrementadas de carbono a uma presso de 1 atm.
PUC-Rio - Certificao Digital N 0321309/CA
67
Figura 6 - Composio de equilbrio termodinmico da mistura de MnO2 e Carbono,
como funo da quantidade de C a 25C, 75C e 105C e a presso de 1 atm (21) .
Da figura acima podem ser feitas diversas observaes (21):
* a reduo prevista para acontecer mesmo a 25C.
* a reduo acontece provavelmente em vrios estgios com a continuao
da reduo via fases de xidos intermedirios:
MnO2 ----- Mn2O3 ---- Mn3O4 --- MnO.
* a reduo incompleta abaixo de 150C, e
* necessrio uma relao molar MnO2 / C de 2 : 1 para completar a
reduo at MnO.
Observando a mesma figura, interessante notar que mesmo na presena
de excesso de carbono, o MnO no se reduz nem carbetos de mangans so
formados
(21)
. Este acontecimento explicado por Zaki et al.
(33)
, no seu trabalho
onde indica que deve ser notado que esses clculos foram feitos considerando
somente essas fases para as quais dados termodinmicos foram disponveis (33).
68
Vanderstaay et al.
(5)
, com a finalidade de ter uma melhor compreenso e
visualizao da reduo destes xidos apresenta o Diagrama de Ellingham para os
xidos de mangans, ferro e carbono, que visto na figura 14, onde pode se ver
que a reduo pelo carbono de FeO para Fe na condio padro possvel acima
de 750C visto que a reduo de MnO para Mn somente possvel a temperaturas
muito altas, aproximadamente 1420C
(5,29, 34)
. A concluso que os xidos de
ferro da carga sejam reduzidas completamente para ferro durante a fuso, visto
que xidos de mangans requerem condies de reduo mais fortes, embora a
PUC-Rio - Certificao Digital N 0321309/CA
recuperao de mangans no ser completa.
Figura 7 - Diagrama de Ellingham para xidos de Mangans, Ferro e Carbono (5).
Na figura 14, no se apresenta a linha correspondente a Si / O2(g) / SiO2 a
qual est um pouco abaixo da linha de Mn / O2(g) / MnO. Ento, condies de
69
reduo mais fortes aumentariam a recuperao de mangans, mas tambm
aumentariam a reduo da SiO2 para Si (5).
6.2.1.
Diagrama de equilbrio Ferro Mangans
O mangans tem quatro formas alotrpicas (, , , ) com as seguintes
faixas de temperatura de existncia estvel (46):
- at 727C , Mn .
- 1100 1135C, Mn , e
- 1135 1245C, Mn .
PUC-Rio - Certificao Digital N 0321309/CA
O Mn possui a rede tetragonal de faces centradas (TFC), muito prxima,
no que diz respeito a seus parmetros, da rede de faces centradas Fe . Este o
fator que origina a formao duma soluo slida contnua com Fe e Mn (46).
O diagrama de equilbrio do sistema ferro-mangans do tipo aberto e
mostra quatro formas de mangans. O ferro livremente solvel no mangans e
no e forma um intervalo completo de solues slidas com o mangans ,
cbico de faces centradas, e claro que os tomos de ferro e mangans se
assemelham muito um ao outro (45).
O diagrama Fe-Mn mostra as fases presentes em condies to prximas do
equilbrio verdadeiro quanto possam ser obtidas por resfriamento muito lento ou
recozimento muito prolongado. A figura 15 mostra o diagrama de equilbrio do
sistema Fe-Mn.
Como se pode ver no diagrama Fe-Mn, a temperatura de fuso do Mn de
1245C. Ligas de Fe-Mn com teores at 25% de Fe apresentam temperaturas
liquidus menores que 1250C que tambm visualizado no diagrama.
PUC-Rio - Certificao Digital N 0321309/CA
70
Figura 8 - Diagrama de equilbrio do sistema Fe- Mn (45).
Assim, espera-se que o produto da reao de reduo temperatura de
1250C seja uma liga no estado lquido, podendo esta ser uma liga de mangans
contendo baixos teores de outros elementos de liga ou ainda, uma liga Fe-Mn com
teores de Ferro variando at 25 % (30).
Como todos os aos contm mangans, no possvel traar uma linha
divisria entre aos carbono e aos ligados contendo mangans. O mangans
adicionado aos aos carbono para neutralizar os efeitos prejudiciais do enxofre.
Na ausncia de mangans, este enxofre fica principalmente na forma de sulfeto
ferroso, FeS, que forma euttico de baixo ponto de fuso com o ferro, isto gera a
existncia de filmes frgeis ao redor dos cristais primrios formados na
solidificao. O baixo ponto de fuso responsvel pelo fenmeno de fragilidade
a quente na laminao. A adio de mangans resulta na formao de sulfeto
71
manganoso, muito estvel, de alto ponto de fuso e que se mantm slido
temperatura de laminao (45).
Quando o enxfre no anormalmente alto, pode-se considerar como
limite superior para aos carbono um teor de mangans da ordem de 0,8%;
adies maiores de mangans levam principalmente obteno de aos perlticos,
nos quais o efeito do mangans produzir endurecimento por soluo slida da
matriz ferrtica e refinar apreciavelmente a estrutura da perlita.
A adio de mangans abaixa a temperatura do eutetide e a percentagem
PUC-Rio - Certificao Digital N 0321309/CA
de carbono da composio eutetide, como mostra a figura 16.
Figura 9 - Efeito de alguns metais comuns sobre a temperatura e composio eutetide
nos aos (45).
Assim como o nquel, o mangans poderoso estabilizador de . Com
adies ainda maiores de mangans, possvel obter-se aos mangans
72
austenticos, dos quais o mais conhecido o ao austentico Hadfield; este foi
desenvolvido a partir de 1890 aproximadamente e contm 13% Mn e 1,2% C em
peso (45).
Na figura 17 se podem ver as relaes de equilbrio nas ligas Fe-Mn-C e
mostrando tambm que a composio do ao Hadfield no esto no campo
temperatura ambiente. Por isto, estes aos so austenitizados a temperaturas da
ordem de 1000C ou mais e depois so resfriados bruscamente para reter a
estrutura austentica. Esta estrutura mantm-se tenaz a baixas temperaturas e
apresenta notvel endurecimento por encruamento, o que muito til em
PUC-Rio - Certificao Digital N 0321309/CA
aplicaes que exijam resistncia ao impacto, como trilhos, por exemplo.
Figura 10 - Sistema Fe-Mn-C, mostrando a seo vertical do diagrama ternrio em 13%
Mn (45), para o ao Hadfield.
A alta temperatura na qual estes aos so austenitizados pode provocar
descarbonetao superficial, esta regio, aps o resfriamento, transforma-se numa
casca frgil de martensita; em algumas ligas este efeito reduzido com adies
de nquel, que estabiliza as ligas com menor teor de carbono e assim neutraliza a
tendncia para formao de martensita e compensa a perda de carbono (45).
73
6.2.2.
Reduo dos xidos de mangans e de ferro pelo monxido de
carbono
Nos processos de fabricao das ferro-ligas de mangans, praticamente todo
o Fe presente no minrio reduzido a metal, como tambm 80-90% do Mn
presente no mesmo. Portanto o estudo termodinmico do processo de reduo dos
minrios de mangans deve considerar a reduo conjunta dos dois metais em
presena de carbono.
A reduo do ferro pelo CO(g), comeando pelo maior estado de oxidao
do ferro que a Hematita (Fe2O3), acontece em trs estgios
(38)
, para
temperaturas acima de 570C:
PUC-Rio - Certificao Digital N 0321309/CA
II
Fe2O3
Fe3O4
III
FexO
Fe
So apresentados a seguir os calores de reao a 25C destas trs reaes
(39)
3Fe2O3 + CO
2Fe3O4 + CO2
H = - 10317 cal
eq.(20)
Fe3O4 + CO
3FexO + CO2
H = 7223 cal
eq.(21)
Fe + CO2
H = - 4139 cal
eq.(22)
FexO + CO
Como pode ser visto, as entalpias envolvidas das reaes (20) e (22) so
exotrmicas, enquanto que a reao (21) endotrmica.
Para temperaturas abaixo de 570C, o FexO chamado de wustita,
metaestvel e a reduo em baixas temperaturas ocorre em apenas dois estgios,
ao invs de trs como no caso anterior. Porm, a magnetita produzida de acordo
com a reao (20) reduzida a ferro diretamente, ou seja, sem passar pela reao
(21) formadora de FexO:
74
Fe3O4 + CO
Fe + CO2
H = - 936 cal
eq.(23)
Como as reaes de reduo dos xidos de ferro ocorrem em temperaturas
acima de 570C, as etapas da reao global de reduo de Fe2O3 para FexOe Fe
esto apresentados nas reaes (20), (21) e (22), as quais apresentam as seguintes
PUC-Rio - Certificao Digital N 0321309/CA
variaes de energia livre (36):
G20 = - 10317 12,50 T
cal / mol CO2
eq.(24)
G21 =
7223 6,98 T
cal / mol CO2
eq.(25)
G22 = - 4139 + 5,01 T
cal / mol CO2
eq.(26)
Para as reaes (20), (21) e (22) podem-se calcular as constantes de
equilbrio para uma dada temperatura conhecendo-se as variaes de energia livre
no estado padro:
K20 = (a Fe3O4)2 * PCO2 / (aFe2O3)3 * PCO
eq.(27)
K21 = (aFeO)3 * PCO2 / aFe3O4 * PCO
eq.(28)
K22 = aFe * PCO2 / aFeO * PCO
eq.(29)
Para o caso dos xidos de mangans, a reduo do mangans na forma de
Mn
+4
para Mn+2 ocorre basicamente em trs etapas, e em presena de carbono as
reaes so exotrmicas, com exceo da reduo do Mn3O4 para MnO que por
sua vez ela endotrmica.
2 MnO2 + CO(g)
Mn2O3 + CO2 (g)
eq.(30)
75
3 Mn2O3 + CO(g)
2 Mn3O4 + CO2(g)
eq.(31)
Mn3O4 + CO(g)
3 MnO + CO2 (g)
eq.(32)
CO2(g) + C
2 CO(g)
eq.(33)
PUC-Rio - Certificao Digital N 0321309/CA
As variaes de energia livre para estas reaes so (36):
G30 = - 47368 5,17 T
cal / mol CO2
eq.(34)
G31 = - 45359 + 2,02 T
cal / mol CO2
eq.(35)
G32 = - 15039 7,26 T
cal / mol CO2
eq.(36)
G33 =
39995 41,06 T cal / mol CO2
eq.(37)
Para as reaes (30), (31), (32) e (33) podem-se calcular as constantes de
equilbrio para uma dada temperatura conhecendo-se as variaes de energia livre
no estado padro:
K30 = (a Mn2O3) * PCO2 / (aMnO2)2 *PCO
eq.(38)
K31 = (a Mn3O4)2 * PCO2 / (a Mn2O3)3 * PCO
eq.(39)
K32 = (a MnO)3 * PCO2 / a Mn3O4 * PCO
eq.(40)
K33 = (PCO)2 / (PCO2) * a C
eq.(41)
Na reduo dos xidos slidos pelo carbono, o agente redutor efetivo o
CO(g), mas a presso parcial de CO2 produzida no aumenta devido reao de
Boudouard, pela qual CO(g) continuamente formado. Como j vimos, as
76
relaes termodinmicas para o processo correspondem reduo pelo carbono
com interveno gasosa, dizer, com formao de uma mistura CO - CO2 em
equilbrio numa dada temperatura, enquanto que a taxa de reduo depender da
velocidade das reaes gs-slido envolvidas (47).
Quando a reao ocorre em presena de carbono, o CO2 gerado reage com
este carbono a partir de temperaturas em torno de 800C segundo a reao (33).
Na eq. (41) onde se considera a atividade do C igual a 1, tem-se a constante de
equilbrio a uma dada temperatura da reao de Boudouard.
Os mecanismos de reduo de MnO anlogo aos de FeO.
Em
temperaturas acima de 1000C, o mecanismo predominante a reduo direta na
PUC-Rio - Certificao Digital N 0321309/CA
qual o xido aparece na reao diretamente com o carbono (5).
A reduo do MnO pelo monxido de carbono:
MnO + CO(g)
Mn + CO2(g)
eq.(42)
Com variao de energia livre (36):
G42 =
25909 + 2,14 T
cal / mol CO2
eq.(43)
e a sua constante de equilbrio para uma dada temperatura :
K42 = (a Mn) * PCO2 / a MnO * PCO
eq.(44)
A reduo do MnO ocorre realmente de acordo com a reao (42), mas
como logo em seguida ocorre a reao de Boudouard (33), podemos representar a
reduo como sendo a soma das duas reaes (5,30,47), ou seja:
MnO + CO(g)
Mn + CO2(g)
eq.(42)
CO2(g) + C
2 CO(g)
eq.(33)
ento, obtemos:
77
MnO + C
Mn + CO(g)
com variao de energia livre
G45 =
eq.(45)
(36)
65904 - 38,92 T cal / mol
eq.(46)
e a sua constante de equilbrio para uma dada temperatura :
K45 = (a Mn * PCO) / (a MnO * a C)
eq.(47)
A reao (45) a reao global da reduo do MnO e o produto da
reao de reduo por CO(g) e conseqente gaseificao de carbono pela reao
PUC-Rio - Certificao Digital N 0321309/CA
de Boudouard.
Os processos de reduo direta so muito endotrmicos e precisam de
calor dentro do forno
(5)
. Em temperaturas abaixo de 1000C, o processo de
reduo conhecido como reduo indireta e procede de acordo com a reao de
Boudouard. As reaes de reduo indiretas so exotrmicas (5).
No forno eltrico a arco, a reduo direta ocorre na regio mais quente
abaixo dos eletrodos em quanto que a reduo indireta ocorre na carga mais fria
(5)
. Ambas as zonas so aquecidas e reduzidas pelo CO(g).
A temperatura na qual os xidos sero reduzidos pelo monxido de carbono
depende termodinamicamente, da composio dos gases no forno (47).
Silveira
(47)
, por meio de sondagens em um forno eltrico para a produo
de gusa, operando com carvo vegetal, determinou a evoluo da composio dos
gases, em CO e CO2, atravs do forno.
Para temperaturas inferiores a 800C em fornos operados com carvo
vegetal, e 950C em fornos operados com coque, a relao em CO e CO2 dos
78
gases vai depender da quantidade de oxignio a ser extrada da carga at 800C ou
950C respectivamente, conforme o redutor utilizado e do consumo de redutor.
Espera-se que o gs de topo na produo de FeMn, seja mais oxidado do
que na produo de gusa. Mas, por outro lado, o maior consumo de carbono na
fabricao de FeMn em relao ao gusa, ocasiona um volume maior de gases, que
leva a um aumento da relao CO / CO+CO2 do gs de topo(47). de se esperar
que, como uma primeira aproximao, a relao CO / CO+CO2 dos gases no seja
alterada substancialmente quando se passa da produo de gusa para FeMn, de
modo que o comportamento termodinmico dos xidos seja alterado.
Na produo de ferro-mangans alto carbono em fornos eltricos operados a
coque, a relao CO / CO+CO2 do gs de topo em torno de 0,60 para basicidade
PUC-Rio - Certificao Digital N 0321309/CA
de 0,7 e para uma %MnO na escria de 40% e, tm-se uma relao CO /
CO+CO2 de 0,8 para basicidade de 1,2 e uma %MnO na escria de 20%. Quando
o forno opera com carvo vegetal, a relao CO / CO+CO2 atinge valores at 0,6
para basicidade de 1,2 e 20% de MnO na escria(47).
6.2.3.
A gaseificao do carbono (reao de Boudouard)
O carbono forma dois xidos (47):
C(s) + O2(g)
2C(s) + O2(g)
CO2(g)
2CO(g)
eq.(48)
eq.(49)
as correspondentes energias livres padro de formao so:
G48 = - 94928 0,13 T
cal / mol O2
eq.(50)
G49 = - 54933 41,19 T
cal / mol O2
eq.(51)
79
Para a reao (48), S aproximadamente nulo, pois no h variao no
nmero de moles gasosos. Resulta ento que a reta do CO2 no diagrama de
potencial de oxignio paralela ao eixo horizontal.
Para a reao (49) S positivo, do que resulta para o CO inclinao
contrria dos demais xidos. Significa que o CO tem estabilidade crescente com
o aumento da temperatura (38,47).
O carbono ocupa uma posio nica como redutor devido a seu baixo custo,
e o fato de que enquanto o elemento virtualmente no-volatil, forma dois xidos
volteis.
PUC-Rio - Certificao Digital N 0321309/CA
Como j se tem dito, na reduo dos xidos slidos pelo carbono, o agente
redutor efetivo o CO(g), mas a presso parcial de CO2(g) no aumenta devido
reao de Boudouard, pela qual o CO(g) continuamente formado (47):
CO2 + C
2 CO
G33 =
39995 41,06 T cal / mol CO2
eq.(33)
eq.(37)
A reao de Boudouard forma a base para a reduo carbotrmica de metais
e extremamente importante em processos de reduo envolvendo carbono como
agente redutor, tendo como exemplo os processos no alto forno.
No Diagrama de Ellingham da figura 14, pode-se ver que a 1 atm, a energia
livre padro da oxidao de carbono para formar monxido de carbono CO(g) e
para formar dixido de carbono CO2(g) esto mesma temperatura,
aproximadamente 710C, ou seja, as duas linhas de formao dos dois xidos de
carbono se cortam nessa temperatura. Abaixo desta temperatura o CO(g) o
agente redutor mais ativo, visto que acima desta, o grafite slido o agente
redutor mais ativo.
80
A oxidao de carbono produzir uma mistura de CO(g) e CO2(g), mas
sob baixas temperaturas o CO2(g) ser o componente predominante da fase gasosa
em equilbrio com carbono slido, visto que em altas temperaturas o CO(g) tornase o componente gasoso predominante.
As condies de equilbrio da reao se calculam mediante a constante de
equilbrio, como segue:
K33 = (PCO)2 / (PCO2 * a C)
eq.(41)
e considerando a reao com carbono sob a forma de grafite, isto , na sua forma
padro, sendo portanto aC = 1, resulta:
PUC-Rio - Certificao Digital N 0321309/CA
K33 = (PCO)2 / PCO2
eq.(52)
e sendo a presso total do sistema igual soma das presses parciais, temos:
P total = P CO(g) + P CO2(g)
eq.(53)
A constante de equilbrio da eq.(49) se calcula em funo da energia livre
como funo da temperatura, atravs da equao:
ln K33 = - G33 / RT
eq.(54)
Ento fazendo uso destas relaes, podemos representar graficamente na
figura 18 a Curva de Boudouard, que mostra a composio da mistura gasosa
em equilbrio com o carbono.
81
CO2 + C = 2 CO(g)
1
CO2
frao molar de CO(g) : N CO
0,9
0,8
0,7
Diag. Boudouard a
P total = 1 atm
0,6
0,5
CO
0,4
0,3
0,2
0,1
0
PUC-Rio - Certificao Digital N 0321309/CA
200
400
600
800
1000
1200
1400
1600
1800
2000
Temperatura ( C )
Figura 11 - Curva de equilbrio da reao de Boudouard.
6.2.3.1.
Efeito da presso sobre a reao de Boudouard
Note-se na figura seguinte, a influncia da presso sobre o equilbrio do
sistema. Como pode se observar da reao de Boudouard, um volume de CO2(g)
produz dois volumes de CO(g) presso constante, logo esta reao causar um
aumento na presso total do sistema.
Como seria de se esperar pelo Principio de Le Chatelier, um decrscimo de
presso favorece o processamento da reao (CO2 + C = 2 CO ) da esquerda para
a direita, isto , a produo de CO(g); enquanto que, um acrscimo de presso
favorece a produo de CO2 (47), decompondo o CO(g) em CO2(g) e C. Por outro
lado, para manter a mesma relao CO / CO2, em presses maiores, a temperatura
aumentaria.
Resumindo, na figura 19 pode-se ver que para aumentos de presso a
curva de equilbrio da reao de Boudouard desloca-se para a direita e para
decrscimos de presso desloca-se para a esquerda.
82
Curva de Boudouard
1
0,9
frao molar de CO(g)
0,8
0,7
P total = 1 atm
P total = 0,1 atm
0,6
P total = 10 atm
0,5
0,4
0,3
0,2
0,1
0
PUC-Rio - Certificao Digital N 0321309/CA
200
400
600
800
1000
1200
1400
1600
1800
2000
Temperatura (C)
Figura 12 - Efeito da variao na presso sobre o equilbrio da reao de Boudouard.
6.2.4.
Diagrama Operacional de Predominncia de Fases Fe C O
A termodinmica de reduo dos xidos de ferro estuda o equilbrio entre os
xidos e os agentes redutores. Os diagramas de predominncia das reaes de
reduo relacionam as composies gasosas no equilbrio, com a temperatura.
Estas composies gasosas no equilbrio podem ser calculadas a partir das
constantes de equilbrio K.
A figura 20 mostra o equilbrio para o sistema Fe-C-O o qual muito
importante para os processos de reduo dos xidos de ferro (43). Da figura pode se
ver que em temperaturas acima de 710C, todos os xidos de ferro podem ser
reduzidos por misturas de CO/CO2 a uma presso total de 1 atm os quais esto em
equilbrio com carbono e podem ser reduzidos conseqentemente pelo prprio
carbono (43).
83
Diagrama de Predominncia dos xidos de Ferro
1
frao m o lar d e C O (g ) : N C O
0,9
3 Fe2O3 (s) + CO(g) = 2 Fe3O4 + CO2
0,8
Fe3O4(s) + CO = 3 "FeO" + CO2
0,7
Fe3O4 (s) + CO (g) = 3FeO (l) + CO2 (g)
0,6
Fe3O4(s) + 4CO = 3Fe(s) + 4CO2(g)
0,5
0,4
" FeO" + CO(g) = Fe(s) + CO2(g)
0,3
FeO(l) + CO(g) = Fe(s) + CO2(g)
0,2
CO2 + C = 2 CO(g)
PUC-Rio - Certificao Digital N 0321309/CA
0,1
0
200
400
600
800 1000 1200 1400 1600
Temperatura ( C )
Figura 13 - Diagrama de Predominncia Operacional Fe-C-O. Equilbrio entre os xidos
de ferro, o CO, o CO2 e C. P CO(g) + P CO2(g) = 1 atm.
A baixas temperaturas s algumas misturas tm ao de reduo sobre
wustita a qual esta supersaturada com carbono e que conseqentemente, de acordo
reao de Boudouard, deve reagir para a deposio de carbono (43).
Segundo Treptow
(38)
e Ross
(39)
o diagrama de predominncia mostra as
zonas onde as fases so estveis, numa atmosfera de mistura de gases CO e CO2,
para uma presso total das fases gasosas igual a 1 atm. Se a atmosfera tem uma
alta relao PCO/PCO2, ser um forte agente redutor e existir Fe(s) ou Fe(l). Por
outro lado, se a relao baixa, a atmosfera atua como um agente oxidante e
xidos de ferro sero estveis (38).
Para ilustrar a aplicao deste diagrama, consideremos uma temperatura de
800C com a fase gasosa contendo 20% de CO, nestas condies a fase estvel
magnetita (Fe3O4). Isto significa que, se a composio do gs permanecer
constante, a reao (20) ir ocorrer no sentido indicado, ou seja, a hematita
84
(Fe2O3) ser reduzida a magnetita; mas as reaes (21) e (22) iro ocorrer no
sentido contrario ao indicado, ou seja, iro se oxidar o ferro e a wustita para
magnetita (39).
Ento este diagrama, conhecido como Diagrama de Chaudron fornece as
fronteiras de ocorrncia dos xidos de ferro e do ferro metlico, em funo da
temperatura e do potencial redutor da atmosfera gasosa. Pode-se ento a partir de
qualquer temperatura, definir-se a relao CO/CO2 necessria para que as reaes
de reduo ocorram at cada estado de oxidao possvel ( Fe2O3, Fe3O4,Fe(1-x)O
e Fe ) (37,38).
PUC-Rio - Certificao Digital N 0321309/CA
6.3.
Cintica da reduo carbotrmica dos xidos de mangans e de
ferro
O estado final de uma reao pode ser previsto usando conceitos de
termodinmica, sem embargo, esta cincia no proporciona informao alguma
acerca da rapidez com que pode se alcanar o equilbrio
(29)
. A cintica estuda os
processos longe do equilbrio e na coordenada tempo, ela, no s til no
desenho de reatores seno tambm na investigao dos mecanismos de reao. Ao
conhecer as etapas atravs das quais se verifica uma reao, ento temos as
condies para favorec-la ou inhibi-la (61).
6.3.1.
Mecanismos da reao de Boudouard (gaseificao do carbono)
Com o intuito do entendimento dos mecanismos que governam a reao de
Boudouard, muitos trabalhos indicam que os principais fatores que afetam a
cintica da reao so (37,61):
- Temperatura
- Caractersticas da atmosfera gasosa
- Tipo de material carbonoso (porosidade, estrutura qumica, etc).
- Condies experimentais (por exemplo, eficincia de transferncia de
calor para a reao que altamente endotrmica).
- Condies de pre-aquecimento, etc.
85
- Catlise, por exemplo, dos componentes das cinzas do carvo.
A gaseificao de carbono acontece segundo etapas qumicas e fsicas
principais (61):
- difuso interna e intraparticular dos gases reagentes e produtos, e
- reao qumica com adsoro e desoro nos stios livres da superfcie de
carbono.
De um modo geral, considerado que existem diferentes regimes de
temperatura que correspondem a diferentes etapas limitantes da reao. A baixas
temperaturas, a velocidade depende da reao qumica. A temperaturas medias e
mais altas, as etapas controladoras seriam as difuses atravs das partculas
porosas de carbono e transferncia de CO2 para a superfcie externa das partculas.
PUC-Rio - Certificao Digital N 0321309/CA
As temperaturas limites entre estes regimes iro depender das variveis do
processo.
Diferentes mecanismos para a reao de Boudouard j foram propostos,
sendo que, atualmente aceito o seguinte mecanismo bsico de reao (61):
1) Troca reversvel de oxignio entre o CO2 da fase gasosa e a superfcie
de carbono:
Cf (s) + CO2 (g) = (O) c + CO (g)
eq.(55)
2) Desoro irreversvel de CO na fase gasosa aps a reao entre o
oxignio adsorvido e a superfcie de carbono:
( O )c
CO (g) + Cf (s)
eq. (56)
onde:
Cf e (O)c so, respectivamente, stios livres e ocupados na
superfcie de carbono.
86
Valores de energias de ativao para a gaseificao de carbono entre 170 a
380 KJ/mol so encontrados na literatura, variam principalmente em funo do
tipo (reatividade) do carbono.
6.3.2.
Cintica das reaes de auto-reduo
Devido a sua grande importncia nos processos emergentes de reduo,
como a utilizao de aglomerados auto-redutores nos processos clssicos, as
reaes de auto-reduo so foco de varias pesquisas aplicadas, estas pesquisas
foram iniciadas devido ao desenvolvimento do processo SL/RN que usa carbono
slido como redutor na produo de ferro.
PUC-Rio - Certificao Digital N 0321309/CA
Muitos autores sugerem que a cintica de auto-reduo seja controlada pela
transferncia de calor para o aglomerado e pela reao de oxidao e gaseificao
de carbono.
J foram utilizadas em varias pesquisas, misturas de xido de ferro com
carbono e considera-se como consenso que a reao global de auto-reduo ocorre
via a reao slido-slido via intermedirios gasosos, que seriam produtos
formados pelas seguintes reaes que ocorrem paralelamente (37,61):
FexOy
(s)
+ CO (g) = FexOy -1 (s) + CO2 (g)
eq.(57)
ou
FexOy (s) + yCO (g) = xFe (s) + yCO2 (g)
xC (s) + xCO2 (g) = 2xCO(g)
eq. (58)
eq. (59)
Estequiometricamente, a reao global de reduo seria:
FexOy (s) + xC (s) = FexOy-1 (s) + (2x-1)CO (g) + (1-x)CO2 (g)
eq.(60)
ou
FexOy
(s)
+ xC (s) = xFe (s) + (2x-y)CO (g) + (y-x)CO2 (g)
eq.(61)
87
As reaes reais slido-slido entre os gros de xido de ferro e de carbono,
ocorrem de maneira muito limitada, por ter cintica desfavorvel, podendo ser
desprezadas sem afetar as anlises dos mecanismos de reao.
J para o caso das reaes de auto-reduo dos xidos de mangans, pode-se
considerar que a reao ocorre via as seguintes reaes em paralelo:
MnO2 (s) + CO (g) = MnO (s) + CO2 (g)
xC (s) + xCO2 (g) = 2xCO (g)
eq.(62)
eq.(59)
e a reao global seria:
PUC-Rio - Certificao Digital N 0321309/CA
MnO2 (s) + xC (s) = MnO (s) + (2x-1)CO (g) + (1-x)CO2 (g)
eq.(63)
6.3.2.1.
Etapas da auto-reduo
A figura 21 apresenta as etapas pelas quais se passa a auto-reduo.
Figura 14 Etapas da auto-reduo.
Estas etapas esto indicadas como:
88
1) Difuso de CO atravs da camada porosa dos micro-poros que esto
sendo reduzidos.
2) Reao de reduo dos xidos.
3) Difuso de CO2 atravs da camada porosa da partcula.
4) Transporte de CO2 pelo gs.
5) Reao de Boudouard.
6) Difuso de CO pelo gs nos poros.
*7) Reduo slido-slido (acontece quando carbono encosta na partcula).
6.3.3.
Cintica das reaes de reduo dos xidos de ferro
A cintica de reduo dos xidos de ferro j foi amplamente estudado por
PUC-Rio - Certificao Digital N 0321309/CA
vrios pesquisadores e, por no ser parte principal na avaliao dos resultados
experimentais deste trabalho, conforme indicado nos objetivos do mesmo,
decidimos no abordar o assunto detalhadamente.
Segundo Treptow
(38)
, o coque serve como combustvel e como agente
redutor. Para ser cinticamente efetivo, deve ser convertido em monxido de
carbono CO(g). A figura 22 apresenta o efeito do CO(g) na reduo de minrio de
ferro. Esta figura tem uma vista do corte seccional de uma partcula de Fe2O3
depois de uma exposio ao gs CO em alta temperatura.
Figura 15 - Partcula de Fe2O3 parcialmente reduzida, baseado em fotomicrografa (38).
Pode se verificar que a superfcie da partcula tornou-se Fe. A aparncia de
ptalas sobre a partcula, resulta da contrao do volume que acompanha a
89
formao de FeO. Esta contrao faz a partcula ficar porosa e permite que o
CO(g) penetre nela. O mecanismo est bem proposto para as reaes de reduo
no qual tomos de ferro migram para o centro da partcula deixando atrs tomos
de oxignio para reagir com CO(g) na superfcie exterior, este mecanismo
baseado em que dois xidos de ferro no so estequiomtricos em altas
temperaturas (38).
6.3.4.
Cintica das reaes de reduo dos xidos de mangans
Yastreboff et al.
(16)
, estudou o efeito da composio gasosa na reduo
carbotrmica de xidos de mangans. No seu trabalho examinou a reduo, com
grafita, de xido de mangans puro a 1300C, minrio de mangans australiano a
PUC-Rio - Certificao Digital N 0321309/CA
1300C e 1350C, finos de silico-mangans a 1350C e escrias de ferromangans a 1400C. A reduo foi feita em diferentes atmosferas: de argnio,
variando a composio do gs Ar e CO e Helio. A taxa e a extenso da reduo
foi determinada por anlise termogravimtrica (TGA) e por monitoramento das
concentraes de CO e CO2 no gs de sada.
A taxa total de fluxo de gs foi mantida em 1,6 l/min. A sada de gs foi
continuamente amostrada numa taxa de aproximadamente 0,1 l/min e dirigida
para um analisador infravermelho de CO/CO2. Os cadinhos utilizados para as
experincias foram de grafite. As amostras usadas foram de 0,5 g.
Os resultados apresentados pelo autor
(16)
, referentes reduo de MnO
puro apresentam dados de TGA sobre a perda de massa do MnO nas experincias
de reduo a 1300C sob variadas composies de gs CO-Ar, e so apresentados
na figura 23.
90
PUC-Rio - Certificao Digital N 0321309/CA
Figura 16 - Reduo de MnO por grafita a 1300C, em atmosfera de Ar-CO com
concentraes variadas de CO (%vol) no percurso da reduo (16).
Nestes experimentos, a concentrao de CO na mistura gasosa Ar-CO,
decresceu de 100 para 35 % em volume, logo aumentou para 45 % em volume,
depois mudou para 100 % em volume de CO. Pode se verificar que a adio de
CO ao Ar retardou fortemente a reduo de MnO. Nesta temperatura, a reduo
comeou quando a quantidade de CO estava abaixo de 75 % em volume e
continuou a uma taxa razovel somente quando a percentagem de CO estava
abaixo de 35-45 % em vol. A mudana da atmosfera gasosa para 100 % em vol de
CO, causou a re-oxidao parcial do mangans (16).
Por outro lado, nos experimentos no-isotrmicos apresentados na figura
24, a reduo de MnO puro por grafita em atmosfera de CO, comeou a 1320C.
91
Figura 17 - Reduo de MnO por grafita em atmosfera de CO a diferentes temperaturas
PUC-Rio - Certificao Digital N 0321309/CA
(16)
O autor explica que a reduo de MnO pelo carbono slido numa atmosfera
de CO foi mais lenta que aquela sob argnio Ar. Porm, conclui-se que o efeito da
composio gasosa CO-Ar na reduo de MnO decresce com o incremento da
temperatura (16).
Nos experimentos da reduo do Minrio de Mangans, o autor
(16)
fez
uma comparao da reduo nas temperaturas de 1300 e 1350C, em atmosfera
de CO com aquela sob atmosfera de Ar. A figura 25 descreve os resultados.
Figura 18 - Efeito do CO na reduo do Minrio de Mangans por grafita (16).
92
Pode se ver que a reduo de minrio de mangans numa atmosfera de CO
foi mais lenta que numa atmosfera de Ar, particularmente em temperatura menor
de 1300C. O estgio inicial da reduo, em que os xidos de ferro foram
reduzidos a ferro metlico e os xidos de mangans mais estveis para MnO, no
foram notavelmente afetados. O efeito retardador do CO foi mostrado no segundo
estagio da reduo, em que MnO foi reduzido para a fase metlica.
Em alguns experimentos feitos pelo autor a 1300C, a atmosfera original
de CO foi mudada para Ar, e tambm a atmosfera de Ar foi mudada para CO. A
mudana de CO para Ar acelerou fortemente o processo de reduo, isso se pode
ver na figura 25. A mudana na atmosfera de Ar para CO causou alguma reoxidao da amostra. A re-oxidao de carbeto de mangans foi muito mais lenta
PUC-Rio - Certificao Digital N 0321309/CA
que a reduo de MnO, possivelmente devido passivao. A re-oxidao,
praticamente parou, aps atingir um grau de reao de aproximadamente 10% (16).
O autor
(16)
, tambm examinou a reduo de minrio de mangans sob
atmosfera de He a 1400C, a figura 26 apresenta os resultados.
Figura 19 Perda de massa e evoluo de CO na reduo de minrio de mangans por
grafita, em atmosferas de Ar e He a 1400C (16).
93
Na figura 26, pode se ver que as curvas de reduo obtidas em atmosferas
de He e Ar, so prximas entre si. O minrio de mangans foi reduzido
ligeiramente mais rpido em He do que em Ar (16).
Yastreboff
(16)
, indica que o minrio de mangans acima da fuso consiste
de duas fases: a fase slida de MnO, que pode ser um xido puro de MnO ou uma
soluo slida de MnO-MgO, e uma fase lquida de xido referida fase escria.
O processo de reduo de minrio de mangans inclui a dissoluo da fase MnO
na escria fundida e a reduo do MnO da escria.
A reduo do MnO por grafita ou carbono dissolvido no metal
apresentado pela seguinte reao:
PUC-Rio - Certificao Digital N 0321309/CA
(MnO) + C =
[ Mn ] + CO
eq.(64)
O autor indica que a reao de reduo inclui as seguintes etapas:
1) a dissoluo da fase slida MnO dentro da fase escria fundida, na
reduo de minrio de mangans e finos de silico-mangans,
2) transferncia de massa da fase lquida de MnO,
3) dissoluo do carbono dentro da fase metal,
4) transferncia de massa do carbono no metal lquido,
5) reao qumica carbono-xido ( controle intrnsico ), e
6) transferncia de massa de CO da reao de interface para a fase gasosa.
Yastreboff (16), no seu trabalho fez algumas consideraes:
* Considera que a resistncia devido dissoluo e difuso do carbono no
metal lquido usualmente considerado insignificante.
94
* A resistncia devido transferncia de MnO na escria fundida pode
contribuir ao controle da taxa, embora dados na literatura sobre essa matria
so controvrsias.
* De acordo com este trabalho, a escria agitada na reduo carbotrmica da
escria de ferro-mangans no teve nenhum efeito sobre a taxa de reduo, o
que significa que a resistncia devido transferncia de massa na fase
escria pode ser negligenciada. Segundo o autor, isto tambm foi concludo
por Tangstad sobre a base da anlise do perfil de concentrao do MnO na
escria. O controle intrnsico da reduo do MnO extensamente aceitada
na literatura.
*A resistncia devido transferncia de massa de CO na fase gasosa pode
PUC-Rio - Certificao Digital N 0321309/CA
tambm contribuir cintica de reduo.
* A reduo de minrio de mangans retardada pelo incremento da presso
parcial de CO.
* Dados obtidos por Terayama e Ikeda sobre reduo carbotrmica de MnO
em atmosfera de Helio mostra que o MnO reduzido mais rapidamente em
Helio que em Argnio, isto pode ser relacionado pelos diferentes
coeficientes de difuso do CO em Helio e em Argnio (16).
O autor conclui:
* A reduo carbotrmica de xido de mangans puro, minrio de mangans e
escria de ferro-mangans fortemente influenciado pela composio
gasosa.
* A taxa de reduo de MnO em gs Ar-CO incrementou-se com o decrscimo
da presso parcial de CO.
* A reduo de xido de mangans em atmosfera de Helio foi mais rpida que
em atmosfera de Argnio.
95
* Para as condies experimentais empregadas no seu trabalho, a taxa de
reduo teve um controle misto pela reao qumica de interface e a
transferncia de massa de CO na fase gasosa.
A taxa da reao qumica proposta pelo autor (16), a seguinte:
R = k* Ac ( a MnO PiCO * a Mn / K )
eq.
(65)
PUC-Rio - Certificao Digital N 0321309/CA
Onde:
R
: taxa da reao ( mol* s -1 )
: constante de taxa da reao qumica ( mol * m2 S -1 )
Ac
: rea da interface da reao de reduo ( m2 )
a MnO
: atividade de MnO na escria fundida
PiCO
: presso parcial de CO na interface da reao ( atm )
a Mn
: atividade de mangans na fase metlica
: constante de equilbrio da reao de reduo
Ostrovski & Webb
(17)
, estudaram o mecanismo e cintica da reduo
carbotrmica de minrios e de xidos puros de mangans. Estes mecanismos e a
cintica do processo de reduo so significativamente dependentes dos materiais
usados. Este trabalho investiga o efeito da composio do minrio, especialmente
aquele de alto contedo de slica, sobre os mecanismos e cintica da reduo deste
minrio.
Os autores trabalharam na reduo de minrio de mangans silicoso
contendo 41.0 % em peso de Mn e 11.0% em peso de SiO2. Usou-se grafita como
redutor em atmosfera de Argnio a 900, 1200 e 1400C. Fez medidas de perda de
massa, seguido por anlises de Raios X e anlises em microscpico. O minrio
tinha um tamanho de -150+53 m e foi preliminarmente calcinado durante 2 horas
a 1000C em argnio, atingindo uma perda de peso de 17% durante esse perodo,
isso foi feito para assegurar que a perda de peso nas experincias, seriam
96
totalmente atribudas reduo dos xidos presentes. A grafita teve uma frao de
tamanho de 300 + 100 m e tambm foi pre-queimado em argnio a 1000C,
atingindo uma perda de peso de 0,4%. A extenso da reduo foi calculada
relativa a 100% da reduo de ferro e mangans. Perto de 6% da reduo foi
observada aps 2 horas a 900C, 35% aps 2 horas a 1200C; e 132% de reduo
foi encontrado aps 6 horas a 1400C, isto foi devido reduo da slica.
Os experimentos de reduo foram executadas num forno de resistncia
vertical de alta temperatura. Usou-se uma balana eletrnica com preciso de
0,0001 g. para pesar propores de minrio e grafita, eles misturavam-se
intimamente e colocavam-se num cadinho de alumina de 10 ml. Foi usado nos
experimentos, aproximadamente 30 % excesso de grafita relativa quantidade
estequiomtrica de carbono requerido para o 100 % da reduo de ferro e reduo
PUC-Rio - Certificao Digital N 0321309/CA
de mangans para carbetos. As massas das amostras foram de 1,2 a 2,5 g, elas
eram suspensas ao topo do tubo do trabalho. A taxa de fluxo de argnio usado em
todos os experimentos foi de 2.1 L /min.
Referente aos mecanismos que se passa na reduo do minrio de
mangans, os autores comentam:
A reduo a 900C foi limitada reduo de xidos de ferro para FeO.
Dois estgios de reduo foram distinguidos a 1200C e 1400C:
- Durante o primeiro estgio, o qual se extendeu a aproximadamente 25%
em ambos os casos (1200 e 1400C) por 4 a 6 min, xidos de ferro
reduzidos a ferro metlico e xidos de mangans para MnO. O autor
sugere que neste estgio, os xidos so reduzidos pelo gs CO.
- No segundo estgio, acontece a reduo de MnO para Mn e ocorre via
carbono na fase metlica. O autor sugere que neste estgio tm-se um
controle pela difuso do MnO no estado slido a 1200C e a difuso do
MnO no estado lquido a 1400C.
97
As baixas taxas de reduo de minrio de mangans observadas nos
experimentos podem ser atribudos ao alto teor de slica no minrio.
Na figura 27 apresenta-se a evoluo da reduo do minrio de mangans
nas diferentes temperaturas, pode se observar que a taxa inicial de reduo de
minrio de mangans acrescenta-se com o aumento da temperatura de 900C para
PUC-Rio - Certificao Digital N 0321309/CA
1200C (17).
Figura 20 - Reduo de minrio de mangans silicoso a 900, 1200 e 1400C (17).
Como tambm indica Ostrovski & Webb
(17)
, Rankin e Van Deventer, e
Terayama e Ikeda, investigaram a reduo de xidos de mangans por grafita em
atmosfera inerte. Terayama e Ikeda fizeram experincias na faixa de temperatura
de 1070C a 1200C, nestas temperaturas o produto da reduo do mangans foi
carbeto Mn7C3 quando se usou carbono em excesso em relao quantidade
estequeomtrica. Sem carbono em excesso, formou-se mangans metlico pela
reao entre o MnO slido e o carbeto. Por outro lado, nas experincias de
Rankin e Van Deventer, as temperaturas de ensaio foram maiores, 1200C a
1425C, nestas temperaturas, o produto da reduo de MnO foi um outro carbeto
Mn5C2. Em ambos trabalhos, a reao de gaseificao de grafita foi a etapa
controladora da taxa.
98
Segundo Ostrovski & Webb
(17)
, Eric e Burucu investigaram os
mecanismos e cintica de reduo dos minrios de mangans de Manatwan
(frica do Sul). Neste estudo, a reduo de minrios finamente modos usando
grafita pulverizada como redutor, foram examinadas sob uma atmosfera de
argnio entre 1000C e 1350C. Pode-se observar que a reduo tem trs
diferentes estgios, que so:
1) O primeiro estgio da reduo foi muito rpida e foi observado at
aproximadamente 30 % de reduo de minrio. Isto coincide com a reduo dos
xidos de mangans e de ferro completamente para FeO e MnO. Os autores
sugerem que a reduo foi iniciada pela reao direta de oxido com grafita para
formar gs CO e que seguida pela reduo via este CO(g) formado, segundo as
PUC-Rio - Certificao Digital N 0321309/CA
seguintes reaes:
Me2O3 (s) + C (s) = 2 MeO (s) + CO (g)
eq.(66)
Me2O3 (s) + CO (g) = 2 MeO (s) + CO2 (g)
eq.(67)
O gs CO2 formado regenerado para CO(g) via a reao de Boudouard, o
qual assegura as condies de reduo. A taxa deste estgio controlada pela
difuso de gs atravs da camada porosa de produto.
2) O segundo estgio da reduo inclui a nucleao da fase metlica rica
em ferro que crescem em tamanho e incrementam-se na quantidade de mangans,
formando um carbeto misturado ( Mn,Fe)5C2. Neste estgio, a reduo de MnO
para carbeto ocorre predominantemente pelo CO(g). Foi sugerido que a etapa
controladora da taxa a reao qumica entre a fase oxidada e o gs redutor em
juno com a reao de gaseificao de carbono (17).
3) O terceiro estgio mais lento e inclui a reduo dos xidos
remanescentes pelo carbono dissolvido na fase carbeto a temperaturas acima de
1200C, seguindo a reao seguinte:
MnO (s) + C (carbeto) = Mn (carbeto) + CO (g)
eq.(68)
99
O autor sugere que este estgio controlado pela difuso de carbono para a
interface carbeto / oxido atravs da fase carbeto e a retirada de CO2 (g), ademais
da difuso de MnO para a interface oxido / carbeto atravs da fase silicatada a
qual reveste as partculas de xido e reduz especialmente a reao de interface
para o fim da terceira fase.
O esquema geral da reduo dos minrios de mangans na produo de
ligas de mangans em forno eltrico a arco, pode ser apresentado na seguinte
seqncia (17):
- Primeiro, os xidos de ferro e de mangans so reduzidos para FexO e
PUC-Rio - Certificao Digital N 0321309/CA
MnO pelo CO(g), isto acontece ainda no estado slido.
- A fase metlica comea com a reduo de FexO para Fe, provavelmente
tambm em estado slido.
- Esse processo acompanhado pela dissoluo de carbono no ferro e
formao de carbeto de ferro.
- O Carbono do coque, de outros materiais carbonceos e da fase metlica
reduzem o minrio de mangans a elevadas temperaturas com formao
de mistura de carbetos.
As limitaes em diferentes estgios da reduo de minrios de mangans
dependem do tipo de minrio e tipo de redutor, tamanho de matria prima e de
outros parmetros (17).
Na continuao do trabalho, o autor fez maior referncia ao mecanismo de
reduo do minrio de mangans, onde indica que a reduo do minrio de
mangans a 900C foi esperada para ser via monxido de carbono, como descrito
pelo seguinte trajeto de reao:
Me2O3 (s) + CO (g) = 2MeO (s) + CO2 (g)
eq.(67)
100
CO2 (g) + C (s)
= CO (g)
eq.(33)
A extenso da reduo aumenta significativamente com o incremento da
temperatura de 900C a 1200C. No comeo da reduo, as fotomicrografas
mostram que a fase metlica foi unida s partculas de grafita. Isto indica que na
etapa inicial, na reduo do xido para metal, se tem uma reduo direta na
interface grafita / minrio para produzir ferro metlico, de acordo com a seguinte
reao:
FeO (s) + C (s) =
Fe (s) + CO (g)
eq.(69)
Adicionalmente, pontos de ferro metlico foram observados na maioria do
PUC-Rio - Certificao Digital N 0321309/CA
minrio e no somente na interface grafita / minrio. Isto indica que sozinho com
a reduo direta com grafita, ferro foi reduzido a estado metlico pelo gs CO, de
acordo com a reao:
FeO (s) + CO (g) = Fe (s) + CO2 (g)
eq.(22)
A concentrao do carbono na primeira camada do ferro insignificante e
aumenta com o processo de reduo. O carbono dissolvido no ferro reduz
mangans. Certamente o mangans foi detectado em considerveis propores na
fase metlica em contato direto com partculas de grafita. A composio da fase
metlica indicou que a reduo ocorreu para carbeto de mangans Mn7C3
seguindo a seguinte reao:
14 MnO (s) + 13 C = 2 Mn7C3 + 7 CO2 (g)
eq.(70)
O teor de mangans nos pontos metlicos dentro das partculas de minrio,
os quais so formados via reduo pelo CO relativamente baixa, perto de 32%
em peso. A falta de reduo de MnO pelo CO pode ser devido ao efeito da
sinterizao observada nessas temperaturas, isto decresce a taxa de difuso dos
gases atravs do minrio. Supe-se que a reduo de xidos de ferro foi muito
rpida, tanto quanto que o contedo de ferro no minrio seja zero aps os
101
primeiros cinco minutos de reduo. A reduo dos xidos de ferro podia ocorrer
via difuso do gs CO atravs das partculas antes que a sinterizao comeasse
no processo de aquecimento da amostra.
O mecanismo de reduo do minrio diferente a 1400C, devido fuso
parcial do minrio.
A composio final da fase metlica formada no processo de reduo foi
significativamente diferente que a observada por Eric e Burucu. Isto pode se
explicar pela diferena na composio do material de minrio usado inicialmente.
O minrio de mangans de Manatwan examinado por Eric e Burucu, apresentava
maior contedo de CaO e menor contedo de SiO2. O autor no observou a
reduo da slica e nenhum estagio em seu estudo. O alto contedo de slica pode
PUC-Rio - Certificao Digital N 0321309/CA
ser o principal fator que afeta a cintica de reduo.
O autor
(17)
, tambm indica que a reduo de mangans pelo carbono na
fase metlica, segundo a reao (70), pode ser controlada pela difuso de MnO
atravs da matriz silicatada. Neste caso, como isto foi mostrado por Eric e Burucu,
a taxa de reduo pode ser descrita pela equao de Serin-Ellickson:
k t = 2 D t / r02 = - ln [ 2 ( 1 X ) / 6 ]
eq.(71 )
Onde:
k:
constante de taxa
t:
tempo
D:
coeficiente de difuso
r0:
Raio inicial da partcula
X:
frao de reduo
Esta equao se ajusta bem para os dados experimentais obtidos para o
segundo estagio da reduo do minrio de mangans (15 a 126 min) a 1200C,
onde a reduo ocorreu no estado slido. O coeficiente de correlao encontrado
foi 0,99.
102
A equao (71) se ajusta tambm aos dados experimentais obtidos para a
reduo de minrio de mangans a 1400C durante o tempo de 9 a 64 min, at o
comeo da reduo da slica. Neste caso o coeficiente de correlao encontrado
foi acima de 0,99.
Usando tambm a equao (71), foram calculados os coeficientes de
difuso do MnO dando 5,6 x 10
-11
cm
s-1 a 1200C e 1,2 x 10
- 9
cm
s-1 a
1400C. Estes valores esto muito abaixo dos valores encontrados por Eric e
Burucu, os quais variaram de 8,23 x 10 - 8 para 3,76 x 10 - 7 cm 2 s-1 de 1250C a
1350C. Esta diferena, segundo o autor, atribuda ao alto teor de slica no
minrio de mangans silicoso em comparao com o minrio de mangans de
Manatwan investigado por Eric e Burucu.
PUC-Rio - Certificao Digital N 0321309/CA
Nas fotomicrografas que os autores apresentam, mostram que aps a alta
taxa inicial de reduo durante aproximadamente 15 minutos, a extenso da
reduo a 1200C, lenta e ligeiramente incrementou-se com o tempo. Aps 2
horas a fase metlica na interfase minrio/grafita cresceu em tamanho e
enriqueceu em mangans com contedo aproximadamente de 65 % Mn e 25 %
Fe (% em peso) com carbono remanescente. A composio desta fase metlica
indica a formao de um carbeto complexo (Fe,Mn)7C3. Os pontos metlicos
nucleados nas partculas de minrio tm aproximadamente a mesma composio
das amostras aps 15 min de reduo.
O autor tambm examinou microfotografias de minrio de mangans
reduzido durante 3,5 min a 1400C. Indica que com o incremento do tempo, a
extenso da reduo continua incrementando, aps 9 min de reduo a 1400C, a
extenso de reduo foi aprox. a mesma que aquela atingida aps 2 horas a
1200C. A fotomicrografa da amostra reduzida aps 9 min de reduo
apresentada na figura 28.
PUC-Rio - Certificao Digital N 0321309/CA
103
Figura 21 - Minrio de Mangans submetido a 9 min de reduo a 1400C, 500 X (17).
Akdogan & Hurman (69), investigaram a reduo de minrio de mangans
da mina Wessel da frica do Sul, na faixa de temperaturas de 1100C a 1350C
usando grafita pura como redutor, sob uma atmosfera de argnio. Usaram trs
tipos de minrios de mangans denominados como WH, W1 e W4, concluiram
que a taxa e o grau de reduo aumentam com o incremento de temperatura e o
decrscimo do tamanho das partculas, tanto de minrio como de grafita, isso
acontece mais marcadamente nas temperaturas de 1300 a 1350C. Os autores
tambm avaliaram o efeito da composio qumica dos minrios de mangans na
taxa e o grau de reduo, os resultados mostram que o grau de reduo aumenta
com o decrscimo da relao Mn:Fe do minrio e o incremento do teor de Fe2O3.
104
Indicam que o processo de reduo ocorre em dois estgios distintos. Para
os dois estgios, os autores desenvolveram um modelo cintico detalhado,
levando em considerao os fatores qumicos e difusionais que afetam o processo.
No primeiro estgio, a taxa de controle misto. Indicam que a difuso
interna de CO e a difuso externa de CO2 a travs da camada porosa de produto e
a taxa da reao qumica entre o CO e o xido slido nas paredes dos poros,
influenciam na taxa total. O tratamento matemtico deu valores de difusividade
efetiva de CO-CO2 de 2,5*10-5, 5,10*10-5 e 6,7*10-5 cm2*s-1 para os minrios
WH, W1 e W4, respectivamente, a 1300C. Isso mostrou que a difuso de
Knudsen dominou o mecanismo de transporte gasoso. Enquanto a reduo
prosegue, a contribuio relativa da resistncia qumica aumenta quando aquela
PUC-Rio - Certificao Digital N 0321309/CA
contribuio da resistncia difusional diminui.
As energias de ativao aparentes calculadas a partir dos dados da taxa de
reduo correspondentes ao primeiro estagio da reduo foram 81,3 ; 87,0 e 94,6
KJ/Kg/mol para os minrios W4, W1 e WH, respectivamente.
Referente aos mecanismos de reduo que se passam neste primeiro
estgio, os autores
(69)
, indicam que nas temperaturas estudadas, este estagio
completado entre os primeiros 6 a 10 min de tempo de reteno. Espera-se que a
reduo comea com a reao atravs do contato direto entre partculas de minrio
e de grafita, de acordo a:
3 Mn2O3 + C = 2 Mn3O4 + CO
eq.(72)
3 Fe2O3 + C = 2 Fe3O4 + CO
eq.(73)
essas reaes formam monxido de carbono CO, o qual atua como um agente
redutor em adio grafita, mediante as seguintes reaes:
Fe3O4 + CO = 3 FeO + CO2
eq.(21)
105
Mn3O4 + CO = 3 MnO + CO2
eq.(32)
Esse CO2 reduzido para CO atravs da reao de Boudouard pelo excesso
de carbono presente no sistema. Supe-se que a reduo de Fe2O3 para Fe3O4 e a
de Mn2O3 para Mn3O4 ocorrem instantaneamente e que a reao (21) bastante
rpida e no contribui na taxa de controle.
O segundo estagio, comea aps aproximadamente 10 min, um estagio
mais lento que inicia-se com a nucleao do ferro da wustita. A reao qumica
entre o xido de mangans e o carbono dissolvido no metal ou no carbeto do
PUC-Rio - Certificao Digital N 0321309/CA
metal, pareceu ser o controlador da taxa do processo. A taxa da reao qumica
entre o MnO e Carbeto encontradas esto na faixa de 1,53*10-8 para 1,32*10-7
mol*s-1*cm-2.
As energias de ativao aparentes calculadas foram 102,1 ; 107,8 e 141,7
KJ/Kg/mol para os minrios W4, W1 e WH, respectivamente. Durante este
estgio, a reao est localizada na interface xido/carbeto e procede como um
ncleo diminudo.
Referente aos mecanismos de reduo que se passam neste segundo
estgio, os autores
(69)
, indicam que se forma ferro metlico como resultado da
seguinte reao:
FeO + CO = Fe (ncleos) + CO2
eq.(22)
Assim, o segundo estagio, o qual foi virtualmente ausente a temperaturas
abaixo de 1200C, comeou com nucleao aleatria de ferro metlico da wustita,
ambos no interior das partculas tanto quanto sobre a superfcie exposta ao agente
redutor. Esta nucleao aleatria de ferro pode ser atribuda disperso de xidos
de ferro em toda a matriz de minrio. O ferro metlico formado produto
106
intermedirio e se transforma em carbeto de ferro enquanto a reduo prossegue.
Em seguida, o carbeto de ferro pode agir como um meio atravs do qual o carbono
difunde para a interface oxido de metal carbeto, onde mais oxido reduzido.
As fotografias em MEV (microscopia eletrnica de varredura) mostram
que com o incremento no tempo de reduo acompanhado um aumento no
tamanho do ncleo e por um aumento significante em teor de mangans, o qual
uma indicao da reduo de gros de xidos ricos em MnO, os quais esto em
contato direto com carbetos misturados ricos em ferro. Anlise com EDAX
(anlise de raios X de energia dispersiva), mostrou que os carbetos misturados
foram progressivamente enriquecidos em Mn durante este estagio.
Uma vez que a fase metlica comea a cobrir a fase xido, a reao do
PUC-Rio - Certificao Digital N 0321309/CA
xido com carbeto torna-se dominante. Ento, a reduo de MnO pode ser
representada pela reao:
MnO + ( C )metal
( Mn ) metal
+ CO
eq.(74)
A composio da fase carbeto formada, obtida por EDAX (anlise de raios
X de energia dispersiva), a diferentes tempos de reteno acima de 1200C foram
comparadas com a composio da superfcie liquidus do sistema Fe-Mn-C. Com
os aumentos do tempo de reteno junto com o aumento do contedo de
mangans, diminuiu a temperatura liquidus da fase carbeto, indicando a existncia
de um estado slido-liquido em temperaturas acima de 1300C, o qual reala o
transporte de reagentes e produtos.
Com o incremento da reduo, quando os gros metlicos aumentam em
tamanho, ento a proporo de escoria tambm aumenta. Segundo Akdogan &
Hurman
(69)
, h evidencia que a taxa de reduo de MnO slido pelo carbono
dissolvido em Fe-C-Mn fundido, controlado pela taxa da reao qumica e
altamente possvel que a reao qumica seja o processo controlador da taxa
durante a reduo de MnO dissolvido na escoria pelo carbono do metal, segundo a
seguinte reao:
107
MnO escoria
+ C metal
= Mn metal + CO
eq.(75)
Akdogan & Hurman (69) fizeram uso de analises termo-gravimtrico TGA.
O agente redutor usado nas experincias de reduo foi grafita pura, que continha
menos de 10 ppm de impurezas. O tamanho das partculas de grafita foi 100 % 0,044mm. Assim sendo, foram misturados o minrio de mangans e a grafita
numa relao de 4:1 (em massa) num gral de gata. A mistura foi posta num
cadinho de alumina de 36 mm de dimetro e 56 mm de comprimento e colocadas
num forno a 105C.
As amostras reduzidas foram divididas em parcelas representativas e
analisadas quimicamente por fluorescncia de raios X, espectroscopia de emisso
PUC-Rio - Certificao Digital N 0321309/CA
de plasma indutivamente acoplado, tambm por difrao de raios X (XRD) para
identificao das fases, metalogrficamente e ainda por analises de raios X de
energia dispersiva em microscpio eletrnico de varredura (SEM-EDAX) para
micro-analise de fases.
Os dados de perda de massa foram convertidos para percentagem de
reduo assumindo que a perda em massa da amostra foi devida evoluo de
CO(g). O autor indica que a existncia de quantidades apreciveis de CO2 no
possvel em temperaturas acima de 1000C na presena de carbono. Isto foi mais
seguro ainda, usando excesso de carbono. Ento, a percentagem de reduo foi
descrita pela seguinte expresso:
massa evoluda de CO
%R =
16
*
massa de oxignio removvel originalmente
Segundo os autores
* 100
eq.(76)
28
(69)
, a quantidade estequiomtrica de carbono foi
calculada baseada na reduo de Mn2O3 para Mn7C3 e a de Fe2O3 para Fe3C.
Analisando-se os resultados experimentais obtidos pelos autores, conclui-se
que o fator que tem maior influencia na taxa e o grau de reduo a temperatura,
108
causando um incremento de quase trs vezes no grau de reduo entre 1100C e
1350C, isto pode se ver na figura 29. Tambm possvel distinguir, que em
aproximadamente 6 min.tem-se uma mudana nas inclinaes das curvas
cinticas, que correspondem a 33% de reduo em temperaturas acima de 1200C.
Assim, a reduo perseguiu em dois estgios: um pequeno estagio inicial durante
o qual a taxa e o grau de reduo foram afetados ligeiramente pela temperatura e
um segundo estagio maior durante o qual o efeito da temperatura no grau de
PUC-Rio - Certificao Digital N 0321309/CA
reduo foi substancial.
Figura 22 - Efeito da temperatura na reduo de minrio WH (69).
A influencia de outros fatores como a relao Mn:Fe e os teores de Fe2O3 e
Mn2O3 sobre a redutibilidade do minrio de mangans a 1300C analisados neste
trabalho, so resumidos na tabela 8 e visualizados na figura 30.
Tabela 3 - Efeito da composio qumica na reduo de minrio de mangans de
Wessel, reduzidos a 1300C durante 60 min (69).
109
PUC-Rio - Certificao Digital N 0321309/CA
Figura 23 - Curva reduo versus tempo para trs diferentes minrios de mangans
reduzidos a 1300C (69).
Por outro lado, os autores ao avaliar a taxa de controle na cintica de
reduo, indicam que os dados experimentais para cada minrio de mangans
foram analisados inicialmente fazendo uso da equao de controle qumico,
esboado a seguir:
k t = ( 1 ( 1 F ) 1/3 )
eq.(77)
onde:
F: frao reagida
k: constante de taxa
t: tempo
Quando esta equao foi aplicada para os presentes dados, obtiveram-se
bons ajustes. O coeficiente de correlao (r) obtido foi acima de 0,97 para esta
equao de controle qumico que descreve o processo de reduo a temperaturas
entre 1100C e 1350C.
You might also like
- Acionamento De Jato-ventilador De Acordo Com A Medição De Co2 Programado No PicFrom EverandAcionamento De Jato-ventilador De Acordo Com A Medição De Co2 Programado No PicNo ratings yet
- Processos de Fabricação Do AçoDocument5 pagesProcessos de Fabricação Do AçoJonasNo ratings yet
- Alto FornoDocument41 pagesAlto FornotapeixotoNo ratings yet
- Materiais de Construção Mecânica: AçoDocument5 pagesMateriais de Construção Mecânica: AçoArtur PinheiroNo ratings yet
- Produção de ferro gusa em alto-fornoDocument37 pagesProdução de ferro gusa em alto-fornoHélio De Verónica SoriarNo ratings yet
- Ferros & aços I-60: Tratamentos térmicos e carburizaçãoDocument4 pagesFerros & aços I-60: Tratamentos térmicos e carburizaçãofilipercastro2736No ratings yet
- CV e CoqueDocument9 pagesCV e CoqueAmadeu ResendeNo ratings yet
- Ferro e Aço: Processos de Obtenção e PropriedadesDocument35 pagesFerro e Aço: Processos de Obtenção e Propriedadescarlos augusto do carmo braiaNo ratings yet
- Produção de Ferro Alto-fornoDocument16 pagesProdução de Ferro Alto-fornoRafael LimaNo ratings yet
- Processos de fabricação do ferro primário em alto-fornosDocument135 pagesProcessos de fabricação do ferro primário em alto-fornosrobsonNo ratings yet
- Tipos de FornosDocument8 pagesTipos de FornosHalleph WergenskiNo ratings yet
- Vantagens dos briquetes de cavacos na fundiçãoDocument21 pagesVantagens dos briquetes de cavacos na fundiçãoLeonardoNo ratings yet
- Obtenção do Ferro Gusa no Alto FornoDocument7 pagesObtenção do Ferro Gusa no Alto FornoKatia Ruiz Antonio Do NascimentoNo ratings yet
- Pr3SID22021 Murilo GoesDocument12 pagesPr3SID22021 Murilo GoesJoao GabrielNo ratings yet
- Funcionamento básico do alto-forno a carvão vegetalDocument14 pagesFuncionamento básico do alto-forno a carvão vegetalKim Almeida100% (1)
- Forno CubilôDocument13 pagesForno Cubilôabelmil123No ratings yet
- 8 - Escória de Alto FornoDocument13 pages8 - Escória de Alto FornoAmadeu ResendeNo ratings yet
- Refino de AçoDocument31 pagesRefino de AçoArtur DinizNo ratings yet
- Processo Siderúrgico no Alto FornoDocument12 pagesProcesso Siderúrgico no Alto FornoBruno JuniorNo ratings yet
- Produção de aço por redução direta e processos elétricosDocument5 pagesProdução de aço por redução direta e processos elétricosIverton FariasNo ratings yet
- Siderurgia Apresent. 12.1Document207 pagesSiderurgia Apresent. 12.1Luís Gustavo PascarettaNo ratings yet
- Alto Forno - Carvao VegetalDocument16 pagesAlto Forno - Carvao VegetalÍcaro Cazé NunesNo ratings yet
- Resumo de Tecnologia Dos MateriaisDocument8 pagesResumo de Tecnologia Dos MateriaisldmoreiraNo ratings yet
- Iron Making and Steel MakingDocument37 pagesIron Making and Steel MakingGustavo FelipeNo ratings yet
- Materiais e TecnologiaDocument35 pagesMateriais e TecnologiaAnderson SantosNo ratings yet
- Aula2 - FPMDocument44 pagesAula2 - FPMVitor SantanaNo ratings yet
- SIDERURGIADocument10 pagesSIDERURGIACassiano Verner100% (1)
- Aula 7 Aciaria ElétricaDocument36 pagesAula 7 Aciaria ElétricaRomulo Oliveira Lino AlmeidaNo ratings yet
- Produção do aço em alto-fornoDocument16 pagesProdução do aço em alto-fornoSalomão SantanaNo ratings yet
- Processo produção açoDocument21 pagesProcesso produção açoederupfNo ratings yet
- Processos de Fundição1Document148 pagesProcessos de Fundição1Amber LeeNo ratings yet
- Conversor Ld-EngenhariaDocument44 pagesConversor Ld-Engenhariamaxkakuesasaki001No ratings yet
- Revisão Alto FornoDocument43 pagesRevisão Alto FornoPaula CarvalhoNo ratings yet
- 03 - Alto Forno - Obtenção Do Ferro Gusa - Processo Siderúrgico - Aço - Processos de Fabricação - Aços & Ligas - InfometDocument7 pages03 - Alto Forno - Obtenção Do Ferro Gusa - Processo Siderúrgico - Aço - Processos de Fabricação - Aços & Ligas - InfometCristianeNo ratings yet
- Processo Do Alto FornoDocument16 pagesProcesso Do Alto FornoAbinadab Dos Santos AraújoNo ratings yet
- Impacto Das Propriedades Das Pelotas de Minério de Ferro No Processo de Produção de Gusa No Alto-FornoDocument8 pagesImpacto Das Propriedades Das Pelotas de Minério de Ferro No Processo de Produção de Gusa No Alto-FornoALMERINDO SOARES SILVA JUNIORNo ratings yet
- Resumo Da SiderurgiaDocument10 pagesResumo Da SiderurgiaícαяσNo ratings yet
- Trabalho de FundiçãoDocument11 pagesTrabalho de FundiçãoJoão MoutaNo ratings yet
- Produo de Ferro Gusa e AoDocument14 pagesProduo de Ferro Gusa e AoplisdNo ratings yet
- Processos MetalurgicosDocument64 pagesProcessos MetalurgicosPatriciaQuintanaNo ratings yet
- Fabricacao de Tarugos para ExtrusaoDocument163 pagesFabricacao de Tarugos para ExtrusaoEduardo DeakNo ratings yet
- SiderurgiaDocument49 pagesSiderurgiaEliana Franco100% (1)
- Parte 04 - Fabricacao Do ACODocument24 pagesParte 04 - Fabricacao Do ACOHalleyWeltherJacquesDiasNo ratings yet
- Produção de Ferro Gusa e AçoDocument29 pagesProdução de Ferro Gusa e AçoLuciana Boaventura PalharesNo ratings yet
- Oxidação A Vapor 2Document7 pagesOxidação A Vapor 2antonio2020meNo ratings yet
- Processos de alta siderurgiaDocument7 pagesProcessos de alta siderurgiaJoao GabrielNo ratings yet
- Exercícios fixação processo siderúrgicoDocument3 pagesExercícios fixação processo siderúrgicoRodrigo Nunes100% (1)
- Produção Eteno PropenoDocument3 pagesProdução Eteno PropenoNobody GonnaknowNo ratings yet
- Altos FornosDocument9 pagesAltos FornosArnuso SantosNo ratings yet
- Projeto de Sistema de Limpeza de Gases de Convertedor LD 100tDocument17 pagesProjeto de Sistema de Limpeza de Gases de Convertedor LD 100tBrender VictorNo ratings yet
- SIDERURGIA Da Mat Prima Ao Lam 102 202Document101 pagesSIDERURGIA Da Mat Prima Ao Lam 102 202Antonio MarinhoNo ratings yet
- Processos metalúrgicos da aciaria elétricaDocument57 pagesProcessos metalúrgicos da aciaria elétricaWanderson B AraujoNo ratings yet
- Aula 05Document14 pagesAula 05claraNo ratings yet
- Forno EletricoDocument18 pagesForno EletricoRenata FerreiraNo ratings yet
- ALTO FornoDocument41 pagesALTO FornoPastorzequinha IeqNo ratings yet
- Atividades de Tecnologia Mecânica IDocument68 pagesAtividades de Tecnologia Mecânica Ilaboratorio aciariaNo ratings yet
- Untitled PresentationDocument46 pagesUntitled PresentationThais StephanieNo ratings yet
- Processos Industriais SegurosDocument52 pagesProcessos Industriais Segurosmkvl1987No ratings yet
- Apostila de Matemática - Petrobras PDFDocument23 pagesApostila de Matemática - Petrobras PDFCeli GomesNo ratings yet
- Cap6 Umidade Do ArDocument8 pagesCap6 Umidade Do Aragronomiaccaufpi2009No ratings yet
- Processo de fabricação de pneusDocument15 pagesProcesso de fabricação de pneusCeli GomesNo ratings yet
- Sintaxe concisa e completaDocument64 pagesSintaxe concisa e completaNathann F. Tafarel100% (1)
- PDF BiologiaDocument472 pagesPDF Biologialúcia c.No ratings yet
- Metais AlcalinosDocument6 pagesMetais AlcalinosandreskarNo ratings yet
- ARTIGO - Metais Alcalinos 2014 (Feito)Document6 pagesARTIGO - Metais Alcalinos 2014 (Feito)Celi GomesNo ratings yet
- Atividade Laboratório Físico-QuímicaDocument9 pagesAtividade Laboratório Físico-QuímicaOtoazevedo OtoazevedoNo ratings yet
- Relatório de Fisica: Plano InclinadoDocument14 pagesRelatório de Fisica: Plano InclinadoStefany Yumie KawashimaNo ratings yet
- Pneumática Fatec Taubaté 2014Document11 pagesPneumática Fatec Taubaté 2014pmarcelofNo ratings yet
- 11F NL (Teste2 CC) - Nov2021Document3 pages11F NL (Teste2 CC) - Nov2021diana BaptistaNo ratings yet
- Problemas de TrigonometriaDocument2 pagesProblemas de TrigonometriaRogério CostaNo ratings yet
- Exercícios GeotecniaDocument2 pagesExercícios GeotecniaMaiara NascimentoNo ratings yet
- Relatório sobre experimento de força elástica em molasDocument11 pagesRelatório sobre experimento de força elástica em molasLincoln CesarNo ratings yet
- Faísca - Problemas de Física-1 PDFDocument117 pagesFaísca - Problemas de Física-1 PDFPaulo Kuhana Mudilo Mussaqui100% (4)
- Propriedades e fatores que influenciam a formação e estabilidade de espumas alimentíciasDocument4 pagesPropriedades e fatores que influenciam a formação e estabilidade de espumas alimentíciasRenata KellyNo ratings yet
- NBR 12596 NB 1414 - Dimension Amen To Hidraulico de Chamines de Equilibrio para Pequenas Centrais Hidreletricas (PCH)Document5 pagesNBR 12596 NB 1414 - Dimension Amen To Hidraulico de Chamines de Equilibrio para Pequenas Centrais Hidreletricas (PCH)Jersé MessiasNo ratings yet
- Controle de Vibrações em MáquinasDocument21 pagesControle de Vibrações em MáquinasCarolina TelesNo ratings yet
- Fluido de Perfuração Pf2Document21 pagesFluido de Perfuração Pf2Idalia OliveiraNo ratings yet
- Principios Da Optica Geometrica e Suas eDocument9 pagesPrincipios Da Optica Geometrica e Suas eJair Valadares CostaNo ratings yet
- Ligações Químicas 3Document65 pagesLigações Químicas 3Michel SouzaNo ratings yet
- Solubilidade de compostos químicosDocument5 pagesSolubilidade de compostos químicosgustavoNo ratings yet
- Exercicios Serie2Document3 pagesExercicios Serie2Salvador SantosNo ratings yet
- Material Didático Refrigeração PDFDocument97 pagesMaterial Didático Refrigeração PDFRílammis SantosNo ratings yet
- Como Funciona Um FogueteDocument3 pagesComo Funciona Um FogueteJane FreireNo ratings yet
- Elementos Químicos e Classificação PeriódicaDocument4 pagesElementos Químicos e Classificação PeriódicaMarcos Henrique QuerinNo ratings yet
- Mecânica dos Fluidos e Transferência de Calor - Prova P02Document2 pagesMecânica dos Fluidos e Transferência de Calor - Prova P02THAISA CRISTINA DEMARCONo ratings yet
- O átomo e a eletrizaçãoDocument3 pagesO átomo e a eletrizaçãoRogério Mendes BrancoNo ratings yet
- Física Quântica - 2021.3 - QS - Lista 4 - Tema: Uma Nova Interpretação Da Matéria (Dualidade Onda-Partícula) GabaritoDocument6 pagesFísica Quântica - 2021.3 - QS - Lista 4 - Tema: Uma Nova Interpretação Da Matéria (Dualidade Onda-Partícula) GabaritoAndre Luiz CostaNo ratings yet
- Anexo III - Memória de Reforço - Torre Paranapiacaba - R00Document53 pagesAnexo III - Memória de Reforço - Torre Paranapiacaba - R00Will F AlvesNo ratings yet
- 01 ETEC PotênciaDocument5 pages01 ETEC Potênciaevaristo gonçalves oliveiraNo ratings yet
- Máquinas simples: ferramentas que facilitam o trabalhoDocument3 pagesMáquinas simples: ferramentas que facilitam o trabalhoCarla CardosoNo ratings yet
- 03 - Dee261 - Operacoes - Unitarias - Metodos - de - Operação - Dos - Evaporadores - 2023 - 2Document23 pages03 - Dee261 - Operacoes - Unitarias - Metodos - de - Operação - Dos - Evaporadores - 2023 - 2natalianeumannNo ratings yet
- Atividades 2° AnoDocument3 pagesAtividades 2° AnoanalaurademoraissilvaNo ratings yet
- Segunda Lei de Newton - RelatórioDocument6 pagesSegunda Lei de Newton - RelatórioBruno MendesNo ratings yet
- Ar - Condicionado - 1450 - 1550 Da John DeereDocument35 pagesAr - Condicionado - 1450 - 1550 Da John DeereZezinho zele100% (6)
- Vasos Horizontais - Tampos Torisféricos - ExemploDocument7 pagesVasos Horizontais - Tampos Torisféricos - ExemploMich3lstreetdk100% (1)