Professional Documents
Culture Documents
Am071e PDF
Uploaded by
Elias Cuartas GómezOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Am071e PDF
Uploaded by
Elias Cuartas GómezCopyright:
Available Formats
medigraphic Artemisa
en lnea
ARTCULO DE REVISIN
Modelo celular de la hemostasia y utilidad del factor VII
recombinante activado en la prctica clnica
Ral Carrillo Esper,* Yisel Yudy Antigua Bretn,** Jorge Ral Carrillo Crdova***
Resumen Summary
El modelo de hemostasia que tradicionalmente ha sido The traditional model of haemostasia includes two path-
aceptado consiste en dos vas e incorpora una serie de ways with sequential humoral activation that results in
pasos humorales secuenciales que inducen la produc- the generation of thrombin. The cellular model of hemo-
cin de trombina. El modelo celular de la hemostasia rompe stasis establishes that complex tissue factor-activated
el paradigma anterior y establece que el complejo factor factor VII (TF-FVIIa), in close relation with the surface of
tisular-factor VII activado (FT-FVIIa) en estrecha interac- the platelet activates the rest of the coagulation factors to
cin con plaquetas activadas modula la secuencia del generate thrombin. The sequence initiation, amplifica-
proceso de coagulacin que induce la generacin de trom- tion and propagation are characteristics of this model.
bina. Se caracteriza por los pasos secuenciales de inicia- The use of the recombinant activated factor VII (rFVIIa) is
cin, amplificacin y propagacin. Con base en el mode- sustained in the cellular model activation of coagulation.
lo celular de la hemostasia se introdujo en la prctica rFVIIa is a potent prohemostatic agent in approximately
clnica el empleo del factor VII recombinante activado (FVII- 90% of patients with hemophilia and inhibiting antibod-
ra). El FVIIra es potente agente prohemosttico que se ha ies and other types of complex coagulation disorders.
usado ampliamente en pacientes hemoflicos con anti- The application of rFVIIa in other patients who experi-
cuerpos inhibidores y en otros problemas complejos de ence severe bleeding is promising. rFVIIa is effective and
coagulacin con resultados positivos en el 90% de los appears to be relatively safe with a 1-2% of thrombotic
casos. La aplicacin del FVIIra en otras indicaciones ca- complications.
racterizadas por presentar hemorragia grave y no contro-
lada es promisoria. El FVIIra es efectivo y tiene un amplio
margen de seguridad, reportndose una incidencia de 1
a 2% de complicaciones trombticas.
Palabras clave: Modelo celular de la hemostasia, factor Key words: Cellular model of hemostasis, recombinant
VII recombinante activado, factor tisular, plaquetas. activated factor VII, tissue factor, platelets.
INTRODUCCIN
* Jefe UTI Hospital ngeles Lomas.
** Residente de tercer ao de Medicina Crtica Hospital Re- En los aos 60 se propuso por Davie y Ratnoff un modelo
gional Universitario Jos Mara Cabral y Bez, Santiago de de coagulacin que incorporaba una serie de pasos en don-
Los Caballeros, Repblica Dominicana. de la activacin secuencial de factores resultaba en la gene-
*** Facultad de Medicina. Grupo NUCE. UNAM. racin de trombina. En este modelo las vas de la coagula-
cin se dividieron en dos sistemas, el extrnseco y el
Correspondencia:
Dr. Ral Carrillo Esper edigraphic.com
Hospital ngeles Lomas. Vialidad de la Barranca S/N. Colonia
intrnseco. De manera comn ambas vas activaban al fac-
tor X, el cual en unin con el cofactor Va convertan la pro-
trombina a trombina. Este modelo, denominado tambin
Valle de las Palmas. Huixquilucan, Estado de Mxico 52763.
Correo electrnico: seconcapcma@mail.medinet.net.mx cascada de la coagulacin, es razonablemente bueno para
explicar la activacin in vitro de la coagulacin a travs del
Aceptado: 12-01-2007. tiempo de protrombina (TP) y del tiempo de tromboplasti-
ACTA MDICA GRUPO NGELES. Volumen 5, No. 1, enero-marzo 2007 27
Carrillo Esper R y cols.
na parcial activado (TTPa) que corresponden a las vas ex- que se expresa se une al factor VII para formar el complejo
trnseca e intrnseca respectivamente. Sin embargo, en base FVIIa/FT, el cual una vez anclado a la superficie celular acti-
a los conocimientos generados en los ltimos aos este va a los factores IX y X. Las plaquetas activadas constituyen
modelo es inadecuado para explicar las vas fisiolgicas de SUSTRADODE-M.E.D.I.G.R.A.P.H.I.C
el templete en donde se unen los cofactores VIIIa y Xa y
la hemostasia in vivo, no considera la interaccin del siste- sus enzimas (Factor IXa y Xa), lo que resulta en la formacin
ma con las clulas que participan en la coagulacin y es del:ROP ODAROBALE
complejo FDP
de protrombocinasa. La lesin endotelial por
inconsistente con el comportamiento clnico de la disfun- su parte, expone a la circulacin grandes cantidades de fac-
cin de la hemostasia, como puede determinarse por el torVC ED AS,
tisular queCIDEMIHPARG
junto con la activacin plaquetaria induce
hecho de que no hay una relacin entre la va intrnseca y activacin de trombina. El exceso de trombina es inhibido
extrnseca, ya que la activacin del factor X por la va extrn- porARAP
la antitrombina, proceso que se desarrolla adyacente al
seca no compensa la deficiencia de factor VIII o IX. De endotelio al ser activada la trombomodulina. El complejo
hecho, la activacin de la hemostasia por la va intrnseca in ACIDMOIB ARUTARETIL
trombina-trombomodulina :CIHPARGIDEM
activa a la protena C, la cual en
vivo es cuestionable, en base a que la deficiencia de factor presencia de protena S inactiva a los factores Va y VIIIa, de
XII, ciningeno de alto peso molecular o prekalicrena no esta manera la formacin de trombina y el cogulo hemos-
causan tendencia a la hemorragia; sin embargo, es claro ttico queda localizado a la zona de dao endotelial. Los
que algunos componentes de la va intrnseca como son los mecanismos de control del proceso de coagulacin son el
factores VIII y IX son esenciales para la hemostasia y su inhibidor de la va de factor tisular, la protena C, la anti-
deficiencia resulta en hemofilia.1-6 trombina y los glucosaminoglicanos de la pared vascular.14-18
Por otro lado, varios grupos han reportado procesos fun- El nuevo modelo celular de la hemostasia complemen-
damentales que rompen el paradigma del modelo clsico ta y enriquece el modelo tradicional en donde el papel de
de la coagulacin: 1) La interaccin factor VIIa/factor tisu- las clulas era exclusivamente el de ofrecer una superficie
lar (FVIIa/FT) activa no solamente al factor X sino tambin portadora de fosfatidilcerina que serva para armar a los
al factor IX. 2) El evento disparador de la hemostasia in complejos procoagulantes. De acuerdo al modelo celular
vivo es la formacin del complejo FVIIa/FT. 3) La trombina la hemostasia se desarrolla en tres fases simultneas sobre
activa directamente al factor XI en una superficie cargada. diferentes superficies celulares. La primera o de iniciacin
Las plaquetas activadas son el templete para la activacin se lleva a cabo en clulas portadoras de factor tisular (en-
del factor XI por trombina en condiciones fisiolgicas. De dotelio-subendotelio), en la segunda o de amplificacin,
estas observaciones se ha concluido que es poco probable el sistema se prepara para la produccin a gran escala de
que el modelo tradicional de la coagulacin funcione en trombina y finalmente la tercera fase o de propagacin
condiciones fisiolgicas, por lo que Hoffman y otros inves- ocurre en la superficie plaquetaria (Figura 1).19-26
tigadores han propuesto una alternativa denominada mo-
delo celular de la hemostasia.7-10 1. INICIACIN
MODELO CELULAR DE LA HEMOSTASIA El factor VIIa y el factor tisular son elementos esenciales
para la hemostasia. El factor VII circula en la sangre, pre-
De acuerdo a este modelo, el proceso de la hemostasia dominantemente como molcula inactiva y sus funciones,
se realiza sobre una superficie celular y el disparador es el a concentraciones fisiolgicas, son virtualmente nulas en
complejo FVIIa/FT.11-13 ausencia de su cofactor. El factor tisular no est en contac-
Sus elementos fundamentales son: to con la sangre y se encuentra fuera del sistema vascular
hasta que se pierde su integridad. Al expresarse el factor
1. Factor tisular tisular e interactuar con el factor VII se incrementa la acti-
2. Plaquetas activadas vidad de ste en 107. El complejo VIIa/FT activa a los fac-
3. Clulas endoteliales tores IX y X. El factor Xa genera a nivel local pequeas
4. Mecanismos de control cantidades de trombina. Existe evidencia que esta fase inicial
se desarrolla a pequea escala en la microcirculacin y
El factor tisular es una protena de membrana que se fuera de sta en condiciones fisiolgicas. El factor VII, X y
edigraphic.com
expresa en clulas extravasculares que rodean los vasos san-
guneos (fibroblastos, clulas musculares lisas), endotelio y
la protrombina, son capaces de permear al espacio inters-
ticial y pueden ser detectados en la linfa y tejidos perivas-
leucocitos. Es el nico factor de la coagulacin que normal- culares. En base a estas observaciones, se formul la teo-
mente no est presente en la sangre y su sntesis se en- ra de la mnima funcin, en la cual el sistema del factor
cuentra bajo control transcripcional, activndose en respues- tisular tiene actividad constante, generando pequeas can-
ta a trauma, inflamacin y estmulos hormonales. Una vez tidades de trombina.27-30
28 ACTA MDICA GRUPO NGELES. Volumen 5, No. 1, enero-marzo 2007
Modelo celular de la hemostasia y factor VII recombinante
2. AMPLIFICACIN a 108. La trombina generada condiciona la escisin proteo-
ltica del fibringeno y la formacin de monmero de fi-
La fase de amplificacin depende de las plaquetas activa- brina que se polimeriza para consolidar el inestable cogu-
das y de la interaccin de stas con los factores de la lo inicial de plaquetas en un cogulo firme y organizado
coagulacin, en especial con cantidades limitadas de trom- de fibrina. La trombina a su vez activa al factor XIII, lo que
bina que se genera en la vecindad de la clula portadora da mayor estabilidad al cogulo, la fase de propagacin
de factor tisular. Las plaquetas se activan y desgranulan al tambin se caracteriza por la activacin del sistema de
tiempo que se adhieren y agregan formando un tapn en retroalimentacin negativa a travs de la activacin de la
el endotelio daado. En esta fase las plaquetas expresan antitrombina III, sistema de protena C y S y del inhibidor
en su superficie fosfolpidos de carga negativa como la del factor tisular.35,36
fosfatidilcerina, los cuales sirven como templete para la
activacin del factor X y mayor sntesis de trombina. La FACTOR VII RECOMBINANTE ACTIVADO
trombina recluta plaquetas y retroalimenta de manera posi-
tiva al sistema al activar a los factores V, VIII y XI. El com- Con el modelo celular de la hemostasia se explica el com-
plejo IXa/VIIIa se ensambla en la superficie plaquetaria y portamiento in vivo de la coagulacin, lo que ha revolucio-
genera grandes cantidades de factor X, evento que genera nado no solamente el modelo conceptual del proceso he-
ms trombina.31-34 mosttico, sino que tambin ha servido para desarrollar un
nuevo abordaje teraputico para la hemorragia crtica aguda
3. PROPAGACIN tanto en pacientes hemoflicos como no hemoflicos.
En la fase de propagacin se presenta un cambio de loca- a) FVIIra EN HEMOFILIA
cin en los procesos que llevan a la generacin de trombi-
na, esto es de la clula portadora de factor tisular a la En base a que la hemostasia es iniciada por el complejo
plaqueta activada. La expresin de fosfolpidos plaqueta- FT/FVIIa, el uso de factor VII recombinante activado (FVII-
rios amplifica en esta fase la generacin de trombina en 1 ra) se introdujo a la prctica clnica para el manejo de pa-
Plaqueta
IVFT TROMBINA
Iniciacin
Xa
VIIa VIIa X
Xa Va II VIII / FvW
FT FT
IIa
FvW
VIIIa
Amplificacin
V Va
IX FT
VIIa XI XIa
XIa
IXa VIIIa X II FIBRINGENO
Xa Va
IIa
FIBRINA Propagacin
PLAQUETA
edigraphic.com
TROMBINA
Figura 1. Modelo celular de la hemostasia. FT- Factor tisular, IVFT- Inhibidor del factor tisular, FvW- Factor de von Willebrand.
ACTA MDICA GRUPO NGELES. Volumen 5, No. 1, enero-marzo 2007 29
Carrillo Esper R y cols.
cientes hemoflicos con inhibidores en los aos 90 con diferente etiologa. Hasta el momento se ha descrito su
buenos resultados. Para tener efecto teraputico en este empleo en:46
grupo de pacientes la dosis recomendada debe ser capaz
de incrementar en por lo menos 100 veces los niveles 1. SUSTRADODE-M.E.D.I.G.R.A.P.H.I.C
Reversin de anticoagulantes
fisiolgicos del factor VII. A dosis de 100 g/kg se obtie- 2. Ciruga y trauma
nen niveles sricos de 250 veces el fisiolgico, lo que 3. :ROP ODAROBALE
Hepatopata FDP heptico
y trasplante
induce en pacientes hemoflicos hemostasia por mecanis- 4. Hemorragia cerebral no traumtica
mos dependientes e independientes del factor tisular. A 5. VC ED AS, CIDEMIHPARG
Trombocitopenia y disfuncin plaquetaria
esta dosis domina el mecanismo independiente por el cual 6. Otras indicaciones
el FVIIra se une directamente a la superficie plaquetaria ARAP
reemplazando al complejo de tenasa, lo que induce gene- 1. Reversin de anticoagulacin
racin de grandes cantidades de trombina.37-39 ACIDMOIB ARUTARETIL :CIHPARGIDEM
Se han publicado 156 artculos relacionados al empleo Erhardtsn fue el primero en describir que el FVIIra reverta
de FVIIra en hemofilia A o B con anticuerpos contra los rpidamente el efecto de los anticoagulantes orales de una
factores VIII y IX respectivamente. Los primeros reportes manera dosis-dependiente, lo que posteriormente fue co-
valoraron la eficacia de este medicamento en enfermos rroborado en 28 publicaciones. La dosis recomendada es
que requeran ciruga por artropata hemoflica. Una vez entre 15 a 90 g/kg, la cual deber adecuarse a la prolonga-
demostrada su eficacia y seguridad se reportaron casos cin del INR. En enfermos intoxicados con anticoagulantes
aislados y series de casos que incluyeron a 408 pacien- orales que cursan con hemorragia aguda grave e INR mayor
tes. En todos se demostr de manera concordante que el de 10 se han empleado dosis de hasta 320 g/kg.
FVIIra prevena y/o controlaba la hemorragia. En una re- La hemorragia del sistema nervioso central secunda-
visin sistemtica de la base de datos de 2 estudios inter- ria a anticoagulantes orales tiene una elevada mortali-
nacionales se demostr que dosis de FVIIra 90 g/kg era dad que llega a ser del 60%. En una serie de siete pa-
suficiente para controlar el sangrado en un lapso de 2-3 cientes sobreanticoagulados con warfarina y con
horas en 80-87% de los enfermos con episodios de he- hemorragia cerebral el FVIIra redujo el INR de 7 a 1.5 o
morragia grave espontnea y 91-94% de la hemorragia menos en los primeros 10 minutos de su aplicacin.
quirrgica. En el programa de tratamiento emergente de Tres de estos siete pacientes haban recibido previamen-
hemorragia en hemofilia que incluy a 127 pacientes con te plasma fresco congelado sin haberse presentado res-
253 episodios de hemorragia se demostr que el FVIIra a puesta satisfactoria. Estos mismos resultados se han
dosis de 90 mg/kg de peso fue efectivo en controlar el observado en pacientes con hematoma en el canal es-
sangrado en 93% de los pacientes con hemofilia cong- pinal o subdural que requera descompresin quirrgica
nita y en el 71% de los pacientes con hemofilia adquiri- urgente en los cuales la reversin del efecto anticoagu-
da. En los estudios en los que se valor la efectividad del lante se logr con FVIIra a dosis de 40 a 80 g/kg. En
FVIIra en pacientes con hemofilia y ttulos elevados de ninguna de las series reportadas se presentaron compli-
inhibidores se demostr que era efectivo en controlar la caciones trombticas.47-51
hemorragia en 80-90% de los casos a dosis de 90 g/kg El pentasacrido sinttico fondoparinux inhibe selectiva-
con lo que se logran niveles sricos de 20-30 UI/mL. Es mente al FXa y se emplea la profilaxis de enfermedad trom-
importante mencionar que algunos enfermos requieren boemblica venosa en artroplastia de cadera y rodilla.
una segunda o tercera dosis con intervalos de 2-3 horas y En un estudio aleatorizado y controlado por placebo en vo-
algunos estudios han reportado el uso de infusin conti- luntarios sanos se encontr que el FVIIra a dosis de 90 g/
nua a 50 g/kg/hora. Hasta el momento no hay estudios kg reverta el efecto de 10 mg de fondoparinux restaurando
aleatorizados en los que se comparen la infusin conti- la generacin de trombina. En un estudio similar el FVIIra
nua vs bolos horarios.40-45 corrigi el efecto anticoagulante del idraparinux, el cual es
un pentasacrido con una vida media de 5.5 das.52,53
b) FVIIra EN HEMORRAGIA NO HEMOFLICA An no se ha definido si el FVIIra puede ser usado como
antdoto de los inhibidores directo de trombina como el
edigraphic.com
Una vez validada la eficacia y seguridad del FVIIra en
hemofilia y posterior a un reporte que apareci en 1999
ximelagatran. En un ensayo clnico realizado en volunta-
rios sanos los efectos anticoagulantes del inhibidor de trom-
en el que se describi el uso FVIIra para el control de bina no se vieron afectados por la administracin de FVIIra
hemorragia no controlable en un soldado con herida por a dosis de 90 g/kg. Sin embargo, en este estudio se de-
proyectil de arma de fuego, se inici su aplicacin tera- mostr que el FVIIra increment a los precursores de trom-
putica para el manejo de la hemorragia crtica aguda de bina de manera dosis-dependiente.54
30 ACTA MDICA GRUPO NGELES. Volumen 5, No. 1, enero-marzo 2007
Modelo celular de la hemostasia y factor VII recombinante
2. Ciruga y trauma mer reporte del empleo del FVII en hemorragia por lesio-
nes de guerra fue hecho por el grupo israel, al cual siguie-
La hemorragia crtica aguda no controlada es una de las ron otros reportes. En un estudio aleatorizado el empleo
principales causas de morbimortalidad en trauma y en de FVII redujo de manera significativa la hemorragia y los
periodo perioperatorio. La hemorragia microvascular difu- requerimientos transfusionales. En el estudio de Boffard
sa que se presenta posterior a ciruga de control de daos en los enfermos en los que se emple FVII se redujo en
habitualmente est asociada a la trada letal de hipoter- 63% la incidencia de transfusin masiva. En la guerra de
mia, acidosis y coagulopata. La respuesta de esta compli- Irak se han utilizado 600 dosis de FVIIra en 300 soldados
cacin hemorrgica a la transfusin de concentrados eri- siguiendo el protocolo de una dosis inicial de 90 g/kg al
trocitarios, plasma fresco, concentrados plaquetarios y llegar al servicio de emergencias u otra dosis de 90 g/kg
soluciones coloides y cristaloides es habitualmente infruc- al controlar la hipotermia. En esta experiencia militar se
tuoso y exacerban la dilucin de factores, la coagulopata lleg a la conclusin que el FVIIra tiene una funcin im-
y la hipotermia, lo que induce una mayor hipoperfusin portante en disminuir la hemorragia y los requerimientos
tisular. Por lo anterior, desde hace algunos aos se postul de transfusin en heridas de guerra.60-62
que el empleo de FVIIra podra ser una buena alternativa
teraputica para este grupo de enfermos. Hasta el 2005 3. Hepatopata y trasplante heptico
se haban reportado en relacin a este tpico 21 reportes
de casos, 26 series de casos y un estudio aleatorizado. En La insuficiencia heptica habitualmente se complica con
todos ellos se demostr que el FVIIra a dosis de 90 a 120 coagulopata y hemorragia a diferentes niveles, principal-
g/kg en 1 2 dosis era efectivo y seguro para el control mente variceal, secundaria a hipertensin portal. La coa-
de la hemorragia. En un estudio aleatorizado que incluy a gulopata de la insuficiencia heptica es compleja y multi-
301 pacientes con traumas cerrados o penetrantes el FVII- factorial. Dentro de la fisiopatologa destaca la disminucin
ra a dosis de 400 g/kg en 3 dosis redujo de manera signi- en la sntesis de factores de coagulacin dependientes de
ficativa la hemorragia, los requerimientos de transfusin y vitamina K (II, VII, IX y X), protenas C y S, trombocitope-
la incidencia de disfuncin orgnica mltiple y el sndrome nia, hiperfibrinlisis y disfibrinogenemia. Los niveles de
de insuficiencia respiratoria aguda. El efecto benfico fue factor VII son uno de los indicadores pronsticos ms sig-
ms significativo en el trauma cerrado. En un estudio que nificativos en insuficiencia heptica y cirrosis. En la litera-
incluy a 36 pacientes programados para prostatectoma tura existen mltiples reportes de la seguridad y eficacia
abdominal el FVIIra a dosis de 20 a 40 g/kg en el preope- del FVIIra para el control y profilaxis de la hemorragia aso-
ratorio redujo un 50% la hemorragia.55-58 ciada a insuficiencia heptica tanto en adultos como en la
El FVIIra se ha empleado en los siguientes escenarios poblacin peditrica. La dosis de FVIIra recomendada para
quirrgicos: el control de la hemorragia secundaria a insuficiencia he-
ptica es 80 g/kg. En un estudio aleatorizado que incluy
Trasplante heptico a 245 pacientes con cirrosis heptica e hipertensin portal
Hepatectomas que ingresaron al hospital por hemorragia digestiva alta la
Complicaciones hemorrgicas obsttricas administracin de FVIIra a dosis de 100 g/kg asociado a
Ciruga cardiaca tratamiento endoscpico redujo de manera significativa la
Reparacin de aneurisma artico hemorragia variceal comparado al placebo (7.9 vs 15.4%).
Este efecto se present en pacientes con Child B-C. En
El FVIIra se ha utilizado con xito para el manejo de la otro estudio que incluy a 71 pacientes con cirrosis some-
hemorragia asociada a ciruga cardiotorcica y vascular en tidos a biopsia heptica laparoscpica, la hemorragia se-
los escenarios de colocacin de dispositivos de asistencia cundaria a sta se control en el 74% de los pacientes a
ventricular, oxigenacin extracorprea de membrana y los 10 minutos de haber aplicado una dosis de 120 g/kg
bypass cardiopulmonar. Diferentes series de casos realiza- de FVIIra, 20% de los pacientes requirieron de una dosis
das en adultos y nios sometidos a ciruga cardiaca han de rescate de 80 g/kg.63-66
demostrado que el FVIIra a dosis de 90 a 180 g/kg en En un estudio aleatorizado que incluy a 204 pacientes
edigraphic.com
una o dos dosis disminuyen de manera significativa la he-
morragia no controlada y reduce los requerimientos de
no cirrticos sometidos a hepatectoma el FVIIra a dosis
de 80 g/kg de peso redujo la hemorragia y los requeri-
concentrados eritrocitarios, crioprecipitados, plasma fres- mientos de transfusin de manera significativa comparada
co y afresis plaquetaria.59 a una dosis de 20 g/kg y al placebo. Hendrix y cols. re-
El trauma militar sigue siendo una prioridad a nivel portaron que en pacientes sometidos a trasplante hep-
mundial por el gran nmero de conflictos blicos. El pri- tico ortotpico el FVIIra a dosis de 80 g/kg en una o dos
ACTA MDICA GRUPO NGELES. Volumen 5, No. 1, enero-marzo 2007 31
Carrillo Esper R y cols.
dosis disminua de manera significativa la hemorragia com- ron 664 pacientes con hemofilia A o B tratados con FVIIra
parada a controles histricos. En una serie de casos que se presentaron 7 eventos tromboemblicos. La incidencia
incluy a nios sometidos a trasplantes hepticos, dosis de efectos adversos de todas las series reportadas de uso
de 37 a 148 g/kg de FVIIra redujeron de manera signifi- de SUSTRADODE-M.E.D.I.G.R.A.P.H.I.C
FVIIra en pacientes no hemoflicos es del 1.4%. Las
cativa la hemorragia sin que se presentaran eventos trom- complicaciones ms frecuentemente reportadas son: Trom-
boemblicos.67-69 :ROP
bosis ODAROBALE
venosa profunda y FDP
embolismo pulmonar, aunque tam-
bin se han descrito infarto agudo del miocardio, eventos
4. Hemorragia cerebral no traumtica VC ED AS,
vasculares CIDEMIHPARG
cerebrales trombticos y trombosis arteriales de
extremidades.82-84
La hemorragia cerebral no traumtica es un proceso din- ARAP
mico. Varios estudios han demostrado que la hemorragia CONCLUSIONES
cerebral se expande en las primeras 3-6 horas despus de ACIDMOIB ARUTARETIL :CIHPARGIDEM
que se inicia con un incremento hasta del 38% del volu- El modelo celular de la hemostasia abre un nuevo horizon-
men inicial. Este evento es fundamental, debido a que te para el entendimiento de la coagulacin y explica los
uno de los principales factores de mal pronstico es el eventos que se suceden en la hemorragia crtica aguda no
volumen de la hemorragia. Por este motivo se ha desarro- controlada de diferente etiologa, lo que dio por resultado
llado una nueva alternativa de manejo denominada Tera- la introduccin en la prctica clnica del FVIIra para el
pia hemosttica ultratemprana para el manejo de la he- manejo de la hemostasia en situaciones caracterizadas por
morragia cerebral y que consiste en la aplicacin en las una deficiente generacin de trombina.
primeras 3-4 horas de iniciada la hemorragia de FVIIra. En
un estudio aleatorizado recientemente publicado se de-
mostr que el FVIIra a dosis de 160 g/kg en una sola REFERENCIAS
dosis redujo de manera significativa el volumen de la he-
morragia cerebral, lo que se reflej en una mayor sobrevi- 1. Davie EW, Ratnoff OD. Waterfall sequence for intrinsic blood
da con mejor calidad de vida.70-72 clotting. Science 1964; 145: 13120-1312.
2. McKenna R. Abnormal coagulation in the postoperative period
contributing to excessive bleeding. Med Clin North Am 2001;
5. Trombocitopenia y disfuncin plaquetaria 85: 1277-1310.
3. Oliver J, Monroe D, Roberts H. Thrombin activates factor XI on
Existen varios reportes en la literatura que valida el uso del activated platelets in the absence of factor XII. Arterioescler
FVIIra en pacientes con hemorragia secundaria a trombo- Thromb Vasc Biol 1999; 19: 170-177.
4. Repke D, Gemmel CH, Guha A. Hemophilia as defect of the
astenia de Glanzmann, trombocitopenia grave, secundaria tissue factor and factor VII and IX on factor X activation in a conti-
a mielodisplasia, leucemia aguda mieloide y trasplante de nuous -flow reactor. Proc Natl Acd Sci USA 1990 ; 87: 7623-7627.
mdula sea, sndrome de Bernard-Soulier y enfermedad 5. Hoffman M, Monroe DM, Oliver JA. Factors IX and Xa play
de Von Willebrand.73-79 distinct roles in tissue Factor-dependent initiation of coagula-
tion. Blood 1995; 86: 1794-1801.
6. Bagli FA, Walsh PN. Prothrombin is a cofactor for the binding of
6. Otras indicaciones factor XI to the platelet surface and platelet-mediated factor XI
activation by thrombin. Biochemistry 1998; 37: 2271-2281.
El FVIIra se ha utilizado con xito para el manejo de he- 7. Carrillo ER, Villaseor OP. Coagulopata del paciente quirrgi-
co. El nuevo modelo celular de la coagulacin y su aplicacin en
morragia pulmonar, secundaria a enfermedades autoinmu- anestesiologa. Rev Mex Anest 2004; 27: 219-230.
nes, alveolitis y trasplante de mdula sea.80,81 8. Allen GA, Moroe DM, Roberts HR. The effect of factor X level
A pesar de su eficacia y amplio margen de seguridad el on thrombin generation and the procoagulant effect of activated
uso de FVIIra deber de valorarse cuidadosamente en re- factor VII in a cell-based model of coagulation. Blood Coagul
Fibrinolysis 2000; 11: S3-S7.
lacin a su costo-efectividad y costo-beneficio, debido a 9. Hoffman M, Monroe DM, Roberts HR. Activated VII factor acti-
que este medicamento es costoso y tiene efectos secun- vates factors IX and X on the surface of activated platelets: thoug-
darios. Los efectos adversos del FVIIra estn relacionados ht on the mechanism of action of high-dose activated factor VII.
a su potente efecto prohemosttico y son procesos trom- Blood Coagul Fibrinolysis 1998; 9: S61-S65.
10. Rapaport IS, Rao LV. Initiation and regulation of tissue factor
edigraphic.com
bticos arteriales y/o venosos, sobre todo en situaciones
asociadas a un exceso de factor tisular como sera el caso
dependent blood coagulation. Atheroscler Thromb 1992; 12:
1111-1121.
de la coagulacin intravascular diseminada y ruptura de 11. Roberts HR, Monroe DM, Oliver JA, Chang YJ, Hoffman M.
placas de ateroma. En pacientes con hemofilia la inciden- Newer concepts of blood coagulation. Haemophilia 1998; 4:
331-334.
cia de efectos adversos asociados al uso del FVIIra es de 12. Hoffman M, Monroe DM. The action of high- dose factor VIIa in a
aproximadamente 1%. En un estudio en el que se incluye- cell- based model hemostasis. Dis Month 2003; 49: 178-182.
32 ACTA MDICA GRUPO NGELES. Volumen 5, No. 1, enero-marzo 2007
Modelo celular de la hemostasia y factor VII recombinante
13. Monroe DM, Roberts HR, Hoffman DM. Platelet procoagulant 38. Monroe DM, Hoffman M, Oliver JA. Platelet activity of high-
complex assembly in a tissue factor initiated system. Br J Hae- dose factor VIIa is independent of tissue factor. J Haematol 1997;
matol 1994; 88: 364- 371. 99: 542-547.
14. Nemerson Y, Esnouf MP. Activation of proteolytic system by a 39. He S, Blomback M, Ekman GJ. The role of recombinant factor VII
membrana lipoprotein: Mechanism of action of tissue factor. a (FVIIa) in fibrin structure in absence of FVIII/FIX. J Thromb
Proc Natl Acd Sci USA 1973; 70: 310-314. Haem 2003; 1: 1215-1219.
15. Kirchhofer D, Nermerson Y. Initiation of blood coagulation: the 40. Shapiro AD, Gilchrist GS, Hoots WK. Prospective, randomized
tissue factor/factor VIIa complex. Curr Opin in Biotech 1996; 7: trial of two doses of rFVIIa (NovoSeven) in haemophilia patients
386-391. with inhibitors undergoing surgery. Thromb Haemost 1998; 80:
16. Roberts HR, Monroe DM, Escobar MA. Current Concepts of 773-778.
Hemostasis. Anesthesiology 2004; 100: 722-730. 41. Hay CR, Negrier C, Ludlan CA. Treatment of bleeding in acqui-
17. Giesen PL, Nermerson Y. Circulating Tissue factor on loose. red haemophilia with recombinant factor VIIa. A multicentre
Semin Thromb Hemost 2000; 26: 379-384. study. Throm Haemost 1997; 78: 1463-1467.
18. Rauch U, Nemerson Y. Circulating tissue factor and thrombosis. 42. Ingerslev J, Thykjaer H, Kudsd JO. Home treatment with recom-
Curr Opin Hematol 2000; 7: 273-277. binant activated factor VII: Results from one centre. Blood Coa-
19. Carrillo ER, Salmern NP, Carvajal RR, Domnguez DV. Rom- gul Fibrinolysis 1998; 9: 107-110.
piendo un paradigma: del modelo humoral al modelo celular 43. Laurean Y, Goudemand J, Negrier C. Use of recombinant activa-
de la coagulacin. Su aplicacin clnica en el enfermo grave. Rev ted factor VII as first line therapy for bleeding episodes in hae-
Asoc Mex Med Crit y Ter Int 2004; 18: 17-23. mophilics with factor VIII or IX inhibitors. Blood Coagul Fibrino-
20. Rao L, Williams T, Rapaport S. Studies of the activation of factor lysis 1998: 155-156.
VII bound to tissue factor. Blood 1996; 87 37: 738-748. 44. Smith MP, Ludlam CA, Collins PW. Elective surgery on factor VIII
21. Dahlback B. Blood Coagulation. Lancet 2000; 335: 1627-1632. inhibitor patients using continuous infusion of recombinant acti-
22. Rao L, Rapaprot S, Bajaj S. Activation of human factor VII in the vated factor VII: Plasma factor VII activity of 10 IU/mL is associa-
initiation of tissue factor-dependent coagulation. Blood 1986; ted with an increased incidence of bleeding. Thromb Haemost
68: 685-691. 2001; 86: 949-953.
23. Hofman M, Monroe D, Oliver J, Roberts H. Factors IXa and Xa 45. Ludlam CA, Smith MP, Morfin M. A prospective study of recom-
play distinct roles in tissue factor-dependent initiation of coagu- binant activated factor VII administered by continuous infusion
lation. Blood 1995; 86: 1794-1801. to inhibitor patients undergoing elective major orthopaedic sur-
24. Lau H. The interaction between platelets and factor VII/VIIa. gery: A pharmacokinetic and efficacy evaluation. Br J Haematol
Transf Apheresis Sci 2003; 28: 279-283. 2003; 120: 808-813.
25. Doschi S, Marmur J. Evolving role of tissue factor and its pathway 46. Kenet G Walden R, Eldad A. Treatment of traumatic bleeding
inhibitor. Crit Care Med 2002; 30: S241-250. with recombinant factor VIIa. Lancet 1999; 354: 1879-1881.
26. Hoffman M. A cell-based model of coagulation and the role of 47. Erhardtsen E, Nony P, Dechavanne M. The effect of recombinant
factor VIIa. Blood Rev 2003; 17: 51-55. factor VIIa (NovoSeven) In healthy volunteers receiving aceno-
27. Brummel KE, Paradisi SG, Butenas S. Thrombin functions du- coumarol to an international normalized ratio above 2.0. Blood
ring tissue factor-induced blood coagulation. Blood 2002; 100: Coagul Fibrinolysis 1998; 9: 741-748.
148-152. 48. Deveras RA, Kessler CM. Reversal of warfarina-induced exces-
28. Hockin MF, Jones KC, Everse SJ. A model for the stoichiometric sive anti-coagulation with recombinant human factor VIIa con-
regulation of blood coagulation. J Biol Chem 2002; 277: 1832- centrate. Ann Intern Med 2002; 137: 884-888.
1833. 49. Sorensen B, Johansen P, Nielsen GL. Reversal of the internatio-
29. Ten Cate H, Bauer K, Levi M. The action of factor X and pro-
nal normalized ratio with recombinant activated factor VII in
thrombin by recombinant factor VII a in vivo is mediated by
central nervous system bleeding during warfarin thrombo-
tissue factor. J Clin Invest 1993; 92: 1207-1212.
phylaxis: clinical and biochemical aspects. Blood Coagul Fibri-
30. Mann K. Potential analyzes for the diagnosis of thrombosis: An
nolysis 2003; 14: 469-477.
overview. Ann Epidemiol 1992; 2: 365-370.
50. Lin J, Hanigan WC, Tarantino M. The use of recombinant factor
31. Monroe DM, Hoffman M, Oliver JA. Platelet activity of high-
VII to reverse warfarin induced anticoagulation in patients with
dose factor VIIa is dependent of tissue. Br J Haematol 1997; 99:
hemorrhages in the central nervous system: preliminary fin-
542-547.
ding. J Neurosurg 2003; 98: 737-740.
32. Kjalke M, Ezban M, Monroe D. High- dose factor VIIa increases
initial thrombin and mediates master platelet activation in throm- 51. Park P, Fewel M, Garton HJ. Recombinant activated factor VII for
bocytopenia like conditions in a cell based model system. Br J the rapid correction of coagulopathy in nonhemophilic neuro-
Haematol 2001; 14: 114-120. surgical patients. Neurosurgery 2003; 53: 34-38.
33. Osterud B. The role of platelets in decrypting monocyte tissue 52. Bijsterveld NR, Moons AH, Boekholdt SM. Ability of recombi-
factor. Semin Hematol 2001; 38: 2-8. nant factor VIIa to reverse the anticoagulant effect of the penta-
34. Bom VJ, Bertina RM. The contributions of Ca, phospholipids saccharide fondaparinux in healthy volunteers. Circulation 2002;
and tissue factor apoprotein to the activation of human blood- 106: 2550-2554.
coagulation factor X by activated factor VII. Biochem J 1990; 53. Bijstervelde NR, Vink R, Van Aken BE, Fennenma H, Peters RJ.
265: 327-336. Recombinant factor VIIa reverses the anticoagulant effect of the
edigraphic.com
35. Mann KG. Thrombin: Physiology and Pathophysiology. Chest
2003; 124: 1-7.
long acting pentasaccharide idraparinux in healthy volunteers.
Br J Haematol 2004; 24: 653-658.
36. Golino P. The inhibitors of the tissue factor: factor VII pathway. 54. Wolzt M, Sarich TC. Effect of recombinant factor VIIa on melaga-
Thromb Res 2002; 106: 257-265. tran-indiced inhibition of thrombin generation and platelet activa-
37. Friederich PW, Levi M, Bauer KA. Ability of recombinant factor tion in healthy volunteers. Thromb Haemost 2004; 91: 1090-1096.
VII to generate thrombin during inhibition of tissue factor in 55. Friederich PW, Henny CP, Messelink EJ. Effect of recombinant
human subjects. Circulation 2001; 103: 2555-2559. activated factor VII on perioperative blood loss in patients un-
ACTA MDICA GRUPO NGELES. Volumen 5, No. 1, enero-marzo 2007 33
Carrillo Esper R y cols.
dergoing retropubic prostatectomy: A double-blind placebo- 70. Davis SM, Broderick J, Hennerici M, Brun NC, Diringer MN,
controlled randomized trial. Lancet 2002; 361: 201-205. Mayer AS, Begtrup, Steinner T. Hematoma Growth is a determi-
56. Kenet G, Wlden R, Eldad A. Treatment of traumatic bleeding nant of mortality and poor outcome after intracerebral hemorr-
with recombinant factor VIIa. Lancet 1999; 354: 1879-1884. hage. Neurology 2006; 66: 1175-1181.
57. Martinowitz U, Kenet G, Segal E. Recombinant Activated Factor 71.SUSTRADODE-M.E.D.I.G.R.A.P.H.I.C
Mayer SA, Brun NC, Begtrup K. Recombinant activated factor
VII adjunctive hemorrhage control in trauma. J Trauma 2001; VII for acute intracerebral hemorrhage. N Engl J Med 2005; 352:
51: 431-438. :ROP ODAROBALE FDP
777-785.
58. Boffard KD, Warren B, Lau P. Decreased transfusion utilization 72. Mayer SA, Rincn F. Ultra-early hemostatic therapy for Acute
and improved outcome associated with the use of recombinant Intracerebral hemorrhage. Semin Hematol 2006; 43: 70-76.
factor VII as an adjunct in trauma. J Trauma 2004; 57: 451-459. 73.VC ED M,
Peters AS,Heijboer
CIDEMIHPARG
H. Treatment of a patient with Bernant-
59. Enomoto MT, Thorboorg P. Emerging off-label Uses for Recom- Soulier Syndrome and recurrent nosebleeds with recombinant
binant Activated Factor VII: Grading the evidence. Crit Care Clin ARAP
factor VIIa. Thromb Haemost 1998; 80: 352-354.
2005; 21: 611-632. 74. Poon MC, Demers C, Jobin F. Recombinant factor VIIa is effecti-
60. Sebesta J. Special Lessons Learned from Iraq. Surg Clin N Am ve for bleeding and surgery in patients with Glanzmann Throm-
2006; 86: 711-726. ACIDMOIB
basthenia. Blood ARUTARETIL :CIHPARGIDEM
1999; 94: 3951-3953.
61. Harrison T, Daniel DO, Laskosky J. Low dose Recombinant acti- 75. Poon Mc, dOrioron R, Von Depka M. Prophylactic and thera-
vated factor VII (rFVIIA) results in less packed red blood cell peutic recombinant factor VIIa administration to patients with
( PRBC) use in traumatic hemorrhage. J of Trauma Injury Infec- Glanzmanns thrombasthenia: Results of an International Sur-
tion and Crit Care 2004; 57: 1383-l389. very. J Thromb Haemost 2004; 2: 1096-1103.
62. Boffard KD, Riou B, Warren B. For the Novoseven Trauma Study 76. Tramholm M, Rojkjaer R, Pyke C. Recombinant factor VIIa redu-
Group. Recombinant factor VIIa as adjunctive therapy for blee- ces bleeding in severely thrombocytopenic rabbits. Thromb Res
ding control in severely injured trauma patients: two parallel 2003; 109: 217-223.
randomized, placebo-controlled, double blind clinical trials. J 77. Kristensen J, Killander A, Hippe E. Clinical experience with re-
of Trauma Injury Infection and Crit Care 2005; 59: 18. combinant factor VIIa in patients with thrombocytopenia. Hae-
63. Bernstein DE, Jeffers L, Erhardtsen E. Recombinant factor VIIa mostasis 1996; 26: 159-164.
corrects prothrombin time in cirrhotic patients: a preliminary 78. Erhardtsen E. Ongoing NovoSeven trials. Intensive Care Med 2002;
study. Gastroenterology 1997; 113: 1930-1937. 20: 248-255.
64. Ejlersen E, Melsen T, Ingerslev J. Recombinant activated factor 79. Vidarsson B, Onundarson PT. Recombinant factor VIIa for blee-
VII (rFVIIa) acutely normalizes prothrombin time in patients with ding in refractory thrombocytopenia. Thromb Haemost 2000;
cirrhosis during bleeding from aesophageal varices. Scand J Gas- 83: 634-635.
troenterol 2001; 36: 1081-1085. 80. Pastores MS, Papadopoulos E, Voigt L, Halpern N. Diffuse Alveo-
65. Bosch J, Thabut D, Bendtsen F. Recombinant factor VII for upper lar Haemorrhage after Allogeneic Hematopoietic Stem-Cell
gastrointestinal bleeding in patients with cirrhosis: A randomi- Transplantation. Treatment with recombinant factor VIIa. Chest
zed double- blind trial. Gastroenterology 2004; 127: 1123-1130. 2003; 124: 256-260.
66. Jeffers L, Chlasani N, Balart L. Safety and efficacy of recombinant 81. Hicks K, Peng D, Gajewski JL. Treatment of diffuse alveolar he-
factor VIIa in patients with liver disease undergoing laparoscopic morrhage after allogeneic bone marrow transplant with recom-
biopsy. Gastroenterology 2002; 123: 118-126. binant factor VIIa. Bone Marrow Transplant 2002; 30: 975-978.
67. Hendriks Hg, Meijer K, de Wolf JT. Reduced transfusion requi- 82. Roberts HR. Clinical experience with activated factor VII: focus
rements by recombinant factor VIIa in orthotopic liver trans- on safety aspects. Blood Coagul Fibrinolysis 1998; 9: 115-118.
plantation: A pilot study. Transplantation 2001; 71: 402-405. 83. Peerlinck K, Vermylen J. Acute myocardial infarction following
68. Lodge P, Jonas S, Jaeck D. Recombinant factor VIIa in partial administration of recombinant activated factor VII (NovoSeven)
hepatectomy: A randomized placebo- controlled, double blind in patients with haemophilia A and inhibitor. Thrombo Haemost
clinical trial. J Hepatol 2003; 36: 117-122. 1999; 82: 1175-1176.
69. Markiewez M, Kalicinski P, Kaminski A. Acute coagulopathy after 84. Aledort LM. Comparative thrombotic event incidence after in-
reperfusion of the liver graft in children correction with recom- fusion of recombinant factor VIIa versus factor VIII inhibitor bypass
binant activated factor VII. Transplant Pro 2003; 35: 2318-2319. actively. J Thromb Haemost 2004; 2: 1700-1708.
edigraphic.com
34 ACTA MDICA GRUPO NGELES. Volumen 5, No. 1, enero-marzo 2007
You might also like
- Historia Clinica Multi Modal AdolescentesDocument11 pagesHistoria Clinica Multi Modal AdolescentesNayeli Garcia100% (10)
- Cirugia General Examen NormalDocument5 pagesCirugia General Examen NormalDaniel Buelvas87% (15)
- Preguntas PATOLOGIA ROBBINS 1Document12 pagesPreguntas PATOLOGIA ROBBINS 1Ana Paula Flores80% (25)
- CFC - PericardioDocument39 pagesCFC - PericardioGildasio Frazão100% (1)
- Prueba de Antiglobulina DirectaDocument17 pagesPrueba de Antiglobulina DirectaElias Cuartas GómezNo ratings yet
- Utilidad Clínica Del Extendido de Sangre PeriféricaDocument18 pagesUtilidad Clínica Del Extendido de Sangre PeriféricaElias Cuartas GómezNo ratings yet
- Utilidad Clínica Del Extendido de Sangre PeriféricaDocument18 pagesUtilidad Clínica Del Extendido de Sangre PeriféricaElias Cuartas GómezNo ratings yet
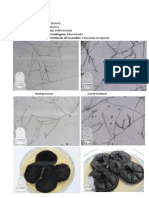
- Atlas Final ConidiogenesisDocument18 pagesAtlas Final ConidiogenesisElias Cuartas GómezNo ratings yet
- HIPERMAGNESEMIADocument5 pagesHIPERMAGNESEMIAAileen100% (1)
- Abdomen AgudoDocument28 pagesAbdomen AgudohaisenhairNo ratings yet
- Tarea 1 MorfofisiologiaDocument17 pagesTarea 1 MorfofisiologiaEsteban FinoNo ratings yet
- Disnea, Dolor Torácico, Dolor PleuríticoDocument21 pagesDisnea, Dolor Torácico, Dolor PleuríticoCarlos IzaguirreNo ratings yet
- Historia Clinica - Revision Por SistemasDocument32 pagesHistoria Clinica - Revision Por SistemasJose Orlando Quintero Correa33% (6)
- Ganoderma en El Tratamiento de EnfermedadesDocument16 pagesGanoderma en El Tratamiento de EnfermedadesNicolás AlzagaNo ratings yet
- FSSTA 006 DivulgaciónDocument6 pagesFSSTA 006 DivulgaciónElim JiménezNo ratings yet
- Laboratorio 1 de Agricola - NosotrasDocument12 pagesLaboratorio 1 de Agricola - Nosotrasnestorrojas07100% (1)
- DifilobotriasisDocument29 pagesDifilobotriasisFrancisco Javier Espitia RomeroNo ratings yet
- Anamnesis AdultoDocument4 pagesAnamnesis AdultoMyriam LenkaNo ratings yet
- Mundo Rottero 4Document67 pagesMundo Rottero 4ClaudioPenaNo ratings yet
- Historia Natural de PeritonitisDocument2 pagesHistoria Natural de PeritonitisAna Tapia62% (37)
- Aborto, Emb Ectopico y Mola HidatiformeDocument44 pagesAborto, Emb Ectopico y Mola HidatiformeWilliam CaleroNo ratings yet
- Novamil RefluxDocument8 pagesNovamil RefluxErica SanchezNo ratings yet
- Gota y Diseccdisis en ReptilesDocument6 pagesGota y Diseccdisis en ReptilesAlberto Delgado MayaNo ratings yet
- Sutura MecanicaDocument11 pagesSutura Mecanicalainskaster50% (2)
- Aparato Reproductor FemeninoDocument3 pagesAparato Reproductor FemeninoHebert AgNo ratings yet
- Sistema de Clasificacion Icta de Canales y Cortes 3 PDFDocument46 pagesSistema de Clasificacion Icta de Canales y Cortes 3 PDFGabriela ArciniegaNo ratings yet
- Respuesta Metabolica Al EstrésDocument19 pagesRespuesta Metabolica Al EstrésWhitney Calderón DíazNo ratings yet
- Aguirre - Santana - Morfofisiologia Humana. Diseccion de Corazon. 1Document8 pagesAguirre - Santana - Morfofisiologia Humana. Diseccion de Corazon. 1Veronica graciela AguirreNo ratings yet
- Marco Conceptual de La Lactancia MaternaDocument3 pagesMarco Conceptual de La Lactancia MaternaAnaOrtega100% (1)
- Manejo Del SGB en 10 Pasos. EspañolDocument13 pagesManejo Del SGB en 10 Pasos. EspañolEliana NataliaNo ratings yet
- Cadena Productiva Plantas MedicinalesDocument38 pagesCadena Productiva Plantas MedicinalesmsilestNo ratings yet
- Caballos y RazasDocument25 pagesCaballos y RazasSandra Milena Ramírez CajícaNo ratings yet
- Mal Levantamiento de Bolsas de Cemento en Una ConstrucciónDocument6 pagesMal Levantamiento de Bolsas de Cemento en Una ConstrucciónJose Manuel Cayllahua CaceresNo ratings yet