Professional Documents
Culture Documents
Contribución Al Estudio Citológico de Los Ciliados Hipotricos
Contribución Al Estudio Citológico de Los Ciliados Hipotricos
Uploaded by
Anonymous hQLzdXVo0 ratings0% found this document useful (0 votes)
18 views164 pagesOriginal Title
Contribución al estudio citológico de los ciliados hipotricos
Copyright
© © All Rights Reserved
Available Formats
PDF or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as PDF or read online from Scribd
0 ratings0% found this document useful (0 votes)
18 views164 pagesContribución Al Estudio Citológico de Los Ciliados Hipotricos
Contribución Al Estudio Citológico de Los Ciliados Hipotricos
Uploaded by
Anonymous hQLzdXVoCopyright:
© All Rights Reserved
Available Formats
Download as PDF or read online from Scribd
You are on page 1of 164
UNIVERSIDAD DE SEVILLA
BRARETARIA CIENCIAS
[ean AY
eae no _442,
CONTRIBUCION AL ESTUDIO CITOLOGICO DE
LOS CILIADOS HIPOTRICOS
Trabajo presentado para optar al Grado de Doctor
por la Licenciada D2 CONCEPCION FEDRIANI IRISO.
Q deans
Sevilla, Marzo de 1974
Prof. D. Julio Pérez Silva
Catedrético de Microbjologia “Atlas
s ¢
[= Si
emu &
Png a Y
aT
UNIVERSIDAD DE SEVILLA
FACULTAD DB BIOLOGIA
BistioTeca
Doy mi autorizacién a la Biblioteca de esta Facultad para
9.
que mi Tesis Doctoral.
af be
beatin. el Coleen
ey defo bes
= Consulta en depésito.
— Préstamo interbibliotecario.
— Reproduccién parcial.
- Reproduccién total.
= Tipo de Usuarios,
= Otros términos.
(O Alu au
Firmado: (Ces «
Sevilla, all de
El presente trabajo iniciado en 1971, ha sido rea-
lizado en el Departamento de Microbiologfa de la Facultad
de Ciencias de la Universidad de Sevilla, bajo la direccién
del Prof. J. Pérez Silya,a quien agradezco cordialmente su
orjentacién, interés y constante dedicacién.
Mis sinceros agradecimientos,
Al Dr. Rafael Molina y Pifial de Castilla y a Isabel
Sanchez. por-la valiosa y desinteresada ayuda que me han pres.
tado constantemente.
A la Dra. Gil Alvarez, del Instituto “Jaime Ferrdn”
de Microbiologia del C.S.1I.C. por la elaboracién de las mi -
crografias electrénicas.
A Antonio Torres Rueda,alumno de 5% Curso de Cien -
cias Btol6égicas y a José Arroyo Lépez, Licenctado en Ciencias
Blolégicas as{ como a los restantes compafieros de este Depar
tamento por su yaliosa ayuda.
Por Gltimo, agradezco el apoyo ecanémico que me han
prestado la Universidad de Sevilla y el Ministerio de Educa-
cién y Ciencia a través del Plan de Formacién de Personal In
vestigador.
INTRODUCCION....... bee e eee cece e ene eee
MATERIAL Y METODOS.....seseeeseeeeeeeees eee
A. MATERIALES.
B. METODOS...........- seen eee eres tenes
1,- Seleccién del material ........
2.- Medios de cultivo....... aeeeeee
3.- ObservaciGn in VivO.....eeeeeee
4,- Tincién de orgdnulos superfi -
ciales..
5.- Tincién de nacleos...........4+
6.- Tinciones para la observaci6n
con fluorescencia.......--. vee
7.- Técnicas para la microscopfa
electréntca. beeeee
RESULTADOS......
A. ESTUDIO SISTEMATICO DE LOS CILIADOS
DEL VALLE DEL GUADALQUIVIR..... tees
B. ESTUDIOS REALIZADOS CON LAURENTIA sp.
36
40
44
46
47
48
56
1.- Condiciones de cultivo........-e- 57
Zoe DESCHIPCLON. ..csecceeseeeseseeeees 59
B.~ DIVISION. cece eee ewe wae eeseeeae 67
a) Divisién nuclear.
b) Reorganizacién de los organulos
superficiales.. n
4.- Exquistamiento.....sseeeeeeeseeees 75
B.> ConjugactOn......ceseeeeecesseeees 78
C. ESTUDIOS REALIZADOS CON STYLONYCHIA MY
ILLUS eee eee eee eee Beene +. 80
DESCUSION. .c...6c cscs Geode eseseasseccdecase 5 88.
PONCLUSIONES.. 0... ee cece cece cece ncecnrveces | 94
RESUMEN. oc cceeeceseccceseccrctesveecseccveene) 99
BEBLIQGRAPIA......ccissccetsecesoeedeaetesees «103
INTRODUCCION
Comores sabido, los ciliados hipotricos son un
grupo de protozoos que se conoce desde hace mas de dos si-
glos y cuyos caracteres principales son: cuerpo aplanado
dorsoventralmente; cilios somdticos fusionados formando
rros en la superficie ventral; peristoma amplio con zona
adoral de membranelas bién desarrotlada; reproduccién ase~
xual por escisi6n binaria, reproduccién sexual por conjuga
cién; la mayorfa son formas libres que viven en agua dulce,
salobre o salada, y solo unos pocos son pardsitos.
De todos estos caracteres, la presencia de cirros
y la amplia zona adoral de membranelas son los dos rasgos
diferenciales mas importantes, ya que dan unidad a las casi
400 especies descritas hasta la fecha.
Segin datos que hemos recogido en las obras de
KAHL (40), KUDO (47), GRELL (30), HALL (32), CORLISS (16),
DOGIEL (23), asf como en la reciente versién de BORROR (15)
y-. en otras publicaciones que hemos consultado directamente,
el primer intento de clasificacién de los hipotricos fue
realizado en 1786 por MULLER, quiém reunié todas las espe-
ctes en dos géneros: Trichoda, con 89 especies, y Kerona,
con 14, basdndose en que todos presentan el caracter coman
de poseer “6rganos externos".
En 1830, EHRENBERG realizé una serie de trabajos
encaminados a establecer una clasificacién mas completa y
que culminan con el recenocimiento de 4 familias: la fami-
lia OXYTRICHIDAE, con cuatro géneros (Oxitricha, Kerona,
Urostyla, Stylonychia); la familia EUPLOTIDAE, con dos gé-
neros (Euplotes y Discocephalus); la familia ASPIDISCIDAE,
con un género (Aspidisca) y por Gitimo, la familia TRACHE-
LIDAE, con seis géneros de los cuates cinco no se conside-
ran actualmente como hipotricos.
En 1859, STEIN establece seis familias dentro de
los hipotricos, dos de las cuales se consideran actualmen-
te como pertenecientes a los holotricos; una, a los hetero
tricos, y las tres restantes, que son familias OXYTRICHI -
DAE, EUPLOTIDAE y ASPIDISCIDAE, son las que se admiten hoy
como pertenecientes al grupo de los hipotricos.
En 1889, BUTSCHLI reconoce sélo cuatro familias
de las seis establecidas por STEIN, pero sigue admitiendo
la familia PERITROMIDAE, que actualmente se incluye entre
los heterotricos. Ademés, establece una serie de subfami-
lias dentro de la familia Oxytrichidae.
Es POCHE (56) quien en 1909 deja reducido el gru
po de los hipotricos a las tres familias actualmente admi-
tidas.
Los trabajos de ALFRED KAHL marcan un hito en la
historia de la clasificacién de Tos ciliados hipotricos.
Su monograffa, publicada hace unos cuarenta afios (41) per.
manece vigente como recopilacién de las descripciones de
la mayoria de las especies publicadas antes de 1930. KAHL
divide el orden de los hipotricos em las tres familias ad-
mitidas por POCHE, y las define de acuerdo con los carac-
teres siguientes:
FAMILIA OXYTRICHIDAE: Zoma de membranelas bién
desarrollada. La dotacién de cirros corresponde esencial-
mente al tipo oréginal. Las hileras de cirros ventrales
suelen estar més o menos reducidas, pero siempre se con-
servan dos hileras (denominadas hiteras marginales). Exis,
ten cerdas dorsales.
FAMILIA EUPLOTIDAE: Zona de membranelas bién de
sarrollada. La dotacién de cirros esté m&s bién formando
grupos aislados. Las hileras margimales y ventrales no se
reconocen como tales. Existen cerdas dorsales.
FAMILIA ASPIDISCIDAE: Zoma de membranelas reducida
a una pequefia regién preoral aislada. En la parte anterior
izquierda se conserva todavia un resto dificilmente visi-
ble de membranelas muy pequefias, parecidas a cirros. La do
tacién de cirros se presenta en dos grupos claramente dis-
tintos en cuanto a su organizacién y configuraci6n: grupo
fronto ventral, que suele estar formado por siete cirros,
y el grupo transversal originariamente de cinco cirros,
que faltan a veces.
En cuanto a las subfamilias, KAHL considera que
las propuestas por BUTSCHLI estan justificadas por el
gran némero de géneros que comprende la familia Oxytrichi
daes pero, puesto que el propio KAHL descubrié gran ndme-
ro de formas intermedias (que tendfan a unir las subfami-
lias) asf como una serie de géneros nuevos que harian ne-
cesario la creacién de otras nuevas, no intenté revisar
las familias, sino que las dividié directamente en géneros.
Como veremos mas adelante, las especies objeto
de nuestro estudio pertenecen a la familia Oxytrichidae,
subdividida por KAHL en 26 géneros atendiendo principalmen
te a la existencia y disposicién de los cirros transversa-
les, caracter al que da preferencia sobre la disposici6n de
los cirros frontales.
A continuacién exponemos parte de la clave de
los géneros que nos va a ser necesaria a la hora de clasi
ficar las especies que hemos seleccionado para realizar el
presente trabajo.
1(24)
2g (1)
40(25)
41 (46)
42(43)
43(42)
44 (45)
45 (44)
4641)
Faltan los cirros transversales.
- En el campo frontal no existe ningin cirro espe-
cial mas engrosado y aistado. Las hileras ventra-
les se prolongan parcialmente hacia el campo fron
tal, hasta el borde anterior y no presentan ape-
nas cirros més gruesos. 26
- En el campo frontal existen cirros atslados y cla
ramente reforzados, casi siempre estén especial-
mente reforzados los tres cirros més anteriores.41
- Todos los cirros ventrales estén formando hileras
(de 1 a 6 hileras). En el caso de que haya cirros
ventrales totalmente aistados por detras de la bo-
ca, éstos no estén reforzados y son poco ostensi-
bles. En un género faltan complétamente los cirros
ventrales. 42
- Cirros ventrales formando cuatro o més hileras:
Urostyla.
- Cirros ventrales formando una a tres hileras, 0
faltan. 44
- Faltan los cirros ventrales (una especie marina
con peristoma en forma de cuello): Trachelostyla.
- De una a tres hileras ventrales: Holostycha
- Cirros ventrales, al menos en parte, reunidos en
grupos. 47
47658)
4g (53)
49 (50)
5049)
51 (52)
52(51)
53 (48)
54 (55)
55 (54)
Cirros yentrales, en parte, formando hasta tres hi.
leras; ademés existe un cirro postoral y un grupo
posterior de pocos cirros aislados. 48
Las hileras ventrales son cerradas, corren parale-
lamente al eje longitudinal. 49
Las hileras ventrales, cerradas, estén una a la iz
quierda y dos a la derecha. Cirros transversales
en hilera cerrada. Qnychodromopsis
Los dos cirros transversales del lado derecho estan
alejados y situados por detraés de los tres izquier
dos. 51
A cada lado hay una hilera cerrada en cirros ventra
les. Allotricha
Dos hileras cerradas de cirros ventrales en el la-
do derecho: Pleurotricha.
Las hileras de cirros ventrales cerradas corren cla
ramente oblicuas desde el lado anterior derecho has
ta el posterior izquierdo. 54
Una hilera oblicua de cirros ventrales que llega
hasta las proximidades de los cirros transversales.
Gastrostyla
Hileras ventrales cortas que apenas rebasan la base
del peristoma. La zona adoral es de posicién late~
ral: Gonostomum
56(47)
57 (58)
- Faltan hileras ventrales cerradas. 57
~ El extremo posterior del animal puede prolongarse
en un largo y delgado peddnculo: Ancystropodium
53 (57) - En el extremo posterior no se observa ninguna pro.
longacién. 59
59(50) _ En et campo frontal existen de 12 a 15 cirros grue
sos. MacronGcleo dividido en cuatro fragmentos
(cuatripartito): Onychodromus
60/59) _ En e1 campo frontal existen pocos cirros (en la ma
yorfa de los casos hay ocho dispuestos en tres gru
pos). Macronicleo casi siempre dividido en dos frag
ment mentos y rara vez en uno o cuatro: Oxytricha
En su libro publicado 1961 CORLISS (16) propone una
nueva clasificacién del orden Hypotricha, pero aunque acla-
ra algunos problemas de nomenclatura, aporta pocos datos
nueyos a tener en consideractén.
En el mismo afio, FAURE-FREMIET (26), bas&ndose en la
distribucién de los cirros, divide los hipotricos en dos
subérdenes:
Sub6rden Strichotrichina, con cirros fronto ventra -
les distribuidos regularmente en hileras y al que dividié
en cuatro familias. Suborden Sporadotrichina con seis o me
nos cirros por hilera y al que divididé también en cuatro
familias.
Esta modificacién fué aceptada como parte de la cla
sificacién propuesta por el Comité de Taxonomfa y Problemas
taxonémicos de 1a Sociedad de Protozoologos, presidido por
HONINGBERG (36).
Como puede verse, todos estos sistemas de clasifica-
cién estan basados en el aspecto morfoldgico que presentan
los individuos durante la interfase y por tanto no reflejan
apenas las posibles relaciones filogenéticas de unos grupos
con otros. Por otra parte, dado que no existen restos fési-
les, estas relaciones han de basarse principalmente en estu
dios comparativos de los procesos marfogenéticos.
En 1972 BORROR (15), basandose en los conocimientos
actuales sobre los procesos de morfogénesis durante la divi
sién de los ciliados hipotricos, ha elaborado un sistema de
clasificacién que pretende ser menos artificial que los an-
teriores y en el que se incluyen nuevas especies descritas
por diversos investigadores en afios recientes.
En este sistema propone las siguientes familias:
Familia Urostylidae, Familia Psilotrichidae, Familia
Holostichidae, Familia Spirofilidae, Familia Oxytrichidae
y Familia Euplotidae, las cuales veremos més adelante en de
talle.
10
Tratando de dar mayor uniformidad a la terminologia,
BORROR ha propuesto una serie de conceptos y términos para
definor los orgdnulos superficiales de los ciliados hipo-
tricos. Esta terminologta es la que adoptamos nosotros en
las descripciones y discusi6n, por ello creemos convenien-
te expresarla a continuacién:
Zona_adoral_de membranelas (ZAM).~ Aunque es facil-
mente-reconocible y aparentemente similar en la mayorfa de
los hipotricos, la ZAM no sélo varfa ampliamente de unos
géneros a otros dentro de una misma familia, sino que ade-
mas est sujeta a variaciones relacionadas coh la morfogé-
nesis. En efecto, durante 1a divisiGén celular, la zona de
membranelas de las células hijas posteriores pueden desarro
Jlarse sobre la superficie de la célula (Holostichia, Kah-
liella, y Urostyla) o bién en un surco subcortical (Euplo-
tes, Keronopsts, Trachelostyla). Por regla general, el pré
tero hereda 1a ZAM de 1a célula parental, pero en Diophrys,
Keronopsis, Trachelostyla y Uronichia 1a ZAM parental se
reabsorbe y es reemplazada por otra de nueva formacién
DEMBORKE (20), KOOL (46), WALLENGREU (77). Esta similitud
en la estomatogénesis del prétero en géneros tan alejados
es de poca importancia taxonémica y, por tanto, se atribuye
a una conyergencia evolutiva. Asf mismo existe cierta varia
11
cién intraespecifica en cuanto al n@mero de membranelas de
la ZAM, pero el aspecto general y de ésta 1a configuracién
(depresiones, crestas, posicién topegréfica) de la cavidad
bucal, es un caracter relativamente estable que puede ser
usado para la identificacién de las especies.
Membrana ondulante (MO).- BORROR admite éste término
dinicamente por su tradicién histérica, ya que sefiala la in-
conveniencia de emplear un nombre que también se aplica a
estructuras no homélogas que existem en otros grupos de pro
tozoos. En la mayorfa de los hipotricos, 1a MO consiste en
una serie longitudinal de cilios que a menudo corresponden
a mas de una hilera, y que estd situada a lo largo del bor-
de derecho de Ta abertura bucal. Durante 1a morfogénesis,
1a MO del prétero se origina por desdiferenciacién de la es
tructura parental y reorganizacién definitiva de una unidad
funcional. En el opisto, 1a MO se desarrolla a partir de
una serie longitudinal de granulos Basales, situados a la
derecha de 1a ZAM. Al parecer hay poca variabilidad intraes
pecifica en la configuracién de ta MO. Dentro de un mismo
género (por ejemplo Oxytricha platistoma) o, incluso dentro
de una familia (por ejemplo Euplotidae) puede haber una ten
dencfa hacia una hipertrofia de ta MO. Sin embargo, en los
Euplotidae, hay algunas especies que tienen una membrana on
dulante modificada, o bién carecen de ella.
12
Cirro bucal.- Durante la estomatogénesis, tos granu-
los basales del extremo anterior del primordio de la MO
proliferan y producen el cirro bucal. Asf, el primer cirro
frontal de Urostyla weissei, uno de tos cirros frontales de
Kahliella y el cirro 1/I de especies de Oxytricha y de los
Euplotidae no estén morfogenéticamente relacionados con los
demas cirros y constituyen un tipo especial de org&nulo. £1
cirro bucal puede aparecer inmediatamente a la derecha de
1a OM, o tener otra localizacién préxima al extremo anterior
de la superficie ventral de la célula.
Los tres tipos de orgdnulos que se acaban de descri-
bir no son exclusivos del Orden Hypotrichida, pues se han
observyado estructuras homélogas también en el heterotrico
CondyTostoma. E1 cirro bucal de Condylostoma se origina, no
a partir de la ciliacién somdtica, como indicé KAHL (41)
ni de Ta zona de membranelas, como imdicé FAURE-FREMIET(26),
sino a partir del extremo anterior de 1a membrana ondulante
desdiferenciada (76).
Los siguientes orgénulos, som privativos de las espe
cies del Orden Hypotrichia.
Cirros frontales.- Los cirros frontales estan situa-
dos en 1a superficte ventral a la derecha de 1a cavidad bu-
cal, y son, més o menos diferentes del resto de la cilia -
cién. Pueden presentarse formando hiteras de finos cirros o
13
bién formando grupos de cirros mas gruesos, y en Urostyla
grandis, por ejemplo, constituyen una parte muy ostensible
de 1a ciliacién. Los cirros frontales pueden originarse por
diferenciacién anterior de un campo de hileras de cilios,
que da lugar en su zona posterior a los cirros medio ventra
les, o bien a las hileras yentrales de cirros no modifica~
dos que aparecen en los Urostylidae y Holostichidae. Los ci
rros que en los Oxytrichidae y Euplotidae ocupan una posi-
cién topogréfica similar no son homélogos de los cirros
frontales y se denominan cirros. frontoventrales.
Cirros frontoventrales.- Est&n situados la superfi
cie ventral de algunos de los Urostytidae y miembros de los
Oxytrichidae y Euplotidae. Los cirros frontoventrales se
originan por coalescencia de los cilios de cinco o més (ge-
neralmente cinco) hileras longirudinales numeradas segdn el
sistema de Wallengren de la siguiente forma: La MO y el ci-
rro bucal se diferencian de la hilera 1; las restantes hile
ras se numeran de izquierda a derecha a través de la super-
ficie ventral, II-VI. Las especies de algunos géneros pre-
sentan una reduccién en el ndmero y un aumento en el tamafio
de los cirros de derecha a izquierda a trayés de la superfi
cie ventral. Es decir, la fila II suele dar lugar a menos
cirros y més grnades que la fila VI. También, En Oxytrichi-
dae y Euplotidae, el nimero total de cirros frontoventrales
14
producidos es un caraécter relativamente estable y a veces
puede utilizarse para la identificacién de géneros e inclu-
so de especies.
Cirros marginales izquierdos.- Alo largo del margen
ventrolateral izquierdo del cuerpo puede haber una o mas hi-
leras longitudinales de cirros marginales. £1 extremo ante-
rior de la hilera (0 hileras) termina en el borde posterior
izquierdo de la cavidad bucal. Los cirros marginales izquier
dos pueden faltar, como en Aspidisca, estar reducidos a dos
cirros como en Euplotes, o bién pueden formar una o més hile
ras longitudinales, pero estén sujetos a poca variaci6n es-
tructural dentro de cada especie. Los cirros marginales iz-
quierdos de las células hijas se originan a partir de hile-
ras longitudinales de cilfos que se desarrollan por dentro,
es decir, por el lado medial, de los cirros marginales iz-
quierdos parentales.
Cirros marginales derechos.- Una o més hileras longi
tudinales de ctrros marginales derechos pueden existir a lo
largo del margen ventrolateral del cuerpo. Aunque estos se
desarrollan de forma similar a los cirros marginales izquier.
dos, differen en variabilidad en cuanto. al némero de hileras
¥ probablemente en la estructura de las fibrillas radicula-
res ciliares (31).
15
Cirros transversales.- Este término tradicional alu-
de a un grupo de cirros cuyo conjunto sigue en muchos hipo-
tricos una trayectoria en forma de J o bién forma una linea
transversal de cinco o mas cirros muy ostensibles cerca del
extremo posterior de la célula. Tales cirros se originan,
al menos por tres procesos morfogenéticos diferentes. Los
cirros transversales de Urostyla weissei se derjvan de ci-
lios que proliferan en el extremo posterior de unas hileras
de algunos cirros parentales, que se desdiferencian. En
los Holostichidos los cirros transversales se diferencian a
partir de ciljos del extremo posterior del campo de cirros
medioventrales. En los Oxytrichidae y Euplotidae se desarro
lan a partir del Gltimo cirro (1/11, 2/111, 1/IV, 1/V, 1/VI)
que se origina junto con los cirros frontoventrales de un
campo de cinco hileras ventrales.
Cilios dorsales.- Los cilios de la superficie aboral
de los hipotricos pueden ser largos y facilmente visibles
(Trachelostyla), cortos y gruesos (Euplotes), o reducidos a
papilas o ausentes (Aspidisca). Sus cuerpos basales a menu-
do estan situados debajo de fosetas corticales y, al parecer,
no presentan cinetodesmos. Debido a Ya dificultad que encie-
rra Ja tincién de estas estructuras, solo en muy pocos casos
se ha estudiado su modo de replicacién (17) (18). En Urosty-
la wessei y Stylonichia (39) las hileras de cilios dorsales
16
se desarrollan por proliferacién cinetosémica de dos regio-
nes (anterior y posterior). Sin embargo, las dos filas dor
sales derechas en Stylonychia, no se fortian por dentro de
las antiguas, sino que aparecen sobre el margen derecho de
la célula, adyacentes al primordio de los nuevos cirros mar
ginales derechos. En Euplotes, los nuevos cirros dorsales
se originan a partir de hileras situadas cerca del plano de
divisién, en el ecuador de 1a célula. Aunque la creacién de
algunas especies est& parcialmente basada en el nimero de
hileras de cilios dorsales (12) (74), esta caracteristica
varfa dentro de las especies (11) (34).
Cirros caudales.- Los cirros posteriores bién dife -
renciados de Stylonychia, se originan a partfr de grdnulos
basales de los extremos posteriores de las cuatro primeras
hileras del lado izquierdo de la superficie dorsal y se lla
man cirros caudales.
Cirros caudales derechos.- Los cirros grandes que hay
en la superficie postlateral derecha de Diophrys y Uronychia,
asi como los pequefios cirros posteriores a los cirros trans-
versales en Euplotes, se derivan de los grénulos basales del
extremo posterior de las hileras de cil.ios del lado derecho
de la superficie dorsal (37) y, por tanto, no son homélogos
a los cirros caudales de Stylonychia. La posicién topografi-
ca comin y el origen morfogenético similar de estos cirros
17
en los Euplotidae, justifica el nombre empleado aqui.
Cirros medioventrales.- Entre los cirros marginales
derechos e izquierdos de los Holostichidae, hay una doble
fila de cirros que, a menudo, estan dispuestos en zig-zag.
Los cirros medioventrales se originan a partir de una serie
de hileras transversales en Urostyla cristata (39), Keronop-
sis rubra, Holosticha diademata, y Uroleptus caudatus (15).
Las hileras se forman por reagrupamiento de los cuerpos ba-
sales y cilios de estas hileras transversales. Tienen poca
yariacién en extensién lateral (p.e. ndmero de hileras). Sin
embargo, en la organizacién de Keronopsis rubra_, un indivi
duo puede tener ocasionalmente el grupo anterior de los ci-
rros medioventrales preexistentes, a un lado del campo re-
cién organizado. Las hileras transversales del extremo pos-
terior de este campo dan lugar a los cirros transversales en
este grupo de ciliados.
SISTEMA DE CLASIFICACION PROPUESTO POR BORROR. Tenien
do en cuenta los procesos morfogenéticos durante la divi -
sién y la dotacién de cirros de los individuos durante la
interfase, BORROR, (15) distingue seis familias:
1.- Familia Urostylidae: BUTSCHLI, 1889. Cirros en
3-12 filas ventrales. No existen cirros marginales, fronto-
18
ventrales o medioyentrales, distintos anatémica o morfogené
ticamente. Nueve géneros, con Urostyla como género tipo.
2.- Familia Psilotrichidae: BUTSCHLI, 1889. Cirros
relativamente uniformes, en 5-10 hileras ventrales oblicuas.
No existen cirros frontales diferenciados. Cirros transver-
sales poco ostensibles. Pequefias formas ovales con ciliaci6n
bucal moderadamente desarrollada y generalmente, con una
gran membrana ondulante. Tres géneros, con Psilotricha como
género tipo.
3.- Familia Holostichidae: FAURE-FREMIET, 1961. Exis
ten cirros marginales izquierdos, derechos y medioventrales.
Los cirros medioventrales generalmente se presentan formando
hileras en zig-zag, que se originan (al menos en Holosticha,
Keronopsis y Uroleptus) de la alineacién de hileras transver
sales de cilios durante la divisién. Siete géneros, con Ho-
losticha como género tipo.
4.- Familia Spirofilidae: VON GELET 1929. Cirros en
hileras helicoidales. Superficie aboral reducida a hileras
helicoidales. Siete géneros, con Hypotrichidium como género
tipo.
5.- Familia Oxytrichidae: EHRENBERG 1838. Al menos
una hilera a cada lado de cirros marginales, cada una de las
cuales contiene por 10 menos cinco y generalmente 20 0 més
19
cirros. Presentan cirros frontoventrales. Cirros transversa-
les generalmente presentes. Catorce géneros, con Oxytricha
como género tipo.
6.- Familia Euplotidae: EHRENBERG, 1838. Cirros mar-
ginales ausentes (excepto en el género Swedmarkia y una espe
cie de Discocephalus). Cirros marginales izquierdos, general
mente ausentes (Aspidisca, Euplotaspis, Gastrocirrus y Paraeu-
plotes) o reducidos a 1-3 cirros (Diophrys, Euplotes, Euploti-
dium, Swedmarkis y Uronychia). Cirros caudales derechos pre-
sentes en Diophrys, Discocephalus, Euplotes y Uronychia. Ci-
rros transversales presentes. Cirros frontoventrales en grupos
que son similares morfogenéticamente a los cirros frontoventra
les de los miembros de los Oxytrichidae. Zona adoral de mem-
branelas y membrana ondulante ampliamente modificadas. Once
géneros (Certesia, Gastrocirrus y Paraeuplotes) se colocan
aquf solo provisionalmente.
BORROR incluye una serie de miembros de los Oxytrichi
dae en otras familias, quedando ésta reducida a un grupo muy
homogéneo que comprende catorce géneros, de los cuales Gastro-
tyla, Histriculus, Oxytricha, Stylonychia y Trachelostila,
presentan una gran similitud en e1 modelo morfogenético de
Jos cirros frontoventrales. Los restantes géneros, se colocan
aqui atendiendo a su semejanza en 1a distribuci6én de cirros
durante la interfase, dado que su morfogénesis no se ha estu-
20
diado adn. Entre estos Gitimos se encuentran:
Género Onychodromus.- Comprende una sola especie des-
crita por STEIN (69) en 1859 con el mombre de 0. grandis. Los
Gnicos trabajos realizados sobre la biologfa de esta especie
son los publicados por los MAUPAS(48} en 1889. Posteriormente
TUFFRAU (73) publicé un trabajo en el que compara la ultraes-
tructura de los cinetosomas en varias especies de ciliados
hipotricos entre las que se encuentra 0.grandis.
Género Laurentia.- Descrito por DRAGUESCO (24) en
1966, con una sola especie, L.macrostoma. Se le considera pré
ximo a Keronopsis y Holosticha. De forma ovoide, con una re-
gién apical ensanchada y una regi6n posterior bastante puntia
guda. La longitud media es de doscientas micras, en animales
fijados. Gran peristoma triangular en forma de embudo, muy
abierto por 1a parte alta y bordeado por potentes membrane -
las, en ndmero de 50 a 60. En e? lado derecho del peristoma
hay una gran membrana ondulante.
La ciliacién es bastante compleja y primitiva; cons-
ta de: dos hileras de cirros marginates; cirros frontoventra-
les de distribucién bastante andrquica y que presentan una
cierta variabilidad; cirros ventrales distribuidos a grandes
rasgos en tres hileras; 6-10 potentes cirros transversales;
9-12 cirros ventrales de disposicién anarquicas a veces, 4-5
cirros caudales bastante largos; 6-7 cirros de forma varia -
ble colocados entre los cirros transversales y caudales.
21
El aparato nuclear est& constitujdo por 3-6 gruesos
macrondcleos de contorno irregular, acompafiados por otros
tantos micronicleos esféricos.
En 1971 DRAGUESCO (25) ha descrito una nueva especie
de éste género L.monilata que no es recogida por BORROR en
su sistema de clasificacién (15) y cuyo cardcter mas signifi
cattyo es el de poseer un macronicleo moniliforme constitui-
do por 9-16 nédulos conectados entre sf por gryesos puentes
carioplasmicos.
Salvo esta descripcién parcial hecha por DRAGUESCO,
no se conoce nada acerca de 1a biologfa del género Laurentia;
por ello, nos ha parecido interesante dedicar cierta aten -
ctén al estudio de una especie aislada y cultivada por noso
tros y que, como veremos mis adelante, responde a las carac
teristicas de éste género.
Son muchos los trabajos que se han realizado en cilia
dos hipotricos, pero la mayorfa de ellos recaen sobre espe-
cies pertenecientes a los géneros Oxytricha, Euplotes y Sty-
Jonychia. Estas especies por su gran difusién en las aguas
y en el suelo y por la relattva facilidad con que se culti-
yan han servtdo para investigaciones muy diversas, algunas
de ellas ciertamente interesantes.
Con varias especies de cada uno de estos géneros se
ha estudiado la citologfa tanto a nivel microscépico como
22
ultramicroscépico, asi como diversos aspectos de su ciclo
biolégico: divisién, conjugacién, autogamia, enquistamjento,
exquistamiento, etc. En muchas de elas se han completado
recientemente los estudios de 1a divisi6n celular con los
de morfogénesis de los orgénutos citidares y los de 1a conju
gacién con los de desarrollo del esbezo macronuclear.
Por citar algunos ejemplos de investigaciones reali-
zadas con dichos géneros mencionalremos, en el caso de Oxy~
tricha, las descripciones de la divisién (66, 60), conjuga-
cién (60,29,42) y 1a demostracién de cromosomas politénicos
@s).
Euplotes ha sido bastante mas estudiado. Se han publi
cado algunos estudios sistematicos (74,14) asi como trabajos
citolégicos entre los que cabe destacar los ya clasicos de
TURNER (75) sobre los sistemas fibrilares y los recientes de
TUFFRAU (73) sobre la ultraestructura de la infraciliacién
de los orgdnulos ciliares. Asimismo, son notables las inyes-
tigaciones de KATASHIMA (43) sobre razas matadoras y los de
HECKMAN (35) en torno a la herencia de los tipos de aparea -
miento. En cuanto a la divisién del macrondcleo, son de des-
tacar los trabajos autorradiogréficos de GALL (27) encamina-
dos a eluctdar el significado de las bandas de reorganizacion.
Y con respecto al desarrollo del esbozo macronuclear, ademas
de los trabajos de ALONSO y PEREZ-SILVA (5) en Tos que demues
23
tra la existencia de cromosomas politénicos, destaca el de
RAO y AMMERMANN (61), en el que se hacen estudios sobre la
incorporacién de uridina y timidina tritiada en el esbozo
macronuclear y en los cromosomas politénicos.
Posiblemente el género més estudiado es Stylonychia,
concretamente la especie S.mytilus. Merecen destacarse los
trabajos sobre la estructura microscGpica realizados por
MAUPAS (48) por la precisién de sus observaciones, asf como
otros sobre la ultraestructura realizados por TUFFRAU (73)
y por ROTH (64) y GIL; ALONSO,P.; y PEREZ-SILVA,d (28).
La divisién celular ha sido estudiada en Stylonychia
pustulata (70), S.muscorum (1), y m&s recientemente se ha
jnvesttgado 1a morfogénesis de los nueyos cirros (31,65,71).
Son varios los estudios publicados sobre 1a conjuga
cién de S.mytilus (54,8,49). También se han descrito este
proceso en S.pustulata (48,55,54,59) y en S.muscorum (3).
Dado que una parte del trabajo que sometemos a la
consideracién del Tribunal verse sobre el desarrollo del es
bozo macronuclear de Stylonychia, creemos conveniente deta-
Jlar algo més los estudios que hemos encontrado en la biblio
graffa referentes a este interesante problema.
AMMERMANN (7), del Zoologisches Institut de Tubinga
(Alemania), en su Tesis Doctoral (8) hizo una descripcién de
24
Ja conjugacién en Stylonychia mytilus, y al estudiar el de
sarrollo del esbozo macronuclear describi6 la existencia
de cromosomas politénicos comparables a los que ya habien
sido descritos en las células de las gldndulas salivares de
las larvas de dipteros. Indic6 que estos cromosomas se encon
traban unidos por sus extremos formando un largo filamento
a modo de espirema, al que denominé cromosoma colectivo.
Al mismo tiempo que AMMERMANN, e independientemente,
ALONSO y PEREZ-SILVA (2), del Instituto “Jaime Ferran" de
Madrid, estudiando la conjugacién y el desarrollo del esbozo
macronuclear de Stylonychia muscorum encontraron también
cromosomas politénicos, que segdn demostraron més tarde, es-
tos mismos autores (5), se encuentran separados, al menos
muchos de ellos, Asimismo PEREZ-SILVA y su grupo (5) encon~
traron estos cromosomas en otros varios géneros y especies
de hipotricos, demostrando el apareamiento somatico en Stei-
nia candens (6).
Aparte de 1a importancia que tiene 1a existencia de
cromosomas politénicos en unos seres tan alejados de los dfp
teros, dos hechos principales, descritos en St.mytilus, pro-
moyieron el estudio de estas estructuras en varios laborato-
rios.del mundo, y estas investigaciones se han ido intensi-
ficando cada vez mis, realizdndose trabajos a nivel molecu-
lar relacionados con las transformaciones que experimenta el
ADN durante el desarrollo del esbozo macronuclear.
25
Los dos hechos a que nos referimos son:
1.- La desaparicién de gran parte del ADN en una determi-
nada fase del desarrollo del esbozo macronuclear.
AMMERMANN (10) midi6 fotométricamente las variaciones
en el contenido de ADN en el esbozo macronuclear, des
de el comienzo del desarrollo del sincarién hasta la
formacién del macronicleo definitivo. Este proceso du
ra unoas 80-100 horas. Al principio se observa un in-
cremento en el contenido de ADN hasta que hacia las
40 horas se produce una caida brusca en la cantidad
de este compuesto, quedando el esbozo macronuclear con
un nivel muy bajo, el cual después de 75 horas comien
za a aumentar rapidamente, durante la fase de endopo-
liploidizaci6n, hasta que se alcanza la cantidad corres
pondiente al macrondcleo definitivo del exconjugante.
La descripci6n de puffs en los cromosomas politénicos.
PEREZ-SILVA y sus colaboradores (4) al estudiar el de-
sarrollo del esbozo macronuclear en Stylonychia mytilus,
encontraron que hacia las 26-30 horas después de la
separactén de los exconjugantes, los cromosomas polité
nicos presentan unos ensanchamientos comparables a los
puffs que ya habfan sido descritos en los dipteros.
Aunque en sus experimentos pretiminares, estos autores
no lograron demostrar con claridad la incorporacién de
26
uridina en dichas regiones ensanchadas, la similitud
morfoldgica con los puffs es tam estrecha que impul-.
s6 en este sentido su estudio por otros investigadores.
Recjentemente PRESCOTT (57,58) investigé el fenémeno
descrito por AMMERMANN, de la desaparicién del ADN durante
e1 desarrollo del esbozo macronuclear y 11eg6 a la sorprenden
te conclusién de que ésta pérdida no es s6lo cuantitatiya,
sino también cualitativa, es decir que el macronicleo adulto
hay menor variedad de ADN que en el sincarién, y, por tanto,
que en el microndcleo. Ello plantea una serie de interrogan
tes en torno a la naturaleza y funcién del ADN que se pierde.
En cuanto a la aparicién de zonas ensanchadas en los
cromosomas de Styionychia mytilus, AMMERMANN (9) realiz6 un
estudio autorradiogréfico para demostrar la incorporacién de
uridina en e] esbozo macronuclear, y, al obtener resultados
negativos, 1leg6 a la conclusién de que en estas zonas no
habia sfntesis de ARN y que, por tanto, se trataba no de ver
daderos puffs sino de artefactos producidos durante la prepa
racién del material. No obstante, RAO y AMMERMANN (61) tra-
bajando con Euplotes ‘euristomus lograron demostrar 1a incor-
poracién de uridina en e1 esbozo macronuclear, aunque la ra-
diactividad no se perdfa totalmente en los testigos tratados
con RN-asa. Esta radiactividad aparece de forma homogénea en
27
todo el esbozo, sin que se detecte una mayor sfntesis en
zonas concretas de éste.
Nuestra idea al iniciar este trabajo de Tesis Docto-
ral fue el contribuir a la elucidacién de estos dos proble-
mas, empleando otra especie de hipotrico que presentara mas
ventajas para el estudio. Por ello 1a primera parte de nues
tro trabajo consisti6 en una busqueda sistemdtica de cilia-
dos que presentasen menor ndmero de cromosomas politénicos
en su-esboso macronuclear; este estudio nos servirfa al mis.
mo tiempo para explorar los ciliados del Valle del Guadal-
quivir.
Como ya indicaremos al exponer los resultados, de
todas las especies encontradas, hemos seleccionado dos: Sty-
Jonychia_ mytilus y Laurentia sp. Esta dltima, muy parecida
a L.macrostoma, descrita por DRAGBESCO en 1966, ofrecfa la
posibilidad de realizar un estudio completo de 1a morfolo~
gia y de la biologia, principalmente en lo referente al de-
sarrollo de] esbozo macronuclear. Sin embargo, sélo pudimos
hacer observaciones parciales de Ta conjugacién y de los
cromosomas politénicos, debido a que al poco tiempo de te -
nerla en el laboratorio dejé de conjugarse. Por ello, con
esta especie nos hemos limitado a estudiar la divisién, mor-
fogénesis y exquistamiento.
28
En cuanto a Stylonychia mytilus, nos ha servido para
aclarar algunos puntos acerca del desarrollo del esbozo ma-
cronuclear. Para ello hemos aplicado las técnicas de tincién
con naranja de acridina (62) y corifosfina(44), recientemen-
te puestas a punto por MOLINA (50) en sus trabajos sobre la
heterocromatina de Allium cepa y de Pleurodeles waltlii.
Como hemos dicho anteriormente de una de las muestras
de agua recogidas, hemos aislado una especie de Laurentia,
que resulté ser un material muy apropiado para los estudios
citolégicos puesto que reunia #as siguientes condiciones:
- Se cultiva bien y muy abundante en el laboratorio.
- Los cirros se tifien con facilidad, lo que permite
hacer estudios de morfogénesis.
- Los micronicleos son relativamente grandes pudien
do ser observados con facilidad.
= Son frecuentes los fenémenos de enquistamiento y
conjugacion.
Sin embargo, a los seis meses de tener estas especies
en eT laboratorio, perdié la facultad de conjugarse de ahf
que solo presentemos un estudio parcial de este fenémeno. Pe
ro, dado que el desarrollo del esbozo macronuclear plantea
probtemas de gran importancia, no hemos querido dejar de es-
tudiar este aspecto de 1a tesis y por ello, después de ensa-
29
yar distintas especies, selecctonamos una Stylonychia myti-
lus que ofrece ventajas para ello.
MATERIAL Y METODOS
31
A. MATERIALES. .
Como ya hemos indicado, el material que nos ha ser.
vido para realizar este trabajo ha sido seleccionado entre
los distintos protozoos que hemos encontrado durante el es
tudio de medio centenar de muestras de aguas, recogidas en
las provincias de Sevilla y Huelva. Han sido objeto de es-
te estudio las siguientes especies:
Laurentia sp.- Aislada de la muestra de agua n2 28,
que fue recogida en una charca del Parque de M2 Luisa de
Sevilla durante el curso 1971-1972, y que desde entonces
se viene cultivando en nuestro laboratorio.
Stylonychia mytilus.- Aisladas repetidas veces de
muestras de aguas recogidas en Puebla del Rio (Sevilla),
durante los cursos 1971-1972.
Como alimento para el cultivo de las anteriores es-
pecies hemos utilizado:
Colpidium sp.- Aislados de muestras de agua de di -
versas procedencias y empleado fundamentalmente como alimen.
to de Laurentia sp.
Chilomonas sp.- Aislado de diversas muestras de agua
y que, cultivado junto con Colpidium sp., ha sido utilizado
para alimentar los cultivos de Stylonychia mytilus.
32
Levaduras.- También hemos empteado como alimento
las siguientes especies de levaduras, aisladas de aceitu-
nas en fermentacién y que nos han sido facilitadas por el
Instituto de la Grasa de Sevilla.
Tomlopsis famata Ansenuta anomala
Criptococcus luteolus Saccharomyces lactis
Pichia membranafacians Saccharomyces roussi
Debariomyces hansenii Saccharomyces oleaginosis
Candida krusei Saccharomyces cerevisial
Saccharomyces chevaliere Kloekera apiculata
Saccharomyces veroneae Candida tropicalis
B. METODOS.
1.- Seleccién del material.
Para la seleccién de las especies objeto de nuestro
estudio, hemos recogido en riachuelos, estanques y charcas
de las provincias de Sevilla y Huelva muestras de aguas’ jun
to con pequefias plantas acudticas, hojas muertas, algas, etc.
Estas muestras fueron tomadas en frascos de plasti-
co y' 1llevadas al laboratorio para su estudio. Porciones de
cada muestra se colocaron en tazas de Boveri con los distin
tos medios de cultivo que describiremos a continuacién y fue
33
ron examinadas en dias sucesivos, durante los cuales, a la
vez que haciamos un estudio sistematico de las especies ob
servadas, seleccionabamos aquellas més interesantes para
el estudio citoldgico.
Para la clasificacién de las especies hemos utili-
zado principalmente las claves de KUDO (47), las de KAHL
(41) y las de JAHN y JAHN (38).
2.- Medios de cultivo.
Como medios de cultivo para 1a obtencién de células
abundantes que nos permitiera realizar los estudios previs-
tos hemos empleado los siguientes:
Medio de extracto de suelo.- Este medio se prepara
partiendo de una solucién madre que se obtiene mezclando
100 gr. de tierra (que no esté abonada con sustancias mine-
rales) con 500 ml. de agua destilada; la mezcla se lleva al
autoclave y se tiene alli durante dos horas a 130°C, luego
se mezclan 50 ml. de esta solucién madre con un litro de
agua destilada y desionizada. A esta mezcla se le afiaden 4
ml. de soluci6én de NO,Na al 0,4% y un ml. de soluci6n de
PO,HNa, al 0,08%. Por Gltimo se esteriliza al autoclave du-
rante 30 minutos a 1202C. 7
A este medio de cultivo se afiadié como alimento se-
gin los casos:
34
- Colpidium sp.- Cultivado en medio de extracto de
suelo al que se le afiadfa una pequefia cantidad de harina
integral de trigo.
- Colpidium sp. y Chilomonas sp.- Cultivados conjun-
tamente en medio de extracto de suelo con harina integral
de trigo.
- Diversas especies de levaduras que fueron cultiva
das en agar Nagai.
La composicién del agar Nagai es la siguiente:
Extracto de levadura. see 2 ge.
Peptona bacteriolégica.......eeree ceevee 158 gr.
Sulfato aménico..........5. Lives oceeeces 1a5'9h.
Fosfato monopotasico Pere reas he
et Rete eer eerie 10 gr.
Aga reer eeeeee tire reece eter sees 18 gre
Agua destilada pao 1000 ml.
El pH final se ajusta a 5,5.
Preparacién: Los compuestos se disuelven en autocla
ye durante cinco minutos, una vez disueltos se filtra; se
reparte en tubos 9 matraces y se esteriliza en el autoclave
durante 20 minutos a 1202C cuidando de que no suba la tempe
ratura.
35
Medio de infusién de lechuga.- Este medio, recomen-
dado por WICHTERMAN (78), se prepara de la siguiente forma:
Se lavan unas cuantas hojas de lechuga en agua co-
rriente. Se colocan extendidas sobre un papel de filtro y
se Ilevan al horno para que se desequen lentamente hasta
que adquieran un color amarillento y se hacen quebradizas.
Se trituran en un mortero hasta dejarlas reducidas a polvo.
A continuacién a un litro de agua destilada hirviendo, se
Je afiade un gramo del polvo de lechuga anteriormente prepa-
rado y se deja reposar durante cinco minutos, se filtra,
se esteriliza en matraces de 200 ml. en autoclave a 120°C
durante 30 minutos. Antes de filtrar, es conveniente afladir
carbonato caélcico para neutralizar e¥ medio.
Este medio lo hemos utilizado casi siempre diluido
a la mitad con extracto de suelo.
3.- Observa
Con microscopio estereoscépico.- Las especies selec
cionadas han sido observadas en vivo bajo 1a lupa binocular,
con objeto de ver su modo de locomocién, flexibilidad y as-
pecto externo.
Con eT microscopio.- Las observaciones con el micros
copio, casi siempre en contraste de fases, se han realiza-
do mediante el método de 1a gota pendiente y también entre
36
porta y cubre. Dado que estos organismos presentan un movi-
miento bastante rapido hemos tenido que emplear una técnica
que nos permitiera disminuir la velocidad y que ha consisti
do en afiadir al medio alguna sustancia, en nuestro caso la
metil-celulosa, que lo hagan viscoso, con 1o cual los orga-
nismos se mueven muy lentamente y se pueden observar con fa
cilidad detalles de morfologfa, estructura y disposicién de
los orgénulos externos.
4.- Tincién de orgénulos superficiales.
Para poner de manifiesto estos orgdénulos hemos em -
pleado las dos técnicas siguientes:
Método de PEREZ-SILVA y RAMIREZ-MONTESINOS (53).
Este procedimiento consiste esencialmente en la fi-
Jaci6én de los organismos con tetréxido de osmio, coloracién
los orgdnulos con cristal violeta y mordentado con gliceri-
na yodada.
El fijador es una solucién acuosa de tetréxido de
osmio al 2%, tamponada a un pH de 7,6 segGn PALADE (52).
El cristal violeta se prepara en solucién alcohéli-
ca concentrada, cuya composicién es:
Cristal violeta.......... 1 gr.
Etanol de 962 20 mi.
37
Esta solucién no se altera con el tiempo siempre
que se conserve herméticamente cerrada para evitar la eva-
poracion.
La solucién de trabajo se obtiene afiadiendo una go
ta de la soluci6n anterior, a 5 ml. de agua destilada. Es
conveniente utilizar esta solucién recién preparada.
La glicerina yodada se prepara mezclando dos partes
de glicerina y una de solucién de lugol. Esta altima tiene
la siguiente composicién:
Yoduro potésico..........--- 0,6 gr.
Yodo. .seeeeeee Gebevbcbevecee 0,3 gr.
Agua destilada...........--. 90 ml.
Método.- En un cubreobjetos se colocan una o dos go
tas del cultivo de protozoos y con una pipeta muy fina se
ya retirando liquido hasta dejarlos casi en seco. Después
se afiade una gota del fijador, el cual se deja actuar duran
te varios minutos, y luego se afiaden dos otres gotas de la
solucién de cristal violeta y Bajo la lupa se observa la co
loracién progresiva de los org4nulos superficiales hasta
que han tomado una coloracién violeta intensa, en cuyo momen
to se detiene la coloracién mediante la adicién de una gota
de glicerina yodada.
A continuaci6n se retira parte del liquido, se afiade
38
una gota de glicerina limpia y se monta sobre un portaobje-
tos.
En la técnica original, los protozoos eran tefiidos
en un porta excavado y de alli eran pasados a un porta usual
mediante una pipeta, y se montaba la preparacién; pero noso
tros hemos comprobado que el hecho de tefirlos directamente
sobre el cubreobjetos, evita la deformacién o pérdida del
material, ya que no son necesarias tantas manipulaciones.
Con esta técnica, en las preparaciones bien teflidas,
los organulos superficiales (cirros, membranas, membranelas)
toman una intensa coloracién violeta, que destaca sobre un
fondo ligeramente tefiido de este mismo color. Estas prepara
ciones no son permanentes, pero se comservan varios dias,
si bien se va perdiendo la coloracién de los cirros al tiem
po que se intensifica la de los niécleos.
odo de BORROR (13
Esta técnica se basa en el empleo de una mezcla fija
dora-colorante, que se obtiene incorporando al fijador de
NISSENBAUM (51) una solucién de nigrosina-formol segdn DEROUX
y FARDY (21), y que tifie especfficamenté los cilios y otras
estructuras superficiales de los ciliados.
Para la realizacién de esta técnica se necesitan dos
39
soluciones madre, que son las siguientes:
Soluci6n A.- Consta de 10 ml. de solucién acuosa
saturada de CloHg; 2 ml. de Acido acético glacial; 2 ml.
de formol concentrado; y 10 ml. de t-butanol.
Solucién B.- 20 ml. de soluci6n concentrada de for
mol; 4 gr. de nigrosina soluble en agua; 100 ml. de agua
destilada.
La solucién de trabajo se obtiene mezélando 12 volad
menes de Ja solucfén A con un voldmen de la soluci6n B.
Procedimiento: Se coloca una gota de un cultivo abun
dante de organismos sobre un portaobjetos limpio, y con una
pipeta se deja caer desde una altura de 2-3 cm. una gota de
Ja solucién de trabajo. Después de varios segundos se incli.
na Tigeramente el portaobjetos a fin de que el exceso de li
quido se deslice a la vez que.se afiaden nueyas gotas de la
soluci6n de trabajo. Después de este procedimiento, los or-
ganismos quedan fijados, tefiidos y adheridos al portaobjetos,
y al cabo de 15 segundos, la preparacién se puede deshidra-
tar, clarificar y montar.
En las preparaciones hien tefiidas los orgdnulos ci-
lfarés aparecen en negro, sobre un fondo gris claro.
40
Inclusi6n en resinas y observaci6n de cortes por
microscopfa de contraste de fases.
Esta técnica serd descrita mas adelante ya que es
la misma empleada para las observaciones al microscopio
electrénico, salvo que los cortes, de 2 u de espesor, se
hicieron en el Piramitén y se montaron con aceite de inmer
sién entre porta y cubre.
5.- Tincién de nicleos.
Para el estudio de la morfologfa de los niicleos y
de los procesos carjolégicos que tienen lugar en la divisi6n,
conjugacién y exquistamiento hemos utilizado las siguientes
técnicas:
Tinci6n con orcefna aceto-clorhidrica.- Hemos segui
do la técnica descrita por TJIO y LEVAN (72). El colorante
se preparé como sigue: 2 gr. de orceina sintética GURR, se
disolvieron en 55 ml. de Acido acético glacial calentado
hasta ebullicion y manteniendo ésta durante diez minutos. A
continuacién se deja enfriar y se afiade agua destilada has-
ta completar 100 ml. y se deja reposar durante 24 horas,
después de las cuales, se filtra, y se afiade C1H 1N en pro-
procfén de una parté de acido clorhfdrico por cada nueve
de Ja solucién de orceina acética.
41
En nuestro caso, 1a solucién asi preparada nos re-
sultaba excesivamente concentrada, por lo que 1a soluci6n
de trabajo la obtentamos diluyendo la anterior, al 50%,
con dcido acético glacial al 45%.
Las preparaciones se realizam colocando en un por-
taobjetos una gota de un cultivo abundante de protozoos y,
con una pipeta fina, se va retirando el liquido hasta de-
jarlos casi en seco; a continuacién, se afiade sobre ellos
una gota de la solucién de orceina, se deja actuar por va
rios minutos, se coloca un cubreobjetos y se puede obser-
var al microscopio.
Esta técnica presenta las ventajas de una gran ra-
pidez y de provocar un ligero hinchamiento de los nfécleos,
lo cual hace que éstos sean mis facilmente visibles; pero
presenta el inconveniente de que las preparaciones no son
permanentes y s6lo pueden ser observadas durante algunas
horas.
Tincién con Verde de metilo-pironina-naranja G
Para esta tincidén hemos utilizado la mezcla neutra
de GROSSO (63) que se prepara de la siguiente forma:
A 75 ml. de.agua destilada se van afiadiendo sucesi
vamente, y precisamente por este orden, soluciones acuosa
saturadas en las siguientes cantidades:
42
Verde de Metilo........ veecees 352 Mm.
Pironina wees - 6,0 ml.
NaranjaiG..... seeeee Vecersecee TO. mt.
A las 24 horas se filtra esta solucién, que queda
asi preparada para ser usada, conservandose durante mucho
tiempo sin alterarse.
Procedimiento.- Los protozoos se fijan sobre portaob
jetos previamente gelatinados con metanol-acético en propor
cién 3:1, y antes de que se sequen se le afiade una gota de
alcohol de 962. Se pasa por los alcoholes 962, 702, 40° y
agua, se vierte el colorante encima y se deja actuar duran
te 5-10 minutos. A continuactén, se escurren el colorante,
se lava con alcohol absoluto y, después de pasar las prepa
raciones dos veces por alcohol absoluto y xilol, se montan
con caedax.
En las preparaciones bien tefidas, los ndcleos apare
cen en verde; el citoplasma, de un ligero color rosa, y las
yacuolas digesttvas, st las hay, de color naranja.
Tirict6n dé Feulgen.- Para esta tincién hemos emplea
do los siguientes reactivos:
Ffjador de Sanfelice compuesto de:
Acido crémico al 1%.
FOrMol.....seeeeeee eee
Actdo acético.........
43
Hidrolisis.- Se Tley6 a cabo en C1H IN.
Reactivo de Schiff.- Lo hemos preparado de la forma
siguiente:
lgr. de fucsina se pone en um matraz Enlermeyer con
200 ml. de agua hirviendo y después de unos cinco minutos
se pasa por decantaci6n a otro matraz. Se deja que se enfrie
hasta 50° y se filtra. Se afiaden 20 mi. de C1H 1N se enfria
al chorro de agua hasta 252, y se disuelve en el liquido un
gr. de SO,HNa. Se deja reposar 24 horas a la temperatura am-
biente mientras la soluci6n se decolora. Este reactivo se
ha de conservar en la oscuridad y bien cerrado.
Agua sulfurosa.- Se mezclan 200 ml. de agua corrien
te con 10 ml. de una solucién al 10% de SO3HNa y 10 ml. de
CIH IN. Esta mezcla ha de utilizarse recién preparada.
Procedimiento.- Se coloca una gota de suspensi6n de
protozoos sobre un porta con albdmina, se retira el agua
con una pipeta muy fina y se afiaden unas gotas de solucién
de Sanfelice. Aicontinuacién, se va separando la parte li-
quida hasta dejar los protozoos casi en seco y se lleva el
portaobjetos a una placa de petri grande que tiene en el
fondo un papel de filtro empapado en formol al 40%, y una
varilla que sirve de soporte al porta; se deja estar de 15
a 20 minutos y después, sin quitarlo de alli, se ponen unas
gotas de Sanfelice sobre la preparacién y se deja estar to-
44
da 1a noche.
Al dia siguiente, se escurre el Sanfelice, se lava
con agua durante 15 a 20 minutos y se pasa por la serie de
alcoholes hasta llegar al de 962 donde se deja toda la no-
che.
Se hidrata pasando por la serie de alcoholes de
concentracién decreciente hasta agua y se procede a la hi-
drolisis introduciendo el porta primeramente en C1H 1N
frio, después se tiene durante 8 minutos en C1H 1N a 602,y
por dltimo se pasa nuevamente a C1H frio. Se lava con agua
y se tiene en el reactivo de Schiff durante hora y media.
Pasado este tiempo, se lava tres veces con agua sul
furosa, 2 minutos cada vez, en tres pocillos diferentes;
por Gltimo, se lava con agua, se pasa por la serie de alco_
holes y se monta la preparaci6n.
6.- Tinciones para 1a observacién con fluorescencia.
Para el desarrollo del esbozo partimos de un culti-
vo de exconjugantes del que hicimos sucesivas preparaciones
a dtstintos tiempos después de su separacién.
La fijactén se 1levé a cabo sobre el portaobjetos
con una solucién recientemente preparada y compuesta de
tres partes de metanol absoluto y una parte de dcido acéti
co glacial.
45
Los colorantes empleados fueron los siguientes:
Tincién con Naranja de Acridina.- La solucién de
trabajo se obtuvo preparando diluciones 1/10.000 y 1/50.000
en tampén fosfato de Sorensen con un pH de 6,8; 7,0 a par-
tir de una solucién stock de Naranja de Acridina (Merck)
0,1% en agua destilada conservada en nevera a 4°C.
El tiempo de tincién fué de 10 minutos y posterior
mente fueron lavadas las preparaciones para lavar el exce-
so de colorante en dos bafios de 2-5 minutos de tampén fos-
fato de Sorensen, pasando posteriormente a montar las pre-
paraciones en el mismo tampén.
Tincién con Corifosfina.- La solucién de trabajo
fué preparada a partir de una solucién stock de Corifosfina
(G.T.GURR. Londres) a1 0,5% en tampGm acetato pH = 4,4 por
diluci6n hasta 1/20.000 y 1/25.000 con solucién fosfato-fe
nol-salino, pasando posteriormente a 1a solucién de colo-
rante durante diez minutos tras los cuales eran montadas en
el tampén antes mencionado y observada en el microscopio
de fluorescencia.
Para la observacién en fluorescencia fué usado el
dispositiyo de fluorescencia del fotomicroscopio Zeiss con
filtros de excitactén BG38 y BG12 y filtros analizadores
53/44 estando preyisto el dispositive de fluorescencia con
46
lémpara Osram HBO-200 de alta presién.
7.- Técnicas para la microscopia electrénica.-
Fijacién.- Para la fijacién se empleé una soluci6n
de tetréxido de osmio al 2% en un tampén de acetato de ve-
ronal a pH 7,4. E1 tiempo de fijaci6n fué de 20 minutos.
Inclusién.- E1] material previamente fijado, se in-
cluyé en agar, cortandose a continuaci6n en pequefios bloques,
a fin de facilitar su manipulacion.
La deshidratacién de estos pequefios bloques se Ilevé
a cabo en una serie de alcoholes desde 50% hasta 100%, a
continuacién se lavaron en 6xido de propileno y se incluye-
ron en Epon 812.
Estas inclusiones fueron talladas con e] Piramiton
donde se hicieron a su vez cortes gruesos (2 micras de espe
sor) para su examen con mtcroscopfa de contraste de fases,
y a continuacién se hicieron los cortes ultrafinos para el
microscopio electrénico en un Ultramicrotomo LKB. Parte de
los bloques se enyiaron al Departamento de Protozoologfa
del Instituto "Jaime Ferrén" del C.S.1.C., donde la Dra.
Gil Alvarez, hizo los cortes y las micrografias electréni-
cas en el Servicio de Microscopio Electrénico del Centro de
Inyestigaciones Biolégicas.
RESULTADOS
48
A.- ESTUDIO SISTEMATICO DE LOS CILIADOS DEL VALLE DEL GUA-
DALQUIVIR.
Esta parte de ia Tesis tiene por objeto el buscar
especies apropiadas para el estudio tznto morfolégico como
de los procesos de reorganizacién del macrondcleo. Al mis-
mo tiempo nos sirve para ampliar los datos sobre los proto
zoos de la Peninsula Ihérica, ya que el Valle del Guadalqui
vir, que nosotros sepamos, no ha sido estudiado nunca en
este sentido; sin embargo cémo el objeto principal de esta
exploracién en la seleccién de material no nos hemos dete~
nido especialmente en la identificacién de las especies,
si bien, hemos procurado reflejar todos los datos posibles
en cuanto a la localizacién de las muestras y en algunos
casos otros datos referentes a las muestras de agua.
Para mayor comodidad los resultados se exponen a
continuacién en un cuadro donde se indica procedencia de
la muestra y los protozoos encontrados.
Con un asterisco se sefialan Tos seleccionados para
su estudio.
49
CUADRO I.- Ciliados observados en las distintas muestras de
MUESTRA
aguas y musgos recogidas en las provincias de Se
villa y Huelva.
Frotonia sp.
Sonderia sp.
Euplotes sp.
Paramecium sp.
Euplotes sp.
Frontonia sp.
Euplotes sp.
Spirostomum sp.
ronucleatum
Frontonia sp.
Urosoma sp.
Loxodes magnus
striatus
PROCEDENCIA CILIADOS OBSERVADOS
Canal de Pue- Stentor coeruleus
bla del Rio. Loxodes magnus
1 " striatus
" rostrum
Spirostomum sp.
Canales del Urocentrum turbo
borde de la ca Coleps elongatus
Zi rretera de Pue Stylonychia sp.
bla del Rio.
Venta de la Urocentrum turbo
3 Cruz a 12 Km. Loxédes rostrum
de Puebla del Paramecium multimic
Rio.
Charca en ca- Stentor coeruleus
rretera de Spirostomum
4 Puebla del ‘cyclidium sp.
Rio. Chilodonella cucullulus
Rio Viar en Paramecium bursaria
Cantillana. Urocentrum turbo
5 Stylonychia mytilus
Paramecium caudatum
Frontonia Teucas
* Aspidisca sp.
Euplotes sp.
50
MUESTRA PROCEDENCIA CILIADOS OBSERVADOS
Cantillana Keronopsis sp. Loxodes magnus
6. Rio Viar Stentor roeseli Trachelius sp.
Charca de jun- Didinium nasutum Coleps elongatus
*
7 cos en carretera Stylonychia mytilus
de Cantillana. Dileptus anser
Rio Viar, zona Trachelius ovum Stentor roeseli
8 derecha. Canti Frontonia acuminata Vorticela sp.
Vana Paramecium bursaria Spirostomum sp.
Stentor coeruleus
Rio Viar. Can Frontonia sp. Dileptus anser
9 tillana. Trachelius ovum Stentor roeseli
Rio Viar. Can. Chidodonella cucullulus
10
tillana.
Charca de la Metopus sp. Caenomorpha me-
il Rinconada, dusula
Paramecium sp.
Musgo de la Colpoda sp.”
12 azotea de la
Facultad.
51
MUESTRAS PROCEDENCIA CILTADOS OBSERVADOS
Carretera Ama Didinium nasutum Spirostomum sp.
rilla. Charca Paramecium sp. Frontonia sp.
13 a la salida Vorticella sp. Oxytricha sp.
de Sevilla.
Charca en ca Stylonichia Coleps sp.
14 rretera de Se Paramecium sp. Loxodes sp.
villa a Brenes Stentor coeruleus Metopus sp.
Vorticella sp.
Carretera de Stylonychia sp. Euplotes sp.
15 Ja Rinconada —-Urocentrum turbo — ,
Arroyo Mira- Paramecium sp. Oxytricha sp.
16 flores. Carre Vorticella sp.
tera de Brenes
Arroyo las cu. Urocentrum turbo Frontonia sp.
7 lebras. Carre- Stylonychia sp. Euplotes sp.
tera de Canti-
Tlana.
Musgo de un ca- Stylonychia sp. Paramecium sp.
18 nal en la carre Oxytrichia sp.
tera de Brenes.
Sierra de Ca- G0nestomum sp. Colpidium sp:
19 Chilodonela cucultulus
bra.
52
MUESTRA PROCEDENCIA CILIADOS OBSERVADOS
Salinas de Frontonia sp. Dyophrys sp.
207 S. Fernando
(Cadiz).
Estanque de Stylonychia sp Trachelius ovum
las magnolias.
a1 Parque de M2
Luisa. (Sevilla)
*
Canal de Villa Stylonychia mytilus
22 franco del Gua
dalquivir.
Charca carre- Stentor coeruleus Paramecium sp.
23 tera de Alcalé Didinium nasutum
de Guadaira.
Canal de la Stentor roeseli Frontonia sp.
24 carretera de Urocentrum turbo
Utrera. Chilodonella cucullulus
Carretera de | Paramecium sp.
25 Alcala de Gua .
daira.
Carretera de Coleps hirtus
26 Alcala de Gua Oxytricha sp.
daira.
MUESTRA
27
28
29
30
31
32
33
PROCEDENCIA
Charca de las
Palmeras. Carre
tera de Puebla.
Charca del Par
que de M2 Lui-
sa (Sevilla).
Torreblanca
(carretera de
Alcala de Guadai
ra).
Torfeblaica
(carretera de
Alcala de Gua-
daira).
Charca de To
rreblanca.
Torreblanca
Torreblanca
53
CILIADOS OBSERYVADOS
Lacrimaria sp.
Stentor roeseli
Vorticella sp.
Dileptus anser
Laurentia-sp.
Oxytricha sp.
Frontonia sp.
Euplotes sp.
Halteria
Euplotes sp.
Frontonia sp.
Urocentrum turbo
Paramecium sp.
Urocentrum turbo
Paramecium sp.
Loxodes sp.
Frontonia sp.
Spirostomum sp.
Frontonia sp.
Paramecium sp.
Frontonia sp.
MUESTRA
34
35
36
37
38
39
PROCEDENCLA
Canal de To-
rreblanca.
Parque de M9
Luisa (Sevilla).
Estanque de
los Lotos
(Parque de M2
Luisa).
Charca en ja
carretera Canti
llana-Villaverde.
Coto de Dofiana
(lucio del Pa-
lacio).
Coto de Dofiana
(charca detras
del Palacio).
54
CILIADOS OBTENIDOS
Euplotes sp. Frontonia sp.
Stylonychia mytilus
Halteria sp. Stentor coeruleus
Stylonychia sp.
Coleps elongatus
Stylonychia sp.
Euplotes sp.
Didinium nasutum
Euplotes sp.
Holosticha sp.
Halteria sp.
Frontonia sp.
Uroleptus sp.
Prorodon discolor
Halteria sp.
MUESTRA
40
41
42
43
44
PROCEDENCIA
Pozo artesiano.
Coto de Dofiana.
Charca del Co
to de Cofiana.
Charca del Co-
to Dofiana.
Charca del Co-
to de Dofiana.
Charca del Co-
to Dofiana.
55
CILIADOS OBTENIDOS
Loxodes sp. Spirostomum sp.
Sonderia sp. Halteria sp.
Euplotes sp. Stylonychia sp.
Frontonia leucas
Urocentrum turbo
Urosoma caudata
Frontonia sp. Paramecium sp.
Metopus sp. Lacrymaria sp.
Oxytricha sp.
Dileptus anser
Stylonychia mytilus
Lacrymaria sp.
Euplotes sp.
Frontonia leucas
Halteria sp.
Euplotes sp.
Paramecium bursaria
Frontonia sp.
Lacrymaria sp.
Frontonia leucas
56
MUESTRA PROCEDENCIA CILIADOS OBSERVADOS
Carretera del Frontonia sp. Halteria sp.
45 Coto de Dofiana Stentor igneus Stentor sp.
(Huelva). Climacostomum virens
Urostyla sp. Oxytricha sp.
Stylonychia sp.
Carretera del Halteria sp. Oxytricha sp.
46 Rocio. (Huelva). Paramecium sp. Urosoma caudata
Lacrymaria sp.
Stylonychia mytilus
Charca en la Colpidium sp.
47 carretera de Holosticha sp.
Constantina.
Charca préxima Stylonycha sp.
48 a Cazalla. Oxytricha sp.
Halteria sp.
Chilodonella sp.
B.- ESTUDIOS REALIZADOS CON LAURENTIA SP.
Como se dijo en 1a introduccién se conocen dos espe
cites de Laurentia descritas por DRAGUESCO (24) (25) creador
del género y que, como veremos, son a primera vista muy pare
cidas a Onychodromus, sobre todo Laurentia macrostoma, que
57
suele tener el macronGcleo dividido en cuatro fragmentos tal
como describié MAUPAS (48) para Onychodromus sin embargo, la
dotacién y distribucién de los cirros es muy diferente y,
por tanto, estos dos géneros son féciles de distinguir tan
pronto como se hace una tincién de cirros, si bien el término
de comparacién empleado ha sido siempre la descripcién e ilus
traciones de MAUPAS, puesto que hasta el momento no conocemos
otras descripciones. Por ello, nos parecié interesante hacer
una descripcién detallada de la especie de Laurentia, que he-
mos aislado, para luego hacer un estudio de las condiciones
de cultivo, morfologfa, division, y exquistamiento asi como
algunas observaciones sobre 1a conjugaci6n.
1.- Cond
ones de cultivo.- Los Gnicos estudios publi.
cados sobre Lavrentia son los de DRAGUESCO, los cuales son
bastante incompletos ya que solo se hace una descripci6n par-
cial sobre individuos que probablemente se encontraban en las
muestras originales, sin haber sido previamente aislados y
cultivados; por ello, creimos necesario establecer las condi-
ciones de cultivo en que estos ciliados se desarrollan mejor,
sin lo cual serfa imposible estudiar los procesos de division
y¥ Morfogénesis.
Dada su afinidad con Stylonychia, probamos primeramen
te los medios que segdn nuestra propia experiencia son mas
apropiados para esta Gltima; asf ensayamos el medio de extrac
58
to de suelo afiadjendo como alimento distintos protozoos o le
vaduras. Cada uno de estos microorganismos se ensayaron como
elemento en experimentos por duplicado para comprobar cual
de ellos soportaba mejor el desarro-lo de Launentia. Se vid
que en todas las levaduras probadas se desarrollaba pero len
tamente. La adicién de una mezcla de Colpidium y Chilomonas,
que, como veremos més adelante, es el alimento éptimo para
Stylonychia, puede servir para el crecimiento de Laurentia,
pero estos protozoos se alimentan principalmente de Colpidium,
acumulandose los Chilomonas en el cultivo; por ello, el me-
jor alimento result6é ser Colpidium sp, sobre el cual depredan
activamente los Laurentia dividiendose con gran rapidez. To-
dos los dem&s alimentos resultaron menos apropiados que Colpi
dium.
Cuando en lugar de medio de tierra se ponfa medio de
infusién de lechuga se observaba tos primeros dias un creci-
miento satisfactorio, que luego se hacfa m&s lento a medida
que se enturbiaba el medio de lechuga debido al crecimiento
de bacterias.
Después de una serie de tanteos elegimos como medio
éptimo para el cultivo de Laurentia, el siguiente: medio de
extracto de suelo al que se afiade un cultivo de Colpidium sp.
cultivado a su vez en medio de extracto de suelo al que se
afiade harina de trigo integral. Es conyeniente que el Colpi-
59
dium proceda de un cultivo de 5 dias como minimo. Dado que
Laurentia es un depredador muy activo es conveniente que en
lugar de afiadir todos los alimentos una vez diaria afiadirlo
dos veces al dia.
En cuanto a la temperatura de cultivo, hemos ensa -
llado dejarlo a 1a temperatura del laboratorio o en una ca-
mara climatizada a 202 C11 y no se han observado diferencias
apreciables en el rendimiento de los cultivos.
2.- Descripcién.- Los ejemplares tefiidos por los mé-
todos de PEREZ-SILVA y RAMIREZ-MONTESINOS (53) y de BORROR
(13) experimenta relativamente pocas deformaciones, y por
tanto la descripcién hecha sobre estas prepardciones coinci
de prdacticamente con las observaciones que hemos hecho sobre
individuos vivos por microscopfa de contraste de fases.
Son de tamafio relativamente grande, de 250 a 320 u
de longitud por 100 a 150 u de anchura méxima. E1 cuerpo es
de contorno ovalado, més ancho por la parte anterior y estre
chado por la parte posterior, que suele terminar en punta
(fig.1). Es muy aplanado dorsoventralmente con muchos entran
tes y salientes destacando una profunda depresién en la mitad
anterior de 1a parte ventral (Fig.2).
La_dotacién de cirros es bastante compleja y respon-
de a la descripcién parcial que ha hecho DRAGUESCO (24) para
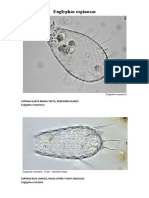
Fig. 1.- Laurentia ‘sp.Micrograffa de un individuo visto
por el lado ventral en la que se puede apreciar ‘
el aspecto general y Ja dotacién de orgdnulos
superficiales. Técnica de BORROR.
Laurentia sp. Micrograffa de un corte sagital de
un individuo observado por microscopfa de con -
traste de fases. Puede aprecierse que el cuerpo
es aplanado dorsoventralmente,
Esquema de la morfologfa general y de la dotacién
de cirros de Laurentia sp, Dibujado sobre proyec-
ctones de diapositivas hechas a partir de prepara.
ciones tefitdas por el método de PEREZ-SILVA y R.
MONTESINOS y de BORROR.
Fig.
Fig. 4.- Laurentia sp. Micrograffa de un corte longitudt-
nal observado por mtcroscopfa de contraste de fa
ses. Se puede apreciar parte de la zona adoral
de membranelas, 1a membrana ondulante que delimit
tan el amplio peristoma.
Fig. 5 y 6.- Laurentia sp. Micrografias de dos cortes ho-
rizontales pertenectentes a una misma serie en
las que puede apreciarse que la zona de membrane
las penetra en el interior de la célula y dos
fragmentos de macrondcleos, en uno de ellos se dis.
tinguen unos corpdsculos més oscuros que se corres
ponden con los nucleolos.
60
Laurentia macrostoma, basada en las observaciones sobre unos
pocos individuos. Nosotros, después de haber observado cerca
de 600 individuos creemos que podemos dar una descripci6n
bastante completa de la distribucién de los cirros y membra-
nelas.
El peristoma es muy amplio (Fig.3, 4) de forma trian
gular y en su parte anterior pasa al lado dorsal. Por su
parte posterior termina en punta hacia 1a mitad del cuerpo.
Esté bordeado por unas 60 membranelas muy desarrolladas so-
bre todo las que se insertan en el borde anterior del cuer-
po del individuo, haciendose cada vez mas pequefias a medida
que se acercan al vértice del peristoma, el cual penetra ha-
cia el interior de la célula (Figrs. 5 y 6). En las microgra
fias electrénicas se observa que cada membranela esta forma-
da por tres filas completas de cilios (Figrs. 7 y 8) a las
que se afiade una cuarta fila incompleta, formada por dos o
tres ctlios.
En el borde derecho del peristoma se observa clara-
mente una membrana ondulante (Fig. 9) en las preparaciones
tefiidas con cristal violeta o con nigrosina, y en los cortes
favorables observados por microscopia de contraste de fases
puede apreciarse que ocupa aproximadamente las tres cuartas
partes del borde derecho del peristoma. Los cilios que la
integran son relativamente largos. De las micrograftas elec
trénicas puede deducirse que hay dos membranas o bien que
Figrs. 7 y 8.- Lauzentia sp. Micrograffas electrénicas en
las que puede apreciarse que las membranelas es-
tan formadas por tres filas de cilios. En una de
las membranelas se observa una 42 fila formada
por tres cilios, (Fig.7).x 8.094 y x10.000.
- Laurentia sp. Micrograffa de un individuo visto
por la cara ventral en el que puede apreciarse
claramente la membrana ondulante en el borde dere
cho del pertstoma. Por delante de esta membrana
se distingue el cirro bucal y a la derecha de ella
Tas hileras de cirros frontoventrales. Tinctén de
BORROR.
61
dicha membrana es doble, aunque Jas dos hileras muy cerra-
das de cilios que se cbservan, estén bastantes separadas
entre. sf (Fig. 10).
Bordeando la cara ventral del animal hay una hilera
de cirros marginales a cada lado (Figrs. 1 y 3). Los cirros
marginales derechos se extienden desde la parte anterior
del cuerpo hasta el vértice posterior y su némero oscila en
tre 40 y 45. La hilera marginal izquierda estd formada por
25 a 30 cirros aproximadamente del mismo tamafio que los mar
ginales derechos. Esta hilera comienza en las proximidades
del vértice peristomético y, por tanto, muy cerca de la li-
nea media del individuo, y desde alli se dirige hacia el
margen, siguiendo hasta el extremo posterior del cuerpo, don
de se continda con la hilera derecha.
Los cirros frontoventrales (Figrs. 1, 3 y 9_ se dis
ponen formando las seis hileras admitidas por BORROR (15)
y que se designan con los ndmeros romanos del I al VI.
La hilera I no contiene més que el cirro bucal (Fig.9),
que es quizdés el més desarrollado de todos y esta situado
inmediatamente delante del extremo anterior de 1a membrana
ondulante:
La hilera II est& formada por cinco cirros que se
alinean a la derecha de la membrana ondulante y siguiendo .-
Fig. 10.- Laurentia sp. Micrograffa electrénica de un cor
te horizontal de un individuo, que afecta el mar
gen derecho del peristoma. Pueden apreciarse dos
hileras cerradas de cilios que forman parte de la
membrana ondulante. x3.192,
62
una direccién paralela a ésta, estos cirros estan ligeramen
te menos desarrollados que el cirro bucal, pero, son més
robustos que los de Jas restantes hileras.
La hilera III se extiende desde 1a parte anterior
hasta el extremo posterior del peristoma y esté formada por
siete cirros dispuestos regularmente y de tamafio bastante
menor que los de la hilera Il.
La hilera ndmero IV rebasa el vértice peristomatico,
Tegando casi hasta 1a parte anterior de los cirros trans-
versales, y esté formada por siete u ocho cirros sensiblemen
te iguales a los de la hilera III.
La hilera V comienza algo més retrasada que la IV y
se extiende hasta las proximidades de los cirros transversa
Jes; esta formada por ocho o nueve cirros.
La hilera VI paralela a la anterior consta de ocho
o nueve cirros y termina muy préxima a los cirros transversa
les.
A la derecha de esta dltima hilera y en su parte
posterior existen de dos a cuatro cirros alineados que puede
considerarse como una VII hilera muy reducida.
Los cirros transversales son bastante m&és largos que
Jos anteriores y algo mas robustos. Suelen ser seis, o siete
de los cuales cuatro forman hileras y los otros dos estan si
You might also like
- The Subtle Art of Not Giving a F*ck: A Counterintuitive Approach to Living a Good LifeFrom EverandThe Subtle Art of Not Giving a F*ck: A Counterintuitive Approach to Living a Good LifeRating: 4 out of 5 stars4/5 (5819)
- The Gifts of Imperfection: Let Go of Who You Think You're Supposed to Be and Embrace Who You AreFrom EverandThe Gifts of Imperfection: Let Go of Who You Think You're Supposed to Be and Embrace Who You AreRating: 4 out of 5 stars4/5 (1093)
- Never Split the Difference: Negotiating As If Your Life Depended On ItFrom EverandNever Split the Difference: Negotiating As If Your Life Depended On ItRating: 4.5 out of 5 stars4.5/5 (845)
- Grit: The Power of Passion and PerseveranceFrom EverandGrit: The Power of Passion and PerseveranceRating: 4 out of 5 stars4/5 (590)
- Hidden Figures: The American Dream and the Untold Story of the Black Women Mathematicians Who Helped Win the Space RaceFrom EverandHidden Figures: The American Dream and the Untold Story of the Black Women Mathematicians Who Helped Win the Space RaceRating: 4 out of 5 stars4/5 (897)
- Shoe Dog: A Memoir by the Creator of NikeFrom EverandShoe Dog: A Memoir by the Creator of NikeRating: 4.5 out of 5 stars4.5/5 (540)
- The Hard Thing About Hard Things: Building a Business When There Are No Easy AnswersFrom EverandThe Hard Thing About Hard Things: Building a Business When There Are No Easy AnswersRating: 4.5 out of 5 stars4.5/5 (348)
- Elon Musk: Tesla, SpaceX, and the Quest for a Fantastic FutureFrom EverandElon Musk: Tesla, SpaceX, and the Quest for a Fantastic FutureRating: 4.5 out of 5 stars4.5/5 (474)
- Her Body and Other Parties: StoriesFrom EverandHer Body and Other Parties: StoriesRating: 4 out of 5 stars4/5 (822)
- The Emperor of All Maladies: A Biography of CancerFrom EverandThe Emperor of All Maladies: A Biography of CancerRating: 4.5 out of 5 stars4.5/5 (271)
- The Sympathizer: A Novel (Pulitzer Prize for Fiction)From EverandThe Sympathizer: A Novel (Pulitzer Prize for Fiction)Rating: 4.5 out of 5 stars4.5/5 (122)
- The Little Book of Hygge: Danish Secrets to Happy LivingFrom EverandThe Little Book of Hygge: Danish Secrets to Happy LivingRating: 3.5 out of 5 stars3.5/5 (401)
- The World Is Flat 3.0: A Brief History of the Twenty-first CenturyFrom EverandThe World Is Flat 3.0: A Brief History of the Twenty-first CenturyRating: 3.5 out of 5 stars3.5/5 (2259)
- The Yellow House: A Memoir (2019 National Book Award Winner)From EverandThe Yellow House: A Memoir (2019 National Book Award Winner)Rating: 4 out of 5 stars4/5 (98)
- Devil in the Grove: Thurgood Marshall, the Groveland Boys, and the Dawn of a New AmericaFrom EverandDevil in the Grove: Thurgood Marshall, the Groveland Boys, and the Dawn of a New AmericaRating: 4.5 out of 5 stars4.5/5 (266)
- Team of Rivals: The Political Genius of Abraham LincolnFrom EverandTeam of Rivals: The Political Genius of Abraham LincolnRating: 4.5 out of 5 stars4.5/5 (234)
- A Heartbreaking Work Of Staggering Genius: A Memoir Based on a True StoryFrom EverandA Heartbreaking Work Of Staggering Genius: A Memoir Based on a True StoryRating: 3.5 out of 5 stars3.5/5 (231)
- On Fire: The (Burning) Case for a Green New DealFrom EverandOn Fire: The (Burning) Case for a Green New DealRating: 4 out of 5 stars4/5 (74)
- The Unwinding: An Inner History of the New AmericaFrom EverandThe Unwinding: An Inner History of the New AmericaRating: 4 out of 5 stars4/5 (45)
- Itinerario Geoturístico Cuenca Guadíx-BazaDocument32 pagesItinerario Geoturístico Cuenca Guadíx-BazaAnonymous hQLzdXVoNo ratings yet
- Diversidad Local y Global de Los Protozoos Ciliados de Agua Dulce (Tesis) ILUSTRACIONESDocument23 pagesDiversidad Local y Global de Los Protozoos Ciliados de Agua Dulce (Tesis) ILUSTRACIONESAnonymous hQLzdXVoNo ratings yet
- Diversity and Geographic Distribution of CiliatesDocument19 pagesDiversity and Geographic Distribution of CiliatesAnonymous hQLzdXVoNo ratings yet
- Cristigera PleuronemoidesDocument6 pagesCristigera PleuronemoidesAnonymous hQLzdXVoNo ratings yet
- Key For Centropyxis and Similar TaxaDocument3 pagesKey For Centropyxis and Similar TaxaAnonymous hQLzdXVoNo ratings yet
- Freshwater Testate Amoebae - Mazei-Tsyganov, 2006 (In Russian) PDFDocument304 pagesFreshwater Testate Amoebae - Mazei-Tsyganov, 2006 (In Russian) PDFAnonymous hQLzdXVoNo ratings yet
- Guide To Testate Amoebae PDFDocument132 pagesGuide To Testate Amoebae PDFAnonymous hQLzdXVoNo ratings yet
- Galerías Subterráneas de OsunaDocument4 pagesGalerías Subterráneas de OsunaAnonymous hQLzdXVoNo ratings yet
- Euglyphas Espinosas PDFDocument4 pagesEuglyphas Espinosas PDFAnonymous hQLzdXVoNo ratings yet
- Geological Formations of IndiaDocument17 pagesGeological Formations of IndiaAnonymous hQLzdXVoNo ratings yet
- Guía de Georrecursos de Andalucía - Cabo de Gata-Bahía de AlmeríaDocument26 pagesGuía de Georrecursos de Andalucía - Cabo de Gata-Bahía de AlmeríaAnonymous hQLzdXVoNo ratings yet
- Oasis of Art in The Sahara - National Geographic - Agosto de 1987Document12 pagesOasis of Art in The Sahara - National Geographic - Agosto de 1987Anonymous hQLzdXVoNo ratings yet