Professional Documents
Culture Documents
Fuerzas Intermoleculares
Uploaded by
Lyseth Gómez0 ratings0% found this document useful (0 votes)
6 views10 pagesOriginal Title
Fuerzas intermoleculares
Copyright
© © All Rights Reserved
Available Formats
PDF or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as PDF or read online from Scribd
0 ratings0% found this document useful (0 votes)
6 views10 pagesFuerzas Intermoleculares
Uploaded by
Lyseth GómezCopyright:
© All Rights Reserved
Available Formats
Download as PDF or read online from Scribd
You are on page 1of 10
Componente ental
CComponsnte D (apidal
2255 a lurlineaimente polarizad penetrsndo en
una musta (desde la aque] se puede wsulzar
ammo superposcén de dos componentes
poarzada irclormentelerpesentads por ls dos
‘inaros que realmente, estan superpuestos als
‘muesta} con una relacion de ass determinads
‘Sua componente se propaga en et medio ms
rapidement que la ota, cuando slen su relacion
eases ha cambiado yl esultane es ura Isr
polarized en un pano rotado 80 especto ass
twientacibn origi
Plano de
polarizacion
22.6 tasuperosiciin dela Fig.225 ta como
‘era un observadorsituado frente a haz inciente
22.3 INTERACCIONES ENTRE DIPOLOS 661
siendo cy ¢ las velocidades de las dos componente en el medio. En funcin de los indi-
ces de refraccidn, esta diferencia es
Ate t= alt
Por tanto, ia diferencia de fase ente fas dos componentes cuando salen de fa muestra es
2aodt 2nl
d= anvat= EEE (ny - a) FE
siendo /.ta longitud de onda de la luz. A ta salida los dos vectores eléctricos tienen una
diferencia de fase distinta de la que tenian iniciaimente, par lo que su superposicin ge-
nera un haz polarizado en un plano que ha rotado un angulo A respecto al plano del
haz ineidente. Por tanto, el angulo de rotacian éptica es proporcional ala diferencia en-
tre los indies de reraecién, nm,
Sie eS
Para explicar por qué ls indices de eefraccin dependen del sentido de rotacin de la
luz hay que examinar por qué las polarzebilidades dependen de este sentido de ratacibn.
Una posible interpretacién es que si una molécula tiene una estructura helicodal(inlu-
vendo, sila molécula es pequeta, cualquier estructura que se pueda considerar como un
‘agmento de hélice) su polarieabildad dependerd desi el camo eléetrico incidente rota 0
ro en el mismo sentido que la hlice. Las moléeulas can estructura helcoidal son quirales,
{que a condicion para la existencia de actividad dptica discutida en la Scecidn 16.26.
El dngulo de la rotacin dptica depende de la frecuencia de la radiacién, denomindndo-
se a esta dependencia dispersin éptica rotatoria {ORD}. La variacion es debids @ las dls-
petsiones individuals de las poarzabilidades (y de 1s indices de refaccién) para la luz
polarizada circularmente a la derecha y a fa i2quierda, y se puede utilizar para estudiar la
‘stereoquimica de las moléculas.
Asociada 3 la diferencia entre dos indices de refraccién (la biretringencia circular del
sedi) existe une diferencia entre las ntensidates de absorcin par tw Ive pulaizada ci
cularmente a a derecha y a fa iquiersda, Jp eZ, respectivamente. Esta diferencia se conoce
‘coma dieroismo circular (CD). El espectro CD de una muestra es la representacién de J ~ Jy
frente a la frecuencia dela radiacién ! dcroismo circular es particularmente itl para de-
terminar la confguracién absoluta de los complejos de metales d, dado que complejos con
geometria similar conducen a espectros CD con caracterstcas parecidas
Fuerzas intermoleculares
Las fuereas de van der Waals son interacciones entre moléculas que practicamente to
perturban su identidad quimica. De este tipo son las interacciones exstentes entre cargas
parciales de moléculas potares o las interacciones repulsivas que evitan el colapso de la ma~
teria 2 1as densidades nucleares. Las interacciones repulsivas surgen de las repulsiones de
Coulomb y, de forma indirecta, del principio de Pauli o de ta exclusion de los electrones
de las zonas del espacio donde se solapan los orbitals de especies vecinas. En esta seccion
consideraremos las fuerzas atractivas entre moléculas y las relacionaremos con [as propic~
dads eléctricas tratadas en la Seccidn 22.1
223 Interacciones entre dipolos
La mayoria de las discusiones de esta seecdn estin basadas en la energia potencial de
‘Coulumb de interaccidn entre dos cargas (Ec. 130). Esta expresidn es facil de adaptar para
obtener fa energiapotencial entre una carga y un dipao y extendera ala interacion entre
os polos.
662
22.7 La energia potencial de imeracdn ent
tun poo yuna carge puntua sa sum de a
repulin entre carga del mismo signe yl ataecin
fntecargs de ign contri. Para un éipolo
purtual (d (30)
Este potecial es sorpendentement til para explicar bastantes propiedad, Ota aprox
mmacton amplamente utiizaa cs potential de Mie
en
con n> m El primer temino representa las repulsiones y el segundo las atracciones. El po~
tenciat de Lennard-Jones &> un caso particular del potencial de Mie enn n= 12 ym
(Fig, 22.17), menudo se eseribe deta forme:
vewe(-(3| wa
eae ee tener ee
Ls ss inode carase och o= 2 aun pte
Lennard-Jones se ha utilizada en muchos calculos, es bastante evidente que 1/r es una
ma exponencial del tipo ¢°". Dado que las. funciones de onda atomicas disminuyen expo-
rennet anion raps epi en
re ee ean 25 bn st pron es
Fo le Tampon Tne se inf" Se
FS aa ceado en dternan ea ner
2 aclu see afer ct na at pb
670
Probatilidad
Velocided molecular
20.19 Desplazamiento dela veloidad mea y
anchura dela distrinuciénconsequida mediante
usode une boquills supersinies,
Orificio \.
Filteo—!
Colimador
Horne
22.20 Una boguils supersinica fia algunas de as
smoleuls del choo ysroporiona un ha con una
\elocidd bien defini,
2 PROPIEDADES ELECTRICAS Y MAGNETICAS DE LAS MOLECULAS.
oe
Ay
XY [iti
tom 7 —
= yn
BE ‘Selector
de velocidades
15 Exquema basco de un dspositva de haves molcuaes os Stamos o moéculessugen de uns
fuente caliente ypasana través de ur stlector de vloidaes, unten de discos rotates La dispersion
‘se produce ene gas objetve (qu también puede estar en forma de hae y se registra el jo de particls
‘que enran en el detector aun deteminado anguo
de tamaiio molecular y una superfice (ver Seccibn 28.2f, es la fuerza la que se ha conver
tido en el centro de atencién, Como toda fucrza, Fes la pendiente negativa del potencial;
para un potencial de Lennard-Jones entre moléculas individuals,
pe Be fof)” J 63)
a Cele
La fuerza neta atractiva tiene el valor maximo para ¢ = (26/7)""ry, 0 1.2441, ya esta distan-
cia es iqual a ~144(7/26)"e/13r, 0 ~2.397¢, Para pardmetros normales, a magaitud de
esta fuerza es de unos 10 pl
3 inoleculares
22.5 Intevacci
Las fuerzas intermoleculares se pueden estudiar mediante haces moleculares, que consis-
ler ei ute Hae eulimady y muy estrecho de moléculas moviéndase ea un recipiente en ¢l
‘que se ha hecho el vacio. El haz se drige hacia atras maléculas, de manera que la disper-
sin que se produce al colisionar ests relacionada con las fuerzas intermolecular.
(a) Principios basicos
La Figura 22.18 muestra el eispostivo basiea necesario para un experimento de haces mole-
culares. Si se incrementa Ia presion de vanor en Ia fuente de tal manera que el recorido li-
bore medio de las moléculas del gas emergente sea mucho mas pequero que el digmeteo del
orificio, se producen muchas colisiones incluso por detrs de la fuente. El efecto neto de e5-
tas colisiones,origen del flujo hidrodindmico, es ura transferencia de momento en la direc~
cin del haz. De este modo fas maléculas del haz se mueven con unas velocidades muy simi
lares y pueden avanzar posteriormente con pocas colisiones entre elas. Esta condicién se
clenomina flujo molecular. Dado que la distribucién de velocidades es muy estrecha, las mo-
leculas estén en un estado con una temperatura de traslacién muy baja (Fg. 22.19). Esto
‘temperatura de traslacion puede ser tan baja como para aleanzar un valor de 1K, Estos cho-
ras se denaminan supersénicos porque fa velocidad media de las moléculs en el chorro es
‘mucho mayor que fa velocidad del sono para las moléculas que no forman parte de! haz
Un chorro supersdnico se puede convertir en un haz supersBnico mas paraleo si se “fl+
tra en fa zona de fujo hidrodindmico y se saca el gas en exceso. E filtro consiste en una
boquilla cénica que evita que las ondas de choque supersonicas se esparzan par el gas, he-
cho que cumentaris la temperatura de taslaci6n (Fig. 22.20), También se puede nbrener un
haz utilizando helio @ neén como gas principal € inyectando las moléculas de interés en
este haz en fa zona de flujo hidrodindmica,
You might also like
- The Subtle Art of Not Giving a F*ck: A Counterintuitive Approach to Living a Good LifeFrom EverandThe Subtle Art of Not Giving a F*ck: A Counterintuitive Approach to Living a Good LifeRating: 4 out of 5 stars4/5 (5807)
- The Gifts of Imperfection: Let Go of Who You Think You're Supposed to Be and Embrace Who You AreFrom EverandThe Gifts of Imperfection: Let Go of Who You Think You're Supposed to Be and Embrace Who You AreRating: 4 out of 5 stars4/5 (1091)
- Never Split the Difference: Negotiating As If Your Life Depended On ItFrom EverandNever Split the Difference: Negotiating As If Your Life Depended On ItRating: 4.5 out of 5 stars4.5/5 (842)
- Grit: The Power of Passion and PerseveranceFrom EverandGrit: The Power of Passion and PerseveranceRating: 4 out of 5 stars4/5 (590)
- Hidden Figures: The American Dream and the Untold Story of the Black Women Mathematicians Who Helped Win the Space RaceFrom EverandHidden Figures: The American Dream and the Untold Story of the Black Women Mathematicians Who Helped Win the Space RaceRating: 4 out of 5 stars4/5 (897)
- Shoe Dog: A Memoir by the Creator of NikeFrom EverandShoe Dog: A Memoir by the Creator of NikeRating: 4.5 out of 5 stars4.5/5 (537)
- The Hard Thing About Hard Things: Building a Business When There Are No Easy AnswersFrom EverandThe Hard Thing About Hard Things: Building a Business When There Are No Easy AnswersRating: 4.5 out of 5 stars4.5/5 (345)
- Elon Musk: Tesla, SpaceX, and the Quest for a Fantastic FutureFrom EverandElon Musk: Tesla, SpaceX, and the Quest for a Fantastic FutureRating: 4.5 out of 5 stars4.5/5 (474)
- Her Body and Other Parties: StoriesFrom EverandHer Body and Other Parties: StoriesRating: 4 out of 5 stars4/5 (821)
- The Emperor of All Maladies: A Biography of CancerFrom EverandThe Emperor of All Maladies: A Biography of CancerRating: 4.5 out of 5 stars4.5/5 (271)
- The Sympathizer: A Novel (Pulitzer Prize for Fiction)From EverandThe Sympathizer: A Novel (Pulitzer Prize for Fiction)Rating: 4.5 out of 5 stars4.5/5 (122)
- The Little Book of Hygge: Danish Secrets to Happy LivingFrom EverandThe Little Book of Hygge: Danish Secrets to Happy LivingRating: 3.5 out of 5 stars3.5/5 (401)
- The World Is Flat 3.0: A Brief History of the Twenty-first CenturyFrom EverandThe World Is Flat 3.0: A Brief History of the Twenty-first CenturyRating: 3.5 out of 5 stars3.5/5 (2259)
- The Yellow House: A Memoir (2019 National Book Award Winner)From EverandThe Yellow House: A Memoir (2019 National Book Award Winner)Rating: 4 out of 5 stars4/5 (98)
- Devil in the Grove: Thurgood Marshall, the Groveland Boys, and the Dawn of a New AmericaFrom EverandDevil in the Grove: Thurgood Marshall, the Groveland Boys, and the Dawn of a New AmericaRating: 4.5 out of 5 stars4.5/5 (266)
- A Heartbreaking Work Of Staggering Genius: A Memoir Based on a True StoryFrom EverandA Heartbreaking Work Of Staggering Genius: A Memoir Based on a True StoryRating: 3.5 out of 5 stars3.5/5 (231)
- Team of Rivals: The Political Genius of Abraham LincolnFrom EverandTeam of Rivals: The Political Genius of Abraham LincolnRating: 4.5 out of 5 stars4.5/5 (234)
- On Fire: The (Burning) Case for a Green New DealFrom EverandOn Fire: The (Burning) Case for a Green New DealRating: 4 out of 5 stars4/5 (74)
- The Unwinding: An Inner History of the New AmericaFrom EverandThe Unwinding: An Inner History of the New AmericaRating: 4 out of 5 stars4/5 (45)
- LaboratorioDocument5 pagesLaboratorioLyseth GómezNo ratings yet
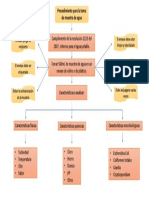
- Procedimiento para La Toma de Muestra de AguaDocument1 pageProcedimiento para La Toma de Muestra de AguaLyseth GómezNo ratings yet
- Guia de Aprendizaje 2Document9 pagesGuia de Aprendizaje 2Lyseth GómezNo ratings yet
- Práctica No. 3 Electroforesis de ADNDocument3 pagesPráctica No. 3 Electroforesis de ADNLyseth GómezNo ratings yet
- Evidencia 2-Estudio Casual, Determinar Las Enfermedades de Origen Hídrico, Sus Causas, Consecuencias y Manejo.Document3 pagesEvidencia 2-Estudio Casual, Determinar Las Enfermedades de Origen Hídrico, Sus Causas, Consecuencias y Manejo.Lyseth GómezNo ratings yet
- Práctica No. 3 Reconocimiento de Propiedades Químicas y Físicas de ProteinasDocument4 pagesPráctica No. 3 Reconocimiento de Propiedades Químicas y Físicas de ProteinasLyseth GómezNo ratings yet
- Práctica No. 4 Extracción de Fosfatasa Alcalina, Efecto de PH, Temperatura, Velocidad de Reacción-Actividad de SustratoDocument7 pagesPráctica No. 4 Extracción de Fosfatasa Alcalina, Efecto de PH, Temperatura, Velocidad de Reacción-Actividad de SustratoLyseth GómezNo ratings yet
- INFORME PRACTICA 6 BQ MetanogenesisDocument6 pagesINFORME PRACTICA 6 BQ MetanogenesisLyseth GómezNo ratings yet
- Taller Proteínas PDFDocument1 pageTaller Proteínas PDFLyseth GómezNo ratings yet
- Práctica No. 7 ZimogramaDocument4 pagesPráctica No. 7 ZimogramaLyseth GómezNo ratings yet
- MisibilidadDocument2 pagesMisibilidadLyseth GómezNo ratings yet
- Practica No 1 Puntos de Ebullición y Fusión de Compuestos OrgánicosDocument8 pagesPractica No 1 Puntos de Ebullición y Fusión de Compuestos OrgánicosLyseth GómezNo ratings yet
- Informe Practica 3 OrganicaDocument6 pagesInforme Practica 3 OrganicaLyseth GómezNo ratings yet
- Práctica de Polímeros y Colorantes en CasaDocument4 pagesPráctica de Polímeros y Colorantes en CasaLyseth GómezNo ratings yet
- Compuesto 84 Informe PDFDocument5 pagesCompuesto 84 Informe PDFLyseth GómezNo ratings yet
- Plantilla Poster XVIIICCQ 1Document1 pagePlantilla Poster XVIIICCQ 1Lyseth GómezNo ratings yet
- Informe Aminoacidos y ProteinasDocument7 pagesInforme Aminoacidos y ProteinasLyseth GómezNo ratings yet
- Aceite de LorenzoDocument2 pagesAceite de LorenzoLyseth GómezNo ratings yet