Professional Documents
Culture Documents
Lineamientos Generales Del Pvu 2024
Lineamientos Generales Del Pvu 2024
Uploaded by
Isaac Alejandro Castro Ramírez0 ratings0% found this document useful (0 votes)
27 views64 pagesCopyright
© © All Rights Reserved
Available Formats
PDF or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as PDF or read online from Scribd
0 ratings0% found this document useful (0 votes)
27 views64 pagesLineamientos Generales Del Pvu 2024
Lineamientos Generales Del Pvu 2024
Uploaded by
Isaac Alejandro Castro RamírezCopyright:
© All Rights Reserved
Available Formats
Download as PDF or read online from Scribd
You are on page 1of 64
SALUD
SECRETARIA DE SALUD
oe on
Y
ae
PROGRAMA DE VACUNACION UNIVERSAL
Lineamientos Generales 2024
Toe =
CONTENIDO
Introduceién...
Marco Legal es
Objetivo General del Programa de Vacunacién Universal
Objetivo de los Lineamientos Generales del Programa de Vacunacién Universal ..6
‘Componentes del Programa de Vacunacién Ur
1 Rectoria
2 Coordinacién Estatal :
21 Funciones de! COEVA.
22 Integrantes del COEVA.
23 Sesiones del COEVA...
24 Actividades del COEVA.
25 Evaluacién...
3 Distribucién de Poblacion de Responsabilad institucional en el Sistema Nacional de
salud, one
31 Objetivo General.
32 Objetivos Especiticos,
33 Politica dela gistribucign de poblacién de responsabilidad institucional en ol Sistema
Nacional de Salud 2024. '
3.4 Fuentes de InforMnaCiON wn =
35 Distribucién de la poblacién a nivel federal ci
36 Propésito de la distribucién de poblacién de responsabilidad institucional 12
4 Capacitaci6n®... - oe
§ Superba ices esses
6 Operacién del Programa de Vacunacion
6.1 Planificacién (Metodologia de Calculo).
62 Programa Permanente de Vacunacién (PPV)
G3 Lineamientos de Aplicacién,
6.4Programacién de actividades.
65 Red de frio
66Poltca de frascos abiertos. oe
6:7 Manejo de Residuos Peligrosos Blolégico Infecciosos (RPBI)
6. 8Seguridad y vacunacién.
69Vacunacion simulténea ¢ intervalos minimosy méximosde Aplicacién 32
B10. Esquema de Vacunacion sn 35
T1Desempeno del Programa de Vacunacion ium: 52
G12 Registro de Dosis Aplicadas en el Programa Permanente y evaluacién del
desempeno del Programa De Vacunacién UnWvEESAl wm
615 Eventos Supuestamente Atribuibles a la Vacunacién o Inmunizacién (ESAVI)
614 Comunicacién,
G15 _Vacunacién en situaciones de emergencia,
16 _Vacunacién a personas en situacién de migracién, desplazamiento, refugiados y
privados de la libertad...
617 Fuentes de informaci6n..
618 Evaluacién
-. S Ss &
dg. 2
B
INTRODUCCION
El presente documento establece los Lineamientos Generales del Programa de
Vacunaci6n Universal (PVU) que se desarrollaré en el pafs durante el afio 2024, los
cuales son de aplicacién obligatoria en todos los niveles técnico-administrativos del
Sistema Nacional de Salud (SNS).
EI PVU es una politica ptiblica de salud, cuyo objetivo es otorgar proteccidn especifica
a la poblacién contra enfermedades prevenibles por vacunacién (EPV)
Los Lineamientos Generales del PVU contienen las acciones que deben Ilevarse a cabo
en todas las Instituciones del SNS para contribuir a la mitigacin, control, eliminacion
yerradicacion de las EPV.
Las metas y objetivos del PVU son los siguientes:
+ Alcanzar y mantener el 95 % de cobertura de vacunacién por entidad federativa
con cada uno de los biolégicos de! PVU (cuadro 1).
+ Alcanzary mantener el 90 % de cobertura de vacunacién en el esquemna completo
para nifias y nifios menores de un afio de edad, de uno, cuatro y seis afios de edad
por entidad federativa
‘+ Mantener la eliminacion de la poliomielitis por virus silvestre en el pais y contribuir
ala erradicacién mundial de este padecimiento,
«| Mantener la eliminaci6n del tétanos neonatal.
© Mantener [a eliminacién del sarampi6n, la rubéola y el sindrome de rubéola
congénita
* Mantener el control epidemiolégico de los siguientes padecimientos
inmunoprevenibles:
Tuberculosis meningea y miliar.
Tétanos no neonatal.
Neumoniay meningitis producidas por Haemophilus influenzae tipo b.
Neumonia y meningitis producidas por Streptococcus pneumoniae.
Enteritis grave causada por rotavirus.
Parotiditis.
+ Mitigar el riesgo de complicacién en infecciones respiratorias agudas atribuibles a
la influenza estacional y COVID-19,
+ Contribuir a la reduccién de Ia incidencia de infeccién por el Virus del Papiloma
Humano (VPH) en mujeres, y sus complicaciones en mujeres y hombres CIS y
TRANS que viven con VIH
rzya>pa0g9
i:
. eee
Hepatitis B.
Difteria. }
Tos ferina.
* Coadyuvar en el monitoreo de la incidencia de los Eventos Supuestamente
Atribuibles a la Vacunacién o Inmunizaci6n (ESAVI)
‘+ Apoyar con informacién técnico-cientifica la innovacién y cambios requeridos en
el PVU, en beneficio de la poblacién
Gree ea ee Nees
GRUPO DE EDAD /ACUNA NUMERO DE Dosis
BCC Una dos
Sea eee ANTI HEPATITIS B Una dosis |
HEXAVALENTE ACELULAR | 1h, ®y 3° dosis
“ANTI NEUMOCOCICA
Py 2" dosis
MENORES DE UN ARlO | —CONLCADA
ANTI-ROTAVIRUS Py 2" dosis (RVI)
ANTI INFLUENZA ya: desis (eseuemns:
inicial)
ANTI NEUMOCOCICA ua
i CONJUGADA " we
eee TRIPLE VIRAL (SRP) ¥ dosis f
ANTIINFLUENZA, Dosis Anual
TRIPLE VIRAL SRPF 2 dosis™
buatenmae HEXAVALENTE ACELULAR Dosis de refuerzo
CUATRO ANOS TRIPLE BACTERIANA (OPT)_| Dosis de refuerzo,
SEIS ANOS TRIPLE VIRAL (SRP) 2 doss™
“ET cambio de ezauerne de Vacunacln de SRP, se reales con Base Gn Ts aCURTOOseStaDICRTGS Oh Ta Reunion Te
Expertos en Vacunacin, eda OS de noviembre de 2019.
‘Se aplica alas nia y nies que cumplan id meses de edad en 2026,
"Se apica a las nites y nifos que cumplan 6 afos en 2024, Dicha estrategia se implementaré hasta 2026
pesterinmente se dejar de aplicara esta edad paro se seguird aplcando anifiasy nis de 18 meses de edd
Referente a la vacunacién contra la COVID-19, deberd considerarse que a la
fecha de publicacién del presente lineamiento, la rectoria de la estrategia :
Operativa Correcaminos' sigue vigente, por lo que, la informacién descrita en
estos lineamientos Unicamente son de caracter técnico, hasta su transicion al
Programa de Vacunacién Universal a cargo de la Secretaria de Salud a través
del CENSIA. \
ete RUN:
Marco LEGAL
+ Constitucién Politica de los Estados Unidos Mexicanos, Articulo IV.
+ Ley General de Salud, Titulo 8°, Capitulo I, Articulos 134, 135, 141, 144, articulo 157 Bis 1a
16; Titulo 18°, Capitulo |, Articulo 404, inciso IV, Articulo 408; Capitulo VI, Articulo 462 Bis,
DOF: tiltima reforma 07/0/2021,
+ Ley de Infraestructura de la Calidad, Capitulo IV, Articulo 10, inciso |; Titulo 3°, Articulo
147.
+ DECRETO por el que se reforman y adicionan diversas disposiciones de la Ley General
de Salud, en materia de vacunaci6n. DOF: 19/06/2017.
+ DECRETO por el que se crea el Consejo Nacional de Vacunacién, DOF: 24/01/1991, ultima
reforma 05/07/2001.
‘* DECRETO por el que se determina la integracion del Consejo Nacional de Vacunacion,
DOF: 26/1/2018.
+ Reglamento Interior de la Secretaria de Salud, Articulo 47, fracciones | a XIX, se
establecen las funciones del Centro Nacional para la Salud de la Infancia y Adolescencia
(CENSIA). DOF: ultima reforma 07/02/2018.
+ Plan Nacional de Desarrollo 2019-2024,
+ NORMA Oficial Mexicana NOM-004-SSA3-2012, Del expediente clinico. DOF: 15/10/2012.
+ NORMA Oficial Mexicana NOM-007-SSA2-2016, Para la atencién de la mujer durante el
embarazo, parto y puerperio, y de la persona recién nacida. DOF: 07/04/2016.
* NORMA Oficial Mexicana NOM-O10-SSA-2023, Para la prevencién y el control de la
infeccién por virus de la inmunodeficiencia humana,
«NORMA Oficial Mexicana NOM-017-SSA2-2012, Para la Vigilancia Epidemiolégica, DOF:
19/02/2013.
+ NORMA Oficial Mexicana NOM-031-SSA2-1999, Para la atenci6na la salud del nifio. DOF:
09/02/2001
+ NORMA Oficial Mexicana NOM-034-SSA2-2013, Para la prevencién y control de los
defectos al nacimiento. DOF: 24/06/2014.
‘+ NORMA Oficial Mexicana NOM-036-SSA2-2012, Prevencion y control de enfermedades.
Aplicacién de vacunas, toxoides, faboterdpicos (sueros) e inmunoglobulinas en el
humano. DOF: 28/09/2012.
+ NORMA Oficial Mexicana NOM-087-SEMARNAT-SSAI-2002, Proteccién ambiental -
salud ambiental - residuos peligrosos biolégico-infecciosos - clasificacién y
especificaciones de manejo. DOF: 17/02/2003.
+ NORMA Oficial Mexicana NOM-220-SSAL-2016, Instalacién y operacién de la
farmacovigilancia. DOF: 19/07/2017.
+ NORMA Oficial Mexicana NOM-010-SSA2-2023, Para la prevencién y el control de la
infecci6n por virus de la inmunodeficiencia humana, DOF: 02/06/2023.
* ACUERDO por el que se establecen diversas medidas relacionadas con el Plan de
Gestién a largo plazo para el control de la COVID-18. DOF: 15/06/2023,
Pag. 5 atten
ae aa
aie oo *\
Vy
Dag
OBJETIVO GENERAL DEL PROGRAMA DE VACUNACION UNIVERSAL
Contribuir al ejer
io del derecho a la proteccién de salud de la poblacién a través de
la vacunacién en la linea de vida, para mantener la eliminacién, control epidemiolégico
y disminucién en la incidencia de las enfermedades que se previenen con esta
intervencién en salud publica.
OBJETIVO DE LOS LINEAMIENTOS GENERALES DEL PROGRAMA DE
‘VACUNACION UNIVERSAL
Establecer criterios para la planeacién, programacion, ejecucién, monitoreo y
evaluacion del PVU.
COMPONENTES DEL PROGRAMA DE VACUNACION UNIVERSAL
La ejecucién del PVU se lleva a cabo mediante sus componentes de rectoria y
operacién, cada uno engloba diferentes puntos que se explican a continuacién.
Pag. 6 ab Te0ss
1 Rectoria
La rectoria en materia de vacunacién a cargo de la Secretaria de Salud Federal, se
fortalecera a través de la coordinacién sectorial e interinstitucional del PVU en la
mitigaci6n, control, eliminacién 0 erradicaci6n de algunas enfermedades trasmisibles
y prevenibles por vacunacién. La coordinacién interinstitucional es una estrategia
clave para el buen desemperio operative.
Las instituciones de salud deben establecer mecanismos de coordinacién,
seguimiento y monitoreo para el andlisis de sus poblaciones objetivo y la evaluacion
de coberturas; asi como emitir recomendaciones y/o estrategias de mejora en el
cumplimiento de la normatividad establecida para el PVU.
La Direccién General de Promocién de la Salud (DGPS), planeard, coordinaré y dard
seguimiento a las Jornadas Nacionales de Salud Publica (JNSP), una actividad de
cardcter interinstitucional, en las cuales todas las instituciones del SNS participan de
forma activa para el cumplimiento de actividades programadas bajo la rectoria de la
DGPS; para ello tendran concertacién de carécter intersectorial con la Secretaria de
Educacion Publica (SEP), los Servicios Estatales de Educaci6n (SEE), los Sistemas para
el Desarrollo Integral de la Familia (SNDIF}, e! Instituto Nacional para la Educacién de
los Adultos (INEA], el Instituto Nacional de los Pueblos Indigenas (INPI), entre otros.
2 COORDINACION ESTATAL
La Secretaria de Salud estatal, como parte de su funcién rectora coordinara a través
del Consejo Estatal de Vacunacién (COEVA) organo colegiado en el cual confluyen los
representantes de las Instituciones ptiblicas del Sector Salud prestadoras de servicios
de salud operativos del PVU.
2.1 FUNCIONES DEL COEVA.
Convocar y realizar reuniones ordinarias y extraordinarias abordando temas
relacionados con el PVU, tales como:
© Coberturas de vacunacién y reporte de dosis aplicadas (RDA) por tipo de biolégico,
grupo de edad ¢ institucidn en los niveles estatal, distrital/jurisdiccional y municipal
© regional.
+ Seguimiento al abasto de biolégicos.
* Distribucién de poblacién de responsabilidad institucional (DPR).
+ Eventos Supuestamente Atribuibles a la Vacunacion 0 Inmunizacin de tipo grave.
+ Casos y brotes de enfermedades prevenibles por vacunacion
«Red de frio.
Pag. 7 atte
Ss
SY
a
4
* Vacunacién contra la COVID-19.
+ Capacitacién y supervision.
* Seguimiento de acuerdos del Sector Salud,
* Campaias especiales de vacunacién.
demas de analizar e implementar estrategias para la prevencién, control, eliminacion
y erradicacién de las EPV acorde a la realidad epidemiolégica de la entidad.
2.2. INTEGRANTES DEL COEVA
Presidente (Secretario de Salud de la entidad federativa).
Secretario Técnico (Director de los Servicios de Salud u homdélogos).
Titular del Organo Operativo Administrativo Desconcentrado (OOAD} Estatal 0
Regional del Instituto Mexicano del Seguro Social (IMSS) Régimen Obligatorio.
+ Coordinador Estatal de los Servicios de Salud del Instituto Mexicano del Seguro
Social para el Bienestar (IMSS-BIENESTAR) en las entidades cuyos servicios de
salud hayan sido transferidos.
Supervisor Médico del Programa IMSS-Bienestar en el OOAD.
Delegadio Estatal del Instituto de Seguridad y Servicios Sociales de los Trabajadores
del Estado (ISSSTE}
Responsable de Sanidad Militar en la region (SEDENA).
Responsable Estatal del Programa de Atencién a la Salud de la Infancia y la
‘Adolescencia (PASIA) de la Secretaria de Salud.
Responsable Estatal del PVU de la Secretarfa de Salud.
Acorde a la presencia de las instituciones de salud en las entidades, en caso de que
aplique, deberé participar el responsable de Sanidad Naval en la region (SEMAR) y
el responsable regional de los Servicios de Salud de Petréleos Mexicanos (PEMEX).
Responsables institucionales de los sisternas de informacién de vacunacién
universal
Consideraciones:
+ Exclusivarnente una persona por institucién podré emitir su voto,
+ Enausencia de los titulares de las instituciones, se deberd designar mediante oficio.
un representante con atribucion para toma de decisiones y emision de voto.
2.3 SESIONES DEL COEVA
Los COEVA realizaran cuatro sesiones ordinarias al afio como minimo, una por
trimestre, pudiendo realizar un mayor numero de reuniones de acuerdo con sus
necesidades. Las reuniones extraordinarias dependeran de las necesidades del PVU,
esate essen esacnessenecnneneeenenen 3 ESSRSSSIEESSeanUeneeSOUUneRNOEEEEE = bq
eae
Ce
PANU Cale TON Vaso
al ser de caracter emergente, no se establecen criterios para su programacién y, por lo
tanto, tampoco se consideran para la evaluacién de los indicadores correspondientes.
2.4 ACTIVIDADES DEL COEVA
+ Elaborary enviar al CENSIA antes del 15 de febrero de 2024 el cronograma anual de
reuniones del COEVA, debiendo especificar el mes de realizacién de la reunion,
+ EI COEVA levantard un acta o minuta de acuerdos por cada sesién celebrada,
mismas que se enviarén al CENSIA para dar fe de su cumplimiento. Adicionalmente
deberan remitir las presentaciones 0 documentos de apoyo que se utilizaron
durante la sesién al correo censia.info@salud.gob.mx . Los archives deberan
remitirse por via oficial o electrénica al CENSIA con las siguientes fechas de corte:
+ Primer trimestre, a mas tardar el 05 de abril de 2024,
+ Segundo trimestre, a mas tardar el 05 de julio de 2024,
+ Tercer trimestre, a més tardar el 04 de octubre de 2024.
© Cuarto trimestre, a mas tardar el 10 de enero de 2025,
+ Analizar, evaluar y validar las coberturas de vacunacién de manera sectorial con la
validacién por sus integrantes, de manera mensual por tipo de biolégico y por
grupo de edad en el nivel local, distrital/jurisdiccional y estatal de todo el sector de
manera trimestral.
+ Coordinar las actividades de las INSP de todo el sector; cada COEVA elaboraré su
calendario de trabajo. Las fechas de realizacién de las JNSP seran publicadas por la
Direccién General de Promocién de la Salud (DGPS) a través de medios oficiales y
estaran sujetas a los lineamientos que se publiquen para tal efecto, Las actividades
© aplicaciones que se deriven de las JNSP se incluiran en los registros informaticos
mensuales correspondientes a cada institucién, asi como los definidos por la DGPS
en coordinacién con el CENSIA.
= Convocar al Comité Estatal de Expertos de ESAVI para garantizar la investigacion
de los casos de ESAVI graves a través del dictamen de los mismos.
25 EVALUACION
EI CENSIA validard la recepcién de las actas 0 minutas trimestrales de los COEVA con
el fin de verificar que se hayan celebrado las sesiones programadas,
Al ser los COEVA organismos con autonomia, el CENSIA Gnicamente podrd participar
como orientador de alguno de ellos, previa solicitud e invitacion del COEVA.
La cobertura de vacunacién del programa permanente deberd abordarse por el
COEVA, en cada una de las reuniones programadas por trimestre, en el entendido
del envio del RDA.
Pag. 9 uateens
a
T LAS
=e
y
Png J
y
Men 7
En el supuesto de que se presenten casos y brotes por EPV, el COEVA y Ia
coordinacién interinstitucional correspondiente al nivel estatal y
distritaljurisdiccional sesionardn de forma urgente y extraordinaria, a fin de
establecer las medidas necesarias y lineas de accién para el control del brote, en
coordinacién con el nivel federal.
De ser necesario, los COEVAs deberdn modificar su reglamento interno de los
Consejos Estatales de Vacunacién, con el fin de cumplir con lo establecido dentro
del presente lineamiento.
3 DISTRIBUCION DE POBLACION DE RESPONSABILIDAD INSTITUCIONAL EN
EL SISTEMA NACIONAL DE SALUD
La distribucién de la poblacién de la Reptiblica Mexicana implica que cada una de las
instituciones publicas del Sistema Nacional de Salud conozca su poblacién de
responsabilidad a vacunar, asf como la asignacién a nivel estatal de las areas
geograficas que quedaran bajo su responsabilidad, con la finalidad de cubrir el cien
por ciento de las localidades del pais,
Es decir, las vacunas se otorgan a todas las personas susceptibles de ser vacunadas de
manera gratuita en el sector ptiblico en [a linea de vida, sin distincion alguna:
derechohabiencia, condicién social, migratoria, econémica, étnica © nacionalidad,
atendiendo a la gratuidad y universalidad de! Programa establecidos en Ia legislacion
de México de conformidad con el articulo 187 Bis I, Capitulo I! Bis, DECRETO por el que
se reforman y adicionan diversas disposiciones de la Ley General de Salud, en materia
de vacunacién, DOF 19/06/2017,
3.1 OpseTivo GENERAL
Que cada institucién publica del SNS conozca con precisién su poblacién de
responsabilidad menor de 8 afios de edad, y el total de la poblaci6n de otros grupos
de riesgo que reside en la Reptiblica Mexicana, para garantizar el acceso a todas las
vacunas del esquema basico del PVU, tanto en fase permanente, como en campaiias
intensivas, operativos especiales y brotes de EPV.
3.2. Opserivos Especiricos
+ Distribuir la poblacion total de la Reptiblica Mexicana por grupo de edad entre las
instituciones piiblicas del SNS.
? https: dof. gob mx/n
Pag. 10
© Con base en la distribucién realizada, cada institucién publica del SNS, debe contar
con el insumo suficiente para llevar a cabo las acciones de vacunacién de acuerdo
con la poblacién menor de 8 afios de edad bajo su responsabilidad, asi como dela
poblaci6n restante de acuerdo con los grupos especificos y de riesgo.
3.3 POLITICA DE LA DISTRIBUCION DE POBLACION DE RESPONSABILIDAD
INSTITUCIONAL EN EL SISTEMA NACIONAL DE SALUD 2024
+ Temporalidad: La distribucién de la poblacién debe elaborarse oportunamente,
con [a finalidad de que las instituciones de salud en los niveles estatales estén en
posibilidad de estimar sus presupuestos para la adquisicién de insumos necesarios
para el funcionamiento del PVU. En el afio 2022, se realizé la distribucién de
poblacién de responsabilidad institucional del Programa de Vacunacién Universal
en el Sistema Nacional de Salud 2023-2024, atendiendo el requerimiento de
compra de vacunas bianual del extinto Instituto de Salud para el Bienestar
(INSAB))..
* Responsables: Instituciones puiblicas del Sisterna Nacional de Salud
© Universo: Las 32 entidades federativas.
3.4 FUENTES DE INFORMACION
Los Sistemas de informacién de nuestro pais estén fragmentados, contando cada
institucion con sus propios criterios y procedimientos de recoleccién de datos en
arquitecturas tecnolégicas heterogéneas, por lo que, corresponde a cada institucién:
+ Bajo la rectoria de la Secretaria de Salud, y en las entidades cuyos servicios de salud
han sido trasferidos a los Servicios de Salud de IMSS-BIENESTAR, las Proyecciones
Oficiales de! Consejo Nacional de Poblacién (CONAPO), con base en la encuesta
intercensal 2015 (cifras publicadas en septiembre de 2018).
* Para el Instituto Mexicano del Seguro Social (IMSS) en su régimen obligatorio, la
base programatica sera determinada por la Direccién de Incorporacién y
Recaudacién (DIR), Poblacién Adscrita a Medico Familiar.
* Para el Programa IMSS-Bienestar, la base programitica considera los datos de la
Coordinacién de Atencién Integral a la Salud y Coordinacién de Planeacion
Estratégica y Padrén de Beneficiarios.
+ Para el ISSSTE, la base programatica considera la Poblacion derechohabiente
registrada por la Subdireccién de Afiliacién y Vigencia de Derechos del ISSSTE.
«Para la SEDENA, la base programética considera la Poblacién derechohabiente
registrada por el Instituto de Seguridad Social para las Fuerzas Armadas Mexicanas
(ISSFAM./SEDENA)
a
= gh
3.5 DISTRIBUCION DE LA POBLACION A NIVEL FEDERAL
+ La Direccién General de Informacién en Salud (DGIS}, es la encargada de realizar la
distribucién de poblacién correspondiente a cada una de las instituciones publicas
del SNS, en coordinacién con los responsables federales del PVU.
+ Los responsables de! PVU del nivel federal del IMSS-Obligatorio, programa IMSS-
Bienestar e ISSSTE, validan dicha poblacién, e informan al CENSIA su poblacion
desglosada por grupo de edad (< | aio), 2, 3, 4,5, 6, 7, 8, 9, 10, 11,12, 13 y 14 afios de
edad, los grupos de 15 a 19, 20 a 39, 40 a 49, 50 a 59, y 60 aitos y mas, y por entidad
federativa; el resto de la poblacién sera responsabilidad de la Secretaria de Salud,
en las entidades federativas que no se encuentren federalizadas.
+ EI CENSIA calculara las poblaciones intermedias de responsabilidad (15, 16, 25, 26,
35, 36, 45, 46, 55, 56, 60, 61, 62, 63, 64, 65 y 66 afios), las cuales seran validadas por la
Dols.
* Una vez validada la informacién, se procede a la firma de comtn acuerdo y una vez
firmada, se envia via oficial a los 32 COEVAs, para darla a conocer a las diferentes
instituciones estatales de salud
* Esta es la poblacién oficial que cada institucién de salud tendré bajo su
responsabilidad y se utilizar para la programacién del PVU 2024, Esta base de
datos se utilizaré para el calculo de dosis requeridas y sera la base para el
denominador del célculo de coberturas de vacunacién.
* Los COEVAs son los responsables de distribuir la poblacién conforme a la
identificacién de las redes locales de servicios de salud con capacidad de aplicar
vacunas, por grupo de edad y por institucién, hasta el nivel municipal, Para el IMSS-
Obligatorio la distribucién se realizard de acuerdo a sus CLUES.
* Los COEVAs deberan fortalecer la coordinacin interinstitucional para la
corganizacién, planeacién y distribucién de la poblacién de responsabilidad por
institucién, asi como la asignacién de las 4reas geograficas que quedarén bajo su
responsabilidad.
+ El Grupo de Trabajo interinstitucional (GT!) federal, tomara conocimiento de los
acuerdos que se establezcan en los COEVAs.
+ Ante alguna problematica que se presente del nivel de resolucién estatal, el COEVA
deberd informar al CENSIA con oportunidad para que se evalle y establezca la
coordinacién con la institucién que corresponda para determinar lo procedente.
+ La poblacion de 9, 10,11, 12, 13 y 14 aftos de edad y la poblacién por grupo de edad
de 15 a 19; 20 a 39; 10 a 49; 50 a 59, y de 60 0 mas aos de edad, que es atendida por
derechohabiencia, y de acuerdo con los grupos especificos de riesgo, como son:
adolescentes, personas embarazadas, adultos mayores, personal de salud y
personas privadas de su libertad y personal que trabaja en guarderias y asilos.
3.6 PROPOSITO DE LA DISTRIBUCION DE POBLACION DE RESPONSABILIDAD
INSTITUCIONAL
Pag. 12 ates
5
an
y
4
+ A nivel federal forma parte de la base de calculo para la adquisicién de los
biolégicos requeridos por las instituciones del SNS y define los denominadores para
las coberturas de vacunacién.
+ Anivel estatal, es el elemento para la construccién de un plan de trabajo anual con
poblacién de responsabilidad asignada a la red de servicios de salud y define los
denominadores para el célculo de la cobertura por biolégicos y esquemas
completos a nivel local/municipal, jurisdiccional/delegacional y estatal.
4 CAPACITACION?
Elnivel nacional de la Secretaria de Salud debera realizar en el afio, al menos un evento
de capacitacién (presencial y/o virtual) con Ia participacién de los 32 responsables
estatales del PVU y ly los responsables del nivel federal de los Servicios de Salud del
Instituto Mexicano del Sequro Social para el BIENESTAR, IMSS Obligatorio, Programa
IMSS-Bienestar, ISSSTE, PEMEX, SEDENA, y SEMAR. Los temas por abordar seran
definidos por el CENSIA.
EI nivel estatal, delegacional/jurisdiccional realizarn en el afio, al menos cuatro
eventos de capacitacién, para lo cual se elaborard un plan anual de capacitacién que
incluya:
a) Participacién de los responsables de vacunacién de los Servicios de Salud de la
Secretaria de Salud, Servicios de Salud del Instituto Mexicano del Seguro Social
para el BIENESTAR, IMSS-Obligatorio, Programa IMSS-Bienestar, ISSSTE y demas
instituciones de salud que integren el sistema estatal de salud.
b) Carta descriptiva.
c) Lista de asistentes que incluya nombre, firma e institucién a la que pertenece.
d) Se recomienda contar con la asistencia de al menos el 90 % del personal
convocado, adscrito a las unidades de responsabilidad de cada una de las
instituciones, deberan incluir al personal de unidades de segundo y tercer nivel que
apliquen vacunas.
) Se recomienda al nivel estatal incluir en la capacitacion los siguientes contenidos.
Primera sesi6n de capacitacién:
« Lineamientos Generales del PVU.
© Esquema de vacunacién universal vigente para todas las vacunas, y las
actualizaciones en los esquemas de vacunaci6n vigentes; incluida la (s) vacuna (5)
contra la COVID-9.
«+ Indicaciones y contraindicaciones de los diferentes biolégicos.
Pag. 13, tren
al
+ Oportunidades perdidas de vacunacién, vacunacién simultanea.
* Priorizacién de actividades en grupos vulnerables.
+ Eventos Supuestamente Atribuibles a la Vacunaci6n o Inmunizacion (ESAVI)
+ Vigilancia epidemiolégica de enfermedades prevenibles por vacunacién.
Siguientes sesiones de capacitacion’
+ Procedimientos para la vacunacion segura.
+ Técnicas de aplicacién de los biolégicos.
* Manejo normative, Almacenamiento y conservacién de la red de frio.
+ Instalacién y preparacién del termo en el puesto de vacunacién.
+ Demostracién fisica de la presentacion de los diferentes biolégicos.
+ Manejo de frascos abiertos (para uso intramuros y extramuros; politica de frascos
abiertos).
+ Mantenimiento preventivo y/o correctivo de la red de frio (unidades refrigerantes).
+ Accidentes de red de
* Manejo de residues peligrosos biolégico infecciosos (RPBI). a
i
+ Registro y control de entradas y salicas del biolégico
+ Vacunacién simulténea,
+ Sistema de informaci6n de vacunacién: reporte de dosis aplicadas (RDA), cobertura
de vacunacién, calidad del dato y monitoreo rapido de vacunacién en areas de
riesgo (MRV), plataformas de registro en Camparias de Vacunacién, Ambiente para
la Administracién y Manejo de Atenciones en Salud (AAMATES)
Por tratarse de una tarea operativa, la evidencia de las capacitaciones realizadas
@ nivel estatal, delegacional/jurisdiccional y en unidades de salud, deberd ser
resguardada en Ia unidad aplicativa correspondiente, siendo responsabilidad de
los niveles correspondientes verificar su cumplimento y respectivo
almacenamiento.
5 SUPERVISION?
para la mejora del Programa, proporcionando asesoria para la solucién de los
problemas identificados,
Para priorizar los lugares de las entidades federativas que se deberan supervisar, se
tomaran en cuenta las prioridades técnicas del PVU, la presencia de brotes de algunas ‘y
Para evaluar las acciones rutinarias e intensivas del PVU, se desarrollaran actividades
de asesoria y supervision que permitan identificar desviaciones y areas de oportunidad \
Pag. 6 wahoo!
2 —=_—
ON UNIVERSAL
enfermedades prevenibles por vacunacién, bajas coberturas de vacunacién,
incidencia 0 prevalencia de accidentes de Red de frio u otros aspectos técnicos que
requieran dar prioridad al estado seleccionado.
Hasta donde sea posible, las supervisiones por los responsables estatales se realizarén
en forma interinstitucional, siendo las autoridades institucionales a nivel local (estado,
delegaciones institucionales) las que financien estas actividades.
EI CENSIA pone a disposicién para consulta el modelo de cédula de supervision del
PVU, la que podra adicionar rubros que considere importantes en su entidad con base
en la cedula de supervision para su uso e implementacién (sin eliminar los
componentes establecidos en la presente}. El nivel estatal realizaré un cronograma de
supervision anual:
+ Se realizaran al menos dos supervisiones a las Jurisdicciones de menor cobertura
de vacunacion o que hayan presentado incidentes que ameriten supervision, y al
menos dos visitas de supervision a las unidades de salud de menor desempefio en
el PVU, o que hayan presentado incidentes que ameriten supervisi6n.
Se realizara al menos una supervision a las unidades de salud que presenten mas
de laccidente de red de frio en un periodo de 6 meses
Elnivel estatal y delegacionaV/jurisdiccional debera dar seguimiento al curnplimiento
‘oavance de las recomendaciones emitidas, acorde al nivel supervisado. Al tratarse de
herramientas operativas destinadas a la mejora permanente del programa, éstas
deberdn ser conservadas en Ia unidad administrativa correspondiente, siendo
responsabilidad del drea estatal y local que supervis6 verificar el seguimiento.
La supervision debera realizarse con un componente de evaluacién considerando los
siguientes puntos:
1. Estructura: En esta seccién se exploran los siguientes rubros: organigrama,
recursos humanos, fisicos y materiales, incluyendo la red de frio.
2. Proceso: Organizacién (coordinacién institucional, sectorial}, _procesos
(normatividad, capacitacién, supervision, red de frio) y procedimientos (técnica de
reconstitucion, higiene de manos, técnica de aplicacién, manejo adecuade de
frascos multidosis, cumplimiento de la norrnatividad del PVU), ingresos y egresos
de biol6gicos.
3. Resultado:
Indicadores de coberturas por tipo de biolégico y esquemas completes.
Pag. 15 atts
—-s-
Las supervisiones, as/ como las capacitaciones realizadas a nivel estatal y
jurisdiccional seran responsabilidad de los servicios estatales e institucionales de
salud, en cuyo acompariamiento técnico podria participar el COEVA o bien el
CENSIA.
La metodologia de cdlculo para las vacunas del PVU se realiza en apego al esquema
de vacunacién y base poblacional oficiales (ver cuadro 2). Las vacunas contra la
hepatitis A y contra Ia varicela no forman parte del esquema bdsico de
vacunacién. Al igual, que la vacuna contra la COVID-19, a la fecha de publicacién de
este linearniento, se encuentra bajo uso de emergencia.
La fuente de cdlculo para la planificacién de biolégicos en el PVU deberd ser la
poblacién de responsabilidad por entidad federativa y grupo de edad para el afio 2024,
misma que fue calculada con base en los “Lineamientos para la distribucién de
poblacién de responsabili
el Sistema Nacional de Salud, México 2023-2024",
Para el cdlculo de vacunas, las instituciones a nivel federal podran realizar
ajustes, con base en Ia situacién de oferta de vacunas por los distribuidores y/o
laboratorios productores, las cuales se notificardn por los medios de notificacién
oficial al nivel estatal. El porcentaje de “factor de pérdida” estard sujeto a la
operacién de cada institucién, sin superar los rangos sefialados en el cuadro No.
2, correspondiente al rango aceptado por e! PVU.
De forma adicional, las entidades federativas y las instituciones del Sector Salud a nivel
estatal, con la intencién de medir la trazabilidad de la operacién rutinaria del
programa, podran considerar:
6 OPERACION DEL PROGRAMA DE VACUNACION
6.1 PLANIFICACION (METODOLOGIA DE CALCULO)
fad institucional del Programa de Vacunaci6n Universal en
RDA.
Registro de distribucién de biolégico a punto operativo (Distrito/Jurisdiccion
Sanitaria y Unidad Médica).
Niveles de Prevencién con servicio de vacunacién (Identificado por CLUES).
Capacidad instalada de ted de frio por unidad médica, jurisdiccién y entidad
federativa
q
Pag. 16 “aa bE Cen &
eet
my
Y
Z
A
\ |
&
\
CUNACION UNIV
rr
Peers
Dose] FACTOR
cusve vacua | postacton atanco cvcuto ron | oe
esquewa | pERDIDA
spo. c00s8aToT | Vacmns BEE | Seconsidere una dose | (Poblacan menor de
par el 100% de as nate
nits ni mente :
Geunaro, misuna | Poblaciones de 1239 4
dosisparaclSecdetas | ahoex003) :
nifas y nifos de uno a x eaLmne 50-50%
cuatioates. | slactorde péraia
(rezagados}, todas de
Tecponsatiided | Ajuste cl esutado ala
intuctnal decena superior
BO.900RERTOO | VIG Secansider una Toa] obiacn menor deay
Recombinante | para e100 %de las ate
gems be | alteapelfes earn :
epettis@ HB10 | deunstode | s%sfectordepéraida | osm | 35%
mg responsabiiged
irethucional, | Ajusteet resultado ala
docena super
aae.c008500-| —Vacana | ~Seconaieranres | Poblacion menor de
reravaterte | dosisparali00%de | unatox 3}
toporsaesio-tit) |" tacrifesy nos :
menores de afi, rns | [Poblacion de un afo)
vacuna saul | "yna dose para e100 *
antipetussi,con | se lasrinasy ninas | (Pobloionesde 2,3 4
toxoides difterico y de lafio, mas una afios x 0.05)
bois dosis para el 5 % de las 2 oSmt 35%
vceoridoscn | Tinasymitosde 204 | stactorde prio
anvipotomiettica | *8tezau84e5,
vanaaindn con, | sesponsabiided | Alustwetesukad af
cane conjugada | euconal ecena superior
Infvonsae tno by
heats
caopooesaar | —vacana | —Secarexderan dos —| Poblacion mener dean
Gzoc00010.05 | monovatente | dosisparael100 % de cron?
ceo.o00.ewe0% | contavtanrus | lasniney nitos i
ezoeoeowoes | (RV) | menoresde unahode | %tactorde perdida | 1SmL | 345%
recporesiidac!
Tretucional, | Ajusteetresultaco ala
decena superior
qappaoIsEas | —vacura | ~Secanaideran dex | TPobiacion menor de
o20.000.014601 | antneumococca | dostsparaetio0%de | unahox?)
Coriugeds | ie rifasy nitos :
meneresdeunare, | (Poblaciéndeunano) | osm. | 55%
mas una dsis para el :
100 % de las nifias y {Poblacién de 60 afios)
rifoeds tao une :
Pog. 17 —
eee ceras
1
As
x
NNN
GUE scone een ieee eee)
ciave VACUNA, POBLACION BLANCO chcuo | por | be
i ESQUEMA | PERDIDA
oss para e100 % de_| (Poblacion de Tans y
fa poblacién de 60 mas x005))
aos, més una dosis x
para el 5% de la 9% factor de pérdida
poblacién de 61 aftos y
més (rezagados), | Ajuste el resultado ala
todas de decena superior.
responsabilidad
institucional
(020.0006317.00_| Vacuna Se_consideran dos | (Poblacion desaTr
620.000.6317.01 | antiinfluenza _| dosis para e!100% dela meses x2)
620.000.6317.02 | estacional" poblacién de 6 a .
meses, més una dosis,
para el 100% de ta
poblacion de 12 2 59
meses, més una dosis
para el 100% de la
poblacién de 60 afiosy
més, més_una dosis
para la poblacén de Sa
59 afios considerada
de riesgo (7% de la
poblacin de 5 a 59
afios), més una dosis
para el 100% de las
embarazadas (100% de
la poblacion menor de
Un afio), mas uns dosis
para el 100% del
personal de salud,
(Poblacion de 12a 59
meses de edad)
(Poblacién de 60 aftos y
mas)
(Poblacién de 5 a 59
anos? x0.07)
(Poblacién menor de un
anor)
(Personal de salud de
responsabilidad)
% factor de pérdida
‘Ajuste el resultado ala
osmt | 310%
ae
jn
todas de} decena superior.
responsabilidad
institucional
Pag. 18
pte
4
he
Ad f
DOSIS- ] FACTOR
clave VACUNA POBLACION BLANCO cALcuLo, Por De
Esquema | PERDIDA
"020,000,3820.00 | Vacuna triple viral | Se considera una dosis | ((Poblacionde un anox | OS5mL | S10%.
(020.000.3821.00 | |SRP) contra | para el 100 % de las 2)
sarampién, ninas y nifios de un +
rubéola y | ahode edad (ira dosis}, | (Poblacién de 6 arios)
parotiaitis mas una dosis para el +
100 % de las niftas y| —_(Poblaciones de
nifias de 18 meses (2da | 23,4.5,7,89y 10 afios x
dosis), mas una dosis 0.05))
para el 100 % de las x
nifas ynifiosde Garis | 120 para atencion a
(2d dosis), mas una brotes)
dosis para el 5 % de la x
poblacion de 2,3, 4,5, | %factorde perdida
7, 8 9 y 10 afos de
edad |rezagados de | Ajusteol resultado ale
ambos esquemas),|__decena superior.
todos de
responsabilidad
institucional
Mas el 20 % para
atencién de brotes
(bloqueos),
'020,000,3805.00 | Vacuna Se considera una desis | [Poblacion de4 anos) | OSmt | 520%
antipertussis con
toxoides diftérico
y teténieo (DPT)
para el 100 % de las
nihas y nihos de 4
afios, mas una dosis
para 015% de las nifias
y nines de $y 6 altos
rezagados). todas de
responsabilidad
{Poblaciones de Sy 6
‘afhos x 0.05))
‘6 factor de pérdida
Ajuste el resultado ala
institucional decena superior
020.000.4172.00 | Vacuna contra I | Seconsidera unadosis | ((Poblacionde1o— | OSmt— «| ES%
020.000.4172.01 | virus del | para el 100 % de las anosi2"
papiloma adolescentes de 10 +
humane (vPH) | afios, mas tres dosis | (Mujeres y hombres cis,
para el 100 % de las | ytrans de Tl a 49 afios
mujeres cis y trans y| que viven con VIH x 3)
hombres cis y trans x
de Ta 49 afos que | %factor de pérdida
viven con VIH, todas de
responsabilidad Ajuste el resultado a la
institucional decena superior.
Pag. 19 atfensn
>
Noreen a
GUI el kan een eee ere
DosIs
cuave vacuna | POBLACION BLANCO cAtcuto POR
cae Esquema | PERDIDA
020.0005810.00 | Toxoides Tetanico | Se considera una dosis | (Poblacién de Safes [OSmL — | 510%
020.000:3810.01 | yaiiterico (Ta) | para ol 100 % de la :
poblacion Safos, més | (Poblaciones de 25,35,
Una desis para el 50 % | 45,55 65.0 x050)
de fa poblacion de 25, :
35, 45, 55 y 65 aos | [Poblaciones de 16, 2,
(refuezo cada 10 | 36,46, 56y66ahosx
aos). Mas una desis 005)
para ol 5% dela *
ppblacion de 16 26,36, | (Poblacion menor de?
4%, 56 y 66 anos] aforx030})
(rezagados), mis una x
dosis para of 30 %6 de | % factorde pérdics
tes mujeres
embarezedas. Todas | Ajuste el resultado aa
de responsabilidad | decena superior
institucional
3265060252600 | Vacuna Se_consideraré una | (Pobladnde20a33_ [Tmt] 530%
Recombinante | dosis parael 5 dela | anos x005)
contra 1a | poblacion de 20 a 39 x
Hepatitis 6 de 20 | aos de | sfactorde péecia
meg responsabilidad
institucional Ajuste el resultado al
ecena superior
€20.0003808.00 | Vacuna de | Se considera ura dose | (Poblacion menords? | OSmt | 55%
020.000.3808.01 | Refuerzo contra | pare el 80 % de las} aorx0.00)
020.000:3008.02 | cifteria,etano= y | embarazadas de x
020.000.3808.03 | tos ferina aceuler | responsabilidad ‘factor de péraida
020.000.3808.04 | (TPs) institucional
Ajuste el resultado a la
ecena superior
020.000.014600 | vacua Se considera uns desis | WPobiacion de lanosx J osm | 510%
antineumacécica | para el 30 % de la 03)
polisacirida | poblacién de 61 afos, +
mas una dosis para el | (Poblaciones de 62, 63,
20 % de la poblacisn | 64, 65366 afos 0.2)
de 62a 66 afos ,
(rezagados}, todas de | —% factor de pérdida
responsabilidad
institucional Ajuste el resultado 3a
decena superior
{020:000;3800.60 | Vacuns Dobie | Se considera una dosis | (Poblacion de 20a39 | OSmL [570%
Viral (SA) contra} para el 5% de ta) anosx0.05)
Sarampién | poblacién de 20 a 39 x
Rubéola ates de | 120 para atenciéna
responsabilidad brotes)
Pag. 20 ith
OGRAMA DE
Ire mecca!
EEE
FACTOR,
clave VACUNA POBLACION BLANCO cALcuLo, POR DE
ESQUEMA | PERDIDA
Tnstitucional, mas ef 20 x
% para atencién de | %factor de pérdida
brotes (bloqueos),
‘Ajuste el resultado a la
decena superior.
{020,000,3825,00 | Vacuna contra Ta | Se considera una dosis | [(Poblacion de un ariox [OSmL | 5%
020.000.3825.01 | Hepatitis A para el 50% de Is 050)
(020.000.3825.02 poblacion de 1 afio de *
020.000.3825.03, edad de | —_{Poblaciones de
020.000.3825.04 responsabilidad 123.4567 y 8 anos x
(020.000.3825.05 institucional, que se 0.05))
(020.000.3825.06 considera asiste a x
(020.000.3825.07 albergues, guarderias | _% factor de pérdida
(020,000.3825.08, © casa cuna. Mas una 7
020.000.3825.09 dosis para el 5% de la | Ajuste el resultado a la
poblaciéndelaBafios | decena superior.
de responsabilidad
institucional,
considarada como
hijos de _jornaleros
agricalas, 7
|920,000.6056.00 | Vacuna contra |Se consideran dos | (Poblaciéndeunaho) [OSmL | 35%
020.000.6056.01 | Varicela dosis para el 50 % de la x
poblacion de 1 ano de | (110 para atencidn a
responsabilidad desastres y pacientes
institucional, que se con cancer)
considera asiste a x
alberques, guarderias | % factor de pérdida
(9 casas cuna, Mas un
10 % adicional para | Ajuste el resultado ala
atencién de desastres | decena superior.
y pacientes con
‘Vaeuna con | Vacunas Se considera una Goss | (Poblacion deSaso | OSmi=™ | SOG0%F
autorizacion de | disponibles en el | para la poblacién de $ afios? x 0.05)
uso de | pais contra la | a $9 aftos que vive con +
‘emergencia covib-19 ‘alguna comorbilidad | (Poblacién de 60 afios y
contra la COVID-
vw!
de tiesgo™; mas una
‘dosis para el 100 % de
la poblacion de 60
afios y més; mas una
dosis para el 100 % de
las personas,
emberazadas (100%
de Ia poblacién menor
de un aho de edad,
mis)
(Poblacién menor de un
aos)
(Personal de salud de
responsabilidad)
si factor de pérdida
o-=
Pag. 21
atten
—=S
ee
GESnca pecans nel eee Oc ieeeeees
CLAVE VACUNA POBLACION BLANCO cALcULO
Tas una dosis para ef
100 % del personal de | Ajuste el resultado a la
salud, todas de | decena superior.
responsabilidad
institucional.
VET CaTEuIb Gls Poblacion Gbjatvs Se Yeaiza Con asa en os grupos blanco de fa Venvaneion, Gn lbd GrunOE Ge HESQGV EN Ts GEPOTDNGAG
‘La vacuna BCC se presenta an rascos ampula de 10 desis, una ver reconstituia, plorde su wablldad después de 6 horas, por fo que, 26
considera un factor de pércida ato,
Se considera como poblacion de riesgo al 5 % de a poblacion de 5. 49 aos
*Se considera la poblacisn de ernbarazadas y mujeres en periode de pucrperi, igual que la poblacion mena de un ato.
* ara ol caso de los hombres cis y trans que viven con VIN sida, pod iniciar © completar os esquemas de vacunacién conforme a la
"lsponiblial dela vacuna en el nivel stata, dalegacianalfuracielonal yf loca
"se consira ala poblacion de ninas adolescentes come la poblacion total por grupo de edad entre dos.
"Bara 2024, se consiserars come factor de perdia ol $0 al 90%, toda vez que se eat realizando el andleis prospective reepectoal promedio
e factor de percida, considerando que las presentaciones disponibles en México, ze encuentra en frase mulkidosis, asso, a vida i
varia de 2 hasta ¥6 horas, una ver abiert el asco,
‘As fecha de publicacion del presente linearniento las vacunas deponibies contra la COVID:%9 en México se encantraban bajo of uso de
‘omergencia, sin embargo, esto puede modifica‘ en el ranscurso de 2024 y contar con vacuras que estén bajo resbtro sanitaio emitido
For la Instancia rgulatoria en el pais, COFEPRIS. Aaicicnalmente, of pasade 29 do teptiemore de 2025, 22 lew a cabo la primer y ica
Sesion ordinaria del Consejo Nacional de Vacunacién {CONAVA), donde se emité el siguiente acuerdo: “Acuerdo OLCONAVA 202% El
Consejo Nacionalde Vacunacién considera viable laincorporacion dea vacuna contra COVID-19al Programa de Vacunacion Universal (PV)
«partir del ejerciclo 2024, por lo que la Secretaria de Salud, determinara su integracion en términos del Anicua 157 bis de la Ley General
do Salud Finalmente, esto apicara una vez que se realice Ia transicign mediante los proceso: acministratwos necesarios para su
Incorporacton al PYU Plan de Gestion a largo plaza integracion a la Lay General do Salus entte otros que considere necesaris a Secretaria
se Satu,
% Poblacion objetivo y de riesgo para la aplcacién de la vacunsa contra la COVID-18: Adultos de 60 aos y mas, personas ernbarazadas,
personal de salud, Personas que ven con Diabetes Melitus Cardiopatias agudas 0 erénicas, Cancer e Hipertensién Arteria. Enfermedad
pulmonar Obstructiva Cronica (EOC) asma, Insuflciencia nal Crénie (IC), Infeccion poral Vitus dela Inmunodefciencia Humana Vl}
1y manifestacionesclnicas del Sindrome ce Inrmunodiefciencia Adquirica (sia), Obesidad morbida para nina rinos a partir do los Safes
‘do edad adolescentes y adultos.
‘+ Sujto a a] vacuna 6) disponible [6 enel pais
6.2 PROGRAMA PERMANENTE DE VACUNACION (PPV)
Las actividades permanentes de vacunacién son acciones que se desarrollan de
manera intramuros en la red de servicios de salud, y extramuros a través de la
instalacién de puestos de vacunacién en lugares estratégicos de la comunidad y con
brigadas que realizan visitas casa a casa. Las actividades se realizan durante todo el
aio en los servicios de primer, segundo y tercer nivel de atencién en las instituciones
poblacionales especificas: nifias y nifios menores de un afio, un afio de edad, 4 afios y
Gajios de edad, para la administracién oportuna de las vacunas, asf como la planeacion
del SNS que cuentan con servicios de vacunacién.
El esquema de vacunacién tiene a su grupo blanco estratificado en sary \
y adecuacién de esquemas emergentes en caso necesario, facilitando se completen
los esquemas de acuerdo con el grupo de edad especifico, lo que ne significa que se L y
Pag. 22 aah Tcensu 4
dejen de iniciar 0 completar esquemas en otros grupos con rezago de vacunacién,
en los que técnicamente pueda hacerse.
6.3 LINEAMIENTOS DE APLICACION
6.4 PROGRAMACION DE ACTIVIDADES
Con el propésito de alcanzar y mantener coberturas de vacunacién 295% por biolégico
y 290 % de promedio de cobertura de vacunacién en el esquema completo para nihas
y nifios menores de un aio de edad, al afio, a los 4 y a los 6 aftos de edad, las
instituciones realizaran las actividades necesarias en las unidades de salud, incluyendo
las hospitalarias, ademas de otras actividades intramuros y extramuros de acuerdo
con su poblacién de responsabilidad institucional.
Toda vacuna administrada debe ser registrada en |e Cartilla Nacional de Salud (CNS), ee
Censo Nominal y formatos administrativos y/o nominales de dosis aplicadas que
cada institucién determine, con los datos que especifique el Manual de Vacunacin
vigente y los Lineamientos de operacién del programa vigentes.
En la CNS, ademas de anotar la fecha de aplicacién de la vacuna administrada, se
registrara la unidad de salud vacunadora, el numero de lote y la caducidad del
biolégico administrado. Preferentemente, con ldpiz, se anotara la fecha de la proxima
dosis @ aplicar del esquema, como un recordatorio a |a madre o tutor del menor
respecto del calendario de vacunacion.
6.5 REDDEFRIO
La red o cadena de frio es un proceso logistico que asegura la correcta conservacién,
almacenamiento y transporte de las vacunas; desde el lugar de fabricacién, hasta el y
sitio de aplicacién a la poblacién, manteniendo asf su potencia inmunogénica.
Para garantizar la conservacién de las vacunas, es necesario que ninguno de los
eslabones de la cadena de frio se vea afectado, para ello se deberan almacenar en
condiciones éptirnas, manteniéndolas bajo vigilancia y monitoreo continuo respecto
ala temperatura, tiempo de almacenamiento, caducidad, exposicién a radiacién solar
‘© luminosa directa, humedad 0 cualquier forma de contaminaci6n, entre otros [ver
especificaciones del Manual de Vacunaci6n vigente).
Los niveles de la cadena de frio tienen como funcién almacenar, conservar y jy
transportar los productos biolégicos hasta su aplicacién a la poblacién. El numero de
niveles depende de las condiciones geograficas, la organizacién de las instituciones y
el volumen de vacunas que se requiera almacenar. Se consideran los siguientes
niveles: nacional, estatal, delegacional/distrital/jurisdiccional, coordinacién médica,
regional o municipal y el nivel local o zonal (unidad médica o brigada de vacunacion,
Pag. 23 atresia
—
NY
aplicativo); cada institucién determinara, de acuerdo con su organizacién, a qué nivel
corresponde el sitio donde se almacenen y conserven los biolégicos, debiendo
asegurar la capacidad de almacenamiento de los insumnos de acuerdo con la demanda
programada para el ejercicio presupuestal 2024.
6.4.1 ALMACENAMIENTO.
En todos los niveles operativos donde se realice almacenamiento bajo condiciones
de refrigeracién, asimismo, y durante su traslado, las vacunas deberan
conservarse en un rango de temperatura +2°C a +8°C.
El tiempo maximo de almacenamiento de los biolégicos depende de cada nivel en
que se encuentren (sin ser acumulativo entre los niveles)
Nivel nacional: hasta su fecha de caducidad.
Nivel estatal o delegacional: 9 meses.
Nivel delegacional/distrital/jurisdiccional, regional y/o municipal: 4 meses.
Nivel local 0 zonal: 3 meses.
ROUND
Si el periodo de almacenamiento de los biolégicos en alguno de los niveles ha
superado el tiempo establecido previamente y cuenta caducidad vigente, debera
solicitar al CENSIA, la anuencia de permanencia por un periodo adicional, siempre y
cuando existan registros de temperatura que sustenten que se ha conservado en un
rango de +2°C a #8°C y se implementen las estrategias necesarias para su distribucion
y aplicacién antes de su fecha de expiracién, considerando que si existe una
reincidencia en la solicitud de anuencias, deberé otorgar al CENSIA una justificaci6n
técnica del retraso en su aplicacién, toda vez que, las vacunas distribuidas
corresponden al ejercicio presupuestal del afio en curso, asimismo, las metas
establecidas de aplicacién a la poblaci6n objetivo de cada vacuna de manera mensual
© bien los logros estimados durante las campaiias intensivas de vacunacién. \
Ses at
las solicitudes de anuencia. se deberan enviar. al_—correo
censiareddefrio@salud.gob.mx (correo electrénico oficial de Red de Frio del CENSIA).
Una vez recibida la solicitud, se confirmara de recibido y se asignaré un numero dex /
folio para su trazabilidad y pronunciamiento por el CENSIA.
wee
6.4.2 ACCIDENTES DE RED DE FRI (ARF)
Un ARF ocurre cuando las vacunas han salido de los parémetros normados
(refrigeracién, congelacién y en su caso ultracongelacién) por el motivo que sea, si esto
ocurre, se procedera a realizar las siguientes acciones establecidas en el Manual de
Vacunacién vigente:
Fs a
Pag. 24 aa ET CENA
Naso
* Elaboraci6n del acta circunstanciada (Consultar Anexos del Manual de Vacunacion
2021 en 7 mx/salu' ia/documentos/formatos-de|-manual-de-
yvacunacion), misma que deberd enviarse al correo electrénico oficial de Red de Frio
de manera inmediata y oportuna en un lapso no mayor a 5 dias habiles, a partir
de su recepcion en el nivel estatal, a fin de optimizar los tiempos para su
dictaminacién por el Grupo Técnico de Accidentes de Red de Frio (GTARF}, con el
‘objetivo de conservar el mayor ntimero de dosis para su aplicaci6n.
* Una vez notificado el accidente a este Centro Nacional, se confirmara de recibido y
se asignara un numero de folio a cada ARF para su trazabilidad,
* EIGTARF serd el encargado de realizar el dictamen de los bioldgicos afectados.
«Finalmente, el CENSIA notificara mediante los canales de comunicacién oficiales el
dictamen de las vacunas. Nota: Para el caso del IMSS, la notificacién de los ARF
deberd seguir curso similar especificado en su normatividad vigente, al contar con
estructura organica responsable de esta funcién.
Para saber mas sobre este proceso, consulte el Manual de Vacunacién vigente.
6.6 POLITICA DE FRASCOS ABIERTOS
Todos los frascos abiertos de vacunas liquidas de presentacién multidosis como
DPT, Ta, anti influenza, anti hepatitis B y anti neumocécica conjugada, usados
dentro de las unidades de salud y en los puestos méviles de vacunacion, podran
/
ser utilizados hasta 28 dias después de abierto el frasco, siempre y cuando la
fecha de caducidad no haya expirado, se hayan almacenado y transportado
dentro de los pardmetros de temperatura normados (+2°C a +8 °C) y se hayan
manipulado con buenas practicas asépticas, siendo indispensable el registro en la
etiqueta del frasco, la fecha y hora de apertura de las vacunas.
\
Las vaeunas liofilizadas como BCG sepa Moscow (vacuna distribuida actualmente
en México), SR y SRP, podrén ser utilizadas hasta 6 horas después de haber sido
reconstituido el vial o al finalizar Ia jornada de trabajo, lo que ocurra primero.
Excepto la vacuna BCG cepa Tokio, la cual podra ser utilizada Unicamente 4 horas
después de ser reconstituida, al término de las cuales, debera ser desechada. Lo
anterior porque [a estabilidad térmica de las vacunas liofilizadas disminuye
considerablemente cuando se reconstituyen con su diluyente, 0 cuando son
expuestas a la radiaci6n ultravioleta.
4
Respecto a las vacunas disponibles en México contra la COVID-19, a Ia fecha y A
derivado del soporte técnico y bibliogrdfico, no podré utilizarse la politica de f YY
fences ablertor en ninguna de las distintas plataformas, por lo que, deberd |
consultarse Ia vida util de cada una. ¥
Pag. 25 atten 4
PG
ae
aN
Las acciones que se deben considerar en los frascos abiertos multidosis, son las
siguientes:
+ Utilizar antes de la fecha de vencimiento.
+ Escribir en el frasco la fecha y hora de apertura.
+ Almacenar y transportar entre +2°C y +8°C.
+ Manipular con buenas practicas asépticas.
Y poner atencién en:
+ No utilizar la vacuna si se identifica 0 se sospecha que el tapén del frasco fue
sumergido en agua del deshielo de los paquetes refrigerantes, o la etiqueta se
encuentra mojada © desprendida (independientemente si se trata de frasco
abierto o cerrado).
+ Prohibido el uso de aguja piloto (aguja introducida en el tapén del frasco para la
extraccién de varias dosis de vacuna de forma subsecuente), ya que aumenta el
riesgo de contaminacién de la vacuna
+ Lasjeringas se preparan con la vacuna sdlo antes de la administracién de la misma,
por lo que, no se deben precargar las jeringas con la vacuna sino se va a aplicar de
forma inmediata. No es adecuado precargar las dosis dias u horas antes de iniciar
los procedimientos de vacunacién, ya que se puede contribuir a fa reduccion
potencial de la efectividad de la vacuna, fomenta la mala praxis y permite el posible
desarrollo de microorganismos en las jeringas con vacunas precargadas.
Al terminar las actividades de campo, las vacunas en frascos cerrados multidosi
(liofilizadas 0 liquidas) que se hayan conservado todo el tiempo a la temperatura
normativa (entre +2 °C y +8 °C), podrdn ser utilizadas, siempre y cuando no haya
expirado la fecha de caducidad. Las vacunas en frascos cerrados unidosis deberan
utilizarse una vez abiertas, ya sea dentro de las unidades de salud 0 en campo; si por
alguna causa no se utilizan, y las condiciones de almacenamiento/transporte
fueron las adecuadas, deberdn ser devueltas al refrigerador destinado a su
conservacién en la unidad de salud, siempre respetando el tiempo maximo
permitido para su utilizacién, una vez abiertos.
En los casos de sospecha de contaminacién del biolégico en frascos previamente
abiertos, expuestos a congelamiento o que exceda la vigencia de su uso con relacién
a la fecha de apertura de los frascos; los productos biolégicos deben darse de baja,
inactivarse y desecharse; ademas, de realizarse las acciones correspondientes para su
Rotificacién al CENSIA, conforme a lo descrito en el Manual de Vacunacién vigente.
Para el caso de vacunas contra la COVID-19 se deberé realizar el desecho conforme lo
establecido en las Gufas técnicas de aplicacién de los diversos biolégicos.
Al ser una actividad operativa, el resguardo de las actas de inactivacién quedara
bajo resguardo del nivel estatal, delegacional/distrital/jurisdiccional y/o local.
Pag. 26 Lan bens
\
on
Ns
VA
Para evitar pérdidas en la operacion y un desperdicio que genere desabasto en la
unidad de salud se deber realizar una planeacién adecuada de las actividades de
vacunacién extramuros.
6.7 MANEIO DE RESIDUOS PELIGROSOS BIOLOGICO INFECCIOSOS (RPBI)
La eliminacién de RPBI esta regulada por la Ley General del Equilibrio Ecolégico y la
Proteccién al Ambiente, Ley General para la Prevencién y Gestion Integral de los
Residuos, las Normas Oficiales Mexicanas: NOM-098-SEMARNAT-2002, Proteccion
ambiental-Incineracion de residuos, especificaciones de operacién limites de
emisién de contaminantes; NOM-052-SEMARNAT-2005, Que establece las
caracteristicas, el procedimiento de identificaci6n, clasificacién y los listados de los
residuos peligrosos, y la NOM-087-ECOL-SSAI-2002, Proteccién ambiental - salud
ambiental - residuos peligrosos biolégico-infecciosos - clasificacién y especificaciones
de manejo, 0 las que las sustituyan.
Aunque la normatividad no es especifica para vacunacién, se consideraron los criterios
generales de las mismas, por lo que, la eliminacién de los RPBI debe cumplir con las
disposiciones correspondientes a las siguientes fases de manejo (ver cuadro 3}:
a) Identificacién de los residuos.
b) Envasado de los residuos generados.
c} Almacenamiento temporal.
d) Recoleccién y transporte externo.
e) Tratamiento.
f) Disposicién final
rr RCo nee Cen ha
pees eee hee eee Mec
Tipoderesiduo L
‘Agujas ylo jeringas prellenadas.
Reciniente rigido de
Pea Rojo | Empresa autorizada
Jeringas usedas para Ta aplicacion de
vvacunas virales 0 bacterianas atenuadas*. | Bolsa de polietiieno | Roja | Empresa autorizada
Torundas empapadas de sangre.
TTorundas con sangre seca o manchadas de
sangre, fundas protectoras de la aguja y
envoltura.
Frascos de vacunas inactivadas 0
recombinantes, asi como jeringas usadas
para la aplicacion de éstas.
Frascos de vacunas virales © bacterianas
atenuades*, que previamente hayan sido | Bolsadepolietiino | | Basurero municipal
sometidas a proceso de inactivacién.
uacuas Tipe Wal SAP, dobre val SR. anti verse, GCG, Conta Fisbre amavis y ose VaCUnARRTanaadaS,
Se colocard en bolas de cualquier col, excepto roja o ama
Bolsa de polietileno | | Basurero municipal
Pag. 27 arene
a
Wy
La Norma Oficial Mexicana NOM-087-ECOL-SSAI-2002 considera como RPBI a los
utensilios desechables usados para contener, transferir, inocular y mezclar cultivos de
agentes biolégicos-infecciosos, por lo tanto, las jeringas usadas de vacunas atenuadas
se deben desechar en bolsa roja. Los recipientes de los residuos peligrosos para
punzocortantes y las bolsas rojas deben cumplir con las especificaciones indicadas en
la NOM-087-ECOL-SSAI-2002.
6.7.1 ALMACENAMIENTO TEMPORAL
Se debera destinar un area para el almacenamiento temporal de! RPBI, excepto en los
establecimientos de nivel I, los cuales podrdnn ubicar los contenedores en el lugar mas
apropiado dentro de sus instalaciones, cuidando que no obstruya las vias de acceso y
que no se encuentre en contacto con el personal ni can la poblacién.
El periodo de almacenamiento temporal esté sujeto al tipo de establecimiento
generador
a) Nivel I: Maximo 30 dias
) Nivel Il: Maximo 15 fas.
¢) Nivel Ill: Maximo 7 dias.
\
0
4
6.7.2 RECOLECCION Y TRANSPORTE EXTERNO DE LOS RPBI a »
Para la recoleccion y transporte de RPBI se requiere la autorizaci6n por parte de la
Secretaria del Medio Ambiente y Recursos Naturales (SEMARNAT). Dicho transporte
debe cumplir con lo siguiente:
+ Sdlo podra recolectarse los RPBI que cumplan con el envasado, embalado y
etiquetado de acuerdo con la NOM-087-ECOL-SSAI-2002.
+ Los RPBI no deben ser compactados durante su recoleccién y transporte.
+ Los vehicules recolectores deben ser de caja cerrada y hermética, contar con
sistema de captacién de escurrimientos, y operar con un sistema de enfriamiento
para mantener los residuos a una temperatura de 4 °C.
+ Durante el transporte, los RPBI sin tratamiento no deberan mezclarse con ningtin
otro tipo de residue municipal o de origen indust
NX
\
\
SEL eee. soca cates sre nc eneaecomean eae
SBT ano con co cotton epee na Se
Neen ee ea ee a ee
SITS a ann nc
ES carpe sara ct ec poe er ces
scutes
Pag. 28 athe
eee
y
6.7.3 DISPOSICION FINAL
Los RPBI tratados e irreconocibles, podran disponerse como residuos no peligrosos en
sitios autorizados por la autoridad competente.
6.73.1 CONSIDERACIONES SOBRE EL USO DE CAJAS RECOLECTORAS EN LAS
‘CAMPANAS DE VACUNACION
Las “cajas de carton incineradoras de agujas" o "cajas recolectoras incinerables con
Jeringas", anteriormente tuvieron como finalidad servir como contenedor de los RPBI
Puncocortantes para llevar a cabo la incineracién de los mismos; sin embargo, la caja
recolectora incinerable con jeringas est elaborada con cartén con un forro interior de
aluminio, por lo que, ne cumple con las especificaciones que marca la Norma Oficial
Mexicana NOM-087-ECOL-SSA1-2002 para los recipientes de los residuos peligrosos
punzocortantes; por lo tanto, no se deben usar para tal fin,
Adicionalmente, con las cajas de cartén es poco factible que se Ileve a cabo el
tratamiento de incineracién, ya que, si bien estas contienen un bote con alcohol s6lido
y cerillos para incineracién, éste no genera las condiciones de combustién
(temperatura, tiempos de retencién y turbulencia) requeridos para realizar la
incineraci6n; ademas, de no contar con los dispositives de control de temperatura, de
composicién de gases, ni tolvas para la captacién de cenizas, por lo que, no pueden
ser consideradas como un incinerador,
6.8 SEGURIDAD Y VACUNACION
Las practicas de inyeccién segura incluyen no causar dafo al paciente, al trabajador
de salud, a la comunidad, nial ambiente,
Se debe cumplir con los procedimientos normalizados para el transporte,
almacenamiento, distribucién, conservacién, manipulacién, _reconstitucién,
administracién y eliminacién de cada una de las vacunas e insurnos involucrados en
el PVU. Con el fin de tener riesgos minimos en la vacunacién o inmunizacién de la
poblacién, se deberdn seguir las practicas seguras de vacunacién
6.8.1.1 SEGURIDAD EN LAADMINISTRACION L
+ Realizar la técnica de higiene de manos con agua y jabén o soluciones alcoholadas
antes y después de cada procedimiento respetando los 5 momentos de higiene de
manos.
* Revisar indicaciones, contraindicaciones y precauciones [ver Manual de
Vacunacion y Manual de procedimientos estandarizados para la vigilancia
epidemiolégica de Eventos Supuestamente Atribuibles @ la Vacunacién o
Inmunizacién (ESAVI}, vigentes), asi como, realizar una anamnesis previa a la
vacunacién,
Pég.29 ies
———
0
x
}
a8
a
:
le
E VACUNACION UNIVER
+ Verificar la viabilidad de los insumos previo a su administracién, mostrar al usuario
(madre, padre o responsable del cuidado de la nifia, nifio 0 adolescent) la jeringa
© aguja, e informar que es nueva y de uso Unico para la persona a la que se le
aplicara la vacuna, adicionalmente, se debera leer en voz alta la fecha de caducidad
impresa en el empaque, asi como abrirlo frente al usuario.
+ Revisar el nombre en la etiqueta del frasco, mostrar al usuario, leer en voz alta el
nombre de la vacuna y la enfermedad (s) que previene.
+ Revisar la fecha de caducidad de la vacuna, leer en voz alta la fecha de caducidad,
nombre del laboratorio, en caso de frascos multidosis leer la fecha y hora de
apertura.
* Cuando aplique, realizar una adecuada reconstituci6n, utilizando el diluyente
especifico.
+ Utilizar la misma aguja para realizar la carga del bioldgico y la aplicacién de
éste, queda prohibido el uso de agujas “piloto”.
« Extraer la cantidad indicada de dosis a aplicar, sin excedentes.
+ Técnica de administraci6n: verificar que sea la dosis correcta para la edad, el
intervalo correcto de aplicacién entre dosis, la via correcta (parenteral uoral),el sitio
de aplicacién correcto y los insumos adecuados (agujas, jeringas y diluyentes). Ver
cuadro 4.
« Identificar correctamente al paciente antes de la aplicacion de la vacuna (5)
| Mantener las vacunas en condiciones normativas de temperatura en todo
momento, verificar que antes dle iniciar la jornada de trabajo los termometros de
vastago estén calibrados.
+ Verificar la limpieza y descontaminacién del puesto de vacunacién (mesa, termo,
contenedores de agujas y jeringas) al inicio de cada jornada laboral en la unidad de
salud y en actividades de campo.
+ No re-encapuchar las agujas.
+ Desechar acorde a la politica de frascos abiertos
+ Eliminacion segura de RPBI,
* No cargar jeringas antes de su uso.
© Queda prohibido el uso de aguja piloto.
Intramuscular
Anti Hepatitis B
Hexavalente acelular
(OPaT-VIP-HB-Hib)
“Anti neumocselca conjugads
DPT
Ta
Tapa
‘Anti VHT
Anil influenza
‘Anti hepatitis A
‘Anti neumooscica pollsacsrida
COVIDS
Sitio anatémicos de aplicacién de vacunas.
‘Vias de administracién de vacunas.
‘Subeutanea intrad@rmica | Oral
SRP BCG “Anti rotavirus
SR
‘Anti varicela
El lado anatémico (izquierdo 0 derecho) dependera de cada vacuna, en nifas y nifios menores de 18.
meses de edad la administracién es en el tercio medio de la cara anterolateral externa del muslo; 2
partir de los 18 mases de edad en la region deltoidea det brazo.
Rotavirus (VO) a
BCG (10),
Hexavalente Acelular (IM) <
Anti Neumocescica (IM)
“Izquierda
DPT (iM)
‘SRP (SC)
+ Anti Influenza >18 meses (iM)
‘Anti Hepatitis B (IM)
“Anti Influenza (M) 4
Vo: via oral
1: ntradérmi
IM intramuscular
Sc: Subcuténea
Pég. 31
Hexavalente Acelular refuerzo (iv) wp \
Viade ers eae =
‘VWacunass [Eee Media de a agua ' Jeringas
BCG intradermica | 27Gxis mm osm"
‘Anti Intramuscular | Recién nacidos: 250 x16 mm os mt
25% en nifios menores de 5
afios; yen mayores de § afios que tengan un recuento de CD4 2200 célulss)
* La realizacién del PPD en personas inmunocomprometidas (recién nacides con
desnutricién, que viven con VIH, etc.) con o sin antecedente de BCG se debe realizar
de acuerdo con lo establecido en la NOM-006-SSA2-2013, para la prevencién y
control de tuberculosis; con el fin de detectar tuberculosis latente y decidir si se
requiere tratamiento inmediato para infeccisn 0 enfermedad,
‘+ Las instituciones a nivel estatal/delegacional y jurisdiccional, deberan coordinarse
a fin de abastecer vacuna 8CG en el 100 % de las unidades médicas de atencién
eg _—
N
ae _.
7
y
|
h
‘
\
-
You might also like
- Her Body and Other Parties: StoriesFrom EverandHer Body and Other Parties: StoriesRating: 4 out of 5 stars4/5 (822)
- A Heartbreaking Work Of Staggering Genius: A Memoir Based on a True StoryFrom EverandA Heartbreaking Work Of Staggering Genius: A Memoir Based on a True StoryRating: 3.5 out of 5 stars3.5/5 (231)
- Devil in the Grove: Thurgood Marshall, the Groveland Boys, and the Dawn of a New AmericaFrom EverandDevil in the Grove: Thurgood Marshall, the Groveland Boys, and the Dawn of a New AmericaRating: 4.5 out of 5 stars4.5/5 (266)
- The Sympathizer: A Novel (Pulitzer Prize for Fiction)From EverandThe Sympathizer: A Novel (Pulitzer Prize for Fiction)Rating: 4.5 out of 5 stars4.5/5 (122)
- The Little Book of Hygge: Danish Secrets to Happy LivingFrom EverandThe Little Book of Hygge: Danish Secrets to Happy LivingRating: 3.5 out of 5 stars3.5/5 (401)
- On Fire: The (Burning) Case for a Green New DealFrom EverandOn Fire: The (Burning) Case for a Green New DealRating: 4 out of 5 stars4/5 (74)
- Team of Rivals: The Political Genius of Abraham LincolnFrom EverandTeam of Rivals: The Political Genius of Abraham LincolnRating: 4.5 out of 5 stars4.5/5 (234)
- Elon Musk: Tesla, SpaceX, and the Quest for a Fantastic FutureFrom EverandElon Musk: Tesla, SpaceX, and the Quest for a Fantastic FutureRating: 4.5 out of 5 stars4.5/5 (474)
- The Unwinding: An Inner History of the New AmericaFrom EverandThe Unwinding: An Inner History of the New AmericaRating: 4 out of 5 stars4/5 (45)
- Hidden Figures: The American Dream and the Untold Story of the Black Women Mathematicians Who Helped Win the Space RaceFrom EverandHidden Figures: The American Dream and the Untold Story of the Black Women Mathematicians Who Helped Win the Space RaceRating: 4 out of 5 stars4/5 (897)
- The World Is Flat 3.0: A Brief History of the Twenty-first CenturyFrom EverandThe World Is Flat 3.0: A Brief History of the Twenty-first CenturyRating: 3.5 out of 5 stars3.5/5 (2259)
- The Emperor of All Maladies: A Biography of CancerFrom EverandThe Emperor of All Maladies: A Biography of CancerRating: 4.5 out of 5 stars4.5/5 (271)
- Shoe Dog: A Memoir by the Creator of NikeFrom EverandShoe Dog: A Memoir by the Creator of NikeRating: 4.5 out of 5 stars4.5/5 (540)
- Grit: The Power of Passion and PerseveranceFrom EverandGrit: The Power of Passion and PerseveranceRating: 4 out of 5 stars4/5 (590)
- The Yellow House: A Memoir (2019 National Book Award Winner)From EverandThe Yellow House: A Memoir (2019 National Book Award Winner)Rating: 4 out of 5 stars4/5 (98)
- The Subtle Art of Not Giving a F*ck: A Counterintuitive Approach to Living a Good LifeFrom EverandThe Subtle Art of Not Giving a F*ck: A Counterintuitive Approach to Living a Good LifeRating: 4 out of 5 stars4/5 (5813)
- The Hard Thing About Hard Things: Building a Business When There Are No Easy AnswersFrom EverandThe Hard Thing About Hard Things: Building a Business When There Are No Easy AnswersRating: 4.5 out of 5 stars4.5/5 (348)
- The Gifts of Imperfection: Let Go of Who You Think You're Supposed to Be and Embrace Who You AreFrom EverandThe Gifts of Imperfection: Let Go of Who You Think You're Supposed to Be and Embrace Who You AreRating: 4 out of 5 stars4/5 (1092)
- Diagrama de Instalación de Sonda VesicalDocument2 pagesDiagrama de Instalación de Sonda VesicalIsaac Alejandro Castro Ramírez50% (2)
- Never Split the Difference: Negotiating As If Your Life Depended On ItFrom EverandNever Split the Difference: Negotiating As If Your Life Depended On ItRating: 4.5 out of 5 stars4.5/5 (844)
- Caso Clinico Del EstresDocument18 pagesCaso Clinico Del EstresIsaac Alejandro Castro RamírezNo ratings yet
- Herpes GenitalDocument4 pagesHerpes GenitalIsaac Alejandro Castro RamírezNo ratings yet
- Faringitis y Amigdalitis EstreptocócicasDocument4 pagesFaringitis y Amigdalitis EstreptocócicasIsaac Alejandro Castro RamírezNo ratings yet
- Hildegard Peplau 231007 092748Document32 pagesHildegard Peplau 231007 092748Isaac Alejandro Castro RamírezNo ratings yet
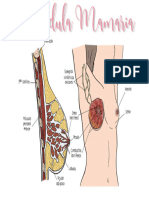
- Glandula MamariaDocument1 pageGlandula MamariaIsaac Alejandro Castro RamírezNo ratings yet
- Lineamientos Generales Del Pvu 2024Document64 pagesLineamientos Generales Del Pvu 2024Isaac Alejandro Castro RamírezNo ratings yet
- Infografía Salud Mental Orgánico Creativo Rosado y Blanco - 20240110 - 185432 - 0000Document1 pageInfografía Salud Mental Orgánico Creativo Rosado y Blanco - 20240110 - 185432 - 0000Isaac Alejandro Castro RamírezNo ratings yet
- Ilovepdf - Merged (4) - RemovedDocument26 pagesIlovepdf - Merged (4) - RemovedIsaac Alejandro Castro RamírezNo ratings yet