Professional Documents
Culture Documents
Cinetică
Cinetică
Uploaded by
Diana Valentina0 ratings0% found this document useful (0 votes)
2 views15 pagesCopyright
© © All Rights Reserved
Available Formats
PDF or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as PDF or read online from Scribd
0 ratings0% found this document useful (0 votes)
2 views15 pagesCinetică
Cinetică
Uploaded by
Diana ValentinaCopyright:
© All Rights Reserved
Available Formats
Download as PDF or read online from Scribd
You are on page 1of 15
“Cineticit ~ Lucrari practice”
> UPA TEMPERATE
ASUPRA UTE
ox nanems
Seoprll luernfi
Determinarea experimentalii a varia
reacfie funcjie de temperatur’.
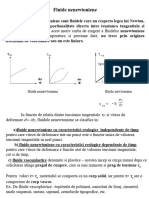
Consideratil teonaties
Primele cercetiri de cinetict chimici au
aritat cA prin cresterea temperaturii se miireste in
mod considerabil viteza de reactie.
Svante Arrhenius a gisit in 1885 0 relafie
empiricd care exprima dependenta constantei de
viteza de temperaturi:
i vitezei de
B
Igk =1g A-—
Be A-F oy
in care A si B sunt constante empitice iar T este
temperatura.
Deoarece aceasti ecuajie empiric este
Scanned with CamScanner
verificat’ de experienfi s-a pus problema gisiri
tei interpretii teortce, care si permité alarea
prin calcul aconsaatelor AsiB.
a prima ineerare de a da ecuafiet i
Arrhenius (8) o interpretae teoretica s-a pomit de
4s aseminarea ei eu izobara de racic a
Hott 9):
o
Deoarece constanta de ecilitey
Vitec arose de gf So constate as
"ant Hoff emai poate series PM obra
dink, 4,
at “Ret! (10) gi
tink, | Hy
aT Rett (yy
unde I - constant
Considerind I= 00m aves reli:
“Cinetcd— Luerde practice”
BBE ay
Rr RT
B
2 as
a)
core prin integra cone
a
Bay ceact 0)
a a- Ee am koAeF
k= ase
its si factor
Constanta de integrre A, mami i
de frecventh sau factor preexponenfial no Jenin
Ge concentra ee apne independent
tempera.
Scanned with CamScanner
“Cinetict — Lueritri practice”
Iilod dle lena
in 5 eprubete se introduc cate 5 mL solutie
KL. fn alte 5 eprubete se introduc cfte 5 mL solujie
apa oxigenati gi citeva piciituri de amidon.
Cele 10 eprubete se introduc in baia de apa
sise fixeaz’ termometrul. CAnd temperatura a ajuns
la 20°C, se amesteca solufiile de KI cu H,O2. Se
repeti operatia pentru temperaturi de 30°C, 40°C,
50°C si 60°C.
Se cronometreazA timpul pand la aparifia
culorii albastre.
Callculul gi intenpretarea reaulttattelor
1. Se noteazi pentru fiecare experiment
temperatura Ia care s-a lucrat si timpul pind la
aparifia culorii albastre
2. Se calculeazi viteza de reacfie cu ajutorul
. 1
relafiei: v= i ©
3. Se traseazi graficul dependenjei vitezei de
reactie de temperatura.
27
Scanned with CamScanner
“Cineticd ~ Lueriri practice”
” iENpA CoNeEIMRATIa
ASUPRA UNTZEE
OR RBACTIE
Scopul lucrérii
Determinarea vitezei de reacfie a sistemului_ apd
oxigenati-ioduri de potasiu pentru diferite
concentrafii de reactant.
Consideratil taonatics
Viteza de reactie in analogie cu definifia
vitezei din mecanict, reprezint& variafia cantitijii
de substan in unitatea de timp.
Cantitatea de substanfi se exprim’, de
obicei in numir de moli, care este o mirime
‘extensivi. De aceea, se obisnuieste 8% se raporteze
numérul de moli transformafi la unitatea de volum
fa sistemului, cfnd viteza de reactie devine 0
mirime intensivi, independent de dimensiunile
Ristemului, Deci, viteza de reactie se poate defini
astfel:
Scanned with CamScanner
1
rah
© ss foloseste pent reactan, iar (+) petra
rodusi de racic. . =
acd se Inread int-un sister cu vo!
constan, “se pose tnoeui raporal m/V ot
concentra $i expresia vtec de react devie:
&,
ey @
Se ober cea itz deine $i
indcele stoeciomec al component din
‘ecuafia chimicd. De aceea, uneori, este indicat si se
‘inlocuiasc’ concentrajia sau numarul de moli, cu 0
aki varbilt de rece, independent de
coefciental stoecionet, mumittsvansrca
react, variabils notath co X
fotructt X are aceeasi valoare pent toi
reactanjil, viteza de reacfic va avea 0 semnificaie
‘nil pentru toi component:
vod ae
re
“Chnetics—Lucripractce”™
0 ait varisbl ae pou utiliza pects
eine vier de reat exe gral de converse, x
x
FOE ce Gi X, este totam poaitv
exprimi avanarea_reacfci, prin concentaia
‘mento port oka c
cronometra
KIQIM
0.3%
samidon
ltd de lnera
4) Se hucreazh In concentra varbile de KI
conform tabeluli a:
Scanned with CamScanner
“Cine Lucril practice”
Se reitese in & cpr wile de HO; de
Aerts concer. Se nigh in are in cee
‘prubcte cite | mL sola amidon Pes conta
flecitei rite se tort ele 5 mi. shape KI,
Gonometindose tinged seus pink bs aria
Caleta st tatargratarea rancitataler
1 Secaleuleartvieza de reat wild relia
EO; sicte 1 sole de ito.
Pete ski de KI prepara anterior toa
te $m de HO; $i se coments interval de
tip pi le aprifia colrt abste cae indich
prezejs ion der a mel de eae.
8) Se Iucreazt ix concemaii variable de Hi02
4
Scanned with CamScanner
Ak asnspIn a Gono!
Seopuil inert «=| AAS PNHIIED
Determinarea timpului de injumatatire al reactiei de hidroliza a aspirinei
Considaratil teoretice
Analiza cineticd a reactiei pe care o poate suferi un medicament in solutie apoasi
poate servi la stabilirea unor criterii obiective pentru aprecierea stabilitatii sale, in solutie, 1a
© anumitd temperatura.
Un astfel de criteriu il constituie timpul de injumatitire, adici timpul in care
Jumatate din cantitatea initiala de component limitativ s-a transformat. Pentru substantele
care sufera procese de degradare chimica cu viteza relativ mare, timpul de injumatatire poate
fi apreciat pe cale empiricd prin determindiri cantitative la diferite intervale de timp. Analiza
cineticd a procesului ofera posibilitatea determina prin calcul a timpul de injumatatire, att
pentru substanfele care se descompun, cu o vitezi mare, cat si pentru cele care se
descompun cu vitezd mica.
Daca procesul urmeaza o cinetica de ordinul I, inlocuind in expresia constantei de
vitezA pe x prin a/2 se obtine:
Rezulta e4, pentru substanfele care la descompunere urmeaza o cinetica de ordinl I,
timpul de injumatafire poate fi calculat cunoscénd constanta de vitezi\ a procesului.
Dacd o substanta medicamentoast sufetdi un proces degradativ dupa o cinetica de
ordinul II, nlocuind in expresia constantei de vitezA pe x cu a/2 se obtine:
1
ke
(57)
; (58)
In solutia apoasd aspirina suferd reactia de hidrolizt,
Scanned with CamScanner
de vedere cintic
Aces reactie este de pul pseudomolecuar,corespunzitor din punct de Neuse Ce
mesa ce ae a Ba re
4 ss Dea cits eae numa noi ale
‘cca rena do mone dead er seh ds a
‘cree in timpul reactiei. Cresterea aciditii se urmicese pin irae e¥)
Aparatera gf matedale necesare
+ pohare Erlenmayer
~ baie de apa
+, sid aceisatctie
NaOH 001N
* fenlfaein
{Wed de bacew
lun pshar Erlenmayer se introduc 025 g acid sets gi 200 ml. ap
isla gi se agi bine 10-15 secunde, penta dzavare.
Se ilteaz solu, Sei prob de 10 is tiréaz8 eu NaOH OLN in prezeth
de fenolfalein, notin cu n vlumul sole NaOH cu care stat. Restul de sole ©
imenjine pe baie de apa pina ee atnge temperatura de 70°C api se ao prob de 10 ml, se
reste repede let de pag se treat, notind eu, vbiumul de NsOH utiliza
Se noteazh oral care s- ful acca exrapere, deoarece misurarea tn
face din acest moment, consierat ea iil. Diferenfa yn reprezints mL. de NaOH
corespurzitor acidull aes eae - hidoizat in ipul inert, Sedan aeast
ifeen din valoarea afl nual de mL NOH crespurzitor cil sali, eas
‘nchidroizat la mometul 0 respect marimea a din exresia constant de vite
asnin-n) (59) -
Din sla meni pba de ap Ia 70°C a din 10 in 10 mate ete 10 ma
«ae dpa ire si et de ps ead chases! sii de NOH, Se noel eu,
PymmL de NaOH flo.
Difrenj dine naar de ml floss un moment cureare imum de mL
fos la tire inials orspunde eat x de acd acetic desconpas te
intervalul respectiv de timp. a
“Cneticd — Lucrri practice”
Inteopretarea gl ealeutel renuitatelor
1. Datel experiestle se tefl
Tabetnr.7
2. ‘Sedtermindconsania de vies soa i eaic
2. Secalculea timpul de mire.
Scanned with CamScanner
OFERUMARZA CONSTANT
OF USA
ARZACPINOZ OFIOMRUIEAT
AMPDOMGATE
Seopul lcci
in lucrarea de fafi se determina constanta de vitezi pentru reactia de descompunere a H:O2,
o reactie de ordinul I, de tipul:
A Produsi
Consideraffil teoretice
Cinetica chimicd urmareste evolufia in timp a reactiei chimice, stabilind viteza de reac
precum si influenja diferitlor factori asupra acesteia in scopul stabilirit mecanismului de reacte.
Prin viteza de reactie se infelege variatia in timp a concentrajiei participantilor la reactie. in general,
pentru o temperaturd dati, dependenfa vitezei de reactie de concentratie este dati de o ecuatie
diferengiala de forma:
de
Ho ket, unde:
a .
£ = este viteza de reactie,
it
mncentrafia reactantului la timpul t,
‘onstanta de proporfionalitate care se numeste constanta de vitezi,
n=este ordinul de reactic.
Aparetura sf materiale mecesee
- biureta
= balon cotat
- pipete
-pahare Erlenmeyer
- 1,02 3%
- FeCh
~ KMin0, 0,0SN
- H,SO,2N
Me
Scanned with CamScanner
Iifod de lycra
Se amesteci 30.mL solujie H202 cu 3.niL H,
ct 30. 3804 2N si cu 3m. sol ch. Dis
amestecul de reactie se iau probe de cite § ml. din 10 in 10 minwte alse tae eS oe ec Din
in 10 minute $i se titreaza cu KMnO, 0,0SN.
care amestecul supus
inute,
pal. Se vor efectua 6 titra, la intervale de 10 mi
Ecuatia reactiei ce are loc la titrare este :
H,02 + 2KMnO4 + 3H3S0,— 2MnS04 + K,S0,
H 2 + 41,0 +30,
iar din datele obsinute se va calcula concentratia HO,
Caleulul gi fnterpretarea rezultatelor
3
1. Cum raportul de oxido-reducere este >, concentraja de pa oxigenata se va afl din relia
Views
V,
niw
Sy0 = “Crauo, mol/L,
190,
unde:
€y,0, = concentrafia de apa oxigenat
Cxxwo, = concentratia de KMnO,
Visto, = Volumul de KMnOs utiliza la titrare N
Vigo = Volum de probit
2. Rezultatele objinute se tree in tabelul nr.
unde:
Co concentratia inigiald a HO; (3%)
= concentrajia HO, la momentul t Fe
3. Se prezinti grafic Ig (£2) = f(t) iar din panta dreptei obfinute se calculeazA valoarea constantei de
c
vitez.
Scanned with CamScanner
DETER NIN AR EALCU SLANE
oniznez
ARGAO IDO CMOUZA
AUNTIE AD a
Scape tuerictt
Determinarea constantei de viteza pentru o reacfie autocataliticd.
Considaratit taaretice
ibstitujie nucleofild bimoleculars.
Cel mai adesea reacfile de hidroliza decurg ca reacfii de su
fr catalica acid hidroliza esterilor este un proces reversibil, care in eazul acetatului de el
are ecustia:
CHsCOOC3Hs + H0 —+ CH;COOH + C3H;OH
Corespunzitor acestui mers al reacfiei procesul direct poate fi descris de ecustia cinesicd:
ac
Gok @-3)-0-2)
Concentratia apei fiind mai mare decét concentrajia esterului, se poate considers practic
cconstanti si in acest caz ecuatia devine:
S-k,b-(a-)
cb este constantl, ceea ce inseamnd eX reacfia asculth de o lege de vitezA corespunzatoare onginulut
tunu. In acest caz, ordinul de reactie s-a redus cu o unitate, reactia devenind pseudomonomolecular
Integrind relafia anterioara objinem:
ia initials me otal, eu ea) cu diferenta dintre concentratia
acidului a. dup& hidroliza total $i concentratia acidului ay Ia inceputul experientei.
B= Ae - Ao
Concentrafia esterului (a-x) este egal la timpul t cu concentrafia a a acidului la timpul t:
X= t= &
inlocuind, objinem:
2,303
k, = 283
eee a,
Cinetica reactiei se urmAreste titrind acidul format in timp cu o baza. Daca Vj este volurmul
de baxd corespunzAtor sfiritului reactiel iar Vj, Vz..(V)) sunt volumele de baz\ corespunzStoare
momentelor t,t. atunci constanta de vitezA ki= kab poate fi pusd sub forma:
2303, Vy-¥
pettdladditbhsh oiidit i iecthd ij
i titi
Scanned with CamScanner
“Cinetict - Lucritri practice”
{fled de fora
in vasul de reactie se introduc 2 mL acetat de
ctil, 5 mL solufic HCI 0,1N si 30 mL apa distilata.
Vasul se pune intr-o cutie Petri cu gheati si se
pistreazA pe tot parcursul reacfici. Se iau repede cu
pipeta 5 mL de probi si se introduc in vasul de
titrare, Din aceastii prima proba luati foarte rapid se
poate considera cf se titreazii numai HCl introdus,
rimfndind ca in cclelalte cazuri si se titreze un
amestec de acizi format din HCI introdus gi acidul
‘acetic aplirut, ca produs de reactic.
Titrarea se efectueazi cu NaOH O1N
utilizfind drept indicator fenolftaleina. Probele se iau
Ja ty = 10%, ty = 205 ty = 307, ty = 45, ts = 50".
Interpratanca gf callie acitattsse
1, Rezultatele experimentale objinute se tree Intr-un
tabel de forma :
Tabel nr.
“Cineticd - Lucrari practice”
unde:
Vj; = volumul de NaOH utilizat pentra titrarea
‘amestecului de acid corespunziitor momentelor th, 2,
snes.
‘Ve= volumul de bazi utilizat la titrire, corespunziitor
procesului de hidroliza,
2. Se va calcula valoarea lui k pentru momentele th,
ty, le ts, folosind relafia (35),
Scanned with CamScanner
Aparaturad gi materiale necesare
pipete
un cilindru gradat
= balon cu dop rodat, ce serveste ca vas de reactie
+ un vas pentru titrare
- CH3COOCHs 0,2N
‘NaOH 0,1N
- HCLO,IN
+ fenolftaleina
Qed de bere
fn vasul de reacfie se introdue 2 mL acetat de etil, 5 mL solutie HCI 0,1N si 30 mL apa
distilata. Vasul se pune intr-o cutie Petri cu gheafa si se pistreazA pe tot parcursul reactiei, Se iau
repede cu pipeta 5 mL de proba si se introduc in vasul de titrare. Din aceasta prima proba Iuatit
foarte rapid se poate considera c& se titreaz numai HCl introdus, riméngnd ca in celelalte cazuri si
se titreze un amestec de acizi format din HC! introdus si acidul acetic aparut, ca produs de reactic.
Titrarea se efectueazi cu NaOH 0,1N utilizind drept indicator fenolftaleina. Probele se iau
lat) = 10, 2 = 20, ts = 30, y= 45, ts = 50".
Imerpretarea gi caleulul reauitatelor
ww \ |
Aisi dich di ddvicn iat iit
iihiibad sishadplishil sali)
wees ‘scanned with CamScanner
“Chimie Fizict ~ Caiet de lucrari practice”
6.
STUDIUNGINENIGIIOESCONBUNERT
Apes ener hn paz
DE(CATANIZATOR|
er
Se studiaza cinetica reactiei de descompunere a apei oxigenate in prezenti de
catalizator, de catalizator promotat si de catalizator cu inhibitor.
Consideratil teoreties
La temperatura camerei apa oxigenata se descompune lent cu degajare de O2
reactia flind de ordinul inti:
H,0; > H,0 + 1/202
Reacfia este accelerata de ionii fierului trivalent sub forma de FeCls.
Mecanismul reactiei catalitice presupune existenfa a doug etape:
2Fe" +H,0;-92Fe? + 2H" +02 (1)
2Fe"? +H,0; + 2H" > 2Fe* +2H30 2)
Reacfia globala este:
2Fe"* + 2H,0; -> 2Fe"? + 2H,0 + Op
Etapa lenta determinant’ de viteza, este reacfia (1) care este de ordinul inti in
raport cu apa oxigenatd. Concentratia catalizatorului, desi este micd rimdne constant,
deoarece acesta se reface in cursul reactiei. Viteza de reactie se poate scric
unde key reprezint& constanta cinetic& global& care se determind experimental.
Catalizatorii reprezint& substanjele care maresc viteza de reactie prin micsorarea
cenergiei de activare a procesului gi care se regisesc integral la sfirsitul acestuia, Pentru a
2
Scanned with CamScanner
“Chimie ici ~Caiet de eri practice”
interac, lect promotor, see ssa ca
tn ea cv ep saa. Exo caguedecasee
med ea a ae op
iran fas. :
tear oi pt a mio cla
oxen pba hich nome oe ee, Cae Ge op ig
compan tum ez mist a amen (0, canines dens
Saeed vokend mist sya V2.
2303,
i= hog (128)
unde
1 timpal
V.=volumal de gaz masurat la Agi reacie
= vluml de gaz masurat tmp
\Vz-V,= cantata de ap oxigentl rast nereationat la momentul
Aparetard gf matertale aecesans
> biuret de gz
+ val dereacie
+ HO 3%
> Fel,
+ CuCl; 0.005M
+ acai 005M
Hod de buera
Insalajia in care fectuer8descompuneea ape oi
s escompuneea ape oxgenate se compune dintran
{emosat i cr se nuce vas de reac inchs emnetis cu un dop de cauive
brevzt yun ob rl rn cares face guano burt de ga. In vast de ence
‘fdas 5m sli ap cxigenat se face Iguacu burt de gaz, ad a0
cu parade nivel. Se into aol 3 mL sole FeCl se asuph vasul. Se agit putemic
an & race ow decane crnometl, Se ntczavolumul de gaz degjt dn
Talmadge Par de il uae ein in permanente veal
“hon fests oe es Ha. Cee
3 spl val de reac ein exer i
(gry pace Fon, Erne In prezed de FeCl sf CuCl
Sons raps ga Cain. Se voradlugs 3 mL salu GX
“Chime Fticd ~ Cait de wert practice”
Interpretanca gl caleulal recaitetelar
1. Secaleulea valoarea constantelr de vite, corespunzitoare cer tei procese de
escompunere aap exigeate, uid relia (1.28)
Rezutatel cinat se te intel mL.
2. Se compart ezulatel objute pentru eacta de descompunere ear are loc in prezentt
‘ecatlizator de eataliatr§ promotor respec de catalizator inhibitor.
Scanned with CamScanner
You might also like
- The Subtle Art of Not Giving a F*ck: A Counterintuitive Approach to Living a Good LifeFrom EverandThe Subtle Art of Not Giving a F*ck: A Counterintuitive Approach to Living a Good LifeRating: 4 out of 5 stars4/5 (5813)
- The Gifts of Imperfection: Let Go of Who You Think You're Supposed to Be and Embrace Who You AreFrom EverandThe Gifts of Imperfection: Let Go of Who You Think You're Supposed to Be and Embrace Who You AreRating: 4 out of 5 stars4/5 (1092)
- Never Split the Difference: Negotiating As If Your Life Depended On ItFrom EverandNever Split the Difference: Negotiating As If Your Life Depended On ItRating: 4.5 out of 5 stars4.5/5 (844)
- Grit: The Power of Passion and PerseveranceFrom EverandGrit: The Power of Passion and PerseveranceRating: 4 out of 5 stars4/5 (590)
- Hidden Figures: The American Dream and the Untold Story of the Black Women Mathematicians Who Helped Win the Space RaceFrom EverandHidden Figures: The American Dream and the Untold Story of the Black Women Mathematicians Who Helped Win the Space RaceRating: 4 out of 5 stars4/5 (897)
- Shoe Dog: A Memoir by the Creator of NikeFrom EverandShoe Dog: A Memoir by the Creator of NikeRating: 4.5 out of 5 stars4.5/5 (540)
- The Hard Thing About Hard Things: Building a Business When There Are No Easy AnswersFrom EverandThe Hard Thing About Hard Things: Building a Business When There Are No Easy AnswersRating: 4.5 out of 5 stars4.5/5 (348)
- Elon Musk: Tesla, SpaceX, and the Quest for a Fantastic FutureFrom EverandElon Musk: Tesla, SpaceX, and the Quest for a Fantastic FutureRating: 4.5 out of 5 stars4.5/5 (474)
- Her Body and Other Parties: StoriesFrom EverandHer Body and Other Parties: StoriesRating: 4 out of 5 stars4/5 (822)
- The Emperor of All Maladies: A Biography of CancerFrom EverandThe Emperor of All Maladies: A Biography of CancerRating: 4.5 out of 5 stars4.5/5 (271)
- The Sympathizer: A Novel (Pulitzer Prize for Fiction)From EverandThe Sympathizer: A Novel (Pulitzer Prize for Fiction)Rating: 4.5 out of 5 stars4.5/5 (122)
- The Little Book of Hygge: Danish Secrets to Happy LivingFrom EverandThe Little Book of Hygge: Danish Secrets to Happy LivingRating: 3.5 out of 5 stars3.5/5 (401)
- The World Is Flat 3.0: A Brief History of the Twenty-first CenturyFrom EverandThe World Is Flat 3.0: A Brief History of the Twenty-first CenturyRating: 3.5 out of 5 stars3.5/5 (2259)
- The Yellow House: A Memoir (2019 National Book Award Winner)From EverandThe Yellow House: A Memoir (2019 National Book Award Winner)Rating: 4 out of 5 stars4/5 (98)
- Devil in the Grove: Thurgood Marshall, the Groveland Boys, and the Dawn of a New AmericaFrom EverandDevil in the Grove: Thurgood Marshall, the Groveland Boys, and the Dawn of a New AmericaRating: 4.5 out of 5 stars4.5/5 (266)
- A Heartbreaking Work Of Staggering Genius: A Memoir Based on a True StoryFrom EverandA Heartbreaking Work Of Staggering Genius: A Memoir Based on a True StoryRating: 3.5 out of 5 stars3.5/5 (231)
- Team of Rivals: The Political Genius of Abraham LincolnFrom EverandTeam of Rivals: The Political Genius of Abraham LincolnRating: 4.5 out of 5 stars4.5/5 (234)
- On Fire: The (Burning) Case for a Green New DealFrom EverandOn Fire: The (Burning) Case for a Green New DealRating: 4 out of 5 stars4/5 (74)
- The Unwinding: An Inner History of the New AmericaFrom EverandThe Unwinding: An Inner History of the New AmericaRating: 4 out of 5 stars4/5 (45)
- Curs 1Document13 pagesCurs 1Diana ValentinaNo ratings yet
- Curs 3Document9 pagesCurs 3Diana ValentinaNo ratings yet
- CamScanner 10-09-2023 08.41Document11 pagesCamScanner 10-09-2023 08.41Diana ValentinaNo ratings yet
- 03.laborator Nr. 1 Si 2Document2 pages03.laborator Nr. 1 Si 2Diana ValentinaNo ratings yet
- ChemosphereDocument14 pagesChemosphereDiana ValentinaNo ratings yet
- Curs 5Document9 pagesCurs 5Diana ValentinaNo ratings yet
- Subiecte Examen BICDocument1 pageSubiecte Examen BICDiana ValentinaNo ratings yet
- 06.laborator Nr. 3Document3 pages06.laborator Nr. 3Diana ValentinaNo ratings yet
- Catb 5Document3 pagesCatb 5Diana ValentinaNo ratings yet
- Parțial ReactoareDocument46 pagesParțial ReactoareDiana ValentinaNo ratings yet
- Catb 12Document5 pagesCatb 12Diana ValentinaNo ratings yet
- Curs 5 AIC 2023Document16 pagesCurs 5 AIC 2023Diana ValentinaNo ratings yet
- CamScanner 2023-10-17 12.04Document15 pagesCamScanner 2023-10-17 12.04Diana ValentinaNo ratings yet
- Ali Men TaraDocument47 pagesAli Men TaraDiana ValentinaNo ratings yet
- Curs 3Document45 pagesCurs 3Diana ValentinaNo ratings yet
- CamScanner 2023-10-17 12.07Document2 pagesCamScanner 2023-10-17 12.07Diana ValentinaNo ratings yet
- Etapa Proiect 3 PTM 02.11.2023Document13 pagesEtapa Proiect 3 PTM 02.11.2023Diana ValentinaNo ratings yet
- Ali Men TaraDocument47 pagesAli Men TaraDiana ValentinaNo ratings yet
- Curs 2Document3 pagesCurs 2Diana ValentinaNo ratings yet
- TH Alimentare Part 1Document120 pagesTH Alimentare Part 1Diana ValentinaNo ratings yet
- Curs AplicatiiDocument15 pagesCurs AplicatiiDiana ValentinaNo ratings yet
- Derivati Functionali Ai Acizilor CarboxiliciDocument45 pagesDerivati Functionali Ai Acizilor CarboxiliciDiana ValentinaNo ratings yet
- Raport SaptamanalDocument2 pagesRaport SaptamanalDiana ValentinaNo ratings yet
- Curs 4. Precipitare OmogeneDocument10 pagesCurs 4. Precipitare OmogeneDiana ValentinaNo ratings yet
- Curs PatruDocument51 pagesCurs PatruDiana ValentinaNo ratings yet
- Curs 5. Coprecipitarea - Prelucrarea PrecipitatelorDocument15 pagesCurs 5. Coprecipitarea - Prelucrarea PrecipitatelorDiana ValentinaNo ratings yet