Professional Documents
Culture Documents
The Isomerization and Oxidation of Carotenoid Compounds in The Oil Palm Fruit During Productions of Cpo
Uploaded by
Gilang Septian SiregarOriginal Description:
Original Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
The Isomerization and Oxidation of Carotenoid Compounds in The Oil Palm Fruit During Productions of Cpo
Uploaded by
Gilang Septian SiregarCopyright:
Available Formats
48 Indo. J. Chem.
, 2009, 9 (1), 48 - 53
THE ISOMERIZATION AND OXIDATION OF CAROTENOID COMPOUNDS IN THE OIL PALM
FRUIT DURING PRODUCTIONS OF CPO
Isomerisasi dan Oksidasi Senyawa Karotenoid dalam Buah Kelapa Sawit Selama Pengolahan CPO
Reni Subawati Kusumaningtyas1,2 and Leenawaty Limantara3*
1
Magister Biology, Universitas Kristen Satya Wacana, Jl. Diponegoro 52-60 Salatiga 50711
2
SMART Research Institute, Jl. Teuku Umar 19 Pekanbaru, Riau 28112
3
Ma Chung Research Center for Photosynthetic Pigment, Univ. Ma Chung, Malang 65151
Received May 14, 2008; Accepted March 3, 2009
ABSTRACT
Isomerization and oxidation have been known as the major factors of the degradation of carotenoid
compounds. Results showed that the isomerization of the carotenoid in the oil palm fruit, during the sterilization
process, promotes the decrease of the concentration of trans - and trans -carotene approximately 21and 8%. The
decrements have continued on the fruit digestion, pressing, and clarification processes. The isomerization is also
indicated by the decreasing of the main peak spectra absorption intensity of - and -carotene about ±10,4%. The
spectra showed hypsocromic shift by ±3 nm. On the other hand, the oxidation of carotenoid has occurred in all
steps of crude palm oil (CPO) production. The oxidation of -carotene has caused the increasing amount of lutein:
49% of fruit after sterilization proces (BSt), 57% of crude oil after pressing (MSK), 17% of oil expurifier (MPF), and
5% of CPO product. The oxidation of -carotene will increase the amount of zeaxantin: 53% of fruit after sterilization
proces (BSt), 9% of crude oil after pressing (MSK), and 4% of oil expurifier (MPF).
Keywords: Isomerization Carotenoid, oxidation Carotenoid, oil palm
PENDAHULUAN menjadi senyawa baru dengan berat molekul yang
lebih rendah daripada bentuk epoksinya [5].
Minyak sawit (CPO: crude palm oil) dikenal Menurut Tay dan Choo [6,7], pemanasan
sebagai salah satu sumber karotenoid [1]. Konsentrasi merupakan salah satu faktor penyebab isomerisasi
karotenoid dalam CPO menjadi salah satu penentu senyawa karotenoid. Dalam pengolahan CPO,
kualitasnya. Beberapa importir menetapkan batas pemanasan merupakan aktifitas yang sangat vital dan
minimum kandungan karotenoid dalam CPO yaitu ≥ 500 mempengaruhi hasil ekstraksi minyak. Selama proses
ppm, bahkan India sebagai negara importir terbesar sterilisasi pemanasan dilakukan hingga suhu sterilizer
menetapkan sebanyak ± 700 ppm. mencapai 142,9 C. Pada proses pembantingan buah,
Pada dasarnya kandungan karotenoid total dalam pelumatan, ekstraksi minyak, klarifikasi, dan purifikasi
buah kelapa sawit diketahui sebesar 630-700 ppm [2], suhu dipertahankan 88-90 C [8]. Tahapan proses
sedangkan Sundram [3] melaporkan sebesar 700-800 pengolahan selanjutnya adalah melalui pengeringan
ppm. Namun, kandungan karotenoid tersebut vakum (vacuum drying) untuk menurunkan kadar air
mengalami penurunan selama proses pengolahan. produk CPO.
Konsentrasi karotenoid dalam produk CPO rata-rata Identifikasi senyawa-senyawa karotenoid dan
hanya sebesar 500 ppm. Diduga sejumlah karotenoid produk degradasinya dapat dilakukan dengan
mengalami degradasi selama proses pengolahan CPO menggunakan kromatografi cair kinerja tinggi (KCKT)
berlangsung [3]. yang dilengkapi dengan detektor photodiode array
Mekanisme degradasi dapat terjadi melalui proses (PDA). Metode ini mampu menunjukkan komposisi
isomerisasi maupun oksidasi. Isomerisasi menyebabkan senyawa-senyawa karotenoid dalam sebuah
terjadinya perubahan struktur geometris senyawa kromatogram [7]. Kombinasi antara data komposisi
karotenoid dari bentuk trans menjadi bentuk cis. karotenoid dan hasil analisis kandungan karotenoid
Berbeda dengan isomerisasi, terjadinya oksidasi akan total yang dilakukan dengan metode PORIM 1995 [9]
menyebabkan karotenoid termodifikasi dan membentuk menghasilkan informasi mengenai kandungan setiap
epoksi-epoksinya, yaitu berupa mono- dan di-oksigenasi senyawa karotenoid dalam produk utama maupun
karotenoid yang memiliki berat molekul lebih tinggi [4,5]. produk samping pengolahan CPO.
Bentuk-bentuk epoksi tersebut dapat terdegradasi
* Corresponding author. Tel/Fax : +62-341-556400/550175
Email address : leenawaty.limantara@machung.ac.id
Reni Subawati Kusumaningtyas and Leenawaty Limantara
Indo. J. Chem., 2009, 9 (1), 48 - 53 49
Penelitian ini diharapkan dapat memberikan kembali dengan pelarut yang sama sampai semua
informasi tentang perubahan komposisi karotenoid pigmen terangkat.
akibat isomerisasi dan oksidasi selama pengolahan
CPO dan menjadi dasar bagi penelitian-penelitian Pemisahan lemak sampel
lanjutan yang bermanfaat untuk pengembangan produk Lemak sampel perlu dipisahkan karena dapat
kelapa sawit. menyebabkan kerusakan kolom. Proses pemisahan
Penelitian dapat diarahkan pada pemanfaatan lemak dilakukan secara filtrasi pada suhu dingin.
limbah-limbah yang banyak dihasilkan pabrik Ekstrak pekat karotenoid dalam aseton 100%
pengolahan kelapa sawit seperti janjang kosong dan diletakkan di dalam freezer bersuhu -20 °C selama 4
serabut kelapa sawit. Pada pabrik dengan kapasitas jam sehingga lemak-lemak dalam ekstrak akan
olah 60 ton per hari, dapat dihasilkan janjang kosong menggumpal dan memisah dari karotenoid terlarut.
dan serabut kelapa sawit masing-masing sebanyak 13,2 Larutan karotenoid dalam aseton dipisahkan dengan
dan 5,7 ton (berat basah) per hari [8]. Adanya filtrasi dan selanjutnya dipekatkan dengan
kandungan karotenoid dalam limbah pabrik pengolahan menggunakan gas N2.
kelapa sawit ini merupakan potensi yang dapat
dikembangkan menjadi produk-produk lain dengan nilai Analisis komposisi karotenoid dengan
jual yang cukup tinggi. Secara komersial, karotenoid kromatografi cair kinerja tinggi [7]
dimanfaatkan sebagai pewarna alami makanan, Komposisi karotenoid yang terdapat dalam
suplemen vitamin A, obat-obatan, dan kosmetik. sampel dianalisis menggunakan kromatografi cair
Karotenoid juga dikenal sebagai bahan makanan kinerja tinggi (KCKT) yang dilengkapi dengan detektor
tambahan yang baik untuk kesehatan dan banyak PDA pada panjang gelombang 222–800 nm. Metode
diminati oleh masyarakat. analisis menggunakan metode yang dikembangkan
oleh Yap dkk. [12], yaitu dengan sistem isokratik
METODE PENELITIAN menggunakan kolom C18 RP (4.6 mm i.d. × 25 cm, 5
µm), dan campuran pelarut asetonitril : diklorometan
-1
Penelitian terhadap senyawa karotenoid dilakukan (89 : 11 v/v) dengan laju alir 1 mL.min
mulai dari bahan baku (kelapa sawit), produk-produk Data yang diperoleh dianalisis dengan program
antara dalam pengolahan CPO, hingga produk akhir Matlab 6.5 untuk memperoleh grafik kromatogram
CPO. Sampel-sampel tersebut meliputi buah segar KCKT dan melihat bentuk spektra masing-masing
(BS), buah steril (brondolan 1) pasca perebusan dan puncak yang muncul dalam kromatogram tersebut.
pembantingan/thresing (BSt), minyak sawit kasar pasca Identifikasi senyawa karotenoid dilakukan pada
klarifikasi (MSK), minyak bersih dari tanki purifier (MPF), puncak-puncak yang terbaca dalam grafik
dan produk akhir yang telah dikurangi kadar airnya kromatogram KCKT. Kromatogram tersebut dipilih
dengan vacuum drier (CPOvd). Pengambilan sampel pada sinyal 444 nm dan 286 nm. Setiap puncak yang
dilakukan di salah satu pabrik pengolahan kelapa sawit muncul identik dengan satu jenis senyawa karotenoid.
yang terletak di kabupaten Siak, Provinsi Riau. Bahan Identifikasi jenis senyawa dilakukan berdasarkan
kimia yang digunakan: aseton 100%, n-heksana, panjang gelombang maksimum dari puncak-puncak
kalsium karbonat (CaCO3) sebagai penetral, gas N2 spektra yang muncul.
teknis, asetonitril anhidrat grade KCKT, diklormetana
grade KCKT, isopropil alkohol grade KCKT, metanol Analisis kandungan karotenoid total
100% grade KCKT. Metode yang dipergunakan dalam analisis
kandungan karotenoid total mengacu pada metode
Prosedur Kerja PORIM 1995 [9]. Analisis dilakukan dengan cara
mengekstrak sampel dengan n-heksana dalam labu
Ekstraksi karotenoid kasar [10,11] ukur. Ekstrak yang diperoleh diukur bsorbansinya pada
Senyawa karotenoid dalam bahan diisolasi dalam panjang gelombang 446 nm. Konsentrasi karotenoid
larutan aseton 100%. Sampel diekstraksi dengan aseton total dihitung dengan rumus:
100% dengan perbandingan sampel dan pelarut 1 : 10 p 383
w/v. Pada waktu ekstraksi, sampel ditambahkan CaCO3 C (a - b )
100 s
sebagai agen penetral dan asam askorbat sebagai Keterangan: C = kandungan karotenoid total (ppm)
antioksidan untuk mencegah oksidasi. Ekstraksi p = pengenceran
dilakukan secepat mungkin untuk menghindari oksidasi s = berat sampel (gram)
dan degradasi enzimatik. Selanjutnya, ekstrak disaring a = absorbansi sampel
dengan kertas saring, residu yang diperoleh diekstraksi b = absorbansi blanko
Reni Subawati Kusumaningtyas and Leenawaty Limantara
50 Indo. J. Chem., 2009, 9 (1), 48 - 53
350
300
250
konsentrasi (ppm)
200
150
100
50
0
BS BSt MSK MPF CPO vd
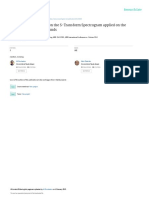
Gambar 1. Histogram perubahan konsentrasi trans/cis α- dan β-karoten selama proses pengolahan CPO. ( ) trans
β-karoten, ( ) trans α-karoten, ( ) cis β-karoten, ( ) cis α-karoten, (BS) buah segar, (BSt) buah setelah
perebusan, (MSK) produk setelah proses pengepresan, (MPF) produk setelah proses purifikasi, (CPOvd) produk
setelah keluar dari vacuum drier.
HASIL DAN PEMBAHASAN
Proses pengolahan CPO yang selalu melibatkan
pemanasan mengakibatkan sebagian karotenoid
terdegradasi. Degragasi karotenoid selama proses
pengolahan CPO terjadi melalui proses isomerisasi dan
oksidasi.
Isomerisasi α- dan β-karoten
Struktur geometris molekul karotenoid dalam buah
kelapa sawit segar (BS) lebih didominasi oleh bentuk
trans. Dominasi tersebut ditunjukkan oleh tingginya
konsetrasi trans α- dan β-karoten daripada cis α- dan β-
karoten dalam BS (Gambar 1). Hasil analisis ini sesuai
dengan penelitian yang dilakukan oleh Lessin dkk. [13]
dan Tay dkk. [14].
Struktur geometris tersebut mengalami perubahan Gambar 2. Pola spektra PDA isomerisasi trans dan cis
selama proses pengolahan CPO. Perubahan terjadi pada senyawa α dan β karoten: (a) α-karoten, (b) β-
___
melalui proses isomerisasi trans menjadi cis. Hasil karoten, ( ) bentuk trans, (---) bentuk cis
isomerisasi terlihat dari peningkatan konsentrasi α- dan
β-karoten dalam bentuk cis yang diimbangi dengan dan minyak pada suhu 88-90 C saat pengepresan,
penurunan bentuk trans-nya. Peningkatan konsentrasi klarifikasi, dan purifikasi, terbukti menyebabkan
cis α- dan cis β-karoten terjadi mulai dari proses isomerisasi struktur molekul α- dan β-karoten dalam
sterilisasi, yang terlihat pada kenaikkan konsentrasinya mesokarp buah kelapa sawit.
dalam BSt, dan konsentrasinya mencapai maksimum Terjadinya isomerisasi struktur molekul α- dan β-
pada MSK. Pada MSK tidak terdapat lagi α- dan β- karoten dibuktikan dengan adanya perubahan pola
karoten dalam bentuk trans (Gambar 1). spektra PDA (photodiode array) α-karoten (Gambar 2a)
Tay dan Choo [7] menyatakan bahwa pemanasan dan β-karoten (Gambar 2b). Pada spektra karotenoid
merupakan salah satu faktor penyebab isomerisasi bentuk cis terdapat puncak di daerah sinar ultraungu
senyawa karotenoid. Proses pemanasan yang dilakukan (daerah panjang gelombang () 300-400 nm) [11].
dalam pengolahan CPO, baik untuk sterilisasi buah Dalam penelitian ini puncak yang terbentuk pada 330
(142,9 C) maupun untuk mempertahankan kondisi buah nm.
Reni Subawati Kusumaningtyas and Leenawaty Limantara
Indo. J. Chem., 2009, 9 (1), 48 - 53 51
Gambar 3. Kromatogram KCKT senyawa karotenoid dalam produk-produk yang dihasilkan pada 5 tahap
___
pengolahan CPO. ( ) Hasil scaning pada 444 nm, (--) Hasil scaning pada 286 nm, (a) buah segar, (b) buah setelah
perebusan, (c) produk paska proses pengepresan, (d) produk paska proses purifikasi, dan (e) produk CPO setelah
keluar dari vacuum drier.
500
Stabilitas β-karoten ditunjukkan dengan penurunan
konsentrasi bentuk trans pada proses sterilisasi (dari
400
BS ke BSt) hanya sebesar 8%, sedangkan penurunan
konsentrasi (ppm)
300
pada α-karoten mencapai 21%. Meskipun demikian,
penurunan ini terus berlangsung dalam MST, MPF
200
hingga pada CPOvd tidak terdapat lagi trans α- dan β-
karoten. Menurut Dutta dkk. [15], isomerisasi geometris
100
senyawa-senyawa karotenoid disebabkan karena
ketidakstabilan rantai poliena dalam struktur
0 molekulnya.
BS BSt MSK MPF CPOvd Senyawa karotenoid dalam bentuk cis diketahui
juga memiliki stabilitas lebih rendah dibandingkan
Gambar 4. Histogram konsentrasi empat senyawa bentuk trans [16]. Rendahnya stabilitas senyawa
karotenoid yang stabil selama proses pengolahan CPO: karotenoid dalam bentuk cis ini mengakibatkan
( ) β-karoten, ( ) α-karoten, ( ) lutein, ( ) senyawa ini mudah teroksidasi pada proses
zeaxantin pemanasan lebih lanjut.
Selain munculnya puncak di daerah sinar Oksidasi senyawa-senyawa karotenoid
ultraungu, perubahan struktur geometris dari trans ke cis
juga ditandai dengan penurunan absorbansi di puncak Peristiwa oksidasi senyawa-senyawa karotenoid
utamanya dan pergeseran puncak utama secara selama proses pengolahan CPO terlihat dari
hipsokromik (ke arah yang lebih kecil). Dalam perubahan pola kromatogram KCKT pada CPO dan
penelitian ini terjadi pergeseran hipsokromik sejauh ± 3 produk-produk antaranya (Gambar 3). Perubahan pola
nm dan penurunan absorbansinya ± 10,4%. kromatogram tersebut mencerminkan perubahan
Perbandingan jumlah kandungan senyawa α- dan komposisi karotenoid (Tabel 1). Selama ini oksidasi
β-karoten dalam bentuk trans dan bentuk cis dikenal sebagai penyebab utama terdegradasinya
menunjukkan bahwa senyawa β-karoten memiliki senyawa-senyawa karotenoid [17].
stabilitas lebih baik dari pada senyawa α-karoten.
Reni Subawati Kusumaningtyas and Leenawaty Limantara
52 Indo. J. Chem., 2009, 9 (1), 48 - 53
Tabel 1. Identifikasi karotenoid berdasarkan waktu tambat dan serapan maksimum
Waktu Komposisi karotenoid (ppm)**
No Identifikasi spektra* max
Tambat (min) BS BSt MSK MPF CPO
1 10,4 lutein - 421 443 473 6,8 13,2 30,3 36,4 38,1
2 11,1 zeaxantin - 425 452 472 14,1 30,0 33,0 34,4 34,3
3 15,8 belum teridentifikasi 299 421 442 463 10,3 - - - -
4 16,4 belum teridentifikasi - 422 446 471 8,4 - - - -
5 16,9 α-zeakaroten - 402 423 449 - - - 9,7 10,2
6 17,6 belum teridentifikasi - 421 472 483 - 16,6 - - -
7 17,8 turunan zeaxantin - 420 440 - 21,6 - - - -
8 18,3 β-zeakaroten - 408 429 451 - - - 9,7 6,3
9 19,1 -carotene - 428 450 475 26,8 34,5 - - -
10 20,8 belum teridentifikasi - 411 433 463 9,1 - - - -
11 21,2 belum teridentifikasi 376 405 441 485 - - - 15,8 -
12 21,2 belum teridentifikasi - 421 442 463 - - - - 11,5
13 21,6 belum teridentifikasi - 429 448 472 5,1 - - - -
14 22,4 belum teridentifikasi 329 420 441 473 9,8 - - - -
15 24,4 neurosporene 331 419 440 464 - - 10,5 9,8 9,3
16 25,2 belum teridentifikasi 329 421 442 472 7,8 8,6 - -
17 26,5 cis α-caroten 333 420 443 471 29,7 55,3 151,2 161,2 158,0
18 26,9 α-karoten - 422 447 475 136,4 107,5 - - -
19 28,5 β-karoten - 430 452 478 270,6 249,5 - - -
20 28,9 cis β-carotene 344 420 448 474 67,3 68,6 224,1 190,7 207,6
21 36,3 cis phitoen 250 278 288 298 - - - 7,5 8,5
22 38,1 phitoen 277 288 300 12,2 - 10,4 - -
* identifikasi berdasarkan referensi Gross [11], Tay dan Choo [7], dan Rodriguez-Amaya [5]
** komposisi karotenoid ditentukan berdasarkan perbandingan luas puncak dari 4 ulangan
a-karoten b-karoten
OH
OH
OH
OH
Lutein Zeaxan tin
Gambar 5. Struktur senyawa α-karoten, β-karoten, lutein dan zeaxantin
Degradasi senyawa α- dan β-karoten ditandai sterilisasi, pengepresan, dan mencapai maksimal pada
dengan penurunan konsentrasi kedua pigmen ini dan proses purifikasi. Persentase kenaikan zeaxantin pada
peningkatan konsentrasi lutein dan zeaxantin (Gambar BSt, MSK dan MPF masing-masing sebesar 53, 9 dan
4). Peningkatan konsentrasi lutein dan zeaxantin 4%, sedangkan pada proses pengeringan minyak
tersebut ditentukan berdasarkan persentase kenaikan dalam vacuum drier konsentrasi zeaxantin relatif
konsentrasi lutein pada setiap produk antara dengan konstan.
produk sebelumnya. Hasil analisis menunjukkan bahwa Meskipun dikenal sebagai senyawa yang cukup
konsentrasi lutein semakin meningkat selama proses stabil, pemanasan dan keberadaan oksigen selama
pengolahan hingga produk CPO. Persentase kenaikan proses pengolahan CPO mengakibatkan α- dan β-
lutein pada BSt, MSK, MPF dan CPOvd masing-masing karoten teroksidasi dan membentuk senyawa
sebesar 49, 57, 17 dan 5%. Berbeda dengan lutein, turunannya. Senyawa tersebut dapat dideteksi dari
konsentrasi zeaxantin semakin meningkat pada proses kesamaan struktur molekulnya dengan struktur α- dan
Reni Subawati Kusumaningtyas and Leenawaty Limantara
Indo. J. Chem., 2009, 9 (1), 48 - 53 53
β-karoten dan persamaan nama sistematisnya. Secara DAFTAR PUSTAKA
sistematis lutein disebut sebagai ,-carotene-3,3’diol,
yaitu senyawa α-karoten (,-carotene) yang mengikat 2 1. Khosla, P., 2006, Agro-food Industry by Tech., 17,
gugus OH di kedua cincinnya, sedangkan zeaxantin 21-23.
disebut sebagai ,-carotene-3,3’diol yaitu senyawa β- 2. Zeb, A. and Mehmood, S., 2004, Pakistan Journal
karoten (,-carotene) yang mengikat 2 gugus OH di of Nutrition, 3, 199-204.
kedua cincinnya (Gambar 5). Dengan demikian lutein 3. Sundram, K., 2007, Palm Oil: Chemistry and
dan zeaxantin diduga merupakan produk degradasi α- Nutrition Updates, Malaysian Palm Oil Board
dan β-karoten. (MPOB), Kuala Lumpur.
Dalam proses biosintesis karotenoid, α-karoten 4. Fiedor, J., Fiedor, L., Winkler, J., Scherz, A., and
juga dikenal sebagai prekursor lutein [18,19] dan β- Scheer, H., 2001, Photochemistry and
karoten merupakan prekursor zeaxantin [18]. Photobiology, 74 (1), 64-71.
Mekanisme biosintesisnya yaitu melalui hidroksilasi yang 5. Rodriguez-Amaya, D.B., 2001, A Guide to
dipercepat dengan oksidasi. Menurut Gross [11], proses Carotenoid Analysis in Food, International Life
hidroksilasi tersebut dapat mengakibatkan penurunan Science Institute, Washington.
konsentrasi β-karoten hingga 1-2%. 6. Tay, B.Y.P. and Choo, Y.M., 1999, Journal of Oil
Diduga hidroksilasi dan oksidasi yang terjadi pada Palm Research, 2, 62-78.
saat sterilisasi menyebabkan hilangnya beberapa 7. Tay, B.Y.P. and Choo, Y.M., 2000, Palm Oil
senyawa karotenoid [3, 4, 7, 10, 13, 14] dan Development, 33, 13-17.
terdegradasinya senyawa α-, β-, dan -karoten dalam 8. Naibaho, P., 1998, Teknik Pengolahan Kelapa
BS (Tabel 1). Degradasi -karoten diduga membentuk α- Sawit, Pusat Penelitian Kelapa Sawit (PPKS),
zeakaroten sebagai turunannya. Medan.
Selain lutein, zeaxantin dan α-zeakaroten juga 9. Siew, W.L., Tang, T.S., and Tan, T.A., 1995,
ditemukan 2 jenis karotenoid baru yang diidentifikasikan PORIM Test Methods: Method of Test for Palm Oil
sebagai β-zeakaroten dan neurosporene. Keduanya and Palm Oil Products, Palm Oil Research Institute
diduga merupakan hasil degradasi karotenoid yang of Malaysia, Kuala Lumpur.
hilang sebelumnya. Selain membentuk senyawa lain, 10. Britton, G., Liaaen-Jensen, S., and Pfander, H.,
sebagian karotenoid juga mengalami kerusakan 1995, Carotenoids Vol. 1A: Isolation and Analysis,
sehingga konsentrasi karotenoid total dalam produk Birkhäuser Verlag, Boston.
menurun. 11. Gross, J., 1991, Pigmen in Vegetables:
Chlorophylls and Carotenoids, Van Nostrand
KESIMPULAN Reinhold, New York.
12. Yap, S.C., Choo, Y.M., Ooi, C.K., Ong, A.S.H., and
Terjadinya isomerisasi pada senyawa α- dan β- Goh, S.H., 1997, Elaeis, 3, 309-378.
karoten dalam buah kelapa sawit ditandai oleh 13. Lessin, W.J., Catigani, G.L., and Schwartz, S.J.,
perubahan struktur geometris dari trans ke cis, juga 1997, J. Agric. Food Chem., 54, 3728-3732.
penurunan absorbansi spektra α- dan β-karoten ± 10,4% 14. Tay, B.Y.P., Choo, Y.M., Gwendoline, E.C.L., and
di puncak utamanya dan pergeseran puncak utama Goh, S.H., 2002, Journal of Oil Palm Research, 13,
secara hipsokromik ± 3 nm. Isomerisasi senyawa 23-32.
karotenoid selama proses pengolahan kelapa sawit 15. Dutta, D., Chaudhuri, U.R., and Chakraborty, R.,
menyebabkan penurunan konsentrasi trans α- dan β- 2005, African Journal of Biotehcnology, 4, 1510-
karoten, yaitu sebanyak 21 dan 8% pada proses 1520.
sterilisasi. Penurunan ini terus berlangsung pada proses 16. Ladislav, F., Pacakova, V., Stulik, K., and Volka,
pelumatan buah, pengepresan, dan klarifikasi. Proses K., 2005, Current Analitical Chemistry, 1, 93-102.
oksidasi terjadi pada seluruh tahap pengolahan CPO. 17. Paiva, S.A.R. and Russell, R.M., 1999, Journal of
Oksidasi α-karoten menyebabkan kenaikkan lutein The American College of Nutrition, 18, 426-433.
sebesar 49, 57, 17 dan 5% pada BST, MSK, MPF dan 18. Bauernfeind, J.C., 1972, J. Agric. Food Chem., 20,
CPOvd. Oksidasi β-karoten menyebabkan kenaikkan 456-473.
zeaxantin sebesar 53, 9 dan 4% pada BST, MSK dan 19. Tay, B.Y.P. and Gwendoline, E.C.L., 2006, Journal
MPF. of Oil Palm Research, 18, 189-197.
Reni Subawati Kusumaningtyas and Leenawaty Limantara
You might also like
- Processing Contaminants in Edible Oils: MCPD and Glycidyl EstersFrom EverandProcessing Contaminants in Edible Oils: MCPD and Glycidyl EstersNo ratings yet
- Optimization Carotenoids Isolation of The Waste Crude Palm Oil Using - Amylase, - Amylase, and CellulaseDocument6 pagesOptimization Carotenoids Isolation of The Waste Crude Palm Oil Using - Amylase, - Amylase, and CellulaseInternational Organization of Scientific Research (IOSR)No ratings yet
- Black Soldier Fly Products: Generic Description and Analysis of the Production Process for Chitosan, Proteins and Lipid from Black Soldier Fly Larvae.From EverandBlack Soldier Fly Products: Generic Description and Analysis of the Production Process for Chitosan, Proteins and Lipid from Black Soldier Fly Larvae.Rating: 4 out of 5 stars4/5 (1)
- Deasidifikasi/ Netralisasi CpoDocument6 pagesDeasidifikasi/ Netralisasi CpoPaul ColemanNo ratings yet
- Control of Deacidification Process in Purification of Red Palm Oil For Pilot Plant ScaleDocument10 pagesControl of Deacidification Process in Purification of Red Palm Oil For Pilot Plant ScaleEnjang FathurrohmanNo ratings yet
- Coupling Microwave-Assisted Drying and SupercriticDocument6 pagesCoupling Microwave-Assisted Drying and Supercriticsyahirah abubakarNo ratings yet
- Analisis Komposisi Dan Kandungan Karotenoid TotalDocument10 pagesAnalisis Komposisi Dan Kandungan Karotenoid TotalHermanto MarvianNo ratings yet
- Biomass and Bioenergy: Research PaperDocument7 pagesBiomass and Bioenergy: Research PaperM. AlfinandaNo ratings yet
- Chen 2008Document8 pagesChen 2008Yunita PujiastutiNo ratings yet
- Terjadinya Isomerisasi Dan Oksidasi - Dan - Karoten Selama Proses Pengolahan CPODocument3 pagesTerjadinya Isomerisasi Dan Oksidasi - Dan - Karoten Selama Proses Pengolahan CPOFilipi TariganNo ratings yet
- NMR020008 1 5.0111708Document10 pagesNMR020008 1 5.0111708Sahri YantiNo ratings yet
- EJLST SatyaDocument5 pagesEJLST Satyasatya vaniNo ratings yet
- Fraksinasi Minyak Sawit Kasar Dengan Pelarut Organik Dalam Pembuatan Konsentrat KarotenoidDocument9 pagesFraksinasi Minyak Sawit Kasar Dengan Pelarut Organik Dalam Pembuatan Konsentrat KarotenoidFaFi SaLaNo ratings yet
- GC MS ReportDocument10 pagesGC MS ReportWahyuniAntariNo ratings yet
- 2019 Hura CrepitansDocument8 pages2019 Hura CrepitansNONVIHO GuévaraNo ratings yet
- Ipi 419250Document11 pagesIpi 419250DefiNo ratings yet
- Ektraksi AdalahDocument11 pagesEktraksi AdalahFEBRIAN HUTAHAEANNo ratings yet
- 89 SoyDocument13 pages89 SoyaaNo ratings yet
- RRL 3Document3 pagesRRL 3Aprille Kaye TayoneNo ratings yet
- Thin Layer Chromatographic Analysis of ADocument11 pagesThin Layer Chromatographic Analysis of AAndres GuzmanNo ratings yet
- Purwwasena 2009Document8 pagesPurwwasena 2009Emharion DinNo ratings yet
- 26018-Article Text-80410-2-10-20191022Document8 pages26018-Article Text-80410-2-10-20191022La Ode AdhanNo ratings yet
- Ekstraksi Asam Lemak Bebas Dari Minyak Dedak Padi PDFDocument11 pagesEkstraksi Asam Lemak Bebas Dari Minyak Dedak Padi PDFRani TriwrdhNo ratings yet
- Microalgal Lipid Extraction and Evaluation of Single-Step Biodiesel ProductionDocument10 pagesMicroalgal Lipid Extraction and Evaluation of Single-Step Biodiesel ProductionMuhammad AminNo ratings yet
- Synthesis and Characterization of Green Biodegradable Palm Oleic Acid Based PolyesterDocument13 pagesSynthesis and Characterization of Green Biodegradable Palm Oleic Acid Based Polyestermorganreynoldsgreen98No ratings yet
- JurnalllDocument7 pagesJurnalllAlifa FadhilaNo ratings yet
- Jurnal Khamir RotiDocument11 pagesJurnal Khamir RotiTaufiq AliNo ratings yet
- Engineering Processof Deodorizationto Improve Product Qualityof Red Palm OilDocument8 pagesEngineering Processof Deodorizationto Improve Product Qualityof Red Palm OilAryoga HerdyarNo ratings yet
- Food Chemistry 269 (2018) 252-257Document6 pagesFood Chemistry 269 (2018) 252-257terNo ratings yet
- Cpo JurnallDocument6 pagesCpo JurnallIneke AuliaNo ratings yet
- The Produce of Methyl Ester FRDocument7 pagesThe Produce of Methyl Ester FRIzzatisaharNo ratings yet
- Date SeedsDocument8 pagesDate SeedsValeria MurilloNo ratings yet
- 8609 16261 3 SP PDFDocument13 pages8609 16261 3 SP PDFNaniekTriUtamiNo ratings yet
- Glycerol Residue-A Rich Source Glycerol and Medium Chain Fatty AcidDocument5 pagesGlycerol Residue-A Rich Source Glycerol and Medium Chain Fatty AcidRikardo LumbantoruanNo ratings yet
- Physicochemical Properties of Palm Stearin and Palm Mid Fraction Obtained by Dry FractionationDocument5 pagesPhysicochemical Properties of Palm Stearin and Palm Mid Fraction Obtained by Dry FractionationkirdipNo ratings yet
- Kinetics of Palm Oil Transesterification in Methanol With Potassium Hydroxide As A CatalystDocument7 pagesKinetics of Palm Oil Transesterification in Methanol With Potassium Hydroxide As A Catalystshabrina nurhafizhahNo ratings yet
- Rice Bran OilDocument5 pagesRice Bran OilPinku RajNo ratings yet
- J Sciaf 2020 E00498Document24 pagesJ Sciaf 2020 E00498Ilyas KhanNo ratings yet
- Lee 2019Document8 pagesLee 2019Tia MaharaniNo ratings yet
- Reactive Extraction of Jatropha Curcas L. Seed For Production of Biodiesel Process Optimization StudyDocument7 pagesReactive Extraction of Jatropha Curcas L. Seed For Production of Biodiesel Process Optimization Studydstar13No ratings yet
- Evaluation of Major Fatty Acids Determin cb410d05Document9 pagesEvaluation of Major Fatty Acids Determin cb410d05Hesty Nurul HuriyahNo ratings yet
- 04 Saripah SobahDocument8 pages04 Saripah SobahArdifal JumaidiNo ratings yet
- Sian Ournal of HemistryDocument5 pagesSian Ournal of HemistryYlm PtanaNo ratings yet
- Hydroprocessing of Palm Oil Using Rh/HZSM-5 For The Production of Biojet Fuel in A Fixed Bed ReactorDocument12 pagesHydroprocessing of Palm Oil Using Rh/HZSM-5 For The Production of Biojet Fuel in A Fixed Bed ReactorNguyễn Văn MinhNo ratings yet
- 2018 - Optimisation and Modelling of Supercritical CO2 Extraction ProcessDocument9 pages2018 - Optimisation and Modelling of Supercritical CO2 Extraction ProcesssutarsiNo ratings yet
- Determination of Physico-Chemical Properties of Castor Biodiesel A PotentialDocument7 pagesDetermination of Physico-Chemical Properties of Castor Biodiesel A PotentialIAEME PublicationNo ratings yet
- 3344 1411 1 SPDocument11 pages3344 1411 1 SPYessy ErmawardaniNo ratings yet
- Ipi518812 PDFDocument9 pagesIpi518812 PDFAriNo ratings yet
- 66 Ess17078Document9 pages66 Ess17078AJ ManurungNo ratings yet
- Batistella2002 Article MolecularDistillationProcessFo PDFDocument11 pagesBatistella2002 Article MolecularDistillationProcessFo PDFSrđan TufegdžićNo ratings yet
- Purification of Crude Glycerol From Transesterific PDFDocument11 pagesPurification of Crude Glycerol From Transesterific PDFesiNo ratings yet
- 27 - Free Fatty Acid Separation From Vegetable Oil Deodorizer Distillate Using Molecular Distillation ProcessDocument7 pages27 - Free Fatty Acid Separation From Vegetable Oil Deodorizer Distillate Using Molecular Distillation ProcessmrjevinNo ratings yet
- 1 SMDocument10 pages1 SMZadira AyuNo ratings yet
- Print - JSIR 71 (12) 822-828Document7 pagesPrint - JSIR 71 (12) 822-828Shurooq TaibNo ratings yet
- Production of Biodiesel by TransesterifiDocument14 pagesProduction of Biodiesel by TransesterifiRUNGSAN RUNGRUENGSEENo ratings yet
- Optimization of Scco Extraction of Rambutan Seed Oil Using Response Surface MethodologyDocument4 pagesOptimization of Scco Extraction of Rambutan Seed Oil Using Response Surface MethodologyAna MardliyahNo ratings yet
- The Comparison Survey Antioxidant Power and Content of Extracted Astaxanthin From Shrimp Waste With Acid, Alkaline and Enzymatic MethodsDocument3 pagesThe Comparison Survey Antioxidant Power and Content of Extracted Astaxanthin From Shrimp Waste With Acid, Alkaline and Enzymatic MethodsSintya Dwika PutriNo ratings yet
- Aqueous Two Phase Extraction For Purification of C-PhycocyaninDocument9 pagesAqueous Two Phase Extraction For Purification of C-PhycocyaninRuxandra SimionNo ratings yet
- Composition of Coconut Testa, Coconut Kernel and Its OilDocument8 pagesComposition of Coconut Testa, Coconut Kernel and Its OilRic MnsNo ratings yet
- Physic-Chemical Characteristic of Nata de Coco: IOP Conference Series: Earth and Environmental ScienceDocument9 pagesPhysic-Chemical Characteristic of Nata de Coco: IOP Conference Series: Earth and Environmental Scienceyusria1982No ratings yet
- DISCIPLINESPECS - 20170810 - Standard Specifications For IT Network Configur.... PDF - DOC634349Document21 pagesDISCIPLINESPECS - 20170810 - Standard Specifications For IT Network Configur.... PDF - DOC634349Todd ENo ratings yet
- FA2020 - ENE505 - L4.5 - Fossil Fuels - Oil & Gas Env ImpactsDocument43 pagesFA2020 - ENE505 - L4.5 - Fossil Fuels - Oil & Gas Env ImpactsTommy TrojanNo ratings yet
- Physical Science (Specialization) Reviewer 494 Items With Rationalization PDFDocument118 pagesPhysical Science (Specialization) Reviewer 494 Items With Rationalization PDFKaren DellatanNo ratings yet
- The Darwinian Concept of EvolutionDocument6 pagesThe Darwinian Concept of EvolutionAlfredo VergaraNo ratings yet
- Ross Jeffries - Nail Your Inner Game NotesDocument12 pagesRoss Jeffries - Nail Your Inner Game NotesJohn Second100% (1)
- User Manuel - ESCODocument38 pagesUser Manuel - ESCOSerhat YıldırımNo ratings yet
- Should The Age of Driving Be RaisedDocument2 pagesShould The Age of Driving Be RaisedhakimNo ratings yet
- Shannon Entropy Based On The S-Transform Spectrogram Applied On The Classification of Heart SoundsDocument6 pagesShannon Entropy Based On The S-Transform Spectrogram Applied On The Classification of Heart SoundsdenyspestanaNo ratings yet
- Republic of The Philippines Batangas State University College of Engineering, Architecture & Fine ArtsDocument3 pagesRepublic of The Philippines Batangas State University College of Engineering, Architecture & Fine ArtsDianne VillanuevaNo ratings yet
- SimulationDocument2 pagesSimulationVin Mamuric Meneses100% (1)
- E Locking Cessna 172Document3 pagesE Locking Cessna 172RAJ MOHANNo ratings yet
- Pathoma CH 1 NotesDocument2 pagesPathoma CH 1 NotesjdNo ratings yet
- Science Summative Test 1st and 2ndDocument11 pagesScience Summative Test 1st and 2ndGabrielMichaelMalubayCapuyan67% (3)
- Dr. Sajjad Hussain Sumrra Isomerism (CHEM-305) Inorganic Chemistry-IIDocument48 pagesDr. Sajjad Hussain Sumrra Isomerism (CHEM-305) Inorganic Chemistry-IITanya DilshadNo ratings yet
- Report On Attendance: Magwawa Integrated SchoolDocument2 pagesReport On Attendance: Magwawa Integrated SchoolEeve YhoungNo ratings yet
- Task Antropology of Law (Paper Bahasa Inggris Antropologi Hukum)Document7 pagesTask Antropology of Law (Paper Bahasa Inggris Antropologi Hukum)Ratri NugraheniNo ratings yet
- Boiler & Turbine Efficiency: Rohit Verma Dy - Director NPTI, FaridabadDocument77 pagesBoiler & Turbine Efficiency: Rohit Verma Dy - Director NPTI, FaridabadLakshya Soni100% (3)
- ESTUDIO5506 6506 7506ACsdcDocument517 pagesESTUDIO5506 6506 7506ACsdcthanh nguyendatthanhNo ratings yet
- Basic First Aid 0808Document72 pagesBasic First Aid 0808BS AnilKumarNo ratings yet
- Analysis of Traumatic Brain Injury: and Correlation Between NCCT Findings and GCS AssessmentDocument5 pagesAnalysis of Traumatic Brain Injury: and Correlation Between NCCT Findings and GCS AssessmentIJAR JOURNALNo ratings yet
- RQ - RP - RPT & FBNDocument35 pagesRQ - RP - RPT & FBNSlim.B100% (2)
- IRENA Biofuels For Aviation 2017Document52 pagesIRENA Biofuels For Aviation 2017u06l4j3bNo ratings yet
- Ulkus PeptikDocument26 pagesUlkus PeptikKang MunirNo ratings yet
- II. Executive Summary: Olympus' Endoscopic Solutions Operating RoomDocument7 pagesII. Executive Summary: Olympus' Endoscopic Solutions Operating RoomMaricar PinedaNo ratings yet
- (Answer: τ (y = 1 mm) = 1.49 Pa) : MEE20003 Fluid Mechanics 1 Tutorial 1Document2 pages(Answer: τ (y = 1 mm) = 1.49 Pa) : MEE20003 Fluid Mechanics 1 Tutorial 1Afwan IrfanNo ratings yet
- Jee Advanced October 2021 Chemistry Paper 1 Solution PHP 1Document10 pagesJee Advanced October 2021 Chemistry Paper 1 Solution PHP 1Indian PUBG GamerzNo ratings yet
- Manual Ifp Mn-00665Document92 pagesManual Ifp Mn-00665Cristian SilvaNo ratings yet
- Temperature Press. Control ValveDocument63 pagesTemperature Press. Control ValveGeorgiNo ratings yet
- The Subjunctive Mood in Modern Greek: Na +rima Se Enestota)Document3 pagesThe Subjunctive Mood in Modern Greek: Na +rima Se Enestota)Emmanuel BarabbasNo ratings yet
- In Vitro and in Silico Platforms For Evaluating Liver ToxicityDocument1 pageIn Vitro and in Silico Platforms For Evaluating Liver ToxicityGeetika PremanNo ratings yet
- The Secret of the Golden Flower: A Chinese Book Of LifeFrom EverandThe Secret of the Golden Flower: A Chinese Book Of LifeRating: 5 out of 5 stars5/5 (4)
- The Hundred Remedies of the Tao: Spiritual Wisdom for Interesting TimesFrom EverandThe Hundred Remedies of the Tao: Spiritual Wisdom for Interesting TimesRating: 5 out of 5 stars5/5 (3)
- Alone With Others: An Existential Approach to BuddhismFrom EverandAlone With Others: An Existential Approach to BuddhismRating: 4 out of 5 stars4/5 (30)
- The Eternal Tao Te Ching: The Philosophical Masterwork of Taoism and Its Relevance TodayFrom EverandThe Eternal Tao Te Ching: The Philosophical Masterwork of Taoism and Its Relevance TodayRating: 4 out of 5 stars4/5 (6)
- The Essence of Self-Realization: The Wisdom of Paramhansa YoganandaFrom EverandThe Essence of Self-Realization: The Wisdom of Paramhansa YoganandaRating: 4.5 out of 5 stars4.5/5 (43)
- The Essence of the Bhagavad Gita: Explained by Paramhansa Yogananda as remembered by his disciple, Swami KriyanandaFrom EverandThe Essence of the Bhagavad Gita: Explained by Paramhansa Yogananda as remembered by his disciple, Swami KriyanandaRating: 4.5 out of 5 stars4.5/5 (41)
- The Mandarin Tree: Manifest Joy, Luck, and Magic with Two Asian American MysticsFrom EverandThe Mandarin Tree: Manifest Joy, Luck, and Magic with Two Asian American MysticsNo ratings yet
- Shakti Rising: Embracing Shadow and Light on the Goddess Path to WholenessFrom EverandShakti Rising: Embracing Shadow and Light on the Goddess Path to WholenessRating: 5 out of 5 stars5/5 (21)
- Going to Pieces without Falling Apart: A Buddhist Perspective on WholenessFrom EverandGoing to Pieces without Falling Apart: A Buddhist Perspective on WholenessRating: 3.5 out of 5 stars3.5/5 (112)
- The Divine Feminine Tao Te Ching: A New Translation and CommentaryFrom EverandThe Divine Feminine Tao Te Ching: A New Translation and CommentaryRating: 4.5 out of 5 stars4.5/5 (5)
- Taoism for Beginners: A Guide to Balanced LivingFrom EverandTaoism for Beginners: A Guide to Balanced LivingRating: 4.5 out of 5 stars4.5/5 (2)
- World Religion 101: From Buddhism to Judaism, History, Beliefs, and Practices of the Great ReligionsFrom EverandWorld Religion 101: From Buddhism to Judaism, History, Beliefs, and Practices of the Great ReligionsRating: 5 out of 5 stars5/5 (9)
- Chinese Symbolism and Art Motifs Fourth Revised Edition: A Comprehensive Handbook on Symbolism in Chinese Art Through the AgesFrom EverandChinese Symbolism and Art Motifs Fourth Revised Edition: A Comprehensive Handbook on Symbolism in Chinese Art Through the AgesRating: 4 out of 5 stars4/5 (14)
- Swami Vivekananda Echoes of Eternity: America’s 1st Guru in His Own WordsFrom EverandSwami Vivekananda Echoes of Eternity: America’s 1st Guru in His Own WordsRating: 4.5 out of 5 stars4.5/5 (28)
- Everyday Tao: Living with Balance and HarmonyFrom EverandEveryday Tao: Living with Balance and HarmonyRating: 4 out of 5 stars4/5 (39)
- Buddha to Thomas Merton: Wisdom from the Great Mystics, Sages, and Saints, FromFrom EverandBuddha to Thomas Merton: Wisdom from the Great Mystics, Sages, and Saints, FromRating: 4.5 out of 5 stars4.5/5 (8)
- Tao Te Ching: A New English VersionFrom EverandTao Te Ching: A New English VersionRating: 4.5 out of 5 stars4.5/5 (131)
- Awaken to Superconsciousness: How to Use Meditation for Inner Peace, Intuitive Guidance, and Greater AwarenessFrom EverandAwaken to Superconsciousness: How to Use Meditation for Inner Peace, Intuitive Guidance, and Greater AwarenessRating: 5 out of 5 stars5/5 (1)
- God As Nature Sees God: A Christian Reading of the Tao Te ChingFrom EverandGod As Nature Sees God: A Christian Reading of the Tao Te ChingRating: 4.5 out of 5 stars4.5/5 (3)