Professional Documents
Culture Documents
Physique
Physique
Uploaded by
Jabri Imene0 ratings0% found this document useful (0 votes)
5 views5 pagesOriginal Title
physique
Copyright
© © All Rights Reserved
Available Formats
PDF or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as PDF or read online from Scribd
0 ratings0% found this document useful (0 votes)
5 views5 pagesPhysique
Physique
Uploaded by
Jabri ImeneCopyright:
© All Rights Reserved
Available Formats
Download as PDF or read online from Scribd
You are on page 1of 5
REPUBLIQUE TUNISIENNE
MINISTERE DE L'EDUCATION Epreuve : SCIENCES P!
OO00 Baeeaa
EXAMEN DU BACCALAUREAT eee
SESSION 2015 Coefficient : 4
Section : Mathématiques ~~ Session principale
Le sujet comporte 5 pages numérotées de 1/5 5/5.
La page 5/5 est & remplir par le candidat ef 4 remettre avec sa copie.
Chimie (7 points)
Exercice 1 (3 points)
On prépare, dans deux erienmeyers propres et secs & I’instant t= 0, deux mélanges homogenes (A) et (B)
identiques et équimolaires formés d’acide méthanoique (HCOH), d’éthanol (CAyCH,OH) ct de quelques
gouttes dacide sulfurique concentré, pris comme catalyseur. Immédiatement aprés, on place :
- Verlenmeyer contenant le mélange (A) dans un bain d’eau glacée ;
- erlenmeyer contenant le mélange (B) dans un bain porté & une température constante de 50°C, aprés
Favoir équipé d’un réfrigérant a air.
A instant t) = 10 min, la moitié du volume du mélange (A) est retirée du bain d'eau glacée et
immédiatement dosée par une solution aqueuse (Sp) de soude (NaOH) de concentration C= 1 mokL?, en
présence d’un indicateur coloré approprig. Le volume de (Sp) ajouté a léquivalence est Via = 15 mL.
A Vinstant f = 20 min, on retire, du bain d’eau glacée, autre moitié du mélange (A) et on refait la méme
expérience précédente de dosage. Le volume de (Sp) ajouté 4 P’équivalence est Vox = 15 mL.
Le mélange (B) est le sige d’une ue qui atteint I'état d’équilibre & Linstant ts, moment &
partir duquel le mélange obtenu est dosé par la méme solution (Sp). Le volume de (Sp) ajouté a 'équivalence
est Vp = 10 mL.
Pour chacun des dosages, on supposera négligeabie la quantité d’ions HO* provenant de Macide sulfurique
devant celle provenant de l’acide méthanoique.
4- Donner Te nom de Ja réaction qui apparait dans le mélange (B) avant d°atteindre l'équilibre et préciser les
proprigiés qui la caractérisent.
2- a- Justifier le résultat expérimental Via = V2, bien que tr # tr.
b- Montrer que la quantité de matiére initiale mp d’alcool dans fe mélange (B) est np=
107 mol.
3+ a- Déterminer la valeur du taux d’avancement final ty de fa réaction qui se produit dans le mélange (B).
b- Préciser la propriété caractéristique, de la réaction qui se produit dans le mélange (B), qui est confirmée
par Ia valeur trouvée de ty,
4- Dans le but d'augmenter expérimentalement la valeur de ty pour le mélange (B), préciser, en le justifiant, si
chacun des cas suivants y convient :
a augmenter la quantité d°acide sulfurique
b- ¢liminer, par un moyen approprié, ia quantité d’eau au fur et & mesure qu'elle se forme.
Exercice2 (4 points)
Toutes les solutions sont considérées & 25 °C. température a laquelle pK, = 14.
‘On considére une solution aqueuse (Sq) d’un acide faible AH de concentration C, = 0,1 mol et de
pH =2,9. On suppose que I’on pourra négliger les ions dus ionisation propre de T’eau.
1- Dresser le tableau descriptif d’avancement volumique noté y, relatif a la réaction de I’acide AH avec l'eau.
a/s
2 a- Exprimer le taux d’avancement final ty, de la réaction de l'acide AH avec eau, en fonction du. pH et de
Cq. Calculer la valeur de ty.
10°",
it,
¢- Vérifier que le pK, du couple AH/ A’ s'écrit: pK, = pH - logry. Indiquer approximation utilisé
3. Maintenant, on prépare, par dilution eau distllée & partir de (Sq), deux solutions aqueuses (Sa1) et (Sas)
de méme volume V = 50 ml et de concentrations respectives C41 et Caa. En fait, pour obtenir (Sax), on
dilue deux fois un volume voy de (Sa) et pour obtenir (S42) on dilue dix fois un volume vex de (Sa).
a- Préciser la valeur de vor.
b- Décrire brigvement le mode opératoire qui permet de préparer (Sx) en indiquant le matériel adéquat.
On dispose de: un flacon d’un litte de (Sx); une pissette remplie d'eau distillée ; fioles jaugées de
50 mL, 100 mL et 250 mL ; béchers de 100 mL ; pipettes jaugées de 3 mL, 10 mL et 25 mL ; agitateur.
& Les concentrations, les pH des solutions
'b- Montrer que la constante d’acidité K, du couple acide / base AW / A’, peut s’écrire : Ky=
précédentes et les valeurs des ty correspondants | Solution _ |S) [Se] Gx) |
sont consignés dans le tableau ci-contre. Concentration (molt) | Ot | a |e
¢1- Reproduire puis compléter le tableau précédent | PH 2,90_| 3,05 |
en faisant les calculs nécessaires. % BIBS |» | :0,0398
x Calculer Ja valeur du pK, du couple AH / A”.
x Identifier, en le justifiant, le couple AH / A” parmi les couples donnés dans le tableau suivant :
Couple acide/ base
DKs
y | CH3CO.H/CH;COs HNO, /NOz
48 _ 33
Physique (13 points)
Exercice 1 (5,5 points)
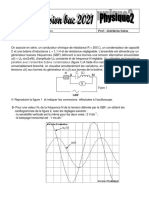
. Figure 1
Le pendule élastique de la figure 1 est constitué dun ressort ©
(R) & spires non jointives, de masse supposée négligeable et de =r ym .
raideur k, lié & un solide ($) de masse m qui peut se déplacer sur un AAJ ARIK.
plan horizontal ; ot |"énergie potentielle de pesanteur est suppose x’— +! >
nulle. A I’équilibre, le centre d'inertie G de (S) coincide avec oe
Vorigine O d'un repre (0,7) porté par un axe horizontal x'x, Dans ce repére, la position, de (S) & un instant t
donné, est repérée par son abscisse x(t) et sa vilesse instantanée est v(t).
A/Expérience 1
On écarte le solide (S) de sa position d’équilibre d'une distance d et on le Hiche sans vitesse initiale, il se
met a osciller. A ’aide d’un dispositif d'enregistrement appropri, on obtient la courbe de la figure 2 de Ia
page 5/5 représentant les variations de !’élongation x(Q),
1- Montrer que lors de son mouvement, le solide (S) est soumis a des forces de frottement,
2 On assimile la pseudopériode ‘Ta la période propre Ty des oscillations, Déterminer la fréquence propre No
des oscillations.
3- a- Exprimer I’énergie mécanique E du systéme {(R) + (S)} en fonction de m, k, x et v.
b- Soient Ep et E; les valeurs des énergies mécaniques du systtme {(R) + (S)}, respectivement aux instants
to = 0 ef t= 2Ty, On note Xme ct Xa, les amplitudes respectives des oscillations 4 ces deux instants.
EB, _ Xn
‘0 Xho
Montrer que
2s
Calculer —!., En déduire que E ne se conserve pas.
B/ Expérience 2
Les forces de frottements exercées sur Je solide sont équivalentes & une force de frottement visqueux
Ff = —h¥ ; oth est une constante positive et V’ est le vecteur vitesse instantanée du solide (S).
Un excitateur transmet au systéme {(R) + (S)} une force excitatrice F() paralléle a axe du ressort et
expression F () = Fosin(@2nNet). t, amplitude Fy constante et de fréquence Ne réglable.
Le systéme {(R) + (S)} oscille en régime sinusoidal foreé; ot Télongation de G s’écrit
x(t) = Xq.sin (ZxNet + gx) ; avec Xm son amplitude et x sa phase initiale, L"équation différentielle qui régit
Je mouvement de G s'éerit : nt + 1S + kx=
Pour une valeur Ny de la fréquence Ne de lexcitateur, on obtient la construction de Fresnel associée &
Péquation différentielle du mouvement du solide (S), telle que représentée par Ia figure 3 de la page 5/5 A
remplir par le candidat et a remettre avec sa copie
sin(2nN,.t).
1+ Compléter les indications qui manquent sur la construction de Fresnel de la figure 3 de Ia page 5/5.
2+ En utilisant la constru
de Fresnel, montrer que : ® 0,777. En déduire la valeur de Ny.
Ne
3- Sachant que k= 20 N.m", déterminer les valeurs de Xw», hy m et x.
4 On fait varier la fréquence Ne jusqu’é une valeur Ni, pour laquelle x(#) devient en quadrature retard de
phase par rapport 4 F(f). Montrer que, dans ce cas, le systéme {(R) + (S)} est le sidge d'un phénomene
physique particulier qu’on précisera son nom. Donner alors la valeur de Ni,
Exercice 2 (4,5 points)
Figure 4
On dispose d’un vibreur muni d’une fourche @ pointe
unique et d'une cuve ondes. Au repos, Ia pointe verticale
affleure 1a surface libre de la nappe d’eau de la cuve en un
point S. En mettant le vibreur en marche, la pointe impose au
point S des vibrations verticales sinusoidales de fréquence N
réglable qui se propagent a la célérité v. Les bords de la cuve a ondes sont tapissés de mousse pour éviter toute
réflexion des ondes (figure 4). On néglige amortissement des oné= et le phénomene de dilution de Pénergie
lors de la propagation des ondes. Le mouvement de S est étudié par rapport & un repére fixe (O,F'} vertical
ascendant, A Vinstant t= 0, Vorigine O coincide avec Ie point $ au repos, L’élongation y, de la source $ A un
instant € > 0, s’écrit
(t) = 2.10°sin(40nt + @,) : avec t exprimé en seconde et y, en métre.
¥s
1+ Ecrire I’équation horaire yyq(t) du mouvement d’un point M de la surface de l'eau, situé au repos, & une
distance radiale d= SM de la source 8.
2- La figure 5 de la page 5/5, schématise aspect de la surface de l'eau & un instant t= © a l’échelle 1/2 (20m
de la surface de l'eau correspondent a 1 cm sur la figure). Les points situés 4 la distance D = 4,5 em de S
sont atteints par les ébranlements a instant = 0.
Les crétes sont représentées par des cercles en traits continus, alors que les ereux sont représentés par des
cereles en pointillés.
a- Determiner, & partir de la figure 5, la valeur de la longueur d’onde 2.
b- Calculer la valeur de la célérité v de onde.
¢- Justifier qu’ V’instant t = @, I’élongation du point S est y,=- 2mm.
3/5
¢- Déterminer la valeur de 0.
€- Déterminer la phase initiale @, de ys.
£ Représenter, sans faite de calcul et en le justifiant, & échelle 1 (I em de la surface de I'eau correspond a
Jem sur la figure), aspect d’une coupe transversale de la surface de I’eau par un plan vertical passant
par le point $ 4 instant t=.
Dans cette partie, on excite périodiquement Ja surface de Figure 6
Peau a l'aide d’une régletie mince. On obtient des ondes
reetilignes progressives de célérité v = 0,4 ms" et de
fréquence N = 20 Hz. On place un obstacle muni d’une fente
F de largeur a, ~ 0,5 om sur le trajet des ondes (figure 6),
a Représenter, sur la figure 7 de la page S/S et al’échelle 1/2, aspect de la surface de eau au-dela de la
fente F en supposant que toute a surface de Peau est atteinte par onde. Justifier.
b- Justifier que la célérité de onde se conserve avant et aprés la fente F.
Exercice 3 (3 points) « Etude d'un document scientifique »
La demi-vie d’un radioélément
La période ou demi-vie d'un élément radioactif est définie comme le temps nécessaire pour que la
moitié des atomes de cet élément, initialement présent dans un échantillon, ait disparue par désintégration
radioactive. L’activité de Méchantillon, c’est-a-dire le nombre de désintégrations qui s"y produisent par seconde,
est done également divisée par deux au bout d’un laps de temps égal a une demi-vie. Lorsque la période d’un
élément radioactif atteint le million ou le milliard d’années, le temps nécessaire pour constater une diminution
de activité, et done en déduire la période, est trop long. Cependant, l'activité A, qui est inversement
proportionnelic & ia demi-vie T, est aussi proportionnelle au nombre N d’atomes, si bien qu'une mesure de
activité dun échantillon dont la concentration en radioélémenis est connue, permet un acces indirect & la
période. Cette mesure est rapide. Ainsi, un gramme uranium 238 pur, contenant 2,53.10"" atomes, produit
12400 désintégrations par seconde, ce qui permet de déduire une période d’environ 4,5 milliards d’années.
Toutefois, les difficultés expérimentales sont multiples: elles vont de lobtention d'un échantillon pur ne
contenant qu'un seul radioélément a la connaissance précise du rendement de détection et de la sélectivité de
Fappareil de mesure utilisé
La Recherche —le 01/07 / 2009 mensuel n° 432- Jean ~ Christophe Sabroux, IRSN Gif-sur-Yvette
On donne : 1 an = 31,536.10° s.
Pour répondre aux questions, on se référe au texte.
1- Donner la définition de chacun des termes suivants :
a- période T d'un élément radioactif ;
b- activité A d’un échantillon radioactif d'un élément donné.
2+ a- Dégager expression qui traduit la définition de I’activité A.
b-En déduire que: A = 9.8
3- Citer les difficultés expérimentales qu’on peut rencontrer lors de la détermination de la période d’un élément
radioactif.
ays
Signatures des
‘Section : N° d'inscription : Série ‘surveillants
Nom et prénom
Date et lieu de naissance
Epreuve : Sciences Physiques (section Mathématiques).
Feuille & remplir par le candidat et & remettre avec sa copie.
Physique - Exercice 1
Figure 3
Fa= 0,707 N
0,50N
Physique ~ Exercice 2
Figure 5 Figure 7
5/5
You might also like
- Her Body and Other Parties: StoriesFrom EverandHer Body and Other Parties: StoriesRating: 4 out of 5 stars4/5 (821)
- The Sympathizer: A Novel (Pulitzer Prize for Fiction)From EverandThe Sympathizer: A Novel (Pulitzer Prize for Fiction)Rating: 4.5 out of 5 stars4.5/5 (122)
- Devil in the Grove: Thurgood Marshall, the Groveland Boys, and the Dawn of a New AmericaFrom EverandDevil in the Grove: Thurgood Marshall, the Groveland Boys, and the Dawn of a New AmericaRating: 4.5 out of 5 stars4.5/5 (266)
- Team of Rivals: The Political Genius of Abraham LincolnFrom EverandTeam of Rivals: The Political Genius of Abraham LincolnRating: 4.5 out of 5 stars4.5/5 (234)
- A Heartbreaking Work Of Staggering Genius: A Memoir Based on a True StoryFrom EverandA Heartbreaking Work Of Staggering Genius: A Memoir Based on a True StoryRating: 3.5 out of 5 stars3.5/5 (231)
- Hidden Figures: The American Dream and the Untold Story of the Black Women Mathematicians Who Helped Win the Space RaceFrom EverandHidden Figures: The American Dream and the Untold Story of the Black Women Mathematicians Who Helped Win the Space RaceRating: 4 out of 5 stars4/5 (897)
- The Unwinding: An Inner History of the New AmericaFrom EverandThe Unwinding: An Inner History of the New AmericaRating: 4 out of 5 stars4/5 (45)
- The Yellow House: A Memoir (2019 National Book Award Winner)From EverandThe Yellow House: A Memoir (2019 National Book Award Winner)Rating: 4 out of 5 stars4/5 (98)
- The Emperor of All Maladies: A Biography of CancerFrom EverandThe Emperor of All Maladies: A Biography of CancerRating: 4.5 out of 5 stars4.5/5 (271)
- The World Is Flat 3.0: A Brief History of the Twenty-first CenturyFrom EverandThe World Is Flat 3.0: A Brief History of the Twenty-first CenturyRating: 3.5 out of 5 stars3.5/5 (2259)
- Shoe Dog: A Memoir by the Creator of NikeFrom EverandShoe Dog: A Memoir by the Creator of NikeRating: 4.5 out of 5 stars4.5/5 (537)
- The Little Book of Hygge: Danish Secrets to Happy LivingFrom EverandThe Little Book of Hygge: Danish Secrets to Happy LivingRating: 3.5 out of 5 stars3.5/5 (401)
- ReddmittlDocument5 pagesReddmittlJabri ImeneNo ratings yet
- Grit: The Power of Passion and PerseveranceFrom EverandGrit: The Power of Passion and PerseveranceRating: 4 out of 5 stars4/5 (590)
- Elon Musk: Tesla, SpaceX, and the Quest for a Fantastic FutureFrom EverandElon Musk: Tesla, SpaceX, and the Quest for a Fantastic FutureRating: 4.5 out of 5 stars4.5/5 (474)
- On Fire: The (Burning) Case for a Green New DealFrom EverandOn Fire: The (Burning) Case for a Green New DealRating: 4 out of 5 stars4/5 (74)
- The Subtle Art of Not Giving a F*ck: A Counterintuitive Approach to Living a Good LifeFrom EverandThe Subtle Art of Not Giving a F*ck: A Counterintuitive Approach to Living a Good LifeRating: 4 out of 5 stars4/5 (5807)
- The Hard Thing About Hard Things: Building a Business When There Are No Easy AnswersFrom EverandThe Hard Thing About Hard Things: Building a Business When There Are No Easy AnswersRating: 4.5 out of 5 stars4.5/5 (346)
- The Gifts of Imperfection: Let Go of Who You Think You're Supposed to Be and Embrace Who You AreFrom EverandThe Gifts of Imperfection: Let Go of Who You Think You're Supposed to Be and Embrace Who You AreRating: 4 out of 5 stars4/5 (1091)
- Never Split the Difference: Negotiating As If Your Life Depended On ItFrom EverandNever Split the Difference: Negotiating As If Your Life Depended On ItRating: 4.5 out of 5 stars4.5/5 (842)
- Serie2 PhysiquesDocument5 pagesSerie2 PhysiquesJabri ImeneNo ratings yet
- Serie1 ChimeDocument3 pagesSerie1 ChimeJabri ImeneNo ratings yet
- Correction Ex1 Physession 2020 Bac MathDocument1 pageCorrection Ex1 Physession 2020 Bac MathJabri Imene0% (1)
- Correction Ex1 Chimie Session 2020 Bac MathDocument1 pageCorrection Ex1 Chimie Session 2020 Bac MathJabri ImeneNo ratings yet
- Physique CDocument5 pagesPhysique CJabri ImeneNo ratings yet
- Serie 7 ChimieDocument6 pagesSerie 7 ChimieJabri ImeneNo ratings yet
- Equilibre ChimiqueDocument5 pagesEquilibre ChimiqueJabri ImeneNo ratings yet
- GesundheitDocument4 pagesGesundheitJabri ImeneNo ratings yet