Professional Documents
Culture Documents
سلسلة تمارين في وحدة المعايرة بالحل بلعمري
Uploaded by
benzaza bachirOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
سلسلة تمارين في وحدة المعايرة بالحل بلعمري
Uploaded by
benzaza bachirCopyright:
Available Formats
ثانوية اإلمام مالك بن أنس سيدي عيسى وزارة التربية الوطنية
التمرين()1
أعط أسماء األنواع الكٌمٌائٌة واكتب المعادالت النصفٌة للثنائٌات أساس/حمض التالٌة:
.
.
.
.
.
.
.
التمرين()2
من بٌن التفاعالت التالٌة ،حدد تلك التً تمثل تفاعل حمض-أساس:
.
.
.
.
التمرين()3
،ونضٌف لها من هٌدروجٌنوكربونات الصودٌوم ذي الصٌغة نضع فً دورق الكتلة
تدرٌجٌا محلوال مائٌا لكلور الهٌدروجٌن.
)1ما هً الثنائٌات أساس/حمض المشاركة ؟
)2أعط المعادلة النصفٌة الموافقة لكل ثنائٌة.
)3أكتب معادلة التفاعل الذي ٌتم فً الدورق.ما اسم الغاز الذي ٌنتج عن هذا التحول؟
الذي ٌجب صبه حتى ٌتوقف تكون )4أحسب الحجم لمحلول كلور الهٌدروجٌن ذي التركٌز
الغاز.
)5ما هو إذن حجم الغاز الناتج ؟
. نعطً الحجم المولً فً ظروف التجربة:
، ، ،
األستاذ :بلعمري براهيم الصفحة 1من 11
التمرين()4
انطالقا من حمض النترٌك التجاري الذي تحمل لصٌقته المعلومات التالٌة : نحضر محلوال مائٌا لحمض النترٌك
. ، ،
)1هل المحلول التجاري خالص أم هو محلول مائً لحمض النترٌك ؟ .علل جوابك .
تركٌز المحلول التجاري . )2أحسب
)3اكتب معادلة تفاعل حمض النترٌك مع الماء محددا كال من الحمض واألساس .
من حمض النترٌك ثم نصبه فً حوجلة عٌارٌة من فئة )4بواسطة ماصة معٌارٌة نأخذ حجما
ثم نضٌف الماء المقطر حتى الخط العٌاري فنحصل على محلول .
أ) ما اسم هذه العملٌة ؟ .
ب) أحسب تركٌز المحلول .
ج) أنشٌئ جدول التقدم لتفاعل حمض النترٌك مع الماء باعتبار الحمض متفاعال محدا .
من محلول هٌدروكسٌد الصودٌوم ذي التركٌز من المحلول مع حجم )5نمزج حجما
.
أ) أعط الصٌغة الكٌمٌائٌة لمحلول هٌدروكسٌد الصودٌوم .ثم أكتب معادلة ذوبان هٌدروكسٌد
الصودٌوم فً الماء .
ب) أعط الثنائٌات أساس/حمض الموجودة فً كل من محلول حمض النترٌك ومحلول هٌدروكسٌد
الصودٌوم .
ج) أكتب معادلة التفاعل الذي ٌحدث عند مزج المحلولٌن .
𝐿𝑚
. د) احسب الحجم لمحلول هٌدروكسٌد الصودٌوم الالزم الختفاء جمٌع شوارد
التمرين ()5
من الكتلة من ،المحلول ٌحتوي على ٌكتب صانع مادة للتنظٌف على القنٌنة اإلشارات التالٌة:
هٌدروكسٌد الصودٌوم.نرٌد،بواسطة المعاٌرة بقٌاس الناقلٌة التأكد من هذه النسبة.
. هو )1بٌن أن تركٌز هذا المحلول
)2للقٌام بهذه المعاٌرة ،نستعمل محلوال مائٌا لحمض كلور الماء تركٌزه
أكتب معادلة تفاعل المعاٌرة.
بعد من المحلول مرة للحصول على المحلول .نعاٌر الحجم )3نخفف المحلول
كل إضافة للمحلول المعاٌر نسجل القٌم الفعالة للتوتر بٌن قطبً خلٌة قٌاس المواصلة والتٌار المارفٌها.
نسجل القٌاسات فً الجدول التالً:
. أ) أحسب قٌمة الناقلٌة عند كل إضافة للحجم
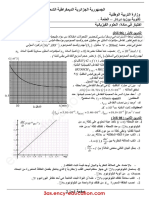
. ب) مثل البٌان
الحجم المضاف عند التكافؤ. ج) استنتج الحجم
األستاذ :بلعمري براهيم الصفحة 1من 11
. د) أحسب تركٌز شوارد الهٌدروكسٌد فً المحلول ثم فً المحلول
.هل النتٌجة مطابقة لتلك المعلن عنها من ه) أحسب النسبة المئوٌة الكتلٌة لهٌدروكسٌد الصودٌوم فً المحلول
طرف الصانع ؟
التمرين()6
لحمض اإلٌثانوٌك .لتحدٌد التركٌز المولً ٌحتوي محلول الخل التجاري على حمض اإلٌثانوٌك
من هذا المحلول المخفف ونعاٌره مرة .نأخذ حجما الموجود فً محلول الخل ،نحضر محلوال مخففا
. ذي تركٌز مولً بواسطة محلول هٌدروكسٌد الصودٌوم
. ٌساوي حجم المتفاعل المعاٌر المضاف عند التكافؤ
حدد الثنائٌتٌن أساس /حمض الداخلتٌن فً التفاعل الذي ٌحدث خالل هذه )1
−
𝑎𝑁 𝐻𝑂 المعاٌرة .واكتب المعادلة االجمالٌة.
فسر لماذا ٌكون من الضروري إضافة كاشف ملون فً الخلٌط. )2
أنجز جدول التقدم للجملة الكٌمٌائٌة عند التكافؤ ،ثم حدد كمٌة مادة حمض )3
اإلٌثانوٌك المعا ٌَر.
استنتج التركٌز لحمض اإلٌثانوٌك الموجود فً الخل التجاري. )4
𝐻𝑂𝑂𝐶 𝐻𝐶
التمرين()7
من محلول حمض كلور من مسحوق الحدٌد الخالص فً كأس ٌحتوي على الحجم نضع الكتلة
فنالحظ اختفاء كل الحدٌد عند نهاٌة التصاعد الغازي. تركٌزه الماء
المتفاعلتٌن. )1حدد الثنائٌتٌن
)2أكتب المعادلة النصفٌة اإللكترونٌة لكل ثنائٌة.
)3أكتب معادلة تفاعل أكسدة -ارجاع الحاصل.
)4أحسب حجم الغاز المتصاعد.
)5برهن على أن كمٌة مادة الحمض كانت بوفرة.
)6عند انتهاء التفاعل ،نضٌف الى محتوى الكأس قطرات من محلول مائً لهٌدروكسٌد الصودٌوم ،فٌتكون راسب
أخضر فاتح.
أ) ما اسم الراسب المتكون.
ب) أكتب معادلة التفاعل.
ج) أحسب كتلة الراسب.
. الحجم المولً:
األستاذ :بلعمري براهيم الصفحة 3من 11
التمرين()8
على لحمض كلور الماء تركٌزه المولً من محلول فً كأس ،نصب حجما
وٌتصاعد غاز ثنائً الهٌدروجٌن. من األلومنٌوم ،فتتكون شوارد األلومنٌوم كتلة
صف كٌف ٌمكنك إبراز وجود شوارد األلومنٌوم ؟ نفس السؤال بالنسبة لغاز ثنائً الهٌدروجٌن . )1
ما طبٌعة التفاعل الحاصل؟ )2
أكتب معدلة التفاعل معٌنا النوع المؤكسد والنوع المرجع. )3
أحسب كمٌتً المادة االبتدائٌتٌن للمتفاعلٌن. )4
أنشئ جدول التقدم وحدد المتفاعل المحد والتقدم األعظمً. )5
حدد حصٌلة المادة عند نهاٌة التفاعل. )6
أحسب التركٌز المولً لشوارد األلومنٌوم فً الكأس. )7
ما حجم غاز ثنائً الهٌدروجٌن المتصاعد ؟ . )8
. ،
التمرين()9
بمحلول برمنغنات البوتاسٌوم تركٌزه من حمض األوكسالٌك نعاٌر حجما
نحصل عند نقطة التكافؤ عند إضافة الحجم ( المحمض تركٌزه )
من المحلول المعاٌر.
⁄ و ⁄ الثنائٌتٌن الداخلتٌن فً التفاعل هما :
)1صف التجربة التً تمكن من القٌام بهذه المعاٌرة.
)2أكتب معادلة تفاعل المعاٌرة.
𝑞𝑎 𝐾( 𝑂𝑛𝑀 ) )3كٌف ٌتم التعرف على حجم التكافؤ ؟
𝑞𝑎
)4أنجز جدوال لتقدم التفاعل حتً نقطة التكافؤ.
التركٌز المولً لمحلول حمض األوكسالٌك. )5حدد
)6تم الحصول على محلول حمض األوكسالٌك بوضع الكتلة من
ثم إضافة الماء حتى الخط الحمض فً حوجلة من فئة
المعٌاري.
𝑂 𝐻 𝐶 أحسب قٌمة .
، ،
األستاذ :بلعمري براهيم الصفحة 4من 11
الحلول
التمرين()1
أسماء األنواع الكٌمٌائٌة وكتابة المعادالت النصفٌة للثنائٌات أساس/حمض التالٌة:
المعادالت النصفٌة للثنائٌات أساس/حمض أسماء األنواع الكٌمٌائٌة
الماء.
شاردة الهٌدرونٌوم
شاردة الهٌدروكسٌل
الماء.
شاردة النترات .
حمض النترٌك .
األمونٌاك .
شاردة األمونٌوم .
شاردة االٌثانوات .
حمض االٌثانوٌك .
هٌدروجٌنو كبرٌتات .
حمض الكبرٌت .
شاردة الكبرٌتات .
هٌدروجٌنو كبرٌتات .
التمرين()2
من بٌن التفاعالت التالٌة ،حدد تلك التً تمثل تفاعل حمض-أساس:
من حمض ثنائٌة الى أساس ثنائٌة أخرى . التفاعل حمض-أساس هو تفاعل ٌتم فٌه انتقال بروتون
. فهو تفاعل حمض-أساس إلى انتقل بروتون من
. فهو تفاعل حمض-أساس إلى انتقل بروتون من
. فهو تفاعل حمض-أساس إلى انتقل بروتون من
ال ٌوجد انتقال بروتون فهولٌس تفاعل حمض-أساس
التمرين()3
)1الثنائٌات أساس/حمض المشاركة .
معادلة ذوبان هٌدروجٌنو كربونات الصودٌوم فً الماء
. →
األستاذ :بلعمري براهيم الصفحة 5من 11
معادلة تفاعل كلور الهٌدروجٌن مع الماء:
.
. و ⁄ الثنائٌات المشاركة فً التفاعل
)2المعادلة النصفٌة الموافقة لكل ثنائٌة.
. المعادلة النصفٌة للثنائٌة
.
. ⁄ للثنائٌة المعادلة النصفٌة
)3أكتب معادلة التفاعل الذي ٌتم فً الدورق.ما اسم الغاز الذي ٌنتج عن هذا التحول؟
.
. الغاز الناتج هو ثنائً أوكسٌد الكربون
الذي ٌجب صبه حتى ٌتوقف تكون لمحلول كلور الهٌدروجٌن ذي التركٌز )4أحسب الحجم
الغاز.
.
. مساوٌة ل كمٌة مادة كلور الهٌدروجٌن التً ٌجب صبها لٌتوقف تكون
.
.
.
.
)5ما هو إذن حجم الغاز الناتج ؟.
.
.
.
التمرين()4
)1هل المحلول التجاري خالص أم هو محلول مائً لحمض النترٌك ؟ .علل جوابك .
. المحلول التجاري خالص ألن نسبة النقاوة
تركٌز المحلول التجاري . حساب )2
األستاذ :بلعمري براهيم الصفحة 6من 11
)3معادلة تفاعل حمض النترٌك مع الماء محددا كال من الحمض واألساس .
من حمض النترٌك ثم نصبه فً حوجلة عٌارٌة من فئة )4بواسطة ماصة معٌارٌة نأخذ حجما
ثم نضٌف الماء المقطر حتى الخط العٌاري فنحصل على محلول .
د) ما اسم هذه العملٌة ؟ .
اسم هذه العملٌة التمدٌد .
. تركٌز المحلول ه) أحسب
. وبالتالً
.
و) أنشٌئ جدول التقدم لتفاعل حمض النترٌك مع الماء باعتبار الحمض متفاعال محدا .
بوفرة
− بوفرة
− بوفرة
من محلول هٌدروكسٌد الصودٌوم ذي التركٌز مع حجم من المحلول )5نمزج حجما
.
أ) أعط الصٌغة الكٌمٌائٌة لمحلول هٌدروكسٌد الصودٌوم .ثم أكتب معادلة ذوبان هٌدروكسٌد الصودٌوم فً الماء .
. الصٌغة الكٌمٌائٌة لمحلول هٌدروكسٌد الصودٌوم :
. → معادلة ذوبان هٌدروكسٌد الصودٌوم فً الماء :
ب) أعط الثنائٌات أساس/حمض الموجودة فً كل من محلول حمض النترٌك ومحلول هٌدروكسٌد الصودٌوم .
. و
ج) أكتب معادلة التفاعل الذي ٌحدث عند مزج المحلولٌن .
. لمحلول هٌدروكسٌد الصودٌوم الالزم الختفاء جمٌع شوارد د) احسب الحجم
( )
األستاذ :بلعمري براهيم الصفحة 7من 11
.
.
التمرين ()5
. هو )1بٌن أن تركٌز هذا المحلول
.
.
)2أكتب معادلة تفاعل المعاٌرة.
بعد من المحلول مرة للحصول على المحلول .نعاٌر الحجم )3نخفف المحلول
كل إضافة للمحلول المعاٌر نسجل القٌم الفعالة للتوتر بٌن قطبً خلٌة قٌاس المواصلة والتٌار المار فٌها.
نسجل القٌاسات فً الجدول التالً:
. عند كل إضافة للحجم أ) أحسب قٌمة الناقلٌة
.
. ب) مثل البٌان
الحجم المضاف عند التكافؤ. ج) استنتج الحجم
.
ثم د) أحسب تركٌز شوارد الهٌدروكسٌد فً المحلول
فً المحلول
عند التكافؤ
( )
.
األستاذ :بلعمري براهيم الصفحة 8من 11
التمرين ()6
)1الثنائٌتٌن أساس /حمض الداخلتٌن فً التفاعل و المعادلة االجمالٌة. :
و
معادلة التفاعل:
)2تفسٌر ضروة اضافة كاشف ملون:
بما أن جمٌع األنواع المتفاعلة عدٌمة اللون ،فإنه من الضوري إضافة كاشف ملون .
)3جدول التقدم:
هً كمٌة مادة المتفاعل المعاٌر
الحالة االبتدائٌة بزٌادة
الحالة االنتقالٌة − − بزٌادة
الحالة النهائٌة − − بزٌادة
نستنتج أن كمٌة مادة حمض اإلٌثانوٌك المعا ٌَر هً:
. )4التركٌز
التركٌز المولً لحض اإلٌثانوٌك فً المحلول المخفف:
التمرين ()7
المتفاعلتان هما: )1الثنائٌتان
و
: )2المعادلة النصفٌة األلكترونٌة للثنائٌة
األستاذ :بلعمري براهيم الصفحة 9من 11
: المعادلة النصفٌة األلكترونٌة للثنائٌة
)3معادلة تفاعل أكسدة -ارجاع الحاصل:
)4لحساب حجم الغاز المتصاعد ننشئ جدول التقدم للتفاعل:
الحالة االبتدائٌة
الحالة االنتقالٌة − −
الحالة النهائٌة − −
بما أن الحدٌد اختفى كله فإنه المتفاعل المحد وبالتالً:
ومنه −
نجد من جدول التقدم
)5حسب جدول التقدم كمٌة مادة الحمض االبتدائٌة تساوي:
كمٌة مادة الحدٌد االبتدائٌة :
ومنه فإن الحمض موجود بوفرة. نالحظ أن: و لنقارن
)6اسم الراسب المتكون هو هٌدروكسٌد الحدٌد - IIصٌغته
− أ) معادلة التفاعل :
ب) حساب كتلة الراسب: -
حسب معادلة تفاعل الترسٌب:
من جهة أخرى :
نحصل على:
التمرين()8
ٌتم إبراز وجود األلومنٌوم فً محلول بواسطة محلول هٌدروكسٌد الصودٌوم ،إذ ٌتكون راسب أبٌض قابل الذوبان ٌ .تم
الكشف عن ثنائً الهٌدروجٌن بكونه ٌحدث تفرقعا بالقرب من لهب.
تفاعل أكسدة -ارجاع .
معادلة تفاعل أكسدة -ارجاع
. والمرجع هو المؤكسد هو
األستاذ :بلعمري براهيم الصفحة 11من 11
حساب كمٌة المادة لكل من المتفاعلٌن:
جدول التقدم
الحالة االبتدائٌة 0 0 بزٌادة
الحالة االنتقالٌة − − بزٌادة
الحالة النهائٌة − − بزٌادة
فإن − *إذا كان ℓهو المتفاعل المحد فإن :
فإن − هو المتفاعل المحد فإن: *إذا كان
. والمتفاعل المحد هو وبالتالً ٌكون التقدم األعظمً
حصٌلة المادة عند نهاٌة التفاعل:
− −
متفاعل محد. ألن
حساب تركٌز أٌونات األلومنٌوم:
حجم ثنائً الهٌدروجٌن المتصاعد: حساب
قانون الغاز المثالً
التمرين()9
من محلول حمض األوكسالٌك فً الكأس ،ونصب تدرٌجٌا محلول برمنغنات البوتاسٌوم من )1نصب الحجم
السحاحة حتى نقطة التكافؤ.
)2معادلة تفاعل المعاٌرة:
األستاذ :بلعمري براهيم الصفحة 11من 11
( )
)3تتمٌز نقطة التكافؤ بعدم اختفاء اللون البنفسجً الممٌز لمحلول برمنغنات البوتاسٌوم فً الكأس.
)4جدول التقدم :
ح ابتدائٌة بز بز
عند − − بز بز
التكافؤ
عند التكافؤ نكتب:
ومنه
. )5تركٌز الحمض فً المحلول المائً
. )6قٌمة
األستاذ :بلعمري براهيم الصفحة 11من 11
You might also like
- تمارين الأحماض و الأسسDocument1 pageتمارين الأحماض و الأسسmouad drouicheNo ratings yet
- سلسلة المكتسبات القبلية 2023 (جبالي رفيق)Document3 pagesسلسلة المكتسبات القبلية 2023 (جبالي رفيق)Hina BouzerzourNo ratings yet
- سلسلة المعايرةDocument3 pagesسلسلة المعايرةالغزيزال الحسن EL GHZIZAL HassaneNo ratings yet
- تجميعية اختبارات الفصل الأول هندسة الطرائق -تجميع الأستاذ بروال هانيDocument63 pagesتجميعية اختبارات الفصل الأول هندسة الطرائق -تجميع الأستاذ بروال هانيNounou Berhail100% (1)
- ملخص تفاعل محلول حمضي مع معدن مع تطبيقات السنة الرابعة متوسطDocument3 pagesملخص تفاعل محلول حمضي مع معدن مع تطبيقات السنة الرابعة متوسطAlaa AliNo ratings yet
- سلسلة تمارين المادة و تحولاتهاDocument4 pagesسلسلة تمارين المادة و تحولاتهاsomono momo100% (1)
- 2AS-019 - موضوع اختبار تجريبيDocument6 pages2AS-019 - موضوع اختبار تجريبيAmir OuerdiNo ratings yet
- Ground WaterDocument10 pagesGround WaterAbdulghani AsalaiNo ratings yet
- سلسلة تمارين 1Document5 pagesسلسلة تمارين 1lisaNo ratings yet
- سلسلة المراجعة في عطلة الشتاءDocument13 pagesسلسلة المراجعة في عطلة الشتاءFouad Ayadi100% (1)
- Orca Share Media1633638512013 6851976545494249941-ArDocument18 pagesOrca Share Media1633638512013 6851976545494249941-ArJojo BoubNo ratings yet
- حالة توازن مجموعة كيميائيةDocument7 pagesحالة توازن مجموعة كيميائيةالغزيزال الحسن EL GHZIZAL Hassane100% (1)
- 2 PDFDocument1 page2 PDFSmail Ain SemeneNo ratings yet
- أين كتلة المنحلDocument2 pagesأين كتلة المنحلAhmed BelguenouneNo ratings yet
- 1 F 8 CCDD 1 Edee 7130Document8 pages1 F 8 CCDD 1 Edee 7130I DNo ratings yet
- z1 Sewage Rev 2Document5 pagesz1 Sewage Rev 2TahirJabbarNo ratings yet
- 2-05-1 - تعيين كمية المادة عن طريق قياس الناقليةDocument34 pages2-05-1 - تعيين كمية المادة عن طريق قياس الناقليةInda MineNo ratings yet
- مسائل محلولة في الكيمياء التحليلية .Document24 pagesمسائل محلولة في الكيمياء التحليلية .فقدت طفلة في زمن الحرب100% (1)
- الفرض الثانيDocument2 pagesالفرض الثانيbebboukha yousra100% (2)
- TP Prof 2as 13Document3 pagesTP Prof 2as 13Mêly CrêâzyGîrl100% (1)
- سلسلة تمارين خرسانة مسلحةDocument13 pagesسلسلة تمارين خرسانة مسلحةahmedNo ratings yet
- Exercices Transf Rapidesett - LentesDocument2 pagesExercices Transf Rapidesett - LentesAbderrazak Aferyad100% (2)
- FicheElevPrem16 FaizaDocument48 pagesFicheElevPrem16 FaizaManouNo ratings yet
- 1-01-1 - بنية أفراد بعض النواع الكيميائيةDocument58 pages1-01-1 - بنية أفراد بعض النواع الكيميائيةNadia Ould AmarNo ratings yet
- االمعايرة الملوانيةDocument2 pagesاالمعايرة الملوانيةoukhitamazigh67% (3)
- دروس وتمارين في الكيمياء الحركية 1Document13 pagesدروس وتمارين في الكيمياء الحركية 1Zobir SaciNo ratings yet
- الوحدة 02 العمل والطاقة الحركية مخففةDocument12 pagesالوحدة 02 العمل والطاقة الحركية مخففةhouda midouNo ratings yet
- الطاقة الكامنةDocument6 pagesالطاقة الكامنةalaa eddineNo ratings yet
- المعايرة الحمضية القاعديةDocument4 pagesالمعايرة الحمضية القاعديةالغزيزال الحسن EL GHZIZAL Hassane100% (13)
- التتبع الزمني لتحول كيميائيDocument7 pagesالتتبع الزمني لتحول كيميائيالغزيزال الحسن EL GHZIZAL Hassane100% (5)
- الزراعة خارج التربةDocument3 pagesالزراعة خارج التربةFarid Cos100% (1)
- Almondjid - 3-02Document52 pagesAlmondjid - 3-02AMIRAFORTASNo ratings yet
- 3AS U01 - E3 - Cour-Exe 03 - 2Document35 pages3AS U01 - E3 - Cour-Exe 03 - 2kamelNo ratings yet
- ملخص الوحدة 4 الناقلية 2022 2023Document3 pagesملخص الوحدة 4 الناقلية 2022 2023badrNo ratings yet
- Physics 3se19 1trim4Document4 pagesPhysics 3se19 1trim4Nadia Bougherira100% (1)
- تمارين مقترحة حول دفع و كبح متحرك5Document3 pagesتمارين مقترحة حول دفع و كبح متحرك5aicha physiqueNo ratings yet
- الاتحاد الأوربي نحو اندماج شاملDocument3 pagesالاتحاد الأوربي نحو اندماج شاملBen FahNo ratings yet
- ابن طفيلDocument9 pagesابن طفيلMOHAMED MEKTANENo ratings yet
- دروس الفيزياء 3 متوسطDocument47 pagesدروس الفيزياء 3 متوسطfattahNo ratings yet
- تحلون الدم التواصل الهرمونيDocument12 pagesتحلون الدم التواصل الهرمونيkhadija missaouiNo ratings yet
- 2AS-016 - موضوع اختبار تجريبيDocument9 pages2AS-016 - موضوع اختبار تجريبيaicha physiqueNo ratings yet
- الوعي البيئيDocument5 pagesالوعي البيئيد. محمد عوضNo ratings yet
- 2AS U05 - E5 - Exercice 039 - تمرينDocument5 pages2AS U05 - E5 - Exercice 039 - تمرينladjaliyamina16No ratings yet
- تلخيص رواية جريمة في بيت الطالباتDocument5 pagesتلخيص رواية جريمة في بيت الطالباتFouad Haiag0% (1)
- ملف به 7وحدات ملخصات+تمارين+حلول لسنة 3 نهائي مادة علوم فيزيائية PDFDocument310 pagesملف به 7وحدات ملخصات+تمارين+حلول لسنة 3 نهائي مادة علوم فيزيائية PDFRanim Mouhamed100% (1)
- اسلسلة لتحولات النوويةDocument2 pagesاسلسلة لتحولات النوويةayman lamzouriNo ratings yet
- المطر الحمضيDocument13 pagesالمطر الحمضيamal amelNo ratings yet
- 2AS U02 - E3 - Cour-Exe 04 PDFDocument13 pages2AS U02 - E3 - Cour-Exe 04 PDFRodaina Hadji0% (1)
- السلسلة رقم 04 (المعايرة اللونية) الاستاذ عليوات عامرDocument3 pagesالسلسلة رقم 04 (المعايرة اللونية) الاستاذ عليوات عامرbeautyy100% (1)
- الوحدة الثالثة للسنة الثالثة كاملة جميع الشعب استثنائية ملكي عليDocument20 pagesالوحدة الثالثة للسنة الثالثة كاملة جميع الشعب استثنائية ملكي عليSmail Ain SemeneNo ratings yet
- UntitledDocument87 pagesUntitledDjamel AbdelliNo ratings yet
- ميكانيكا الموائع المتحركةDocument65 pagesميكانيكا الموائع المتحركةhaboooooosh1188100% (1)
- التحليل البعدي Dimensional AnalysisDocument4 pagesالتحليل البعدي Dimensional Analysisphysics4No ratings yet
- الطاقة الكامنة المرونيةDocument2 pagesالطاقة الكامنة المرونيةamine milano100% (1)
- Dzexams Docs 2as 904863Document12 pagesDzexams Docs 2as 904863Benmimoun WalidNo ratings yet
- Dzexams Docs 2as 904863Document13 pagesDzexams Docs 2as 904863AZ AMNo ratings yet
- 2as Serie 07Document20 pages2as Serie 07Ninou ZinouNo ratings yet
- الطبيعة القانونية لعقد العمل في القانون الجزائريDocument64 pagesالطبيعة القانونية لعقد العمل في القانون الجزائريAnonymous EOxpqDCFNo ratings yet
- MEISSA Mohamed PDFDocument235 pagesMEISSA Mohamed PDFbenzaza bachirNo ratings yet
- ملخص الديناميكا الحرارية PDFDocument3 pagesملخص الديناميكا الحرارية PDFbenzaza bachirNo ratings yet
- الصف الأول الثانوي - الكيمياء PDFDocument182 pagesالصف الأول الثانوي - الكيمياء PDFbenzaza bachirNo ratings yet
- MatlabDocument140 pagesMatlabEng MunaNo ratings yet
- 252505925 علم نفس النمو PDFDocument28 pages252505925 علم نفس النمو PDFbenzaza bachirNo ratings yet