Professional Documents
Culture Documents
Kémia: Emelt Szintű Írásbeli Vizsga
Uploaded by
language danishOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Kémia: Emelt Szintű Írásbeli Vizsga
Uploaded by
language danishCopyright:
Available Formats
Azonosító
jel:
2 0 0 9 . o k t ó b e r 2 8.
KÉMIA
EMELT SZINTŰ
ÍRÁSBELI VIZSGA
2009. október 28. 14:00
●
Az írásbeli vizsga időtartama: 240 perc
ÉRETTSÉGI VIZSGA
Pótlapok száma
Tisztázati
Piszkozati
OKTATÁSI ÉS KULTURÁLIS
MINISZTÉRIUM
Kémia emelt szint — írásbeli vizsga 0822
Kémia — emelt szint Azonosító
jel:
Fontos tudnivalók
• A feladatok megoldására 240 perc fordítható, az idő leteltével a munkát be kell fejeznie.
• A feladatok megoldási sorrendje tetszőleges.
• A feladatok megoldásához szöveges adatok tárolására nem alkalmas zsebszámológépet és
négyjegyű függvénytáblázatot használhat, más elektronikus vagy írásos segédeszköz hasz-
nálata tilos!
• Figyelmesen olvassa el az egyes feladatoknál leírt bevezető szöveget és tartsa be annak
utasításait!
• A feladatok megoldását tollal készítse! Ha valamilyen megoldást vagy megoldásrészletet
áthúz, akkor az nem értékelhető!
• A számítási feladatokra csak akkor kaphat maximális pontszámot, ha a megoldásban
feltünteti a számítás főbb lépéseit is!
• Kérjük, hogy a szürkített téglalapokba semmit ne írjon!
írásbeli vizsga 0822 2 / 16 2009. október 28.
Kémia — emelt szint Azonosító
jel:
1. Egyszerű választás
Írja be az egyetlen megfelelő betűjelet a válaszok jobb oldalán található üres cellába!
1. Melyik az a sor, amely kizárólag szabályos (tetraéder vagy síkháromszög) téralkatú,
delokalizált elektronokat tartalmazó összetett ion nevét tünteti fel?
A) Szulfátion, nitrátion, foszfátion.
B) Szulfátion, ammóniumion, oxóniumion.
C) Formiátion, ammóniumion, foszfátion.
D) Oxóniumion, acetátion, foszfátion. Nitrátion, ammóniumion, szulfátion.
2. Melyik az a sor, amely növekvő saverősségük szerint tünteti fel a savakat?
A) Hangyasav, ecetsav, fenol, szénsav, hidrogén-klorid.
B) Szénsav, fenol, hangyasav, ecetsav, hidrogén-klorid.
C) Fenol, szénsav, ecetsav, hangyasav, hidrogén-klorid.
D) Fenol, szénsav, hangyasav, ecetsav, hidrogén-klorid.
E) Hidrogén-klorid, hangyasav, ecetsav, fenol, szénsav.
3. Melyik sor tartalmazza olyan fémeknek a vegyjelét, amelyek a híg, illetve a tömény
kénsavoldat közül csupán az egyikben oldhatók fel?
A) Fe, Cu, Au
B) Zn, Mg, Al
C) Pb, Co, Zn
D) Fe, Cu, Al
E) Au, Mg, Zn
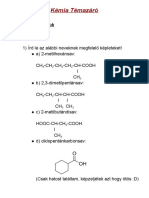
4. Melyik szerves molekulánál nem lép föl a térizoméria egyetlen fajtája sem?
A) tejsav
B) 2-metilpent-1-én
C) but-2-én
D) 2-klór-bután
E) borkősav
5. Grafitelektródok között elektrolizáljuk a következő sók vizes oldatát. 1930 C töltés
hatására melyik esetben tapasztalható a legnagyobb tömegű fém kiválása?
A) Alumínium-nitrát.
B) Réz-szulfát.
C) Nátrium-karbonát.
D) Króm(III)-klorid.
E) Cink-szulfát.
5 pont
írásbeli vizsga 0822 3 / 16 2009. október 28.
Kémia — emelt szint Azonosító
jel:
2. Esettanulmány
Olvassa el figyelmesen a szöveget és válaszoljon a kérdésekre!
Páros és páratlan számok a szerves kémiában
Ismeretes, hogy a nyíltláncú szerves vegyületek számos tulajdonsága függ attól is, hogy a
molekulát alkotó szénlánc páros vagy páratlan számú szénatomból áll. Ilyen sajátságok pl. az
alkánok olvadáspontja, az alkánsavak olvadáspontja, hármaspontja és olvadáshője. A
polimerkémiában ismert, hogy a párosszámú CH2-csoportot tartalmazó poliamidok és
poliészterek magasabb olvadáspontúak, mint a páratlan számúak. Érdekes különbség az is, hogy
az élő rendszerekben előforduló gliceridek és foszfolipidek szinte elhanyagolható
mennyiségben tartalmaznak páratlan szénatomszámú zsírsavrészeket. Ennek következménye
például az is, hogy a kőolajban sokkal nagyobb mennyiségben találunk páros szénatomszámú
komponenseket, míg a mesterségesen előállított krakkbenzinben nincs ilyen különbség a páros
és páratlan szénatomszámú termékek gyakoriságában.
A páros és páratlan szénatomszám hatását a vegyületek tulajdonságára egyszerűen
szemléltethetjük a telített, nyíltláncú dikarbonsavak oldhatóságának meghatározásával.
Készítsünk telített vizes oldatot a dikarbonsavak homológ sorának első 5 tagjából (amelyek
neve rendre: oxálsav, malonsav, borostyánkősav, glutársav, adipinsav)! Sav-bázis titrálással
(vagy egyszerűen az oldás során bekövetkezett tömegnövekedés mérésével) meghatározható a
telített oldatok koncentrációja, vagyis a dikarbonsavak oldhatósága.
Az oldhatóságok: oxálsav: 107 g/dm3, malonsav: 800 g/dm3, borostyánkősav: 75 g/dm3,
glutársav: 700 g/dm3, adipinsav: 20 g/dm3.
A jelenség egy lehetséges magyarázata az, hogy a páratlan szénatomszámú dikarbonsavak
esetén a két láncvégi karboxilcsoport cisz-helyzetű, a páros szénatomszámúakban transz-
helyzetű. Ez utóbbi esetben a molekulák között – az asszociátumok térbeli elrendeződéséből
következően – erősebb kölcsönhatás alakul ki szilárd fázisban, ezért kisebb az oldhatóságuk.
O
HO OH
O O
HO OH
O
O
HO OH
O
A borostyánkősav molekulaasszociátumai
HO O
O OH HO O
O OH
A glutársav hidrogénkötéseinek kedvezőtlenebb térbeli elrendeződése
Ezt támasztja alá a telítetlen négyszénatomos dikarbonsavak oldhatóságával kapcsolatos
tapasztalat is: a maleinsav (cisz-buténdisav) majdnem százszor jobban oldódik vízben, mint a
fumársav (transz-buténdisav).
(Journal of Chemical Education (1992/1.), a Kökélben (1997/4.) megjelent fordítása alapján)
írásbeli vizsga 0822 4 / 16 2009. október 28.
Kémia — emelt szint Azonosító
jel:
a) A tanultak és a szöveg alapján soroljon fel 3 tényezőt, ami meghatározza az alkánok
és alkánsavak olvadáspontját! Hogyan határozzák meg a felsorolt tényezők az
olvadáspontot?
b) „Az élő szervezetre jellemzőbb a páros szénatomszám.” Indokolja a szövegből vett 2
példával az állítás helyességét!
c) Adja meg az alkándisavak homológ sora 4. tagjának tudományos nevét!
d) Fejezze ki a malonsav oldhatóságát anyagmennyiség-koncentrációban!
e) Hasonlítsa össze a borostyánkősav és a glutársav vízben való oldhatóságát! Moláris
tömegük alapján melyiknél várható nagyobb oldhatóság? Indokolja az oldhatósági
értékeket!
11 pont
írásbeli vizsga 0822 5 / 16 2009. október 28.
Kémia — emelt szint Azonosító
jel:
3. Négyféle asszociáció
Az alábbiakban két anyagot kell összehasonlítania. Írja be a megfelelő betűjelet a táblázat
üres celláiba!
A) Szén-monoxid
B) Hidrogén
C) Mindkettő
D) Egyik sem
1. Molekulájában az atomok elérték a nemesgázszerkezetet.
2. Molekulája tartalmaz datív kötést.
3. Erősen dipólusos molekula.
4. 25 °C-on, standard nyomáson színtelen, szagtalan gáz.
5. Éghető gáz.
6. Víz alatt (vízen keresztül buborékoltatva) felfogható.
7. Hangyasavból vízelvonással előállítható.
8. Használják fémek előállítására.
9. Oxidálódhat és redukálódhat is.
9 pont
írásbeli vizsga 0822 6 / 16 2009. október 28.
Kémia — emelt szint Azonosító
jel:
4. Elemző feladat
Vizsgáljuk az alább felsorolt szerves vegyületek tulajdonságait!
A: glicin E: etil-klorid
B: benzol F: etil-acetát
C: piridin G: etén
D: metil-amin
A következő állítások mellé írja a fentiek közül a megfelelő anyag(ok) betűjelét, majd
válaszoljon a feltett kérdésekre!
a) Standard nyomáson, 25 °C-on szilárd halmazállapotú:
Milyen típusú rácsban kristályosodik?
b) Standard nyomáson, 25 °C-on színtelen, szúrós szagú, vízoldható gáz:
Reakciója vízzel (egyenlet):
c) Aromás vegyület, mely megfelelő körülmények között brómmal szubsztitúciós
reakcióba lép:
A reakció(k)ban kapott szerves termék(ek) neve(i):
d) Hidrogén-klorid vizes oldatával sav-bázis reakcióba lép:
e) Amfoter vegyület:
f) Melyik két vegyületre jellemző, hogy egyik a másikból egyetlen kémiai reakcióval
átalakítható:
Az egyik reakció egyenlete:
g) Nátrium-hidroxid-oldat hatására a reakcióban kétféle szerves anyag keletkezik
belőle:
A reakció egyenlete:
12 pont
írásbeli vizsga 0822 7 / 16 2009. október 28.
Kémia — emelt szint Azonosító
jel:
5. Táblázatos feladat
Töltse ki a táblázatot!
Sárga foszfor Nátrium
Alapállapotú atomjában a
– vegyértékelektron-szerkezet: 1. 4.
– párosítatlan elektronok száma: 2. 5.
– lezárt héjak betűjele: 3. 6.
Az elem rácstípusa: 7. 8.
Reakcióképesség (kicsi, nagy): 9. 10.
Tárolásának módja: 11. 12.
Mi történne, ha fordítva 13. 14.
helyeznénk el a két elemet a
tároló edényeikben? (Ahol van,
ott a reakció egyenletét is írja le!)
15. 16.
Levegőn történő égésének
reakcióegyenlete:
17.
Az égéstermék reakciója vízzel
(reakcióegyenlet):
Egy, a természetben előforduló 18.
ásványának neve és képlete:
11 pont
írásbeli vizsga 0822 8 / 16 2009. október 28.
Kémia — emelt szint Azonosító
jel:
6. Kísérletelemzés
Kísérletek réz-szulfáttal
a) Rézgálicot óvatosan hevítve, fehér, szilárd anyagot kapunk. Ha a rézgálicot oldjuk vízben,
az oldat lehűl, a kihevített rézgálic vizes oldatának elkészítésekor viszont az oldat
felmelegszik.
Írja fel a hevítés során bekövetkező változás reakcióegyenletét!
Mi állapítható meg a kísérletben szereplő anyagok oldáshőjéről?
rézgálicé: réz-szulfáté:
b) Réz(II)-szulfát-oldatba cinklemezt helyezünk.
Mit tapasztalunk?
Írja fel a folyamat ionegyenletét!
Ha az oldatba ezüstlemezt helyeztünk volna, vajon tapasztaltunk volna változást?
Miért?
c) Réz(II)-szulfát-oldathoz nátrium-hidroxid-oldatot öntünk. A kiváló csapadékot leszűrjük,
megszárítjuk, majd kihevítjük.
Írja fel a folyamatok reakcióegyenleteit!
Adja meg a kísérlet során keletkezett rézvegyületek színét!
d) Réz(II)-szulfát-oldathoz annyi ammóniaoldatot adagoltunk, hogy a kezdetben leváló
csapadék feloldódjon.
Milyen színű oldat keletkezett? Adja meg az oldat színét okozó részecske képletét!
e) Réz(II)-szulfát-oldatot csepegtetünk tojásfehérje oldatához.
Mit tapasztalunk?
Változna-e tapasztalatunk és hogyan, ha meglúgosított tojásfehérje-oldattal végeztük
volna el a kísérletet? Ha igen, hogyan?
12 pont
írásbeli vizsga 0822 9 / 16 2009. október 28.
Kémia — emelt szint Azonosító
jel:
7. Számítási feladat
10,0 gramm kalcium-karbonátot oldunk sztöchiometrikus mennyiségű salétromsav-oldatban.
A salétromsavoldat sűrűsége 1,16 g/cm3, tömegkoncentrációja 315 g/dm3.
A reakcióban keletkező gáz távozása után az oldatból elpárologtattunk 20,0 gramm vizet,
majd megmértük a kiváló kristályvízmentes só tömegét.
Adott hőmérsékleten 100 gramm víz 62,1 gramm vízmentes kalcium-nitrátot old.
a) Írja fel a reakció egyenletét!
b) Mekkora térfogatú salétromsavoldatban oldottuk a mészkövet?
c) Mekkora tömegű só vált ki a víz elpárologtatása után?
9 pont
írásbeli vizsga 0822 10 / 16 2009. október 28.
Kémia — emelt szint Azonosító
jel:
8. Számítási feladat
Zárt tartályban hidrogén- és nitrogéngázból 350 °C-on, katalizátor jelenlétében ammóniát
állítunk elő. Az egyensúlyi rendszerben kialakult koncentrációk a következők:
[H2] = 3,60 mol/dm3, [N2] = 1,20 mol/dm3, [NH3] = 0,540 mol/dm3.
a) Mekkora az egyensúlyi állandó értéke?
b) A bemért nitrogén, illetve hidrogén hány százaléka alakult át?
c) Számítsa ki az egyensúlyi gázelegy nyomását!
d) Mekkora volt a tartály térfogata, ha 1,00 kg ammóniát sikerült előállítanunk?
9 pont
írásbeli vizsga 0822 11 / 16 2009. október 28.
Kémia — emelt szint Azonosító
jel:
9. Számítási feladat
Egy standard nyomású, 25,0 °C-os gázelegy etánt és egy szintén két szénatomos amint tartal-
maz. A gázelegy a brómos vizet nem színteleníti el, sósavba vezetve viszont térfogatának
60,00%-a elnyelődik. A gázelegy 10,00 dm3-ét oxigéngázban tökéletesen elégetve 671,3 kJ hő
szabadul fel. (A forró füstgáz szén-dioxidot, vízgőzt, nitrogént és oxigént tartalmaz.)
Képződéshő adatok: ΔkH(C2H6(g)) = – 84,6 kJ/mol
ΔkH(CO2(g)) = – 394,0 kJ/mol ΔkH(H2O(f)) = – 286,0 kJ/mol
ΔkH((CH3)2NH(g)) = – 46,7 kJ/mol ΔkH(CH3CH2NH2(g)) = – 87,4 kJ/mol
a) Határozza meg a kiindulási gázelegy térfogatszázalékos összetételét!
b) Számítsa ki az etán, majd a kísérlet adataiból az ismeretlen amin égetésének
reakcióhőjét!
c) A rendelkezésére álló adatok segítségével, az ismeretlen képződéshőjének
kiszámításával azonosítsa az ismeretlen gázt és adja meg a nevét!
13 pont
írásbeli vizsga 0822 12 / 16 2009. október 28.
Kémia — emelt szint Azonosító
jel:
10. Számítási feladat
3,15 gramm kristályvíztartalmú oxálsavat vízben oldunk. Az így kapott oldat egytizede 12,5
cm3 térfogatú, 0,0800 mol/dm3 koncentrációjú kálium-permanganát-oldatot színtelenít el
kénsavas közegben, az alábbi (rendezendő!) reakcióegyenlet szerint:
KMnO4 + (COOH)2 + H2SO4 = K2SO4 + MnSO4 + CO2 + H2O
a) Oxidációs számok jelölésével rendezze a fent jelölt reakció egyenletét!
b) Határozza meg a kristályvizes oxálsav képletét!
7 pont
írásbeli vizsga 0822 13 / 16 2009. október 28.
You might also like
- Szerves Kemia PDFDocument62 pagesSzerves Kemia PDFMónika TamásNo ratings yet
- Kemia Teszt 8 DDocument16 pagesKemia Teszt 8 DDávid KisfalviNo ratings yet
- Kémia ZáróvizsgaDocument34 pagesKémia ZáróvizsgaDániel MassonNo ratings yet
- Kémia Témazáró 1Document7 pagesKémia Témazáró 1Dániel FincickyNo ratings yet
- Kémia: Emelt Szintű Írásbeli VizsgaDocument13 pagesKémia: Emelt Szintű Írásbeli Vizsgalanguage danishNo ratings yet
- E Kem 15maj FLDocument16 pagesE Kem 15maj FL123321iNo ratings yet
- Kémia: Írásbeli Érettségi - Felvételi Feladatok 2004Document8 pagesKémia: Írásbeli Érettségi - Felvételi Feladatok 2004DevrcsabiNo ratings yet
- K Kemia 05okt FLDocument16 pagesK Kemia 05okt FLNem JolikaNo ratings yet
- E Kem 15okt FLDocument16 pagesE Kem 15okt FL123321iNo ratings yet
- Kémia: Emelt Szintű Írásbeli VizsgaDocument12 pagesKémia: Emelt Szintű Írásbeli Vizsgalanguage danishNo ratings yet
- Kémia: Írásbeli Érettségi-Felvételi Feladatok 2003Document8 pagesKémia: Írásbeli Érettségi-Felvételi Feladatok 2003Csaba ÁrmósNo ratings yet
- E Kemia FLDocument16 pagesE Kemia FLBenyó LeventeNo ratings yet
- Kemiahazi 2020 Majus 1Document16 pagesKemiahazi 2020 Majus 1Gábor EngelbrechtNo ratings yet
- Kem1 Flap2f Oktv 2223Document12 pagesKem1 Flap2f Oktv 2223logikaijatek22No ratings yet
- Kémia: Írásbeli Érettségi-Felvételi Feladatok 1995Document5 pagesKémia: Írásbeli Érettségi-Felvételi Feladatok 1995Csaba ÁrmósNo ratings yet
- BAC 2020 Kemia Anorg 2.varians Oltean EvaDocument4 pagesBAC 2020 Kemia Anorg 2.varians Oltean EvaBéla KintelNo ratings yet
- Kemia Kozep Irasbeli MintaDocument22 pagesKemia Kozep Irasbeli MintaMónika SzegváriNo ratings yet
- Kémia: Írásbeli Érettségi-Felvételi Feladatok 1999Document6 pagesKémia: Írásbeli Érettségi-Felvételi Feladatok 1999Csaba ÁrmósNo ratings yet
- 2023-24 Kemia 10oszt I FordDocument3 pages2023-24 Kemia 10oszt I FordkovidoxagNo ratings yet
- Kemia Emelt Irasbeli MintaDocument21 pagesKemia Emelt Irasbeli MintaMónika SzegváriNo ratings yet
- E - D - Chimie - Anorganica - 2024 - Var - Simulare - LMA - CopieDocument2 pagesE - D - Chimie - Anorganica - 2024 - Var - Simulare - LMA - CopieMarin FlorinaNo ratings yet
- Értékelés Összesen: 100 PontDocument6 pagesÉrtékelés Összesen: 100 PontMelinda TörökNo ratings yet
- E Vegy 23okt UtDocument7 pagesE Vegy 23okt Utbaloghmilan10No ratings yet
- Kémia: Írásbeli Érettségi-Felvételi Feladatok 2000Document6 pagesKémia: Írásbeli Érettségi-Felvételi Feladatok 2000Csaba ÁrmósNo ratings yet
- Hevesy Keruleti 8 2020 FeladatlapDocument4 pagesHevesy Keruleti 8 2020 FeladatlapBori BorbélyNo ratings yet
- Problémafeladatok SzóbeliDocument4 pagesProblémafeladatok SzóbeliLuca DavidNo ratings yet
- E Vegy 21maj FLDocument12 pagesE Vegy 21maj FLren008No ratings yet
- E D Chimie Anorganica 2022 Var 01 LMADocument2 pagesE D Chimie Anorganica 2022 Var 01 LMAIrina BarboiuNo ratings yet
- E D Chimie Anorganica 2021 Var Simulare LMADocument2 pagesE D Chimie Anorganica 2021 Var Simulare LMAluminst68220% (1)
- Kémia: Írásbeli Érettségi-Felvételi Feladatok 1996Document6 pagesKémia: Írásbeli Érettségi-Felvételi Feladatok 1996Csaba ÁrmósNo ratings yet
- ZH 20160517Document2 pagesZH 20160517Reg KrechtNo ratings yet
- BAC 2020 Kemia Anorg 1.varians Oltean EvaDocument3 pagesBAC 2020 Kemia Anorg 1.varians Oltean EvaBéla KintelNo ratings yet
- C KérdésekDocument4 pagesC Kérdésekboszoky viragNo ratings yet
- Kem2 Flap2f Oktv 1617Document16 pagesKem2 Flap2f Oktv 1617wiimenudeNo ratings yet
- E D Chimie Anorganica 2019 Var 02 LMADocument3 pagesE D Chimie Anorganica 2019 Var 02 LMAadriancaraimanNo ratings yet
- 13 Hun Tour2 TaskDocument16 pages13 Hun Tour2 TaskNy KAÉNo ratings yet
- 04 Anyagi HalmazokDocument6 pages04 Anyagi HalmazokBence MészárosNo ratings yet
- Röpdolgozat (Oxigén, Nitrogén)Document2 pagesRöpdolgozat (Oxigén, Nitrogén)gabor23 /No ratings yet
- Szerves KémiaDocument30 pagesSzerves KémiaDudás DávidNo ratings yet
- Félévi Évvégi Tudásszintm 9 JavDocument20 pagesFélévi Évvégi Tudásszintm 9 JavZsuzsanna Kalmárné BarcsaiNo ratings yet
- E Kemma 19maj FLDocument16 pagesE Kemma 19maj FLegyzso20dNo ratings yet
- Javítóvizsga FeladatokDocument18 pagesJavítóvizsga FeladatokCiliNo ratings yet
- 05.1. KarbonsavakDocument30 pages05.1. KarbonsavakMónika GazdagNo ratings yet
- NEMFÉMES ELEMEK ÖsszefoglalásaDocument5 pagesNEMFÉMES ELEMEK ÖsszefoglalásaMarica BajánNo ratings yet
- K Kemia 07maj FLDocument16 pagesK Kemia 07maj FLRéka HegyiNo ratings yet
- E D Chimier Organica 2020 Test 02 LB MaghiaraDocument3 pagesE D Chimier Organica 2020 Test 02 LB MaghiaratomiNo ratings yet
- Szervetlen Kémia Dolgozat - Megoldások - Lénárt GergelyDocument9 pagesSzervetlen Kémia Dolgozat - Megoldások - Lénárt GergelypatriciaburutsNo ratings yet
- ZH 20180904 MegoldasokDocument2 pagesZH 20180904 MegoldasokReg KrechtNo ratings yet
- Tit 010 Chimie P 2023 Var 03 LMADocument3 pagesTit 010 Chimie P 2023 Var 03 LMAKatalin FülöpNo ratings yet
- Def 010 Chimie P 2019 Var 03 LMA PDFDocument2 pagesDef 010 Chimie P 2019 Var 03 LMA PDFMaria StanNo ratings yet
- I. Bevezetés A Kémiába ADocument2 pagesI. Bevezetés A Kémiába ARéka SzilágyiNo ratings yet
- 2023 II Fordulo II Kategoria FeladatDocument15 pages2023 II Fordulo II Kategoria FeladatDorner SáraNo ratings yet
- Péter Kovács - 9kémia - Oldatok - Oldodas - Ozmozis - FeladatokElmDocument5 pagesPéter Kovács - 9kémia - Oldatok - Oldodas - Ozmozis - FeladatokElmPéter KovácsNo ratings yet
- Szobeli 2023maj em MintatetelekDocument7 pagesSzobeli 2023maj em MintatetelekCinege ScratchNo ratings yet
- 2006 Orszagos MDocument6 pages2006 Orszagos Mvanyokrisztina444No ratings yet
- 00 Emelt Szintu Egyszeru Valasztasos Feladatok VegyesDocument68 pages00 Emelt Szintu Egyszeru Valasztasos Feladatok VegyesJajahhhNo ratings yet