Professional Documents
Culture Documents
ملخص في الترموديناميك
ملخص في الترموديناميك
Uploaded by
Kader Baghdad brahimCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
ملخص في الترموديناميك
ملخص في الترموديناميك
Uploaded by
Kader Baghdad brahimCopyright:
Available Formats
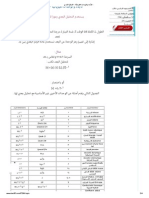
مول من غاز مثالي من الحالة 1إلى الحالة 2 تحول n
االنتالبية H الطاقة الداخلية U كمية احلرارة Q w العمل
)W=-n.R.T. ln(Vf /Vi حتول حتت حرارة اثبتة
H = 0 U = 0 Q = -W )W= n.R.T. ln(Pf /Pi
Transformations
isothermes): T = Cte
Qv = n Cv .T )W = -Pext .(Vf – Vi حتول حتت حجم اثبت
)H= nCp (T2-T1 )U= nCv (T2-T1 W=0
)Qv = nCv (T2-T1
Transformations
isochores: V = Cte
Qp = n Cp .T )W = -Pext .(V2 – V1 حتول حتت ضغط اثبت
)H= n Cp (T2-T1 )U= nCv (T2-T1 )W = -nR (T2 -T1
W nRT1 T2
)Qp = nCp (T2-T1
Transformations
isobares: P = Cte
حتول ادايابتيكي
)H= nCp (T2-T1 )U= nCv (T2-T1 Q=0 )W = nCv (T2-T1
Transformations
adiabatiques
تقاس كمية الحرارة عمليا انطالقا من العالقةQ = m.C.T : عبارة كمية الحرارة:
:Cالحرارة الكتلية ،)J/g. K( chaleur massiqueوتدعى أيضا بالحرارة النوعية ()chaleur spécifique
°
ولكون المسعر الحراري يحتوي على الماء ،فإن Cتمثل الحرارة الكتلية للماء و تساوي4,185 J/g.°K :
من اجل 1مول C p - Cv = R العالقة بين Cpو :Cv
العالقة بين UوHلغاز مثالي:
أو Qp= Qv + Δng RT ΔH = ΔU + Δng RT
عالقة كرشوف ):(Kirchhof
T
°
ΔH T = ΔH To + °
cpdT
To
(المتفاعالت) ( -Σ ni Cpالنواتج) Δ Cp = Σni Cp
من خالل مبدأ الحالة االبتدائية والحالة النهائية يمكن كتابة قانون Hessمن أجل التفاعل من الشكل: قانون :Hess
a A + b B — c C + d D
(المتفاعالت) ( – Σ ΔH°ƒالنواتج) ΔHr = ΣΔH°ƒ
ΔΗ οيرمز ألنطالبي التفاعل ،و ΔHοfيرمز ألنطالبي التشكل.
r
حساب أنطالبي التفاعل من خالل طاقات الروابط:
(النواتج) ( – Σ ΔH°dissالمتفاعالت) ΔHr = ΣΔH°diss
(النواتج) ( + Σ ΔH°fالمتفاعالت) ΔHr = ΣΔH°diss
ΔH°dissتكون دوما موجبة علما ان طاقة الربط ربط ΔHοf = Eتكون دوما سالبة أما
R=8.314 J.K-1.mol-1 = 2 Cal K-1.mol-1 = 0.082Latm K-1.mol-1 K-1.mol-1 ثابت الغازات
1Cal =4.18 J / 1atm =1.013.105pascal =1.01325 bar
أ :سالمة مختار
You might also like
- ملخص الديناميكا الحرارية PDFDocument3 pagesملخص الديناميكا الحرارية PDFSômè Ônë100% (3)
- قانون هوكDocument4 pagesقانون هوكIbrahim AlabdalyNo ratings yet
- Lab RebortDocument2 pagesLab RebortWegdan Aldobai83% (6)
- المقاطع الطولية والعرضيةDocument10 pagesالمقاطع الطولية والعرضيةAbdulla Hamid80% (5)
- المساحة التاكيومتريهDocument11 pagesالمساحة التاكيومتريهabsbond0% (2)
- ملخص الديناميكا الحرارية PDFDocument3 pagesملخص الديناميكا الحرارية PDFbenzaza bachir50% (2)
- سلسلة تمارين في الديناميككا الحراريةDocument13 pagesسلسلة تمارين في الديناميككا الحراريةamineNo ratings yet
- تعيين معامل للازوجة لسائل باستخدام قانون ستوكسDocument5 pagesتعيين معامل للازوجة لسائل باستخدام قانون ستوكسSaro H100% (1)
- تعيين معامل اللزوجة للجلسرين 00Document2 pagesتعيين معامل اللزوجة للجلسرين 00طه الحصنNo ratings yet
- التحليل البعدي Dimensional AnalysisDocument4 pagesالتحليل البعدي Dimensional Analysisphysics4No ratings yet
- قانون دارسيDocument12 pagesقانون دارسيabdullah80% (5)
- ايجاد ارتفاع الأهدافDocument9 pagesايجاد ارتفاع الأهدافislam hammad100% (1)
- التعرف على قانون بويلDocument2 pagesالتعرف على قانون بويلAhmad AbdNo ratings yet
- الأبعاد والوحدات الفيزيائية - التحليل البعديDocument2 pagesالأبعاد والوحدات الفيزيائية - التحليل البعديUnkownKïllêr0% (1)
- Vibrations Et Ondes1-TPDocument8 pagesVibrations Et Ondes1-TPليا ربتتذ0% (2)
- الشد السطحي 2Document30 pagesالشد السطحي 2mohammed kadhim100% (2)
- المعايرة الحمضية القاعديةDocument4 pagesالمعايرة الحمضية القاعديةالغزيزال الحسن EL GHZIZAL Hassane100% (13)
- تجربة البثقDocument13 pagesتجربة البثقابراهيم حسين خلف الجبوريNo ratings yet
- حلول سلسلة تمارين في الترموديناميكDocument12 pagesحلول سلسلة تمارين في الترموديناميكHichamHbbNo ratings yet
- ConductionDocument76 pagesConductionKorichiKarim100% (2)
- ميكانيك الموائع ع المحاضرة الأولىDocument14 pagesميكانيك الموائع ع المحاضرة الأولىBakheit LayliNo ratings yet
- المحاضرة الاولى ميكانيك الموائعDocument10 pagesالمحاضرة الاولى ميكانيك الموائعريگاي به هةشتNo ratings yet
- الفصل الثالث المبدأ الثانيDocument12 pagesالفصل الثالث المبدأ الثانيMohamed OuichaouiNo ratings yet
- الكروماتوغرافياDocument5 pagesالكروماتوغرافياsettou bouthGpNo ratings yet
- انحراف العوارض ذات الاسناد البسيط والاسناد المثبتDocument9 pagesانحراف العوارض ذات الاسناد البسيط والاسناد المثبتȚĥě Ł Ŏśț Ĥŏpě50% (2)
- مسائل محلولة في الكيمياء التحليلية .Document24 pagesمسائل محلولة في الكيمياء التحليلية .فقدت طفلة في زمن الحرب100% (1)
- تجميعية اختبارات الفصل الأول هندسة الطرائق -تجميع الأستاذ بروال هانيDocument63 pagesتجميعية اختبارات الفصل الأول هندسة الطرائق -تجميع الأستاذ بروال هانيNounou Berhail100% (1)
- الطاقة الكامنة الفتلية-عمل مخبري PDFDocument3 pagesالطاقة الكامنة الفتلية-عمل مخبري PDFKhairedine Latamna60% (5)
- مقاومةDocument6 pagesمقاومةȚĥě Ł Ŏśț Ĥŏpě50% (2)
- دروس و تمارين حول الزوايا المركزية و الزوايا المحيطيةDocument9 pagesدروس و تمارين حول الزوايا المركزية و الزوايا المحيطيةنصيحة كل يومNo ratings yet
- البندول البسيطDocument5 pagesالبندول البسيطseraj ibramem75% (8)
- 5 2545 244Document5 pages5 2545 244عمر ناجيNo ratings yet
- Physics 3se19 1trim4Document4 pagesPhysics 3se19 1trim4Nadia Bougherira100% (1)
- تجربة عزم الالتواءDocument4 pagesتجربة عزم الالتواءMohammed AssadawiNo ratings yet
- تجربة 1Document4 pagesتجربة 1Mohammed AliraqiNo ratings yet
- مخططات الاطوارDocument20 pagesمخططات الاطوارComputer Apps100% (1)
- 5 - القدمة ذات الورنيةDocument5 pages5 - القدمة ذات الورنيةMostafa Ahmed Zein100% (1)
- Mass TransferDocument6 pagesMass TransferErfan Ali100% (3)
- فيزياء تمارين محلولةDocument8 pagesفيزياء تمارين محلولةحمزة الفيتوري100% (1)
- Publication 11 19618 460Document4 pagesPublication 11 19618 460muud uuudNo ratings yet
- تطبيق معادلة برنولي-مختبر فلود تجربة 2Document13 pagesتطبيق معادلة برنولي-مختبر فلود تجربة 2Murtez83% (6)
- تعيين معامل انكسار الزجاج باستDocument4 pagesتعيين معامل انكسار الزجاج باستAbody Dody50% (2)
- حرارة المحاضرة الأولىDocument6 pagesحرارة المحاضرة الأولىengineer63No ratings yet
- دروس وتمارين في الكيمياء الحركية 1Document13 pagesدروس وتمارين في الكيمياء الحركية 1Zobir SaciNo ratings yet
- معايرة حمض قوي بقاعدة قويةDocument5 pagesمعايرة حمض قوي بقاعدة قويةMeyaceen Geologist0% (1)
- كل ما يخصّ البروتوكولات التجريبية في الفيزياء PDFDocument16 pagesكل ما يخصّ البروتوكولات التجريبية في الفيزياء PDFdjilali belemehdiNo ratings yet
- امتحان تجريبي في الفيزياء مع التصحيح PDFDocument10 pagesامتحان تجريبي في الفيزياء مع التصحيح PDFzakkou100% (6)
- تقرير البندول البسيطDocument5 pagesتقرير البندول البسيطصالح الوايلي0% (1)
- حدود ميكانيك نيوتنDocument6 pagesحدود ميكانيك نيوتنCHAREFHAMMA100% (5)
- معامل اللزوجةDocument5 pagesمعامل اللزوجةAli Mohamed Khalil100% (1)
- خواص الموائعDocument38 pagesخواص الموائع84000008450% (2)
- تجربة انتقال الحرارة بالحمل و الاشعاعDocument10 pagesتجربة انتقال الحرارة بالحمل و الاشعاعhidar m0% (1)
- 2AsU9 2Document9 pages2AsU9 2Meriem AehNo ratings yet
- تقرير تجربة البندول البسيطDocument4 pagesتقرير تجربة البندول البسيططه الحصن100% (1)
- 1674892624593019Document7 pages1674892624593019rym.sd2017No ratings yet
- رسائل واطاريح الكيمياءDocument27 pagesرسائل واطاريح الكيمياءIbrahim Al-mswariNo ratings yet
- تقرير الفلود عبدالله حامد عبد الزهره جابر PDFDocument8 pagesتقرير الفلود عبدالله حامد عبد الزهره جابر PDFAbdulla HamidNo ratings yet
- البلوراتDocument54 pagesالبلوراتIyad Abou-Rabii100% (5)
- Pitot Static Tube - تقرير أنبوب بيتوت السكونDocument18 pagesPitot Static Tube - تقرير أنبوب بيتوت السكونEng.AhmedShamkhiNo ratings yet
- ملخص الديناميكا الحرارية PDFDocument3 pagesملخص الديناميكا الحرارية PDFfatmasalah707No ratings yet
- الديناميكا الحرارية La Thermodynamique هندسة الطرائق ثالثة ثانويDocument18 pagesالديناميكا الحرارية La Thermodynamique هندسة الطرائق ثالثة ثانويKader Baghdad brahimNo ratings yet
- مبحث خاص فى اسم الله تعالىDocument8 pagesمبحث خاص فى اسم الله تعالىKader Baghdad brahimNo ratings yet
- تعريف الارطفونياDocument1 pageتعريف الارطفونياKader Baghdad brahimNo ratings yet
- الديناميكا الحرارية La thermodynamique هندسة الطرائق ثالثة ثانويDocument18 pagesالديناميكا الحرارية La thermodynamique هندسة الطرائق ثالثة ثانويKader Baghdad brahim100% (2)
- تعريف الارطفونياDocument1 pageتعريف الارطفونياKader Baghdad brahim100% (1)
- مبحث خاص فى اسم الله تعالىDocument8 pagesمبحث خاص فى اسم الله تعالىKader Baghdad brahimNo ratings yet