Professional Documents
Culture Documents
Atomy I Cząsteczki - Zadania Zamknięte Test (Bez Widocznej Punktacji)
Uploaded by
zofiamasOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Atomy I Cząsteczki - Zadania Zamknięte Test (Bez Widocznej Punktacji)
Uploaded by
zofiamasCopyright:
Available Formats
Grupa A Klasa .................... Data ................
Imię .................................................................................. Liczba punktów ...... / ...... p. Ocena .............
Atomy i cząsteczki - zadania zamknięte
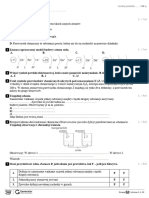
1 Przeanalizuj modele. Zaznacz poprawne dokończenia zdań.
1. 2. 3.
1. Zbiór atomów różnych pierwiastków chemicznych przedstawia model
A. 1 B. 2 C. 3
2. Cząsteczki tego samego związku chemicznego przedstawia model
A. 1 B. 2 C. 3
3. Cząsteczki różnych pierwiastków i cząsteczkę związku chemicznego przedstawia model
A. 1 B. 2 C. 3
2 Oceń prawdziwość podanych zdań. Zaznacz P, jeśli zdanie jest prawdziwe, lub F – jeśli jest fałszywe.
Dyfuzja to samorzutne wnikanie cząstek jednej substancji między cząstki
1. P F
drugiej substancji.
2. Zjawisko dyfuzji zachodzi tylko w cieczach. P F
3. Dyfuzja najwolniej zachodzi w cieczach. P F
4. Zjawisko dyfuzji jest dowodem na ziarnistą budowę materii. P F
3 Oblicz i przyporządkuj masy cząsteczkowe do związków chemicznych o podanych wzorach
sumarycznych.
1. H2S 2. MgS 3. MgO 4. H2O 5. SO2
A. 18 u B. 40 u C. 34 u D. 56 u E. 64 u
1. _____ 2. _____ 3. _____ 4. _____ 5. _____
4 Zaznacz zestaw wzorów sumarycznych tlenków uporządkowanych zgodnie ze zmniejszającą się masą
cząsteczkową.
A. CaO, NO, CO B. CO, NO, CaO C. NO, CaO, CO D. CaO, CO, NO
KNIJHODILJHQKIL Grupa A | strona 1 z 4
5 Ustal nazwę pierwiastka chemicznego X wchodzącego w skład związku chemicznego o wzorze X2O i masie
cząsteczkowej 44 u. Zaznacz poprawne dokończenie zdania.
Pierwiastkiem X jest
A. magnez. B. węgiel. C. wodór. D. azot.
6 W próbce jest 100 atomów chloru. 75 z nich stanowi izotop atomu 35Cl, a pozostałe 25 – izotop
atomu 37Cl. Oblicz liczbę neutronów w tej próbce i zaznacz poprawną wartość.
A. 1350 B. 500 C. 1850 D. 5000
7 Na uproszczonych modelach została przedstawiona budowa atomów pierwiastków chemicznych X, Y, Z.
Zaznacz poprawne uzupełnienie zdania (A–C) oraz jego uzasadnienie (1–3).
X Y Z
Budowę atomów izotopów tego samego pierwiastka chemicznego przedstawiają modele
Xi taką samą liczbę protonów i różną liczbę neutronów w jądrze
A. 1.
Y, atomowym.
Yi różną liczbę protonów i taką samą liczbę neutronów w jądrze
B. ponieważ mają 2.
Z, atomowym.
Xi
C. 3. taką samą liczbę elektronów walencyjnych.
Z,
8 Zaznacz poprawne dokończenia zdań.
1. Model przedstawia budowę atomu
A. azotu. B. fosforu. C. węgla.
2. Pierwiastek chemiczny w układzie okresowym znajduje się w
A. 2. okresie i 16. grupie. B. 5. okresie i 15. grupie. C. 2. okresie i 14. grupie.
3. Atom pierwiastka chemicznego zawiera
A. 5 elektronów walencyjnych. B. 4 elektrony walencyjne. C. 7 elektronów walencyjnych.
4. Atom pierwiastka chemicznego zawiera
A. 6 nukleonów. B. 8 nukleonów. C. 12 nukleonów.
KNIJHODILJHQKIL Grupa A | strona 2 z 4
9 Uczniowie zapisali konfigurację elektronową atomu glinu: 13Al: K2L8M3.
Zaznacz poprawne uzupełnienie zdania.
Najbliższym gazem szlachetnym dla atomu glinu jest
helowiec o konfiguracji elektronowej
A. K2L8
B. K2L8M8
C. K2
D. K2L8M18N8
10 Schemat przedstawia charakter chemiczny atomów pierwiastków chemicznych 1. i 17. grupy oraz 3. okresu.
Oceń prawdziwość podanych zdań. Zaznacz P, jeśli zdanie jest prawdziwe, lub F – jeśli jest fałszywe.
1. Najbardziej aktywnym niemetalem w 17. grupie jest fluor. P F
2. Najbardziej aktywnym metalem w 1. grupie jest lit. P F
KNIJHODILJHQKIL Grupa A | strona 3 z 4
11 Schemat przedstawia charakter chemiczny atomów pierwiastków chemicznych 1. i 17. grupy oraz 3. okresu.
Zaznacz poprawne dokończenia zdań.
1. Im więcej powłok elektronowych mają niemetale 17. grupy, tym
A. większy jest ich promień atomowy. B. mniejszy jest ich promień atomowy.
2. W 17. grupie w kierunku zwiększania się promienia atomowego pierwiastków chemicznych
A. zwiększa się ich aktywność chemiczna. B. zmniejsza się ich aktywność chemiczna.
12 Schemat przedstawia charakter chemiczny atomów pierwiastków chemicznych 1. i 17. grupy oraz 3. okresu.
Zaznacz poprawne uzupełnienie zdania (A–B) oraz jego uzasadnienie (1–2).
Zgodnie z kierunkiem strzałki aktywność pierwiastków 1. grupy
A. zmniejsza się, 1. zwiększa się zdolność do oddawania elektronów.
ponieważ
B. zwiększa się, 2. zwiększa się zdolność do przyjmowania elektronów.
KNIJHODILJHQKIL Grupa A | strona 4 z 4
Grupa B Klasa .................... Data ................
Imię .................................................................................. Liczba punktów ...... / ...... p. Ocena .............
Atomy i cząsteczki - zadania zamknięte
1 Przeanalizuj modele. Zaznacz poprawne dokończenia zdań.
1. 2. 3.
1. Cząsteczki tego samego związku chemicznego przedstawia model
A. 1 B. 2 C. 3
2. Cząsteczki różnych pierwiastków i cząsteczkę związku chemicznego przedstawia model
A. 1 B. 2 C. 3
3. Zbiór atomów różnych pierwiastków chemicznych przedstawia model
A. 1 B. 2 C. 3
2 Oceń prawdziwość podanych zdań. Zaznacz P, jeśli zdanie jest prawdziwe, lub F – jeśli jest fałszywe.
1. Zjawisko dyfuzji zachodzi tylko w cieczach. P F
Dyfuzja to samorzutne wnikanie cząstek jednej substancji między cząstki
2. P F
drugiej substancji.
3. Dyfuzja najwolniej zachodzi w cieczach. P F
4. Zjawisko dyfuzji jest dowodem na ziarnistą budowę materii. P F
3 Oblicz i przyporządkuj masy cząsteczkowe do związków chemicznych o podanych wzorach
sumarycznych.
1. SO2 2. H2O 3. MgO 4. MgS 5. H2S
A. 18 u B. 40 u C. 34 u D. 56 u E. 64 u
1. _____ 2. _____ 3. _____ 4. _____ 5. _____
KNIJHODILJHQKIL Grupa B | strona 1 z 4
4 Zaznacz zestaw wzorów sumarycznych tlenków uporządkowanych zgodnie ze zwiększającą się masą
cząsteczkową.
A. CaO, NO, CO B. CO, NO, CaO C. CaO, CO, NO D. NO, CaO, CO
5 Ustal nazwę pierwiastka chemicznego X wchodzącego w skład związku chemicznego o wzorze X2O i masie
cząsteczkowej 44 u. Zaznacz poprawne dokończenie zdania.
Pierwiastkiem X jest
A. wodór. B. azot. C. magnez. D. węgiel.
6 W próbce jest 100 atomów chloru. 75 z nich stanowi izotop atomu 35Cl, a pozostałe 25 – izotop
atomu 37Cl. Oblicz liczbę neutronów w tej próbce i zaznacz poprawną wartość.
A. 1350 B. 1850 C. 500 D. 5000
7 Na uproszczonych modelach została przedstawiona budowa atomów pierwiastków chemicznych X, Y, Z.
Zaznacz poprawne uzupełnienie zdania (A–C) oraz jego uzasadnienie (1–3).
X Y Z
Budowę atomów izotopów tego samego pierwiastka chemicznego przedstawiają modele
Xi różną liczbę protonów i taką samą liczbę neutronów w jądrze
A. 1.
Z, atomowym.
Yi taką samą liczbę protonów i różną liczbę neutronów w jądrze
B. ponieważ mają 2.
Z, atomowym.
Xi
C. 3. taką samą liczbę elektronów walencyjnych.
Y,
KNIJHODILJHQKIL Grupa B | strona 2 z 4
8 Zaznacz poprawne dokończenia zdań.
1. Model przedstawia budowę atomu
A. azotu. B. fosforu. C. węgla.
2. Pierwiastek chemiczny w układzie okresowym znajduje się w
A. 2. okresie i 14. grupie. B. 2. okresie i 16. grupie. C. 5. okresie i 15. grupie.
3. Atom pierwiastka chemicznego zawiera
A. 4 elektrony walencyjne. B. 2 elektrony walencyjne. C. 6 elektronów walencyjnych.
4. Atom pierwiastka chemicznego zawiera
A. 7 nukleonów. B. 12 nukleonów. C. 8 nukleonów.
9
Uczniowie zapisali konfigurację elektronową atomu glinu: 13Al: K2L8M3.
Zaznacz poprawne uzupełnienie zdania.
Najbliższym gazem szlachetnym dla atomu glinu jest
helowiec o konfiguracji elektronowej
A. K2L8M8
B. K2L8
C. K2
D. K2L8M18N8
10 Schemat przedstawia charakter chemiczny atomów pierwiastków chemicznych 1. i 17. grupy oraz 3. okresu.
Oceń prawdziwość podanych zdań. Zaznacz P, jeśli zdanie jest prawdziwe, lub F – jeśli jest fałszywe.
1. Najbardziej aktywnym metalem w 1. grupie jest lit. P F
2. Najbardziej aktywnym niemetalem w 17. grupie jest fluor. P F
KNIJHODILJHQKIL Grupa B | strona 3 z 4
11 Schemat przedstawia charakter chemiczny atomów pierwiastków chemicznych 1. i 17. grupy oraz 3. okresu.
Zaznacz poprawne dokończenia zdań.
1. Im więcej powłok elektronowych mają niemetale 17. grupy, tym
A. mniejszy jest ich promień atomowy. B. większy jest ich promień atomowy.
2. W 17. grupie w kierunku zwiększania się promienia atomowego pierwiastków chemicznych
A. zmniejsza się ich aktywność chemiczna. B. zwiększa się ich aktywność chemiczna.
12 Schemat przedstawia charakter chemiczny atomów pierwiastków chemicznych 1. i 17. grupy oraz 3. okresu.
Zaznacz poprawne uzupełnienie zdania (A–B) oraz jego uzasadnienie (1–2).
Zgodnie z kierunkiem strzałki aktywność pierwiastków 1. grupy
A. zwiększa się, 1. zwiększa się zdolność do oddawania elektronów.
ponieważ
B. zmniejsza się, 2. zwiększa się zdolność do przyjmowania elektronów.
KNIJHODILJHQKIL Grupa B | strona 4 z 4
Grupa C Klasa .................... Data ................
Imię .................................................................................. Liczba punktów ...... / ...... p. Ocena .............
Atomy i cząsteczki - zadania zamknięte
1 Ustal nazwę pierwiastka chemicznego X wchodzącego w skład związku chemicznego o wzorze X2O i masie
cząsteczkowej 44 u. Zaznacz poprawne dokończenie zdania.
Pierwiastkiem X jest
A. azot. B. magnez. C. węgiel. D. wodór.
2 Oceń prawdziwość podanych zdań. Zaznacz P, jeśli zdanie jest prawdziwe, lub F – jeśli jest fałszywe.
1. Zjawisko dyfuzji jest dowodem na ziarnistą budowę materii. P F
Dyfuzja to samorzutne wnikanie cząstek jednej substancji między cząstki
2. P F
drugiej substancji.
3. Dyfuzja najwolniej zachodzi w cieczach. P F
4. Zjawisko dyfuzji zachodzi tylko w cieczach. P F
3 Oblicz i przyporządkuj masy cząsteczkowe do związków chemicznych o podanych wzorach
sumarycznych.
1. H2O 2. SO2 3. H2S 4. MgS 5. MgO
A. 18 u B. 40 u C. 34 u D. 56 u E. 64 u
1. _____ 2. _____ 3. _____ 4. _____ 5. _____
4 Zaznacz zestaw wzorów sumarycznych tlenków uporządkowanych zgodnie ze zmniejszającą się masą
cząsteczkową.
A. CO, NO, CaO B. CaO, NO, CO C. NO, CaO, CO D. CaO, CO, NO
KNIJHODILJHQKIL Grupa C | strona 1 z 4
5 W próbce jest 100 atomów chloru. 75 z nich stanowi izotop atomu 35Cl, a pozostałe 25 – izotop
atomu 37Cl. Oblicz liczbę neutronów w tej próbce i zaznacz poprawną wartość.
A. 1850 B. 1350 C. 500 D. 5000
6 Na uproszczonych modelach została przedstawiona budowa atomów pierwiastków chemicznych X, Y, Z.
Zaznacz poprawne uzupełnienie zdania (A–C) oraz jego uzasadnienie (1–3).
X Y Z
Budowę atomów izotopów tego samego pierwiastka chemicznego przedstawiają modele
Xi różną liczbę protonów i taką samą liczbę neutronów w jądrze
A. 1.
Z, atomowym.
Yi taką samą liczbę protonów i różną liczbę neutronów w jądrze
B. ponieważ mają 2.
Z, atomowym.
Xi
C. 3. taką samą liczbę elektronów walencyjnych.
Y,
7 Zaznacz poprawne dokończenia zdań.
1. Model przedstawia budowę atomu
A. azotu. B. fosforu. C. węgla.
2. Pierwiastek chemiczny w układzie okresowym znajduje się w
A. 2. okresie i 15 grupie. B. 5. okresie i 15. grupie. C. 2. okresie i 16. grupie.
3. Atom pierwiastka chemicznego zawiera
A. 3 elektrony walencyjne. B. 2 elektrony walencyjne. C. 5 elektronów walencyjnych.
4. Atom pierwiastka chemicznego zawiera
A. 7 nukleonów. B. 8 nukleonów. C. 14 nukleonów.
8
Uczniowie zapisali konfigurację elektronową atomu glinu: 17Cl: K2L8M7.
Zaznacz poprawne uzupełnienie zdania.
Najbliższym gazem szlachetnym dla atomu chloru jest
helowiec o konfiguracji elektronowej
A. K2
B. K2L8
C. K2L8M8
D. K2L8M18N8
KNIJHODILJHQKIL Grupa C | strona 2 z 4
9 Schemat przedstawia charakter chemiczny atomów pierwiastków chemicznych 1. i 17. grupy oraz 3. okresu.
Oceń prawdziwość podanych zdań. Zaznacz P, jeśli zdanie jest prawdziwe, lub F – jeśli jest fałszywe.
1. Najmniej aktywnym metalem w 1. grupie jest lit. P F
2. Najmniej aktywnym niemetalem w 17. grupie jest fluor. P F
10 Schemat przedstawia charakter chemiczny atomów pierwiastków chemicznych 1. i 17. grupy oraz 3. okresu.
Zaznacz poprawne dokończenia zdań.
1. Im więcej powłok elektronowych mają metale 1. grupy, tym
A. większy jest ich promień atomowy. B. mniejszy jest ich promień atomowy.
2. W 1. grupie w kierunku zwiększania się promienia atomowego pierwiastków chemicznych
A. zmniejsza się ich aktywność chemiczna. B. zwiększa się ich aktywność chemiczna.
KNIJHODILJHQKIL Grupa C | strona 3 z 4
11 Schemat przedstawia charakter chemiczny atomów pierwiastków chemicznych 1. i 17. grupy oraz 3. okresu.
Zaznacz poprawne uzupełnienie zdania (A–B) oraz jego uzasadnienie (1–2).
Zgodnie z kierunkiem strzałki aktywność pierwiastków 17. grupy
A. zwiększa się, 1. zwiększa się zdolność do oddawania elektronów.
ponieważ
B. zmniejsza się, 2. zwiększa się zdolność do przyjmowania elektronów.
KNIJHODILJHQKIL Grupa C | strona 4 z 4
Grupa D Klasa .................... Data ................
Imię .................................................................................. Liczba punktów ...... / ...... p. Ocena .............
Atomy i cząsteczki - zadania zamknięte
1 Ustal nazwę pierwiastka chemicznego X wchodzącego w skład związku chemicznego o wzorze X2O i masie
cząsteczkowej 44 u. Zaznacz poprawne dokończenie zdania.
Pierwiastkiem X jest
A. magnez. B. azot. C. węgiel. D. wodór.
2 Oceń prawdziwość podanych zdań. Zaznacz P, jeśli zdanie jest prawdziwe, lub F – jeśli jest fałszywe.
1. Dyfuzja najwolniej zachodzi w cieczach. P F
Dyfuzja to samorzutne wnikanie cząstek jednej substancji między cząstki
2. P F
drugiej substancji.
3. Zjawisko dyfuzji jest dowodem na ziarnistą budowę materii. P F
4. Zjawisko dyfuzji zachodzi tylko w cieczach. P F
3 Oblicz i przyporządkuj masy cząsteczkowe do związków chemicznych o podanych wzorach
sumarycznych.
1. MgO 2. MgS 3. SO2 4. H2S 5. H2O
A. 18 u B. 40 u C. 34 u D. 56 u E. 64 u
1. _____ 2. _____ 3. _____ 4. _____ 5. _____
4 Zaznacz zestaw wzorów sumarycznych tlenków uporządkowanych zgodnie ze zwiększającą się masą
cząsteczkową.
A. CO, NO, CaO B. CaO, NO, CO C. CaO, CO, NO D. NO, CaO, CO
KNIJHODILJHQKIL Grupa D | strona 1 z 4
5 W próbce jest 100 atomów chloru. 75 z nich stanowi izotop atomu 35Cl, a pozostałe 25 – izotop
atomu 37Cl. Oblicz liczbę neutronów w tej próbce i zaznacz poprawną wartość.
A. 1350 B. 500 C. 5000 D. 1850
6 Na uproszczonych modelach została przedstawiona budowa atomów pierwiastków chemicznych X, Y, Z.
Zaznacz poprawne uzupełnienie zdania (A–C) oraz jego uzasadnienie (1–3).
X Y Z
Budowę atomów izotopów tego samego pierwiastka chemicznego przedstawiają modele
Xi taką samą liczbę protonów i różną liczbę neutronów w jądrze
A. 1.
Z, atomowym.
Xi różną liczbę protonów i taką samą liczbę neutronów w jądrze
B. ponieważ mają 2.
Y, atomowym.
Yi
C. 3. taką samą liczbę elektronów walencyjnych.
Z,
7 Zaznacz poprawne dokończenia zdań.
1. Model przedstawia budowę atomu
A. fosforu. B. azotu. C. węgla.
2. Pierwiastek chemiczny w układzie okresowym znajduje się w
A. 5. okresie i 15. grupie. B. 2. okresie i 16. grupie. C. 2. okresie i 15 grupie.
3. Atom pierwiastka chemicznego zawiera
A. 3 elektrony walencyjne. B. 5 elektronów walencyjnych. C. 2 elektrony walencyjne.
4. Atom pierwiastka chemicznego zawiera
A. 7 nukleonów. B. 14 nukleonów. C. 8 nukleonów.
8 Uczniowie zapisali konfigurację elektronową atomu glinu: 17Cl: K2L8M7.
Zaznacz poprawne uzupełnienie zdania.
Najbliższym gazem szlachetnym dla atomu chloru jest
helowiec o konfiguracji elektronowej
A. K2
B. K2L8M18N8
C. K2L8
D. K2L8M8
KNIJHODILJHQKIL Grupa D | strona 2 z 4
9 Schemat przedstawia charakter chemiczny atomów pierwiastków chemicznych 1. i 17. grupy oraz 3. okresu.
Oceń prawdziwość podanych zdań. Zaznacz P, jeśli zdanie jest prawdziwe, lub F – jeśli jest fałszywe.
1. Najmniej aktywnym niemetalem w 17. grupie jest fluor. P F
2. Najmniej aktywnym metalem w 1. grupie jest lit. P F
10 Schemat przedstawia charakter chemiczny atomów pierwiastków chemicznych 1. i 17. grupy oraz 3. okresu.
Zaznacz poprawne dokończenia zdań.
1. Im więcej powłok elektronowych mają metale 1. grupy, tym
A. mniejszy jest ich promień atomowy. B. większy jest ich promień atomowy.
2. W 1. grupie w kierunku zwiększania się promienia atomowego pierwiastków chemicznych
A. zwiększa się ich aktywność chemiczna. B. zmniejsza się ich aktywność chemiczna.
KNIJHODILJHQKIL Grupa D | strona 3 z 4
11 Schemat przedstawia charakter chemiczny atomów pierwiastków chemicznych 1. i 17. grupy oraz 3. okresu.
Zaznacz poprawne uzupełnienie zdania (A–B) oraz jego uzasadnienie (1–2).
Zgodnie z kierunkiem strzałki aktywność pierwiastków 17. grupy
A. zmniejsza się, 1. zmniejsza się zdolność do przyjmowania elektronów.
ponieważ
B. zwiększa się, 2. zmniejsza się zdolność do oddawania elektronów.
KNIJHODILJHQKIL Grupa D | strona 4 z 4
You might also like
- Kornelia 3 Unit Test - EkowydrukDocument38 pagesKornelia 3 Unit Test - EkowydrukMagdalena BorysNo ratings yet
- Atomy I Cząsteczki - Zadania Otwarte I Zamknięte Test (Bez Widocznej Punktacji)Document12 pagesAtomy I Cząsteczki - Zadania Otwarte I Zamknięte Test (Bez Widocznej Punktacji)MonikaNo ratings yet
- Atomy I Czasteczki Zadania Otwarte I Zamkniete Test Z Widoczna PunktacjaDocument12 pagesAtomy I Czasteczki Zadania Otwarte I Zamkniete Test Z Widoczna PunktacjaPaulina Marasek0% (1)
- Sprawdzian NR 1 Dla Ucznia 20240207 072048Document5 pagesSprawdzian NR 1 Dla Ucznia 20240207 072048Krzysztof GogółNo ratings yet
- Budowa Atomu. Układ Okresowy Pierwiastków Chemicznych Test (Z Widoczną Punktacją)Document2 pagesBudowa Atomu. Układ Okresowy Pierwiastków Chemicznych Test (Z Widoczną Punktacją)gaciusjazgot100% (3)
- (.... / 1 PKT) ZadanieDocument4 pages(.... / 1 PKT) ZadanieMikołaj MaszczyńskiNo ratings yet
- Test (12) AtomDocument4 pagesTest (12) AtomModne Ciuszki AniaNo ratings yet
- Sprawdzian 1 Budowa Atomu Uklad Okresowy Pierwiastkow Chemicznych Grupa ADocument1 pageSprawdzian 1 Budowa Atomu Uklad Okresowy Pierwiastkow Chemicznych Grupa ANatan Smogór77% (13)
- Klasa 7 Atom I Układ Okresowy Pierwiastków Chemicznych Test (Z Widoczną Punktacją)Document11 pagesKlasa 7 Atom I Układ Okresowy Pierwiastków Chemicznych Test (Z Widoczną Punktacją)КУСЬ 2009100% (1)
- Dział. IV. Łączenie Się Atomów. Równania I Reakcje Atomów. Test - EkowydrukDocument23 pagesDział. IV. Łączenie Się Atomów. Równania I Reakcje Atomów. Test - Ekowydrukmalkossa02No ratings yet
- WIAZANIA CHEMICZNE GENERATOR Test Z Widoczna PunktacjaDocument10 pagesWIAZANIA CHEMICZNE GENERATOR Test Z Widoczna Punktacjafilipowicz.goNo ratings yet
- Badani 1lo 1TDocument4 pagesBadani 1lo 1TJoanna BińczykNo ratings yet
- Chemia KL 8Document16 pagesChemia KL 8lena.mizgalskaaNo ratings yet
- Sprawdzian 1 Budowa Atomu Uklad Okresowy Pierwiastkow Chemicznych Grupa ADocument1 pageSprawdzian 1 Budowa Atomu Uklad Okresowy Pierwiastkow Chemicznych Grupa Aj.kaminskabozkoNo ratings yet
- Atomy I Cząsteczki-Klasa 7Document11 pagesAtomy I Cząsteczki-Klasa 7Ola Okońska82% (34)
- Chemia Kl. 7 Test. Łączenie Się Atomów. Równania Reakcji Chemicznych. Patrycja Suder 19.05.2020Document2 pagesChemia Kl. 7 Test. Łączenie Się Atomów. Równania Reakcji Chemicznych. Patrycja Suder 19.05.2020andem168No ratings yet
- Łączenie Się Atomów - Równania Reakcji Chemicznych.: Grupa - Strona 1 Z 4Document1 pageŁączenie Się Atomów - Równania Reakcji Chemicznych.: Grupa - Strona 1 Z 4Julia BochenekNo ratings yet
- Dział. III. Atomy I Cząsteczki Test (Z Widoczną Punktacją)Document24 pagesDział. III. Atomy I Cząsteczki Test (Z Widoczną Punktacją)Marzena Pakosz-Białasik100% (5)
- Atomy TestDocument22 pagesAtomy TestLuke K100% (1)
- Chemia SPP ZP Kl1 Sprawdzian 2 B Nowa EdycjaDocument4 pagesChemia SPP ZP Kl1 Sprawdzian 2 B Nowa Edycjabgrabuszynska7No ratings yet
- Sprawdzian Budowa Atomu Grupa A I B ZPDocument2 pagesSprawdzian Budowa Atomu Grupa A I B ZPTest100% (2)
- Sprawdzian 1 Budowa Atomu Uklad Okresowy Pierwiastkow Chemicznych Grupa BDocument1 pageSprawdzian 1 Budowa Atomu Uklad Okresowy Pierwiastkow Chemicznych Grupa Bakomorowska101No ratings yet
- Sprawdzian 1 Budowa Atomu Uklad Okresowy Pierwiastkow Chemicznych Grupa BDocument1 pageSprawdzian 1 Budowa Atomu Uklad Okresowy Pierwiastkow Chemicznych Grupa BNatan Smogór80% (5)
- Test 2 ChemiaDocument26 pagesTest 2 ChemiaWeronikaNo ratings yet
- Test Aczenie Sie Atomow. Rownania Reakcji Chemicznych Test Z Widoczna PunktacjaDocument8 pagesTest Aczenie Sie Atomow. Rownania Reakcji Chemicznych Test Z Widoczna PunktacjaTymek JaszczakNo ratings yet
- Budowa Atomu. Układ Okresowy Pierwiastków Chemicznych: WWW - Dlanauczyciela.pl Strona ZDocument1 pageBudowa Atomu. Układ Okresowy Pierwiastków Chemicznych: WWW - Dlanauczyciela.pl Strona ZWiktoria JugowiecNo ratings yet
- Powt.R1 Test (Z Widoczną Punktacją)Document18 pagesPowt.R1 Test (Z Widoczną Punktacją)natzg.comNo ratings yet
- AtomyDocument2 pagesAtomyMartyna GNo ratings yet
- Sprawdzian ZR Budowa AtomuDocument1 pageSprawdzian ZR Budowa AtomuPawełka GawełkaNo ratings yet
- Test AtomyDocument2 pagesTest Atomyx Cotton x Candy x0% (1)
- 1.1.test - Budowa AtomuDocument8 pages1.1.test - Budowa Atomubgrabuszynska7No ratings yet
- Sprawdzian 3 Atomy I Czasteczki Grupa DDocument2 pagesSprawdzian 3 Atomy I Czasteczki Grupa DAgnieszka Sacała100% (1)
- Sprawdzian 3 Atomy I Czasteczki Grupa D Compress 240109 170037Document2 pagesSprawdzian 3 Atomy I Czasteczki Grupa D Compress 240109 170037Emilka ŚNo ratings yet
- Ilona Włodarczyk Sprawdzian 1 Budowa Atomu Uklad Okresowy Pierwiastkow Chemicznych Grupa BDocument4 pagesIlona Włodarczyk Sprawdzian 1 Budowa Atomu Uklad Okresowy Pierwiastkow Chemicznych Grupa BJulianna Sitko67% (3)
- Łączenie Się Atomów-Klasa 7Document9 pagesŁączenie Się Atomów-Klasa 7Ola Okońska79% (19)
- Tes T Łączenie Się Atomów. Rów Nania Reakcji ChemicznychDocument9 pagesTes T Łączenie Się Atomów. Rów Nania Reakcji ChemicznychKarolNo ratings yet
- Łączenie Atomów. Równania GR ADocument3 pagesŁączenie Atomów. Równania GR AJulia ZawiślanNo ratings yet
- Atom - Grupa 2 - Praca KlasowaDocument3 pagesAtom - Grupa 2 - Praca KlasowafelicjaaNo ratings yet
- Budowa AtomuDocument5 pagesBudowa AtomuSonia GmińskaNo ratings yet
- Laczenie AtomowDocument2 pagesLaczenie AtomowGreta WinegretaNo ratings yet
- TestDocument13 pagesTestAlexander PiegzaNo ratings yet
- Atomy I Czasteczki 2 TestDocument2 pagesAtomy I Czasteczki 2 TestPaweł JankowskiNo ratings yet
- Chemia OrganicznaDocument2 pagesChemia OrganicznaZdzisławNo ratings yet
- Powtorzenie Wiadomosci Z Dzialu Laczenie Sie Atomow Rownania Reakcji Chemicznych 1Document2 pagesPowtorzenie Wiadomosci Z Dzialu Laczenie Sie Atomow Rownania Reakcji Chemicznych 1Greta WinegretaNo ratings yet
- Zadania Chemia Klasa 7Document6 pagesZadania Chemia Klasa 7bar1wirczarNo ratings yet
- Masy Atomu Węgla. Składniki. 1 12Document3 pagesMasy Atomu Węgla. Składniki. 1 12PiotrekNo ratings yet
- Sprawdzian 3 Atomy I Czasteczki Grupa CDocument2 pagesSprawdzian 3 Atomy I Czasteczki Grupa CAgnieszka Sacała100% (6)
- Przed Probna Matura SPR 1 2019Document9 pagesPrzed Probna Matura SPR 1 2019emiign0% (1)
- Sprawdzian 4 Laczenie Sie Atomow Rownania Reakcj 4Document2 pagesSprawdzian 4 Laczenie Sie Atomow Rownania Reakcj 4Patryk Paszko Baranowski100% (6)
- Test Eko-32Document4 pagesTest Eko-32Magdalena BorysNo ratings yet
- 4 Uklad OkresowyDocument15 pages4 Uklad OkresowygpfpbmgbvqNo ratings yet
- Sprawdzian 3 Atomy I Czasteczki Grupa DDocument2 pagesSprawdzian 3 Atomy I Czasteczki Grupa Dakomorowska101No ratings yet
- Wiązania Chemiczne - GR.BDocument2 pagesWiązania Chemiczne - GR.BDawid Makasa100% (1)
- Karta Pracy Laczenie Sie Atomow Rownania Reakcji ChemicznychDocument12 pagesKarta Pracy Laczenie Sie Atomow Rownania Reakcji Chemicznychj.kaminskabozkoNo ratings yet
- Arkusz - PALLADIUM - Kwiecień 2022Document22 pagesArkusz - PALLADIUM - Kwiecień 2022Mateusz JaskólskiNo ratings yet
- Kartkowka - Dzia 1 Tem. 456 Test Z Widoczna PunktacjaDocument4 pagesKartkowka - Dzia 1 Tem. 456 Test Z Widoczna PunktacjaAntoni AntoniNo ratings yet
- Sprawdzian 3 Atomy I Czasteczki GrupaDocument3 pagesSprawdzian 3 Atomy I Czasteczki GrupaOliwia Dulska100% (5)
- 27.03.2020r. Sprawdzian Z J. Polskiego kl.3-1Document3 pages27.03.2020r. Sprawdzian Z J. Polskiego kl.3-1zofiamasNo ratings yet
- 27.03.2020 R. Sprawdzian Z Matematyki Klasa 3.Document3 pages27.03.2020 R. Sprawdzian Z Matematyki Klasa 3.emiliachlebek87No ratings yet
- Atomy I Cząsteczki - Zadania Otwarte I Zamknięte Klucz OdpowiedziDocument4 pagesAtomy I Cząsteczki - Zadania Otwarte I Zamknięte Klucz OdpowiedzibeataNo ratings yet
- Atomy I Cząsteczki - Zadania Zamknięte Klucz OdpowiedziDocument5 pagesAtomy I Cząsteczki - Zadania Zamknięte Klucz OdpowiedzibeataNo ratings yet
- Az Szkolny 21-22 MatematykaDocument10 pagesAz Szkolny 21-22 MatematykazofiamasNo ratings yet
- Az Szkolny 22 23 MatematykaDocument14 pagesAz Szkolny 22 23 Matematykawikiwach3No ratings yet
- Kwiecien Nowi TropicieleDocument3 pagesKwiecien Nowi TropicielezofiamasNo ratings yet
- Inżynieria Chemiczna I ProcesowaDocument54 pagesInżynieria Chemiczna I ProcesowaMichał KisielewskiNo ratings yet
- Skrypt Do Cwiczen Z FarmakologiiDocument81 pagesSkrypt Do Cwiczen Z FarmakologiiAlicja JaśkiewiczNo ratings yet
- Test FizykaDocument4 pagesTest FizykaZuzanna Zet100% (2)
- Obróbka CieplnoDocument3 pagesObróbka Cieplnotomekaminski01No ratings yet
- Transport Leków Przez Błony BiologiczneDocument8 pagesTransport Leków Przez Błony BiologiczneJędrzej LisNo ratings yet
- TestDocument6 pagesTestJulia Czerniawska100% (2)