Professional Documents
Culture Documents
TP Le Dichlore
Uploaded by
Ouidad OUDADESSOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
TP Le Dichlore
Uploaded by
Ouidad OUDADESSCopyright:
Available Formats
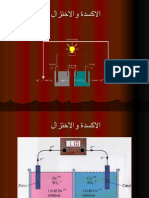
التفاعالت القسرية :التحليل الكهربائي
) 1التحوالت القسرية .
1ـ ) 1إجبار مجموعة كيميائية على تغيير منحى تطورها .
* تجربة : 1
نغمر مسحوق النحاس ) Cu (sفي محلول لثنائي البروم ). Br2(aq
حالة بدئية )(a حالة نهائية )(b
يتغير لون محلول ثنائي البروم بوجود النحاس الفلزي .
معادلة التفاعل تكتب على الشكل :
–Br2(aq) + 2 e )2 Br–(aq
)Cu(s –Cu2+(aq) + 2 e
)Br2(aq) + Cu(s )2 Br–(aq) + Cu2+(aq
المجموعة الكيميائية تتطور تلقائيا في المنحى المباشر .حيث تنتقل اإللكترونات مباشرة من النحاس نحو ثنائي البروم .
بعد مرور بعض الدقائق ،المجموعة ال تتطور ماكروسكوبيا :و صولها إلى حالة توازن .
* تجربة : 2
على العكس ،محلول يحتوي على أيونات النحاس (اا) و أيونات البرومور ال يخضع ألي تحول كيميائي .
لكن بتطبيق توتر كهربائي بين إلكترودين مغمورين في هذه المجوعة الكيميائية ،يؤدي إلى ظهور لون برتقالي جوار أحد
اإللكترودين ،بينما يتوضع جسم صلب أحمر على اإللكترود األخرى :يتكون على التوالي ثنائي البروم و النحاس .
األستاذ :عزيز العطور http://elotor.e-monsite.com Page 1
المجموعة الكيميائية في حالة توازن المجموعة الكيميائية بعد مرور التيار الكهربائي
و بذلك فإن المجموعة في هذه الحالة تتطور في المنحى المعاكس .حيث أن اإللكترونات تنتقل بطريقة غير مباشرة من أيونات
البرومور إلى أيونات النحاس (اا) بسبب وجود مولد كهربائي .
نقول بأننا أنجزنا تحوال قسريا ،أصبح ممكنا بسبب المولد الذي يفرض على المجموعة انتقال لإللكترونات .
1ـ ) 2تطور خارج التفاعل :
في حالة مجموعة كيميائية تتكون بدئيا من مسحوق النحاس ) Cu (sو محلول ثنائي البروم ) ، Br2(aqثابتة التوازن المقرونة
بالمعادلة :
– 2+
)Br2(aq) + Cu(s )2 Br (aq) + Cu (aq
2
Br Cu 2
Qr,i i i
0 هي ، K 1x1025و خارج التفاعل البدئي له التعبير :
2 i
Br
Br Cu 2 0 ألن :
i i
في هذه الحالة حيث ، Qr,i Kالمجموعة تتطور تلقائيا في المنحى المباشر .قيمة خارج التفاعل Q rتزداد خالل التحول و
تؤول إلى قيمة ثابتة التوازن . K
في حالة التجربة ( 2أيونات البرومور و أيونات النحاس اا ) المجموعة بدئيا في حالة توازن . Qr,i Kمرور التيار الكهربائي
المفروض من طرف المولد يسمح بحدوث تحول قسري يؤدي إلى تكون ثنائي البروم و النحاس بتفاعل أيونات النحاس (اا) و
أيونات البرومور .تراكيز أيونات البرومور و النحاس (اا) تنقص في الوسط التفاعلي ،بينما تركيز ثنائي البروم يزداد .
إلنجاز تحول قسري ،يجب التوفر على منبع خارجي يزود المجموعة الكيميائية بالطاقة الالزمة ،و يجبرها على
التطور في المنحى المعاكس للتطور التلقائي .
خالل تحول قسري ،على عكس التحول التلقائي ،يبتعد خارج التفاعل Q rعن ثابتة التوازن . K
األستاذ :عزيز العطور http://elotor.e-monsite.com Page 2
) 2التحليل الكهربائي .
2ـ ) 1تعريف :
التحليل الكهربائي تحول قسري ناتج عن مرور التيار الكهربائي المفروض من طرف مولد .المولد يمنح الطاقة الكهربائية الضرورية
إلجبار المجموعة الكيميائية على التطور في المنحى المعاكس للمنحى التلقائي ،و ذلك باالبتعاد عن حالة التوازن .
2ـ ) 2حركة حملة الشحنة الكهربائية .
اصطالحا منحى التيار الكهربائي من القطب الموجب للمولد نحو قطبه السالب .في اإللكترودين و في األجزاء الفلزية للدارة ،
اإللكترونات هي حملة الشحنة .و هي تتحرك في المنحى المعاكس لمنحى التيار الكهربائي .
كما في األعمدة ،األيونات هي حملة الشحنة في المحاليل .الكاتيونات ،المشحونة بشحنة موجبة ،تتحرك في منحى التيار ،
بينما األنيونات ،المشحونة بشحنة سالبة فإنها تتحرك في المنحى المعاكس لمنحى التيار .
2ـ ) 3التفاعالت التي تحدث جوار اإللكترودين .
اإللكترونات المحررة من طرف القطب السالب للمولد تكتسب من طرف نوع كيميائي في المحلول عند سطح اإللكترود المرتبطة
بهذا القطب .على مستوى هذه اإللكترود ،النوع الكيميائي يخضع لتفاعل إختزال .
2
). (Sn (aq 2C )(aq مثال :تحليل محلول كلورور القصدير )
2
) Sn (aqتكتسب إلكترونات عند سطح اإللكترود فتتحول إلى أيونات القصدير
2
)Sn (aq 2e )Sn (s ذرات القصدير الفلزي ): Sn (s
هذه الذرات تتوضع على إلكترود الغرافيت .
اإللكترونات الواردة على القطب الموجب للمولد ،قد حررت من طرف نوع كيميائي
موجود في المحلول ( أيونات ) ) C (aqفي تماس مع اإللكترود المرتبطة
بهذا القطب .يحدث تفاعل أكسدة لهذا النوع على مستوى هذه اإللكترود .
إذن أيونات الكلورور ) C (aqتفقد إلكترونات عند تماسها باإللكترود لتتحول إلى
2C )(aq C )2(aq 2e جزيئات ثنائي الكلور :
للكشف عن وجود ثنائي الكلور يمكن االستعانة ببعض قطرا النيلة )(indigo
حيث يزال لونها .
كاألعمدة ،اإللكترود التي تكون مقر تفاعل إختزال تسمى الكاتود .و اإللكترود التي تكون مقر تفاعل أكسدة
تسمى آنود .
2ـ ) 4حصيلة المادة لتحليل كهربائي .
نحصل على معادلة التفاعل لتحليل كهربائي بجمع أنصاف معادالت أكسدة ـ إختزال التي تحدث جوار كل إلكترود .مع مراعات أن
عدد اإللكترونات المكتسبة عند إلكترود يساوي عدد اإللكترونات المفقودة عند اإللكترود األخرى .
مثال :معادلة التفاعل للتحليل الكهربائي لمحلول حمض الكبريتيك .
2x –2 H+(aq) + 2 e )H2(g عند الكاتود :
)2 H2O (l O2(g) + 4 H+(aq) +4e- عند األنود :
)2 H2O(l )O2(g) + 2 H2(g الحصيلة :
األستاذ :عزيز العطور http://elotor.e-monsite.com Page 3
نالحظ أن حجم ثنائي الهيدروجين المتكون يساوي ضعف حجم ثنائي األوكسجين ،و هذا ما نالحظه بوضع أنبوب اختبار مملوء
بالماء و مقلوب على كل إلكترود ( .انظر الشكل أسفله ) :
خالل إنجاز تحليل كهربائي مدته tبواسطة تيار شدته ثابتة ، Iكمية الكهرباء Qالتي تمر عبر مقطع دارة كهربائية له التعبير:
Q I.t
هذه الكمية من الكهرباء مرتبطة بكمية مادة اإللكترونات ) n(eالمنتقلة من إلكترود إلى أخرى :
Fثابتة فرداي مع Q n(e ).F
بإنشاء جدول للتقدم ألحد التفاعالت الحاصلة عند اإللكترودين ،يمكن أن نجد عالقة بين كمية مادة اإللكترونات المنتقلة و كميات
المادة لمختلف االنواع الكيميائية المختزلة أو المؤكسدة .
* مثال :خالل التحليل الكهربائي لمحلول حمض الكبريتيك ،من التفاعل الحاصل عند األنود نحصل على الجدول الوصفي
التالي:
+ –
تفاعل األكسدة 2 H2O O2 + 4H + 4e
+
حالة المجموعة التقدم )n(H2O )n(O2 ) n(H )–n(e
الحالة البدئية 0 بوفرة 0 بوفرة 0
خالل التحول x بوفرة x بوفرة 4x
الحالة النهائية xf بوفرة xf بوفرة 4 xf
I t
n e 4 x f كمية مادة اإللكترونات المنتقلة خالل هذا التحليل تحقق العالقة :
F
I t
xf و منه :
4F
I t
n O 2 f x f نستنتج كمية مادة ثنائي األوكسجين المتكون عند اآلنود عند نهاية التحليل :
4F
كمية مادة االنواع الكيميائية المتكونة أو المستهلكة أثناء التحليل ترتبط بالمدة الزمنية tو شدة التيار المفروض من طرف
المولد .
يتوقف التحول القسري لمجموعة كيميائية :
ـ عندما يستهلك كليا أحد المتفاعالت .
ـ أو توقيفه بفتح الدارة الكهربائية .
) 3أمثلة تطبيقية .
3ـ ) 1المراكم Les accumulateurs :
نظريا اعتمادا على التحليل الكهربائي ،يمكن إعادة تكوين المتفاعالت المستهلكة في عمود .لكن ،أغلب األعمدة تحمل
اإلشارة " غير قابل للشحن " حيث أن التحليل الكهربائي لمكونات عمود مستهلك يمكن أن تؤدي إلى الحصول على غازات قادرة
على إتالف العمود .
إذن ال يجب محاولة شحن عمود مستهلك يحمل اإلشارة " غير قابل للشحن " .
هناك مجموعات كهروكيميائية قابلة للشحن ،حيث يمكن إعادة تكوين المتفاعالت بواسطة التحليل الكهربائي :نسميها مراكم.
مركم الرصاص ،المستعمل في بطاريات السيارات ،و المراكم القالئية المستعملة في األجهزة اإللكترونية ( الهاتف النقال ) ،
تمثل أغلب المراكم الموجودة في السوق .
األستاذ :عزيز العطور http://elotor.e-monsite.com Page 4
في مركم ،يحدث تفاعل تلقائي لألكسدة ـ إختزال خالل مرحلة التفريغ ( اشتغاله كعمود ) .على العكس ،خالل مرحلة
الشحن ،يكون مقر تحول قسري لألكسدة ـ إختزال ( اشتغاله كمحلل كهربائي ) .
اخترع سنة 9581من طرف ، Gaston Plantéيحتوي مركم الرصاص على إلكترود من الرصاص الخالص و إلكترود من الرصاص
تمت تغطيتها بثنائي أوكسيد الرصاص ) ) PbO2(s) ( (IVالمغمورة في محلول مائي لحمض الكبريتيك المركز .
مركم من الرصاص خالل تفريغه ،
حيث يشتغل كعمود .
التحول تلقائي .
اآلنود :صفيحة الرصاص الخالص
( التي تتأكسد )
عند الكاتود : PbO2 (s) + SO42-(aq) + 4 H+(aq) + 2 e- )PbSO4 (s) + 2 H2O(l
عند اآلنود : )Pb(s) + SO42-(aq PbSO4 (s) + 2 e-
الحصيلة ): PbO2 (s) + 2SO42-(aq) + 4H+(aq) + Pb(s )2 PbSO4 (s) + 2 H2O(l
شحن مركم الرصاص
يشتغل كمحلل كهربائي
التحول قسري
اآلنود :صفيحة الرصاص
الخالص ( إختزال ) PbSO4
التفاعالت في هذه الحالة عكس التفاعالت السابقة ( حالة التفريغ )
في الواقع ،بالنسبة للبطاريات المستعملة ،يتم تجميع عدة مراكم على التوالي للحصول على قدرة أكبر .كل مركم له قوة
كهرمحركة تقارب ، 2Vنجمع 6مركمات على التوالي للحصول على بطارية سيارة ذات . 12V
األستاذ :عزيز العطور http://elotor.e-monsite.com Page 5
3ـ ) 2تطبيقات صناعية
3ـ 2ـ ) 1التوضع الفلزي .
يستعمل التحليل الكهربائي لكي يحصل توضع بعض الفلزات ،مثل الذهب ،النحاس أو الزنك على أجسام موصلة للتيار
الكهربائي بهدف حمايتها من التأكسد أو لكي تصبح المعة .
يغمر الفلز المراد تغليفه ( تغطيته ) في محلول يحتوي على أيونات الفلز المتوضع .ثم نربطه بالقطب السالب للمولد لكي يلعب
دور الكاتود خالل التحليل الكهربائي .
3ـ 2ـ ) 2إنتاج ماء جافيل .
نحصل على ماء جافيل صناعيا بالتحليل الكهربائي لمحلول كلورور الصوديوم .
عند الكاتود –2 H2O(l) + 2 e )H2(g) + 2 HO–(aq
عند اآلنود )2 Cl–(aq )Cl2(g
الحصيلة )2 H2O(l) + 2 Cl–(aq )Cl2(g) + H2(g) + 2 HO–(aq
) (HO (aqيتفاعل مع أيونات الهيدروكسيد لكي نحصل على أنواع من بينها أيون تحت ثنائي الكلور الناتج في وسط قاعدي )
) C O(aqالنوع النشيط في ماء جافيل . كلوريت
)Cl2(g) + 2 HO–(aq )ClO–(aq) + Cl–(aq) + H2O(l
األستاذ :عزيز العطور http://elotor.e-monsite.com Page 6
You might also like
- (08) الباب الثامنDocument25 pages(08) الباب الثامنTaleen SakayanNo ratings yet
- 3- تحولات قسريةDocument4 pages3- تحولات قسريةالغزيزال الحسن EL GHZIZAL Hassane100% (1)
- Les Transformations Spontanées Dans Les Piles Et Production D'énergiDocument6 pagesLes Transformations Spontanées Dans Les Piles Et Production D'énergivbzrgNo ratings yet
- التحليل الكهربائي البسيطDocument4 pagesالتحليل الكهربائي البسيطdhiaa-eddine100% (2)
- التحليل الكهربائي البسيطDocument3 pagesالتحليل الكهربائي البسيطdhiaa-eddine100% (4)
- التحليل الكهربائي البسيطDocument4 pagesالتحليل الكهربائي البسيطdhiaa-eddine91% (11)
- Galvanic CellDocument14 pagesGalvanic CellMariam SadiqNo ratings yet
- ppt.درس الأعمدةDocument10 pagesppt.درس الأعمدةالغزيزال الحسن EL GHZIZAL Hassane100% (9)
- الأكسدة والإختزالDocument14 pagesالأكسدة والإختزالfaqed ilzakiraNo ratings yet
- 2- التحولات التلقائية في الأعمدة وتحصيل الطاقةDocument8 pages2- التحولات التلقائية في الأعمدة وتحصيل الطاقةالغزيزال الحسن EL GHZIZAL Hassane100% (1)
- الإمتحان الوطني للبكالوريا مادة الفيزياء والكيمياء الدورة الإستدراكية 2016 شعبة العلوم الرياضية أ و بDocument8 pagesالإمتحان الوطني للبكالوريا مادة الفيزياء والكيمياء الدورة الإستدراكية 2016 شعبة العلوم الرياضية أ و بAyoub SetineNo ratings yet
- Conductimytrie - CoursDocument6 pagesConductimytrie - CoursYoussef ArbaNo ratings yet
- 2ع ف دروس الدعم في الكيمياءDocument2 pages2ع ف دروس الدعم في الكيمياءmohamed yassine rghif100% (1)
- مذكرة الباب الرابع خالد صقر خليك اونلاين pdfDocument148 pagesمذكرة الباب الرابع خالد صقر خليك اونلاين pdfÃĤϻẸĎ ŴÃẸĹ ÃβẸĎNo ratings yet
- فرض محروس رقـم 4Document4 pagesفرض محروس رقـم 4HAMADA1972No ratings yet
- ي ناثلا باتكلا ليلاعت و فيراعت - ر شع يداحلا ءايميك - .أ .. يدنف هشيم - sara247 y @MaDocument5 pagesي ناثلا باتكلا ليلاعت و فيراعت - ر شع يداحلا ءايميك - .أ .. يدنف هشيم - sara247 y @MaOMARNo ratings yet
- Kim 318 ElectrolysisDocument18 pagesKim 318 ElectrolysisMariam SadiqNo ratings yet
- 2 - 4Document2 pages2 - 4Ayoub MahiNo ratings yet
- Altholat Alsriaa Oaltholat Albtiia Aldrs 3Document6 pagesAltholat Alsriaa Oaltholat Albtiia Aldrs 3Amine AlaoUii AlaouiNo ratings yet
- Altholat Alsriaa Oaltholat Albtiia Aldrs 3Document6 pagesAltholat Alsriaa Oaltholat Albtiia Aldrs 3Amine AlaoUii AlaouiNo ratings yet
- Dzexams 4am Physique 609343Document6 pagesDzexams 4am Physique 609343Hamou006No ratings yet
- Dzexams 4am Physique 339837Document4 pagesDzexams 4am Physique 339837Sarra RoseNo ratings yet
- ElectrolysisDocument7 pagesElectrolysisMariam SadiqNo ratings yet
- التحليل الكهربائيDocument18 pagesالتحليل الكهربائيkawthar 12mezealNo ratings yet
- 59028 - الباب 6هـ التوزيع الإلكتروني وأرقام الكمDocument22 pages59028 - الباب 6هـ التوزيع الإلكتروني وأرقام الكمamir gamalNo ratings yet
- المكافى الكيميائى الكهربى للنحاس 3Document11 pagesالمكافى الكيميائى الكهربى للنحاس 3Mohamed AalwiNo ratings yet
- 3- المحاليل الإلكتروليتية و التراكيزDocument10 pages3- المحاليل الإلكتروليتية و التراكيزMr GamerNo ratings yet
- Dzexams 4am Physique E1 20211 759792Document6 pagesDzexams 4am Physique E1 20211 759792ياسمين لقرافNo ratings yet
- الاختبار 1 س 4Document5 pagesالاختبار 1 س 4miraNo ratings yet
- Dzexams Docs 2as 906580Document5 pagesDzexams Docs 2as 906580chaymachamchouma1225No ratings yet
- مقارنات خلايا الكتروليتيةDocument1 pageمقارنات خلايا الكتروليتيةHealthyATP 100No ratings yet
- الجدول الدوري و توازن جسم صلب خاضع 2و3 قوىDocument1 pageالجدول الدوري و توازن جسم صلب خاضع 2و3 قوىYASSINE CHAACHOUENo ratings yet
- إجابة امتحانات الباب الرابعDocument16 pagesإجابة امتحانات الباب الرابعMoaz EmamNo ratings yet
- Dzexams 4am Physique 388351Document4 pagesDzexams 4am Physique 388351Sarra RoseNo ratings yet
- Instrumental Chapter 3 ElectrochemicalDocument61 pagesInstrumental Chapter 3 ElectrochemicalElsayed ElazazyNo ratings yet
- استعد لبكالوريا2015 الموضوع6Document1 pageاستعد لبكالوريا2015 الموضوع6Med BiologisteNo ratings yet
- Dzexams 4am Physique 787017Document6 pagesDzexams 4am Physique 787017mehdiihaddadene12No ratings yet
- Dzexams Docs 3as 907655Document4 pagesDzexams Docs 3as 907655maadzha14No ratings yet
- - نسخة Exercise-2 (1) copyDocument6 pages- نسخة Exercise-2 (1) copysafNo ratings yet
- 3as Phy Cour U1 KichahDocument16 pages3as Phy Cour U1 Kichahapi-238281709No ratings yet
- 2s CompoDocument2 pages2s Compoamine milanoNo ratings yet
- سلسلة تمارين حول الأعمدة وتحصيل الطاقةDocument3 pagesسلسلة تمارين حول الأعمدة وتحصيل الطاقةPhobos ElfaNo ratings yet
- التركيز والمحاليل الإلكتروليتيةDocument3 pagesالتركيز والمحاليل الإلكتروليتيةKhalid IdrissiNo ratings yet
- 2- التحولات التلقائية في الأعمدة وتحصيل الطاقة (Récupéré)Document7 pages2- التحولات التلقائية في الأعمدة وتحصيل الطاقة (Récupéré)HarounSamihNo ratings yet
- 2 التحولات التلقائية في الأعمدة وتحصيل الطاقةDocument8 pages2 التحولات التلقائية في الأعمدة وتحصيل الطاقةالغزيزال الحسن EL GHZIZAL HassaneNo ratings yet
- تمارين في الأعمدة والتحولات القسرية PDFDocument5 pagesتمارين في الأعمدة والتحولات القسرية PDFأبو أيوبNo ratings yet
- تمارين في الأعمدة والتحولات القسرية PDFDocument5 pagesتمارين في الأعمدة والتحولات القسرية PDFأبو أيوبNo ratings yet
- تمارين في التحولات القسرية PDFDocument5 pagesتمارين في التحولات القسرية PDFأبو أيوبNo ratings yet
- الاتحاد الكيميائى + 320 سؤالDocument20 pagesالاتحاد الكيميائى + 320 سؤالUsama Waly100% (1)
- ملخص الوحدة 6 الجزء الاول الاعمدة الكهربائية 2023Document3 pagesملخص الوحدة 6 الجزء الاول الاعمدة الكهربائية 2023Zaki LaidouneNo ratings yet
- بطارية الرصاص تفكك استبدالDocument4 pagesبطارية الرصاص تفكك استبدالع. خ. خNo ratings yet
- JDGDHDocument1 pageJDGDHYassineNo ratings yet
- Dzexams 1as Physique 471167Document3 pagesDzexams 1as Physique 471167Fight HeroNo ratings yet
- Ccond LouizaDocument12 pagesCcond LouizaAnonymous 0orlpwqkNo ratings yet
- ملخص الوحدة الثانية التحولات النووية PDFDocument7 pagesملخص الوحدة الثانية التحولات النووية PDFNour El Din Sayoud100% (1)
- سلسلة الأكسدة والإرجاع مع الحلول المفصلة - الأستاذ كريم سني 2022Document7 pagesسلسلة الأكسدة والإرجاع مع الحلول المفصلة - الأستاذ كريم سني 2022widad doudiNo ratings yet
- كيمياء الكهربية الباب الرابعDocument52 pagesكيمياء الكهربية الباب الرابعأحمد غياضNo ratings yet