Professional Documents
Culture Documents
أهم التعاريف ا+ المتابعة+ملخص+ مخطط PDF
Uploaded by
Amoula HayatieOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
أهم التعاريف ا+ المتابعة+ملخص+ مخطط PDF
Uploaded by
Amoula HayatieCopyright:
Available Formats
1
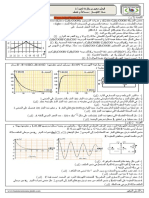
مخطط تمرين بكالوريا الوحدة1
في تمرين بكالوريا الوحدة 1دوما يعطى لنا تحول كيميائي بطيء وتام بين متفاعلين Aو Bحسب االحتماالت التالية:
االحتمال :1المتفاعلين Aو Bمحلولين مائيين حجمهما VAو VBيكون( ()VT=VA+VBحجم الوسط التفاعلي)
االحتمال :2المتفاعلAمحلول مائي حجمه VAو Bنوع كيميائي صلب يكون( )VT=VA
االحتمال :3محلول مائي حجمه Vيتفكك ذاتيا (مثل تفكك الماء األوكسجيني) يكون()VT=V
معطيات التمرين تشمل نوعين:
المعطيات الكمية :تسمح لنا بحساب كمية مادة كل متفاعل تعطى المقادير التالية
حسب االحتماالت التالية:
االحتمال :1يعطى تركيز المحلول المائي Cوحجمه .( n C V ( V معادلة التحول :فيها احتمالين:
m االحتمال :1تعطى لنا الثنائيتين ox1/red2و ox2/red2فيطلب منا كتابة المعادلة التحول.
). n ( m االحتمال :2كتلة النوع الكيميائي
M االحتمال :2تعطى لنا معادلة التحول الكيميائي فيطلب منا إيجاد الثنائيتين ox1/red2وox2/red2
أو كثافته dتحسب وكتلته الحجمية االحتمال :3يعطى حجم محلول مائي V
m
d H 2O و ) n و m V كمية مادته كما يلي( :
M
H 2O حيث 1g / cm 3 1kg / L 1000g / L
مالحظة هامة جدا )1:اذا كانت كمية مادة المتفاعلين Aو Bمعلومة نستطيع مباشرة تحديد المتفاعل المحد
وحساب Xmaxو التركيب المولي للمزيج النهائي: ماهي األسئلة واإلشكاليات التي تطرح في تمرين البكالوريا:
aAحيث a,b,c,dأعداد ستيوكيومترية للتحول الكيميائي التالي bB cC dD :
n n أوال:األسئلة المعرفية والنظرية :يطرح سؤال أو سؤالين نظريين أو تعريف من الدرس تجدونه
لتحديد المتفاعل المحد ،نحسب 0Aو 0Bفتكون النسبة األصغر متفاعلها هو المتفاعل المحد. في صفحة األسئلة المتوقع طرحها في البكالوريا ( 0.5نقطة)
b a
ثانيا :أسئلة المكتسبات القبلية تشمل األسئلة الثابتة التالية دوما:
n n n
أ)إذا كان 0 A 0 B :سيكون المتفاعل Aهو المتفاعل المحد فيكون X max 0 Aفيكون )1كتابة معادلة التحول أو إيجاد الثنائيتين 0.5( ox/redنقطة).
a a b
)2إنشاء جدول التقدم (1ن).
التركيب المولي النهائي للمزيج n A f 0 :و n Bf n 0 B bX max
)3إيجاد المتفاعل المحد وحساب Xmaxو Xfوإيجاد التركيب المولي للمزيج النهائي اذا كانت
nCf c X maxو n Df d X max كمية مادة المتفاعلين معلومة من المعطيات( 1نقطة).
n n n ثالثا:بعد ذلك يعطى في التمرين دوما متابعة زمنية لهذا التحول بأحد المقادير التالية :التقدم)،X(t
X max ب) اذا كان 0 A 0 B :سيكون المتفاعل Bهو المتفاعل المحد فيكون 0 B
b a b كمية مادة أو تركيز أو كتلة متفاعل أو ناتج أو حجم غاز منطلق أو بالناقلية أو بالضغط
فيكون التركيب المولي النهائي للمزيج n Bf 0 :و n Af n 0 A aX max أو بحجم التكافؤ أو ب phالمحلول.....الخ.
وتكون اما بوثيقة أو جدول يكمل ويرسم بيانه بداللة الزمن ،وتطرح األسئلة الثابتة التالية دوما:
nCf c X maxو n Df d X max )1إيجاد من البيان Xfو Xmaxوتحديد المتفاعل المحد وحساب المقدار المجهول(التركيز Cأو
n0A n0B n0A n0B الحجم Vاو الكتلة ... mالخ (1نقطة).
X max هنا يتحقق الشرط الستيوكيومتري فيصبح: ج) اذا كان:
a b a b )2تعريف زمن نصف التفاعل t 1/ 2وإيجاد قيمته بيانيا(0.5نقطة).
فيكون التركيب النهائي للمزيج: )3حساب سرعة التفاعل أو السرعة الحجمية ( لحظية ،تشكل ،أختفاء) ( 0.5نقطة).
n A f 0و n Bf 0
)4طرح سؤال نظري عن احد العوامل الحركية أو التفسير المجهري لسرعة التحول الكيميائي
nCf c X maxو n Df d X max أوالتفسير المجهري للتحول الكيميائي ( 0.5نقطة).
)2إذا كانت كمية مادة أحد المتفاعلين معلومة ولتكن n 0Aللمتفاعل Aمعلومة ،وكمية مادة المتفاعل B ) 5عند اكمال جدول دوما يطلب منا إيجاد عالقة نظرية بين مقدارين كيميائيين احداهما معطى في
n 0Bمجهولة هنا يحدد المتفاعل المحد كما يلي: الجدول والثاني مجهول يكمل به الجدول (مثال تمرين 1سؤال 0.5()2نقطة).
Xمن الوثيقة المعطاة في المتابعة الزمنية ،وبما Xإما معلوم أو يحسب أ)في هاته الحالة سيكون ) 6يطرح سؤال فني لحل اإلشكالية الكيميائية التي طرحت في بداية التمرين ( 1- 0.5نقطة).
f max
.X max أن التحول الكيميائي تام سيكون X f
n 0A
ب)هنا نفرض المتفاعل Aالذي لدينا كمية مادته n 0Aالمعلومة هو المتفاعل المحد ونحسب
a تلخيص وتنظيم األستاذ خلفاوي إ
ونقارنها مع X maxفينتج عن ذلك احتمالين:
n 0A
) فيكون المتفاعل Aهوالمحد المفروض، االحتمال :1نجد (
BAC2020
=X max
a
n
) Xسيكون المتفاعل Bهو المتفاعل المحد ومنه يصبح max االحتمال :2وهو الراجح نجد ( 0 A
a
n0B
X max
b
)3اذا كان التحول تام فانX max X f :
)4دوما X fيحسب من الوثيقة فهو قيمة حقيقية.
2
أهم التعاريف واألسئلة النظرية الممكن طرحها في بكالوريا الوحدة1
)1األكسدة:هي تحول كيميائي يفقد فيه الفرد الكيميائي إلكترون أو أكثر (يسمى الفرد هنا بالمرج.)red
)2اإلرجاع :هي تحول كيميائي يكسب فيه الفرد الكيميائي إلكترون أو أكثر (يسمى الفرد هنا بالمؤكسد.)ox
)3الجسم المؤكسد :كل فرد كيميائي يكسب إلكترون أو أكثر خالل تحول كيميائي(يحدث له تحول إرجاع).
)4الجسم المرجع :كل فرد كيميائي يفقد إلكترون أو أكثر خالل تحول كيميائي(يحدث له تحول أكسدة).
)5المتفاعل المحد :هو المتفاعل الذي يختفي تماما في نهاية التفاعل(يسبب توقفه).
)6التحول الكيميائي التام :هو تحول كيميائي يوجد فيه متفاعل محد أو يتحقق في التفاعل الشرط الستيوكيومتري(.يدرس في الوحدة.)1
)7التحول الكيميائي الغير التام:هو تحول كيميائي ال يوجد فيه متفاعل محد( أي في نهاية التفاعل تبقى كمية من المتفاعلين األول والثاني مع
النواتج)(يدرس في الوحدة)4
)8الشرط الستوكيومتري :هو تحول كيميائي يختفي فيه المتفاعلين معا في نفس اللحظة.
)9التكافؤ :هو تحول كيميائي يتحقق فيه الشرط الستيوكيومتري.
)10التحول الكيميائي السريع:هو تحول كيميائي يصل إلى نهايته بعد تالمس المتفاعالت مباشرة(يستغرق أجزاء من الثانية وال تميز العين المجردة تطوره)
)11التحول الكيميائي البطئ:هو تحول كيميائي نستطيع متابعة تطوره بالعين المجردة ويستغرق ثواني أو دقائق أو ساعات.
)12التحول الكيميائي البطئ جدا :هو تحول كيميائي يستغرق أيام أو أشهر أو سنوات.
1 dx
V vol (t ) )13السرعة الحجمية للتفاعل:هي مقدار تغير تقدم التفاعل بالنسبة للزمن في وحدة الحجم للمزيج المتفاعل تعطى بالعبارة
V T dt
)14زمن نصف التفاعل:هو الزمن المستغرق لبلوغ التفاعل نصف تقدمه األعظمي Xmaxأو هو الزمن المستغرق الستهالك نصف المتفاعل المحد .
)15العامل الحركي:هو عامل يساعد على تسريع التفاعل يشمل الوسيط ،والتراكيز االبتدائية،ودرجة الحرارة.
)16الوسيط:هو نوع كيميائي يسرع التفاعل دون أن يدخل في التفاعل وال يغير في الحالة النهائية للجملة الكيميائية.
)17التحفيز .والتحفيز الذاتي:التحفيز هي عملية تسريع التفاعل وإذا كان أحد النواتج هو المسرع للتفاعل يكون التحفيز ذاتي.
)18السقي:هو إضافة الماء البارد أو المثلج للمتفاعلين لتوقيف التفاعل.
)19الوساطة:هي عملية تأثير الوسيط على التفاعل الكيميائي.
)20ماهي أنواع الوساطة:تنقسم الوساطة إلى ثالث أنواع :الوساطة المتجانسة ،الوساطة الغير متجانسة ،الوساطة اإلنزيمية.
)21الوساطة المتجانسة :نقول عن الوساطة أنها متجانسة إذا كان الوسيط من نفس الحالة الفيزيائية للمتفاعالت.
)22الوساطة الغير متجانسة :نقول عن الوساطة أنها غير متجانسة إذا كانت الحالة الفيزيائية للوسيط الوسيط تختلف عن الحالة الفيزيائية للمتفاعالت.
)23الوساطة اإلنزيمية :نقول عن الوساطة أنها إنزيمية إذا كان الوسيط إنزيم.
)24كيف تتطور سرعة التفاعل خالل التحول الكيميائي :تتطور من قيمة عظمى عند لحظة المزج( )t=0sللمتفاعلين وتتناقص تدريجيا حتى تنعدم في
نهاية التفاعل.
)25ماهو المدلول الكيميائي لزمن نصف التفاعل:أ)يسمح لنا من مقارنة تفاعلين من حيث السرعة فزمن نصف التفاعل األصغر يكون تفاعله أسرع واألكبر
هو األبطأ.
. 7و 4 بين قيمتها تتراوح αحيث t f = α× t ½ التفاعل نهاية فزمن التفاعل ينتهي متى بمعرفة لنا ب)يسمح
)26لماذا نبرد المزيج المتفاعل :نبرد المزيج المتفاعل لتوقيف التفاعل.
)27مامعنى التصادم الفعال :هو تصادم بين المتفاعالت ينتج عنه تغير في بنية األفراد الكيميائية للمتفاعالت(كتفكك فرد كيميائي أو اندماج فردين
كيميائيين).
)28فسر مجهريا حدوث التفاعل الكيميائي :يحدث التفاعل الكيميائي بسبب التصادمات الفعالة بين األفراد الكيميائية للمتفاعالت.
)29فسر مجهريا تأثير درجة الحرارة والتراكيز االبتدائية على التفاعل:أ)بازدياد درجة الحرارة تزداد سرعة حركة األفراد الكيميائية للمتفاعالت فيزداد عدد
التصادمات التصادمات الفعالة فتزداد سرعة التفاعل.
ب)بازدياد التراكيز االبتدائية للمتفاعالت يزداد عدد األفراد الكيميائية للمتفاعالت في وحدة الحجم فيزداد عدد التصادمات والتصادمات الفعالة فتزداد سرعة
التفاعل.
)30فسر مجهريا تناقص سرعة التفاعل من قيمة عظمى إلى القيمة صفر :في البداية يكون عدد األفراد الكيميائية للمتفاعالت كبير فيكون عدد التصادمات
الفعالة كبير فتكون السرعة أكبر بمرور الزمن تتناقص األفراد الكيميائية المتفاعلة بسبب التفاعل فتتناقص عدد التصادمات الفعالة فتنقص معها سرعة
التفاعل حتى تنعدم مع انتهاء احد األفراد الكيميائية المتفاعلة.
)31التقدم األعظمي :Xmaxهو التقدم الموافق الستهالك المتفاعل المحد كليا( وهو قيمة حقيقة اذا كان التحول تام ونظرية اذا كان غير تام).
)32التقدم النهائي :Xfهو التقدم المالحظ عند توقف تطور الجملة الكيميائية(وهو قيمة حقيقية دوما).
BAC2020 تلخيص وتنظيم األستاذ خلفاوي إ
3
مخطط المتابعة الزمنية للتحول الكيميائي
لتحول كيميائي ما معادلته:
δ،σ،β،αأعداد ستيوكيومترية(ع س) B,Aمتفاعالت D,C،نواتج
فيكون جدول
التقدم لهذا التحول:
يمكن إجراء المتابعة الزمنية للتحول الكيميائي بإحدى الطرق التالية :
كمية المادة في لحظة t
تقدم التفاعل )X= f(t
للمتفاعالت والنواتج
)X (mol
fX
كمية مادة أحد المتفاعالت كمية مادة أحد النواتج
)nA=f(t )nB=f(t )nD=f(t )nC=f(t
)nB (mol تركيز تقدم التفاعل )nD (mol )nC (mol
nA )(mol
n0B هنا المتفاعل Bغير محد
n0A هنا المتفاعل Aمحد فيكون المتفاعل Aمحد : []X
فيكونn0A : n0B- nBf
=X f =Xf npf
α β fX
] X[ f = V ع س = Xf
nBf T
Xf=VT. [X]f
)1الرمز (ع س) يمثل العدد الستيوكيومتري في
معادلة التحول الكيميائي وهو دوما مقدار ثابت.
تركيز أحد المتفاعالت )2الرمز npfيمثل كمية المادة النهائية ألحد تركيز احد النواتج
)]A[= f(t )]B[= f(t النواتج ،والرمز ]P[fهو التركيز النهائي ألحد )]D[= f(t )]C[= f(t
النواتج.
)]B[ (mol/L []D )]C[ (mol/L
)]A[ (mol/L )(mol/L
n0B هنا المتفاعل Bغير محد
n0A =]B[0 فيكون المتفاعل Aمحد : ] D[ f = V ]C[f = V
]A[0= VT هنا المتفاعل Aمحد VT n0B- nBf T T
فيكونn0A : =Xf
=X f β
α nBf
=]B[f VT˟ [p]f
VT ع س = Xf
TVهو حجم الوسط التفاعلي يحسب حسب معطيات التمرين
األحتمال : 1المتفاعل األول صلب والمتفاعل الثاني محلول
مائي حجمه Vفيكون حجم الوسط التفاعليTV=V :
األحتمال : 2المتفاعل األول محلول مائي حجمه1Vوالمتفاعل
الثاني محلول مائي حجمه 2Vفيكون حجم الوسط التفاعلي:
TV=1V+2V كتلةأحد النواتج
األحتمال: 3محلول مائي حجمه Vيحدث له تفككك ذاتي أثناء
كتلة أحد المتفاعالت التحول الكيميائي فيكون حجم الوسط التفاعلي: )mD=f(t )mC=f(t
)mA=f(t )mB=f(t TV=V
مالحظة :دوما حجم الوسط التفاعلي TVثابت اليتغير أثناء
التحول الكيميائي. )mD (g )mC (g
)mA (g )mB (g D
m0B هنا المتفاعل Bغير محد mDf= nDf ˟ MD mCf= nCf ˟ MC
m0A هنا المتفاعل Aمحد فيكون المتفاعل Aمحد :
فيكونn0A : n0B- nBf
=X f =Xf
α β
Mالكتلة المولية للفرد الكيميائي الذي
mBf
يجرى له المتابعة الزمنية وهي مقدار
ثابت دوما أثناء التحول الكيميائي mf
m0A= n0A ˟ MA m0B= n0B ˟ MB = Xf
mAf=0 g mBf= nBf ˟ MB ع س˟ M
BAC2020 تلخيص وتنظيم األستاذ خلفاوي إ
4
You might also like
- BBL AbedDocument4 pagesBBL Abedعبد العزيز مروىNo ratings yet
- Bac Physics 2016 Se 2Document8 pagesBac Physics 2016 Se 2abdelhak AouadiNo ratings yet
- الموضوعDocument8 pagesالموضوعallalmayar2022No ratings yet
- 5 1 08Document1 page5 1 08smjamal100% (1)
- 2-07-1 - تعيين كمية المادة عن طريق المعايرةDocument56 pages2-07-1 - تعيين كمية المادة عن طريق المعايرةaicha physiqueNo ratings yet
- ch2 4-Suivi D'une Transformation Chimique ActivitéDocument2 pagesch2 4-Suivi D'une Transformation Chimique ActivitéRachid SadNo ratings yet
- Dev2 BenchakouDocument1 pageDev2 Benchakouben amor melikaNo ratings yet
- Révision BAC 2018Document172 pagesRévision BAC 2018ZineChini100% (5)
- تقويم الوحدة 01 المتابعة الزمينة لتحول كيميائيDocument2 pagesتقويم الوحدة 01 المتابعة الزمينة لتحول كيميائيNa LineNo ratings yet
- 8Document2 pages8e.maskarNo ratings yet
- اختبار فيزياء مقترح بكالوريا 2017 ن 11Document4 pagesاختبار فيزياء مقترح بكالوريا 2017 ن 11مدرسة100% (2)
- 1.الدراسة الحركية لتفاعل عن طريق الموصليةDocument2 pages1.الدراسة الحركية لتفاعل عن طريق الموصليةBRAHIMdeSAFINo ratings yet
- Corpsvtn 212Document7 pagesCorpsvtn 212Farid HaririNo ratings yet
- Dzexams 2as Physique As - E2 20210 2133411Document3 pagesDzexams 2as Physique As - E2 20210 2133411sof chimisteNo ratings yet
- الفرض المنزلي رقم 1 الدورة الثانية ثانية علوم الحياة والأرض 1 و 2Document2 pagesالفرض المنزلي رقم 1 الدورة الثانية ثانية علوم الحياة والأرض 1 و 2الغزيزال الحسن EL GHZIZAL HassaneNo ratings yet
- Composition de Physique 3AS - Sujet 05Document2 pagesComposition de Physique 3AS - Sujet 05Hasan RajawiNo ratings yet
- حالة توازن مجموعة كيميائيةDocument7 pagesحالة توازن مجموعة كيميائيةالغزيزال الحسن EL GHZIZAL Hassane100% (1)
- Exo TerminalDocument11 pagesExo TerminalshadowNo ratings yet
- فرض محروس 2 ع رDocument1 pageفرض محروس 2 ع رMajed GharibNo ratings yet
- ثالثة تر التبسيDocument2 pagesثالثة تر التبسيWissam GouasmiaNo ratings yet
- تمارين بالحلDocument23 pagesتمارين بالحلchahinez Mecherrak0% (1)
- lateur1الأختبار الثاني 2008-2009 الجزائرDocument2 pageslateur1الأختبار الثاني 2008-2009 الجزائرassembleur7777100% (1)
- التمرين6Document4 pagesالتمرين6foud18No ratings yet
- سلسلة المكتسبات القبلية 2023 (جبالي رفيق)Document3 pagesسلسلة المكتسبات القبلية 2023 (جبالي رفيق)Hina BouzerzourNo ratings yet
- حالة توازن و التحولات النوويةDocument2 pagesحالة توازن و التحولات النوويةRachid SadNo ratings yet
- حالة توازن و التحولات النوويةDocument2 pagesحالة توازن و التحولات النوويةRachid SadNo ratings yet
- Serie 2 Chimie 1Document9 pagesSerie 2 Chimie 1Belf MehdNo ratings yet
- Composition de Physique 3AS - Sujet 12Document2 pagesComposition de Physique 3AS - Sujet 12Hasan RajawiNo ratings yet
- يتفاعل الزنك مع محلول حمض الكبريتيكDocument1 pageيتفاعل الزنك مع محلول حمض الكبريتيكanon-774739100% (2)
- Contr 1ér S 3-2 2bacDocument2 pagesContr 1ér S 3-2 2bacyoucard50% (2)
- Examin 000Document2 pagesExamin 000dam 12No ratings yet
- Exos BelkacemDocument4 pagesExos BelkacemMilia dyNo ratings yet
- الأستاذ خلفاوي - مذكرة 01Document17 pagesالأستاذ خلفاوي - مذكرة 01Hei SuNo ratings yet
- Exam 2021Document2 pagesExam 2021سمير دبيليNo ratings yet
- Mentouri AinMlilaDocument2 pagesMentouri AinMlilamohamed rezigNo ratings yet
- تمرين حول حجم غاز,Document2 pagesتمرين حول حجم غاز,Achref SaidNo ratings yet
- نموذج 02 لاختبار الفصل 2 للسنة 2 تر - 2019Document2 pagesنموذج 02 لاختبار الفصل 2 للسنة 2 تر - 2019Abdelnour AffelayNo ratings yet
- Dzexams Bac Mathematiques MT 20181 3218595Document12 pagesDzexams Bac Mathematiques MT 20181 3218595Badr EddineNo ratings yet
- حل الوحدة الأولى تمارينDocument17 pagesحل الوحدة الأولى تمارينMohamed LoghbiNo ratings yet
- التحولات حمض قاعدة و الكهرباء 5Document1 pageالتحولات حمض قاعدة و الكهرباء 5HarounSamihNo ratings yet
- Bbl13 BouzidDocument7 pagesBbl13 Bouzidcylia ciciNo ratings yet
- Dzexams 3as Physique d1 20210 1615130Document2 pagesDzexams 3as Physique d1 20210 1615130yacine yacineNo ratings yet
- التحولات ح,ق و الكهرباءDocument1 pageالتحولات ح,ق و الكهرباءYassine0% (1)
- السرعــة والسرعـــة الحجميــةDocument6 pagesالسرعــة والسرعـــة الحجميــةboustakatbNo ratings yet
- Devoir3 SVTDocument4 pagesDevoir3 SVTSiMo ElbNo ratings yet
- Mama DevDocument1 pageMama Devyanisferhat6No ratings yet
- فروض الفيزياء والكيمياء الثانية باك علوم فيزيائية الدورة الاولى المرحلة 2 النموذج 12 غ.مDocument2 pagesفروض الفيزياء والكيمياء الثانية باك علوم فيزيائية الدورة الاولى المرحلة 2 النموذج 12 غ.مYuta HaiseNo ratings yet
- المتفوق 01 by DEBILI Samir Lycee Malek Bennabi TEBESSADocument1 pageالمتفوق 01 by DEBILI Samir Lycee Malek Bennabi TEBESSAAmdjed BahaaNo ratings yet
- 2- حالة توازن مجموعة كيميائيةDocument7 pages2- حالة توازن مجموعة كيميائيةالغزيزال الحسن EL GHZIZAL HassaneNo ratings yet
- 2s CompoDocument2 pages2s Compoamine milanoNo ratings yet
- Examen2 smb1Document2 pagesExamen2 smb1Amine AlaoUii AlaouiNo ratings yet
- التحولات النووية 02Document10 pagesالتحولات النووية 02Prof de PhysiqueNo ratings yet
- تمرين اليوم15-11-2023Document1 pageتمرين اليوم15-11-2023Abderrahmane BekhtiNo ratings yet
- اختبار فيزياء تجريبيDocument8 pagesاختبار فيزياء تجريبيSaied Mansour Saied MansourNo ratings yet
- JDGDHDocument1 pageJDGDHYassineNo ratings yet
- Bac2023 Ytb Unite 01 03Document2 pagesBac2023 Ytb Unite 01 03استاذك في الفيزياءNo ratings yet
- دليل الاجادة الاعرابية فى اللغة العربية PDFDocument23 pagesدليل الاجادة الاعرابية فى اللغة العربية PDFAmoula HayatieNo ratings yet
- -درس-التصرف العام لدارة كهربائيةDocument1 page-درس-التصرف العام لدارة كهربائيةAmoula HayatieNo ratings yet
- 75Document4 pages75Amoula HayatieNo ratings yet
- مميزة ثنائي القطب النشيطDocument6 pagesمميزة ثنائي القطب النشيطAmoula HayatieNo ratings yet
- دور التعلمDocument226 pagesدور التعلمAmoula Hayatie100% (1)