Professional Documents
Culture Documents
الوثيقة 1
الوثيقة 1
Uploaded by
Soumia KerdCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
الوثيقة 1
الوثيقة 1
Uploaded by
Soumia KerdCopyright:
Available Formats
المتابعة الزمنية لتحول كيميائي
الوثيقة رقم 10
Bac 2023 المتابعة الزمنية عن طريق المعايرة :
النشاط :
نريد متابعة تطور التحول الكيميائي المنمذج بالمعادلة الكيميائية التالية:
)𝒍( 𝑶 𝟐 𝑯𝟐 𝑯𝟐 𝑶𝟐 (𝒂𝒒) + 𝟐𝑯+ (𝒂𝒒) + 𝟐𝑰−(𝒂𝒒) = 𝑰𝟐 (𝒂𝒒) +
لهذا نمزج 𝐿𝑚 𝑉1 = 50من الماء األكسجيني الشفاف تركيزه المولي 𝐿 𝐶1 =55 𝑚𝑚𝑜𝑙/مع 𝐿𝑚 𝑉2 = 50من محلول يود
البوتاسيوم الشفاف تركيزه . 𝐶2 = 0.1 𝑚𝑜𝑙. 𝐿−1نقسم المزيج التفاعلي إلى 10عينات متساوية الحجم.
في اللحظة t1نقوم بسقي العينة ،1ثم نعاير اليود المتشكل بواسطة محلول ثيوكبريتات الصوديوم ) (2𝑁𝑎+ + 𝑆2𝑂32−تركيزه
المولي 𝐿 . 𝐶 ′= 0.1 𝑚𝑜𝑙 /ولهذا الغرض نضيف كيمة من صمغ النشاء ،ثم نسجل الحجم المضاف عند التكافؤ 𝐸𝑉.
)𝒒𝒂(𝑰𝟐 (𝒂𝒒) + 𝟐𝑺𝟐 𝑶𝟑𝟐− (𝒂𝒒) = 𝟐𝑰 − (𝒂𝒒) + 𝑺𝟒𝑶 𝟔𝟐− معادلة تفاعل المعايرة:
نقوم بنفس العملية مع باقي العينات ونسجل النتائج في الجدول الموالي:
-01ماذا نقصد بسقي العينة ،ماهي أنواعه؟ وما الغرض منه.
- 02هل يؤثر إضافة الماء والجليد على نتائج التجربة؟
-03متى نضيف صمغ النشاء للعينة؟ ما الهدف من ذلك؟
- 04هل التفاعل بطيء أم سريع؟ كيف نالحظ تطور هذه الجملة الكيميائية؟
-05ما هي شروط تفاعل المعايرة؟
-06أنشيء جدول تقدم تفاعل اﻟرﺋﯾﺳﻲ
-07عبر عن كمية مادة ثنائي اليود المتشكل في الع ينة بداللة 𝐸𝑉 و𝐶 ′
-08استنتج العالقة التي تعبر عن كمية مادة ثنائي اليود الموجودة في المزيج التفاعلي الكلي.
-09أنشيء جدول قيم لتقدم التفاعل 𝑥 خالل الزمن في المزيج التفاعلي.
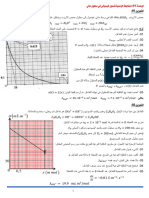
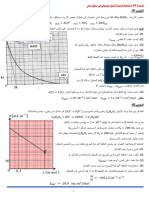
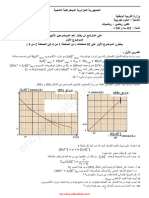
-10أرسم البيان𝑥 = 𝑓(𝑡) :
-11أوجد تركيب المزيج التفاعلي عند اللحظة 𝑛𝑖𝑚 𝑡 = 10
Abdellatif abdellatif_phys
You might also like
- الماء الأكسجيني و الدرجة الكلورومتريةDocument6 pagesالماء الأكسجيني و الدرجة الكلورومتريةMokhtar LadjineNo ratings yet
- سلسلة الوحدة 1 المتابعة الزمنيةDocument8 pagesسلسلة الوحدة 1 المتابعة الزمنيةMohamed Anis LounisNo ratings yet
- الوحدة 01 سلسلة تمارين حصص zoomDocument4 pagesالوحدة 01 سلسلة تمارين حصص zoomferiel taibiNo ratings yet
- 4 5879874055732990293Document5 pages4 5879874055732990293Loup le DésertNo ratings yet
- تمرين 1-3Document2 pagesتمرين 1-3Hani StarkNo ratings yet
- تمارين مع الحل المفصل حول الأسترة للاستاذ الفاضل بلياسين عبد الجليل1653418652Document27 pagesتمارين مع الحل المفصل حول الأسترة للاستاذ الفاضل بلياسين عبد الجليل1653418652Amrouche KarimaNo ratings yet
- - تمرين لمراجعة الناقلية و المعايرة في الفيزياء للسنة الثانية ثانوي الشعب العلمية للاستاذ عابديDocument1 page- تمرين لمراجعة الناقلية و المعايرة في الفيزياء للسنة الثانية ثانوي الشعب العلمية للاستاذ عابديBlyn LylyNo ratings yet
- Bac21 Doc3Document2 pagesBac21 Doc3medNo ratings yet
- تمارين الوحدة 01Document2 pagesتمارين الوحدة 01elandaloussimeriem59No ratings yet
- سلسلة تمارين 2Document6 pagesسلسلة تمارين 2lisaNo ratings yet
- سلسلة تمارينDocument6 pagesسلسلة تمارينMalak ElaichouchiNo ratings yet
- تقويم الوحدة 2024Document4 pagesتقويم الوحدة 2024widad doudiNo ratings yet
- التتبع الزمني لتحول كيميائيDocument8 pagesالتتبع الزمني لتحول كيميائيYou ZbirNo ratings yet
- وثيقة الأستاذDocument2 pagesوثيقة الأستاذIkram KimiNo ratings yet
- الأسئلة النظريةDocument10 pagesالأسئلة النظريةYeah Yeah100% (4)
- (الفرض الأول (3ر+تقرDocument2 pages(الفرض الأول (3ر+تقرNasser Eddine AbdouNo ratings yet
- الماء الأكسجيني و الدرجة الكلورومتريةDocument6 pagesالماء الأكسجيني و الدرجة الكلورومتريةydygsgs623No ratings yet
- الأسئلة النظرية الوحدة الأولىDocument2 pagesالأسئلة النظرية الوحدة الأولىnourmalaklarbi29No ratings yet
- Acide BaseDocument2 pagesAcide Baseayman lamzouriNo ratings yet
- المقرونة تمارينDocument8 pagesالمقرونة تمارينayoubberramram5No ratings yet
- Exercices PC 2bac 0013Document8 pagesExercices PC 2bac 0013aharrar jamilaNo ratings yet
- 100 سؤال وجواب في العلوم الفيزيائيةDocument14 pages100 سؤال وجواب في العلوم الفيزيائيةsamirNo ratings yet
- الوحدة 01 سلسلة المتابعة الزمنية عن طريق قياس الحجمDocument2 pagesالوحدة 01 سلسلة المتابعة الزمنية عن طريق قياس الحجمZizo Dark100% (2)
- Compo215MTer ArbaouiDocument4 pagesCompo215MTer ArbaouiNabilKarmNo ratings yet
- Altholat Alkimiaiia Almqrona Baltfaalat HMDH Qaada Slsla Altmarin 3 2Document2 pagesAltholat Alkimiaiia Almqrona Baltfaalat HMDH Qaada Slsla Altmarin 3 2muka fihNo ratings yet
- ________ (6) _____ ___ ________ _______ __ ____ ____ ________ (5)Document5 pages________ (6) _____ ___ ________ _______ __ ____ ____ ________ (5)mask blob 2No ratings yet
- الوثيقة 2araDocument2 pagesالوثيقة 2araSoumia KerdNo ratings yet
- الوثيقة 2Document2 pagesالوثيقة 2Soumia KerdNo ratings yet
- Bbl14bS MohamedDocument9 pagesBbl14bS MohamedrachidNo ratings yet
- وثيقة التلميذDocument3 pagesوثيقة التلميذIkram KimiNo ratings yet
- Exercices de Chimie Transformation Chimique S'effectuant Dans Les Deux Sens TPC SM Classe 10Document3 pagesExercices de Chimie Transformation Chimique S'effectuant Dans Les Deux Sens TPC SM Classe 10keomatNo ratings yet
- Physics 2se20 2trim1Document4 pagesPhysics 2se20 2trim1noureddine SILININo ratings yet
- تمرين شامل في الوحدة الأولى المتابعة الزمنية لتحول كيميائيDocument19 pagesتمرين شامل في الوحدة الأولى المتابعة الزمنية لتحول كيميائيmlkmehdidNo ratings yet
- التتبع الزمني لتحول كميائي سرعة التفاعلDocument10 pagesالتتبع الزمني لتحول كميائي سرعة التفاعلalmuslim80% (5)
- Cours - 7 - Thermodynamique (2022-2023)Document10 pagesCours - 7 - Thermodynamique (2022-2023)Farouk FeddaNo ratings yet
- Bb13B AflouDocument4 pagesBb13B AflouProfchaari SciencesNo ratings yet
- الوحدة 01 سلسلة 02 السنة ثالثةDocument1 pageالوحدة 01 سلسلة 02 السنة ثالثةÊš Pőîř100% (1)
- All PDFDocument8 pagesAll PDFayoubberramram5No ratings yet
- - - - - الحلقة (8) تمرين حول المتابعة الزمنية عن طريق المعايرة اللونيةDocument6 pages- - - - الحلقة (8) تمرين حول المتابعة الزمنية عن طريق المعايرة اللونيةAbdou0% (2)
- Local Media1736541324Document18 pagesLocal Media1736541324benhamdiadil24No ratings yet
- وثيقة المعايرة الـpH-متريّة (فارغة)Document2 pagesوثيقة المعايرة الـpH-متريّة (فارغة)emmmy1792No ratings yet
- مراجعة 2 PDFDocument4 pagesمراجعة 2 PDFBOBI TANo ratings yet
- بطاقة التلميذDocument1 pageبطاقة التلميذIkram KimiNo ratings yet
- تمارين تتبع تطور تحول كيميائي أولى باك النموذج1Document12 pagesتمارين تتبع تطور تحول كيميائي أولى باك النموذج1yahya elbahieNo ratings yet
- سلسلة تمارين الوحدة الأولى 1Document1 pageسلسلة تمارين الوحدة الأولى 1picaking9No ratings yet
- تمارين الوحدة 01Document1 pageتمارين الوحدة 01MY GAMINGNo ratings yet
- Alttba Alzmni Lthol Kimiaii Sraa Altfaal Aldrs 2Document9 pagesAlttba Alzmni Lthol Kimiaii Sraa Altfaal Aldrs 2ilyass kannaniNo ratings yet
- ملخص السنة الثانية #مجال #المادة وتحولاتهاDocument6 pagesملخص السنة الثانية #مجال #المادة وتحولاتهاtouhami messiidNo ratings yet
- 1 6Document5 pages1 6azizNo ratings yet
- Ø Ù Ø Ù Ø Ø 02Document3 pagesØ Ù Ø Ù Ø Ø 02alaa daysNo ratings yet
- Sujet 455Document6 pagesSujet 455akramadd2006No ratings yet
- سلسلة تمارين1 في الأكسدة ارجاع وتقدم التفاعل بكالورياDocument1 pageسلسلة تمارين1 في الأكسدة ارجاع وتقدم التفاعل بكالورياKhalid100% (1)
- الوحدة 01 سلسلة 01 السنة ثالثةDocument2 pagesالوحدة 01 سلسلة 01 السنة ثالثةÊš PőîřNo ratings yet
- Physics 3se22 1trim d1Document4 pagesPhysics 3se22 1trim d1souissi souissiNo ratings yet
- Physics 3mtm22 1trim d4Document4 pagesPhysics 3mtm22 1trim d4Radovane PhysiqyeNo ratings yet
- الدرس 03Document7 pagesالدرس 03mekhadem rayaneNo ratings yet
- Physics 3se22 1trim2Document2 pagesPhysics 3se22 1trim2yacine yacineNo ratings yet
- الدرس 03Document8 pagesالدرس 03ayadilyes79No ratings yet
- وحدة444444Document1 pageوحدة444444Houssem HassouNo ratings yet
- تقويم تشخيصي سنة 3 ثانوي كDocument9 pagesتقويم تشخيصي سنة 3 ثانوي كSoumia KerdNo ratings yet
- BAC2023 Doc1Document2 pagesBAC2023 Doc1Soumia KerdNo ratings yet
- الوحدة الولى تركيب البروتين 2022 2Document14 pagesالوحدة الولى تركيب البروتين 2022 2Soumia KerdNo ratings yet
- مجلة الجوهرة الوضعية المشكلة 3 الية الاستنساخDocument2 pagesمجلة الجوهرة الوضعية المشكلة 3 الية الاستنساخSoumia KerdNo ratings yet
- العلاقة بين بنية ووظيفة البروتين3Document11 pagesالعلاقة بين بنية ووظيفة البروتين3Soumia KerdNo ratings yet
- الوثيقة 2araDocument2 pagesالوثيقة 2araSoumia KerdNo ratings yet
- الوثيقة 2Document2 pagesالوثيقة 2Soumia KerdNo ratings yet
- pristige ووظيفة البروتين3Document11 pagespristige ووظيفة البروتين3Soumia KerdNo ratings yet