Professional Documents
Culture Documents
المراجعة رقم
المراجعة رقم
Uploaded by
Meli RtaCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
المراجعة رقم
المراجعة رقم
Uploaded by
Meli RtaCopyright:
Available Formats
المراجعة رقم -2-
اقسام الثالثة ثانوي ماي 2023
الشعبة :رياضيات ،تقني رياضيات ،علوم تجريبية ثانوية فرحات عباس
المدة :ساعتين مادة :العلـوم الفيزيـائيـة
التمرين األول:
ندرس خالل هذا التمرين حركة سقوط قطرة من ماء يمكن إعتبارها كروية الشكل نصف قطرها rو كتلتها mموجودة
على ارتفاع hمن سطح االرض .ننسب حركة القطرة لمحور ) (O, kالشاقولي وموجه نحو األسفل و يطابق مبدؤه القطرة
عند اللحظة t=0حيث v(t=0)=0أنظر الوثيقة .-5-
نعطي g=9.8N/kg :الكتلة الحجمية للماء ρeau=1000kg/m3حجم القطرة
4
V = .r 3
3
الجزء األول :
نعتبر أن قطرة الماء تخضع لتأثير وزنها فقط .
-1أوجد المعادالت الزمنية لحركة مركز عطالة القطرة.
-2أحسب سرعة وصول القطرة إلى سطح االرض نأخد . h=10m
الجزء الثاني :
تبين الدراسة التجريبية أن سرعة القطرة بجوار سطح األرض ثابتة و تأخد القيمة
. Vl=2.3.10-2m.s-1
-1أعط عبارة دافعة أرخميدس المطبقة على القطرة بداللة ρairو Vgحجم القطرة و gتسارع الجاذبية االرضية .
-2عبر عن ثقل القطرة بداللة ρeauو Vgو gو قارنه مع شدة دافعة أرخميدس .
نعطي .ρair =1.3kg/m :
3
-3نهمل في بقية التمرين دافعة أرخميدس و نعتبر أن القطرة تخضع لقوى احتكاك مائعة مطبقة من طرف الهواء و
عبارتها . f = −k v
أ .أوجد في المعلم ) (O, kالمعادلة التفاضلية التي يخضع لها مركز عطالة القطرة
dv
. و بين أنها تكتب على الشكل =av+b
dt
ب .عبر بداللة mو gو kعن السرعة الحدية . Vl
ج .حدد عبارة aو bبداللة معطيات التمرين ثم أحسب قيمهما .
نعطي . r=5,4.10-6m
د .أوجد وحدة . k
التمرين الثاني:
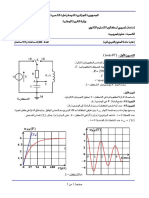
لدينا دارة كهربائية تحتوي على وشيعة ) , (L , rناقل أومي مقاومته R = 85Ωومولد توتر مستمر قوته المحركة
الكهربائية E = 10 Vو قاطعة Kعلى التسلسل ,نغلق القاطعة Kعند اللحظة . t=0s
-1كيف يمكن ربط راسم اإلهتزاز المهبطي لمشاهدة التوتر ULو التوتر الكلي في الدارة .
-2باستعمال قانون جمع التوترات بين أن المعادلة التفاضلية بداللة ULفي الدارة تكتب على الشكل :
dUL R + r rE
+ = UL
dt L L
األستاذ :صيد م العلوم الفيزيائية
الهاتف0775 049 049 :
الصفحة1 : الثالثة ثانوي
حيث A, B, αثوابت -3إن حل هذه المعادلة التفاضلية يعطى من الشكل 𝑈𝐿 = 𝐴 + 𝐵 𝑒 −𝛼𝑡 :
يطلب تعيينها .
𝐿 𝑈𝑑
dt
)( V/s -4باستعمال التحليل البعدي بين المدلول الفيزيائي
1
لكل من. A, B , 𝛼 :
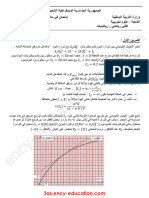
-5بواسطة تقنية مناسبة تمكنا من رسم المنحنى
𝐿𝑈𝑑
150 البياني ) 𝐿𝑈( 𝑓 =
𝑡𝑑
)UL (V أ -أوجد المعادلة النظرية للبيان .
1.5 10
ب -إستنتج المعادلة البيانية .
-6اوجد كل من :
المقاومة الداخلية للوشيعة rو ذاتيتها . L
-7إستنتج ثابت الزمن τوقيمة التيار في النظام الدائم.
-8حد د قيمة الطاقـــة المخزنة في الوشيعــة عند ما يبلـــغ
-850 التوتربين طرفيها (.) UL= 1.5 v
-9أرسم كيفيا المنحنى ) UL=f(tوالمنحنى ) UR=g(tفي نفس المعلم .
التمرين الثالث:
تتميز الم ثفات بخاصية تخزين الطاقة ال هربائية وإم انية استرجاعها عند الحاجة .وت ُم ّن هذه الخاصية من استعمال
الم ثفات في عدة أجهزة منها تشغي مصباح وامض بعض آالت التصوير.
)uC (V
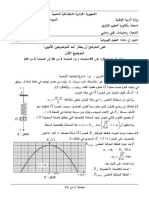
الجزء -Iشحن م ثف:
12 ننجز التركيب التجريبي الممثل في الشكل ()1
والمكون من مكثف سعته ، Cغير مشحون بدئيا،
8
مركب على التوالي مع موصل أومي مقاومتــــه
الكهربائية Rوقاطع التيار .K
يخضع ثنائي القطب RCلرتبة توتر معرفة كالتالي:
4 -بالنسبة ل ، U = 0 t<0
-بالنسبة ل U = E t ≥ 0حيث. E = 12 V :
)t(s نغلق الدارة عند اللحظة t = 0ونعاين ،باستعمال
0 1 2 3 4 وسيط معلوماتي على شاشة حاسوب ،تغيرات
2 الش التوتر uCبين مربطي المكثف بداللة الزمن.
يعطي الشكل ( )2المنحنى ). uc = f(t
-1.1أثبت المعادلة التفاضلية التي يحققها التوتر ).uC(t
−t
تحقق أن التعبير ) uC(t) = E .(1 − e حل للمعادلة التفاضلية بالنسبة ل t ≥ 0؛ حيث τثابتة الزمن. -1.2
حدد تعبير τو بيّن ،باعتماد معادلة األبعاد ،أن ل τبعدا زمنيا. -1.3
عيّن مبيانيا τواستنتج أن قيمة Cهي . C = 100 μFنعطي . R = 10 kΩ -1.4
احسب الطاقة الكهربائية التي يختزنها المكثف في النظام الدائم. -1.5
)2الجزء - IIتفريغ م ثف :
يتطلب تشغيل وامض آلة تصوير طاقة عاليــة ال يمكن الحصول عليها باستعمال المولد السابق .للحصول على الطاقة
الالزمة ،يُشحن المكثف السابق بواسطة دارة إلكترونية تُم ِّ ّكن من تطبيق توتر مستمر بين مربطي المكثف قيمته
UC =360 V
األستاذ :صيد م العلوم الفيزيائية
الهاتف0775 049 049 :
الصفحة2 : الثالثة ثانوي
نفرغ المكثف ،عند اللحظة ،t = 0في مصباح وامض آلة التصوير الذي ننمذجه بموصل أومي مقاومته ( rالشكل )3؛
−t
K
فيتغير التوتر بين مربطي المكثف وفق المعادلة uC = 360.e ' :؛
C
uC
r حيث ’ τثابتة الزمن و ) u C (tمعبرعنها بالفولط ). (V
3 الش
-2.1أوجد قيمة rمقاومة مصباح وامض آلة التصوير علما أن التوتر بين مربطي المكثف يأخذ القيمة = )uC(t
132,45 Vعند اللحظة . t = 2 ms
-2.2اشرح كيف يجب اختيار مقاومة وامض آلة التصوير لضمان تفريغ أسرع للمكثف.
الجزء الثاني:
التمرين التجريبي:
الجزء األول:
معطيات :الكتلة المولية إليثانوات الصوديوم M(CH3COONa) = 82 g/mol :
الجداء الشاردي للماء ، Ke = 10-14 :ثابت الحموضة للثنائية CH3COOH / CH3COO-عند الدرجة : 25°C
، KA2 = 1,6x10-5جميع القياسات ت ّمت عند الدرجة . 25°C
-Iنذيب كتلة m = 410 mgمن ب ّلورات إيثانوات الصوديوم في الماء المقطر للحصول على محلول S1غير مشبّع
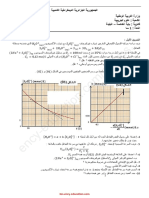
حجمه ، V = 500 mLو تركيزه المولي . C1نقيس pHالمحلول S1فنجده . pH = 8,4
-1أكتب معادلة التفاعل بين شوارد اإليثانوات و الماء .
-2بعد إنشاء جدول التقدم ،عبّر عن نسبة التقدم النهائي τ1للتفاعل الحاصل بداللة . C1 ، pH ، Ke
-3عبّر عن ثابت التوازن Kالمقرون بمعادلة التفاعل الحاصل بداللة C1و ، τ1ثم تحقّق أن . K = 6,3x10-10 :
-4نأخذ حجما Vمن المحلول S1و نضيف له الماء المقطر للحصول على محلول S2حجمه 10Vو له . pH = 8
-أحسب في هذه الحالة نسبة التقدم النهائي τ2للتفاعل بين إيثانوات الصوديوم و الماء ،ماذا تستنتج ؟
-IIنمزج حجما V1 = 90 mLمن محلول مائي إليثانوات الصوديوم تركيزه المولي C = 10-2 mol/Lمع حجم
V2 = 10 mLمن محلول مائي لحمض الميثانويك HCOOHله نفس التركيز المولي . C
ننمذج التحول الحاصل بتفاعل كيميائي معادلته :
CH3COO + HCOOH = CH3COOH + HCOO-
-
تُعطى الناقلية النوعية للمزيج التفاعلي عند لحظة tبداللة التقدم بالعالقة ، σ = 81,9 + 13,7 x :حيث σمقاسة
بـ mS.m-1و التقدم xمقاس بـ . mol
-1نقيس الناقلية النوعية للمزيج التفاعلي عند التوازن فنجدها . σéq = 83,254 mS.m-1 :
أ) تحقّق أن ثابت التوازن Kالمقرون بمعادلة التفاعل هو . K ≈ 10
ب) إستنتج قيمة ثابت الحموضة KA1للثنائية . HCOOH / HCOO-
-2أحسب pHالمزيج عند التوازن ،ثم إستنتج الفردين الكيميائيين المهيمنين (المتغلبين) في المزيج عند التوازن من بين
األفراد . HCOO- ، HCOOH ، CH3COO- ، CH3COOH :
الجزء الثاني:
يعرف اثانوات البنتيل أوعطر األجاص باسم اسيتات األميل نحصل عليه بتفاعل حمض اثانويك مع كحول أميلي تم
استخالصه قديما من البطاطا صيغته نصف مفصلة
1ـ أعط اسم المجموعة المميزة الموجودة في هدا الجزئي
2ـ أكتب المعادلة الكيميائية للتفاعل للحصول على اثانوات البنتيل
3ـ عند اللحظة t=0نمزج 0.5molمن الحمض و 0.5molمن الكحول
ثم نضيف كمية قليلة من حمض الكبريت نحافظ على الخليط في درجة حرارة ثابتة 25°الحجم الكلي للليط المتفاعل
هو V=83ml
نحدد خالل كل 5minكمية المادة nالثانوات البنتيل المتكون فنحصل على الجدول التالي
األستاذ :صيد م العلوم الفيزيائية
الهاتف0775 049 049 : الصفحة3 : الثالثة ثانوي
أ .ارسم المنحنى )n=f(t
ب .انشئ جدول تقدم التفاعل
ج .ماهي العالقة بين nو التقدم x
د .ما اسم الحالة التي توجد عليها المجموعة ابتدأ من اللحظة t=45min
ه .حدد في هذه الحالة تركيب المزيج و استنتج قيمة ثابت التوازن
و .ماهو مردود العملية
4ـ عند التوازن نضيف 0.1 molمن الكحول حدد جهة تطور الجملة ؟
5ـ أحسب قيمة السرعة اللحظية عند اللحظة t=20min
6ـ نعتبر الحالة التي يتم فيها التفاعل دون إضافة حمض الكبريت ارسم شكل المنحنى المحصل عليه في هـذه الحالة
موضحا الحالة النهائية
األستاذ :صيد م العلوم الفيزيائية
الهاتف0775 049 049 : الصفحة4 : الثالثة ثانوي
You might also like
- باك ت 08 + الحل - ع تج - فيزياء - نافع 2023Document15 pagesباك ت 08 + الحل - ع تج - فيزياء - نافع 2023Chaïma BenlounisNo ratings yet
- فيزياء - باقة الامتياز تحضيرا للفصل 2 - نافع بكالوريا 2024Document114 pagesفيزياء - باقة الامتياز تحضيرا للفصل 2 - نافع بكالوريا 2024keniaconte0No ratings yet
- Exam 07Document4 pagesExam 07Abdessalam BOUMARAF100% (1)
- Dzexams 3as Physique E3 20201 1002090Document11 pagesDzexams 3as Physique E3 20201 1002090yacine yacineNo ratings yet
- Dev01 SHHDocument1 pageDev01 SHHAVENIRBNo ratings yet
- Bac Physics 2016 Se 2Document8 pagesBac Physics 2016 Se 2abdelhak AouadiNo ratings yet
- Bac Blanc DEBILI Samir Lycee Fatima Zohra Tebessa Mai18 BisDocument4 pagesBac Blanc DEBILI Samir Lycee Fatima Zohra Tebessa Mai18 Bisسمير دبيليNo ratings yet
- إمتحان المنافسة العلمية في مادة العلوم الفيزيائية 2010Document9 pagesإمتحان المنافسة العلمية في مادة العلوم الفيزيائية 2010Is LamNo ratings yet
- الاختبار الثانيDocument4 pagesالاختبار الثانيwissamNo ratings yet
- Physique Trim3 MathtechDocument1 pagePhysique Trim3 MathtechSara BoumrarNo ratings yet
- Sujet 02-1Document3 pagesSujet 02-1ahmed bacaloriaNo ratings yet
- فيزياء -باك ت 08+الحل -رياضي+تر-نافع 2024Document18 pagesفيزياء -باك ت 08+الحل -رياضي+تر-نافع 2024mounilegend123No ratings yet
- أختبار مصححDocument3 pagesأختبار مصححmutraceNo ratings yet
- فرض منزلي رقم 3 الدورة الثانية ع ف 2013 2014Document2 pagesفرض منزلي رقم 3 الدورة الثانية ع ف 2013 2014Tahiri MehdiNo ratings yet
- الفرض الثانيDocument2 pagesالفرض الثانيbebboukha yousra100% (2)
- تمارين السقوط الشاقولي و الحرDocument2 pagesتمارين السقوط الشاقولي و الحرdounia amel50% (2)
- TP D HallDocument12 pagesTP D HallMaroua MerNo ratings yet
- Dzexams 3as Physique d2 20201 1502131Document7 pagesDzexams 3as Physique d2 20201 1502131yacine yacineNo ratings yet
- مراجعة الأختبارDocument2 pagesمراجعة الأختبارrana141129No ratings yet
- 3as Meca 1internet PDFDocument1 page3as Meca 1internet PDFSabbih El HabibNo ratings yet
- Dzexams 3as Physique 801166Document4 pagesDzexams 3as Physique 801166Izak DzNo ratings yet
- هشاموالسقوط الشاقوليDocument6 pagesهشاموالسقوط الشاقوليhicham.madani996No ratings yet
- Contr 1ér S 1-2 2bacDocument7 pagesContr 1ér S 1-2 2bacbalawisolaymanNo ratings yet
- Sujet 01-1Document4 pagesSujet 01-1ahmed bacaloriaNo ratings yet
- CPC 5Document2 pagesCPC 5Ayoo Oub OubeddaNo ratings yet
- المـــــدةDocument3 pagesالمـــــدةDaoud AllalNo ratings yet
- الوحدة 02 سلسلة تمارين شاملةDocument4 pagesالوحدة 02 سلسلة تمارين شاملةmokranidounia586No ratings yet
- فرض محروس رقم 3 الدورة الأولى ع ف 2012 2013 2 1Document2 pagesفرض محروس رقم 3 الدورة الأولى ع ف 2012 2013 2 1المتفوق في المعلومياتNo ratings yet
- الفرض الثالثDocument1 pageالفرض الثالثAmeur BounouarNo ratings yet
- سلسلة تمارين 06Document2 pagesسلسلة تمارين 06Majed GharibNo ratings yet
- Dzexams 3as Physique 1835017Document5 pagesDzexams 3as Physique 1835017xofawot518No ratings yet
- PhysicsDocument2 pagesPhysicsyacine yacineNo ratings yet
- ثالثة تر التبسيDocument2 pagesثالثة تر التبسيWissam GouasmiaNo ratings yet
- Alfrdh 1 Nmothj 1 Alfiziaa Oalkimiaa Thania Bak Alom Fiziaiia Aldora Alaola 1Document2 pagesAlfrdh 1 Nmothj 1 Alfiziaa Oalkimiaa Thania Bak Alom Fiziaiia Aldora Alaola 1younes ebahsayinNo ratings yet
- فرض رقم 4 الثانية علوم فيزيائية : الدورة الثانيةDocument4 pagesفرض رقم 4 الثانية علوم فيزيائية : الدورة الثانيةالغزيزال الحسن EL GHZIZAL Hassane100% (3)
- رقم02 اختبار الفصل الثاني بالحل 22 23 نحن سندكDocument10 pagesرقم02 اختبار الفصل الثاني بالحل 22 23 نحن سندكAyoubNo ratings yet
- Ds 3 PC 1 2bac Ar Prof - Bel Filali (WWW - Pc1.ma)Document4 pagesDs 3 PC 1 2bac Ar Prof - Bel Filali (WWW - Pc1.ma)Nassima ElNo ratings yet
- Série N2 2023Document1 pageSérie N2 2023Etudes AsNo ratings yet
- Compo2012 MHDocument4 pagesCompo2012 MHRiad ErENo ratings yet
- نص الموضوع 04Document4 pagesنص الموضوع 04Ana Oum AwladiNo ratings yet
- Dzexams Docs 3as 907410Document5 pagesDzexams Docs 3as 907410abdouNo ratings yet
- Physics 3se20 1trim5Document3 pagesPhysics 3se20 1trim5louaiboualleg570No ratings yet
- Bac U3Document12 pagesBac U3imeneNo ratings yet
- فرض محروس 1 الدورة 2Document2 pagesفرض محروس 1 الدورة 2Mouhibi AbdellahNo ratings yet
- Dzexams 3as Physique 737955Document13 pagesDzexams 3as Physique 737955rafiklammari16No ratings yet
- Sujet SC 2018 BLIDA-1Document8 pagesSujet SC 2018 BLIDA-1oussamimedNo ratings yet
- Revision21 ChuteDocument5 pagesRevision21 ChuteGindomNo ratings yet
- Dzexams Bac Physique MTM 20171 3959652Document23 pagesDzexams Bac Physique MTM 20171 3959652I KedirNo ratings yet
- Devoir Physique 2bacDocument1 pageDevoir Physique 2bacDehayni Abdelhamid100% (1)
- Bac2020 Sugg Physics Se s2Document5 pagesBac2020 Sugg Physics Se s2Anis LatrecheNo ratings yet
- Execices RL SM Classe 10 - 11 AllalDocument5 pagesExecices RL SM Classe 10 - 11 AllalkeomatNo ratings yet
- BBL BelkacemDocument2 pagesBBL BelkacemŞâmīhã ßęlNo ratings yet
- فرض محروس رقم 2 الدورة الثانية ع ف 2012 2013 1Document3 pagesفرض محروس رقم 2 الدورة الثانية ع ف 2012 2013 1Tahiri MehdiNo ratings yet
- Alfrdh 2 Nmothj 4 Alfiziaa Oalkimiaa Thania Bak Alom Fiziaiia Aldora Althania 1Document2 pagesAlfrdh 2 Nmothj 4 Alfiziaa Oalkimiaa Thania Bak Alom Fiziaiia Aldora Althania 1mohmedNo ratings yet