Professional Documents
Culture Documents
Na SO: C Mol L
Na SO: C Mol L
Uploaded by
Chi KouOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Na SO: C Mol L
Na SO: C Mol L
Uploaded by
Chi KouCopyright:
Available Formats
8
...................................................................
بـطاـقــة التلميــذ عـمل تـــجـر يـــبي
...................................................................
تستخدم القياسات الـكهربائية في عدة مجالات ومنها
في قياس كمية المادة للمحاليل الشاردية.
ما العلاقة بين كمية المادة والمقادير الـكهربائية ؟
مخطط التركيب التجريبي خطوات العمل التجريبي
❶ املأ السحاحة بمحلول ثيوكبريتات الصوديوم ) (2Na S 2O32 )(aq
تركيزه . c 2 0,1mol / L
c1 ❷ خذ حجما V 1 100 mLمن محلول ثنائي اليود ) I 2 (aqتركيزه المولي
وضعه في كأس بيشر.
❸ اغمر مسبار جهاز قياس الناقلية في كأس البيشر السابق مع قضيب
مغناطيسي ثم ضعهم فوق مخلاط مغناطيسي .
❹ نبدأ عملية المعايرة بإضافة حجم V 2من محلول ثيوكبريتات الصوديوم
إلى كأس البيشر وندون في كل مرة قيمة الناقلية .
) V 2 (mL 0 2 4 6 8 10 12 14 16 18 20
) G (mS
❶ علما أن الثنائيتين (مرجع/مؤكسد) الداخلتين في التفاعل هما ) (S 4O62 / S 2O32و ) ، (I 2 / I اكتب المعادلتين النصفيتين
للأكسدة والارجاع ثم استنتج معادلة التفاعل الحادث .
8
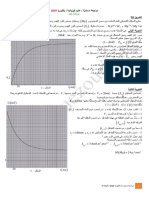
❷ ارسم منحنى تغيرات ناقلية المزيج Gبدلالة الحجم V 2المضاف من السحاحة ) G f (V 2ثم حدد حجم التكافؤ .
9 )G(mS
8
7
6
5 V2E=10mL
4
3
2
1
)V2(mL
0
0 2 4 6 8 10 12 14 16 18 20 22
❸ أنجز جدولا لتقدم التفاعل عند التكافؤ .
❹ استنتج عبارة c1بدلالة c 2 ، V 1و V 2Eثم احسب قيمته .
You might also like
- Révision BAC 2018Document172 pagesRévision BAC 2018ZineChini100% (5)
- تمارين في درس قياس المواصلةDocument1 pageتمارين في درس قياس المواصلةaziz75% (4)
- Na SO: C Mol LDocument2 pagesNa SO: C Mol Lramydib900No ratings yet
- Na SO: C Mol LDocument2 pagesNa SO: C Mol Lramydib900No ratings yet
- التتبع الزمني لتحول كيميائي - سرعة التفاعلDocument6 pagesالتتبع الزمني لتحول كيميائي - سرعة التفاعلAmine taikNo ratings yet
- Kanem U1Document1 pageKanem U1Alilou GuevarachéNo ratings yet
- النموذج الثالثDocument1 pageالنموذج الثالثChi KouNo ratings yet
- Composition de Physique 3AS - Sujet 03Document2 pagesComposition de Physique 3AS - Sujet 03Hasan RajawiNo ratings yet
- المعايرة المباشرة Le dosage directDocument1 pageالمعايرة المباشرة Le dosage directYassine BerchilNo ratings yet
- ملف مساعدة بلغيثDocument8 pagesملف مساعدة بلغيثnadja7.nadja7No ratings yet
- _-_-_-_-_-_-_Document25 pages_-_-_-_-_-_-_آلاء الرحمن100% (2)
- فيزياء - الموضوع التحضيري 01 التصحيح للفصل الأول - نافع - بكالوريا 2022Document12 pagesفيزياء - الموضوع التحضيري 01 التصحيح للفصل الأول - نافع - بكالوريا 2022Ahmed FerdjiouiNo ratings yet
- Exoch1- التــــحولات السريعة و ت. البطيئة-2-5Document4 pagesExoch1- التــــحولات السريعة و ت. البطيئة-2-5jamal ELYAKOUTINo ratings yet
- تمارينات المتابعة الزمنية لتحول كيميائي للأستاذ التيجاني دهام PDFDocument6 pagesتمارينات المتابعة الزمنية لتحول كيميائي للأستاذ التيجاني دهام PDFAmine ChettafNo ratings yet
- Dzexams 1as Physique 2834393Document5 pagesDzexams 1as Physique 2834393Lydia KhelifiNo ratings yet
- Physics 2mtm22 2trim3Document1 pagePhysics 2mtm22 2trim3agboubiNo ratings yet
- السلسلة رقم 04 (المعايرة اللونية) الاستاذ عليوات عامرDocument3 pagesالسلسلة رقم 04 (المعايرة اللونية) الاستاذ عليوات عامرbeautyy100% (1)
- المعايرة المباشرة-تمارينDocument1 pageالمعايرة المباشرة-تمارينNoureddine Elkouay38% (8)
- Alttba Alzmni Llthol Sraa Altfaal Anshta 1Document3 pagesAlttba Alzmni Llthol Sraa Altfaal Anshta 1Raja AferyadNo ratings yet
- Composition 2 Eme Trimestre 2AS MDocument2 pagesComposition 2 Eme Trimestre 2AS MdfdfdfNo ratings yet
- سلسلة تمارين وحدة المتابعة الزمنية لتحول كيميائي في الفيزياء للسنة الثالثة ثانوي الشعب العلمية 2020 - 2021Document16 pagesسلسلة تمارين وحدة المتابعة الزمنية لتحول كيميائي في الفيزياء للسنة الثالثة ثانوي الشعب العلمية 2020 - 2021سمير دبيليNo ratings yet
- التتبع الزمني لتحول كميائي سرعة التفاعلDocument10 pagesالتتبع الزمني لتحول كميائي سرعة التفاعلalmuslim80% (5)
- Examin 000Document2 pagesExamin 000dam 12No ratings yet
- الاختبار العملي-1 - 231212 - 070223Document4 pagesالاختبار العملي-1 - 231212 - 070223alasmaylya9No ratings yet
- Dzexams 2as Physique 176279Document5 pagesDzexams 2as Physique 176279sammouad49No ratings yet
- Dzexams Uploads Sujets 1021979Document5 pagesDzexams Uploads Sujets 1021979Kerboub IdrisNo ratings yet
- Bac Blan 01Document4 pagesBac Blan 01Hamza ZianeNo ratings yet
- 2s CompoDocument2 pages2s Compoamine milanoNo ratings yet
- Physics 2se22 2trim7Document2 pagesPhysics 2se22 2trim7Youcef JousephNo ratings yet
- Compo3Prem SoumiaDocument3 pagesCompo3Prem SoumiaManou100% (1)
- تمارين مقترحة حول من المجهري الى العياني12Document3 pagesتمارين مقترحة حول من المجهري الى العياني12simousimgsmNo ratings yet
- التتبع الزمني لتحول كيميائي - سرعة التفاعل-الأنشطة1Document4 pagesالتتبع الزمني لتحول كيميائي - سرعة التفاعل-الأنشطة1Mostafa ELJETTINo ratings yet
- Dzexams Docs 3as 907353Document17 pagesDzexams Docs 3as 907353Abderrahmane henniNo ratings yet
- EXM 2 SC FINELDocument4 pagesEXM 2 SC FINELYoucef JousephNo ratings yet
- سلسلة تمارين حول الناقليةDocument2 pagesسلسلة تمارين حول الناقليةabbird935No ratings yet
- Dzexams Docs 3as 907415Document5 pagesDzexams Docs 3as 907415abdouh4214No ratings yet
- PpppooDocument2 pagesPpppooImad Eddine sahraouiNo ratings yet
- Dzexams 2as Physique 722291Document6 pagesDzexams 2as Physique 722291Mohamed MohamedNo ratings yet
- Dzexams 3as Physique 469651Document3 pagesDzexams 3as Physique 469651Abdou AbdouNo ratings yet
- 2AS U12 - E3 - Cour-Exe 04Document34 pages2AS U12 - E3 - Cour-Exe 04sylvie jackline50% (2)
- الموضوع رقم 1Document4 pagesالموضوع رقم 1Espoire Lavie0% (1)
- Physics 2se22 2trim7Document2 pagesPhysics 2se22 2trim7BOUCHEFFA HalimNo ratings yet
- 8Document2 pages8e.maskarNo ratings yet
- بطاقة التلميذ رقم 01Document2 pagesبطاقة التلميذ رقم 01FLASH FFNo ratings yet
- Physics 2se18 2trim d1Document2 pagesPhysics 2se18 2trim d1mussariNo ratings yet
- CC 1013Document2 pagesCC 1013mussariNo ratings yet
- Procedes 2mt20 1trim6Document2 pagesProcedes 2mt20 1trim6مولودNo ratings yet
- Abb 2Document1 pageAbb 2Amel HbNo ratings yet
- Tamarind As - U7 - Oxred - 2023Document3 pagesTamarind As - U7 - Oxred - 2023Ma Ry100% (1)
- تعيين معامل اللزوجة للجلسرين 00Document2 pagesتعيين معامل اللزوجة للجلسرين 00طه الحصنNo ratings yet
- سلسلة الأكسدة والإرجاع مع الحلول المفصلة - الأستاذ كريم سني 2022Document7 pagesسلسلة الأكسدة والإرجاع مع الحلول المفصلة - الأستاذ كريم سني 2022widad doudiNo ratings yet
- Dzexams 2as Physique As E2 20181 722291Document5 pagesDzexams 2as Physique As E2 20181 722291AS SIANo ratings yet
- سلسلة المراجعة في عطلة الشتاءDocument13 pagesسلسلة المراجعة في عطلة الشتاءFouad Ayadi100% (1)
- السلسلة 4Document2 pagesالسلسلة 4Sami RabhiNo ratings yet
- سلسة رقم 2 الدور ة 1 إنتشار موجة ضوئية ، التتبع الزمني لتحول كيميائي 2015 2014Document4 pagesسلسة رقم 2 الدور ة 1 إنتشار موجة ضوئية ، التتبع الزمني لتحول كيميائي 2015 2014PAUSE RACENo ratings yet
- سلسلة المكتسبات القبلية 2023 (جبالي رفيق)Document3 pagesسلسلة المكتسبات القبلية 2023 (جبالي رفيق)Hina BouzerzourNo ratings yet
- Dzexams 2as Physique 698131Document3 pagesDzexams 2as Physique 698131yassminmayaNo ratings yet
- Dzexams 2as Physique 772341Document3 pagesDzexams 2as Physique 772341Zohra MedNo ratings yet
- 1 PDFDocument14 pages1 PDFDjom AnaNo ratings yet
- الدرس الثانيDocument5 pagesالدرس الثانيChi KouNo ratings yet
- OxrdDocument2 pagesOxrdChi Kou100% (1)
- النموذج الثالثDocument1 pageالنموذج الثالثChi KouNo ratings yet
- Exam 2as Trim2Document2 pagesExam 2as Trim2Chi KouNo ratings yet
- نظام الجماعة التربوية في المؤسسات التربويةDocument10 pagesنظام الجماعة التربوية في المؤسسات التربويةChi KouNo ratings yet