Professional Documents
Culture Documents
Identifikasi Kation Golongan Ii A
Uploaded by
Lilis Setiawati0 ratings0% found this document useful (0 votes)
45 views10 pagesBagan pemisahan golongan II A
Original Title
KELOMPOK 2
Copyright
© © All Rights Reserved
Available Formats
PPTX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentBagan pemisahan golongan II A
Copyright:
© All Rights Reserved
Available Formats
Download as PPTX, PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
45 views10 pagesIdentifikasi Kation Golongan Ii A
Uploaded by
Lilis SetiawatiBagan pemisahan golongan II A
Copyright:
© All Rights Reserved
Available Formats
Download as PPTX, PDF, TXT or read online from Scribd
You are on page 1of 10
IDENTIFIKASI KATION GOLONGAN II A
AHMAD REVAN SYAH REZA
AI CUCU KARLINA
AIDA NUR AZIZAH
BALQIS YUMNA KALTSUM
ISMA NUR FAUJIAH
HFAHMI SHIHAB
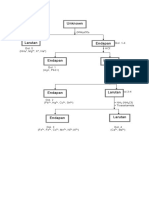
Endapan HgS/PbS/Bi2S3,CdS dan CuS+
+ 5 ml
HNO3 encer
HgS Cd2+ Slide 4 Bi3+ Pb2+
Hitam Cu2+
+ NH3 Pekat >
sentrifugasi
[Cu(NH3)4]2+
BiOH3 , PbOH2
[Cd(NH3)4]2+
+ 5 ml NaOH
Tak berwarna Biru
Bagi larutan menjadi 2 bagian
Alirkan H2S
Filtrat
BiOH3 Bagian Besar Bagian Kecil
[PbOH4]2- Endapan
kuning CdS +KCN( Biru + CH3COOH
Hilang) + [K4(Fe)CN3]
+ HNO3 + CH3COOH + H2S
Cuci dgn H2O
Saring + 2 tetes K2CrO4
+ Na₂[Sn(OH)₄] Endapan
Kinkonina KI Coklat Merah
Kuning CdS
Merah (kuning)PbCrO4
Residu Hitam/Bi
Jingga/Bi
Endapan HgS/PbS/Bi₂S₃,CdS dan CuS+
1 Pindahkan endapan ke cawan porselen dan tambahkan 5
ml HNO3 encer
Endapan 2 Didihkan perlahan lahan selama
beberapa menit
3 Saring dan cuci dengan sedikit air
Cd2+ Bi3+ Pb2+ Cu2+
ditambahkan NH3 berlebihan
Cd2+ Cu2+ Menjadi Bi3+ Pb2+ diendapkan
kompleks dan tetap sebagai hidroksida
tinggal dalam larutan
Cd2+ Cu2+ Menjadi kompleks
dan tetap tinggal dalam larutan
Cu²⁺ + 4NH₃ → [Cu(NH₃)₄] ²⁺
Cd²⁺ + 4NH₃ → [Cd(NH₃)₄] ²⁺
Bi3+ Pb2+ diendapkan
sebagai hidroksida
Biᵌ⁺ + 3NH₃ + 3H₂O → Bi(OH)₃↓ + 3NH₄⁺
Pb²⁺ + 2NH₃ + 3H₂O → Pb(OH)₂↓ + 2NH₄⁺
Persamaan reaksi
Cu2+ + 4NH3 → [Cu(NH3)4]2+
Cd2+ + 4NH3 → [Cd(NH3)4]2+
Bi3+ + 3NH3 + 3H2O→ Bi(OH)3 ↓ + 3 NH4+
Pb2+ + 2NH3 + 2H2O→ Pb(OH)2 ↓ + 2NH4+
Pb(OH)2 ↓ + 2OH- → [Pb(OH)4]2-
Cu2+ Hg2+ Cd2+ Bi3+ Pb2+
+ H2S
CuS HgS CdS BiS PbS
+ HNO3 encer
+ H2O Cuci
CuS CdS BiS PbS
HgS
Putih + H2SO4 (e) + Alkohol
+ H2O aduk
+ NaOCl + H2O cuci
+ HCl encer
Panaskan PbSO4
HgCl2 Cu2+ Cd2+ Bi3+
Putih
+ SnCl2 + NH4COOH
+ NH3 Pekat >>
+ CH3COOH
Hg (hitam)
+ K2Cr2O7 Bi3+ [Cu(NH3)4]2+
Putih
PbCrO4 (Kuning) [Cd(NH3)4]2+
+ H2O cuci + CH3COOH
+ HCl encer
Cu2+ Cd2+
BiOH3 Hitam
+ KCN
+ [K4(Fe)CN3]
+ H2S
Cu2[Fe(CN)6] Coklat CdSCN
Kemerahan Kuning
Persamaan reaksi
3PbS↓ + 8H⁺ + 2NO₃⁻ → 3Pb²⁺ + 3S↓ + 2NO↑ + 4H₂O
Bi₂S₃↓ + 8H⁺ + 2NO₃⁻ → 2Bi³⁺ + 3S↓ + 2NO↑ + 4H₂O
3CuS↓ + 8H⁺ + 2NO₃⁻ → 3Cu²⁺ + 3S↓ + 2NO↑ + 4H₂O
3CdS↓ + 8H⁺ + 2NO₃⁻ → 3Cd²⁺ + 3S↓ + 2NO↑ + 4H₂O
HgS↓ + OCl⁻ + 2H⁺ + Cl⁻ → HgCl₂ + S↓ + H₂O
2HgCl₂ + Sn²⁺ → Hg₂Cl₂↓ + Sn⁴⁺ + 2Cl⁻
Pb²⁺ + SO₄²⁻ → PbSO₄
PbSO₄↓ + 4CH₃COO⁻ → [Pb (CH₃COO)₄]²⁻ + SO₄²⁻
[Pb (CH₃COO)₄]²⁻ + CrO₄²⁻ → PbCrO₄↓ + 4CH₃COO⁻
Bi³⁺ + 3NH₃ + 3H₂O → Bi(OH)₃↓ + 3NH₄⁺
Cu²⁺ + 4NH₃ → [Cu(NH₃)₄]²⁺ (biru)
Cd²⁺ + 4NH₃ → [Cd(NH₃)₄²⁺ (tak berwarna)
2Bi3+ + 3[Sn(OH)4]2- + 6OH- → 2Bi↓ + 3[Sn(OH)6]2-
[Cu(NH3)4]2- + 4CH3COOH → Cu2+ + 4NH4+ + 4CH3COO-
2Cu2+ + [fe(CN)6]4- →Cu2[Fe(CN)6]↓
[Cd(NH3)4]2+ + H2S → CdS↓+ 4NH4+ +2NH3
[Cd(NH3)4]2+ + 4CN- → [Cd(CN)4]2-+ 4NH3
2[Cu(NH3)4]2+ + 10CN- →2[Cu(CN)4]3- + (CN)2↑+
8NH3
(CN)2+2NH3+H2O → CNO- + CN- + 2NH4+
[Cd(CN)4]2- + H2S+ 2NH3→CdS↓ + 2NH4+ + 4CN-
You might also like
- Colored Gold.Document30 pagesColored Gold.Allah dittaNo ratings yet
- Round 18.07.2019Document2 pagesRound 18.07.2019Shital Tayshete100% (1)
- List of ChemicalsDocument2 pagesList of ChemicalsShahzaibUsman100% (1)
- Evaluation of A Diagnostic Leaching Technique For Gold inDocument12 pagesEvaluation of A Diagnostic Leaching Technique For Gold inEdgar PérezNo ratings yet
- 2020-I-Marcha Sistematica I-Ii-IiiDocument2 pages2020-I-Marcha Sistematica I-Ii-IiiAdrianQuispeNo ratings yet
- Analisis Kation Golongan IIDocument27 pagesAnalisis Kation Golongan IInabilaNo ratings yet
- Chemistry SummaryDocument22 pagesChemistry SummaryEmma Isabella GraceNo ratings yet
- Chemistry Lecture Notes: TopicDocument5 pagesChemistry Lecture Notes: TopicRahul NairNo ratings yet
- Ag, Pb, Hg Hno, Nacl Agcl, Hg Cl, Pbcl Δ Agcl, Hg Cl PbDocument3 pagesAg, Pb, Hg Hno, Nacl Agcl, Hg Cl, Pbcl Δ Agcl, Hg Cl PbDina Donna AnzNo ratings yet
- Class 11 Chemistry Practicals (Qualitative Analysis)Document5 pagesClass 11 Chemistry Practicals (Qualitative Analysis)Ravibabu BoddaNo ratings yet
- Grap Nhom Halogen Hay So 1Document4 pagesGrap Nhom Halogen Hay So 1Anonymous hsV1btNo ratings yet
- CationDocument6 pagesCationableskotaNo ratings yet
- Class 11 Chemistry Practicals (Qualitative Analysis)Document5 pagesClass 11 Chemistry Practicals (Qualitative Analysis)Freak 9710No ratings yet
- QUALITATIVE ANALYSIS OF IONS (USP ID Tests)Document12 pagesQUALITATIVE ANALYSIS OF IONS (USP ID Tests)Kirsten Joyce VillajuanNo ratings yet
- CationDocument4 pagesCationApril Anne Tigue0% (1)
- 34 Qualitative Analysis Formula Sheets QuizrrDocument11 pages34 Qualitative Analysis Formula Sheets QuizrrSwapnil SharmaNo ratings yet
- Chemistry 12th Formula SheetDocument138 pagesChemistry 12th Formula Sheetnikhils.ind18No ratings yet
- Chapter 3cationDocument31 pagesChapter 3cationDexan Ross AlquilitaNo ratings yet
- MINDMAP Alkene, Benzene, HaloalkaneDocument3 pagesMINDMAP Alkene, Benzene, HaloalkaneLeow JiashengNo ratings yet
- Inorganic Radical TestsDocument6 pagesInorganic Radical TestsChesterBourdonNo ratings yet
- Aqueous Ion ColoursDocument1 pageAqueous Ion ColoursAnita OguniNo ratings yet
- Chemical Equation (2019)Document1 pageChemical Equation (2019)Ismalinda AbdullahNo ratings yet
- Scheme of Salt Analysis 1 PDFDocument13 pagesScheme of Salt Analysis 1 PDFFreyaNo ratings yet
- Worksheet No. 8 Group IIA Cations GROUP4 PCQADocument4 pagesWorksheet No. 8 Group IIA Cations GROUP4 PCQAAndrew CraigieNo ratings yet
- Heating EffectDocument9 pagesHeating Effectshubhra.kuldeep2003No ratings yet
- Separation & Identification of GROUP II CationsDocument12 pagesSeparation & Identification of GROUP II CationsxbillupsNo ratings yet
- Salt Analysis - TheoryDocument8 pagesSalt Analysis - TheoryBeat StabberNo ratings yet
- Salt AnalysisDocument8 pagesSalt AnalysisSyed Mohdammad AliNo ratings yet
- Chemical Reference Material: Formulae and Names of Some Common IonsDocument8 pagesChemical Reference Material: Formulae and Names of Some Common Ionsbmnyandu2003No ratings yet
- Tarea 10 Equilibrios de Formación de Complejos y Valoraciones ComplejométricasDocument6 pagesTarea 10 Equilibrios de Formación de Complejos y Valoraciones ComplejométricasSebastian bravo gañanNo ratings yet
- Analitik Analisis Kation PDFDocument17 pagesAnalitik Analisis Kation PDFekaNo ratings yet
- Salt Analysis: Test For AnionsDocument5 pagesSalt Analysis: Test For AnionsMamata RNo ratings yet
- Met Al Aqueous Ion Limited Naoh Limited NH Excess Naoh Excess NH Na Co HCLDocument2 pagesMet Al Aqueous Ion Limited Naoh Limited NH Excess Naoh Excess NH Na Co HCLZeenat AfrozeNo ratings yet
- Wa0019.Document13 pagesWa0019.shreyassantoshkurupNo ratings yet
- XII Chemistry Practical 2022-23Document28 pagesXII Chemistry Practical 2022-23Tech ArjunNo ratings yet
- NOTES Inorganic ReactionsDocument43 pagesNOTES Inorganic Reactionsvaishnavi singhNo ratings yet
- 17 - Qualitative Analysis (Anion)Document3 pages17 - Qualitative Analysis (Anion)Aditya SrivastavaNo ratings yet
- Systematic Analysis of A Simple Salt Anion PartDocument5 pagesSystematic Analysis of A Simple Salt Anion Partnightcore tamikoNo ratings yet
- Unknown: Uji KationDocument3 pagesUnknown: Uji Kationainun tasbihNo ratings yet
- Nhận Biết. OrganicDocument3 pagesNhận Biết. OrganicTrung Hoàng HuyNo ratings yet
- Tabele Chimie Analitica Grupele 1 2 Si 4Document38 pagesTabele Chimie Analitica Grupele 1 2 Si 4I IiNo ratings yet
- Salt AnalysisDocument8 pagesSalt AnalysisRaziaNo ratings yet
- SALTANALYSISLABMANUAL 9owo8xhodwx68kh7Document13 pagesSALTANALYSISLABMANUAL 9owo8xhodwx68kh7Lalith AdityaNo ratings yet
- Bagan Kation 1 - 3Document7 pagesBagan Kation 1 - 3Angelica ErnitaNo ratings yet
- Bagan Kation 1 - 3Document7 pagesBagan Kation 1 - 3Angelica ErnitaNo ratings yet
- Bagan Kation 1 - 3Document7 pagesBagan Kation 1 - 3Angelica ErnitaNo ratings yet
- Qualitative Analysis of Cation Group 2 enDocument14 pagesQualitative Analysis of Cation Group 2 enMelissa SueltoNo ratings yet
- Identifikasi KationDocument3 pagesIdentifikasi KationNormanPrabowoNo ratings yet
- Bagan Pemisahan Kation Kation Golongan IDocument4 pagesBagan Pemisahan Kation Kation Golongan IOra DuweNo ratings yet
- Oxidation Numbers 11Document2 pagesOxidation Numbers 11SimonNo ratings yet
- (Class Xii Chemistry Practicals) : Experiment - 1 Classification of Anions Group Reagent Observation InferenceDocument26 pages(Class Xii Chemistry Practicals) : Experiment - 1 Classification of Anions Group Reagent Observation InferenceMeena QueenNo ratings yet
- (Class Xii Chemistry Practicals) : Experiment - 1 Classification of Anions Group Reagent Observation InferenceDocument15 pages(Class Xii Chemistry Practicals) : Experiment - 1 Classification of Anions Group Reagent Observation InferenceAbhay ManwalNo ratings yet
- Xii Chemistry Practical Salt AnalysisDocument13 pagesXii Chemistry Practical Salt AnalysisNupur GuptaNo ratings yet
- Heating Effects (12th&13th)Document4 pagesHeating Effects (12th&13th)Raju SinghNo ratings yet
- Qualitative Analysis of Group B CationsDocument4 pagesQualitative Analysis of Group B CationsShane AmolarNo ratings yet
- Scheme For The Analysis of Inorganic Mixtures2Document12 pagesScheme For The Analysis of Inorganic Mixtures2MinuNo ratings yet
- Heating Effect of Carbonate & Bicarbonate SaltsDocument3 pagesHeating Effect of Carbonate & Bicarbonate Saltsvishwajit patilNo ratings yet
- 06 1092 S CationAnalysisGroup II 0302Document16 pages06 1092 S CationAnalysisGroup II 0302Ana Laura Mendoza AriasNo ratings yet
- 5 Centrifuge Tubes Evaporating Dish Test Tube Holder Crucible Tongs Two Droppers Latex Gloves LabelsDocument16 pages5 Centrifuge Tubes Evaporating Dish Test Tube Holder Crucible Tongs Two Droppers Latex Gloves LabelsMatti MendozaNo ratings yet
- 2c ANSWERS Balancing Equations (2017)Document1 page2c ANSWERS Balancing Equations (2017)Karina LeungNo ratings yet
- IOC All ReactionsDocument56 pagesIOC All ReactionsKeerthana MNo ratings yet
- Salt AnalysisDocument9 pagesSalt AnalysisAnanyaNo ratings yet
- LN46B530P7F Parts ListDocument17 pagesLN46B530P7F Parts ListChris FleckNo ratings yet
- Iijs 2012 Floor PlanDocument1 pageIijs 2012 Floor PlanPalak ShahNo ratings yet
- Pupuk PT SSA PDFDocument2 pagesPupuk PT SSA PDFNurul HardiyantiNo ratings yet
- Fluktuasi LimbahDocument5 pagesFluktuasi LimbahpraditioramaNo ratings yet
- An Important Exhibition of Seven Rare Gem DiamondsDocument8 pagesAn Important Exhibition of Seven Rare Gem DiamondsClaireNo ratings yet
- Lista Llantas JL SPORT 2017-18Document4,061 pagesLista Llantas JL SPORT 2017-18Bernardo RamirezNo ratings yet
- MPC's Entire Brass Mortise Catalogue NewDocument32 pagesMPC's Entire Brass Mortise Catalogue NewayaanNo ratings yet
- IndexDocument49 pagesIndexImelda SitumorangNo ratings yet
- QC Chart - ICP-OES - FINALDocument62 pagesQC Chart - ICP-OES - FINALConsultant JerocasNo ratings yet
- Comparison List Copper Bronze 2011 1Document7 pagesComparison List Copper Bronze 2011 1NaldoVicenteNo ratings yet
- Build Your Own Engagement Ring - Engagement Ring Settings Brilliant Earth PDFDocument1 pageBuild Your Own Engagement Ring - Engagement Ring Settings Brilliant Earth PDFMarisa EsquerNo ratings yet
- The Beatitudes V MartynovDocument22 pagesThe Beatitudes V Martynovada.shakespeare6183No ratings yet
- RoundDocument2 pagesRoundHarsh Kukadia100% (1)
- Bracelets On Cartier® Official Website Cartier USDocument1 pageBracelets On Cartier® Official Website Cartier USAntea JukićNo ratings yet
- 3935 A722-43007 - Rev00 - 01Document55 pages3935 A722-43007 - Rev00 - 01Elena CucerNo ratings yet
- Copper Alloy Datasheet - AmericanDocument58 pagesCopper Alloy Datasheet - Americanyw_oulalaNo ratings yet
- Silver-Anklets Broad-Match in 2024-04-02Document6 pagesSilver-Anklets Broad-Match in 2024-04-02MNR SolutionsNo ratings yet
- Report of Analysis: EL/I/15/ 06.2820 Air Limbah Waste WaterDocument2 pagesReport of Analysis: EL/I/15/ 06.2820 Air Limbah Waste WatergintaniNo ratings yet
- Pendants PDFDocument161 pagesPendants PDFmohammad nadherNo ratings yet
- Professional Jewelry MakingDocument30 pagesProfessional Jewelry MakingGeorge AnkiriNo ratings yet
- Skripsi Tanpa Bab Pembahasan PDFDocument81 pagesSkripsi Tanpa Bab Pembahasan PDFKiki RifkyNo ratings yet
- GRAFFDocument6 pagesGRAFFumangNo ratings yet
- Resistivity of MaterialsDocument1 pageResistivity of MaterialsMocharu ArtNo ratings yet
- Accustandard: Inorganic Reference Standards For Use With Popular Analytical InstrumentationDocument12 pagesAccustandard: Inorganic Reference Standards For Use With Popular Analytical InstrumentationAlexSNo ratings yet
- Pear Cut Diamond Size Chart (Carat Weight To MM Size)Document1 pagePear Cut Diamond Size Chart (Carat Weight To MM Size)Hitesh SinghviNo ratings yet
- Exploded View & Part ListDocument80 pagesExploded View & Part Listslb04786No ratings yet