Professional Documents
Culture Documents
Materijalni Bilansi Rev1
Uploaded by
Mile ZoricOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Materijalni Bilansi Rev1
Uploaded by
Mile ZoricCopyright:
Available Formats
1
Primer 1
Potrebno je pripremiti 5 % mas suspenziju Ca(OH)
2
u vodi tako to e se razblaiti suspenzija
koncentracije 20 % mas. Odrediti masu vode i koncetrovane suspenzije da bi se dobilo 2000 kg
razblaene suspenzije.
* * *
Oznake:
m masa u kg;
g maseni udeo Ca(OH)
2
;
1 (u indeksu) koncentrovana suspenuija;
2 (u indeksu) voda;
3 (u indeksu) razblaena suspenzija.
Podaci:
m
3
= 2000 kg
g
1
= 0,05
g
2
= 0
g
3
= 0,2
Potrebno je odrediti:
m
1
i m
2
Postavljaju se jednaine ukupnog i komponentnog bilansa koje s odnose na stanje posmatranog
sistema pre i posle razblaenja:
m
1
+ m
2
= m
3
g
1
m
1
+ g
2
m
2
= g
3
m
3
Obzirom da je g
2
= 0, iz bilansa Ca(OH)
2
neposredno se dobija:
m
1
= g
3
m
3
/g
1
= 0,052000/0,2 = 500 kg
Zamena m
1
u jednainu ukupnog bilansa daje:
m
2
= m
3
m
1
= 2000 500 = 1500 kg
2
Primer 2
U reaktor se uvodi gasna smea etena, kiseonika, azota i hlovodonika iji je sastav dat u sledeoj
tabeli:
Komponenta % mas
C
2
H
4
16
O
2
9
N
2
31
Ako se zna da je protok etena 4000 Nm
3
/h izraunati protoke ostalih komponenti i ukupan protok
reakcione smee.
* * *
Kako je protok etena dat u jedinici zapremine po jedinici vremena, a sastav smee u masenim
procentima, potrebno je izvriti izbor izmeu dve mogunosti:
- preraunati masene u zapreminske (molske) procente i traene protoke odrediti u jedinici
zapremine po jedinici vremena;
- preraunati zapreminski protok u maseni i traene protoke odrediti u jedinici mase po jedinici
vremena.
Obzirom da je jednostavnije preraunati jedan zapreminski protok u maseni nego masene procente
svih komponenti u zapreminske procente, bira se druga mogunost.
Na osnovu jednaine stanja idealnog gasa:
m
C2H4
= p
o
V
eten
M
C2H4
/(RT
o
) = 101,325400028,05/(8,3145273,15) = 5006 kg/h
Sledi:
m
ukupno
= 5006/0,16 = 31288 kg/h
m
O2
= 0,0931288 = 2816 kg/h
m
N2
= 0,3131288 = 9699 kg/h
m
HCl
= m
ukupno
m
C2H4
m
O2
m
N2
= 13767 kg/h
Provera maseni procenat HCl:
% HCl = 10013767/31288 = 44
% HCl = 100 16 9 31 = 44
3
Primer 3
Koncentracija hlovodonine kiseline tehnike istoe iznosi 28 % mas. Izraziti koncentraciju HCl u %
mol.
* * *
Moski udeo j-te komponente u tenoj fazi koju ini N komponenti definisan je sa:
=
=
N
1 i
i
j
j
n
n
x
gde je sa n
i
oznaen broj molova i-te komponente, pri emu vai i = 1,N.
Vai:
i
i
i
i
i
M
m g
M
m
n = =
gde je:
m ukupna masa posmatrane smee;
m
i
masa i-te komponente u posmatranoj smei;
g
i
maseni udeo i-te komponente u posamtranoj smei;
M
i
molekulska masa i-te komponente.
Sledi:
=
=
N
1 i i
i
j
j
j
M
g
M
g
x
U konkretnom sluaju dobija se (1 u indeksu HCl; 2 u indeksu H
2
O):
M
1
= 36,461 g/mol
M
2
= 18,0153 g/mol
g
1
= 0,28
g
2
= 1 0,28 = 0,72
1 , 16 161 , 0
0 , 18
72 , 0
5 , 36
28 , 0
5 , 36
28 , 0
x
1
= =
+
= % mol
4
Primer 4
U laboratoriji ustanove za kontrolu kvaliteta roba izvrena je analiza uzorka autogasa uzetog na nekoj
benzinskoj pumpi i pri tom je utvren sledei sastav:
Komponenta % vol
metan 0,11
etan 1,31
propan 35,98
izobutan 26,16
n-butan 35,57
izopentan 0,49
n-pentan 0,38
Prema nacionalnom standardu autogas mora da zadovoljava specifikacije standarda za propan-butan
smeu prema kojem je najmanji dozvoljeni sadraj butana 65 % mas, dok su maksimalno dozvoljene
koncentracije metana i etana 3,0 % mas, a pentana 1,0 %. Da li je analizirani autogas zadovoljava
specifikacije propisane standardom?
* * *
Na osnovu jednaine stanja idealnog gasa vai jednakost izmeu molskih i zapreminskih udela:
j
N , 1 i
i
j
N , 1 i
i
j
j
v
V
V
n
n
y = = =
= =
gde su sa y
j
i v
j
oznaeni molski i zapreminski udeli j-te komponente u gasnoj smei, dok n
j
i V
j
predstavljaju broj molova i zapreminu date komponente u posmatranoj smei. Molski udeli mogu se
preraunati u masene na osnovu sledeeg izraza (n je ukupan broj molova u smei):
=
= = =
=
= = =
N , 1 i
i i
j j
j
N , 1 i
i i
j j
N , 1 i
i i
j j
N , 1 i
i
j
j
M y
M y
g
nM y
nM y
M n
M n
m
m
g
Sledi:
Komponenta % mol M g/mol
(% mol)(M)
% mas
metan 0,11 16,0425 1,75 0,03
etan 1,31 30,068 39,34 0,75
propan 35,98 44,094 1586,34 30,05
izobutan 26,16 58,12 1520,68 28,81
n-butan 35,57 58,12 2067,32 39,17
izopentan 0,49 72,146 35,39 0,67
n-pentan 0,38 72,146 27,53 0,52
S 100,00 5278,34 100,00
5
Sadraj metana i etana:
0,03 + 0,075 = 0,78 < 3,0 % mas zadovoljava
Sadraj butana:
28,81 + 39,17 = 67,98 > 65 % mas zadovoljava
Sadraj pentana:
0,67 + 0,52 = 1,19 mas ne zadovoljava
Prema tome, zbog visokog sadraja pentana analizirani autogas ne zadovoljava standardom propisan
sastav.
6
Primer 5
Da bi se obezbedila kisela funkcija katalizatora na postrojenju za reformiranje benzina, u sirovinski
tok se dozira 1,5 ppm mas propilendihlorida (PDC). Injektiranje PDC-a vri se membranskom dozir-
pumpom iji se kapacitet kontrolie preko kalibracionog nivokaznog stakla. Odrediti potreban protok
PDC-a u cm
3
/min, kao i promenu nivoa PDC-a u nivokaznom staklu u mm u vremenskom intervalu
od 15 min. Izraunati i broj buradi PDC-a potrebnih za godinu dana rada postrojenja pretpostaviti da
e postrojenje imati 330 radnih dana u godini, pri emu uzeti kao meru sigurnosti da je potrebna
koliina PDC-a za 10 % vea od raunski odreene potronje. Sistem za doziranje sa podacima
potrebnim za proraun dat je na priloenoj slici.
A
z
o
t
* * *
Podaci:
- maseni udeo PDC-a u sirovinskom toku, g = 1,510
-6
- zapreminski protok sirovine, V
1
= 72 m
3
/h;
- gustina sirovine,
1
= 740 kg/m
3
;
- gustina PDC-a,
2
= 1150 kg/m
3
;
- unutranji prenik kalibracionog stakla, d = 20 mm = 2 cm;
- zapremina PDC-a u punom buretu, V
b
= 200 dm
3
.
Potrebno je odrediti:
- V
2
zapreminski protok PDC-a, cm
3
/min;
- AH promenu nivoa PDC-a u mm u periodu od 15 min, mm/15min;
- N
b
godinja potronja buradi PDC-a.
7
Maseni protok sirovine:
m
1
=
1
V
1
= 74072/3600 = 14,8 kg/s
Vai:
1
2
2 1
2
m
m
m m
m
g ~
+
=
gde je m
2
maseni protok PDC-a, pri emu je m
2
<< m
1
.
Sledi:
m
2
= gm
1
= 1,510
-6
14,860 = 1,33210
-3
kg/min
Zapreminski protok PDC-a:
V
2
= m
2
/
2
= (1,33210
-3
/1150)110
6
= 1,158 cm
3
/min
V
2
= 1,1586024/1000 = 1,668 dm
3
/dan
Zapremina doziranog PDC-a u periodu od 15 min:
AV = 15V
2
= 151,158 = 17,37 cm
3
Povrina poprenog preseka kalibracionog stakla:
A = d
2
t/4 = 2
2
t/4 = 3,14 cm
2
Promena nivoa PDC-a u kalibracionom staklu u periodu od 15 min:
AH = AV/A = (17,37/3,14)10 = 55,3 55 mm
Godinja potronja PDC-a:
V
2,god
= 330V
2
= 550,44 dm
3
/god
Potreban broj buradi PDC-a za godinu dana rada:
N
b
= 1,1V
b
/V
2,god
= 3 bureta PDC-a
Provera:
(3/1,1)0,21,150 = 0,6273 t PDC/god
7274024330/1000 = 421978 t sirovine/god
g = 0,6273/421978 = 1,510
-6
= 1,5 ppm mas
8
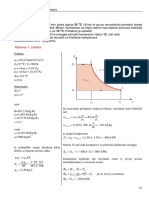
Primer 6
Za skladitenje azota koriste se horizontalni cilindrini rezervoari, pri emu zapremina svakog
rezervoara iznosi 25 m
3
. Punjenje rezervoara vri se kompresorom iji je kapacitet priblino
konstantan i iznosi 300 Nm
3
/h. Odrediti vreme potrebno da se izvri dopuna jednog rezervoara do
pritiska od 100 bar ako je poetni pritisak u njemu 40 bar. Uzeti da je temperatura u rezervoaru
konstantna i da iznosi 300 K.
* * *
ematski prikaz dopune rezervoara azotom:
. const p =
rezervoaru u azota masa , m
p
m 25 V
K 300 T
2
3
=
=
azota protok maseni , m
h / Nm 300 V
3
=
Maseni bilans postavljen za naznaeni bilansni krug:
dt
dm
m =
U posmatranom opsegu pritisaka i na datoj temperaturi moe se uzeti da se azot ponaa kao idealan
gas, te je:
dp
RT
VM
dm
RT
M V p
m
o
o
=
=
gde je p
o
= 101325 Pa, T
o
= 273,15 K (normalni uslovi).
Zamenom poslednje dve jednaine u bilansnu jednainu, njenim sreivanjem i integraljenjem u
granicama t = [0,t] i p = [p
poc
,p
kr
] dobija se:
5 , 4
01325 , 1
) 40 100 (
300
15 , 273
300
25
p
) p p (
T
T
V
V
t
o
poc kr
o
=
=
h
9
Primer 7
Napisati jednainu hemijske reakcije u kojoj se iz etena, hlora i kiseonika dobija vinilhlorid, pri emu
se kao sporedni proizvod reakcije dobija voda.
* * *
Reaktanti:
- eten, C
2
H
4
- hlor, Cl
2
- kiseonik, O
2
Proizvodi:
- vinilhlorid, C
2
H
3
Cl
- voda, H
2
O
Hemijska jednaina:
x
1
C
2
H
4
+ x
2
Cl
2
+ x
3
O
2
= x
4
C
2
H
3
Cl + x
5
H
2
O
Potrebno je odrediti vrednosti x
1
, x
2
, x
3
, x
4
i x
5
. Budui da je broj nepoznatih 5, potreban broj
jednaina dobie se postavljanjem etiri bilansne jednaine za 4 elementa koji ine reaktante i
proizvode i zadavanjem vrednosti 1 jednoj od traenih vrednosti x
i
. Pri postavljanju bilansnih
jednaina uzee se da uz svaku vrednost x
i
u hemijskoj jednaini figurie 1 mol odgovarajue
komponente.
Bilans ugljenika:
2x
1
= 2x
4
(1)
Bilans vodonika:
4x
1
= 3x
4
+ 2x
5
(2)
Bilans hlora:
2x
2
= x
4
(3)
Bilans kiseonika:
2x
3
= x
5
(4)
Napomena: komponentni bilans mase dobija se tako to svaki sabirak ini proizvod atomske mase
elementa, broja atoma datog elementa u odgovarajuem jedinjenju i odgovarajueg koeficijenta x
i
budui da atomska masa figurie u svakom sabirku, moe se izvriti njena eliminacija iz jednaine.
10
Neka je:
x
1
= 1
Sledi:
x
4
= 1 (na osnovu jednaine 1)
x
5
= (4 3)/2 = 1/2 (na osnovu jednaine 2)
x
2
= 1/2 (na osnovu jednaine 3)
x
3
= 1/4 (na osnovu jednaine 2)
C
2
H
4
+ Cl
2
+ O
2
= C
2
H
3
Cl + H
2
O
Mnoei hemijsku reakciju najveim imeniocem dobija se:
4C
2
H
4
+ 2Cl
2
+ O
2
= 4C
2
H
3
Cl + 2H
2
O
11
Primer 8
Vodena suspenzija koja sadri 25 % mas vrste faze uvodi se u filter. Pogaa i filtrat sadre redom 90
i 1 % mas vrste faze. Odrediti protoke filtrata i pogae ako je protok suspenzije 2000 kg/h.
* * *
Crtanje ematskog prikaza procesa sa naznaenim zadatim podacima i nepoznatim koje treba odrediti
i postavljanje bilansnog kruga
Analiza datog sistema i postavljanje osnova za proraun
Sistem ine dve komponente i tri materijalna toka. Sastavi tokova su definisani, tako da se maseni
protoci komponenti mogu odrediti preko sastava i ukupnog protoka datog toka. Od tri ukupna masena
protoka zadat je jedan, tako da je za odreivanje vrednosti masenih protoka preostala dva toka
potrebno postaviti dve bilansne jednaine. Prvu jednainu inie ukupni materijalni bilans postavljen
za naznaeni bilansni krug, druga jednaina bie bilans jedne od komponenti (neka to bude voda).
Bilans e biti raunat u kg/h.
Reenje
Bilansne jednaine:
m
S
= m
F
+ m
P
0,75m
S
= 0,99m
F
+ 0,1m
P
Sledi:
0,75m
S
= 0,99(m
S
m
P
) + 0,1m
P
3 , 539 m
1 , 0 99 , 0
75 , 0 99 , 0
m
S P
=
= kg/h
m
F
= m
S
m
P
= 1460,7 kg/h
Provera
Vri se preko bilansa komponente koji nije korien pri odreivanju traenih vrednosti.
0,25m
S
= 500 kg/h
0,01m
F
+ 0,9m
P
= 500 kg/h
12
Primer 9
U rektifikacionoj koloni vri se razdvajanje benzena i toluena na destilat i ostatak. Sastav napojne
smee je 60 % mol benzena i 40 % mol toluena. Ako se 95 % ulaznog benzena raspodeljuje u destilat,
a 98 % ulaznog toluena u ostatak, odrediti sastave destilata i ostatka, kao i protoke destilata i ostatka.
Protok napojne smee iznosi 250 kmol/h.
* * *
Crtanje ematskog prikaza procesa sa naznaenim zadatim podacima i nepoznatim koje treba odrediti
i postavljanje bilansnog kruga
Analiza datog sistema, postavljanje osnova za proraun i reenje
Broj tokova:
N
s
= 3;
Broj komponenti:
N
k
= 2;
Broj promenljivih:
N
p
= N
s
N
k
= 6;
Broj nezavisnih bilansnih jednaina koje se mogu napisati:
N
n
= N
k
= 2;
Broj promenljivih koje je potrebno zadati da bi se dobilo jednoznano odreeno reenje:
N
z
= N
p
N
n
= 4
13
Napomene:
- N
n
je jednak broju komponenti N
k
jer se moe napisati jedan ukupan bilans i (N
k
1)
nezavisnih komponentnih bilansa bilans jedne preostale komponente proistie iz injenice da
je suma udela svih komponenti za svaki tok ponaosob jednaka 1;
- Sa x je oznaen molski udeo benzena, u indeksu je naznaen tok na koji se dati molski udeo
benzena odnosi molski udeli toluena nisu navedeni jer se podrazumeva da je x
benzen
= 1 x
(iz istog razloga za smeu N
k
komponenti dovoljno bi bilo navesti N
k
1 molskih udela po
toku)
- U optem sluaju, da bi se odredio materijalni bilans rektifikacione kolone u kojoj se na
destilat i ostatak razdvaja napojna smea koju ini N
k
komponenti potrebno je ispisati N
k
nezavisnih bilansnih jednaina i unapred specificirati N
z
= 3N
k
N
k
= 2N
k
promenljivih.
Dakle, u konkretnom sluaju, da bi bilo mogue odrediti protoke D i B, potrebno je unapred znati jo
dve promenljive, x
D
i x
B
. Ove dve promenljive su posredno zadate preko koeficijenata frakcionog
razdvajanja:
- koeficijent frakcionog razdvajanja benzena u destilat, f
1
D
= 0,95;
- koeficijent frakcionog razdvajanja toluena u destilat, f
2
B
= 0,98;
Odreivanje sastava destilata i ostatka preko koeficijenata frakcionog razdvajanja bie najpre
razmotreno za opti sluaj razdvajanja viekomponentnih smea, koji e se potom svesti na konkretan
sluaj.
Molski udeo i-te komponente u destilatu moe se izraunati preko koeficijenata frakcionog
razdvajanja na sledei nain vai:
=
=
=
k
N
1 j
j , F
D
j
i , D i , F
D
i
D x f F
D x F x f
Sledi:
=
=
k
N
1 j
j , F
D
j
i , F
D
i
i , D
x f
x f
x
Slino tome, za molski udeo i-te komponente u ostatku se dobija:
=
=
k
N
1 j
j , F
B
j
i , F
B
i
i , B
x f
x f
x
Pri korienju gornjih jednaina treba imati u vidu da za svako j = 1,N
k
vai:
f
j
D
+ f
j
B
= 1
14
Na osnovu izvedenih jednaina mogu se u konkretnom sluaju izraunati molski udeli benzena u
desilatu i ostatku:
071 , 0
4 , 0 98 , 0 6 , 0 05 , 0
6 , 0 05 , 0
) x 1 ( f x ) f 1 (
x ) f 1 (
x
986 , 0
4 , 0 02 , 0 6 , 0 95 , 0
6 , 0 95 , 0
) x 1 )( f 1 ( x f
x f
x
F
B
2 F
D
1
F
D
1
B
F
B
2 F
D
1
F
D
1
D
=
+
=
+
=
=
+
=
+
=
Sada se mogu postaviti jednaina ukupnog materijalnog bilansa i jednaina materijalnog bilansa
benzena za naznaeni bilansni krug:
F = D + B
x
F
F = x
D
D + x
B
B
Sledi:
x
F
F = x
D
D + x
B
(F D)
54 , 144 250
071 , 0 986 , 0
071 , 0 6 , 0
F
x x
x x
D
B D
B F
=
= kmol/h
B = F D = 105,46 kmol/h
Provera ispravnosti materijalnog bilansa vri se preko bilansa one komponente koji nije iskorien u
izraunavanju bilansa posmatranog sistema:
(1 x
F
)F = 100 kmol/h
(1 x
D
)D + (1 x
B
)B = 0,014144,54 + 0,929105,46 = 100 kmo/h
Provera ispravnosti odreivanja sastava destilata i ostatka preko koeficijenata frakcionog razdvajanja:
x
D
D/(x
F
F) = 0,986144,54/(0,6250) = 0,95 = f
1
D
(1 x
B
)B/[(1 x
F
)F] = 0,929105,46/(0,4250) = 0,98 = f
2
B
15
Primer 10
Na sledeoj pojednostavljenoj emi toka prikazane su osnovne operacije procesa polimerizacije.
Odrediti masene protoke svih struja i prinos polimera iz sveeg monomera ako se proizvodi 10000
kg/h suvog polimera. Ostali podaci:
- koncentracija monomera u vodenoj suspenziji: 20 % mas;
- stepen reagovanja u reaktoru: 90 % monomera;
- potronja katalizatora: 1 kg/1000 kg monomera;
- potronja inhibitora polimerizacije: 0,5 kg/1000 kg neproreagovalog monomera;
- potronja vode za ispiranje filtera: 1 kg/1 kg polimera;
- efikasnost odvajanja polimera u filteru: 99 %;
- efikasnost izdvajanja monomera u koloni: 98 %;
- sadraj vlage na ulazu u sua: 5 % mas
- sadraj vlage u proizvodu: 0,5 % mas.
* * *
16
Oznake tokova:
Oznake komponenti:
1 monomer;
2 voda;
3 katalizator;
4 inhibitor polimerizacije;
5 polimer;
Konvencija:
- maseni protoci bie oznaeni sa m;
- identifikovanje toka i komponente na koji se dati maseni protok odnosi vrie se preko brojeva
u indeksu samo jedan broj u indeksu predstavlja ukupan maseni protok odgovarajueg toka;
dva broja u indeksu oznaavaju maseni protok komponente toka, pri emu se prvi broj odnosi
na tok, a drugi broj predstavlja komponentu;
Na osnovu usvojene konvencije i datih podataka vai:
- maseni protok suvog polimera: m
12,5
= 10000 kg/h
- koncentracija monomera u suspenziji: 20 % mas m
6
/(m
6
+m
2
) = 0,2
- stepen reagovanja u reaktoru: 90 % monomera m
7,5
/m
6
= 0,9;
- potronja katalizatora: 1 kg/1000 kg monomera m
3
/m
6
= 0,001;
- potronja inhibitora polimeriz.: 0,5 kg/1000 kg nepr. mon. m
4
/m
7,1
= 0,510
-3
;
- potronja vode za ispiranje filtera: 1 kg/1 kg polimera m
5
=m
8,5
;
- efikasnost odvajanja polimera u filteru: 99 % m
9,5
= 0,99m
8,5
- efikasnost izdvajanja monomera u koloni: 98 % m
11
= 0,98m
10,1
;
- sadraj vlage na ulazu u sua: 5 % mas m
9,2
= 0,05m
9
- sadraj vlage u proizvodu: 0,5 % mas m
12
,
2
= 0,005m
12
.
Broj podataka = 10.
17
Sve komponente nisu prisutne u svim tokovima, tako da se na samom poetku mogu iz daljeg
razmatranja eliminisati pojedinii komponentni protoci. U tu svrhu formirae se odgovarajua tabela
koja e obuhvatiti sve komponentne i ukupne protoke i unee se nule u one elije koje se odnose na
protoke komponenti koje nisu sadrane u odgovarajuem toku. Formirana tabela koristie se i u
daljem postupku kako bi se moglo utvrditi koliko je nepoznatih odreeno i koliko ih je preostalo
nepoznatih.
Dakle, pojedine tokove ine sledee komponente:
Tok Komponente Tok Komponente
1 1 8 1, 2, 3, 4, 5
2 2 9 2, 5
3 3 10 1, 2, 3, 4, 5
4 4 11 1
5 2 12 2, 5
6 1 13 1, 2, 3, 4, 5
7 1, 2, 3, 5 14 2
Sledi:
Tok
1 2 3 4 5 6 7 8 9 10 11 12 13 14
K
o
m
p
o
n
e
n
t
a
1 0 0 0 0 0 0 0
2 0 0 0 0 0
3 0 0 0 0 0 0 0 0 0
4 0 0 0 0 0 0 0 0 0 0
5 0 0 0 0 0 0 0 0
S
Na ovaj nain obezbeeno je jo 39 podataka. Ukupan broj podataka = 10 + 39 = 49. Ukupan broj
promenljivih jednak je proizvodu broja tokova i broja komponenti = 14x5 = 70. Broj nepozantih
vrednosti = 70 49 = 21. Dakle, da bi se odredile nepoznate vrednosti potrebno je postaviti jo 21
meusobno nezavisnu jednainu.
Bilans polimera
Protok suvog polimera:
m
12,5
= 10000 kg/h (preostalo je jo 9 neiskorienih podataka)
Pre izlaska iz postrojenja polimer prolazi kroz sua u kojem se uklanja samo vlaga. Prema tome,
protok polimera na ulazu u sua, jednak je protoku polimera na izlazu iz postrojenja:
m
9,5
= m
12,5
= 10000 kg/h (1. jednaina od 21)
18
Bilans polimera postavljen za filter:
m
8,5
= m
9,5
+ m
10,5
(2. jednaina)
Kako je efikasnost odvajanja polimera u filteru 99 %, odnosno m
9,5
= 0,99m
8,5
vai:
m
9,5
/0,99 = m
9,5
+ m
10,5
(preostalo je jo 8 podataka)
m
10,5
= m
9,5
(1/0,99 1) = 101 kg/h
m
8,5
= 10000 + 101 = 10101 kg/h
Polimer koji nije odvojen u filteru u potpunosti se izdvaja u na dnu kolone za izdvajanje monomera:
m
13,5
= m
10,5
= 101 kg/h (3. jednaina)
Protok polimera na ulazu u filter jednak je protoku polimera na izalzu iz reaktora:
m
7,5
= m
8,5
= 10101 kg/h (4. jednaina)
Budui da polimer nije prisutan u ostalim tokovima, njegovo bilansiranje je okonano, a dobijene
vrednosti se unose u tabelu:
Tok
1 2 3 4 5 6 7 8 9 10 11 12 13 14
K
o
m
p
o
n
e
n
t
a
1 0 0 0 0 0 0 0
2 0 0 0 0 0
3 0 0 0 0 0 0 0 0 0
4 0 0 0 0 0 0 0 0 0 0
5 0 0 0 0 0 0 10101 10101 10000 101 0 10000 101 0
S
Bilans vode
Obzirom da tok 12 ine samo polimer i vlaga, njegov ukupan protok moe se odrediti na osnovu
podatka da 0,5 % mas izlaznog toka ini vlaga, odnosno da 99,5 % mas toka 12 ini polimer. Sledi:
m
12
= m
12,2
/0,995 = 10000/0,995 = 10050 kg/h (5. jednaina)
m
12,2
= 0,005m
12
=0,00510050 = 50 kg/h (preostalo je jo 7 podataka)
(ili m
12,2
= m
12
m
12,5
= 10050 10000 = 50 kg/h)
Sadraj vlage na ulazu u sua iznosi 5 % mas, tako da tok 9, obzirom da su i u njemu prisutni samo
vlaga i polimer, ini 5 % mas vode i 95 % polimera. Sledi:
m
9
= m
9,5
/0,95 = 10000/0,95 = 10526 kg/h (6. jednaina)
m
9,2
= 0,05m
9
= 0,0510526 = 526 kg/h (preostalo je jo 6 podataka)
(ili m
9,2
= m
9
m
9,5
= 10526 10000 = 526 kg/h)
19
Bilans vode postavljen za sua:
m
14
= m
9,2
m
12,2
= 526 50 = 476 kg/h (7. jednaina)
Maseni protok vode za ispiranje jednak je protoku polimera na ulazu ufilter:
m
5
= m
8,5
= 10101 kg/h (preostalo je jo 5 podataka)
Za dalje bilansiranje vode potrebno je znati vrednost protoka vode na ulazu u reaktor, tok 2. Kako je
ovaj protok odreen preko koncentracije monomera u vodenoj susprenziji u reaktoru, potrebno je
prethodno odrediti protok monomera na ulazu u reaktor, tok 6. No, pre nego to se pree na
bilansiranje monomera, korisno je uneti u tabelu do sada odreene vrednosti:
Tok
1 2 3 4 5 6 7 8 9 10 11 12 13 14
K
o
m
p
o
n
e
n
t
a
1 0 0 0 0 0 0 0
2 0 0 0 10101 0 526 0 50 476
3 0 0 0 0 0 0 0 0 0
4 0 0 0 0 0 0 0 0 0 0
5 0 0 0 0 0 0 10101 10101 10000 101 0 10000 101 0
S
10101 10526 10050 476
Bilans monomera
Ulaz monomera u reaktor moe se odrediti preko stepena reagovanja:
m
6
= m
7,5
/0,9 = 10101/0,9 = 11223 kg/h (preostala su jo 4 podatka)
Protok neproreagovanog monomera na izlazu iz reaktora odreuje se takoe preko stepena
reagovanja:
m
7,1
= (1 0,9)m
6
= 0,111223 = 1122 kg/h (8. jednaina)
Na osnovu eme toka, kao i injenice da tok 9 na izlazu iz filtera ine samo polimer i vlaga, proizilazi
da su protoci neproreagovanog monomera u tokovima 7, 8 i 10 jednaki:
m
8,1
= m
7,1
= 1122 kg/h (9. jednaina)
m
10,1
= m
7,1
= 1122 kg/h (10. jednaina)
Protok recirkulacionog monomera ini 98 % monomera na ulazu u kolonu za njegovo izdvajanje:
m
11
= 0,98m
10,1
= 1100 kg/h (preostala su jo 3 podatka)
20
Protok neproreagovalog monomera koji se gubi sa otpadnim tokom dat je sa:
m
13,1
= (1 0,98)m
10,1
= 22 kg/h (11. jednaina)
Ulazni tok monomera u reaktor ine tok sveeg i recirkulacionog monomera, tako da je:
m
1
= m
6
m
11
= 10123 kg/h (12. jednaina)
Bilansiranje monomera je zavreno i moe se aurirati tabela sa podacima:
Tok
1 2 3 4 5 6 7 8 9 10 11 12 13 14
K
o
m
p
o
n
e
n
t
a
1 10123 0 0 0 0 11223 1122 1122 0 1122 1100 0 22 0
2 0 0 0 10101 0 526 0 50 476
3 0 0 0 0 0 0 0 0 0
4 0 0 0 0 0 0 0 0 0 0
5 0 0 0 0 0 0 10101 10101 10000 101 0 10000 101 0
S
10123 10101 11223 10526 1100 10050 476
Zavretak bilansiranja vode
Protok vode koja se dodaje u reaktor odreen je sadrajem monomera u vodenoj suspenziji, odnosno
protokom monomera na ulazu u reaktor:
m
6
/(m
6
+ m
2
) = 0,2
m
2
= (1 0,2)m
6
/0,2 = 411223 = 44892 kg/h (preostala su jo dva podatka)
Na osnovu eme toka moe se zakljuiti da je protok vode isti u tokovima 2, 7 i 8:
m
7,2
= m
2
= 44892 kg/h (13. jednaina)
m
8,2
= m
2
=
44892 kg/h (14. jednaina)
Bilans vode postavljen za filter glasi:
m
8,2
+ m
5
= m
9,2
+ m
10,2
(15. jednaina)
Odatle je:
m
10,2
= m
8,2
+ m
5
m
9,2
= 44892 +10101 526 = 54467 kg/h
21
Voda iz toka 10 raspodeljuje se potpuno u tok 13:
m
13,2
= 54467 kg/h (16. jednaina)
Bilansiranje vode je zavreno tabela sa podacima:
Tok
1 2 3 4 5 6 7 8 9 10 11 12 13 14
K
o
m
p
o
n
e
n
t
a
1 10123 0 0 0 0 11223 1122 1122 0 1122 1100 0 22 0
2 0 44892 0 0 10101 0 44892 44892 526 54467 0 50 54467 476
3 0 0 0 0 0 0 0 0 0
4 0 0 0 0 0 0 0 0 0 0
5 0 0 0 0 0 0 10101 10101 10000 101 0 10000 101 0
S
10123 44892 10101 11223 10526 1100 10050 476
Preostalo je jo da se odrede protoci katalizatora i inhibitora reakcije polimerizacije.
Bilans katalizatora
Potronja katalizatora odreena je protokom monomera na ulazu u reaktor:
m
3
= 0,001m
6
= 0,00111223 = 11 kg/h (preostao je jo 1 podatak)
Protok katalizatora jednak je isti u tokovima 3, 7, 8, 10 i 13:
m
7,3
= m
8,3
= m
10,3
= m
13,3
= 11 kg/h (17., 18., 19. jednaina)
Bilans inhibitora polimerizacije
Potronja inhibitora polimerizacije zadat je protokom neproreagovalog monomera na izlazu iz
reaktora:
m
4
= 0,510
-3
m
7,1
= 0,510
-3
1122 = 0,56 kg/h (iskorieni su svi podaci)
Protok inhibitora polimerizacje jednak je u tokovima 4, 8, 10 i 13:
m
8,4
= m
10,4
= m
13,4
= 0,56 kg/h (20. i 21. jednaina)
Poto su odreeni svi komponentni protoci mogu se odrediti ukupni protoci tokova 7, 8, 10 i 13
ukupan protok toka jednak je zbiru protoka svih komponenti koje ine dati tok. Dobija se:
Tok
1 2 3 4 5 6 7 8 9 10 11 12 13 14
K
o
m
p
o
n
e
n
t
a
1 10123 0 0 0 0 11223 1122 1122 0 1122 1100 0 22 0
2 0 44892 0 0 10101 0 44892 44892 526 54467 0 50 54467 476
3 0 0 11 0 0 0 11 11 0 11 0 0 11 0
4 0 0 0 0,56 0 0 0 0,56 0 0,56 0 0 0,56 0
5 0 0 0 0 0 0 10101 10101 10000 101 0 10000 101 0
S 10123 44892 11 0,56 10101 11223 56126 56126,56 10526 55701,56 1100 10050 54601,56 476
22
Provera dobijenih rezultata moe se izvriti postavljanjem bilansa za celo postrojenje:
= 65127,56 kg/h (tokovi 1, 2, 3, 4 i 5)
= 65127,56 kg/h (tokovi 12, 13 i 14)
Bilans postrojenja za polimerizaciju je korektan. Prinos polimera u odnosu na monomer iznosi:
= m
12,5
/m
1
= 0,988 = 98,8 %
Zbir svih ulaza
na postrojenje
Zbir svih izlaza
sa postrojenja
Prinos
polimera
23
Primer 11
Da bi se mogao izraunati protok vazduha kroz cevovod odlueno je da se u vazdunu struju dodaje
inertna komponenta iji je sadraj mogue lako i precizno odrediti i u malim koncentracijama. Izabran
je ugljen-dioksid. Koliki je protok vazduha ako je analizom uzorka uzetom posle mesta doziranja
ustanovljena koncentracija CO
2
od 0,45 % vol. Intenzitet doziranja CO
2
bio je 10 kg/h, a prirodna
koncentracija CO
2
u vazduhu iznosi 0,03 % vol.
* * *
Dati molski procenti, obzirom da se radi o gasnoj fazi, ekvivalentni su molskim protocima, stoga e
bilans CO
2
, kao referentne komponente, biti postavljen za molske protoke. Stoga je potrebno maseni
protok doziranog CO
2
preraunati u molski protok.
n
doz
= m
doz
/M
CO2
= 10/44 = 0,227 kmol/h
Bilansni krug:
Bilans CO
2
:
0,0045(n
vaz
+ 0,227) = 0,0003n
vaz
+ 0,227
Molski protok vazduha:
8 , 53 227 , 0
0003 , 0 0045 , 0
0045 , 0 1
n
vaz
=
= kmol/h
Maseni protok vazduha:
m
vaz
= n
vaz
M
vaz
= 53,829 = 1560 kg/h
24
Primer 12
U sledeoj tabeli prikazani su rezultati analize sastava suvog dimnog gasa pei:
Komponenta % vol
CO
2
10,792
O
2
2,105
N
2 87,103
Odrediti koeficijent vika vazduha ako je sastav loivog gasa:
Komponenta % vol
CH
4
95,86
C
2
H
6
0,67
C
3
H
8
1,00
C
4
H
10
1,83
CO
2 0,64
* * *
Koeficijent vika vazduha predstavlja odnos izmeu stvarne i teorijske potronje vazduha:
= L/L
min
Teorijska potronja vazduha L
min
predstavlja koliinu (masu, zapreminu) vazduha potrebnu za
sagorevanje gorivih komponenti u gorivu i odreena je stehiometrijskim jednainama sagorevanja. U
realnom radu pei potrebno je radi efikasnog i potpunog sagorevanja goriva obezbediti dovod vazduha
u loite pei vei od teorijske koliine. Koeficijent vika vazduha, s druge strane, ne sme biti ni preko
mere vei od 1 kako se ne bi bez potrebe energija troila na zagrevanje vazduha. Optimalne vrednosti
koeficijenta vika vazduha kreu se od 1,0 do 1,2 za gasovita goriva, od 1,15 do 1,20 za tena goriva i
od 1,2 do 1,7 za vrsta goriva (u zavisnosti od vrste vrstog goriva i konstrukcije loita).
Bie prikazana tri naina prorauna vrednosti koeficijenta vika vazduha. U prvom nainu odreivanja
koeficijenta vika vazduha bie postavljene jednaina ukupnog masenog bilansa i jedna jednaina
komponentnog bilansa, u drugom nainu postavie se dve komponentne bilansne jednaine, dok e u
treem i najjednosatvnijem sluaju koeficijent vika vazduha biti odreen samo preko sastava dimnih
gasova.
I
Stvarna potronja vazduha moe se odrediti preko ukupnog bilansa i bilansa referentne komponente.
Kao referantna komponenta izabran je azot. Pri izradi bilansa treba imati u vidu da je voda produkt
sagorevanja i da zbog kondenzacije nije obuhvaena analizom sastava dimnog gasa. Bilansne
jednaine bie postavljene u kg svedenim na kg loivog gasa (to znai da e se uzeti da je masa
loivog gasa m
G
= 1 kg), tako da e kao prvi korak u proraunu biti sprovedeno preraunavanje
molskih u masene udele. Pri proraunu uzeti da je sastav vazduha 21 % mol O
2
i 79 % mol N
2
.
25
Preraunavanje molskih (zapreminskih) u masene udele
Dimni gas:
Komponenta y M, g/mol yM g
CO
2
0,10792 44 4,7485 0,1593
O
2
0,02105 32 0,6736 0,0226
N
2 0,87103 28 24,3888 0,8181
S = 1,00000 29,8109 1,0000
Molekulska masa dimnog gasa:
M
D
= 29,8109 g/mol
Loivi gas:
Komponenta y M, g/mol yM g
CH
4
0,9586 16 15,3376 0,8855
C
2
H
6
0,0067 30 0,2010 0,0116
C
3
H
8
0,0100 44 0,4400 0,0254
C
4
H
10
0,0183 58 1,0614 0,0613
CO
2 0,0064 44 0,2816 0,0163
S = 1,0000 17,3216 1,0000
Molekulska masa loivog gasa:
M
G
= 17,3216 g/mol
Vazduh:
Komponenta y M, g/mol yM g
O
2
0,21 32 6,72 0,2330
N
2 0,79 28 22,12 0,7670
S = 1,00 28,84 1,0000
Molekulska masa vazduha:
M
VZ
= 28,84 g/mol
26
Teorijska potronja vazduha
Teorijska potronja vazduha bie najpre odreena za koliinu loivog gasa od 1 mol.
Reakcije sagorevanja komponenti loivog gasa glase:
CH
4
+ 2O
2
CO
2
+ 2H
2
O
C
2
H
6
+ 3,5O
2
2CO
2
+ 3H
2
O
C
3
H
8
+ 5O
2
3CO
2
+ 4H
2
O
C
4
H
10
+ 6,5O
2
4CO
2
+ 5H
2
O
Proraun teorijske potronje vazduha potrebnog za sagorevanje 1 mol loivog gasa:
Gorive
komponente
loivog gasa
Mol. udeo
komponente u
loivom gasu
Broj molova O
2
koji se troi po
molu
komponente
Broj molova O
2
koji se troi na
sagorevanje 1
mol LG
Broj molova vazduha
koji se troi na
sagorevanje 1 mol LG
1 2 3 = 1x2 4 = 3/0,21
CH
4
0,9586 2 1,9172 9,1295
C
2
H
6
0,0067 3,5 0,0235 0,1117
C
3
H
8
0,0100 5 0,0500 0,2381
C
4
H
10
0,0183 6,5 0,1190 0,5664
S = 2,1096 10,0457
Dakle, teorijska potronja vazduha u mol potrebna za sagorevanje 1 mol loivog gasa iznosi:
L
min,n
= 10,046 mol
Teorijska potronja vazduha u kg potrebna za sagorevanje 1 kg loivog gasa dobija se mnoenjem
gornje vrednosti kolinikom molekulskih masa vazduha i loivog gasa:
n min,
G
VZ
min
L
M
M
L = = 16,726 kg
Stvarna potronja vazduha
Pre postavljanja bilansnih jednaina potrebno je odrediti koliinu vode koja nastaje sagorevanjem
loivog gasa. Pri sagorevanju 1 mol loivog gasa, oslobaa se sledea koliina vode:
Gorive
komponente koje
sadre vodonik
Mol. udeo
komponente u
loivom gasu
Broj molova H
2
O
nastao sagorevanjem 1
mola komponente
Broj molova H
2
O
koji se formira
sagor. 1 mola LG
1 2 3 = 1x2
CH4 0,9586 2 1,9172
C2H6 0,0067 3 0,0201
C3H8 0,0100 4 0,0400
C4H10 0,0183 5 0,0915
S = 2,0688
27
Prema tome, produkcija vode u mol pri sagorevanju 1 mol loivog gasa iznosi:
n
V
= 2,0688 mol
Sledi:
V
G
V
V
n
M
M
m = = 2,1498 kg
gde je M
V
= 18 g/mol (molekulska masa vode).
U skladu sa sledeom slikom, postavljaju se jednaine ukupnog materijalnog bilansa i bilansa azota za
pe:
L + m
G
= m
D
+ m
V
0,767L + g
G
m
G
= g
D
m
D
Sledi:
0,767L + g
G
m
G
= g
D
(L + m
G
m
V
)
767 , 0 8181 , 0
1 8181 , 0 1498 , 2 8181 , 0
767 , 0 g
m ) g g ( m g
L
D
G G D V D
= = 18,408 kg
Koeficijent vika vazduha:
= L/L
min
= 18,408/16,726 = 1,10
Prema tome, u loite pei uvodi se 10 % vika vazduha.
II
Reenje se moe dobiti i na drugi nain, tako to e se masa dimnih gasova koja nastaje sagorevanjem
1 kg loivog gasa odrediti preko bilansa ugljenika, dok e se stvarna potronja vazduha izraunati uz
pomo bilansa azota. Na ovaj nain se izbegava stehiometrijsko odreivanje produkcije vode.
28
Bilansni krug za ugljenik:
Sledi:
G
D , C
G , C
D
m
g
g
m =
Maseni udeo ugljenika u dimnom gasu rauna se na nain prikazan u sledeoj tabeli:
Komponente koje
sadre C
Mas. udeo CO
2
u
dimnom gasu
Atomska
masa C
Broj atoma C u
molekulu
komponente
Masa C u
molekulu
komponente
Molekulska
masa
komponente
Maseni udeo
C u
komponenti
Maseni udeo
C u dimnom
gasu
1 2 3 4 =2x3 5 6 = 4/5 7 = 1x6
CO2 0,1593 12 1 12 44 0,2727 0,04344
S = 0,04344
g
C,D
= 0,04344
Slino tome, za loivi gas vai:
Komponente koje
sadre C
Mas. udeo CO2
u loivom gasu
Atomska
masa C
Broj atoma C u
molekulu
komponente
Masa C u
molekulu
komponente
Molekulska
masa
komponente
Maseni udeo
C u
komponenti
Maseni udeo
C u LG
1 2 3 4 =2x3 5 6 = 4/5 7 = 1x6
CH4 0,8855 12 1 12 16 0,7500 0,6641
C2H6 0,0116 12 2 24 30 0,8000 0,0093
C3H8 0,0254 12 3 36 44 0,8182 0,0208
C4H10 0,0613 12 4 48 58 0,8276 0,0507
CO2 0,0163 12 1 12 44 0,2727 0,0044
S = 0,7493
g
C,G
= 0,7493
Rauna se masa dimnog gasa nastala sagorevanjem 1 kg loivog gasa:
249 , 17
04344 , 0
7493 , 0
m
g
g
m
G
D , C
G , C
D
= = = kg
29
Bilansni krug za azot:
Vai:
398 , 18 249 , 17
767 , 0
8181 , 0
m
767 , 0
g
L
D
D
= = = kg
Konano:
= L/L
min
= 18,398/16,726 = 1,10
III
Na kraju, bie prikazana i trei, najjednostavniji nain prorauna koeficijenta vika vazduha zasnovan
samo na sastavu suvog dimnog gasa. Proraun e biti zasnovan na 100 mol dimnog gasa koga ine:
| |
| |
| | mol 103 , 87 N
mol 105 , 2 O
mol 792 , 10 CO
D 2
D 2
D 2
=
=
=
Stvarna potronja kiseonika:
| | | |
D 2 r 2
N
79
21
O =
Koliina kiseonika utroena na formiranje drugih jednjenja u reakcijama sagorevanja (pre svega
vode):
| | | | | | | |
D 2 D 2 r 2 x 2
O CO O O =
Teorijska potronja kiseonika:
| | | | | | | | | |
D 2 r 2 x 2 D 2 t 2
O O O CO O = + =
Koeficijent vika vazduha:
| |
| |
| |
| | | |
| |
| |
1
r 2
D 2
D 2 r 2
r 2
t 2
r 2
O
O
1
O O
O
O
O
)
`
= =
30
Eliminacijom | |
r 2
O iz gornje jednaine dobija se:
| |
| |
1
D 2
D 2
N
O
21
79
1
)
`
=
U konkretnom sluaju:
10 , 1
103 , 87
105 , 2
21
79
1
1
=
)
`
=
Ukoliko je sastav dimnih gasova dat u masenim procentima tada treba koristiti sledei izraz:
| |
| |
1
D 2
D 2
N
O
27
77
1
)
`
=
Iako se primenom ove metode zanemaruje eventualno prisustvo ugljen-dioksida i azota u loivom
gasu (inae, u veini sluajeva, prisustvo ove dve komponente u gorivu i jeste zanemarljivo malo),
primena ove metode je zahvalna zbog jednostavnosti merenjem sastava dimnih gasova moe se
vriti kontrola rada pei i po potrebi regulisati vrednost koeficijenta vika vazduha preko koliine
vazduha koja se uvodi u loite ili intervencijom na koliini goriva. Radi optimizacije rada pei na
dimnjake se postavljaju analizeri kiseonika koji kontinuiarano mere njegovu koncentraciju u dimnim
gasovima. Optimalan sadraj kiseonika u dimnim gasovima kree se okvirno izmeu 1,5 i 3 % vol.
31
Primer 13
Odrediti potrebnu koliinu vazduha u molovima po molu loivog gasa da bi se obezbedio viak od 20
% vazduha pri sagorevanju gasa koji ine 95 % mol CH
4
i 5 % mol C
2
H
6
. Izraunati i sastav suvih
produkata sagorevanja nastalih sagorevanjem 1 mol gasa.
* * *
Reakcije sagorevanja
CH
4
+ 2O
2
CO
2
+ 2H
2
O
C
2
H
6
+ 3,5O
2
2CO
2
+ 3H
2
O
Teorijska potronja vazduha
Gorive
komponente
loivog gasa
Mol. udeo
komponente u
loivom gasu
Broj molova O2
koji se troi po
molu komponente
Broj molova O2 koji
se troi na sagorevanje
1 mol LG
Broj molova vazduha
koji se troi na
sagorevanje 1 mol
LG
1 2 3 = 1x2 4 = 3/0,21
CH4 0,95 2 1,900 9,048
C2H6 0,05 3,5 0,175 0,833
S = 2,075 9,881
L
min
= 9,881 mol
Stvarna potronja vazduha
L = 1,2L
min
= 11,857 mol
Produkti sagorevanja
Ugljen-dioksid:
Komponente
loivog gasa
koje sadre C
Mol. udeo
komponente u
loivom gasu
Broj molova CO
2
koji nastaje
sagorevanjem 1
mol komponente
Broj molova CO2
koji nastaje
sagorevanjem 1
mol LG
1 2 3 = 1x2
CH4 0,95 1 0,95
C2H6 0,05 2 0,10
S = 1,05
n
CO2
= 1,05 mol
Kiseonik:
n
O2
= 0,21(L L
min
) = 0,21( 1)L
min
= 0,415 mol
Azot:
n
N2
= 0,79L = 9,367 mol
32
Voda:
Komponente
loivog gasa
koje sadre
vodonik
Mol. udeo
komponente u
loivom gasu
Broj molova H
2
O
koji nastaje
sagorevanjem 1
mol komponente
Broj molova CO2
koji nastaje
sagorevanjem 1
mol LG
1 2 3 = 1x2
CH4 0,95 2 1,90
C2H6 0,05 3 0,15
S = 2,05
n
H2O
= 2,05
Sastav suvog dimnog gasa:
Komponenta n, mol % mol
CO
2
1,050 9,69
O
2
0,415 3,83
N
2 9,367 86,48
S = 10,832 100,00
33
Primer 14
Na postrojenju za proizvodnju vinilhlorida pirolizom dihloretana smanjena je konverzija na 55 %
kako bi se minimiziralo deponovanje koksa na reaktorskim cevima. Odrediti maseni protok
dihloretana potreban da bi se proizvelo 5000 kg/h vinilhlorida.
* * *
Konverzija (stepen reagovanja) predstavlja udeo reaktanta koji je preao u produkte. U sluaju
reakcije dihloretana (DCE), konverzija je data sa:
X
DCE
= n
DCE,r
/n
DCE,o
= m
DCE,r
/m
DCE,o
gde su sa n i m oznaeni molski i maseni protok dihloretana, dok se r i o u indeksu odnose na protok
proreagovalog ulaznog vinilhlorida.
Reakcija pirolize dihloretana glasi:
C
2
H
4
Cl
2
C
2
H
3
Cl + HCl
Kao to se vidi broj molova, odnosno molski protok proreagovalog dihloretana jednak je broju
molova, odnosno molskom protoku vinilhlorida (VC) nastalog u reakciji:
n
DCE,r
= n
VC
Sledi:
m
DCE,r
/MDCE = m
VC
/M
VC
= = = 5000
50 , 62
96 , 98
m
M
M
m
VC
VC
DCE
r , DCE
7917 kg/h
Protok vinilhlorida na ulazu u reaktor:
m
DCE,o
= m
DCE,r
/X
DCE
= 7917/0,55 = 14394 kg/h
34
Primer 15
Dietiletar dobija se kao sporedni produkt pri proizvodnji etanola hidrolizom etilena. Odrediti
konverziju etilena, kao i reakcione prinose etanola i dietiletra iz etilena u molskim procentima.
Hemijske reakcije i molski sastavi sirovinskog i produktnog toka prikazani na sledeoj slici:
* * *
Oznake:
- n broj molova
- X stepen reagovanja
- Y reakcioni prinos
Oznake u indeksu:
- Tokovi
1 ulaz u reaktor;
2 izlaz iz reaktora;
- Komponente
1 etilen;
2 voda;
3 inertne komponente;
4 etenol;
5 dietiletar
Osnova prorauna 100 mol sirovinskog toka:
n
1
= 100 mol.
Sledi:
n
11
= 55 mol.
n
12
= 5 mol.
n
13
= 45 mol.
Vai:
n
13
= n
23
35
Sledi:
y
13
n
1
= y
23
n
2
n
2
= 70 , 94 100
28 , 5
5
n
y
y
1
23
13
= = mol
Broj molova etilena, etanola i dietiletra u izlaznom toku:
n
21
= y
21
n
2
= 0,522694,70 = 49,49 mol
n
24
= y
24
n
2
= 0,054994,70 = 5,199 mol
n
25
= y
25
n
2
= 0,001694,70 = 0,1515 mol
Stepen reagovanja etilena:
10 1002 , 0
55
49 , 49
1
n
n
1 X
11
21
1
= = = = %
Reakcioni prinosi daju raspodelu raspodelu proizvoda hemijske reakcije. Prinos nekog proizvoda
predstavalja udeo proreagovalog reaktanta koji je konvertovao u dati proizvod. U skladu sa ovom
definicijom i stehiometrijom (1 mol etanola dobija se iz 1 mola etilena; 1mol dietiletra dobija se iz 2
mol etanola) prinosi etanola i detiletra dati su sa:
36 , 94 9436 , 0
51 , 5
199 , 5
X n
n
n n
n
Y
1 11
24
21 11
24
4
= = = =
= % mol
5 , 5 0550 , 0
51 , 5
1515 , 0 2
X n
n 2
n n
n 2
Y
1 11
25
21 11
25
5
= =
= =
= % mol
Provera na osnovu EY
i
= 1 :
Y
4
+ Y
5
= 0,9455 + 0,0550 = 1
Raspodela proizvoda hemijske reakcije uslovljena je prirodom hemijskih reakcija i uslovima u kojima
se ona odvija (pritisak, temperatura, koncentracije reaktanata i proizvoda u reakcionoj smei).
Ostvarena raspodela proizvoda u mnogim sluajevima predstavlja kljuni procesni indikator.
Na primer, u procesu katalitikog raformiranja benzina normalan prinos reformata oktanskog broja 95
kree se izmeu 80 i 82 % mas. Smanjenje prinosa reformata praeno je porastom prinosa lakih
ugljovodonika koji se formiraju u reakcijama hidrokrekovanja i moe biti posledica loe raspodele
aktivnosti katalitikih centara koje u razliitoj meri promoviu odvijanje razliitih reakcija ili proste
injenice da je zbog dugotrajnog rada dolo do deponovanja koksa na katalizatoru tako da se eljeni
oktanski broj moe postii samo na viim reaktorskim temperaturama koje naroito pogoduju
reakcijama hidrokrekovanja (podizanje reaktorskih temperaturama limitirano je sa vie faktora
smanjenjem prinosa proizvoda, energetskim trokovima i termikim ogranienjima katalizatora i
opreme). Problem loe raspodele reava se u ovom sluaju uspostavlanjem ravnotee u aktivnosti
katalitikih centara ili regeneracijom katalizatora.
36
Primer 16
Dihloretan dobija se hlorovanjem etilena, pri emu se neproregovali etilen ne vraa na ulaz reaktora.
Izraunati ukupni i reakcioni prinos dihloretana ako je konverzija etilena 99 % (glavni sporedni
proizvod je trihloretan), a iz 100 mol etilena se dobija 94 mol dihloretana.
* * *
C
2
H
4
+ Cl
2
C
2
H
4
Cl
2
X = 99 %
Reaktor
n
C2H4
= 100 mol n
DCE
= 94 mol
Ukupan prinos nekog proizvoda, Y
tot
, dat je odnosom koliina datog proizvoda i odabranog reaktanta
na ulazu u postrojenje. Ukupan prinos obuhvata i fizike gubitke eljenog proizvoda (ovi gubici mogu
biti najraziitijeg karaktera, poevi od gubitaka zbog loeg zaptivanja postrojenja do gubitaka usled
nemogunosti da se izvri potpuna separacija komponenti smee na izlazu iz reaktora) i po tome se
razlikuje od stepena reagovanja.
Imajui u vidu stehiometriju reakcije hlorovanja etilena, na osnovu gornjih podataka se dobijaju
sledee vrednosti ukupnog prinosa i reakcionog prinosa:
00 , 94 94 , 0
n
n
Y
4 H 2 C
DCE
tot
= = = % mol
95 , 94 9495 , 0
99
94
X n
n
Y
4 H 2 C
DCE
= = = = % mol
37
Primer 17
Blok dijagram prikazan na sledeoj slici prikazuje glavne korake u procesu proizvodnje vinilhlorida
(VC) iz etilena (ET). Svaki blok na dijagram (A, B i C) predstavljaju reaktor i nekoliko drugih
procesnih ureaja. U blokovima su uneti prikazane odgovarajue hemijske reakcije i ukupni prinosi
proizvoda u odnosu na pojedine reaktante.
HCl dobijen pirolizom dihloretana (DCE) usmerava se u sekciju za oksihlorovanje etilena gde
predstavlja reaktant. Protoci etilena prema blokovima za hlorovanje i oksihlorovanje tako su podeeni
da je produkcija HCl uravnoteena sa potrebama procesa (HCl nije prisutan na ulazu u blok C).
Stepen reagovanja DCE u reaktoru za pirolizu iznosi svega 55 %, tako da se neizreagovali DCE nakon
separacije recirkulacionim tokom vraa na ulaz reaktora za pirolizu.
Koristei se podacima datim na blok dijagramu izraunati protoke etilena prema reaktorima u
blokovima A i B, protok dihloretana prema reaktoru u bloku C i ukupan prinos vinilhlorida iz etilena
za celo postrojenje. Protok vinilhlorida na izlazu iz postrojenja iznosi 12500 kg/h.
* * *
Poto su prinosi dati u molskim procentima, postavljae se jednaine molskog bilansa.
Molekulska masa vinilhlorida:
M
VC
= 62,5 kg/h
Molski protok vinilhlorida:
F
VC
= 12500/62,5 = 200 kmol/h
Protok dihloretana na ulazu u blok C (pre spajanja sa recirkulacionim tokom):
F
DCE
= F
VC
/0,99 = 202,02 kmol/h
Protok HCl na izlazu iz bloka C:
F
HCl
= 0,995F
DCE
= 201,01 kmol/h
38
Protok dihloretana prema bloku C predstavlja zbir protoka ove komponente iz blokova A i B:
F
DCE
= F
DCE,A
+ F
DCE,B
Protoci DCE na izlazima iz blokova A i B povezani su sa odgovarajuim protocima etilena preko
ukupnih prinosa za date blokove:
F
DCE,A
= 0,98F
ET,A
F
DCE,B
= 0,95F
ET,B
Sledi:
0,98F
ET,A
+ 0,95F
ET,B
= 202,02 kmol/h
Protok dihloretana na izlazu iz bloka B povezan je sa protokom HCl na ulazu u taj blok preko
odgovarajueg prinosa (obratiti panju na stehiometriju):
F
DCE,B
= 0,90F
HCl
/2 = 0,90201,01/2 = 90,45 kmol/h
Odatle je:
F
ET,B
= F
DCE,B
/ 0,95 = 95,21 kmol/h
Sledi:
F
ET,A
= (202,02 0,9595,21)/0,98 = 113,85 kmol/h
Ukupan protok etilana na ulazu na postrojenje:
F
ET,tot
= 113,85 + 95,21 = 209,06 kmol/h
Prinos vinilhlorida iz etilena za celo postrojenje:
Y
tot
= F
VC
/F
ET,tot
= 200/209,06 = 0,9567 = 95,67 % mol
39
Primer 18
Amonijak se sintetizuje iz azota i vodonika u kontaktnoj pei u prisustvu katalizatora prema sledeoj
hemijskoj reakciji:
N
2
+ 3H
2
2NH
3
Po izlasku iz reaktora amonijak se kondenzuje i razdvaja od neproreagovalog azota i vodonika koji se
recirkulacionim tokom vraaju u reaktor. Smea sveeg azota i vodonika koja uvodi sadri u sebi 0,2
% vol argona. Da bi se spreila prekomerna akumulacija argona u reakcionoj smei posredstvom
recirkulacionog gasa potrebno je vriti ienje gasa tako to e se jedan njegov deo u kontinuitetu
isputati van postrojenja. Odrediti protok gasa koji se isputa da bi koncentracija argona u
recirkulacionom gasu bila manja od 5,0 % vol.
* * *
Pojednostavljena ema procesa sinteze amonijaka sa naznaenim bilansnim krugom:
Kako nije zadat kapacitet postrojenja kao osnova za proraun uzee se da je F
o
= 100 mol, odnosno F
p
e biti odreen u molovima koji se mogu tretirati molski, odnosno zapreminski procenti protoka
sirovinske smee.
Bilans argona:
y
o
F
o
= y
p
F
p
Sledi:
4 100
05 , 0
002 , 0
F
y
y
F
o
p
o
p
= = = mol
40
Primer 19
Na izlasku iz postrojenja za obradu otpadnih voda instalirana je posuda sa meanjem kako bi se
predupredilo isputanje zagaene vode usled nepredvienog porasta koncentracije kontaminanata.
Normalna i maksimalno dozvoljena koncentracija acetona u tretiranoj vodi iznose redom 100 i 200
ppm mas. Zbog havarije na postrojenju dolo je do iznenadnog porasta koncentracije acetona u vodi
na 1000 ppm u trajanju od pola asa. Da li je za to vreme dolo do prekoraenja dozvoljene
koncentracije acetona na izlasku vode iz suda sa meanjem? Radni kapacitet posude sa meanjem je
500 m
3
dok protok vode iznosi 45000 m
3
/h.
* * *
ematski prikaz posmatranog sistema sa naznaenim bilansnim krugom:
M, g
m = 45 t/h
g1 = 1000 ppm mas
m = 45 tg/h
g
Masa vode u sudu:
M = V = 500000 kg = 500 t
Bilans acetona:
dt
dg
M gm m g
1
=
Razdvajanjem promenljivih i integracijom u granicama t = (0, t) i g = (g
o
, g) dobija se:
o 1
1
g g
g g
ln
m
M
t
=
Reenje gornje jednaine po g:
t
M
m
o 1 1
e ) g g ( g g
=
Zamena odgovarajuih vrednosti u dobijenu jednainu (umesto masenih udela mogu se uneti
odgovarajue koncentracije u ppm mas) daje:
140 e ) 100 1000 ( 1000 g
5 , 0
500
45
~ =
ppm mas.
Prema tome, dozvoljena koncentracija acetona u vodi nije bila prekoraena.
You might also like
- ToplinamojazbirkaDocument85 pagesToplinamojazbirkaMiro VucicNo ratings yet
- Fizikalna Kemija-Zbirka ZadatakaDocument88 pagesFizikalna Kemija-Zbirka ZadatakaIva YuiNo ratings yet
- Zadaci Za Vježbu Iz Kolegija Inženjerstvo2 - 18 - 01 - 2013Document38 pagesZadaci Za Vježbu Iz Kolegija Inženjerstvo2 - 18 - 01 - 2013Josip AtlagaNo ratings yet
- Fizikalna Kemija I. - ZBIRKA ZADATAKA PDFDocument88 pagesFizikalna Kemija I. - ZBIRKA ZADATAKA PDFBibo MovaNo ratings yet
- 1.4smjese Idealnih PlinovaDocument12 pages1.4smjese Idealnih PlinovaVildanaHalilovicNo ratings yet
- Rijeseni ZadaciDocument4 pagesRijeseni ZadaciŠetkić SemirNo ratings yet
- Završni RadDocument10 pagesZavršni RadIvan KorlevicNo ratings yet
- Riješeni Zadaci Iz Termodinamike 1Document86 pagesRiješeni Zadaci Iz Termodinamike 1rakablNo ratings yet
- Zadatak 2Document10 pagesZadatak 2almir_brčaninovićNo ratings yet
- 00 Primjeri Parni CiklusiDocument7 pages00 Primjeri Parni CiklusiKenan ZaimovićNo ratings yet
- Mašinski Fakultet SarajevoDocument9 pagesMašinski Fakultet SarajevoAmila TulićNo ratings yet
- Zbirka Zadataka Iz Fizicke Hemije-Farzet Bikic PDFDocument145 pagesZbirka Zadataka Iz Fizicke Hemije-Farzet Bikic PDFMArija RogicNo ratings yet
- Zadatak 1 HD UgljaDocument9 pagesZadatak 1 HD Ugljaalmir_brčaninovićNo ratings yet
- Uroš Lazic R33-18 Elaborat VentilacijaDocument19 pagesUroš Lazic R33-18 Elaborat VentilacijaIvan VukasinovicNo ratings yet
- 04 Iskoristenje Kemijskih Reakcija, Mjerodavni ReaktantDocument6 pages04 Iskoristenje Kemijskih Reakcija, Mjerodavni Reaktantivyy23No ratings yet
- RAVNOTEZA KEMIJSKIH REAKCIJA - Rjesenja - PDFDocument33 pagesRAVNOTEZA KEMIJSKIH REAKCIJA - Rjesenja - PDFBruno KovacicNo ratings yet
- Termodinamika - Zadaci IspitaDocument4 pagesTermodinamika - Zadaci IspitaKristijan100% (1)
- Emisije U ZrakDocument16 pagesEmisije U ZrakMirzaMuijNo ratings yet
- Energetski StrojeviDocument43 pagesEnergetski Strojevi1983_matija100% (1)
- Energetski Procesi - 30 - 03 - 2020 - PDFDocument9 pagesEnergetski Procesi - 30 - 03 - 2020 - PDFElvedin PuzicNo ratings yet
- Seminar 13 - Adsorpcija - Riješeni ZadaciDocument5 pagesSeminar 13 - Adsorpcija - Riješeni Zadacikrlekrle123No ratings yet
- Zbirka Zadataka Iz Analiticke KemijeDocument68 pagesZbirka Zadataka Iz Analiticke KemijesabinaNo ratings yet
- DPL Plin UkopljeniDocument8 pagesDPL Plin UkopljeniSandro PandurevicNo ratings yet
- Book - PFRI - Parne-TurbineDocument142 pagesBook - PFRI - Parne-Turbinegeneactg100% (1)
- Vježba 1 - Plinska Tehnika PDFDocument20 pagesVježba 1 - Plinska Tehnika PDFigorNo ratings yet
- Ravnoteza Kemijskih Reakcija - RjesenjaDocument33 pagesRavnoteza Kemijskih Reakcija - RjesenjaEna1992No ratings yet
- Ravnoteza Kemijskih Reakcija - RjesenjaDocument33 pagesRavnoteza Kemijskih Reakcija - Rjesenjaervin custovic100% (1)
- Auditorne 9Document19 pagesAuditorne 9Ivan VranićNo ratings yet
- Zbirka Zadataka Iz Analiticke Kemije PDFDocument68 pagesZbirka Zadataka Iz Analiticke Kemije PDFEmin Mešić100% (1)
- Kemija ZadatciDocument10 pagesKemija ZadatciIvan BukovacNo ratings yet
- Hidrostatika Zadaci Iz SkripteDocument50 pagesHidrostatika Zadaci Iz SkripteMilan P. Vasic100% (2)
- Te 7 VJ RJDocument10 pagesTe 7 VJ RJIsmarNo ratings yet
- ODredivanje Transportnih KoeficijenataDocument16 pagesODredivanje Transportnih Koeficijenatasime13No ratings yet
- ExergijaDocument5 pagesExergijaMiro VucicNo ratings yet
- Dinamika Procesa Odvajac KapljevineDocument20 pagesDinamika Procesa Odvajac KapljevineDarko MiškovićNo ratings yet
- Kotlovi I Peći It DijagramDocument12 pagesKotlovi I Peći It DijagramDamir Merima MuslicNo ratings yet
- Toplina ZadatciDocument5 pagesToplina ZadatciAna-MarijaNo ratings yet
- Te 13 VJ RJDocument9 pagesTe 13 VJ RJmarkokt22No ratings yet
- Fluidi-Rijeseni ZadaciDocument16 pagesFluidi-Rijeseni ZadaciNejra IkicNo ratings yet
- Opća Kemija (Sikirica) - Riješenja ZadatakaDocument340 pagesOpća Kemija (Sikirica) - Riješenja ZadatakaHrvoje Olić88% (17)
- 06 Vjezbe TEPDocument3 pages06 Vjezbe TEPSenid DelicNo ratings yet
- Generator PareDocument6 pagesGenerator PareAnonymous AEVQaU2giNo ratings yet
- 2 Pumpe PDFDocument9 pages2 Pumpe PDFBoban VelagaNo ratings yet
- Jonski Proizvod VodeDocument2 pagesJonski Proizvod VodeMile ZoricNo ratings yet
- Metanski BrojDocument1 pageMetanski BrojMile ZoricNo ratings yet
- Maseni U Molske I ObrnutoDocument8 pagesMaseni U Molske I ObrnutoMile ZoricNo ratings yet
- Popis Like I Krbave 1712Document426 pagesPopis Like I Krbave 1712miledplayer100% (8)
- Ciklonaut - Standardi Za Felne I GumeDocument3 pagesCiklonaut - Standardi Za Felne I GumeMile ZoricNo ratings yet