Professional Documents
Culture Documents
________ (12) _____ ___ ________ _______ __ ____ ____ _____ (1)
Uploaded by
Abderrahman NemerCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
________ (12) _____ ___ ________ _______ __ ____ ____ _____ (1)
Uploaded by
Abderrahman NemerCopyright:
Available Formats
www.youtube.
com/physicstubeTV شرح دروس مادة الفيزياء – بكالوريا -
الحلقة ( )12تمرين حول المتابعة الزمنية عن طريق قياس الحجم
نص التمرين:
ندخل قطعة كتلتها 𝑚 من معدن المنغنيزيوم 𝑔𝑀 في حوجلة ثم نضيف لها حمض كلور الهيدروجين ) (𝐻3 𝑂+ + 𝐶𝑙 −
حجمه 𝑙𝑚 𝑉 = 60وتركيزه 𝐶 = 5𝑚𝑜𝑙. 𝑙 −1فنالحظ انطالق غاز ثنائي الهيدروجين .
نقيس حجم الغاز المنطلق خالل فترات زمنية مختلفة فنحصل على جدول القياسات التالي:
)𝑛𝑖𝑚(𝑡 0 1 3 4 5 6 7 8 9
𝑙𝑚) 𝑉(𝐻2 0 317 705 779.5 881 916 952 987 987
[𝐻3 𝑂+ ]𝑚𝑜𝑙. 𝑙 −1
المطلوب :
– 01أعط رسم تخطيطي للتجربة السابقة.
– 02أكتب المعادلتين النصفيتين االلكترونيتين اذا كانت الثنائيتين الداخلتين في التفاعل هما:
) 𝟐𝑯(𝑯𝟑 𝑶+ ⁄ )𝒈𝑴(𝑴𝒈+𝟐 ⁄
– أكتب المعادلة االجمالية أكسدة – ارجاع.
– 03أنشئ جدوال لتقدم التفاعل.
– 04أكمل جدول القياسات.
+
– 05أ -مثل المنحنى )𝑡(𝑓 = ] 𝑂 [𝐻3
ب -واستنتج المتفاعل المحد.
- 06أحسب قيمة التقدم األعظمي.
- 07أحسب كتلة المنغنيزيوم 𝑚 المستعملة في التفاعل.
- 08أوجد زمن نصف التفاعل 𝑡1/2انطالقا من البيان.
- 09عيّن السرعة الحجمية للتفاعل عند اللحظتين :
𝑛𝑖𝑚 𝑡 = 3و 𝑛𝑖𝑚 𝑡 = 5ماذا تستنتج؟
- 10لو استعملنا معدن المنغنيزيوم على شكل مسحوق ،هل تتغير النتائج السابقة ؟ علّل.
المعطيات:
−1 −1
𝑙𝑜𝑚 𝑀(𝑀𝑔) = 24,3𝑔. 𝑙𝑜𝑚 𝑉𝑀 = 24𝑙.
𝑚𝑡𝑎 𝑃 = 1 ℃𝑇 = 20
www.facebook.com/touahria.abdelaziz من اعداد األستاذ :طواهرية عبد العزيز
www.youtube.com/physicstubeTV شرح دروس مادة الفيزياء – بكالوريا -
حل التمرين:
– 01رسم تخطيطي للتجربة السابقة:
– 02كتابة المعادلتين النصفيتين االلكترونيتين:
-المعادلة النصفية لألكسدة+2𝑒 − :
+2
)𝑠(𝑔𝑀 → )𝑞𝑎(𝑔𝑀
+ -المعادلة النصفية لالرجاع:
)𝑞𝑎(𝑂 2𝐻3 +2𝑒 − → )𝑞𝑎(𝐻2 )𝑙(𝑂 + 2𝐻2
المعادلة االجمالية أكسدة – ارجاع:
بجمع المعادلتين طرفا لطرف:
𝑴𝒈(𝒔) + 𝟐𝑯𝟑 𝑶+ 𝟐+
)𝒍(𝑶 𝟐𝑯𝟐 (𝒂𝒒) → 𝑴𝒈(𝒂𝒒) + 𝑯𝟐(𝒂𝒒) +
– 03جدول التقدم للتفاعل:
+ +2
معادلة التفاعل )𝑞𝑎(𝑂 𝑀𝑔(𝑠) + 2𝐻3 )𝑞𝑎(𝑔𝑀 = )𝑙(𝑂 + 𝐻2(g) + 2𝐻2
تقدم التفاعل حالة التفاعل كميات األفراد الكيميائية بوحدة mol
x(t) = 0الحالة االبتدائية 𝑛0 𝑛1 0 0 بوفرة
𝑡𝑋 = ) x(tالحالة االنتقالية 𝑡𝑥 𝑛0 - 𝑡𝑥𝑛1 - 2 𝑡𝑥 𝑡𝑥 بوفرة
𝑥𝑎𝑚𝑋 = ) x(tالحالة النهائية 𝑥𝑎𝑚𝑥 𝑛0 - 𝑥𝑎𝑚𝑥𝑛1 - 2 𝑥𝑎𝑚𝑥 𝑥𝑎𝑚𝑥 بوفرة
– 04اكمال جدول القياسات:
لدينا من جدول التقدم في الحالة االنتقالية:
𝒕𝑿𝟐 𝒏𝟏 - 𝒕𝑿𝟐 𝑪. 𝑽 - 𝒕𝑿𝟐
𝒕𝑿𝟐 𝑛(𝐻3 𝑂+ ) = 𝒏𝟏 - = ] [𝐻3 𝑂+ = ] [𝐻3 𝑂+ [𝐻3 𝑂+ ] = 𝐶 −
𝑉 𝑉 𝑉
𝟐𝑯𝑽 𝟐𝑯𝑽𝟐
𝒕𝑿 = ) 𝑛(𝐻2 = 𝒕𝑿 = ) 𝑛(𝐻2 [𝐻3 𝑂+ ] = 𝐶 −
𝑴𝑽 𝑀𝑉 𝑉.
𝟐𝑯𝑽𝟐 )𝟓𝟎𝟕 𝟐(𝟎,
[𝐻3 𝑂+ ] = 5 − [𝐻3 𝑂+ ] = 5 − 𝟏[𝑯𝟑 𝑶+ ] = 𝟒, 𝟎𝟐𝒎𝒐𝒍. 𝒍−
)(0,06). (24 )(0,06). (24
www.facebook.com/touahria.abdelaziz من اعداد األستاذ :طواهرية عبد العزيز
www.youtube.com/physicstubeTV شرح دروس مادة الفيزياء – بكالوريا -
)𝒏𝒊𝒎(𝒕 0 1 3 4 5 6 7 8 9
𝑙𝑚) 𝑉(𝐻2 0 317 705 779.5 881 916 952 987 987
[𝐻3 𝑂+ ]𝑚𝑜𝑙. 𝑙 −1 5 4,56 4,02 3,92 3,77 3,73 3,66 6,63 3,63
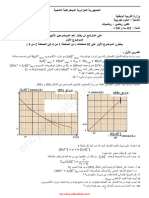
– 05أ -تمثيل المنحنى )𝒕(𝒇 = ] [𝑯𝟑 𝑶+
[𝐻3 𝑂+ ]𝑚𝑜𝑙. 𝑙 −1
5.5
5
4.5
4
3.5
3
2.5
2
1.5
1
0.5
0
0 1 2 3 4 5 6 7 8 9 10
)𝑛𝑖𝑚(𝑡
ب -استنتاج المتفاعل المحد:
+
أن شوارد الهيدرونيوم 𝑂 𝐻3ال تختفي كليّا هند بلوغ التفاعل نهايته وبالتالي المتفاعل المحد هو من المنحنى نستنتج ّ
المنغنيزيوم 𝑔𝑀.
- 06حساب قيمة التقدم األعظمي:
من جدول التقدم في الحالة النهائية:
𝑥𝑎𝑚𝑋𝑛(𝐻3 𝑂+ )𝑓 = 𝐶. 𝑉 - 2 𝑥𝑎𝑚𝑋𝐶. 𝑉 - 2
𝑥𝑎𝑚𝑋𝑛(𝐻3 𝑂+ )𝑓 = 𝑛1 - 2 = 𝑓] [𝐻3 𝑂+
]) +
𝑉
𝑋2 𝑥𝑎𝑚 ൫𝐶- 𝐻([ 3 𝑂 𝑓 ൯. 𝑉
[𝐻3 𝑂+ ]𝑓 = 𝐶 − = 𝑥𝑎𝑚𝑋
𝑉 2
)(5-3,63). (0,06
= 𝑥𝑎𝑚𝑋 𝑙𝑜𝑚𝑋𝑚𝑎𝑥 = 0,0411
2
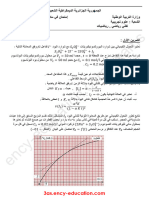
- 08ايجاد زمن نصف التفاعل 𝟐 𝒕𝟏/انطالقا من البيان:
𝒕𝑿𝟐 𝟐𝟐𝑿𝒕𝟏/
[𝐻3 𝑂+ ] = 𝐶 − [𝐻3 𝑂+ ]𝑡1/2 = 𝐶 −
𝑉 𝑉 𝒙𝒂𝒎𝑿
= 𝑥𝑡1/2
𝒙𝒂𝒎𝑿𝟐 𝒙𝒂𝒎𝑿 2
[𝐻3 𝑂+ ]𝑡1/2 = 𝐶 − [𝐻3 𝑂+ ]𝑡1/2 = 𝐶 −
𝑉2 𝑉
𝟏𝟏𝟒𝟎 𝟎.
[𝐻3 𝑂+ ]𝑡1/2 = 5 − [𝐻3 𝑂+ ]𝑡1/2 = 4,315𝑚𝑜𝑙. 𝑙 −1
0,06
www.facebook.com/touahria.abdelaziz من اعداد األستاذ :طواهرية عبد العزيز
www.youtube.com/physicstubeTV شرح دروس مادة الفيزياء – بكالوريا -
باالسقاط على محور األزمنة:
[𝐻3 𝑂+ ]𝑚𝑜𝑙. 𝑙 −1
5.5
5
4.5
4
3.5
3
2.5 𝑛𝑖𝑚𝑡1/2 = 1,9
2
1.5
1
0.5
0
0 1 2 3 4 5 6 7 8 9 10
)𝑛𝑖𝑚(𝑡
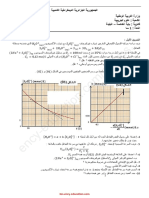
- 09تعيين السرعة الحجمية للتفاعل عند اللحظتين :
𝑥𝑑 1 𝒏𝒊𝒎𝟑 = 𝒕 و 𝒏𝒊𝒎𝟓 = 𝒕 .
𝑙𝑜𝑣𝑣 =
𝑡𝑑 𝑉
𝒕𝑿𝟐 𝒏𝟏 - 𝒕𝑿𝟐 𝑪. 𝑽 - 𝒕𝑿𝟐
𝒕𝑿𝟐 𝑛(𝐻3 𝑂+ ) = 𝒏𝟏 - = ] [𝐻3 𝑂+ = ] [𝐻3 𝑂+ [𝐻3 𝑂+ ] = 𝐶 −
𝑉 𝑉 𝑉
𝒕𝑿𝟐 𝑉 (𝐶 − [𝐻3 𝑂+ ]).
= ] 𝐶 − [𝐻3 𝑂+ 𝒕𝑿𝟐 = 𝑉 (𝐶 − [𝐻3 𝑂+ ]).
𝑉 = 𝒕𝑿
2
𝑉 (𝐶 − [𝐻3 𝑂+ ]).
𝑑1 2 )] 𝑑(𝐶 − [𝐻3 𝑂+ ] 𝑑𝐶 𝑑[𝐻3 𝑂+
𝑙𝑜𝑣𝑣 = = 𝑙𝑜𝑣𝑣 = 𝑙𝑜𝑣𝑣 −
𝑉 𝑡𝑑 𝑡𝑑2 𝑡𝑑2 𝑡𝑑2
] 1 𝑑[𝐻3 𝑂+
𝑙𝑜𝑣𝑣 =−
2 𝑡𝑑
عند 𝒏𝒊𝒎𝟑 = 𝒕 :
] 1 𝑑[𝐻3 𝑂+ ] 1 ∆[𝐻3 𝑂+ 1 4,6 − 3,4
𝑙𝑜𝑣𝑣 =− 𝑙𝑜𝑣𝑣 =− 𝑣𝑣𝑜𝑙 = − = 0,1𝑚𝑜𝑙. 𝑙 −1 . 𝑚𝑖𝑛−1
2 𝑡𝑑 𝑡∆ 2 2 0−6
عند 𝒏𝒊𝒎𝟓 = 𝒕 :
1 4 − 3,5
𝑣𝑣𝑜𝑙 = − = 0,03𝑚𝑜𝑙. 𝑙 −1 . 𝑚𝑖𝑛−1
2 0−8
www.facebook.com/touahria.abdelaziz من اعداد األستاذ :طواهرية عبد العزيز
www.youtube.com/physicstubeTV شرح دروس مادة الفيزياء – بكالوريا -
[𝐻3 𝑂+ ]𝑚𝑜𝑙. 𝑙 −1
5.5
5
4.5
4
3.5
3
2.5
2
1.5
1
0.5
0
0 1 2 3 4 5 6 7 8 9 10
)𝑛𝑖𝑚(𝑡
أن السرعة الحجمية للتفاعل تتناقص مع مرور الزمن وهذا بسبب تناقص تراكيز المتفاعالت نستنتج ّ
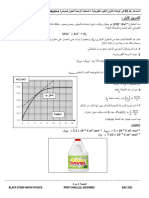
- 10لو استعملنا معدن المنغنيزيوم على شكل مسحوق :
نعم تتغيّر النتائج السابقة حيث تكون سرعة التفاعل أكبر عند استعمال مسحوق المنغنيزيوم.
يعتبرعامل سطح التالمس عامل حركي مؤثر في سرعة التفاعل فكلما زادت مساحة سطح التالمس زادت سرعة التفاعل
والعكس صحيح.
[𝐻3 𝑂+ ]𝑚𝑜𝑙. 𝑙 −1
5.5
5
4.5
4
3.5
3
2.5
2
1.5
1 في حالة مسحوق المنغنيزيم
0.5
0
0 1 2 3 4 5 6 7 8 9 10
)𝑛𝑖𝑚(𝑡
هام جدا :لمشاهدة شرح التمرين على اليوتيوب اتّبع الرابط التالي:
https://youtu.be/e2i2H4tusqY
www.facebook.com/touahria.abdelaziz من اعداد األستاذ :طواهرية عبد العزيز
You might also like
- Alfiziaa Oalkimiaa Alom Fiziaiia 2016 Aldora Alistdrakia Altshih 2Document10 pagesAlfiziaa Oalkimiaa Alom Fiziaiia 2016 Aldora Alistdrakia Altshih 2lydiasf5No ratings yet
- UntitledDocument7 pagesUntitledVidéo StoryNo ratings yet
- - - - - - - - - الحلقة (10) تمرين حول المتابعة الزمنية عن طريق قياس الضغط PDFDocument5 pages- - - - - - - - الحلقة (10) تمرين حول المتابعة الزمنية عن طريق قياس الضغط PDFamina derkaouiNo ratings yet
- - - - - - - - - الحلقة (10) تمرين حول المتابعة الزمنية عن طريق قياس الضغط PDFDocument5 pages- - - - - - - - الحلقة (10) تمرين حول المتابعة الزمنية عن طريق قياس الضغط PDFAbdou100% (1)
- الوحدة 01 سلسلة المتابعة الزمنية عن طريق قياس الحجمDocument2 pagesالوحدة 01 سلسلة المتابعة الزمنية عن طريق قياس الحجمZizo Dark100% (2)
- Physics 3mtm22 1trim d4Document4 pagesPhysics 3mtm22 1trim d4Radovane PhysiqyeNo ratings yet
- Physics 3se22 1trim d1Document4 pagesPhysics 3se22 1trim d1souissi souissiNo ratings yet
- 44alfiziaa Oalkimiaa Alom Fiziaiia 2018 Aldora Alistdrakia AltshihDocument10 pages44alfiziaa Oalkimiaa Alom Fiziaiia 2018 Aldora Alistdrakia AltshihYoussef YoussefNo ratings yet
- 42alfiziaa Oalkimiaa Alom Fiziaiia 2018 Aldora Alaadia AltshihDocument6 pages42alfiziaa Oalkimiaa Alom Fiziaiia 2018 Aldora Alaadia AltshihYoussef YoussefNo ratings yet
- Corppcr 18Document10 pagesCorppcr 18wadiaaboulqassimNo ratings yet
- سلسلة تمارين 2Document6 pagesسلسلة تمارين 2lisaNo ratings yet
- سلسلة تمارينDocument6 pagesسلسلة تمارينMalak ElaichouchiNo ratings yet
- فرض الثالثة نهائي علميDocument1 pageفرض الثالثة نهائي علميnacima.gdppNo ratings yet
- Ficher 23Document3 pagesFicher 23DEBLOFNo ratings yet
- !!Document4 pages!!bouthinaaanrNo ratings yet
- 30alfiziaa Oalkimiaa Alom Fiziaiia 2015 Aldora Alaadia Altshih 1Document9 pages30alfiziaa Oalkimiaa Alom Fiziaiia 2015 Aldora Alaadia Altshih 1Youssef YoussefNo ratings yet
- الفصل الرابعDocument15 pagesالفصل الرابعurrjrjjdjdNo ratings yet
- - - - - الحلقة (8) تمرين حول المتابعة الزمنية عن طريق المعايرة اللونيةDocument6 pages- - - - الحلقة (8) تمرين حول المتابعة الزمنية عن طريق المعايرة اللونيةAbdou0% (2)
- الوحدة 01 سلسلة 02 السنة ثالثةDocument1 pageالوحدة 01 سلسلة 02 السنة ثالثةÊš Pőîř100% (1)
- الحساب الحرفي والمعادلات والمتراجحات من الدرجة الأولى بمجهول واحد واحدDocument2 pagesالحساب الحرفي والمعادلات والمتراجحات من الدرجة الأولى بمجهول واحد واحدReda HadjNo ratings yet
- Physics 3se22 1trim5Document2 pagesPhysics 3se22 1trim5houhouNo ratings yet
- الحساب الحرفي والمعادلات والمتراجحات من الدرجة الأولى بمجهول واحد واحدDocument2 pagesالحساب الحرفي والمعادلات والمتراجحات من الدرجة الأولى بمجهول واحد واحدReda HadjNo ratings yet
- حل تمارين الناقلية. - استعد باكpdfDocument23 pagesحل تمارين الناقلية. - استعد باكpdfSe LmaNo ratings yet
- تمارين مع التصحيح لدرس المعادلات والمتراجحات من الإمتحانات الجهوية لجهة الشمالDocument5 pagesتمارين مع التصحيح لدرس المعادلات والمتراجحات من الإمتحانات الجهوية لجهة الشمالsd.habbadiNo ratings yet
- Ttba Thol Kimiaii Tshih Slsla Altmarin 1 3Document8 pagesTtba Thol Kimiaii Tshih Slsla Altmarin 1 3Amine AlaoUii AlaouiNo ratings yet
- Physics 3se20 1trim5Document3 pagesPhysics 3se20 1trim5louaiboualleg570No ratings yet
- درس المتابعة الزمنية عن طريق المعايرة اللونيةDocument3 pagesدرس المتابعة الزمنية عن طريق المعايرة اللونيةRedouane Reda75% (4)
- الحلقة (7) درس المتابعة الزمنية عن طريق المعايرة اللونية PDFDocument3 pagesالحلقة (7) درس المتابعة الزمنية عن طريق المعايرة اللونية PDFu w uNo ratings yet
- Rapport TP1 Physique MateriauxDocument3 pagesRapport TP1 Physique MateriauxMaroua MerNo ratings yet
- PhysicsDocument2 pagesPhysicsyacine yacineNo ratings yet
- حل السلسلة الإضافية المتابعة الزمنية عن طريق قياس الناقليةDocument6 pagesحل السلسلة الإضافية المتابعة الزمنية عن طريق قياس الناقليةhamoudanouasria178No ratings yet
- تصحيح العمل المنزليDocument10 pagesتصحيح العمل المنزليxdmaroccanmcNo ratings yet
- ملخص الدارة RLDocument2 pagesملخص الدارة RLKenza HmrNo ratings yet
- Alfrdh 1 Nmothj 1 Alriadhiat Aola Bak Alom Tjribia Aldora Althania 2Document1 pageAlfrdh 1 Nmothj 1 Alriadhiat Aola Bak Alom Tjribia Aldora Althania 2Kira FreudNo ratings yet
- Dzexams 2as Mathematiques 472090Document7 pagesDzexams 2as Mathematiques 472090salim maouchiNo ratings yet
- Corppcr 17Document11 pagesCorppcr 17اوىةNo ratings yet
- دوال اسية - - - 231130 - 120200Document81 pagesدوال اسية - - - 231130 - 120200molgarrathgamerNo ratings yet
- مسائل شاملة حول الدوال الأسيةDocument81 pagesمسائل شاملة حول الدوال الأسيةabdobazor000No ratings yet
- سلسلة تمارين1 في الأكسدة ارجاع وتقدم التفاعل بكالورياDocument1 pageسلسلة تمارين1 في الأكسدة ارجاع وتقدم التفاعل بكالورياKhalid100% (1)
- الوحدة 01 سلسلة 01 السنة ثالثةDocument2 pagesالوحدة 01 سلسلة 01 السنة ثالثةÊš PőîřNo ratings yet
- الاهتزاز الحر المخمد001Document11 pagesالاهتزاز الحر المخمد001Hfdfg GfhhhNo ratings yet
- Examens Nationaux 2bac Science Mathematiques PC 2015 NormaleDocument17 pagesExamens Nationaux 2bac Science Mathematiques PC 2015 NormaleFatima Larhmicذڤ1قhNo ratings yet
- مسائل لدوال اسية ولغاريتميةDocument81 pagesمسائل لدوال اسية ولغاريتميةAnonymous peMJV0No ratings yet
- Dzexams Docs 3as 907589Document82 pagesDzexams Docs 3as 907589Khalil MelaouhNo ratings yet
- مسائل لدوال اسية ولغاريتميةDocument81 pagesمسائل لدوال اسية ولغاريتميةAnonymous peMJV0No ratings yet
- سلسلة تمارين متعلقة بالمكتسبات القبليةDocument2 pagesسلسلة تمارين متعلقة بالمكتسبات القبليةBOUCHEFFA HalimNo ratings yet
- السلسلة رقم 02 في الوحدة الأولىDocument4 pagesالسلسلة رقم 02 في الوحدة الأولىzineeddine0750No ratings yet
- حقيبة الأستاذ قزوري في الفيزياء بكالوريا 2020Document91 pagesحقيبة الأستاذ قزوري في الفيزياء بكالوريا 2020طارق أبومعاوية الجزائري احتياطيةNo ratings yet
- الوحدة 01 سلسلة تمارين حصص zoomDocument4 pagesالوحدة 01 سلسلة تمارين حصص zoomferiel taibiNo ratings yet
- ملخص المكتسبات القبلية للسنة الثالثة ثانويDocument4 pagesملخص المكتسبات القبلية للسنة الثالثة ثانويTrainerYoucefDjouadjNo ratings yet
- Dzexams 4am Mathematiques 344531Document3 pagesDzexams 4am Mathematiques 344531bennacer.mansourNo ratings yet
- Altholat Alkimiaiia Almqrona Baltfaalat HMDH Qaada Tshih Slsla Altmarin 3 2Document6 pagesAltholat Alkimiaiia Almqrona Baltfaalat HMDH Qaada Tshih Slsla Altmarin 3 2muka fihNo ratings yet
- امتحان امثلة 2021Document2 pagesامتحان امثلة 2021chahd cherfiNo ratings yet
- العلاقة بين الأفراد الكيميائيةDocument3 pagesالعلاقة بين الأفراد الكيميائيةlynamellah415No ratings yet
- Physics 3se22 1trim2Document2 pagesPhysics 3se22 1trim2yacine yacineNo ratings yet
- Bac Physics 2016 Se 2Document8 pagesBac Physics 2016 Se 2abdelhak AouadiNo ratings yet