Professional Documents
Culture Documents
عمل تطبيقي3 فيزياء - كيمياء حركية
Uploaded by
benyamina imaneOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
عمل تطبيقي3 فيزياء - كيمياء حركية
Uploaded by
benyamina imaneCopyright:
Available Formats
الكيمياء الحركية
و
المدرسة العليا لألساتذة
الكيمياء الكهربائية
2024.2023 السنة الثانية في العلوم الفيزيائية
عمل تطبيقي " 2دراسة حركية لمعادلة كيميائية "
الهدف:
تعيين قيمة درجة التفاعل لمعادلة تفاعل برمنغنات البوتاسيوم مع االيتانول بالنسبة لشوارد البرمنغنات (تتبع تركيز
شوارد البرمنغنات بالمعايرة الحجمية).
مبدأ المعايرة:
ُتأكِس د شوارد البرمنغنات -MnO4شوارد اليود -Iمنتجة ثنائي اليود ، I2نعاير هذا األخير بشوارد ثيوسولفات -S2O32استعانة
بالنشاء الذي يعطي لون أزرق بنفسجي بتفاعله مع ثنائي اليود.
طريقة العمل:
نحضر مزيج التفاعل و ذلك باخذ 10mLمن محلول برمنغنات البوتاسيوم ( )mol. L-1 0,02و 25mLمن محلول -1
حمض الكبريت (( 1mol. L-1ثم نمأل الحوجلة ( )250mLبالماء المقطر الى خط العيار؛
نحضر محلول تيوسولفات الصوديوم Na2S2O3ذو تركيز 2mol. L-1-10. 2,5في حوجلة سعتها 250mLثم نمأل -2
به السحاحة؛
-1
نحضر محلول يوديد البوتاسيوم KIتركيزه 10g.Lلنأخذ منه في كل زمن tحجم 50mLللمعايرة؛ -3
نضع مزيح التفاعل في دورق فوق مخالط كهربائيى ونضيف له 5mLمن االيتانول و نشغل الكرونومتر؛ -4
عند الزمن tنأخذ 10mLمن مزيج التفاعل و نضيفه الى الدورق الذي يحتوي على محلول KIفيصبح لون -5
المحلول أصفر برتقالي؛
نبدأ المعايرة و ذلك بسكب محتوى السحاحة في الدورق حتى يصبح لون المحلول أصفر فاتح نغلق السحاحة و -6
نضيف قليل من النشاء فيتحول لون المحلول الى لون أزرق بنفسجي؛
نكمل المعايرة حتى يختفي اللون ،نأخذ الحجم المسكوب ثم نفرغ الدورق و نعيد نفس التجربة لألزمنة الباقية. -7
)t (min )Na2S2O3 (mL [)mol.L-1( ]-MnO4
5
10
15
20
30
45
60
90
اكتب مختلف معادالت التفاعل؛ -1
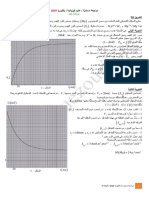
ارسم المنحنيات التالية: -2
) [MnO4-]=f(t
) Ln [MnO4-]=f(t
) 1 / [MnO4-]=f(t
حدد قيمة درجة التفاعل؛ -3
لماذا اضفنا حمض الكبريت لمحلول برمنغنات البوتاسيوم قبل التفاعل. -4
Page 1 of 1
You might also like
- عمل تطبيقي1 فيزياء - كيمياء حركيةDocument1 pageعمل تطبيقي1 فيزياء - كيمياء حركيةbenyamina imaneNo ratings yet
- 5Document4 pages5e.maskarNo ratings yet
- Serie2as - U7 - Oxred - 2023Document3 pagesSerie2as - U7 - Oxred - 2023abdenouraitchikh27No ratings yet
- سلسلة الأكسدة والإرجاع مع الحلول المفصلة - الأستاذ كريم سني 2022Document7 pagesسلسلة الأكسدة والإرجاع مع الحلول المفصلة - الأستاذ كريم سني 2022widad doudiNo ratings yet
- موضوع في الكيمياءDocument1 pageموضوع في الكيمياءSheikh Al-shoteriNo ratings yet
- Compo216PremM BoussetouaDocument2 pagesCompo216PremM BoussetouaMira Bkh0% (1)
- Tamarind As - U7 - Oxred - 2023Document3 pagesTamarind As - U7 - Oxred - 2023Ma RyNo ratings yet
- عمل تطبيقي3 فيزياءDocument2 pagesعمل تطبيقي3 فيزياءbenyamina imaneNo ratings yet
- تمارينات المتابعة الزمنية لتحول كيميائي للأستاذ التيجاني دهام PDFDocument6 pagesتمارينات المتابعة الزمنية لتحول كيميائي للأستاذ التيجاني دهام PDFAmine ChettafNo ratings yet
- العمل المخبري رقم 17- تحديد كميّة المادة بواسطة المعايرة اللونية (أكسدة - ارجاع) - بطاقة التلميذDocument2 pagesالعمل المخبري رقم 17- تحديد كميّة المادة بواسطة المعايرة اللونية (أكسدة - ارجاع) - بطاقة التلميذMohamed Hadj100% (1)
- 1 6Document5 pages1 6azizNo ratings yet
- المعايرة المباشرة-تمارينDocument1 pageالمعايرة المباشرة-تمارينNoureddine Elkouay38% (8)
- 3Document7 pages3e.maskarNo ratings yet
- اسئلة الكيمياء - ثالث متوسطDocument12 pagesاسئلة الكيمياء - ثالث متوسطسوق الكهرباء في عگد النصارىNo ratings yet
- RevCnt1 19rDocument2 pagesRevCnt1 19rMari AmNo ratings yet
- الوحدة 01 السلسلة 01Document3 pagesالوحدة 01 السلسلة 01Manil FélixNo ratings yet
- تسحيح مجهاديDocument9 pagesتسحيح مجهاديiTz-Ja7iM-No ratings yet
- Compo3Prem SoumiaDocument3 pagesCompo3Prem SoumiaManou100% (1)
- سلسلة تمارين في الكيمياءDocument2 pagesسلسلة تمارين في الكيمياءabidooNo ratings yet
- Dzexams Docs 2as 906595Document3 pagesDzexams Docs 2as 906595Chi KouNo ratings yet
- السلسلة 4Document2 pagesالسلسلة 4Sami RabhiNo ratings yet
- Physics 2se22 2trim7Document2 pagesPhysics 2se22 2trim7BOUCHEFFA HalimNo ratings yet
- - سلسلة تمارين في تعيين كمية المادة بواسطة المعايرة أكسدة - إرجاع للسنة 2 الشعب العلمية للاستاذ التيجاني دهامDocument2 pages- سلسلة تمارين في تعيين كمية المادة بواسطة المعايرة أكسدة - إرجاع للسنة 2 الشعب العلمية للاستاذ التيجاني دهامBessekri BessekriNo ratings yet
- Physics 3mtm18 1trim1Document2 pagesPhysics 3mtm18 1trim1safa safaNo ratings yet
- TP2Document3 pagesTP2Haytham KingdomNo ratings yet
- سلسلة مراجعة لأهم المكتسبات القبليةDocument3 pagesسلسلة مراجعة لأهم المكتسبات القبليةTeacher EnglishNo ratings yet
- Procedes 2mt16 1trim1Document2 pagesProcedes 2mt16 1trim1مولودNo ratings yet
- Composition 2 Eme Trimestre 2AS MDocument2 pagesComposition 2 Eme Trimestre 2AS MdfdfdfNo ratings yet
- الاختبار الثاني 2017Document2 pagesالاختبار الثاني 2017sama.benmiciaNo ratings yet
- سلسلة المراجعة في عطلة الشتاءDocument13 pagesسلسلة المراجعة في عطلة الشتاءFouad Ayadi100% (1)
- المعايرة المباشرة Le dosage directDocument1 pageالمعايرة المباشرة Le dosage directYassine BerchilNo ratings yet
- Kichah ExoacideDocument2 pagesKichah Exoacidekhalil75No ratings yet
- تمارين في درس قياس المواصلةDocument1 pageتمارين في درس قياس المواصلةaziz75% (4)
- BAC23 Doc1Document2 pagesBAC23 Doc1Sekkoum AhmedNo ratings yet
- BAC2023 Doc1Document2 pagesBAC2023 Doc1Soumia KerdNo ratings yet
- BAC2023 Doc1Document2 pagesBAC2023 Doc1Hina BouzerzourNo ratings yet
- معايرات اليود - 0Document6 pagesمعايرات اليود - 0Amros AtuirNo ratings yet
- Alttba Alzmni Lthol Kimiaii Sraa Altfaal Tmarin Ghir Mhlola 3Document2 pagesAlttba Alzmni Lthol Kimiaii Sraa Altfaal Tmarin Ghir Mhlola 3Abdellah FaqdaniNo ratings yet
- Alttba Alzmni Lthol Kimiaii Sraa Altfaal Tmarin Ghir Mhlola 3Document2 pagesAlttba Alzmni Lthol Kimiaii Sraa Altfaal Tmarin Ghir Mhlola 3Abdellah FaqdaniNo ratings yet
- أفضل باقة معلوماتية للأستاذ قزوري في الفيزياء - الفصل الأول - عقبة بن نافع - بكالوريا 2021Document96 pagesأفضل باقة معلوماتية للأستاذ قزوري في الفيزياء - الفصل الأول - عقبة بن نافع - بكالوريا 2021Leave me Alone100% (2)
- 3trim Se Physique5Document1 page3trim Se Physique5Zouaoua SlimaneNo ratings yet
- سلسلة تمارين بالحلولالمعايرة جزء01 كريم سنيDocument10 pagesسلسلة تمارين بالحلولالمعايرة جزء01 كريم سنيTarakk KaziNo ratings yet
- Dzexams 3as Physique 469651Document3 pagesDzexams 3as Physique 469651Abdou AbdouNo ratings yet
- Composition de Physique 3AS - Sujet 01Document2 pagesComposition de Physique 3AS - Sujet 01Hasan Rajawi100% (1)
- بطاقة التلميذ رقم 01Document2 pagesبطاقة التلميذ رقم 01FLASH FFNo ratings yet
- Physics 2se22 2trim7Document2 pagesPhysics 2se22 2trim7Youcef JousephNo ratings yet
- Physics 3se20 1trim7 PDFDocument6 pagesPhysics 3se20 1trim7 PDFnino ninoNo ratings yet
- Revision 1Document6 pagesRevision 1habaniNo ratings yet
- سلسلة تمارين الناقلية سنيDocument5 pagesسلسلة تمارين الناقلية سنيaiaimanimina109No ratings yet
- 1AS U07 - E3 - Cour-Exe 04Document6 pages1AS U07 - E3 - Cour-Exe 04Kaddache CharidNo ratings yet
- تمارين الاكسدة والارجاع مع الحلول بلعمريDocument8 pagesتمارين الاكسدة والارجاع مع الحلول بلعمريalaa eddine100% (6)
- Exc7 1bac PDFDocument4 pagesExc7 1bac PDFSouhail Alessandro67% (3)
- BBL AbedDocument4 pagesBBL Abedعبد العزيز مروىNo ratings yet
- فرض رقم 2 السنة الثانية ع - فيزيائيةDocument2 pagesفرض رقم 2 السنة الثانية ع - فيزيائيةالغزيزال الحسن EL GHZIZAL Hassane100% (5)
- Compo12 AsamadDocument2 pagesCompo12 AsamadmutraceNo ratings yet
- تمارين في التحولات القسرية PDFDocument5 pagesتمارين في التحولات القسرية PDFأبو أيوبNo ratings yet
- تمارين في الأعمدة والتحولات القسرية PDFDocument5 pagesتمارين في الأعمدة والتحولات القسرية PDFأبو أيوبNo ratings yet