Professional Documents
Culture Documents
Lampiran A Perhitungan: Vc2H5Ohxpc2H5Oh BM C 2 H 5 Oh GR ML GR Mol
Uploaded by
Nfwciwa0 ratings0% found this document useful (0 votes)
10 views4 pagescontoh
Original Title
Lampiran A
Copyright
© © All Rights Reserved
Available Formats
DOCX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this Documentcontoh
Copyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
10 views4 pagesLampiran A Perhitungan: Vc2H5Ohxpc2H5Oh BM C 2 H 5 Oh GR ML GR Mol
Uploaded by
Nfwciwacontoh
Copyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
You are on page 1of 4
LAMPIRAN A
PERHITUNGAN
Data-data percobaan yang diketahui
Temperatur = 25oC
Volume Umpan = 1000 mL
BM Etanol = 46 gr/mol
BM Air = 18 gr/mol
% etanol = 96 %
Volume Umpan Etanol = 300 mL
Volume Umpan Air = 700 mL
A.1 Perhitungan Kalibrasi Refraktometer
Perbandingan 1:9
V C 2 H 5OH x pC 2 H 5 OH
Mol etanol = x % etanol
BM C 2 H 5 OH
gr
1 mL x 07893
mL
= x 0,96
gr
46
mol
= 0,7893
VH 2O x p H 2O
Mol Air =
BM H 2 O
gr
9 mL x 1,0
mL
=
gr
18
mol
= 8,9604
mol C 2 H 5 OH
Fraksi mol C2H5OH =
mol C 2 H 5 OH + mol H 2 O
0,7893
=
07893+ 8,9604
= 0,032
Data selanjutnya dapat dilihat pada tabel 4.1
A.2 Perhitungan Fraksi Mol Umpan (Xf)
Perbandingan 30 % etanol : 70 % air
V etanol = 0,3 x 1000 mL
= 300 mL
V air = 0,7 x 1000 mL
= 700 mL
Vetanol x p etanol
Mol etanol = x % etanol
BM
300 x 0,95067
= x 0,96
46
= 5,9520
Vair x p air
Mol Air =
BM
700 x 0,997045
=
18
= 38,7739
Fraksi mol umpan (Xf)
mol etanol
Xf etanol =
mol etanol+mol air
5,9520
=
5,9520+38,7739
= 0,13
A.3 Perhitungan Volatilitas Relatif (aavg)
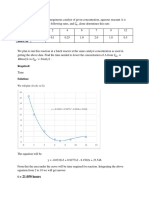
Dari grafik kalibrasi indeks bias didapatkan
XDavg= 0,486 ; XBavg rata-rata = 0,106
Xdavg(1− Xbavg)
aavg =
Xbavg(1− Xdavg)
0,486(1−0,106)
=
0,106(1−0,486)
= 7,9326
A.4 Perhitungan Data Kesetimbangan X-Y dengan Metode McCabe-Thiele
Untuk X1 = 0,1
αAVG. X 1
Y =
1+ ( aAVG−1 ) . X 1
7,9326 x 0,1
=
1+ ( 7,9326−1 ) .0,1
= 0,47
Perhitungan selanjutnya dapat dilihat pada tabel 4.2
A.5 Mencari Refluks Minimum (Rmin) dan y*
Diketahui y’ = 0,39 dari grafik kesetimbangan uap cair
Xd
y’ =
Rmin+1
0,49
0,39 =
Rmin+1
0,39Rmin + 0,39 = 0,49
0,49−0,39
Rmin =
0,39
Rmin = 0,256
Diketahui Rop = 2 x Rmin
Rop = 2 x 0,256
Rop = 0,512
Mencari y*
Xd
y* =
Rop+1
0,49
y* =
0,512+1
y* = 0,32
A.6 Menentukan HETP
Diketahu berdasarkan grafik kesetimbangan uap cair, diperoleh jumlah plat
teoritis sebanyak = 7 plat
Tinggi Kolom
HETP =
Jumlah Plat Teoritis
= 140/7
= 20
A.7 Menentukan Efisiensi
jumlah plat teoritis
η= x 100
jumlah plat aktual
7 plat
¿ x 100
7+ 2 plat
= 77,78 %
You might also like
- Thermodynamics Workshop Problems Model Answers 2010-2011 1Document9 pagesThermodynamics Workshop Problems Model Answers 2010-2011 1djsmilie77No ratings yet
- Solution For 1.4 and 1Document4 pagesSolution For 1.4 and 1lieu_hyacinth0% (1)
- ECP 224 Test 2 2020 SolutionDocument6 pagesECP 224 Test 2 2020 SolutionCaleb MunyairiNo ratings yet
- Gases and VaporsDocument2 pagesGases and VaporsKhristel PenoliarNo ratings yet
- Ullia Nurul - 11.7.6 OtkDocument8 pagesUllia Nurul - 11.7.6 OtkUllia Ismala0% (1)
- DESTILASIIIDocument2 pagesDESTILASIIIargoniodideNo ratings yet
- Lemper RevisedDocument7 pagesLemper RevisedTitin Setya MuktiNo ratings yet
- ChE Day 2Document6 pagesChE Day 2JHuvieCLaireNo ratings yet
- 4 Example On Combustion of CoalDocument12 pages4 Example On Combustion of CoalDale TanNo ratings yet
- CH138P WS 1.2 Lorian, LBDDocument6 pagesCH138P WS 1.2 Lorian, LBDLora BellNo ratings yet
- Che61 At11Document9 pagesChe61 At11Michael Alex MabaoNo ratings yet
- PH O P Total P H O: A) Molal SaturationDocument5 pagesPH O P Total P H O: A) Molal SaturationMiraNo ratings yet
- Vi. Perhitungan: Neraca MassaDocument7 pagesVi. Perhitungan: Neraca MassasabrinaNo ratings yet
- Laporan Amyl AsetatDocument7 pagesLaporan Amyl AsetatWulan SariNo ratings yet
- Solutions of ExercisesDocument87 pagesSolutions of ExercisesDianiTz MendOzaNo ratings yet
- Handout 26 Examples CorrectedDocument4 pagesHandout 26 Examples CorrectedrickNo ratings yet
- Gibbs y MezclasDocument5 pagesGibbs y MezclasRodrigo GarciaNo ratings yet
- For Checking ExamDocument3 pagesFor Checking Examcamille lei CalderonNo ratings yet
- Ponchon-Savarit Method ProblemDocument9 pagesPonchon-Savarit Method ProblemZowiNo ratings yet
- Unit 1 and Unit 2 : CalculationsDocument8 pagesUnit 1 and Unit 2 : Calculationsamr ahmedNo ratings yet
- Distillation Column: Bubble Point ComputationDocument11 pagesDistillation Column: Bubble Point ComputationChua RhickNo ratings yet
- Worksheet 19 - Weak Acids and Bases: 2 4 2 0, C BX Form The of Equations For + +Document4 pagesWorksheet 19 - Weak Acids and Bases: 2 4 2 0, C BX Form The of Equations For + +Link 08769No ratings yet
- Lembar PerhitunganDocument12 pagesLembar PerhitunganArie SetieawanNo ratings yet
- Combustion of CoalDocument12 pagesCombustion of CoalAlteaAl100% (1)
- Q2 Retake CHe 111P 4Th Q 2016-17Document6 pagesQ2 Retake CHe 111P 4Th Q 2016-17Mateo PremarionNo ratings yet
- Separation ReportDocument16 pagesSeparation Reportdhoom 760No ratings yet
- Assignment 5 Ionization (LEC)Document8 pagesAssignment 5 Ionization (LEC)Poison PinkNo ratings yet
- Cálculos Químicos: Cálculos Del Experimento 1: "Volumen Molar de Un Gas"Document4 pagesCálculos Químicos: Cálculos Del Experimento 1: "Volumen Molar de Un Gas"Carl AcuñaNo ratings yet
- Contoh SoalDocument12 pagesContoh SoalHayu ZuhraNo ratings yet
- Lembar Perhitungan Ester p0Document10 pagesLembar Perhitungan Ester p0Zahra AlifiaNo ratings yet
- Statement of The Problem: % RecoveryDocument5 pagesStatement of The Problem: % RecoveryAnthon ToledanoNo ratings yet
- CH Cooc H: AppendiksDocument5 pagesCH Cooc H: AppendiksKatherine PutriNo ratings yet
- Solution Tutorial 6 2022fDocument3 pagesSolution Tutorial 6 2022fcompasscuriosityNo ratings yet
- V F τ C dx r C C: 1 CaseDocument6 pagesV F τ C dx r C C: 1 CaseSaswata PradhanNo ratings yet
- 05 ThermoChemistry and Fuels Spring 2024Document77 pages05 ThermoChemistry and Fuels Spring 2024sajjadf954No ratings yet
- LAMPIRAN II Perhitungan Neraca EnergiDocument15 pagesLAMPIRAN II Perhitungan Neraca EnergiMuadzNo ratings yet
- CHY 47 Assignment #3 Group No. 2: - Log (Ka) Ka Ka Ka Ka Ka KaDocument4 pagesCHY 47 Assignment #3 Group No. 2: - Log (Ka) Ka Ka Ka Ka Ka KaFengari CresentNo ratings yet
- Tut 6 Ideal and Nonideal Solutions - SolutionsDocument19 pagesTut 6 Ideal and Nonideal Solutions - SolutionsAsma NasserNo ratings yet
- CP5077 Tutorial 3B Q4to7 SolutionDocument29 pagesCP5077 Tutorial 3B Q4to7 Solutionsun. shineNo ratings yet
- Model Calculations For Total RefluxDocument5 pagesModel Calculations For Total RefluxZain Ul AbedinNo ratings yet
- ESE-2018 Mains Test Series: Mechanical Engineering Test No: 12Document41 pagesESE-2018 Mains Test Series: Mechanical Engineering Test No: 12ravi kumar kumawatNo ratings yet
- Solution Chemistry OPTandonDocument24 pagesSolution Chemistry OPTandonCaleb AsharleyNo ratings yet
- Distillation ColumnDocument10 pagesDistillation ColumnPrajapati HarshNo ratings yet
- Gas Ab Advanced LevelDocument130 pagesGas Ab Advanced LevelRochim Al IchwanNo ratings yet
- Solution 631049Document3 pagesSolution 631049Gaurav ChaudharyNo ratings yet
- Unit 2 Solution Part 2Document26 pagesUnit 2 Solution Part 2Subbiah S XI-BNo ratings yet
- Kinetics (Gjjkkkgty)Document5 pagesKinetics (Gjjkkkgty)Chrysler Kane DepnagNo ratings yet
- Transferencia de MasaDocument6 pagesTransferencia de MasaJonyzhitop TenorioNo ratings yet
- Lembar Perhitungan HDPDocument4 pagesLembar Perhitungan HDPScandyinHavia EmmuachhNo ratings yet
- (A) Langkah - Langkah:: 1. Menentukan Laju Alir Feed Dalam MolDocument20 pages(A) Langkah - Langkah:: 1. Menentukan Laju Alir Feed Dalam MolToniSilaenNo ratings yet
- Sample Problem #2Document7 pagesSample Problem #2Grazel MDNo ratings yet
- Atkkkkkkkk BaruuuuuDocument27 pagesAtkkkkkkkk BaruuuuuSavira ANo ratings yet
- Sizing StrippingDocument14 pagesSizing StrippingEka trisnawatiNo ratings yet
- Pchem10e Solutions ch05Document39 pagesPchem10e Solutions ch05nohnarimNo ratings yet
- HWK Chap 3Document5 pagesHWK Chap 3Jad GhorraNo ratings yet
- HumidificationDocument5 pagesHumidificationAlbert Junior EvangelistaNo ratings yet
- Combustion Senator. LibyaDocument12 pagesCombustion Senator. Libyasenator.libyaNo ratings yet
- A .Tyas Presentasi Atk 2Document8 pagesA .Tyas Presentasi Atk 2TYASNo ratings yet
- Solution - Colligative Properties Solutions PDFDocument25 pagesSolution - Colligative Properties Solutions PDFGOURISH AGRAWALNo ratings yet