Professional Documents
Culture Documents
Đ Án Nư C Hành Đen Có Gas 2
Uploaded by
Duy Tân NguyễnOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Đ Án Nư C Hành Đen Có Gas 2
Uploaded by
Duy Tân NguyễnCopyright:
Available Formats
TRƯỜNG ĐẠI HỌC CÔNG NGHIỆP TP HCM
Viện Công Nghệ Sinh Học – Thực Phẩm
ĐỀ CƯƠNG ĐỒ ÁN TỐT NGHIỆP
GVHD: PGS.Ts Đàm Sao Mai
Ts.Trần Gia Bửu
NIÊN KHÓA: 2015-2019
LỜI CẢM ƠN
Trước hết, chúng em xin chân thành cảm ơn quý thầy cô bộ môn Công nghệ
thực phẩm đã hết lòng giảng dạy, truyền đạt những kiến thức cũng như các kinh
nghiệm quý báu trong suốt quãng thời gian học tập và nghiên cứu tại trường để
chúng em có được nền tảng kiến thức như ngày hôm nay.
Đặc biệt chúng em muốn gửi lời cảm ơn sâu sắc nhất đến cô Đàm Sao Mai và
cô Trần Gia Bửu. Chúng em cảm ơn các cô đã tận tình hướng dẫn và giúp đỡ chúng
em hoàn thành khoá luận tốt nghiệp một cách tốt nhất.
Chúng em xin chân thành cảm ơn quý thầy cô phòng thí nghiệm đã giúp đỡ
và tạo điều kiện về cơ sở vật chất như: bố trí phòng thí nghiệm, cung cấp các trang
thiết bị, dụng cụ, hóa chất… trong suốt thời gian thực hiện đồ án.
Cuối cùng, chúng em xin cảm ơn gia đình và bạn bè đã bên cạnh hỗ trợ, động
viên chúng em.
Chúng em xin gửi lời chúc sức khỏe đến tất cả thầy cô và bạn bè.
TP. Hồ Chí Minh, ngày 15 tháng 05 năm 2018
Sinh viên thực hiện
Nhóm: Hành Tím Đen 2
CHƯƠNG 1: TỔNG QUAN VỀ TÀI LIỆU
1.1. Mục đích
Nghiên cứu quy trình làm sản phẩm nước uống từ hành đen.
1.2. Mục tiêu
Nâng cao giá trị sử dụng của hành tím, tạo ra sản phẩm mới lạ.
1.3. Đối tượng phạm vi nghiên cứu
Đối tượng: hành tím
Xuất xứ hành tím: hành tím Vĩnh Châu.
1.4. Nội dung nghiên cứu
Khảo sát khả năng chống oxy hóa của sản phẩm.
Khảo sát hàm lượng polyphenol.
Khảo sát hàm lượng Flavonoid.
Cảm quan về mùi vị.
Kiểm tra vi sinh của sản phẩm.
1.5. Tổng quan về cây hành tím
1.5.1 Tên gọi và nguồn gốc
Hành tím có tên khoa học là Allium ascalonicum, bắt nguồn từ chữ Ascalon -
tên của một thị trấn ở miền Nam Palestin, nơi mà các nhà khoa học cho là nguồn gốc
xuất xứ của giống hành này. Ở Vĩnh Châu, chưa ai biết giống hành tím được trồng từ
khi nào. Mọi người thường gọi nó là "hành tàu", bởi nó được người Hoa trồng từ rất
sớm. Gặp được đất phù hợp, "hành tàu" đã phát triển mạnh cho đến ngày nay. Vĩnh
Châu là một trong ba khu vực có diện tích sản xuất hành lớn nhất nước. Ngoài Vĩnh
Châu thì đó là Quảng Ngãi và vùng ngoại thành Hà Nội.
Hành tím thuộc nhóm Aggregatum var. aggregatum . Từ một củ sinh ra nhiều củ
hay chồi và được sử dụng cho nhân giống.
Nhóm: Hành Tím Đen 3
Hành tím có tên khoa học là Allium ascalonicum , bắt nguồn từ chữ Ascalon -
tên của một thị trấn ở miền Nam Palestin, nơi mà các nhà khoa học cho là nguồn gốc
xuất xứ của giống hành này.
Hình 1.1: Cấu tạo cây hành tím [1]
Hành tím trồng được trên nhiều loại đất, nhưng đất cần cao ráo, tơi xốp nhiều
dinh dưỡng, nếu trồng gần nguồn nước mặn phải tưới nước ngọt. Hành rất sợ ngập
úng, vì thế người ta cần bố trí vụ trồng vào thời điểm hết mưa để tránh hiện tượng thối
củ. Làm đất: cày ải trước 1 tháng, trước khi lên liếp 3 - 5 ngày tiến hành rải vôi, nếu
đất sét cần trộn cát mịn đều trên mặt liếp. Làm liếp: liếp cao 15 – 20 cm, mặt liếp rộng
0,7 - 0,9 m, khoảng cách mương giữa 2 liếp 20 – 30 cm. Liếp trồng cần bằng phẳng,
tưới nhẹ và phủ một lớp rơm trước khi trồng.
Tổng diện tích gieo trồng hành tím của tỉnh Sóc Trăng lớn nhất đồng bằng
Sông Cửu Long, gần 4.500 ha, trong đó chỉ riêng huyện Vĩnh Châu đã chiếm khoảng
trên 4.000 ha. Hàng năm, tổng sản lượng hành thương phẩm có thể cung cấp từ 60.000
- 80.000 tấn đến thành phố Hồ Chí Minh và các tỉnh Đồng bằng sông Cửu Long. Thế
nhưng, cho tới nay sản lượng hành tím của tỉnh Sóc Trăng vẫn chưa đáp ứng đủ nhu
cầu tiêu thụ nội địa và xuất khẩu mạnh.
Hành tím được xem là một trong những đặc sản của tỉnh Sóc Trăng, có giá trị kinh tế
cao và có một vị trí quan trọng trong cơ cấu cây trồng của huyện Vĩnh Châu. Để tăng
cao giá trị của hành tím về mặt kinh tế cũng như khoa học, vì vậy chúng tôi quyết định
thực hiện đề tài nghiên cứu “Nghiên cứu quy trình sản xuất nước uống hành đen”.
Nhóm: Hành Tím Đen 4
1.5.2 Các thành phần của củ hành
Củ hành tươi bao gồm chủ yếu là nước (khoảng 88%), saccharides (6%) và
protein (1.5 %). Tuy nhiên thành phần hóa học cụ thể phụ thuộc vào nhiều yếu tố
chẳng hạn như điều kiện phát triển, thời gian thu hoạch, thời gian và điều kiện bảo
quản.
Bảng 1.1_Thành phần hóa học của củ hành tím
Thành phần Hàm lượng (%)
Nước 86-88
Protein 1.2
Glucid 11
Cellulose 0.6
Tro 0.4
Vitamin B1 0.08 mg
Vitamin B2 0.01 mg
Vitamin C 11 mg
Ngoài ra trong hành củ còn chứa nhiều chất khoáng vi lượng khác như 38 mg
Ca, 58 mg P, 0,8 mg Fe, 0.03 mg caroten trong 100g ăn được. các nguyên tố: Na, K,
S, Si; acid acetic tinh dầu bay hơi, glucokinin, oxydase và diatase…
Flavonoid: Trong hành tím có nhiều flavonoid như anthocyanin, kaempferol,
quercetin và các dẫn xuất như isoquercetin, quercetin diglucoside, quercetin
monoglucoside và quercetin tự do.
Nhóm: Hành Tím Đen 5
1.5.3 Công dụng của hành tím
Theo Health Sina, từ xưa đến nay, cả Đông và Tây y đều coi trọng công dụng
của hành tím. Loài này còn có tên gọi khác là hành bóng, hành Hà Lan, được mệnh
danh là “vua của các loại rau” với lịch sử hơn 5.000 năm. Đến nay hành được trồng
phổ biến trên khắp thế giới. [1]
Y học cổ đại Trung Quốc ghi chép rằng hành tím vị ngọt, cay nhẹ, hơi chát, ấm
áp, có tác dụng nhuận trường, lưu thông khí huyết dạ dày, tốt cho lá lách, trừ cảm
lạnh, dễ tiêu hóa, giải độc. Y học hiện đại phát hiện loại củ này có tính kháng khuẩn
chống viêm, lợi tiểu, trị tiêu chảy, giảm đường trong máu, hạ huyết áp, hạ cholesterol,
chống oxy hóa và nhiều vai trò khác. [1]
Nghiên cứu của FAO (1999), Dharmananda (1996) và You (1989) còn cho thấy
tác dụng làm giảm các trường hợp ung thư thực quản và dạ dày ở những người ăn
hành đều đặn. Nghiên cứu mới đây nhất cũng cho thấy tác dụng phòng ung thư tuyến
tiền liệt của hành và tỏi. Hàm lượng Quercetin và Selenium rất cao của hành có thể
giải thích cho tác dụng phòng ung thư của vị thuốc và món ăn này. Củ hành có thể
được sử dụng ở các dạng sống, nấu chín và được bảo quản bằng các phưong pháp: bảo
quản tươi, sấy khô, muối chua,…[1]
Dù không thiếu dược liệu có tác dụng diệt khuẩn, ký sinh trùng, nấm mốc nhưng
cho đến nay, chuyên gia ngành dược vẫn trước sau xếp củ hành vào nhóm đứng đầu
về tính kháng sinh theo cơ chế sinh học, nghĩa là ít gây phản ứng phụ
Chất flavonoids tìm thấy trong hành tím hoạt động như một chất chống ô xy hóa
có tác dụng ngăn chặn các khối u hình thành và phát triển, đồng thời thúc đẩy khả
năng miễn dịch của cơ thể.
Hợp chất quercetin tìm thấy dồi dào trong hành tím đóng vai trò quan trọng
trong việc ngăn ngừa bệnh ung thư, đặc biệt là ung thư ruột kết. Fructo-
oligosaccharides trong hành kích thích sự tăng trưởng của vi khuẩn có lợi trong ruột
kết và giúp giảm nguy cơ phát triển khối u ở ruột kết.
Nhóm: Hành Tím Đen 6
1.6. Tổng quan về enzymes pectinase.
1.6.1. Giới thiệu chung
Enzyme pectinase là một nhóm enzyme thủy phân pectin , sản phẩm của quá
trình này là acid galacturonic, galactose, arabinose, methanol… đây là một nhóm
ezyme được ứng dụng rộng rãi trong công nghiệp chỉ đứng sau amylasevà protease.
Enzyme này ban đầu được phát hiện trong các dịch chiết trái cây như cà rốt, cà chua
hay đại mạch. Đầu tiên phải kể đến là phát hiện của E.fremi (1840) trên đối tượng cà
rốt.
1.6.2. Cấu tạo.
Pectin là polysaccharide dị thể, chủ yếu là một mạch chính gồm các gốc
acid –α–D–1,4 galacturonic, liên kết với nhau bằng liên kết 1,4–O glucozic còn gọi
là acid polygalacturonic hay acid pectic. Pectine hòa tan trong tự nhiên là ester
metylic của acid pectic.
Hình 1.2: Cấu tạo enzymes pectinase. [ ]
Trong thực tế không phải tất cả các nhóm –COOH ở C6 của đường galactose
cũng bị metyl hóa (tạo ester metylic), mà đôi khi một số nhóm –COOH bị decacboxyl
hóa (khử CO2), một số nhóm –COOH thay thế -H bằng kim loại, cũng có lúc giữ
nguyên dạng –COO. Người ta cho rằng protopectine là hợp chất giữa pectine và
araban, galactose hay tinh bột. Trọng lượng phân tử từ 20.000 – 200.000 đvC.
Nhóm: Hành Tím Đen 7
1.6.3. Phân loại.
Enzyme pectinase có thể phân loại theo cơ chế tác dụng của chúng:
Enzymes (tên
STT Enzymes (tên gọi theo hệ thống) Phản ứng xúc tác
thường gọi)
Pectin + H2O = n
1 Pectin-pectinhydrolase pectinesterase
metanol + pectic acid
Endopoly Thủy phân liên kết -
Poly--1,4 galacturonid- 1,4-D- galacturonid
2 galacturonase trong galacturonid
glycano hydrolase-PG
(endo-PG) không theo một trật tự
nào.
Thủy phân liên kết
Exopoly -1,4-D- galacturonid
Poly--1,4-D galacturonidgalacturon - trong pectat, trong
3 galacturonase
hydrolase. galacturonic với sự đứt
(exo-PG) mạch của acid
galacturonic
Endopolymetil- Thủy phân liên kết -
Poly--1,4-D- galacturonidmetilester - 1,4-D- galacturonid
4 galacturonase
Glycanohydrolase. trong pectin không theo
(Endo-PMG) một trật tự nhất định.
Thủy phân liên kết -
1,4-D- galacturonid
Exo-pectatliase trong pectat với sự tạo
5 Poly--1,4-D-galacturonid
(exo-PKTE). thành -4,5
digalacturonoliase.
aciddegalacturonic
không theo một trật tự
nhất định.
Thủy phân liên kết
-1,4-D- galacturonid
Endopectatliase trong pectat, trong
6 Poly--1,4-D-galacturonid galacturonic với sự tạo
glicanoliase (PETE). thành nối đôi không
theo một trật tự nhất
định.
Thủy phân liên kết -
1,4-D- galacturonid
Poly--1,4-D-galacturonid Endopectinliase
7 trong pectin với sự tạo
metylester glicanoliase. (Endo-PTE). thành nối đôi không
theo một trật tự nhất
định.
Nhóm: Hành Tím Đen 8
Pectinesterase (PE): xúc tác sự thủy phân của các nhóm methyl ester. Enzyme
thường tấn công vào các nhóm ester methyl của đơn vị galaturonate nằm kề đơn vị
không bị ester hoá, phân cắt các nhóm methoxy (COOCH3) đứng cạnh các nhóm –
COOH tự do, tạo thành acid pectinic hoặc acid pectic và methanol. Pectinesterase thu
được từ các nguồn khác nhau có giá trị pH tối ưu khác nhau. Nếu thu từ nguồn VSV
thì PH tối ưu từ 4,5-5,5, còn nếu từ nguồn thực vật thì có pH tối ưu từ 5,0-8,5.
Pectinesterase từ nấm mốc có nhiệt độ tối ưu là 30-40 o C và bị vô hoạt ở 55-62o C.
Pectinesterase thường được hoạt hoá bởi các ion Ca2+ và Mg 2+ .
Polygalacturonase: còn có tên gọi là poly -1,4-galacturoniglucanohydrolase,
xúc tác sự phân cắt các mối liên kết –1,4- glycosid. Các exo-PG (exo-poly
1,4--D-galacturonide) galacturonohydrolase, phân cắt từ các đầu không khử, và endo-
PG (endo-poly1,4--D-galacturonide) glycanohydrolase, tấn công ngẫu nhiên
vào giữa mạch cơ chất. Polygalacturonase ít gặp trong thực vật nhưng có chủ yếu
ở một số nấm mốc và vi khuẩn. Polygalacturonase là một phức hệ enzyme gồm có
nhiều cấu tử và thường có tính đặc hiệu cao đối với cơ chất. Trên cơ sở tính đặc hiệu
và cơ chế tác dụng với cơ chất, enzym polygalacturonase được chia làm bốn loại.
Polymethylgalacturonase: hay còn gọi là 1,4-galacturonite
methylesglucanohydrolase, tác dụng trên polygalactorunic acid đã được methoxyl hoá
(tức là pectin). Enzyme này lại được phân thành hai nhóm nhỏ phụ thuộc vào khả
năng phân cắt ở trong hay cuối mạch trong phân tử pectin, đó là endo-glucosidase -
polymethyl galacturonase kiểu I và exo-glucosidase- polymethylgalaturonase kiểu II.
Polygalacturonase, enzyme tác dụng trên pectic acid hoặc pectinic, cũng
được chia thành hai nhóm nhỏ là endo-glucosidase-polygalacturonase kiểu II và exo-
glucosidase-polygalacturonase kiểu IV. Enzyme endo- glucosidase-Polymethyl-
galacturonase kiểu I là enzyme polymethylgalacturonase dịch hoá pectin có mức độ
methyl hoá càng cao thì bị thủy phân bởi enzyme này càng nhanh và càng có hiệu quả.
Trong dung dịch, khi có mặt của enzyme pectinesterase thì hoạt độ của enzyme này
thường bị giảm. Enzyme này rất phổ biến trong các VSV, đặc biệt là nấm mốc A.
niger, A, awamori.
Nhóm: Hành Tím Đen 9
Pectate lyase (PEL): xúc tác sự phân cắt các đơn vị galacturonate không bị
ester hoá. Cả hai enzyme exo-PEL (exo-Poly(1,4-D-galac turonide) lyase) và endo-
PEL (endo-poly(1,4-D-galacturonic lyase) đều tồn tại. Pectate và pectin có lượng
methoxyl thấp là các cơ chất thích hợp hơn cả cho các enzyme này. Nói chung, cả hai
enzyme này đều có khoảng pH tối đa nằm trong khoảng từ 8,0-11, đều cần ion Ca2+ để
hoạt động. Pectate lyase không được tìm thấy trong cây xanh, nhưng có ở vi khuẩn và
nấm. Các enzyme VSV ngoại bào này đóng một vai trò rất quan trọng trong quá trình
gây bệnh ở thực vật, gây ra sự phân hủy mô của thành tế bào, làm mềm và làm mục
còn
–1 được gọi là poly
mô thực vật.
Pectin-transeliminase hay
1.6.4. Đặc điểm của enzymes pectinase.
1.6.1. Enzymes pectinase từ thực vật.
Pectinesterase:
Trong thực vật, hầu hết các loại cây cho trái đều chứa enyme PE.Enzyme này
thường tồn tại dưới nhiều hình thức khác nhau, nằm trong phần vỏ tế bào. PE ở thực
vật nói chung có hoạt độ tối ưu trong khoảng pH hơi kiềm. Các cation kim loại ở nồng
độ thấp, như Ca 2+ chẳng hạn, có khuynh hướng làm tăng nồng độ hoạt động của
enzyme.
Cà chua chứa ít nhất hai loại PE. Cả PE1 và PE2 đều tăng trong giai đoạn đầu
của quá trình chín. Khi bước vào giai đoạn chín, nồng độ enzyme PE1 giảm xuống,
nhưng PE2 tích luỹ dần cho đến khi trái cây có màu đặc trưng của trái chín. PE2 có
khối lượng phân tử 23kD, pH tối ưu 7,6. Enzyme này bị bất hoạt 50% sau 5 phút đun
ở 67oC. Các ion Ca2+ và Na+ làm tăng hoạt độ của enzyme lên tối đa ở các nồng độ
0,005M và 0,05M, theo thứ tự.
PE của đậu nành là protein có khối lượng phân tử 33kD, hoạt động tối ưu tại
pH gần 8. Polygalacturonic acid, là sản phẩm được hình thành do quá trình để methyl
hoá các phân tử galacturonic acid.
Trong thịt quả chuối có hai isoenzyme PE. Cả hai có cùng khối lượng phân tử
là 30kD, nhưng có điểm đẳng điện khác nhau: 8,8 và 9,3. Các enzyme này hoạt động
Nhóm: Hành Tím Đen 10
ở pH tối đa là 7,5. Hoạt độ enzyme tăng lên khi thêm vào dung dịch NaCl ở nồng độ
0,2M, và đưa pH của dung dịch về 6,0. Các enzyme này bị ức chế bởi nhiều loại.
Polyol có khối lượng phân tử thấp, như glycerol, sucrose, glucose, maltose và
galactose.
PE trong quả cam có hai loại: đó là hai isoenzyme PE1 và PE2 có khối lượng
phân tử 36,kD, nhưng có điểm đẳng điện khác nhau là:
10,05 và 11,0, theo thứ tự.
pH tối ưu của PE1 là 7,6, còn của PE2 là 8,0.
Trong thành phần của nhiều thịt quả khác cũng chứa hai isoenzyem, một trong
hai enzyme này có tính bền nhiệt hơn, còn enzyme kia thì ít mẫn cảm hơn khi bị tác
động của protease. Độ ổn định của enzyme có thể liên quan đến mức độ glycosyl hoá
của các phân tử enzyme. Enzyme bền nhiệt hơn và enzyme còn lại có khối lượng là
51kD và 36kD, theo thứ tự.
Hình 1.3: Cấu trúc của pectinesterase từ carrot. [ ]
Cả táo và kiwi cũng chứa hai loại isoenzyme. Các isoenzyme của kiwi có cùng
khối lượng phân tử là 57kD và cùng điểm đẳng điện là 7,3. Tuy nhiên, chúng khác
nhau về mức độ bền nhiệt.
Polygalacturonase:
Hầu hết các nghiên cứu về PG đều trên cơ sở các nguồn VSV. PG thường được
tìm thấy trong các phần tiết ngoại bào của các loài nấm và vi khuẩn gây bệnh, chẳng
hạn như Sacchromyces gragilis, Aspergillus niger, Lactobacillus plantarum,
Nhóm: Hành Tím Đen 11
Cochiliobolus carbonum, Neurospora crassa, cácloài Ascomycete, Phizopus
arrchizus, và Fusarium osyporum. Tuy nhiên, trong thực tế, PG của thực vật bậc cao
được nghiên cứu rất nhiều ở cà chua chín.
Các enzyme PG trong cà chua chín tồn tại dưới hai dạng, và cả hai đều là endo-
enzyme. PG1 có khối lượng phân tử 84kD và có khoảng 50% bị bất hoạt ở nhiệt độ
78oC. PG2 có khối lượng phân tử 44kD và có khoảng 50% bị bất hoạt ở 57oC. PG1 có
độ ổn định tối đa ở pH 4,3, trái lại PG2 ổn định tối đa ở pH 5,6.
Exo-PG thủy phân các đầu không khử của chuỗi polygalacturonic, tạo ra
galacturonic acid là sản phẩm thủy phân chiếm ưu thế.Sự thủy phân polymer này bị
gián đoạn của sự tồn tại của các mạch nhánh trong cơ chất. Mức độ thuỷ phân tăng tỉ
lệ với kích thước cơ chất, đạt tối đa với mức polymer hoá 20 đối với các exo-PG ở cà
rốt và đào. Hoạt động của các exo-enzyme làm tăng nhanh sự tạo thành các nhóm khử
và làm tăng chậm độ nhớt của dung dịch cơ chất. Sự phân hủy polyuronide trong quá
trình chín không gây ra sự tích lũy galacturonic acid, và chỉ có endo-enzyme PG là
có liên quan.
1.6.2. Enzymes pectinase từ vi sinh vật.
Nguồn giàu enzyme pectinase là nấm mốc, nấm men, vi khuẩn.
Nấm mốc: penicillium glaucum, p.ehrlichii, p.chrysogenum, p.expanam,
p.cilrimim, aspergillus awamori, a.foetidus, a.niger, a.terrus, a.saitoi, a.aureus,
a.oryzae, a.wentii, fusarium moniliforme,…
Nấm men: saccharomyces fragilis
Vi khuẩn: bacillus polymyxa, flavobacterium pectinovorum, klebsiella
aerogenes…
Các loài vi sinh vật này thường có trong bề mặt tất cả các loại quả, các bộ phận
khác của thực vật. khi quả bị hư hỏng, hoặc thực vật chết, chúng sẽ cùng các loài vi
sinh vật khác phá huỷ nhanh quả và các bộ phận của thực vật. Người ta thường thu
pectinase từ canh trường bề mặt hoặc từ canh trường bề sâu của nấm mốc.
Nhóm: Hành Tím Đen 12
Các vi khuẩn và nấm men cũng tổng hợp được enzime này a.niger chủ yếu tổng
hợp ra pectinnesterase. con.diplodiella, pen.citrimin tạo ra chủ yếu là
polygalacturonase.
Nấm men sacch.fragilis dường như chỉ tạo ra endopectintraseliminase.
Vi khuẩn bac.polymyxa, bac.species lại chủ yếu tạo ra transeliminase.
Pectinesterase:
Pectinesterase thu được từ các nguồn khác nhau có giá trị PH tối ưu khác nhau:
pH tối ưu của pectinesterase từ nguồn nấm mốc là 4,5 đến 5,5 còn của chế phẩm đã
loại bỏ enzime polygalacturonase sẽ có PH tối ưu từ 2,0 đến 6,5. Trái lại ph tối ưu của
pectinesterase từ nguồn thực vật thượng đẳng là từ 6 đến 7,5 – 8.
Nhiệt độ tối ưu của pectinesterase từ nấm mốc là 40 đến 450 C. Từ 55 đến
620C thì enzime bị vô hoạt, trong khi đó nhiệt độ tối ưu của enzime pectinesterase từ
thực vật thượng đẳng cao hơn: từ 55 – 600oC
Pectinesterase có thể nhận được từ canh trường nấm mốc A.niger có nhiệt độ
tối ưu là 30 – 45oC, Phopt = 4,5-5,5 và bị vô hoạt ở 55- 62oC và từ thực vật (phopt
=7,5-8, toopt = 55-60o C). Khả năng hoạt động của chúng phụ thuộc vào nguồn thu
nhận, mức độ ester hoá của pectin. Ion natri và đặc biệt là ion canxi, cũng như chlorua
của Na, K và Ca sẽ hoạt hóa pectinesterase từ nấm mốc conithyrium diplodiella và từ
a.niger.trái lại các cation hóa trị 3 và 4 (thủy ngân nitrat, chì nitrat, nhôm sunfat và sắt
clorua) sẽ kìm hãm tác dụng của pectinesterase.
Ngoài ra, người ta đã thu được enzime pectinesterase ở trạng thái đông thể và
người ta cũng đã xác lập được rằng n-axit cuối trong phân tử enzime là phenylalanin.
Pectinesterase của nấm mốc sẽ thủy phân trước nhất là nhóm methylester
nằm ở giữa hai nhóm carboxyl tự do. và enzime sẽ thủy phân lần lượt cắt liên kết ester
dọc theo phân tử pectin. hoạt động của pectinesterase phụ thuộc nhiều vào mức độ
ester hóa của pectin và tỷ lệ thuận vào mức độ ester hóa. Chẳng hạn, đối với tác động
của pectinesterase từ nấm mốc a.niger, cần thiết phải có pectin ester hóa ở mức độ cao
không ít hơn 70%.
Nhóm: Hành Tím Đen 13
Polygalacturonase:
Hầu hết các nghiên cứu về Polygalacturonase đều trên cơ sở các nguồn vi sinh
vật. Polygalacturonase thường được tìm thấy trong các phần tiết ngoại bào của các
loài nấm và vi khuẩn gây bệnh, chẳng hạn như: saccharomyces fragilis, asperigillus
niger, lactobacillus plantarum, cochlibolus carbonum, neurosrora crassa, các loài
ascomycete, rhizopus arrchizus và fusarium oxysrorum.
PH tối ưu của các polygalacturonase cũng khác nhau, phụ thuộc vào nguồn thu
và cơ chất. Chẳng hạn polygalacturonase dịch hóa (endopolygalacturonase) khi tác
dụng trên acid pectinic thì ph tối ưu nằm trong khoảng từ 4,0 – 5,5. cũng enzyme đó
nhưng khi tác dụng trên pectin thì lại có ph tối ưu trong khoảng 5,5 – 6. Còn
polygalacturonase đường hóa khi tác dụng trên pectin thì ph tối ưu từ 3 – 4 nhưng khi
tác dụng trên acid pectinic thì ph tối ưu cao hơn một ít ở vùng 4,4- 6
Các polygalacturonase chủ yếu bền vững ở vùng pH từ 4 – 6
Polygalacturonase đường hóa chủ yếu từ A.niger nếu được hoạt hóa bằng thủy
ngân thì có thể bền vững khi pH= 2,5.
Nhiệt độ tối ưu của đa số polygalacturonase nằm trong khoảng từ 40-450C.
Trong khoảng nhịệt độ đó, chúng thường bền vững, nhưng sẽ bị vô hoạt hóa khi ở
nhiệt độ 50 và 55 - 650C.
1.6.3. Trung tâm hoạt động của enzymes pectinase.
Enzyme pectinase chứa vùng có 8 – 10 vòng xoắn kép về phía phải với 2 vòng
tạo thành khe liên kết với cơ chất.
Trung tâm hoạt động của enzyme này chứa axit amin Aspartate và Lysine. Có
1 Histidine nằm gần trung tâm hoạt động sẽ ảnh hưởng đến khả năng xúc tác của
enzyme.
Nhiệt độ tối ưu của enzyme pectinase khoảng từ 45 – 55oC.
Nhóm: Hành Tím Đen 14
1.6.4. Cơ chế tác dụng của enzymes pectinase.
Trong chế biến nước quả, người ta sử dụng các chế phẩm enzym nhằm hai mục
đích cơ bản.
- Phá vỡ thành tế bào thực vật nhằm nâng cao hiệu suất thu nước quả.
- Làm trong và ổn định chất lượng nước.
Phá vỡ thành tế bào
Tế bào thực vật được cấu tạo bằng vỏ tế bào (thành tế bào). Vỏ tế bào như một
lớp thành bảo vệ rất hữu hiệu và tạo hình cho tế bào. Ở vỏ tế bào thực vật có nhiều
chất pectin, các chất pectin được xem như chất ciment gắn các tế bào với nhau. Phá vỡ
sự gắn kết này sẽ tạo điều kiện cho các vật chất trong tế bào thoát ra khỏi tế bào. Các
chế phẩm enzym có chứa không chỉ pectinase mà còn chứa các enzym trong nhóm
cellulase. Các loại enzym này sẽ làm phá vỡ thành tế bào và giúp quá trình thu nhận
dịch tế bào tốt hơn.
Làm trong dịch quả:
Nước quả sau khi được tách khỏi tế bào thường chứa nhiều chất khác nhau.
Trong đó chất pectin chiếm lượng đáng kể và pectin thường gây hiện tượng độ nhớt
cao và gây đục nước quả. Các chất protein có trong bào tương, màng tế bào và gian
bào. Pectin chứa polygalacturonic acid, araban và galactan.Trong đó lượng
polygalacturonic acid chiếm tới 40-60%. Khi bị thủy phân, pectin tách thành hai phần:
Phần trung tính – phức chất galactanoraban
Phần acid – acid pectic.
Trong bào tương, pectin nằm ở dạng hòa tan. Trong màng tế bào và gian bào,
chúng nằm ở dạng không hòa tan gọi là protopectin. Protopectin ở màng gian bào có
chứa lượng kim loại khá lớn và một lượng nhóm metocyl đủ để làm protopectin bền
vững. Còn protopectin ở màng tế bào chứa một lượng kim loại không nhiều, có độ
metocyl hóa cao. Vì thế, tế bào thực vật có khả năng trương nở tốt.
Nếu enzym tham gia phân giải pectin ở gian bào sẽ làm các tế bào khó liên kết
với nhau và thịt quả dễ dàng bị mềm ra.Pectin thường có mối liên kết hydro và liên
Nhóm: Hành Tím Đen 15
kết nguyên tử yếu hơn so với cellulose. Tham gia phân hủy pectin gồm nhiều loại
enzym : cellulose, pectinase,…
1.6.5. Lợi ích khi sử dụng enzymes pectinase.
Từ khi phát hiện ra enzym và khả năng chuyển hóa của enzym loài người đã
tăng nhanh quá trình sản xuất và ứng dụng enzym trong công nghiệp. Số lượng enzym
phát hiện ngày càng nhiều và số lượng enzym được ứng dụng vào công nghiệp cũng
ngày càng nhiều.
Trong sản xuất thực phẩm, người ta thường sử dụng các chế phẩm pectinase
dưới dạng tinh khiết. Người ta không dùng chế phẩm dưới dạng canh trường nấm mốc
sấy khô.
Pectinase thường được sử dụng trong các ngành công nghiếp thực phẩm sau:
Sản xuất rượu vang.
Sản xuất nước quả và nước uống không có cồn;
Sản xuất các mặt hàng từ quả: nước quả cô đặc, mứt nhừ, mứt đông,..
Sản xuất nước giải khát.
Sản xuất cà phê và cà phê hòa tan.
1.7. Phản ứng Maillard và những ứng dụng trong chế biến
thực phẩm
“Một trong những phản ứng tạo ra mùi vị quan trọng nhất trong nấu ăn là phản
ứng Maillard. Đôi khi nó được gọi là “phản ứng tạo màu nâu”, nhưng gọi thế thì chưa
đầy đủ. Thịt nấu chín, hải sản, và các loại thực phẩm giàu protein khác trải qua phản
ứng Maillard làm biến thành màu nâu, nhưng có những phản ứng khác cũng gây ra
màu nâu. Phản ứng Maillard tạo ra sắc tố màu nâu trong sả phẩm theo một cách rất cụ
thể: bằng cách sắp xếp các axit amin và các loại đường đơn giản nhất định, sau đó
chúng tự sắp xếp trong vòng liên kết và phản xạ ánh sáng vào mắt thành màu nâu.”
1.71. Phản ứng Maillard.
Các giai đoạn hình thành phản ứng
+ Giai đoạn đầu của phản ứng tạo melanoidin
Nhóm: Hành Tím Đen 16
Phản ứng ngưng tụ cacbonylamin
Giai đoạn đầu tiên của sự tạo thành melanoidin là sự ngưng tụ đường với
axitamin.
Hình 1.4: Phản ứng chuyển vị Amadori tạo ra 1-amin-1-dezoxy-2-xetozơ
Khi ở nhiệt độ cao thì phức đường amin bị đồng phân hóa hay người ta gọi là
bị chuyển vị nội phân Amadori. Kết quả là giữa nguyên tử cacbon thứ nhất và thứ hai
phát sinh ra nối kép và tạo thành 1 – amin – 1 – dezoxy – 2- xetoza.
Phức đường amin
Dạng enol của 1 – amin -1 deoxy – 2 xetoza
1 –amin -1 deoxy – 2 xetoza
Phẩm vật của sự chuyển vị Amadori là hợp chất có khả năng phản ứng và là
chất khởi đầu để tạo thành polyme có màu sẫm gọi là melanoidin.
Nhóm: Hành Tím Đen 17
Tạo thành furfurol và ozon
Nếu gluxit ban đầu là glucose thì sản phẩm chuyển vị Amadori khi đun nóng sẽ
là furan sau đó chuyển thành bazơ schiff của hydroxymetylfurfurol:
Tạo thành reducton có 6 nguyên tử C
Reducton là những hợp chất hữu cơ có tính khử mạnh do có nhóm endiol.
Thông thường, nhóm endiol của reducton được liên kết với gốc aldehit hoặc axit. Do
đó những hợp chất này rất nhạy với phản ứng oxy hóa khử.
Ví dụ về reducton có sáu nguyên tử C là axit dehydroascobic. Không phải chỉ
riêng reducton mà cả các dạng dehydro của nó cũng góp phần tạo nên màu nâu.
O O
H2C C C HC C C
H H
OH O OH OH
hydroxymetylglioxal reducton hay laø enolaldehit cuûa axit tartric
Phân hủy đường
Một trong những giai đoạn trung gian củ phản ứng tạo melanoidin là sự phân
hủy đường từ sản phẩm chuyển vị Amadori để tạo thành các sản phẩm khác nhau :
triozoreducton, aldehit pỉuvic, axeton, diaxetyl. Một số chất tạo thành khi phân hủy
đường có mùi và vị dễ chịu.
Nhóm: Hành Tím Đen 18
Phân hủy các hợp chất amin
Sản phẩm chuyển vị Amadori có thể kết hợp với axitamin tạo ra CO2 và H2O:
- CO 2
R CH NH2 + R' C CH 2 NH HC R''
- H 2O
COOH O COOH
axit amin aminodezoxyxetoza
H H H COOH
R CH 2 N C CH 2 NH CH R'' R CH N C C N C R''
R' COOH R' H H
bazo schiff
Bazơ schiff tạo thành bị thủy phân thành aldehit và hợp chất amin. Chính hợp
chất amin này sẽ cho các sản phẩm chứa nitơ và có màu nâu sau này. Còn aldehit
được tọa thành trong phản ứng này, so với axitamin đã phản ứng với
aminodezoxyxetoza thì có ít hơn một nguyên tử C.
H
C
NH2
R O
N
R' C H
H H O
R' C H
CH 2
H C H RC +
NH
N H H
R'' C COOH
R'' C COOH
H
CH3
amin
bazo schiff
Giữa furfurol hoặc hydroxymetylfurfurol và axitamin có thể xảy ra sự tương tác
oxy hóa.
Kết quả là từ axitamin tạo thành aldehit có ít hơn 1 nguyên tử C.
Aldehit cũng có thể được tạo thành do kết quả của sự chuyển amin giữa axitamin
với reducton
HC CH
HC CH + O2 O
O
HC C C
HC C C
O OOH
O H
furfurol axit peroxyfurfurolic
+ Giai đoạn cuối
Giai đọan cuối cùng này bao gồm rất nhiều phản ứng phức tạp, chủ yếu là hai
phản ứng sau:
Nhóm: Hành Tím Đen 19
Phản ứng ngưng tụ andol tạo thành polyme màu nâu không chứa nitơ;
Phản ứng trùng hợp aldehitamin tạo thành các hợp chất nitơ dị vòng.
O
O O
+ HCH2 C H3C CH CH2 C
H3C C
H H
H OH
aldehit axetic aldehit axetic aldol
Giai đoạn cuối cùng của phản ứng melanoidin sẽ tạo nên các polyme không no
hòa tan được trong nước, sau đó là các polyme không no và không hòa tan được trong
nước, nhưng đều có màu đậm và gọi chung là melanoidin.
1.72. Các yếu tố ảnh hưởng đến phản ứng Maillard
Thực tế trong hỗn hợp phản ứng có chứa đồng thời tất cả các sản phẩm, nhưng
tỷ lượng của sản phẩm này hay sản phẩm khác chiếm ưu thế là phụ thuộc mức độ tiến
hành phản ứng.
Cường độ màu của phản ứng phụ thuộc vào bản chất axit amin, đường,
nồng độ chất khô trong dung dịch, nhiệt độ, pH và một số yếu tố khác.
Ảnh hưởng của axitamin và đường: Qua cơ chế phản ứng, ta thấy một trong
những sản phẩm của giai đoạn trung gian là furfurol và oxymetylfurfurol kèm theo sự
tái tạo lại axitamin vốn đã tham gia tương tác với đường ở phản ứng đầu tiên. Như
vậy, axitamin có thể xem như một chất xúc tác trong giai đoạn đầu.
Các axitamin tham gia phản ứng khác nhau phụ thuộc vào nhiệt độ, pH và
lượng nước
Theo Kretovic, axitamin có khả năng phản ứng và cho sản phẩm màu mạnh
hơn cả là glicocol, alanin, asparagin. Xistin và tirozin cho sản phẩm màu yếu hơn cả.
Cho mùi mạnh hơn cả là valin và lơxin. Glicocol cho màu rất đậm, mùi của bia và vị
hơi chua. Alanin phản ứng chậm hơn và cho sản phẩm tương tự. Phenylalanin phản
ứng rất chậm, tạo thành sản phẩm có màu nâu sẫm và có mùi thơm hoa hồng. Lơxin
cho sản phẩm có màu không đáng kể nhưng có mùi bánh mỳ đặc trưng. Axit glutamic
có hoạt độ cao, nhưng cho sản phẩm có màu nhạt.
Nhóm: Hành Tím Đen 20
Hình 1. Ảnh hưởng của đường đến phản ứng Mailard
Cường độ của phản ứng cũng phụ thuộc vào bản chất của đường khử. Glucozơ
phản ứng mãnh liệt hơn cả, sau đó là galactozơ và lactozơ.
Cường độ của phản ứng melanoidin còn phụ thuộc vào nồng độ đường. Tỷ lệ
giữa axitamin và đường thích hợp nhất là 1/2 hoặc 1/3. Nếu tăng nồng độ đường sẽ
làm cho melanoidin tạo ra có thể tan được ngay cả khi nồng độ của chúng rất cao. Nói
chung, phản ứng có thể tiến hành ngay cả khi nồng độ axitamin không đáng kể và tỷ
lệ axitamin/ đường rất nhỏ như 1/40 thậm chí 1/300.
Ảnh hưởng của nước
Để phản ứng Maillard tiến hành cực đại thì xung quanh mỗi phân tử protein
phải tạo nên lớp đơn phân glucozơ và lớp đơn phân nước. Như vậy, sự có mặt của
nước là điều kiện rất cần thiết để tiến hành phản ứng. Nồng độ chất tác dụng càng cao,
lượng nước càng ít thì phản ứng xảy ra càng mạnh.
Hình 1.7.1: Ảnh hưởng của độ ẩm đến phản ứng Maillard
Ảnh hưởng của nhiệt độ và pH
Ở 0 0C và dưới 0 0C phản ứng melanoidin không xảy ra. . Người ta nhận thấy
khi ở nhiệt độ 95÷ 100 0C phản ứng sẽ cho các sản phẩm có tính chất cảm quan tốt
hơn cả. Khi nhiệt độ quá cao thì các melanoidin tạo thành có vị đắng và mùi khét. Vì
vậy, trong sản xuất để thu được malt màu , người ta thường khống chế phản ứng ở
Nhóm: Hành Tím Đen 21
1600C, mặc dù lượng chất màu đạt cực đại ở 190 0C vì ở nhiệt độ trên 1600C các
melanoidin tạo thành sẽ không hòa tan trong nước do đó giảm khả năng cho màu của
malt thu được.
Phản ứng Maillard có thể tiến hành trong một khoảng pH khá rộng, tuy nhiên
trong môi trường kiềm phản ứng xảy ra nhanh hơn. Trong môi trường axit pH < 3, quá
trình tạo melanoidin rất yếu và chủ yếu là sự phân hủy đường nhưng khi tăng nhiệt độ
tốc độ phản ứng tăng nhanh ngay cả trong môi trường axit (pH = 2).
Chất kìm hãm và chất tăng tốc phản ứng
Phản ứng caramel hóa, oxy hóa và melanoidin là những phản ứng có sự tham
gia của các hợp chất cacbonyl. Do đó chất kìm hãm phản ứng là những chất phản ứng
được với nhóm cacbonyl như dimedon, hydroxylamin, bisunfit. Những chất này sẽ kết
hợp với các chất khác nhau phát sinh ra ở trong giai đoạn trung gian, do đó làm ngừng
các quá trình tiếp theo của phản ứng.
1.73. Ứng dụng của phản ứng Maillard
Trong các sản phẩm thực phẩm đều có chứa đường và axitamin ở các hàm
lượng khác nhau do đó phản ứng Maillard rất phổ biến trong quá trình sản xuất và bảo
quản thực phẩm. Tùy thuộc vào yêu cầu về tính chất cảm quan của từng sản phẩm mà
người ta tạo điều kiện để tăng cường phản ứng đến tối đa hoặc kìm hãm phản ứng đến
mức tối thiểu.
Trong sản xuất bánh mỳ người ta tạo điều kiện cho phản ứng này phát triển tối
đa. Màu sắc của vỏ bánh mỳ hầu như do phản ứng này quyết định. Vì vậy những biện
pháp kỹ thuật tương ứng trong quy trình sản xuất lên men để tạo axitamin tự do,
đường khử, điều chỉnh nhiệt độ trong giai đoạn nướng đều nhằm mục đích đó.
Trong sản xuất bia, màu sắc và hương vị của bia chủ yếu do malt quyết định.
Các biện pháp kỹ thuật trong sản xuất malt đều nhằm điều hòa phản ứng melanoidin.
Để thu được malt vàng, người ta cho mọc mầm trong một thời gian ngắn, làm mất
nước nhanh để thu được lượng axitamin và ít đường làm khó khăn cho phản ứng
cacbonylamin. Trái lại để sản xuất malt đen thì nhiệt độ sấy phải cao hơn, thời gian
sấy lâu hơn. Theo Manxev, do thủy phân gluxit và protein mà tích tụ những hợp chất
có khả năng tạo thành chất thơm. Malt sấy ở nhiệt độ thấp quá sẽ ảnh hưởng xấu đến
Nhóm: Hành Tím Đen 22
vị của bia, còn khi sấy ở nhiệt độ qúa cao, bia sẽ có vị khét. Vì vậy khi sản xuất bia
vàng cần phải kiểm tra sự tạo melanoidin và hạn chế thời gian đun sôi dung dịch lên
men
Hình 1.7.3.1: Ứng dụng phản ứng Mailard trong sản xuất bia.
Trái lại, trong sản xuất rượu người ta tìm cách kìm hãm phản ứng tạo
melanoidin vì phản ứng gây tổn thất tinh bột và đường, đồng thời melanoidin tạo
thành làm kìm hãm hoạt động của enzyme. Zavroxki đã đề ra kỹ thuật nấu nguyên liệu
với một lượng nước lớn để khắc phục ảnh hưởng xấu của phản ứng này, đồng thời
giảm tổn thất đường và nâng cao hiệu suất rượu.
Trong sản xuất thuốc lá, quá trình sấy, trước khi lên men và lên men cũng do
phản ứng Maillard quyết định. Việc làm giảm độ ẩm của môi trường sẽ tạo điều kiện
thuận lợi cho phản ứng đó và tăng cường màu sẫm. Nguyên nhân cơ bản của sự tự ẩm
hóa thuốc lá là phản ứng melanoidin có kèm theo thoát nước. Khi tỷ lệ giữa axitamin
và đường bằng 1/2 thì lượng ẩm thoát ra là xực đại và lượng chất khô là cực tiểu.
Thay đổi tỷ lệ này sẽ có ảnh hưởng nhanh chóng đến lượng nước thoát ra trong phản
ứng.
Trong sản xuất đường, cà phê đường bị sẫm màu cũng là do phản ứng
melanoidin. Phản ứng melanoidin còn có ảnh hưởng lớn đến việc chế biến rau, quả
cũng như bảo quản chúng. Người ta đã thấy rằng do phản ứng giữa đường nghịch đảo
và axitamin hoặc muối amon mà tất cả các siro và nước quả cô đặc đều bị sẫm màu
khi bảo quản, nhất là ở nhiệt độ cao. Trong đồ hộp quả và rau, người ta có khuynh
hướng bảo vệ màu tự nhiên và hương thơm của chúng. Phản ứng Maillard luôn luôn
làm xấu đi không những tính chất cảm quan mà cả giá trị thực phẩm của sản phẩm
nữa. Tóm lại, phản ứng melanoidin rất phổ biến trong mọi sản phẩm thực phẩm có
liên quan với gia nhiệt và thời gian bảo quản lâu dài.
Nhóm: Hành Tím Đen 23
Hình 1.7.3.2: Ứng dụng phản ứng Mailard trong sản xuất cà phê.
Nhóm: Hành Tím Đen 24
Chương 2: VẬT LIỆU VÀ PHƯƠNG PHÁP NGHIÊN CỨU.
2.1. Nguyên liệu và hóa chất
2.1.1. Thời gian và địa điểm thực hiện.
- Địa điểm: Phòng thí nghiệm F6.03 của Viện Công nghệ Sinh học và Thực phẩm
– Trường Đại học Công Nghiệp Thành phố Hồ Chí Minh.
- Thời gian thực hiện: từ ngày / /2018 đến ngày / /2019.
2.1.2. Nguyên liệu.
Hành Vĩnh Châu.
Hành tím được mua ở Sóc Trăng (Nguồn gốc: thị xã Vĩnh Châu, tỉnh Sóc
Trăng). Hành được thu mua vào tháng 6, không sâu mọt, không hư hỏng vật lý.
Hình 2.1: Hành khi được thu mua.
Hành sau khi thu mua sẽ được bóc vỏ rồi trải qua quá trình lên men trong tủ ủ trong
thời gian 21 ngày ở nhiệt độ 70oC. Sau đó, được bảo quản ở nhiệt độ -5oC.
Hình 2.2: Hành sau khi lột vỏ Hình 2.3: Hành được bọc giấy bạc và ủ
Nhóm: Hành Tím Đen 25
Hình 2.4: Tỏi sau 21 ngày được ủ.
Pectinex Ultra SP-L
- Enzyme pectinase thương mại (Enzyme Pectinex Ultra SP-L, công ty Novozymes
Singapore).
- Công ty nhập khẩu và phân phối : công ty TNHH Brenntag Việt Nam ( 202 Hoàng
Văn Thụ, phường 9, quận Phú Nhuận, Thành phố Hồ Chí Minh).
- Thành phần: olygalacturonase PGU: 10589; tỉ trọng: 1,163; tổng số vi khuẩn
sống/G: 100; coliform Bacteria/G<10; Enteropathogenic E.Coli: không phát hiện ;
Salmonella: không phát hiện.
- Khoảng pH tối thích để enzyme có hoạt tính cao nhất là từ 4-9.
- Bảo quản trong lọ kín, giữ ở nơi khô thoáng. Nhiệt độ bảo quản trong khoảng 0-
10oC.
2.1.3. Hóa chất.
Bảng 2.1. Danh sách hóa chất sử dụng trong nghiên cứu.
Công thức hóa
Tên hóa chất Xuất xứ Mục đích sử dụng
học
Tăng hiệu suất quá
Pectinex Ultra SP-L Singapore
trình dịch hoá
Thuốc thử Folin- Xác định hàm lượng
Trung Quốc
Ciocalteu polyphenol tổng
Nhóm: Hành Tím Đen 26
Acid Gallic C7H6O5 Đức
Sodium carbonate Na2CO3 Trung Quốc
1,1-diphenyl-2-
C18 H12N5O6 Đức
picrylhydrazyl
Xác định khả năng
Trolox C14H18O4 Mỹ chống oxy hoá
Cồn 99o C2H5OH Trung Quốc
Chất chuẩn Quercetin Đức
Sodium nitrite NaNO2 Trung Quốc
Xác định hàm lượng
Aluminum Chloride AlCl3.6H2O flavonoid tổng
Trung Quốc
Hexahydrate
Sodium hydroxide NaOH Trung Quốc
2.2. Dung cụ và thiết bị.
Thiết bị Model Xuất Xứ
Cân phân tích 4 số lẻ Sartorius QUINTIX224-1S Đức
Cân phân tích 2 số lẻ Sartorius TE612/SN Đức
Máy sinh tố Philips HR - 2068 Trung Quốc
Máy đo quang UV-VIS Genesys 20 UV-Vis Mỹ
SHELLAB
Thiết bị sấy Mỹ
Model : 1330 FX
Tủ ủ ấm Đức
Nhóm: Hành Tím Đen 27
Một số dụng cụ thông thường khác như: erlen, becher, pipet, ống nghiệm, đũa thuỷ
tinh, cuvet thuỷ tinh...
2.3. Nội dung nghiên cứu.
2.3.1. Sơ đồ quy trình sản xuất hành tím đen từ hành tím.
Hành tím
Xử lý sơ bộ
Lên men
Hành tím đen
Hình 2.5. Sơ đồ quy trình sản xuất hành tím đen từ hành tím.
Thuyết minh quy trình
Nguyên liệu: Hành tím được nhập từ Sóc Trăng. Yêu cầu hành nguyên vẹn, không
dập nát, sâu mọt, chất lượng đạt đồng đều.
Xử lý sơ bộ: Hanh được làm sạch đất cát. Cắt bỏ phần rễ, cuống. Và tiến hành bóc vỏ
sản phẩm. Mục đích của công đoạn bóc vỏ là để làm giảm thời gian của quá trình lên
men hành tím đen từ hành tím tươi. Từ đó giúp tiết kiệm thời gian, chi phí sản xuất.
Lên men: Sau khi xử lý sơ bộ, ta tiến hành quá trình lên men hành tím tươi bằng máy
ủ với các thông số nhiệt độ, thời gian rõ ràng. Cụ thể, hành tím tươi sẽ được lên men ở
nhiệt độ 70 0 C, thời gian 21 ngày.
Nhóm: Hành Tím Đen 28
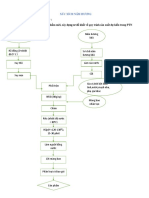
2.3.2. Sơ đồ quy trình sản xuất nước hành tím đen có gas.
Hành tím
Nghiền
Dịch hoá
Nước Đun sôi 89oC, 14 phút
Gừng
Làm nguội
Đun sôi Lọc
Rót chai
Lọc Soda, syrup
Phối chế
Hạ nhiệt độ 0-20 C, giữ trong 20
phút
Đóng chai
Dán nhãn
Sản phẩm
Thuyết minh quy trình
- Nghiền: Hành tím sau khi được lựa chọn được nghiền nhuyễn bằng máy xay.
- Dịch hoá: tiến hành dịch hoá tỏi đen với nước với tỉ lệ tỏi : nước. Khảo sát tỉ lệ hành
nước (1:5, 1:10, 1:15, 1:20, 1:25). Khảo sát nhiệt độ (40-45oC, 45-50 oC, 50-55 oC, 55
C-60, 60-65 oC), thời gian (10 phút, 20 phút, 30,phút, 40 phút, 50 phút), nồng độ
o
pectinase (0.05%, 0.1%, 0.15%, 0.2%,0.25%).
Nhóm: Hành Tím Đen 29
- Đun sôi: sau khi xử lý bằng enzyme pectinase, dịch hành đen được đun sôi ở 89oC
trong 14 phút nhằm mục đích vô hoạt enzyme pectinase.
- Lọc: Lọc dung dịch nước hành đen bằng giấy lọc, bỏ phần bã. Phần nước lọc được
sử dụng ở các công đoạn sau.
- Rót chai: Dịch hành đen sau khi lọc được pha loãng với nước có tỉ lệ là 1:3.
Sau đó rót vào chai 330 ml
- Phối chế: Độ Brix sản phẩm cố định là 11.
Gừng được bỏ sạch vỏ và thái nhỏ, sau đó được đun sôi trong nước với
tỉ lệ 1:1 trong 10 phút và để nguội. Tiến hành lọc bỏ phần bả và giữ
phần nước. Tỉ lệ hành:gừng là 1:0,3
Syrup đường được sử dụng với độ Brix là 60. Sử dụng 60g đường + 60
ml nước + 0.3% acid citric (tránh hiện tượng hồi đường), đun ở lửa lớn
đến khi sôi và tan hoàn toàn đường. Để nguội. Tỉ lệ hành:syup là 1:0,6
Soda: sử dụng soda Chương Dương với tỉ lệ hành:soda là 1:2.
- Hạ nhiệt độ: Sử dụng nước đá và muối hột để hạ nhiệt độ của nước hành đen
đã phối chế. Nước hành đen sau khi phối chế được hạ xuống nhiệt độ 0-20 C và
giữ ở 20 phút.
Mục đích: Bảo hòa CO2 và tiêu diệt vi sinh vật.
- Đóng chai:
- Dán nhãn: Dán nhãn bao bì, hoàn thiện sản phẩm.
Nhóm: Hành Tím Đen 30
2.3.3. Sơ đồ bố trí thí nghiệm.
Xác định hàm lượng
Nguyên liệu
polyphenol, flavonoid
tổng
Hành tím Vĩnh Châu
Khả năng chống oxy hoá
theo phương pháp DPPH
Khảo sát các thông số trong giai Xác định hàm lượng
đoạn dịch hoá polyphenol, flavonoid tổng
Khảo sát 4 thông số: tỉ lệ tỏi đen : Khả năng chống oxy hoá theo
nước, nhiệt độ, thời gian, % phương pháp DPPH
enzyme pectinse bổ sung.
Cảm quan Mức độ chấp nhận sản phẩm
nước hành đen của người tiêu
Sản phẩm: nước tỏi đen dùng.
Kiểm nghiệm vi sinh
Tổng số vi khuẩn hiếu khí
Coliforms
E.coli
S.aureus
Cl.perfringens
Streptococci feacal
Pseudomonas aeruginosa
Tổng số bào tử nấm men, nấm mốc
Nhóm: Hành Tím Đen 31
2.3.4. Khảo sát ảnh hưởng của tỷ lệ dịch chiết đến các hoạt tính chống oxy hóa
của sản phẩm.
Mục đích: Xác định tỷ lệ dịch chiết để trích ly các hợp chất có hoạt tính chống
oxy hóa từ hành đen với hàm lượng cao nhất.
Tiến hành:
- Hành được nghiền nhỏ với nước với tỉ lệ 1:15 (Cho từ từ nước vào và
nghiền)
- Cho 0.1% enzyme pectinase vào hành đã nghiền.
- Đem ủ với từng nhiệt độ trên bảng thí nghiệm.
- Thời gian ủ: 20 phút.
- Sau khi ủ xong dịch hành được lọc và đun bất hoạt ở 89 o C trong 14 phút.
Bảng 2.3: Bố trí thí nghiệm với yếu tố khảo sát là tỷ lệ dịch chiết
Mẫu 1 2 3 4
Tỷ lệ hành:nước 1:5 1:10 1:15 1:20
Thông số cố định:
Tỷ lệ enzymes pectinase 0.1%
Nhiệt độ: 40-45oC
Thời gian: 20 phút
Khối lượng mẫu ban đầu: 5 g hành đen
Thời gian và nhiệt độ bất hoạt: 14 phút – 89o C
Chỉ tiêu đo đạc:
Hoạt tính chống oxy hóa
Hàm lượng Polyphenol tổng
Hàm lượng Flavonoid tổng
Mỗi nghiệm thức được lặp lại 3 lần.
Hàm lượng các chất chống oxy hóa của dịch trích sẽ được xác định sau mỗi thí
nghiệm trích ly.
Nhóm: Hành Tím Đen 32
Điều kiện trích ly nào cho kết quả hàm lượng các chất chống oxy hóa cao nhất sẽ
được chọn để tiếp tục tiến hành nghiên cứu.
2.3.5. Thí nghiệm 2: Khảo sát ảnh hưởng của nhiệt độ lên đến các hoạt tính
chống oxy hóa của sản phẩm.
Mục đích: Xác định nhiệt độ dịch hóa thích hợp nhất để thu được các hợp chất có
hoạt tính chống oxy hóa từ hành đen với hàm lượng cao nhất.
Bảng 2.4: Bố trí thí nghiệm với yếu tố khảo sát là nhiệt độ ủ.
Mẫu M1 M2 M3 M4
Nhiệt độ (o C) 40-45 45-50 50-55 55-60
Cách thực hiện chuẩn bị mẫu
- Hành được nghiền nhỏ với nước với tỉ lệ 1:15 (Cho từ từ nước vào và nghiền)
- Cho 0.1% enzyme pectinase vào hành đã nghiền.
- Đem ủ với từng nhiệt độ trên bảng thí nghiệm.
- Thời gian ủ : 20 phút.
- Sau khi ủ xong dịch hành được lọc và đun bất hoạt ở 89 o C trong 14 phút.
Thông số cố định:
Tỷ lệ enzymes pectinase 0.1%
Thời gian: 20 phút
Tỉ lệ hành nước được cố định từ thí nghiệm 1.
Khối lượng mẫu ban đầu: 5 g hành đen
Chỉ tiêu đo đạc:
Hoạt tính chống oxy hóa
Hàm lượng Polyphenol tổng
Hàm lượng Flavonoid tổng
Mỗi nghiệm thức được lặp lại 3 lần.
Hàm lượng các chất chống oxy hóa của dịch trích sẽ được xác định sau mỗi thí
nghiệm trích ly.
Nhóm: Hành Tím Đen 33
Điều kiện trích ly nào cho kết quả hàm lượng các chất chống oxy hóa cao nhất sẽ
được chọn để tiếp tục tiến hành nghiên cứu.
2.3.6. Thí nghiệm 3: Khảo sát ảnh hưởng của thời gian ủ enzyme đến các hoạt
tính chống oxy hóa của sản phẩm.
Mục đích: Xác định thời gian dịch hóa thích hợp nhất để thu được các hợp chất có
hoạt tính chống oxy hóa từ hành đen với hàm lượng cao nhất.
Bảng 2.5: Bố trí thí nghiệm với yếu tố khảo sát là thời gian ủ.
Mẫu M1 M2 M3 M4
Thời gian (phút) 10 20 30 40
Cách thực hiện chuẩn bị mẫu
- Hành được nghiền nhỏ với nước với tỉ lệ 1:15 (Cho từ từ nước vào và nghiền)
- Cho 0.1% enzyme pectinase vào hành đã nghiền.
- Đem ủ với từng nhiệt độ được xác định từ thí nghiệm 2.
- Thời gian ủ được thực hiện theo bảng 2.5
Thông số cố định:
Tỷ lệ enzymes pectinase 0.1%
Nhiệt độ ủ: Thí nghiệm 2
Tỉ lệ hành nước được cố định từ thí nghiệm 1.
Khối lượng mẫu ban đầu: 5 g hành đen
Chỉ tiêu đo đạc:
Hoạt tính chống oxy hóa
Hàm lượng Polyphenol tổng
Hàm lượng Flavonoid tổng
Mỗi nghiệm thức được lặp lại 3 lần.
Hàm lượng các chất chống oxy hóa của dịch trích sẽ được xác định sau mỗi thí
nghiệm trích ly.
Nhóm: Hành Tím Đen 34
Điều kiện trích ly nào cho kết quả hàm lượng các chất chống oxy hóa cao nhất sẽ
được chọn để tiếp tục tiến hành nghiên cứu.
2.3.7. Thí nghiệm 4: Khảo sát ảnh hưởng của nồng độ enzyme đến các hoạt tính
chống oxy hóa của sản phẩm.
Mục đích: Xác định nồng độ enzymes trong quá trình dịch hóa thích hợp nhất để
thu được các hợp chất có hoạt tính chống oxy hóa từ hành đen với hàm lượng cao
nhất.
Bảng 2.6: Bố trí thí nghiệm với yếu tố khảo sát là nồng độ enzymes.
Mẫu M1 M2 M3 M4
Nồng độ (%) 0,1 0,15 0,2 0,25
Cách thực hiện chuẩn bị mẫu
- Hành được nghiền nhỏ với nước với tỉ lệ từ thí nghiệm 1
- Đem ủ với từng nhiệt độ được xác định từ thí nghiệm 2.
- Thời gian ủ: thí nghiệm 3.
- Nồng độ enzymes sẽ được thực hiện theo bảng 2.6
Thông số cố định:
Nhiệt độ ủ: Thí nghiệm 2
Tỉ lệ hành nước được cố định từ thí nghiệm 1.
Thời gian ủ: thí nghiệm 3
Khối lượng mẫu ban đầu: 5 g hành đen
Chỉ tiêu đo đạc:
Hoạt tính chống oxy hóa
Hàm lượng Polyphenol tổng
Hàm lượng Flavonoid tổng
Mỗi nghiệm thức được lặp lại 3 lần.
Hàm lượng các chất chống oxy hóa của dịch trích sẽ được xác định sau mỗi thí
nghiệm trích ly.
Nhóm: Hành Tím Đen 35
Điều kiện trích ly nào cho kết quả hàm lượng các chất chống oxy hóa cao nhất sẽ
được chọn để tiếp tục tiến hành nghiên cứu.
2.3.8. Thí nghiêm 5: Khảo sát mức độ chấp nhận của người tiêu dùng đối với sản
phẩm.
Mục đích: Xác định được mức độ chấp nhận của người tiêu dùng đối với sản
phẩm.
Số người tối thiểu: 30 người.
Phương pháp: Phương pháp thị hiếu sử dụng thang điểm 9.
Bảng 2.7: Bảng mô tả thí nghiệm.
Xin chào anh, chị, chúng tôi đến từ Viện Công nghệ Sinh học – Thực phẩm trường
Đại học Công nghiệp thành phố Hồ Chí Minh. Hôm nay chúng tôi thực hiện khảo sát
người tiêu dùng để phát triển một sản phẩm mới. Câu trả lời của anh chị có vai trò rất
quan trọng đối với chúng tôi. Mong anh, chị dành chút thời gian giúp chúng tôi hoàn
thành khảo sát này
Xin chân thành cảm ơn Anh / Chị!
PHIẾU HƯỚNG DẪN ĐÁNH GIÁ
Anh / Chị sẽ nhận 1 mẫu nước. Hãy thử nếm mẫu và đánh giá mức độ ưa thích của
Anh / Chị đối với mẫu này bằng cách cho điểm trên thang dưới đây. Ghi nhận câu trả
lời của Anh / Chị vào phiếu trả lời.
Lưu ý: Mỗi mẫu thử ứng với 1 phiếu trả lời và đưa lại cho thực nghiệm viên ngay khi
Anh / Chị trả lời xong. Anh / Chị súc miệng bằng nước lọc trước khi thử mẫu và bất
cứ khi nào Anh / Chị thấy cần thiết. Trong quá trình đánh giá thị hiếu, Anh / Chị vui
lòng không trao đổi ý kiến với những người tham gia đánh giá khác. Mọi thắc mắc
liên hệ người hướng dẫn.
Thang thị hiếu 9 điểm:
□ □ □ □ □ □ □ □ □
1 2 3 4 5 6 7 8 9
Mức độ ưa thích được biểu thị thang điểm 1-9 tương ứng với:
1: Cực kỳ không thích 6: Hơi thích
2: Rất không thích 7: Tương đối thích
Nhóm: Hành Tím Đen 36
3: Tương đối không thích 8: Rất thích
4: Hơi không thích 9: Cực kỳ thích
5: Bình thường
Cảm ơn sự đóng góp của Anh / Chị trong buổi đánh giá hôm nay của chúng tôi!
PHIẾU TRẢ LỜI
Mã số người thử: Ngày thử: / 4 / 2019
Mã số mẫu:
Caau1: Cảm nhận của Anh /Chị về màu sắc của sản phẩm:
□ □ □ □ □ □ □ □ □
1 2 3 4 5 6 7 8 9
Câu 2: Cảm nhận của Anh /Chị về mùi của sản phẩm:
□ □ □ □ □ □ □ □ □
1 2 3 4 5 6 7 8 9
Câu 3: Cảm nhận của Anh /Chị về vị của sản phẩm:
□ □ □ □ □ □ □ □ □
1 2 3 4 5 6 7 8 9
Câu 4: Cảm nhận của Anh /Chị về độ ngọt của sản phẩm:
□ □ □ □ □ □ □ □ □
1 2 3 4 5 6 7 8 9
Câu 5: Cảm nhận của Anh /Chị về hậu vị của sản phẩm:
□ □ □ □ □ □ □ □ □
1 2 3 4 5 6 7 8 9
Câu 6: Cảm nhận của Anh /Chị về trạng thái của sản phẩm:
□ □ □ □ □ □ □ □ □
1 2 3 4 5 6 7 8 9
Câu 7: Cảm nhận của Anh /Chị về nồng độ CO2 của sản phẩm:
□ □ □ □ □ □ □ □ □
1 2 3 4 5 6 7 8 9
Nhóm: Hành Tím Đen 37
Câu 8: Cảm nhận của Anh /Chị về mẫu mã, nhãn của sản phẩm:
□ □ □ □ □ □ □ □ □
1 2 3 4 5 6 7 8 9
Câu 9: Cảm nhận của Anh /Chị về hình thức của sản phẩm:
□ □ □ □ □ □ □ □ □
1 2 3 4 5 6 7 8 9
Câu 10: Mức độ ưa thích sản phẩm của Anh/Chị về sản phẩm:
□ □ □ □ □ □ □ □ □
1 2 3 4 5 6 7 8 9
2.4. Phương pháp phân tích
Chuẩn bị 5g hành đen trên một mẫu phân tích để khảo sát các yếu tố trong giai
đoạn trích ly. Tiến hành xay nhuyễn, trích ly, lọc và phân tích.
Xác định hàm lượng flavonoid [3]
Xác định hàm lượng flavonoid tổng trong dịch chiết hành bằng phương pháp so
màu với dung dịch AlCl3 trong môi trường kiềm.
Cách tiến hành: Dịch trích ly được pha loãng tới nồng độ thích hợp.
Bảng 3.2: Các bước tiến hành để xác định hàm lượng flavonoid tổng
Ống 0 Ống 1
Nước cất (ml) 2 2
Dịch mẫu (ml) 0 1
NaNO2 0,15M (ml) 0,15 0,15
Đợi 5 phút
AlCl3.6H2O 0,4M (ml) 0,15 0,15
Đợi 5 phút
NaOH 1M (ml) 1 1
Đợi 15 phút
Nhóm: Hành Tím Đen 38
Nước cất (ml) 6.5 5.5
- Cường độ hấp thụ ánh sáng được đo ở bước sóng 415nm.
- Thí nghiệm được lăp lại 3 lần.
- Chỉ tiêu đánh giá: Hàm lượng flavonoid được tính toán từ đường chuẩn được xây
dựng bằng quercetin và kết quả được thể hiện bằng miligam quercetin (𝐶15 𝐻10 𝑂7 )
tương đương trong 1 g sản phẩm.
Xác định hàm lượng polyphenol tổng [4]
Hàm lượng Polyphenol tổng số của dịch chiết hành đen được xác định bằng
phương pháp Folin – Ciocalteu.
- Cách tiến hành: Dịch trích ly được pha loãng tới nồng độ thích hợp.
Bảng 3.3: Các bước tiến hành để xác định hàm lượng polyphenol tổng
Ống 0 Ống 1
Mẫu (ml) 0 1
Thuốc thử Folin (ml) 2 2
Na2CO3 1M (ml) 1 1
Để yên 1 phút
Nước cất (ml) 7 6
- Đậy kín để trong bóng tối để ở nhiệt độ phòng trong 30 phút.
- Sau đó tiến hành đo quang phổ với độ hấp thụ ở 750nm.
- Thí nghiệm được lặp lại 3 lần.
- Chỉ tiêu đánh giá: Tổng hàm lượng polyphenol được thể hiện bằng miligam đương
lượng acid gallic (mg GAE/g chất khô).
Xác định hoạt tính chống oxy hóa [5]
Nhóm: Hành Tím Đen 39
Là phương pháp được xác định theo phương pháp của Brand-Williams et al.
(1995) với một vài hiệu chỉnh nhỏ. Khả năng bắt gốc tự do DPPH được thể hiện
thông qua sự giảm độ hấp thu ở bước sóng 517nm, do gốc DPPH bị khử bởi các
thành phần kháng oxy hóa trong mẫu khảo sát.
Nguyên tắc:
DPPH (2,2-diphenyl-1-picrylhydrazyl) là một gốc tự do bền có màu tím đậm.
Dung dịch DPPH có cực đại hấp thu tại bước sóng 517 nm và sản phẩm khử của nó là
2,2-diphenyl-1-picrylhydrazine (DPPH-H) có màu vàng nhạt. Các chất có khả năng
kháng oxy hóa sẽ trung hòa gốc tự do DPPH bằng cách cho hydro, đình chỉ quá trình
oxy hóa bằng sự chuyển các gốc tự do sang trạng thái ổn định hơn, làm giảm độ hấp
thu tại bước sóng cực đại và màu của dung dịch sẽ nhạt dần, chuyển từ tím sang vàng
nhạt.
Hình 3.3: Cơ chế hoạt động của DPPH và chất kháng oxy hóa
Cách tiến hành
Chuẩn bị mẫu dịch chiết: từ dịch trích ly hành: nước là 1:10 (w:v), tiếp tục pha
loãng lần 2 theo tỷ lệ hành: nước là 1:2 (w:v).
Hút 0,2 ml dịch mẫu cho vào ống nghiệm, thêm vào đó 0,5 ml (0,2 mM). Lắc
mạnh hỗn hợp rồi để yên trong bóng tối ở nhiệt độ phòng. Sau 30 phút đo độ hấp thụ
ở bước sóng 517 nm.
Làm mẫu kiểm chứng: làm tương tự mẫu thí nghiệm trong đó dịch chiết được
thay bằng nước cất.
Xử lí kết quả
Khả năng khử gốc tự do DPPH được xác định theo công thức sau:
Nhóm: Hành Tím Đen 40
DPPH (%) = 100 x (ACT – ASP)/ACT
Trong đó:
ACT: Độ hấp thu quang học của mẫu trắng không chứa dịch chiết.
ASP: Độ hấp thu quang học của mẫu có chứa dịch chiết.
Giá trị phần trăm ức chế các gốc tự do thu được thể hiện khả năng chống lại các
gốc tự do gây bệnh trong cơ thể. Vì vậy, giá trị phần trăm càng cao thì hoạt tính
chống oxy hóa càng mạnh.
Nhóm: Hành Tím Đen 41
You might also like
- NHóm 8 tảoDocument15 pagesNHóm 8 tảoTrịnh Tú SươngNo ratings yet
- Sinh Ly Benh Thu yDocument230 pagesSinh Ly Benh Thu yapi-3773922100% (2)
- phát hiện và phòng chống HIVDocument32 pagesphát hiện và phòng chống HIVPham Anh ToanNo ratings yet
- Chan Doan Benh Thu yDocument114 pagesChan Doan Benh Thu yapi-3773922No ratings yet
- ứng dụng của enzyme trong nông nghiệpDocument2 pagesứng dụng của enzyme trong nông nghiệpLe MinhchucNo ratings yet
- Giáo trình An toàn vệ sinh thực phẩm - 1118488Document158 pagesGiáo trình An toàn vệ sinh thực phẩm - 1118488Nguyễn ThuNo ratings yet
- (123doc) Phan Lap Va Tuyen Chon Cac Chung Xa Khuan Streptomyces SP Doi Khang Nam Fusarium OxysporumDocument60 pages(123doc) Phan Lap Va Tuyen Chon Cac Chung Xa Khuan Streptomyces SP Doi Khang Nam Fusarium OxysporumPhương NguyễnNo ratings yet
- Trái cây và Rau củ lên men ở Châu Á: Một nguồn men vi sinh (probiotic) tiềm năng- Báo khoa họcDocument39 pagesTrái cây và Rau củ lên men ở Châu Á: Một nguồn men vi sinh (probiotic) tiềm năng- Báo khoa họcNam NguyenHoangNo ratings yet
- Ngộ độc do Histamin trong cá biểnDocument2 pagesNgộ độc do Histamin trong cá biểnThuan NguyenNo ratings yet
- Copy of Sinh Lí Động Vật-2014Document29 pagesCopy of Sinh Lí Động Vật-2014Lương NhưNo ratings yet
- tách chiết và phân lập pectinaseDocument4 pagestách chiết và phân lập pectinaseJumi CornNo ratings yet
- Đề Cương Ôn Tập KHTP (AutoRecovered)Document23 pagesĐề Cương Ôn Tập KHTP (AutoRecovered)Lý Hoàng Thị ThuNo ratings yet
- TLDocument63 pagesTLlenangxipamNo ratings yet
- 2 - 2 - CCWG - Bien Doi Khi Hau - Tac Dong Kha Nang Ung Pho Va Mot So Van de Chinh Sach 2011 PDFDocument116 pages2 - 2 - CCWG - Bien Doi Khi Hau - Tac Dong Kha Nang Ung Pho Va Mot So Van de Chinh Sach 2011 PDFphandungNo ratings yet
- Những Hợp Chất Chứa Lưu Huỳnh Trong Thực Vật & Khả Năng Phòng Chống Bệnh Tật -Tai TailieutuoiDocument57 pagesNhững Hợp Chất Chứa Lưu Huỳnh Trong Thực Vật & Khả Năng Phòng Chống Bệnh Tật -Tai TailieutuoiNam NguyenHoangNo ratings yet
- STREPTOMYCESDocument77 pagesSTREPTOMYCESTran Do Khoa TienNo ratings yet
- Truyen Giong Nhan Tao Vat NuoiDocument194 pagesTruyen Giong Nhan Tao Vat Nuoivantruong0210No ratings yet
- Acid Folic (Vitamin B9), B12 - Môn Dinh Dư NG Ngư IDocument23 pagesAcid Folic (Vitamin B9), B12 - Môn Dinh Dư NG Ngư INam NguyenHoangNo ratings yet
- Phương pháp nghiên cứu khoa học- sữa chua thanh longDocument29 pagesPhương pháp nghiên cứu khoa học- sữa chua thanh longXanh NgọcNo ratings yet
- Do An Tra Tui Loc Kho Qua AtisoDocument39 pagesDo An Tra Tui Loc Kho Qua AtisoTrân Lê100% (2)
- Enzyme ProteaseDocument44 pagesEnzyme ProteaseMy Minhon100% (4)
- Uống nước sinh tố: Phương pháp kỳ diệu - bảo vệ sức khỏe và trị liệu bệnh tật.From EverandUống nước sinh tố: Phương pháp kỳ diệu - bảo vệ sức khỏe và trị liệu bệnh tật.No ratings yet
- TomtatDocument14 pagesTomtat:V ĐạtNo ratings yet
- Cơ chế xúc tác và ứng dụng của enzym proteaseDocument37 pagesCơ chế xúc tác và ứng dụng của enzym proteaseĐaminh Hoàng Linh40% (5)
- Tong Quan Khao Sat Thanh Phan Hoa Hoc Cay Giao Co LamDocument15 pagesTong Quan Khao Sat Thanh Phan Hoa Hoc Cay Giao Co LamLiễu NguyễnNo ratings yet
- FILE - 20210608 - 100325 - N2 - Tía TôDocument11 pagesFILE - 20210608 - 100325 - N2 - Tía TôKhoa NobiNo ratings yet
- Tinh B T Khoai Tây 1Document43 pagesTinh B T Khoai Tây 1Cẩm TúNo ratings yet
- ppnckh- hoàn chỉnhDocument5 pagesppnckh- hoàn chỉnhBảo Trân Lâm HuỳnhNo ratings yet
- Tiểu luận về enzyme proteaseDocument14 pagesTiểu luận về enzyme proteasely đàoNo ratings yet
- Cong Nghe Enzyme SX Proteaza Tu VSVDocument14 pagesCong Nghe Enzyme SX Proteaza Tu VSVTruc DuongNo ratings yet
- Marinedrugs 12 03487Document29 pagesMarinedrugs 12 03487Tú Lê AnhNo ratings yet
- Tong Quan FinalDocument23 pagesTong Quan FinalHieu PhamNo ratings yet
- bản tổng hợpDocument8 pagesbản tổng hợply đàoNo ratings yet
- Thanh Trâm 20S2010011Document11 pagesThanh Trâm 20S2010011Trâm ThanhNo ratings yet
- Đ Án PectinDocument34 pagesĐ Án PectinBinh Nguyen100% (1)
- Nghien Cuu Pectin Va Ung Dung Trong Cong Nghe Thuc Pham B6uwE 20130225083758 19Document34 pagesNghien Cuu Pectin Va Ung Dung Trong Cong Nghe Thuc Pham B6uwE 20130225083758 19Minh DũngNo ratings yet
- 9 (50) - Nghiên cứu đề xuất quy trình sản xuất bột chanh dây (Passiflora edulis) (Lê Văn Thuận) 31Document9 pages9 (50) - Nghiên cứu đề xuất quy trình sản xuất bột chanh dây (Passiflora edulis) (Lê Văn Thuận) 31Nguyễn Hữu HiệpNo ratings yet
- Nghiên cứu chiết tách xác định một số thành phần hóa học trong dịch chiết lá lốt ở huyện hòa vang tp đà nẵngDocument44 pagesNghiên cứu chiết tách xác định một số thành phần hóa học trong dịch chiết lá lốt ở huyện hòa vang tp đà nẵngnguyenvietphuoc22No ratings yet
- Đề Tài Quy Trình Sản Xuất Nước Chanh Dây Lên MenDocument10 pagesĐề Tài Quy Trình Sản Xuất Nước Chanh Dây Lên MenPhanTrọngHùngNo ratings yet
- Ta Thi Thuy Trang - 2305102054 - Duoc K7Document17 pagesTa Thi Thuy Trang - 2305102054 - Duoc K7nguyenmaihoaiquanNo ratings yet
- Hệ thống nuôi cấy tảo Spirulina Platensis thông minh finalDocument15 pagesHệ thống nuôi cấy tảo Spirulina Platensis thông minh finalHương GiangNo ratings yet
- Do An 2Document29 pagesDo An 2Tran Hoai NamNo ratings yet
- T NG Quan NG D NGDocument3 pagesT NG Quan NG D NGdatthptkm1No ratings yet
- Rong BienDocument42 pagesRong Biensaomai491No ratings yet
- BÁo Cáo Thực Tập Đề Tài Rau Đắng Biển Đang Sửa Bản CupoiDocument28 pagesBÁo Cáo Thực Tập Đề Tài Rau Đắng Biển Đang Sửa Bản CupoiBình PhạmNo ratings yet
- Sesuvium Portulacastrum 1Document4 pagesSesuvium Portulacastrum 1Trần Thiện TàiNo ratings yet
- BÁO CÁO GIỚI THIỆU NGÀNH 1.9Document21 pagesBÁO CÁO GIỚI THIỆU NGÀNH 1.9Lâm Hồng NgọcNo ratings yet
- De Cuong Tuan AnhDocument20 pagesDe Cuong Tuan AnhHo Le PhucNo ratings yet
- GTDinh Duong TAGSDocument142 pagesGTDinh Duong TAGSnothing2902No ratings yet
- Cay đỏ ngọnDocument111 pagesCay đỏ ngọnNguyen Tien HoaNo ratings yet
- Quá Trình Trích Ly Trà TH o M CDocument20 pagesQuá Trình Trích Ly Trà TH o M CHoàng ĐăngNo ratings yet
- Cncbtp Thứ 5 Tiết1-3Document17 pagesCncbtp Thứ 5 Tiết1-3Huy Huỳnh ĐăngNo ratings yet
- Poly PhenolDocument22 pagesPoly Phenoltronghieu010383No ratings yet
- Bìa HsinhDocument29 pagesBìa HsinhNgọc NhớNo ratings yet
- nộp thầy lần 1Document17 pagesnộp thầy lần 1NguyễnNgọcThànhDanhNo ratings yet
- Chiết Tách Hợp Chất Hesperidin Và Naringin Trong Vỏ CamDocument5 pagesChiết Tách Hợp Chất Hesperidin Và Naringin Trong Vỏ CamNam NguyenHoangNo ratings yet
- LVThs - Pham Thi Thanh An 6592Document26 pagesLVThs - Pham Thi Thanh An 6592Tran Ba LuanNo ratings yet
- HoTruongQuynhChau TTDocument23 pagesHoTruongQuynhChau TTHoà BìnhNo ratings yet
- Quy Trinh SX AtisoDocument23 pagesQuy Trinh SX AtisoBang BangNo ratings yet
- Luận Văn - Nghiên Cứu Sản Xuất Nước Uống Đóng Chai Từ Hoa Atiso - Lá Lạc Tiên Tây - 949820Document100 pagesLuận Văn - Nghiên Cứu Sản Xuất Nước Uống Đóng Chai Từ Hoa Atiso - Lá Lạc Tiên Tây - 949820Ngô Kim NgânNo ratings yet
- 06a MẪU ĐƠN MƯỢN PHÒNG THIẾT BỊ DỤNG CỤ SV ĐỒ ÁN 2017Document4 pages06a MẪU ĐƠN MƯỢN PHÒNG THIẾT BỊ DỤNG CỤ SV ĐỒ ÁN 2017Duy Tân NguyễnNo ratings yet
- Joinpdf PDFDocument180 pagesJoinpdf PDFDuy Tân NguyễnNo ratings yet
- Danh Gia CM Quan THC PHMDocument29 pagesDanh Gia CM Quan THC PHMDuy Tân NguyễnNo ratings yet
- QCVN 6 2 PDFDocument6 pagesQCVN 6 2 PDFDuy Tân NguyễnNo ratings yet
- De Cuong PTSPDocument29 pagesDe Cuong PTSPDuy Tân NguyễnNo ratings yet
- TL luật TPDocument130 pagesTL luật TPDuy Tân NguyễnNo ratings yet
- Quản Lý Chuỗi Cung Ứng Trong Chuỗi Thức ĂnDocument8 pagesQuản Lý Chuỗi Cung Ứng Trong Chuỗi Thức ĂnDuy Tân NguyễnNo ratings yet
- TL luật TPDocument33 pagesTL luật TPDuy Tân NguyễnNo ratings yet
- Giao Trinh Cong Nghe San Xuat Cac San Pham Tu Sua Va Thuc Uong Pha Che Tap 1 Cong Nghe San Xuat Cac San Pham Tu Sua Le Van Viet Man PDFDocument337 pagesGiao Trinh Cong Nghe San Xuat Cac San Pham Tu Sua Va Thuc Uong Pha Che Tap 1 Cong Nghe San Xuat Cac San Pham Tu Sua Le Van Viet Man PDFDuy Tân NguyễnNo ratings yet
- DPPH 3 LuanVan-LeThiTuAnh-2012 PDFDocument73 pagesDPPH 3 LuanVan-LeThiTuAnh-2012 PDFDuy Tân NguyễnNo ratings yet
- CNCB Sua DH PDFDocument56 pagesCNCB Sua DH PDFDuy Tân NguyễnNo ratings yet