Professional Documents
Culture Documents
المحور 3 الصناعة الصيدلانية
المحور 3 الصناعة الصيدلانية
Uploaded by
Abdou IslemCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
المحور 3 الصناعة الصيدلانية
المحور 3 الصناعة الصيدلانية
Uploaded by
Abdou IslemCopyright:
Available Formats
هندســة الطـرائق /تحضيـــــــر 1
األسبريــــــن .
..تحضيـــــر األســـبريــــن
)1تمهــــــيد.
استخدم اإلنسان في العصور القديمة أوراق شجر الصفصاف التي تع الج الص داع و آالم الحمى ,وق د تمكن الكيمي ائيون من
استخالص المادة الفعالة الموجودة في هذا النبات عبر سلسلة من األبحاث .لذلك ق اموا باس تخالص حمض الساليس يليك ،ه ذا
المركب أساسي لتحضير حمض األستيل ساليسيليك (االسم العلمي لألسبرين) .في سنة 1860تم تركيب حمض الساليس يليك
انطالقا من الفينول و ثاني أكسيد الكربون كما بدأ تسويق األسبرين لدى الصيدليات العالمي ة س نة 1899من ط رف مؤسس ة
باير ( ) Bayerاأللمانية.
ال يزال األسبرين يحتل المرتبة األولى في مبيعات األدوية إذ بلغ معدل استهالك األسبرين أكثر من 40000طن سنويا.
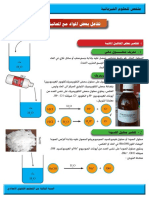
تحضــــير األسبريـــــــن. )2
المرحلة األولــــــى :تحضير حمض الساليسيليك. .1.2
يتفاعل الفينول C6H5OHمع الصود NaOHفتتشكل فينات الصوديوم C6H5ONaوال تي تتح ول إلى مس حوق ن اعم,
ثم يعالج هذا األخير بثاني أكسيد الكربون CO2مع الحرارة و الضغط المرتفعين وهذا لتشكيل ساليسيالت الص وديوم و يتم
استرجاع الكحول المتبقي.
يزال لون ساليسيالت الصوديوم المنحلة في الماء بتمريرها على الفحم النشيط . Charbon actif
المرحلة الثانـــية :التفاعل بين حمض الساليسيليك و بالماء حمض االيثانويك )بالماء حمض الخل( .2.2
يسخن المزيج (حمض الساليسيليك و بالماء حمض الخل) عند حوالي C°90فيتشكل حمض األس تيل ساليس يليك ,لم ا نق وم
بتبريد مزيج التفاعل يترسب حمض األس تيل ساليس يليك على ش كل بل ورات كب يرة الحجم وال تي تفص ل بطريق ة الترش يح.
تغسل هذه البلورات وتجفف لنحصل على األسبرين ,يعلب ه ذا األخ ير على أش كال مختلف ة و ق د تض اف م واد كالنش اء أو
بيكاربونات الصوديوم حسب ا ِالستعمال المناسب.
-المعادلـة الكيميائيـة لتحضـــير األسبريــن:
O O
OH CH3
H3C O
+ O O + H3C
H3C OH
COOH COOH
O
حمض الخل + األسبرين بالماء حمض الخل + حمض الساليسيليك
You might also like
- الأسبرين هو أحد أشهر الأدوية وأكثرها شعبيةDocument3 pagesالأسبرين هو أحد أشهر الأدوية وأكثرها شعبيةطاهر سعيدة100% (1)
- الاسبرينDocument5 pagesالاسبرينالشريف الملاحNo ratings yet
- مقدمة في الاحماض والقواعدDocument59 pagesمقدمة في الاحماض والقواعدHossam SaadNo ratings yet
- محاضرة الكربوهيدرات PDFDocument61 pagesمحاضرة الكربوهيدرات PDFsalemana1972No ratings yet
- ةـــــــــــــــــــــيليسكوبركلا ضامحألا Carboxylic acid: ةــــيمستلا:الوأ ةــــــيماظنلا IupacDocument14 pagesةـــــــــــــــــــــيليسكوبركلا ضامحألا Carboxylic acid: ةــــيمستلا:الوأ ةــــــيماظنلا IupacAYLANo ratings yet
- CourDocument16 pagesCourALI ZWAWINo ratings yet
- 10Document5 pages10e.maskarNo ratings yet
- حمض السلفونيكDocument8 pagesحمض السلفونيكhdhossam274No ratings yet
- الربط والاثراء 2023Document7 pagesالربط والاثراء 2023zabdullahstud1No ratings yet
- الاحماض الكربوكسيلية الاليفاتية والاروماتيةDocument14 pagesالاحماض الكربوكسيلية الاليفاتية والاروماتيةHesham El-RoussassiNo ratings yet
- نبذة تارخية حول الأسبرينDocument8 pagesنبذة تارخية حول الأسبرينaekpcmassina00000No ratings yet
- تحديد الكافيئين وحمض البنزويك في المشروبات الغازيةDocument3 pagesتحديد الكافيئين وحمض البنزويك في المشروبات الغازيةMoradoo MorNo ratings yet
- UntitledDocument72 pagesUntitledمحمد طاهرNo ratings yet
- عرض بوربوينتDocument12 pagesعرض بوربوينتsuhailradain975No ratings yet
- الوحدة 06 الأسترةDocument12 pagesالوحدة 06 الأسترةmaadzha14No ratings yet
- لمحة تاريخية عن الأسبيرينDocument11 pagesلمحة تاريخية عن الأسبيرينuchiha alaa100% (4)
- ملزمة الأحماض والقواعد الجديدة 2023Document56 pagesملزمة الأحماض والقواعد الجديدة 2023محمد طاهرNo ratings yet
- الأسبيرينDocument4 pagesالأسبيرينcyberanoir90No ratings yet
- موضوع في الكيمياءDocument1 pageموضوع في الكيمياءSheikh Al-shoteriNo ratings yet
- Semiconductor MaterialsDocument4 pagesSemiconductor Materialsshahadhaider902No ratings yet
- المعادلات الكيميائيةDocument22 pagesالمعادلات الكيميائيةJannat MahmoodNo ratings yet
- 532703999 الاحماض الكربوكسيلية الاليفاتية والاروماتيةDocument15 pages532703999 الاحماض الكربوكسيلية الاليفاتية والاروماتيةA HNo ratings yet
- محاضرات الكيمياء اللاعضويةDocument32 pagesمحاضرات الكيمياء اللاعضويةhagshhsiauhagah516525No ratings yet
- مراجعة فسيولوجي تحولات ناتجات ثانويةDocument52 pagesمراجعة فسيولوجي تحولات ناتجات ثانويةMahmoidNo ratings yet
- مشروع حول الاسبيرينDocument8 pagesمشروع حول الاسبيرينbacdz hadji100% (1)
- ترجمه كيمياء عملي المحاضره الثالثهDocument11 pagesترجمه كيمياء عملي المحاضره الثالثهمنوعاتNo ratings yet
- Carbohydrate+ +mono+2Document31 pagesCarbohydrate+ +mono+2Yassmin AlarinyNo ratings yet
- 3 CarbohydrateSPUDocument29 pages3 CarbohydrateSPUusama zedanNo ratings yet
- 3 نوبل 2024 كيمياء عضوية درس 3 الميثان 25-04-2023Document13 pages3 نوبل 2024 كيمياء عضوية درس 3 الميثان 25-04-2023Elostaz Educational ChannelNo ratings yet
- الاسبرينDocument5 pagesالاسبرينابتسم فأنت معيNo ratings yet
- الماء و المحاليل المائيةDocument27 pagesالماء و المحاليل المائيةapi-373180488% (8)
- D8a7d984d982d988d8a7d8b9d8af 2020 1Document197 pagesD8a7d984d982d988d8a7d8b9d8af 2020 1jaafarmousa38No ratings yet
- Pubdoc 10 20734 1405Document3 pagesPubdoc 10 20734 1405محمد العراقيNo ratings yet
- محطة التقويم 4Document4 pagesمحطة التقويم 4Soufiane MlikuosNo ratings yet
- Tfaalat Badh Almoad Ma Almhalil Alhmdhia Oalqaadia Mlkhs Aldrs 2Document3 pagesTfaalat Badh Almoad Ma Almhalil Alhmdhia Oalqaadia Mlkhs Aldrs 2EL ATTAOUI Oubaid100% (1)
- 24 Acid Base RegulartionDocument20 pages24 Acid Base RegulartionMaro KaNo ratings yet
- Pubdoc 10 12128 1405Document2 pagesPubdoc 10 12128 1405sciencelab2023No ratings yet
- الوحدة-2- الوضائف الأكسوجينيةDocument6 pagesالوحدة-2- الوضائف الأكسوجينيةfouad elferdiNo ratings yet
- تحويلات و تعليلات العضويةDocument33 pagesتحويلات و تعليلات العضويةMahmoud MarwanNo ratings yet
- UntitledDocument22 pagesUntitledmoh gamerNo ratings yet
- تعريف الصابونDocument6 pagesتعريف الصابونNasre AK 47No ratings yet
- الأسبرينDocument21 pagesالأسبرينAbdelhak AdNo ratings yet
- ملخص الوحدة 04Document20 pagesملخص الوحدة 04abdelrahimdzzeNo ratings yet
- 4 5958760196799992869Document1 page4 5958760196799992869soundousrym2008No ratings yet
- Ex Regul AsservDocument4 pagesEx Regul AsservZahk LbatlNo ratings yet
- الكيمياء 1920 3 الكيمياء الحياتية العمليDocument27 pagesالكيمياء 1920 3 الكيمياء الحياتية العمليهنادي جميلNo ratings yet
- Transformations Chimiques S'effectuant Dans Les Deux SensDocument5 pagesTransformations Chimiques S'effectuant Dans Les Deux SensHarakat ElhoucineNo ratings yet
- Dates and Sugar TechnologyDocument4 pagesDates and Sugar Technologyهداية أحمد عبدالقادر عبدهNo ratings yet
- الخاماتDocument7 pagesالخاماتMahmoud M.EidNo ratings yet
- d6ecc790ef3a415df3d0b1bb951e6ebdDocument115 pagesd6ecc790ef3a415df3d0b1bb951e6ebdkuwatps4No ratings yet
- Projects1an Procedes-Aspirine1Document20 pagesProjects1an Procedes-Aspirine1fkhelfouneNo ratings yet
- بحث الأسبيرينDocument7 pagesبحث الأسبيرينYazid Aouali60% (5)
- شرح وتلخيص الوحدة الثالثة (الحموض والقواعد) كيمياء 12Document63 pagesشرح وتلخيص الوحدة الثالثة (الحموض والقواعد) كيمياء 12Issa ShuqairNo ratings yet
- الأسمدة والتسميدDocument54 pagesالأسمدة والتسميدmaherNo ratings yet
- السكريات الثنائيةDocument6 pagesالسكريات الثنائيةMohamed SalahNo ratings yet
- الايثراتDocument4 pagesالايثراتالعالم الالكتروني100% (1)
- Sec 3Document2 pagesSec 3Walid EbaiedNo ratings yet
- دراغون بولDocument16 pagesدراغون بولAbdou IslemNo ratings yet
- Nanatsu LawsDocument22 pagesNanatsu LawsAbdou IslemNo ratings yet
- ملخص درس الإشتقاقDocument1 pageملخص درس الإشتقاقAbdou Islem100% (2)
- أساسيات المبارزةDocument4 pagesأساسيات المبارزةAbdou IslemNo ratings yet
- ملخص درس الإشتقاقية رياضيات السنة الثالثة ثانوي PDFDocument1 pageملخص درس الإشتقاقية رياضيات السنة الثالثة ثانوي PDFAbdou Islem50% (2)
- تمارين الوحدة الثالثة في البكالوريا بالحلDocument21 pagesتمارين الوحدة الثالثة في البكالوريا بالحلAbdou Islem100% (1)
- اختبار باكالوريا تجريبي مع الحلDocument17 pagesاختبار باكالوريا تجريبي مع الحلAbdou Islem100% (2)