Professional Documents
Culture Documents
Opgave 3 - Kemisk Ligevægt (Disposition)
Opgave 3 - Kemisk Ligevægt (Disposition)
Uploaded by
laurasoeborgOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Opgave 3 - Kemisk Ligevægt (Disposition)
Opgave 3 - Kemisk Ligevægt (Disposition)
Uploaded by
laurasoeborgCopyright:
Available Formats
Disposition Eksamen 2022
Opgave 3 - Kemisk ligevægt
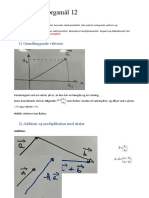
Du skal gennemgå øvelsen: ”Indgreb i et ligevægtssystem”.
Du skal redegøre for:
Definition på en kemisk ligevægt:
- Handler ikke om, at der er lige meget på hver side. Koncentrationerne på hver side af pilen
behøver ikke være ens.
- Der er kemisk ligevægt, når reaktionshastigheden mod højre er ens med
reaktionshastigheden mod venstre.
- Hurtig kemisk reaktion = kommer hurtigt i ligevægt
- Langsom kemisk reaktion = kommer langsomt i ligevægt
Ligevægtsloven
- Et generelt reaktionsskema for en homogen ligevægt er aA +bB ⇌ cC+ dD .
o A, B, C og D angiver formlerne for de molekyler eller ioner, som indgår i ligevægten.
o Prikkerne symboliserer, at der kan være flere reaktionsdeltagere.
o De små bogstaver symboliserer reaktionsskemaets koefficienter.
”Enhver kemisk reaktion har en ligevægtskonstant. Når reaktionen er nået til ligevægt, er
reaktionsbrøken = reaktionens ligevægtskonstant.”
- Ifølge ligevægtsloven kan man opskrive en reaktionsbrøk Y , som ved ligevægt antager en
ganske bestemt værdi. Her anbringes de aktuelle stofmængdekoncentrationer fra
reaktionsskemaets højre side (produktet) i tælleren, og i nævneren anbringes
reaktanterne:
[ C ]c · [ D ]d
Y= a b
=K c (Ved ligevægt)
[ A] ·[B]
- Når ligevægten har indstillet sig, har vi at ligevægtskonstanten K c , som afhænger af
temperaturen (og hvilken reaktion der er tale om), er lig med Y .
- Dvs. ved ligevægt er Y =K c.
- K c har enhed efter hvilket reaktion/brøk man har. (Den beregnes)
[ C ]c · [ D ]d · …
Y= a b
≠ K c (Ikke ligevægt)
[ A] ·[B] ·…
Hvis en af de modgående reaktioner er dominerende:
Y < K c (Reaktionsbrøken er mindre end ligevægtskonstanten)→
- For meget reaktant ift. produkt = nettoreaktion mod højre
[ xxx ] =¿ aktuelle stofmængdekoncentration
Disposition Eksamen 2022
Y > K c (Reaktionsbrøken er større end ligevægtskonstanten)←
- For meget produkt ift. reaktant = nettoreaktion mod venstre
Eksempler på homogen og heterogen ligevægt
Homogen ligevægt:
- Reaktanter og produkter er alle enten på gasform (g) eller i opløsning (L eller aq)
FX (Dannelse af Hydrogeniodid): H 2 ( g )+ I 2 ( g)⇌ 2 HI (g)
Heterogen ligevægt:
- Reaktanter og produkter har ikke samme tilstandsformer. 3+¿( aq) ¿
2+ ¿ ( aq ) ⇌ Ag (s )+ F e ¿
FX (Dannelse af frit sølv): A g+¿ ( aq) +F e ¿
Indgreb i en ligevægt (Le Chateliers princip)
- ”Et ydre indgreb i et ligevægtssystem fremkalder en forskydning, som formindsker
virkningen af indgrebet.”
- Betyder at et ligevægtssystem vil sørge for at indstille sig i ligevægt igen, når man har
forstyrret det.
- Systemet starter i ligevægt inden indgreb - indgreb bevirker, at systemet kommer ud af
ligevægt, og vi skal interessere os for de processer, som sker, når ligevægten indstiller sig
igen.
Faktorer som kan forskyde en kemisk ligevægt
- Man kan fx ændre på koncentrationer, volumen, temperatur, tryk (gasser).
Ændring af en reaktionsdeltagers stofmængdekoncentration:
[ C ]2
- Vi har ligevægten: A+ B ⇌2 C . Dvs. K c = .
[ A]⋅[B]
[ C ]2
- Indgreb: Der tilsættes reaktant (A). Dvs. <Kc⟶
[ A ]⋅[B]
o Ligevægten går i gang med at indstille sig igen. (Bevirker forskydning af ligevægten
mod højre, fordi indgrebet har givet for meget reaktant.)
- Eksempel: H 2 ( g )+ I 2 ( g)⇌ 2 HI (g)
[ HI ] 2
o Der tilsættes H 2. Dvs. <Kc
[ H 2 ] · [ I2 ]
[ xxx ] =¿ aktuelle stofmængdekoncentration
Disposition Eksamen 2022
[ HI ] 2
- Ved tilsætning af produkt (HI ): >Kc
[ H 2 ] · [ I2 ]
Indgreb ved koncentrationsændring set ved farveændring: 2+¿ (aq )¿
−¿( aq)⇌ FeSC N ¿
F e 3+ ¿ (aq )+SC N ¿
- Tilsætning af reaktant ¿: Y < K c →
o Dannes mere produkt = flere FeSC N 2+ ¿¿ioner (rød) og mørkere opløsning
- Tilsætning af produkt ¿
o Lysere opløsning = færre FeSC N 2+ ¿¿ioner (rød)
Temperaturændringer:
- Ligevægtskonstanten K c afhænger af temperaturen.
- Ligevægtens beliggenhed ændres, når temp. Ændres.
- En temperaturstigning vil medføre en forskydning af ligevægten i den endoterme reaktions
retning. Fordi temperaturforhøjelsen modvirkes.
o Endoterm reaktion: Kræver varme for at reagere.
o Exoterm reaktion: Udvikler varme ved reaktion.
- Hvis temp. Sænkes = forskydning af ligevægten i den exoterme reaktions
retning.
Eksempel:
N 2 O4 ( g) 2 N O2 (g)
⇌
Farveløs Brun
- Dvs. spaltning af dinitrogentetraoxid kræver varme.
Volumenændringer (Trykændringer):
- For ligevægte i opløsning kan man forøge systemets volumen ved at tilsætte mere af det
rene opløsningsmiddel (fortynde opløsningen). Ligevægten vil forskydes mod den side,
hvor der er flest partikler.
- Ændring af volumen medfører ændring i stofmængdekoncentrationen.
o Når volumen øges, mindskes molekyletætheden (og omvendt).
- For gasligevægte kan man ændre beholderes volumen, ved fx at forskyde et stempel. (Man
presser gassen sammen, så molekyletætheden øges)
Eksempel:
- Fordoblet volumen og halvering af stofmængdekoncentrationen:
[ xxx ] =¿ aktuelle stofmængdekoncentration
Disposition Eksamen 2022
Y =¿ ¿
- Dvs.Y > K c ⟵
Bilaget skal forklares.
[ xxx ] =¿ aktuelle stofmængdekoncentration
You might also like
- Eksamensopgaver - Vant Hoffs Ligning SVARDocument5 pagesEksamensopgaver - Vant Hoffs Ligning SVARcjs2jdkkyrNo ratings yet
- SkydiveDocument7 pagesSkydiveMorgan Winkler Pohl NielsenNo ratings yet
- KP HER Formelsamling Kemiske PrincipperDocument9 pagesKP HER Formelsamling Kemiske PrincipperAnders AgbarieNo ratings yet
- Fysik FormelsamlingDocument17 pagesFysik FormelsamlingSimon ThiimNo ratings yet
- NV Eksamen DispotionDocument11 pagesNV Eksamen DispotionLaurits BøjeNo ratings yet
- BASISKEMI B. Facit. Helge Mygind Ole Vesterlund Nielsen Vibeke Axelsen. HAASE & SønS ForlagDocument33 pagesBASISKEMI B. Facit. Helge Mygind Ole Vesterlund Nielsen Vibeke Axelsen. HAASE & SønS ForlagJohannes HansenNo ratings yet
- Rapport Bygmek NyDocument16 pagesRapport Bygmek NyDon ProductionNo ratings yet
- Fysikrapport Joules LovDocument5 pagesFysikrapport Joules LovukendtNo ratings yet
- Rapportark Carbonhydrider - RettetDocument3 pagesRapportark Carbonhydrider - RettetshamoNo ratings yet
- Luftmodstand ForsøgDocument2 pagesLuftmodstand ForsøgOlle SkoleNo ratings yet
- KEMI 2000 B-A - NoterDocument30 pagesKEMI 2000 B-A - NoterJhonn HallingsenNo ratings yet
- FysikDocument136 pagesFysikvilashjorthen100% (2)
- Kemi B NoterDocument52 pagesKemi B NoterAske HvassNo ratings yet
- Oplæg Til SRP I ReaktionskinetikDocument7 pagesOplæg Til SRP I ReaktionskinetikhamframarsNo ratings yet
- Opgave 3 - Kemisk Ligevægt (Disposition)Document4 pagesOpgave 3 - Kemisk Ligevægt (Disposition)laurasoeborgNo ratings yet
- Kemi Eksamen 2007Document53 pagesKemi Eksamen 2007Louise Haslev Jønsson0% (1)
- Kemi NoterDocument11 pagesKemi NoterBobi JensenNo ratings yet
- KemiDocument14 pagesKemikagemand25No ratings yet
- Opgave 2 - Reaktionshastighed (Disposition)Document4 pagesOpgave 2 - Reaktionshastighed (Disposition)laurasoeborgNo ratings yet
- Opgave 2 - Reaktionshastighed (Disposition)Document4 pagesOpgave 2 - Reaktionshastighed (Disposition)laurasoeborgNo ratings yet
- Kemi NoterDocument31 pagesKemi Noterjulie falkenbergNo ratings yet
- Opgave Om Kredsproces For Enatomig Ideal Gas (Aflevering 1, Sascha Jensen)Document8 pagesOpgave Om Kredsproces For Enatomig Ideal Gas (Aflevering 1, Sascha Jensen)Sascha JensenNo ratings yet
- Reaktions NoterDocument16 pagesReaktions Noterpandus1106No ratings yet
- Hovedpointer Fra Makro IDocument18 pagesHovedpointer Fra Makro IGAIA secondhandNo ratings yet
- Fysik Eksamensforberedelse - 2017Document17 pagesFysik Eksamensforberedelse - 2017Laileh KaderNo ratings yet
- Hess' Lov EfterbehandlingDocument2 pagesHess' Lov EfterbehandlingS. BalcrickNo ratings yet
- Hjemmeaflevering 16Document5 pagesHjemmeaflevering 16heglundnielsenNo ratings yet
- Eksamensspørgsmål 12Document5 pagesEksamensspørgsmål 12yaman AlsayedNo ratings yet
- Fysik FormlerDocument27 pagesFysik FormlerJeppe BakkensenNo ratings yet
- MP10 EpidemiDocument14 pagesMP10 Epidemiebbe8691No ratings yet
- Opgave 4 - Syrer Og Baser Og PH (Disposition)Document4 pagesOpgave 4 - Syrer Og Baser Og PH (Disposition)laurasoeborgNo ratings yet
- Opgave 4 - Syrer Og Baser Og PH (Disposition)Document4 pagesOpgave 4 - Syrer Og Baser Og PH (Disposition)laurasoeborgNo ratings yet
- Formelsamling Fysik BDocument5 pagesFormelsamling Fysik BMo AzzamNo ratings yet
- Indgreb I Et Ligevægtssystem. RapportDocument5 pagesIndgreb I Et Ligevægtssystem. RapportSigne KrøyerNo ratings yet
- Teori ReaktionshastighedDocument1 pageTeori Reaktionshastighedpandus1106No ratings yet
- ReaktionshastighedDocument6 pagesReaktionshastighedhero gooshwarehNo ratings yet
- Problem Set 6Document10 pagesProblem Set 6oskardyringNo ratings yet
- Fysisk-Kemi 2018 MajDocument7 pagesFysisk-Kemi 2018 MajLaileh KaderNo ratings yet
- Exam PAFF 2016 SvarDocument9 pagesExam PAFF 2016 SvarpraiisejebusNo ratings yet
- Kemirapport - Forskydning Af LigevægtDocument5 pagesKemirapport - Forskydning Af LigevægtAndreas Dyndegaard100% (2)
- Exam PAFF 2017 SvarDocument14 pagesExam PAFF 2017 SvarpraiisejebusNo ratings yet
- Termisk Fysik Eksamen Juni 2010 SvarDocument5 pagesTermisk Fysik Eksamen Juni 2010 SvarGuf GrupeNo ratings yet
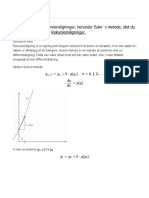
- A Rekursionsligninger Herunder Euler S MetodeDocument2 pagesA Rekursionsligninger Herunder Euler S MetodeMorgan Winkler Pohl NielsenNo ratings yet
- 0185 Projekt NyttevirkningDocument7 pages0185 Projekt NyttevirkningPhillip TranNo ratings yet
- Opg 5Document3 pagesOpg 5Omid NadriNo ratings yet
- Atkins, E1C.9, P1A.8Document5 pagesAtkins, E1C.9, P1A.8EmNo ratings yet
- Eksamen 2019 Fysisk KemiDocument13 pagesEksamen 2019 Fysisk KemiLaileh KaderNo ratings yet
- ReaktionshastighedenDocument8 pagesReaktionshastighedenkejser-1 sharbelNo ratings yet
- Regneregler For Integraler (Matematik B, Integralregning) - WebmatematikDocument2 pagesRegneregler For Integraler (Matematik B, Integralregning) - WebmatematikTheFrederiksenNo ratings yet
- TERMO s203911 PDFDocument6 pagesTERMO s203911 PDFAnton MolsenNo ratings yet
- 2ike Prøve1b BesvarelseDocument3 pages2ike Prøve1b BesvarelseYagmur OvurNo ratings yet
- HA Almen Opgavesæt 11 Efterår 2021 Vejledende LøsningDocument7 pagesHA Almen Opgavesæt 11 Efterår 2021 Vejledende LøsningSisiNo ratings yet
- Forsøg Varmekapacitet KølerDocument5 pagesForsøg Varmekapacitet KølerEmilia LundNo ratings yet
- Dansk - LøsningsforslagDocument8 pagesDansk - LøsningsforslagspoolNo ratings yet
- Teodor Mihail Stefan - SRODocument20 pagesTeodor Mihail Stefan - SROThe Cloth PuppeteerNo ratings yet
- Solpanel Og SolfangerDocument9 pagesSolpanel Og SolfangerJafeNo ratings yet
- Rapport Om Energi - Mick SpelmannDocument6 pagesRapport Om Energi - Mick SpelmannMick Neymar SpelmannNo ratings yet
- Fysikaflevering 7aDocument16 pagesFysikaflevering 7akagemand25No ratings yet
- 3 Reaktioner M Organiske Molekyler 2021Document6 pages3 Reaktioner M Organiske Molekyler 2021Mohammad AltalebNo ratings yet