Professional Documents
Culture Documents
Nghiên cứu cải tiến và hoàn thiện quy trình công nghệ sản xuất nước uống dinh dưỡng từ cây chùm ngây
Uploaded by
Nguyễn Thanh TâmCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Nghiên cứu cải tiến và hoàn thiện quy trình công nghệ sản xuất nước uống dinh dưỡng từ cây chùm ngây
Uploaded by
Nguyễn Thanh TâmCopyright:
Available Formats
ĐẶT VẤN ĐỀ
Trong quá trình thực hiện đề tài nghiên cứu khoa học cấp trường “Nghiên cứu sản xuất
thử nước uống dinh dưỡng từ cây chùm ngây (Moringa Oleifera), chúng tôi đã đạt được nhiều
kết quả khả quan, được thể hiện trong đề tài khóa luận tốt nghiệp “Nghiên cứu sản xuất nước
uống dinh dưỡng từ chùm ngây” của thành viên Đào Ngọc Thủy Tiên. Tuy nhiên quá trình
nghiên cứu vẫn còn tồn tại một số khuyết điểm cần được khắc phục:
Vẫn chưa có những đánh giá về giá trị dinh dưỡng của nguyên liệu và sản phẩm trong thực tế
Sản phẩm làm ra bị xỉn màu do Chlorophyll bị biến màu trong môi trường acid, Các khảo sát
về việc sử dụng chất ổn định vẫn chưa hoàn thiện nên sản phẩm vẫn còn bị kết lắng sau thời
gian dài bảo quản.
Việc khảo sát công thức thanh trùng tuy đã thực hiện tốt, nhưng vẫn còn có thể cải tiến
phương pháp cho hợp lý và hiêu quả hơn.
Xuât phát từ các vấn đề thực tế đó, và theo kế hoạch hoàn thiện đề tài nghiên cứu cấp
trường, chúng tôi quyết định thực hiện thêm các nghiên cứu hoàn thiện sản phẩm, nhằm hoàn
thiên quy trình, nâng cao chất lượng cảm quan và đánh giá được giá trị dinh dưỡng sản phẩm,
được thể hiện thông qua đề tài khóa luận: “Nghiên cứu cải tiến và hoàn thiện quy trình công
nghệ sản xuất nước uống dinh dưỡng từ cây chùm ngây.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 i
Phần I. TỔNG QUAN
1. TÌM HIỂU VỀ CHÙM NGÂY:[Error! Reference source not found.,
Error! Reference source not found., Error! Reference source not
found., Error! Reference source not found., Error! Reference source
not found.]
1.1. Giới thiệu về cây chùm ngây:
Cây chùm ngây có nguồn gốc từ vùng đông bắc Ấn Độ, phía nam của dãy núi Hymalaya.Nó
được trồng rộng rãi ở miền nhiệt đới, phổ biến là ở các nước châu Á, châu Phi và châu Mỹ
Latinh (Fahey et.al, 2001).
1.1.1. Vị trí phân loại: Chùm ngâythuộc:
Giới thực vật : Plantae
Bộ cải : Brassicales
Họ chùm ngây: Moringaceae
Chi: Moringa
Loài: Moringa oleifera
Danh pháp khoa học:Moringa oleifera.
Tên gọi thông thường: Moringa, Ben-oil tree, Drumstick tree, Merunggai, Indian Horseradish
tree, Malunggay, …
Theo Kristin (2000), trong số 13 loài thuộc chi Moringa thì Moringa oleifera là loài được
trồng nhiều nhất vì đây là một loại cây không chỉ chứa hàm lượng dinh dưỡng rất cao mà còn
có nhiều thành phần dược liệu quý hiếm đã được kiểm nghiệm. Chính vì thế, người Ấn Độ đã
trân trọng gọi nó là cây Độ sinh (Tree of life), còn các nhà khoa học đã không ngần ngại đặt
tên cho nó là cây Thần Diệu hay cây Phép Màu (Miracle tree).
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 ii
Đặc điểm hình thái:
Chùm ngây thuộc loại đại mộc, có thể mọc
cao 5 – 10m.
Lá kép (có thể đến 3 lần) dài 30-60mm, có
hình lông chim, màu xanh mốc.
Hoa trắng, có cuống, hình dạng giống như
hoa đậu, thường mọc thành chùy ở nách lá
và có lông tơ.Cây thường trổ hoa từ tháng 1
đến tháng 3.
Hình 1.1 Đặc điểm hình thái của
Quả chín từ tháng 4 đến tháng 6, có dạng chùm ngây
nang treo, dài 25-30cm, ngang 2cm, chỗ có hạt hơi gồ lên, dọc theo quả có khía rãnh.
Hạt quả có màu đen, tròn, 3 cạnh và thường bằng cỡ hạt đậu Hà Lan, có 3 cạnh và 3 cánh màu
trắng dạng màng.
1.1.2. Đặc điểm sinh thái:
Chùm ngây có khả năng sống từ vùng cận nhiệt đới khô đến ẩm và vùng nhiệt đới rất khô cho
đến vùng rừng ẩm. Cây chịu được lượng mưa từ 480-4000 mm/ năm, nhiệt độ 18,7oC –
28,5oC, pH từ 4,5 – 8 và có khả năng chịu hạn rất tốt, có thể phát triển được ở những nơi đất
cát khô, cằn cỗi.
1.1.3. Đặc điểm phân bố:
Cây có nguồn gốc từ Ấn Độ, Arabia, châu Phi,
vùng Viễn Tây châu Mỹ, được trồng và mọc tự
nhiên ở các vùng nhiệt đới châu Phi, nhiệt đới
châu Mỹ, Sri Lanka, Ấn Độ, Mexico, Malabar,
Malaysia và Philippines.
Ở Việt Nam, cây từ lâu được trồng làm nọc trầu tại
Ninh Thuận, Bình Thuận, là thực phẩm chính của
đồng bào Chăm và Raglay. Ngoài ra nó còn Hình 1.2: Tình hình phân bố chùm ngây
mọc hoang và được trồng ở Đà Nẵng, trên thế giới
Khánh Hòa, Nha Trang, Kiên Giang và đảo
Phú Quốc.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 iii
1.2. Giá trị dinh dưỡng cao từ chùm ngây:
1.2.1. Thành phần dinh dưỡng trong chùm ngây:[Error! Reference
source not found., Error! Reference source not found., Error! Reference
source not found.]
Chùm ngây chứa hơn 90 chất dinh dưỡng tổng hợp cần thiết cho sức khỏe con người, giảm
thiểu nguy cơ từ những chứng bệnh suy thoái, chữa trị các bệnh thông thường. Theo các
nghiên cứu khoa học, hầu hết các bộ phận sống của chùm ngây đều chứa đủ các thành phần
dinh dưỡng có thể giúp ích cho sự sống của con người. Chẳng hạn, trong hoa chùm ngây có
chứa hàm lượng khoáng chất rất cao, nổi trội là canxium và potassium, còn trong hạt thì lượng
dầu chiếm đến 40% trọng lượng hạt mà thành phần chủ yếu là acid oliec (70%), đây là một
loại acid béo rất tốt cho cơ thể. Hoặc như trong quả, ngoài các chất dinh dưỡng thường có
trong các loại quả thông thường thì nó còn rất giàu đạm (2,5%) và khoáng (2%).
Bên cạnh đó, một bộ phận có vai trò và giá trị dinh dưỡng đặc biệt nổi trội hơn cả chính là lá
chùm ngây. Trong lá chùm ngây có chứa nhiều vitamin và muối khoáng có ích với hàm lượng
rất cao như vitamin C, provitamin A, calcium, potassium, và ngay cả lượng protein cũng cao
nổi trội so với các loại rau quả khác. Ngoài ra, lá còn chứa nhiều vitamin B, các acid amin có
lưu huỳnh như methionin, cystine, cysteine và nhiều acid amin cần thiết khác thường chỉ có
nhiều ở từ nguồn thực phẩm động vật.Vì thế, lá chùm ngây được xem là một trong những
nguồn dinh dưỡng thực vật có giá trị cao.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 iv
Bảng 1.1 Thành phần dinh dưỡng trong 100g lá tươi chùm ngây ăn được
Thành phần Hàm lượng
Hàm ẩm (%) 75
Calories (cal) 92,0
Protein (g) 6,7
Fat (g) 1,7
Carbohydrate (g) 13,4
Fiber (g) 0,9
Total Minerals (g) 2,3
Minerals
Calcium (mg) 440,0
Magnesium (mg) 24,0
Phosphorous (mg) 70,0
Potassium (mg) 259,0
Copper (mg) 1,1
Iron (mg) 7,0
Oxalic acid (mg) 101,0
Sulphur 137,0
Vitamin
Vitamin A - carotene (mg) 6,8
Vitamin B – Choline (mg) 423,0
Vitamin B1 – Thiamin (mg) 0,21
Vitamin B2 – Riboflavin (mg) 0,05
Vitamin B3 – Nicotinic acid (mg) 0,8
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 v
Vitamin C – Ascorbic acid (mg) 220,0
Vitamin E – Tocopherol (mg) 150-200
Amino acid
Arginine (mg) 406,6
Histidine (mg) 149,8
Lysine (mg) 342,4
Tryptophan (mg) 107,4
Phenylalanine (mg) 310,3
Methionine (mg) 117,7
Threonine (mg) 117,7
Leucine (mg) 492,2
Isoleucine (mg) 299,6
Valine (mg) 374,5
(Nguồn: Effect Of Moringa Leaf Meal (Molm) On Nutrient Digestibility, Growth, Carcass
And Blood Indices Of Weaner Rabbits, Frederick Nuhu (2010) )
Như vậy, theo bảng trên, thành phần dinh dưỡng chứa trong chùm ngây là rất lớn. Các nhà khoa
học đã chứng minh trong 100g lá chùm ngây tươi có
chứa một lượng vitamin C gấp 7 lần quả cam, lượng
canxi gấp 4 lần và lượng protein gấp 2 lần sữa. Bên
cạnh đó, lượng vitamin A chứa trong chùm ngây còn
gấp 4 lần của cà rốt, vitamin E gấp 3 lần rau chân vịt,
potassium gấp 3 lần chuối, và sắt gấp 3 lần quả hạnh.
Theo nghiên cứu của Ray-Yu Yang và cộng sự, hàm
lượng các chất dinh dưỡng chứa trong lá cây trưởng
thành nhiều hơn so với các lá còn non và có thể được Hình 1.3: Hình ảnh so sánh chùm
sấy khô một cách nhanh chóng với sự mất mát chất ngây và một số loại thực phẩm khác
dinh dưỡng là tối thiểu.
Bảng 1.2 Bảng so sánh thành phần dinh dưỡng
của lá non và lá trưởng thành
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 vi
(Nguồn: Nutritional and Functional Properties of Moringa Leaves − From Germplasm, to
Plant, to Food, to Health, Ray-Yu Yang et.al)
Lá cây chùm ngây giàu dinh dưỡng hiện được hai tổ chức thế giới WHO và FAO xem như là
giải pháp ưu việt cho các bà mẹ thiếu sữa và trẻ em suy dinh dưỡng, đây cũng là giải pháp
lương thực cho các nước thuộc thế giới thứ ba.
Đối với trẻ em Việt Nam từ 1-3 tuổi, cứ ăn 50gr lá tươi chùm ngây là đã cung ứng được 50%
canxi, 100% vitamin C, vitamin A, 100% chất sắt, 10% chất đạm cần thiết và bổ sung thêm
phần lớn hàm luợng kali, đồng, kẽm,.. và các vitamin nhóm B cần thiết cho trẻ.
1.2.2. Một số chất dinh dưỡng tiêu biểu trong chùm ngây:
1.2.2.1. Protein:
Protein đóng vai trò rất quan trọng trong mọi hoạt động sống của con người, nếu thiếu đạm thì
cơ thể sẽ bị suy dinh dưỡng, sụt cân, còi cọc, kém tiêu hóa, dễ mắc bệnh nhiễm trùng....
Protein được tổng hợp từ nhiều nhóm nhỏ các acid amin, liên kết với nhau tạo thành dạng
chuỗi. Đa số protein có nguồn gốc từ động vật, còn trong thực vật chủ yếu có ở các loại họ đậu
như đậu nành, đậu Hà Lan, rau bina, gạo đỏ, nấm... Tuy nhiên, đạm thực vật thường không có
đủ các acid amin thiết yếu – là những acid amin mà cơ thể không tự tổng hợp được, và tỷ lệ
giữa các acid amin cũng chưa cân đối. Mặc dù vậy, chùm ngây được đánh giá là loại rau có
chứa hàm lượng protein và các acid amin rất cao, đặc biệt là chứa hầu hết các acid amin thiết
yếu có thể so sánh với hàm lượng protein có trong đậu nành (35-45%).Nghiên cứu của các nhà
khoa học cho thấy lượng protein có trong 100g lá tươi chùm ngây là 6,7g, cao gấp 2 lần so với
lượng protein có trong sữa (3.3g). Đồng thời, với lượng protein này thì 100g lá chùm ngây đã
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 vii
cung cấp đến 19,14% lượng protein cần cho trẻ em từ 1-3 tuổi – lứa tuổi rất dễ mắc chứng suy
dinh dưỡng do thiếu protein.
Bảng 1.3: Bảng so sánh hàm lượng protein trong lá chùm ngây và đậu nành
Dịch trích lá Tham khảo của
Protein đậu nành Moringa Oleifera FAO / WHO dành
Axit amin
Mg / g protein cho trẻ 2-5 tuổi
Mg / g protein Mg / g protein
Histidine 26 31 19
Isoleucine 49 51 28
Leucin 82 98 66
Lysine 63 66 58
Methionine + Cystine 26 21 25
Phenylalanine + Tyrosine 90 105 63
Threonine 38 50 34
Tryptophan 13 21 11
Valine 50 63 35
(Theo F.N. Makkar et.al.)
Như vậy, chùm ngây chính là một giải pháp tuyệt vời để cung cấp đầy đủ chất đạm và các acid
amin thiết yếu cho cơ thể, cũng như góp phần làm phong phú hơn thị trường thực phẩm chay
hiện nay.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 viii
1.2.2.2. Chất khoáng:
Chùm ngây có chứa nhiều khoáng chất quan trọng như Ca, Fe, K, Mg, P…, trong đó, lượng K
gấp 3 lần chuối, lượng Fe gấp 3 lần quả hạnh và lượng Ca là nổi trội nhất, gấp đến 4 lần lượng
Ca có trong yaourt.
Canxi là nguyên tố hoạt động nhất trong cơ thể con người. Canxi chiếm 1,5-2% trọng lượng
cơ thể, trong đó 99% tồn tại trong xương, răng, móng chân, móng tay, chỉ có 1% tồn tại trong
máu, trong tổ chức tế bào và dịch ngoài tế bào.
Công trình khoa học của Tiến sĩ Walloc (người Mỹ) được giải thưởng Nobel năm 1991
đã chỉ ra rằng: Khi thiếu canxi, khả năng miễn dịch của cơ thể sẽ bị rối loạn, gây ra
các chứng bệnh về gan (viêm gan, xơ gan..), da (phong thấp, viêm da, bạch tạng…),
các bệnh về nội tiết (tiểu đường, viêm thận,..), thần kinh (bất thường nhịp tim, suy
nhược thần kinh…) và các bệnh về cơ, xương (viêm khớp, còi cọc, chậm lớn...). Do đó,
việc cung cấp đầy đủ lượng canxi hàng ngày là rất quan trọng.
Trong 100g lá tươi chùm ngây có chứa đến 440mg canxi, cung cấp đầy đủ (100%) nhu cầu
calci cho trẻ 1-3 tuổi và một lương lớn calci (44%) cho phụ nữ đang cho con bú, vốn là hai đối
tượng có nhu cầu calci cao.
Hình 1.4 Biểu đồ so sánh hàm lượng canxi trong chùm ngây và các loại thực phẩm khác
(Nguồn: Growing and processing Moriga leaves, Dr Armelle de Saint Sauveur et Dr Mélanie
Broin)
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 ix
1.2.2.3. Vitamin:
Không chỉ là nguồn protein và khoáng chất dồi dào, chùm ngây còn chứa rất nhiều vitamin cần
thiết cho cơ thể, tiêu biểu là các vitamin A, B1, B3, B6, C, E, K,.. đặc biệt là hàm lượng vitamin A
và vitamin C cao vượt trội so với các loại rau quả khác.
Trong chùm ngây chứa đến 6,8 mg vitamin A (gấp 3 lần cà rốt) và 220 mg vitamin C (gấp 7 lần
cam), vì thế chỉ với 100g lá tươi chùm ngây đã cung cấp đầy đủ lượng vitamin A và C cần thiết
cho cơ thể mỗi ngày, đặc biệt là cho trẻ em từ 1-3 tuổi.
1.2.3. Dược tính của chùm ngây: [Error! Reference source not found.,
Error! Reference source not found., Error! Reference source not found.,
Error! Reference source not found.]
Thành phần dược tính của chùm ngây:
Chùm ngây có chứa tất cả hơn 46 chất chống oxy hóa và 36 hợp chất chống viêm tự nhiên,
được liệt kê dưới đây ở bảng 1.4.
Bảng 1.4 Một số chất kháng viêm và chất chống oxy hóa trong chùm ngây
Chất chống oxy hóa Chất kháng viêm
Vitamin A, Vitamin C, Vitamin E, Arginine, Beta-sitosterol, histidine, tryptophan, Zeatin,
glutathione, Caffeoylquinic Acid, Leucin, kẽm, Selenium, Rutin, Quercetin, Kaempferal,
Chlorophyll, indole Acetic Acid, Indoleacetonitrile,
Vitamin K, vitamin B (Choline), Vitamin B1 Vitamin B1 (Thiamin), Calcium,
(Thiamin), Vitamin B2 (Riboflavin), Vitamin B3 đồng, Kali, lưu huỳnh, Magnesium,
(Niacin), Vitamin B6, Beta-Carotene, Alpha- Omega 3, Omega 6, Omega 9, sợi,
carotene, Campesterol, Carotenoid, Chromium, Acid oleic, Phenylalanine,
Delta-5-Avenasterol, Delta-7-Avenasterol, Stigmasterol, Cystine, isoleucine,
Myristic-Acid, palmitic-Acid, Xanthins, hoàng thể Tyrosine
tố, zeaxanthin, Alanine, Lutein, Methionine,
Prolamine, Proline, Threonine
(Nguồn: http://www.caychumngay.vn/)
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 x
Trong lá đặc biệt có chứa các hợp chất loại flavonoids và phenolic như kaempferol 3-O-alpha-
rhamnoside, kaempferol, syringic acid, gallic acid, rutin, quercetin 3-O-beta-glucoside.Các
flavonol glycosides được xác định đều thuộc nhóm kaempferide nối kết với các rhamnoside
hay glucoside.
Theo S. Sreelatha (Plant Foods For Human Nutrition (2009)), thành phần các hợp chất chống oxy
hóa nói chung và các hợp chất flavonoids, phenolic nói riêng đều có nhiều trong lá chùm ngây
tươi, mà nhiều nhất là có trong lá chùm ngây trưởng thành.
Bảng 1.5Tổng lượng phenolic và flavonoid có trong dịch trích lá chùm ngây
Extract/Standard contents Total phenolic contents Total flavonoid
(mg/g)
Mature leaf extract 45.81 0.02 27 0.03
Tender leaf extract 36.02 0.01 15 0.02
Values are mean of triplicates standard deviation.
Phenolics expressed as mg gallic acid equivalents (GAE)/g plant material.
Flavonoids expressed as mg equivalents of quercetin/g plant material.
(Nguồn: Antioxidant Activity and Total Phenolic Content of Leaves in Two Stages of
Maturity, Sreelatha S. and Padma P. R. (2009))
Như vậy, lá trưởng thành không chỉ có hàm lượng dinh dưỡng cao hơn mà còn chứa nhiều hợp
chất chống oxy hóa có lợi cho cơ thể hơn so với lá non.
1.3. Tình hình sử dụng chùm ngây ở nước ta:[Error! Reference source
not found., Error! Reference source not found.]
ở việt nam chùm ngây được trồng nhiều ở tỉnh Ninh Thuận và Bình Thuận nhưng cũng có mặt
ở những tỉnh khác như Thanh Hóa, An Giang với mục đích để làm thực phẩm, làm thuốc. Lá
dùng để nấu canh, hoa sau khi phơi khô có thể dùng nấu lấy nước uống như một loại trà, trái
non được dùng như đậu ve còn hạt chùm ngây khi già thì có thể đem rang lên và ăn như đậu
phộng.
Người ta cũng dùng lá chùm ngây ướp với hoa lài, sâm tươi, hay phối chế với chè xanh để làm
ra các sản phẩm, bài thuốc bồi bổ sức khỏe, tăng cường sức đề kháng, cung cấp vitamin và các
acid amin, khoáng chất cho cơ thể, cải thiện tốt tình trạng kém ăn, mất ngủ, dùng cho người
bệnh tiểu đường, cao huyết áp, mỡ trong máu, cholesterol cao…
Từ đầu năm 2010 đến nay, huyện Tri Tôn (tỉnh An Giang, Việt Nam) đã bắt tay vào thực hiện
dự án 3 năm "Bảo tồn, phát triển sản xuất và hướng tới chế biến, tiêu thụ sản phẩm cây chùm
ngây" với kinh phí hơn 1 tỉ đồng nhằmmục đích xóa nghèo, cải thiện cuộc sống và tình hình
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xi
đói ăn của đồng bào dân tộc Khmer và người trồng rừng phòng hộ khu vực Bảy Núi. (theo
Niengiamnongnghiep.vn)
1.4. Một số ứng dụng của chùm ngây trong các lĩnh vực:
1.4.1. Nông nghiệp:
Cây chùm ngây thuộc loại cây mọc nhanh và dễ tính, sống được ở những điều kiện đất đai khô
cằn và trong điều kiện khí hậu khắc nghiệt, chịu được hạn hán. Vì vậy, từ lâu, cây chùm ngây đã
được trồng làm hàng rào xanh che chắn cho các khu sản xuất nông nghiệp, che bóng cho các cây
công nghiệp dài ngày, chắn gió, chắn cát bay.
Ngoài ra, cây có khả năng cải tạo đất, lá dùng làm phân xanh và làm thức ăn bổ sung cho gia
súc rất tốt. Bên cạnh đó, do cây có lá nhỏ, thân thon, tán đẹp nên thường được trồng làm cảnh,
trang trí sân vườn.
1.4.2. Môi trường:
Theo nghiên cứu của ông Michael Lea, chuyên gia thuộc Clearinghouse - tổ chức Canada
chuyên nghiên cứu công nghệ lọc nước chi phí thấp – và các cộng sự, hạt chùm ngây có thể
giảm đến 99,99% vi khuẩn trong nước chưa được xử lý.
Hạt chùm ngây có chứa một số hợp chất đa điện giải (polyelectrolytes) tự nhiên có thể dùng
làm chất kết tủa để làm trong nước. Kết quả thử nghiệm lọc nước cho thấy rằng nước đục (độ
đục 15-25 NTU, chứa các vi khuẩn tạp 280-500 cfu/ml, khuẩn Ecoli từ phân 280-500
MPN/100 ml khi dùng hạt chùm ngây làm chất tạo trầm lắng và kết tụ đã cho kết quả rất tốt
(độ đục còn 0.3-1.5 NTU; vi khuẩn tạp còn 5-20 cfu/ml; và khuẩn Ecoli còn 5-10 MPN.
Phương pháp lọc này rất hữu dụng tại các vùng nông thôn của các nước nghèo và được áp
dụng khá rộng rãi tại Ấn độ (Theo Journal of Water and Health, số 3-2005).
Hình 1.5 Hạt chùm ngây được dùng để lọc nước
(Nguồn http://www.jalmandir.com/blog/index.php)
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xii
1.4.3. Thực phẩm:
Chùm ngây được ứng dụng nhiều nhất trong lĩnh vực sản xuất và chế biến thực phẩm. Người
ta thường dùng chùm ngây trong các bữa ăn hàng ngày như dùng lá để ăn sống, hấp với một ít
gia vị như dấm, muối hay nấu canh, xào hoặc nấu chung các loại rau, đậu khác. Thậm chí, lá
chùm ngây còn có thể làm kem, sinh tố; hoa, quả cũng được dùng để làm trà, nấu soup, lẩu
hay chiên xào đều được; riêng hạt còn được ăn như đậu phộng, hoặc ép lấy dầu dùng để nấu
nướng hàng ngày.
Hình 1.6 Một số thực phẩm từ chùm ngây
Ngày nay, chùm ngây không chỉ đơn thuần được sử dụng theo cách thủ công, truyền thống mà
còn được ứng dụng đặc biệt là trong lĩnh vực công nghệ thực phẩm nói chung và thực phẩm
chức năng nói riêng nhằm phục vụ cho nhu cầu sử dụng ngày càng cao của con người. Hiện
nay trên thị trường đã có nhiều sản phẩm từ chùm ngây, nhất là từ lá và hoa, tiêu biểu là các
sản phẩm trà như trà lá chùm ngây, trà hoa chùm ngây dạng sấy khô hay túi lọc.
Các sản phẩm này ngày càng phổ biến và đa dạng hơn bởi sự kết hợp nguồn nguyên liệu chính
là hoa và lá chùm ngây với các loại dược thảo như gừng, atiso, hạt sen, nhân sâm, linh chi…
và các loại trái cây như dâu, lựu, chanh, đào…
Hình 1.7 Nước giải khát từ chùm ngây
Ở các nước thuộc “Thế giới thứ ba”, chùm ngây không chỉ được ăn sống hay nấu canh, mà còn
được nghiền thành bột hoặc nấu chín vo viên để bán hoặc để dùng dần.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xiii
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xiv
Hình 1.8 Sản xuất bột lá chùm ngây
Hình 1.9 Lá chùm ngây viên
Mỹ là quốc gia đi đầu trong việc sản xuất các sản phẩm từ chùm ngây, nổi bật là dòng sản
phẩm mang thương hiệu Zija nổi tiếng khắp thế giới.
Zija là công ty chuyên kinh doanh về các sản phẩm từ chùm ngây ở hầu hết các lĩnh vực thực
phẩm, dược phẩm và mỹ phẩm. Riêng về sản phẩm thực phẩm gồm có các loại bột dinh
dưỡng, nước uống dinh dưỡng, nước uống giàu năng lượng,…
Hình 1.10 Dòng sản phẩm nước giải khát từ chùm ngây của công ty Zija (Mỹ)
1.4.4. Dược phẩm:
Một ứng dụng quan trọng không thể không nhắc tới của chùm ngây đó là ứng dụng trong
ngành y dược. Từ xưa, dân tộc Raglay đã dùng chùm ngây như một loại thuốc tránh thai đơn
giản nhưng lại rất hiệu quả bằng cách: cứ khoảng năm ngày thì lấy hai nắm rễ chùm ngây còn
tươi (chừng 150gam), rửa sạch, xắt nhỏ, sắc giống sắc thuốc nam và uống hai lần trong ngày.
Hiện tại đã có rất nhiều nghiên cứu về chùm ngây mà đa số các nghiên cứu đó được thực hiện
tại các quốc gia như Ấn Độ, Philippines và Phi Châu... Có thể kể đến một số nghiên cứu khoa
học tiêu biểu như:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xv
Nghiên cứu về giá trị đa dụng của Moringa oleifera được thực hiện tại ĐH Nông Nghiệp
Falsalabad, Pakistan chứng minh đây là một loại cây có giá trị kinh tế cao vì vừa là một nguồn
dược liệu vừa là một nguồn thực phẩm rất tốt.
Nghiên cứu về hoạt tính kháng nấm gây bệnh loại Trichophyton rubrum, Trichophyton
mentagrophytes, Epidermophyton floccosum và Microsporum canis từ dịch chiết của lá và hạt
chùm ngây bằng ethanol, được thực hiện tại Institute of Bioagricultural Sciences, Academia
Sinica, Đài Bắc (Taiwan). Các phân tích hóa học đã tìm được trong dầu trích từ lá chùm ngây
có đến 44 hóa chất có khả năng kháng nấm bệnh. (Bioresource Technology Số 98-2007).
Nghiên cứu tại ĐH Baroda, Kalabhavan, Gujarat (Ấn Độ) về hoạt tính trên các thông số lipid
của quả chùm ngây được thí nghiệm trên thỏ bằng cách cho ăn chùm ngây (200mg/kg mỗi
ngày) hay uống lovastatin (6mg/kg/ ngày) trộn trong một hỗn hợp thực phẩm tạo cholesterol
cao, kéo dài 120 ngày. Kết quả cho thấy chùm ngây và lovastatin có tác dụng gây hạ
cholesterol, phospholipid, triglyceride, VLDL, LDL hạ tỷ số cholesterol/ phospholipid trong
máu so với thỏ trong nhóm đối chứng. Khi cho thỏ bình thường dùng chùm ngây hay
lovastatin: mức HDL lại giảm hạ nhưng nếu thỏ bị cao cholesterol thì mức HDL lại gia tăng.
Riêng chùm ngây còn có thêm tác dụng làm tăng sự thải loại cholesterol qua phân (Journal of
Ethnopharmacology Số 86-2003).
Nghiên cứu về hoạt tính kháng sinh của hạt chùm ngây đã xác định 4 (alpha-L-
Rhamnosyloxy) benzyl isothiocyanate có hoạt tính kháng sinh mạnh nhất trong các hoạt chất
trích từ hạt chùm ngây. Hợp chất trên ức chế sự tăng trưởng của nhiều vi khuẩn và nấm gây
bệnh. Nồng độ tối thiểu để ức chế Bacillus subtilis là 56 µmol/l và để ức chế
Mycobacterium phlei là 40 µmol/l (Planta Medica Số 42-1981).
Dựa vào các thành phần dược tính có giá trị cao trong chùm ngây, các công ty dược đã dùng
chùm ngây như một loại nguyên liệu tuyệt vời để bào chế thuốc, dược phẩm nhằm phục vụ
cho y học. Trên thị trường hiện nay có rất nhiều dược phẩm từ chùm ngây, đa số có nguồn gốc
từ Mỹ, ví dụ như thuốc bổ sung vitamin, thuốc bổ cho cho trẻ em, thuốc làm hạ đường huyết,
thuốc giảm stress…
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xvi
Hình 1.11 Sản phẩm dược phẩm từ chùm ngây
1.4.5. Mỹ phẩm:
Không chỉ được ứng dụng trong sản xuất thực phẩm và dược phẩm, chùm ngây còn được biết
đến và sử dụng rộng rãi trong công nghệ dưỡng da, mỹ phẩm cao cấp. Có thể kể đến một số sản
phẩm tiêu biểu như sữa rửa mặt, kem dưỡng ẩm, kem chống nhăn mắt, sữa dưỡng thể, xà phòng,
sữa tắm,… đa số đều có nguồn gốc từ châu Âu.
Hình 1.12 Sản phẩm mỹ phẩm từ chùm ngây
Một số ngành khác:
Dầu từ hạt chùm ngây ngoài việc dùng trong thực phẩm, mỹ phẩm, còn được ứng dụng sản
xuất dầu bôi trơn máy móc, thiết bị.
Trong công nghiệp, chùm ngây được xem là nguồn nguyên liệu tiềm năng cho kỹ nghệ giấy và
còn được dùng để sản xuất các chế phẩm màu xanh.Ngoài ra, vỏ cây còn có khả năng cung
cấp tanin, nhựa dầu và sợi thô.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xvii
Như vậy, dựa vào những nghiên cứu trước đó và những ứng dụng đa dạng của chùm ngây thì
việc tạo ra một sản phẩm nước uống từ lá cây này là rất khả thi, không chỉ giàu giá trị dinh
dưỡng mà còn tạo ra một sản phẩm mới lạ, góp phần đa dạng hóa thị trường đồ hộp nước rau
còn quá eo hẹp ở nước ta.
Hơn nữa, mới đây, một đề tài nghiên cứu về việc phát triển nước uống từ lá chùm ngây
“Development of Moringa Oleifera leaf beverage” của Phyllis Quarcoo (Kwame Nkrumah
university of science and technology) lại một lần nữa khẳng định rằng nước uống từ lá chùm
ngây là một loại nước mới rất có tiềm năng.
2. Tổng quan về hợp chất màu trong tự nhiên.
2.1. giới thiệu chung.
Chất lượng của sản phẩm thực phẩm không những bao hàm giá trị dinh dưỡng mà còn bao
gồm cả giá trị cảm quan. Màu sắc của sản phẩm thực phẩm là một chỉ số quan trọng của giá trị
cảm quan.
1: Chlorophyl
2: Carotenoid
3: Anthocyanin
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xviii
Hình 1: sự phân bố của các sắc tố trong tế bào
Màu của rau quả phụ thuộc vào các hợp chất chứa màu. Các hợp chất màu đó có thể chia ra 4
nhóm chính là:
Chlorophylls: diệp lục hay chất màu xanh lá.
Carotenoids: có trong lục lạp, cho quả và rau màu vàng, cam và màu đỏ.
Flavonoids: có trong không bào, có màu đỏ, xanh, vàng.
Betalains: có trong không bào tạo sắc tố màu vàng đỏ.
Nhiệm vụ chính của những sắc tố này là lôi cuốn côn trùng và động vật mang hạt giống từ nơi
này đến nơi khác. Đối với con người màu sắc trái cây là tiêu chuẩn đầu tiên để đánh giá chất
lượng trái cây. Vì thế, hiểu biết về các tính chất hóa sinh và sinh lý của các quá trình sinh tổng
hợp và dị hóa của các sắc tố là nền tảng để ta hiểu về cơ chế tạo màu của các sắc tố trong rau
trái. Hơn nữa hiểu biết về thành phần sắc tố cũng giúp ta đánh giá hiệu quả của các quá trình
xử lý sau thu hoạch trong việc giữ được màu sắc, chất lượng và kéo dài thời gian bảo quản rau
quả và các sản phẩm từ rau quả.
2.2. Phân loại.
Các chất màu tự nhiên trong nguyên liệu thực vật có thể chia thành nhiều nhóm dựa trên công
thức hóa học, thông thường các chất màu được chia thành 4 nhóm lớn bao gồm:
Phẩm màu là dẫn xuất của isoprene: Carotenoid, Xanthophylls, Lycopen…
Phẩm màu là dẫn xuất của tetrapyrrole: Chlorophyll, Porphyrin, Heme…
Phẩm màu là dẫn xuất của benzopyran: các chất màu thuộc họ Flavonoid.
Phẩm màu là dẫn xuất của các hợp chất khác: Betalain, Phenalone
Tuy nhiên hiện nay các nhà nghiên cứu, các nhà quản lý vẫn chưa thống nhất trong việc lập ra
một hệ thống phân loại chất màu do tính phức tạp và chồng chéo của nó. Trong thực vật nói
chung, chất tạo màu chủ yếu thuộc 3 họ lớn là họ chlorophyll tạo màu xanh lá cây, họ màu
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xix
carotenoid cho màu vàng đến đỏ tan trong dầu và họ flavonoid cho phổ màu rộng từ vàng đỏ
đến tím và tan tốt trong nước.
Vị trí Rau, trái Màu cơ bản Nhóm tạo màu
Cà rốt Cam, vàng, đỏ Carotenoid
Cây củ cải Đỏ, trắng hoặc xanh là cây Anthocyanin,
bền ngoài, màu trắng bên flavonoid
Rễ trong
Cây bà la môn Màu nâu bên ngoài, màu
trắng bên trong
Cây củ cải vàng Màu trắng bên ngoài
Cây cần tây Màu nâu bên ngoài, màu
trắng bên trong
Màu tía,vàng
Cây củ khoai lang ngọt Màu tím đỏ bên ngoài, Carotenoid,
màu trắng bên trong anthocyanin
Thân Cây măng tây Màu trắng và màu xanh lá Chlorophyll
cây
Củ khoai tây Đỏ, vàng, trắng, xanh là Chlorophyll,
cây, màu tía anthocyanin,
flavonoid
Lá Hành Trắng, đỏ Anthocyanin,
flvonoid
Tỏi Trắng – xanh Chlorophyll
Ngò tây Xanh là cây Chlorophyll
Cây thì là Trắng – xanh Chlorophyll
Rau diếp Xanh lá cây Chlorophyll
Cần tây Xanh lá cây Chlorophyll
Rau diếp xoắn Xanh hoặc trắng Chlorophyll
Trái Đậu Hà Lan Xanh lá cây Chlorophyll
Đậu xanh Xanh lá cây Chlorophyll
Trái bí ngô Trắng, vàng, cam, xanh Carotenoid, Chlorophyll
lá cây
Dưa leo Xanh lá cây Chlorophyll
Trá trứng gà Màu tía Anthocyanin,
flavonoid
Bắp Vàng, cam Carotenoid, anthocyanin
Cà chua Đỏ Carotenoid
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xx
Tiêu Vàng, đỏ, xanh Carotenoid
chlorophyll
Bảng 1. Sự
phân bố của các sắc tố trong rau trái
2.3. giời thiệu về Chlorophyll.
Chlorophyll là một sắc tố màu lục ở thực vật, tồn tại khắp nơi trong các bộ phận ăn được của
rau quả: rễ, thân, lá, hoa, quả, hạt và chồi.
Hình: sắc tố Chlorophyll trong lá cây chùm ngây
Chlorophyll tồn tại trong lục lạp, xúc tác cho phản ứng quang hóa sinh tổng hợp glucose từ
CO2 và H2O.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxi
Ở thực vật, Chlorophyll thường có khả năng che khuất các màu khác khiến cho lá cây có màu
xanh đặc trưng. Có vài trường hợp chlorophyll bị che bởi các màu khác. Nhưng trong quá
trình quả chín hoặc lá già thì màu xanh của chlorophyll bị mất đi, thay thế bằng màu của các
chất khác.
Hình 4: Cấu trúc và sự phân bố sắc tố chlorophyll trong lục lạp.
Chlorophyll là hợp chất của porphyrin gồm 4 vòng pyrol. Các vòng này phối trí với ion Mg2+.
Tại pyrol thứ 4, acid propionic liên kết với vòng pyrol và liên kết ester với phân tử rượu
phytol. Cấu tạo này giống với cấu tạo nhóm hemichromes của hồng cầu nhưng khác ở nguyên
tử trung tâm của hemichromes là Fe. Như vậy nguyên tử kim loại trung tâm có vai trò quyết
định trong sự tạo màu của hợp chất
Trong các loại cây thì tỉ lệ chlorophyll a và chlorophyll b biến đổi trong khoảng từ 1 đến 3, tùy
thuộc vào nhiếu yếu tố: loại cây và môi trường. Những cây tiếp xúc nhiều với ánh nắng mặt
trời thì các tỷ số chlorophyll a/chlorophyll b cao hơn những cây ít tiếp xúc với ánh nắng mặt
trời.
Trong thành phần của cây chlorophyll có tổ chức đặc biệt, phân tán trong nguyên sinh chất gọi
là lục lạp hoặc hạt diệp lục. Hạt diệp dục có 2 lớp màng thylakoid, trên 2 màng này là
chlorophyll liên kết với protein.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxii
2.3.1. Tính chất
Dưới tác dụng của nhiệt độ và acid của dịch bào, màu xanh bị mất đi là do protein bị đông tụ
làm cho liên kết cử chlorophyll và protein bị đức chlorophyll dễ dàng tham gia phản ứng:
Chlorophyll + 2HX Pheophytin + MgX2
màu chlorophyll màu pheophytin
Trong môi trường kiềm acid và muối acid của dịch bào bị trung hòa và môi trường kiềm làm
cho chlorophyll bị xà phòng hóa tạo rượu phytol, methanol và acid chlorophllinic. Các acid
cũng như mmuoois của chúng điều cho sản phẩm màu xanh đậm.
Chlorophyll a + kiềm Chlorophyllin + CH3OH + rượu phytol
Chlorophyll b + kiềm Chlorophyllite + CH3OH + rượu phytol
Trong một số cây còn có enzyme chlorophyllase cũng có thể thủy phân được một số liên kết
ester để giải phóng phytol và methanol. Các enzyme này thường được định vị trong các sắc
lạp, khá bền với nhiệt và chỉ được hoạt hóa trong thời gian chín.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxiii
Chlorophyll cũng có thể bị oxy hóa do:
Oxy và ánh sáng (quang oxy hóa).
Tiếp xúc với các lipid bị oxy hóa.
Tác dụng của enzyme lipoxydase.
Các quá trình oxi hóa này có thể xảy ra trong rau khi bảo quản ở đô ẩm tương đối dưới 30%.
Còn ở độ ẩm không khí cao hơn thì chlorophyll lại bị biến thành pheophytin.
Dưới tác dụng của Fe, Sn, Al, Cu thì Mg trong chlorophyll sẽ bị thay thế và sẽ cho các màu
sau:
Fe: cho màu nâu
Sn và Al: cho màu xám
Cu: cho màu xanh sáng
Rau muống xanh Rau muống xào có đồng
2.3.2. Những biến đổi của chlorophyll trong quá trình bảo quản và chế
biến rau quả
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxiv
2.3.2.1. Trong quá trình bảo quản
Rau quả giảm hay mất màu xanh là dấu hiệu của sự lão hóa sau khi thu hoạch. Tùy thuộc vào
sự biến đổi của chlorophyll mà màu của lá có thể chuyển từ xanh sang đỏ hay nâu. Các yếu tố
của môi trường có thể kiềm hảm hoặc thúc đẩy quá trình này.
2.4. Các yếu tố ảnh hưởng đến sự thay đổi chlorophyll trong quá
trình bảo quản:
(i) Loài thực vật :
Ở cải xong thỉ sự giảm hàm lượng chlorophyll nhanh hơn ở ngò tây.
Qủa có đỉnh hô hấp thì sự phá hủy chlorophyll trong quá trình chín diễn ra nhanh hơn quả
không có đỉnh hô hấp.
Hình 5: Hàm lượng chlorophyll ở cải xoong giảm nhanh hơn ngò tây
(ii) Enzyme:
Trong quá trình chín, các enzyme chlorophyllase, Mg-dechetase được hoạt hóa và thực hiện
các phản ứng làm biến đổi màu sắc của chlorophyll. Ngoài ra sự mất màu của chlorophyll còn
diễn ra song song với quá trình oxi hóa được xúc tác bởi các enzyme lipoxygenase,
peroxydase, oxygenase. Quá trình oxi hóa lipid bắt đầu bằng sự tích tụ các acid béo của màng
tế bào trong suốt quá trình chín. Các acid béo tự do có thể bị oxi hóa bởi lipoxygenase tạo
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxv
thành hydroperoxide sau đó hydroperoxide tiếp tục phản ứng với các thành phần khác, đặc biệt
là oxi hóa chlorophyll thành các hợp chất không màu.
(iii) Ethylene:
Ethylene có khả năng thúc đẩy nhanh quá trình chín, do đó nó cũng đẩy nhanh tốc độ mất
màu Chlorophyll ở rau quả.
Xoài xanh Xoài chín
Hình 6: sự biến đổi màu sắc của xoài trong quá trình bảo quản và chế biến
Khi chín màu chlorophyll bị mất đi và màu vàng β-caroten sẽ xuất hiện.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxvi
(iv) Nồng độ CO2
Nồng độ CO2 cao có thể cản trở việc giảm hàm lượng chlorophyll. Đồng thời nếu nồng độ
CO2 cao còn có khả năng ức chế tác dụng của ethylen.
(v) Bảo quản lạnh:
Làm lạnh là phương pháp hiệu quả để duy trì chất lượng rau quả trong thời gian bảo quản lâu
dài. Rau quả thường được chần trước khi bảo quản lạnh nhằm vô hoạt các enzymme làm mất
màu và hương vị. tuy nhiên một vài loại rau quả có thể làm lạnh thô như tỏi tây và cà rốt.
Trong quá trình bảo quản rau quả lạnh kéo dài thì hàm lượng chlorophyll giảm còn hàm lượng
chlorophyllide, pheophytin và pheophobide tăng. Nguyên nhân là do hoạt động của các
enzyme chlorophyllase và peroxydase.
Sự nhạt màu phụ thuộc vào nhiệt độ bảo quản, loại rau quả, thời gian làm lạnh.
Bông cải tươi Bông cải lạnh đông
Hình 7: sự biến đổi màu sắc của bong cải trong quá trình bảo quản
2.4.1.2. Trong quá trình chế biến
(i) Biến đổi trong rau quả fresh-cup
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxvii
Sau quá trình chế biến tối thiểu như cắt gọt thì tế bào rau quả bị phá vở lớp màng bảo vệ làm
cho các thành phần trong rau quả tiếp xúc với các tác nhân oxy, ánh sáng, vi sinh vật…gây
biến đổi chất lượng và thay đổi cảm quan màu sắc, trạng thái.
Chlorophyll rất nhạy cảm với ánh sáng, dưới tác dụng của ánh sáng chlorophyll bị phân hủy
tạo hợp chất đơn giản không màu. Đồng thời dưới tác dụng của oxy sẽ gây ra phản ứng quang
oxy hóa phá hủy chlorophyll.
Dưới tác động của ánh sáng và enzyme lipoxygenase, chất béo bị oxy hóa tạo các gốc tự do,
các gốc tự do này sẽ oxy hóa làm mất màu chlorophyll.
(ii) Biến đổi trong rau quả xử lý nhiệt
Chần
Rau quả có thể mất màu trong quá trình bảo quản lạnh là do hoạt tính của các enzyme
chlorophyllase và peroxydase. Ngoài ra dưới tác dụng của enzyme lipoxygenase sẽ hình thành
gốc hydroperoxy tự do làm mất màu chlorophyll.
Khi chần sẽ giúp vô hoạt các enzyme này làm màu chlorophyll ít bị biến đổi.
Khi chần quá mức sẽ tạo ra những màu không mong muốn cho sản phẩm vì khi đó rau quả bị
phyeophytin hóa hoàn toàn, hình thành phyropheophytin và phá hủy lục lạp.
Quá trình nấu
Tùy thuộc vào quá trình gia nhiệt mà sự biến đổi màu chlorophyll của rau quả khác nhau.
Quá trình nấu đậu Hà Lan trong nước khoảng 3 phút thì không có ảnh hưởng đáng kể
lên tổng hàm lượng chlorphyll và pheophytin.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxviii
Đóng hộp và thanh trùng
Trong quá trình đóng hộp và thanh trùng rau quả xanh màu của chlorophyll cuối cùng sẽ
chuyển đổi từ màu xanh sang màu olive.
Ví dụ: Ở 1210C trong 30 phút màu chlorophyll trong rau bina chuyển thành màu của
pheophytin.
Quá trình tách nước
Thời gian tách nước kéo dài và ở nhiệt độ cao dẫn đến sản phẩm có chất lượng không tốt.
Nguyên nhân là do hoạt động của enzyme và sự nhạt màu dần do tạo thành pheophytin.
Ví dụ: Trong rau ngò sấy khô ở nhiệt độ 80-90oC, 3-7% chlorophyll chuyển thành pheophytin.
(iii) Biến đổi trong rau quả muối và lên men
Muối và lên men rau quả là sự bảo quản bằng cách sử dụng acid. Acid thường được thêm vào
trong quá trình muối còn quá trình lên men thì tự sinh ra acid.
Trong môi trường acid và dưới tác động của enzyme cholorophyllase chlorophyll biến đổi
thành pheophytin và chlorophyllide biến đổi thành pheophorbide.
Hình 8: Rau xanh trước và sau quá trình lên men
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxix
2.4.2. Ứng dụng của chlorophyll trong chế biến thực phẩm
Chlorophyll
Phần lớn chlorophyll được sử dụng trong ngành thực phẩm, tạo màu cho các sản phẩm sữa,
dầu ăn, súp, chewing gum, các sản phẩm mứt và sản phẩm đóng hộp chủ yếu được bổ sung
dựa trên hàm lượng chất béo có trong thực phẩm.
3. Tổng quan phụ gia duy trì cấu trúc thực phẩm.
3.1. định nghĩa và giới thiệu chung.
Theo bộ y tế thì phụ gia thực phẩm (food additive) là những chất không được coi là thực
phẩm hoặc một thành phần của thực phẩm. Phụ gia thực phẩm có ít hoặc không có giá trị dinh
dưỡng, được chủ động cho vào với mục đích đáp ứng yêu cầu công nghệ trong quá trình sản
xuất, chế biến, xử lý, bao gói, vận chuyển, bảo quản thực phẩm. Phụ gia thực phẩm không bao
gồm các chất ô nhiễm hoặc các chất bổ sung vào thực phẩm với mục đích tăng thêm giá trị
dinh dưỡng của thực phẩm.
Tại Hoa kỳ, có khoảng gần 2500 chất gia phụ thực phẩm được cơ quan Thực Dược Phẩm chấp
nhận sử dụng rộng rãi. Việt Nam cũng có một “Danh mục tiêu chuẩn vệ sinh đối với lương
thực, thực phẩm” do Bộ Y Tế ban hành, trong đó có ghi rõ tên các chất gia phụ được phép
dùng, với giới hạn tối đa cho phép trong từng loại thực phẩm.
Trước khi được chấp nhận đưa ra sử dụng, nhà sản xuất phải thử nghiệm an toàn chất phụ gia
ở ba mức độ:
1) Thử xem có hay không tác dụng độc hại tức thì, bằng cách đưa chất đó vào cơ thể một con
vật thí nghiệm;
2) Thử trên hai nhóm súc vật với số lượng nhiều ít khác nhau trong vòng 90 ngày để quan sát
độc tính;
3) Thử nghiệm độc tính khi cho súc vật dùng liên tục trong 2 năm hoặc lâu hơn.
Phụ gia bao gồm các loại như : chất điều chỉnh độ acid, chất điều vị, chất ổn định, chất bảo
quản, chất chống đông vón, chất chống oxy hóa, chất chống tạo bọt, chất độn, chất ngọt tổng
hợp, chế phẩm tinh bột, enzyme, chất khí đẩy, chất làm bóng, chất làm dày, chất làm ẩm, chất
làm rắn chắc, chất nhũ hóa, phẩm màu, chất tạo bọt, chất tạo phức kim loại, chất tạo xốp, chất
xử lý bột.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxx
3.2. một số phụ gia duy trì cấu trúc dùng trong nghiên cứu.
3.2.1. Carboxymethylcellulose
Hợp chất CMC được sản xuất từ việc xử lý cenluloza với dung dịch NaOH và sau đó là phản
ứng Williamson:
như vậy CMC là một dẫn xuất quan trọng của cellulose được cấu tạo từ hợp chất cellulose kết
hợp với natri.
Hình : hợp chất Natri Carboxy methyl cellulose
Ngưỡng sử dụng: ADI 0 - 25mg/kg.
Liều dùng: 25 mg/kg thể trọng.
Các chế phẩm có những tính chất như CMC là:
•Metycelluloza
•Hydrometycelluloza
•Hydroxypropylmetylcelluloza, Metylentycellulose
3.2.1.1. Phương pháp sử dụng:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxxi
Độ chắc và tốc độ tạo đông phụ thuộc vào nồng độ CMC, độ nhớt của dung dịch và lượng
nhóm axetat thêm vào để tạo đông. Nồng độ tối thiểu để CMC tạo đông là 0,2% và của nhóm
axetat là 7% so với CMC.
Người ta sử dụng CMC như tác nhân tạo gel, làm dày, làm phồng, làm ổn định, làm chậm sự
kết tinh đường trong sản xuất các sản phẩm bích quy, sữa, thịt, đồ hộp, mì ăn liền.
Độ hòa tan: Độ hòa tan khác nhau với trọng lượng phân tử carboxymethylation. Nói chung,
cellulose methyl carboxy hòa tan trong nước, sucrose và clorua natri và ethanol, nhưng hòa tan
trong dầu thực vật và glycol propylene là giới hạn. Độ hòa tan giảm khi trọng lượng phân tử
và nồng độ ngày càng tăng, methyl hóa giảm .Độ tan dưới pH = 4
Công nghệ sử dụng trong thực phẩm: carboxy methyl cellulose nên được phân tán trong
nước nóng và làm lạnh để hydrate hóa các polysaccharide, giúp cắt các polymer trọng lượng
phân tử cao thành polymer trọng lượng phân tử thấp để làm giảm độ nhớt.
Độ nhớt của carboxy methyl cellulose là tương đối liên tục giữa pH 4 và 10.
Dạng thương phẩm CMC có dẫn xuất từ 0.4- 1,4. Tuy nhiên có loại cao hơn sử dụng cho các
sản phẩm đặc biệt. Dẫn xuất dưới 0.4 CMC không hòa tan trong nước, CMC dùng trong thực
phẩm có dẫn xuất 0.65- 0.95 và độ tinh khiết lớn hơn 99.5%.
Với CMC dẫn xuất 0.95 và nồng độ tối thiểu 2% cho độ nhớt 25 Mpa tại 250C. Có thể sử dụng
CMC ở dạng nóng hoặc lạnh. CMC là các anion polyme mạch thẳng cho chất lỏng gọi là dung
dịch giả.
Dung dịch 1% thông thường pH = 7- 8.5, còn ở pH = 5- 9 dung dịch ít thay đổi, ở pH < 3 độ
nhớt tăng, thậm chí kết tủa. Do đó, không sử dụng CMC cho các sản phẩm có pH thấp, pH > 7
độ nhớt giảm ít.
Dung dịch CMC có thể bị phá hủy do các vi sinh vật hoặc enzyme khử. Gia nhiệt ở 800C trong
30 phút hoặc 1000C trong 1 phút có thể khử các tác nhân vi sinh vật mà không ảnh hưởng đến
chất lượng CMC. Độ nhớt CMC giảm khi nhiệt độ tăng, tác dụng có tính thuận nghịch.
Độ nhớt của CMC còn chịu ảnh hưởng bởi
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxxii
các ion kim loại:
+ Cation hóa trị I: ít tác dụng ở điều kiện bình thường ( trừ Agar+ )
+ Cation hóa trị II: Ca2+, Mg2+, làm giảm độ nhớt.
+ Cation hóa trị III: Al3+, Cr3+, Fe3+ tạo gel.
Nói chung, tác dụng trên độ nhớt của các loại muối tùy thuộc vào phương pháp thêm vào.
CMC có thể dễ dàng kết hợp với các thành phần hóa học thực phẩm như: đường, protein, tinh
bột và hầu hết các polyme trung tính.
3.2.1.2. Ứng dụng CMC và các dẫn suất cellulose
Cellulose và các dẫn xuất từ cellulose được sử dụng nhiều trong chế biến thực phẩm hơn 10
năm nay. Hiện tại việc sử dụng không ngừng phát triển không những trong việc cải thiện tính
chất sản phẩm mà còn góp phần vào việc sáng tạo các sản phẩm mới. Tính chất tan của dẫn
xuất cellulose trong nước là nguyên nhân làm thay đổi tính chất lưu biến học của thực phẩm,
kết quả là cải thiện được cấu trúc, tạo dáng cho sản phẩm…
Tùy thuộc vào điều kiện sử dụng các dẫn suất cellulose có thể có các chức năng sau: giữ nước,
tạo đặc, ổn định sản phẩm, trợ phân tán,…Vì vậy dùng dẫn xuất celluloza cho một sản phẩm
có một công dụng hoặc nhiều công dụng phát huy cùng lúc. Liều lượng thường sử dụng ở mức
độ nhỏ hơn 1% (thường 0.1-0.5%). Dẫn xuất celluloza sử dụng nhiều trong công nghiệp sản
xuất nước uống, bánh, sản phẩm sữa, mì sợi,…
(i) Dùng trong sản xuất kem và các sản phẩm cùng loại
Kem chứa 10% chất béo, 11% sữa không béo, 15% đường; 0,2 – 0,3% chất ổn định; 0,25 –
0,5% chất nhũ hóa. Các thành phần trên thay đổi tùy theo từng Quốc gia và từng yêu cầu sản
phẩm nhưng chất ổn định không vượt quá 0,5 %. Hiện nay chất dùng làm đặc là CMC, khi hòa
tan sẽ tạo dung dịch có độ nhớt cao, CMC có khả năng làm chậm quá trình kết tinh, làm mịn
tinh thể, cải thiện độ bóng, ngăn cản kem chảy.
(ii) Trong nước uống
Việc sử dụng riêng rẽ hoặc kết hợp với các chất keo khác dùng để giữ ổn định các pha rắn
trong dung dịch. Ngoài ra nó còn có khả năng ngăn cản phân ly tinh dầu/nước trong các sản
phẩm nước quả. Nồng độ thường sử dụng là 1%.
(iii) sản xuất bánh kẹo và các sản phẩm từ tinh bột
Cải thiện được tính chất bột nhào cũng như các sản phẩm, được sử dụng ở nồng độ 0,1 – 0,5%
trên trọng lượng chất khô. Hợp chất CMC có tác dụng làm mềm khối bột nhào, giữ ẩm, kéo
dài thời gian bảo quản, làm sản phẩm dễ trở lại trạng thái ban đầu, chống dính...
(iv) Trong sản xuất các dạng nước sốt
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxxiii
Do CMC tạo sệt tốt nên CMC có thể được dùng để sản xuất các sản phẩm như nước sốt salad,
sốt cà. Chất CMC thích hợp cho các sản phẩm này vì tính hòa tan tốt trong nước lạnh lẫn nước
nóng, có khả năng liên kết với nước tốt và chịu được ở pH thấp.
Nước sốt salad: CMC thường dùng là 7HOF nồng độ 1 % khi thành phần dầu là 30% hay 0,75
% khi thành phần dầu khoảng 50%.
Nước sốt cà chua: tùy theo loại CMC sử dụng mà ta có được các sản phẩm có cấu trúc khác
nhau. Loại 7HOF sẽ cho sản phẩm có cấu trúc dài, còn loại 7HXFMA sẽ cho sản phẩm có cấu
trúc ngắn hơn và mềm hơn.
Nhìn chung, CMC là một hợp chất có vai trò quan trọng trong công nghiệp thực phẩm, việc
phát triển và cải thiện tính chất của CMC góp phần quan trọng đối với công nghiệp sản xuất
thực phẩm.
3.2.2. Pectin
3.2.2.1. Nguồn gốc và cấu tạo:
Pectin là một polysaccharide tồn tại phổ biến trong thực vật, là thành phần tham gia xây
dựng cấu trúc tế bào thực vật. Ở thực vật pectin tồn tại chủ yếu ở 2 dạng là pectin hóa
tan và protopectin không hòa tan. Dưới tác dụng của acid, emzyme protopectin hoặc khi
gia nhiệt thì protopectin chuyển thành pectin.
Pectin là hợp chất cao phân tử polygalactoronic có đơn phân tử là galactoronic và rượu
metylic. Cấu tạo phân tử pectin là một dẫn xuất của acid pectic, acid pectic là một
polymer của acid D-galacturonic liên kết với nhau bằng liên kết 1-4 glycozide.
Cấu tạo pectin
3.2.2.2. Tính chất và khả năng tạo gel của pectin
Dạng bột màu trắng hoặc hơi vàng, tan trong nước, có khả năng tạo gel bền.
Hợp chất pectin được đặc trưng bởi hai chỉ số quan trọng là chỉ số methoxyl thể hiện cho
phần trăm khối lượng nhóm methoxyl –OCH3 có trong phân tử pectin và chỉ số ester hóa
“DE” thể hiện mức độ ester hóa của các phân tử acid galactoronic trong phân tử pectin.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxxiv
Dự trên mức độ methoxyl hóa và ester hóa,trong thương mại chia pectin thành 2 loại
pectin có độ methoxyl hóa cao và pectin có độ methoxyl hóa thấp.
Pectin methoxyl hóa cao (High Methoxyl Pectin-HMP): DE> 50% hay MI>7% chất này
có thể làm tăng độ nhớt cho sản phẩm. muốn tạo đông cần phải có điều kiện pH = 3.1 –
3.4 và nồng độ đường trên 60”%.
Hình : Hight Methoxyl Pectin
Pectin có độ methoxyl hóa thấp ( Low Methoxyl Pectin- LMP): DE <50% hay MI < 7%.
Được sản xuất bằng cách giảm nhóm methoxyl trong phân tử pectin. Pectin methoxy
thấp cò thể tạo đông trong môi trường không có đường. Chúng thường được dùng làm
màng bao bọc cho các sản phẩm.
3.2.2.3. ứng dụng:
Pectin là tác nhân tạo gel quan trọng nhất được sử dụng để tạo ra cấu trúc gel cho thực
phẩm,chủ yếu là những thực phẩm có nguồn gốc từ rau quả. Khả năng tạo gel của nó còn được
sử dụng ở những thực phẩm cần có sự ổn định của nhiều pha, hoặc trong sản phẩm cuối hoặc
ở một giai đoạn tức thời trong quy trình sản xuất.
Tác dụng tạo đặc của pectin được sử dụng chủ yếu ở những loại thực phẩm mà quy định
không cho phép sử dụng những loại gum có giá thành rẻ hơn hay ở những loại thực phẩm cần
có một hình dáng thật tự nhiên.
Mứt trái cây và mứt đông:
Vai trò của pectin là nhằm tạo ra một cấu trúc cho mứt đông và mứt trái cây để những sản
phẩm này khi được vận chuyển vẫn không thay đổi cấu trúc, tạo ra mùi vị thơm ngon cho sản
phẩm, và giảm đến tối đa sự phân rã. Quá trình sản xuất mứt đông và mứt trái cây phải đảm
bảo tạo ra sự phân bố đồng đều của các phân tử trong pha liên tục ngay từ khi quá trình khuấy
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxxv
trộn ngừng lại. Hàm lượng pectin sử dụng trong mứt và mứt đông thường trong khoảng từ 0,1
– 0,4%.
Pectin có khả năng tạo gel nhanh có giá trị đặc biệt trong sản xuất mứt vì yêu cầu của sản
phẩm phải được tạo gel, tạo đặc trước khi đóng hộp. Còn mứt đông trái cây tốt nhất khi chúng
không bị tác động trong suốt quá trình tạo gel. Đó là lý do pectin tạo gel chậm được sử dụng,
và các khâu vào hộp, đóng nắp, dán nhãn, xếp chồng phải được thực hiện trước khi quá trình
tạo gel diễn ra.
Quá trình tạo gel của pectin có thể được tạo ra trong một quy trình lạnh bằng 2 cách:
Trộn syrup đường pectin có hàm lượng chất khô hòa tan từ 60 – 65%, pH = 3,8 -4,2 với dịch
acid trái cây để đạt được pH = 3,0.
Trộn dung dịch pectin có pH = 2,9 và lượng chất khô hòa tan là 25% với syrup đường để thu
được hỗn hợp mới có hàm lượng chất khô 23%.
LMP thường được ứng dụng trong mứt trái cây có hàm lượng chất khô hòa tan < 55%. Loại
LMP được chọn dựa trên hàm lượng chất khô và pH trong sản phẩm. Trong những sản phẩm
có hàm lượng chất khô rất thấp, ví dụ như mứt trái cây không đường cho người bị bệnh tiểu
đường, LMP khó tạo đủ liên kết với nước và carrageenan thích hợp hơn. Trong một số trường
hợp người ta có thể sử dụng cả pectin và carragenan.
3.3. Carrageenan.
3.3.1. Lịch sử phát hiện carrageenan
Carrageenan bắt đầu được sử dụng hơn 600 năm trước đây, được chiết xuất từ rêu Irish
moss tại một ngôi làng bên bờ biển phía nam Ireland trong một ngôi làng mang tên Carraghen.
Vào những năm 30 của thế kỷ XX, carrageenan được sử dụng trong công nghiệp bia và hồ sợi.
cũng trong thời kỳ này những khám phá về cấu trúc hóa học của carrageenan được tiến hành
mạnh mẽ.
Ngày nay, sản xuất công nghiệp carrageenan không còn giới hạn vào chiết tách từ Irish moss,
mà rất nhiều loài rong đỏ thuộc ngành Rhodophyta đã được sử dụng. Những loài này gọi
chung là Carrageenophyte. Qua nhiều nghiên cứu, đã có hàng chục loài rong biển được khai
thác tự nhiên hay nuôi trồng để sản xuất carrageenan.
3.3.2. Cấu trúc của Carrageenan
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxxvi
Carrageenan là một polysaccharide của galactose –galactan. Ngoài mạch polysaccharide chính
còn có thể có các nhóm sulfat được gắn vào carrageenan ở những vị trí và số lượng khác nhau.
Vì vậy, carrageenan không phải chỉ l à một polysaccharid đơn lẻ, có cấu trúc nhất định mà là
các galactan sulfat. Mỗi galactan sulfat là một dạng riêng của carrageenan và có ký hiệu riêng.
Ví dụ: λ – , κ –, ι –, ν – carrageenan
Trong quá trình chiết tách, do tác động của môi trường kiềm các μ-,ν-,λ-carrageenan dễ
chuyển hóa thành κ-, ι-, θ- carrageenan tương ứng. Các carrageenan có mức độ sulfat hóa
khác nhau, thí dụ κ–carrageenan (25 % sulfat), ι–carrageenan (32 % sulfat), λ–carrageenan (35
% sulfat). Các sản phẩm này đã được thương mại hóa, chiếm vị trí quan trọng trong thị trường
polysaccharide
Hình: Sự chuyển hóa cấu trúc Carrageenan.
3.3.3. Tính chất của Carrageenan.
Carrageenan có một tính chất vô cùng quan trọng là tạo gel ở nồng độ thấp (nhỏ hơn 0,5 %). Ở
dạng gel các mạch polysaccharide xoắn v òng như lò xo và cũng có thể xoắn với
nhau tạo thành khung xương không gian ba chi ều vững chất, bên trong có thể chứa nhiều
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxxvii
phân tử nước (hay dung môi). Từ dạng dung dịch chuyển sang dạng gel l à do tương tác giữa
các phân tử polyme hòa tan với các phân tử dung môi ở bên trong, nhờ tương tác này mà gel
tạo thành có độ bền cơ học cao. Phần xoắn vòng lò xo chính là những mầm tạo gel, chúng lôi
kéo các phân tử dung môi vào vùng liên kết.
Sự hình thành gel có thể gây ra bởi nhiệt độ thấp hoặc th êm các cation với một nồng
độ nhất định. Quá trình hình thành gel diễn ra phức tạp, được thực hiện theo hai bước:
- Bước 1: khi hạ nhiệt độ đến một giới hạn n ào đó trong phân tử carrageenan có sự
chuyển cấu hình từ dạng cuộn ngẫu nhiên không có trật tự sang dạng xoắn có trật tự. Nhiệt độ
của quá trình chuyển đổi này phụ thuộc vào dạng và cấu trúc các carrageenan, cũng như phụ
thuộc vào dạng và nồng độ của muối thêm vào dung dịch carrageenan. Do đó, mỗi một dạng
carrageenan có một điểm nhiệt độ tạo gel riêng.
- Bước 2: gel của các polyme xoắn có thể thực hiện ở các cấp độ xoắn. Trong tr ường
hợp đầu, sự phân nhánh và kết hợp lại sẽ xuất hiện cấp độ xoắn thông qua sự h ình thành
không đầy đủ của xoắn kép, theo hướng đó mỗi chuỗi tham gia vào xoắn kép với hơn một
chuỗi khác. Trong trường hợp thứ hai, các phần đã phát triển đầy đủ của đa xoắn tụ hợp lại tạo
thành gel. Còn dưới các điều kiện không tạo gel, ở các nồng độ polyme thấp sự hình thành và
hợp lại của các xoắn sẽ dẫn đến tăng độ nhớt.
Qua đó, có thể mô tả cơ chế tạo gel như sau: trước hết là xuất hiện sự chuyển đổi cấu
hình từ dạng cuộn sang xoắn lò xo, tiếp sau là sự kết hợp các xoắn và tụ hợp lại có trật tự tạo
thành xoắn kép – gel. Như vậy, gel là tập hợp các xoắn có trật tự hay còn gọi là xoắn kép.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxxviii
3.3.4. ứng dụng của carrageenan.
Carrageenan được sử dụng ở nhiều dạng khác nhau trong nhiều sản phẩm mà chúng
ta sử dụng hàng ngày, nhất là trong lĩnh vực thực phẩm và bánh kẹo.
Các sản phẩm có sử dụng carrageenan đã được sử dụng phổ biến trong nhiều thế kỹ. Nhiều
nghiên cứu đã chứng minh độ an toàn của carrgeenan, nó không gây độc, không có dấu hiệu
gây viêm loét trên cơ thể và có thể sử dụng trong thực phẩm với một l ượng không giới hạn.
Tổ chức FDA của Mỹ đã xếp carrageenan vào danh mục các chất an toàn đối với các sản
phẩm thực phẩm. Tính phổ biến của carrageenan đ ược thể hiện ở 4 đặc điểm sau:
Tham gia như một chất tạo đông đối với một số sản phẩm như: kem, sữa, bơ…
Làm bền nhũ tương, giúp cho dung dịch ở trạng thái nhũ tương cân bằng với nhau mà không
bị tách lớp.
Có thể thay đổi kết cấu của sản phẩm với tính chất hóa lý, cơ học mong muốn tạo ra các sản
phẩm đông đặc có độ bền dai.
Giúp ổn định các tinh thể trong các sản phẩm bánh kẹo ngăn chặn đường và nước đá bị kết
tinh.
Chính vì vậy, carrageenan được ứng dụng rộng rãi trong các ngành kinh tế quốc dân.Góp phần
đa dạng hóa các sản
phẩm thực phẩm.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xxxix
Tỉ lệ sử dụng carrageenan trong các sản phẩm khác nhau.
3.4. Xanthan Gum.
3.4.1. Nguồn gốc
Xanthan gum (polysaccharide gum) là dẫn xuất thu được trong quá trình lên men của vi sinh
vật chủng Xanthomonas campestris và tinh khiết bằng cồn isopropyl (năm 1940 tại Mỹ).
+ Khối lượng phân tử: 3- 50.106, Xanthan gum có cấu trúc phức tạp: bao gồm sự liên kết của
đường D-glucose, D-maltose và D-glucuronic acid.
+ Chủng vi sinh vật Xanthomonas campestris là chủng không gây độc cho cả người và súc vật.
Ngưỡng sử dụng: Tiêu chuẩn tinh khiết dùng cho thực phẩm là dư lượng cồn isopropylic
không được vượt quá 750ppm. Dung dịch chứa 1% Xanthan gum và 1% KCl quấy trộn trong
2h đạt độ nhớt tối thiểu tại nhiệt độ 750F là 600 centipolaes trên máy đo độ nhớt Brookfield
Viscometer LVF…
3.4.2. Phương pháp sử dụng:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xl
Phụ gia được dùng trong chế biến thực phẩm tạo ổn định, tạo nhũ tương, tăng độ dày, tăng bọt,
chịu được nhiệt.
Thực phẩm sử dụng: súp, xirô, đồ uống (nước uống có chanh), các sản phẩm từ sữa (sữa
đông), thực phẩm khô, thực phẩm đóng gói (thịt đông, đồ hộp ) và tất cả các sản phẩm thực
phẩm khác.
3.4.3. ứng dung trong thực phẩm:
Xanthan nên được phân tán trong nước lạnh và đun nóng đến 800C trong 10 phút để hydrat
hóa các polysaccharide thành những polymer phân tử nhỏ, làm cho độ nhớt dung dịch bị giảm
xuống.
Các hình thức tập hợp xoắn đơn hoặc đôi của Xanthan tạo thành dạng gel yếu. Sự hình thành
gel yếu này biểu hiện như là một điểm năng suất cao, giúp các hạt ruspend (các loại thảo mộc,
khối trái cây, những giọt nhũ tương) trong dung dịch nhớt đồng nhất. Tương tác kết hợp với
gelatin và gum Arabic. Các hình thức tạo gel giống với locust bean gum và guar gum.
Độ tan % ở nhiệt độ / pH kết hợp khác nhau:
Xanthan hòa tan trong các dung dịch nước, sucrose, natri clorua và ethanol. Nhưng hòa tan
trong dầu thực vật và propylene glycol thì còn bị hạn chế.
Độ hòa tan giảm dần khi trọng lượng phân tử và nồng độ ngày càng tăng. Độ hòa tan tốt ở pH
= 4- 8.
Nhiệt độ cao sẽ cải thiện đáng kể sự phân tán xanthan trọng lượng phân tử cao.
Hình 2.6 : Xanthan gum
3.5. Guar Gum
3.5.1. Nguồn gốc
Guar gum có trong thành phần nội nhũ của hạt
Cyamopsis tetragonolobus, thuộc họ
Leuguminose, với lượng gần 35% được
trồng chủ yếu ở ấn độ, Paskistan và mỹ. Bột Guar
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xli
gum chứa 10-15% ẩm, 5-6% protein; 2.5% xơ; 0.5-0.8% tro.\
nhận gum bằng cách rửa với ethanol hay isopropanol; hay hòa tan trong nước sôi, sau đó lọc,
cô đặc và sấy.
3.5.2. ngưỡng sử dụng:
Guar gum là phụ gia có mức độ độc hại nhẹ. Mức độ giới hạn đối với một số sản phẩm như
0.35% (bánh nướng), 1.2% (ngũ cốc), 0.8% (phô mai), 0.5% (các thực phậm khác)
3.5.3. Cấu tạo và tính chất:
Guar gum là galactomanan gồm mạch chính do các gốc D-mannose kệt hợp lại với nhau bằng
liên kết β-1,4 và các gốc D-galactose nối với D-mannose của mạch chính bằng liên kết α-1,6.
Tỉ lệ galactose:mannose là 2:1.
Guar gum có khả năng hút nước mạnh và có thể liên kết với các phần tử liền kề, kết quả là
tạo ra độ nhớt dung dịch .
3.5.4. Ứng dụng của Guar Gum trong thực phẩm.
3.6. Alginate
3.6.1. Nguồn gốc:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xlii
Alginate được Standford phát hiện ra năm 1881, là một acid hữu cơ có trong tảo nâu, trọng
lượng phân tử từ 32000 – 200000. Cấu tạo hóa học của acid alginic gồm 2 phần tử β-D
mannuronic và α – L – guluronic acid liên kết với nhau bằng liên kết 1- 4 glucozid.
Acid alginic được chiết xuất ra từ tảo nâu dưới dạng natri alginat, alginat có trọng l ượng
phân tử 20000 – 60000.
Hình: β-D mannuronic Hình : α – L – guluronic acid
3.6.2. đặc tính của Alginate
Độ nhớt: khi hóa tan các Alginate vào nước chúng sẽ ngậm nước và tạo dung dịch nhớt. độ
nhớt phụ thuộc vào chiều dài của Alginate. Bột Alginate rất dễ bị giảm nếu không được bảo
quản ở nhiệt độ thấp. Ngoài ra, cách sắp xếp của phân tử Alginate cũng ảnh hưởng đến độ
nhớt của nó.
Độ nhớt cao độ nhớt thấp
3.6.3. sự tạo gel của Alginate
Các alginat có khả năng tạo gel khi có mặt của ion Ca 2+ và acid. Gel được thành lập có thể
kiểm soát thông qua sự giải phóng ion Ca 2+, hoặc acide trong dung dịch alginat. Có thể tạo
gel acide ở pH < 4 (khoảng 3.4) th ường dùng kết hợp với với pectin (HMP). Tham gia tạo gel
các tương tác tĩnh điện qua cầu nối Ca2+ có vai trò quan trọng, vì thế các gel nàykhông thuận
nghịch với nhiệt và ít đàn hồi.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xliii
3.6.4. ứng dụng của Alginate
các Alginate cũng được ứng dụng rộng rãi trong công nghiệp thực phẩm. Thường natri
Alginate được sử dụng nhiều nhất và là hợp chất tạo kết cấu cho nhiều sản phẩm. Trong sản
phẩm natri Alginate là chất làm đặc, làm dày để ổn định các bọt cũng như để tạo cho nước quả
đục những thể đặc biệt.
Với những thực phẩm có độ acid cao không thể d ùng natri alginat được thì propylenglycol
alginat là chất thay thế rất tốt vì nó bền được cả trong vùng pH = 0 – 3. Một
hợp chất của acid alginic có t ên là lamizell một alginat kép của natri và canxi với một tỷ
lượng nhất định. Lamizell tạo ra đ ược một độ nhớt đặc biệt và cho khả năng ăn ngon
miệngcũng được quan tâm trong sản xuất thực phẩm
4. Quá trình thanh trùng, tiệt trùng.
4.1. cơ sở khoa học:
Nhiều loài vi sinh vật khác nhau được tìm thấy trong thực phẩm và nguyên liệu chế biến thực
phẩm. Dựa vào khả năng sinh tổng hợp độc tố và gây bệnh, hệ vi sinh vật trong thực phẩm có
thề chia thành hai nhóm:
Nhóm vi sinh vật có khả năng sinh tổng hợp độc tố và gây bệnh cho người nếu thực phẩm bị
nhiễm nhóm vi sinh vật này thì có thể gây ngộ độc cho người sử dụng. Đứng từ góc độ vệ
sinh an toàn thực phẩm thì đây là nhóm vi sinh vật có hại và chúng ta cần phải áp dụng những
giải pháp kĩ thuật trong quy trình sản xuất để chúng không bị nhiễm vào thực phẩm.
Nhóm vi sinh vật không có khả năng sinh tổng hợp độc tố : nhóm vi sinh vật này hoặc không
có ảnh hưởng xấu hoặc có ảnh hưởng tốt tới sức khỏe người tiêu dùng( ví dụ như
Lactobacillus bulgaricus và Streptococcus thermophilus trong sữa chua yaourt có ảnh hưởng
tốt đến quá trình tiêu hóa thức ăn trong đường ruột ở người). Tuy nhiên, khi nhóm vi sinh vật
này có mặt trong thực phẩm, chúng sẽ thực hiện quá trình trao đổi chất, từ đó gây ra những
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xliv
biến đổi về thành phần hóa học và giá trị cảm quan của thực phẩm. Kết quả là chất lượng thực
phẩm nhanh chóng bị biến đổi theo thời gian bảo quản.
Ngoải ra, chúng ta cũng cần lưu ý đến sự có mặt của các enzyme trong thực phẩm vì chúng sẽ
gây ra những biến đổi hóa sinh và cảm quan, từ đó làm thay đổi các chỉ tiêu chất lượng của
thực phẩm trong quá trình bảo quản.
Tiệt trùng là quá trình tiêu diệt toàn bộ vi sinh vật ( ở dạng tế bào sinh dưỡng hoặc bào tử) và
ức chế không thuận nghịch các enzyme trong thực phẩm. Sau quá trình tiệt trùng, sản phẩm sẽ
trở thành vô trùng. Như vậy, quá trình tiệt trùng không những đảm bảo cho thực phẩm an toàn
về mặt vi sinh mà còn kéo dài thời gian bảo quản thực phẩm, giúp ổn định về các chỉ tiêu chất
lượng của thực phẩm trong một khoảng thời gian dài sau sản xuất.
Tuy nhiên, quá trình tiệt trùng cũng gây ra những biến đổi bất lợi, làm ảnh hưởng xấu đến giá
trị dinh dưỡng và cảm quan của thực phẩm. Trong một số trường hợp, các nhà sản xuất lựa
chọn quá trình thanh trùng để thay thế cho quá trình tiệt trùng.
Thanh trùng là quá trình tiệu diệt các vi sinh vật gây bệnh trong thực phẩm và ức chế quá
trình sinh tổng hợp độc tố của chúng. Chế độ xử lý trong quá trình thanh trùng “ nhẹ nhàng
hơn” so với quá trình tiệt trùng ( ví dụ như đối với phương pháp xử lý nhiệt thì nhiệt độ và
thời gian thanh trùng sẽ thấp hơn so với trường hợp tiệt trùng). Do đó, quá trình thanh trùng
không làm tổn thất đáng kể giá trị dinh dưỡng và cảm quan của thực phẩm. Tuy nhiên, sau quá
trình thanh trùng , hệ vi sinh vật trong thực phẩm vẫn chưa bị tiêu diệt hết, đặc biệt là nhóm vi
sinh vật chịu nhiệt và vi sinh vật có khả năng sinh bào tử. Một số vi sinh vật có khả năng
sinh tổng hợp độc tố gây bệnh cho người đôi khi vẫn còn tồn tại trong thực phẩm sau thanh
trùng( ví dụ như giống Bacillus và Clostridium).
Trong điều kiện sản xuất quy mô lớn, việc xử lý thực phẩm trở nên vô trùng rất khó thực hiện.
Do đó, các nhà sản xuất thực phẩm đã đưa ra khái niệm “thực phẩm vô trùng công nghiệp”.
Những thực phẩm này chưa đạt mức độ vô trùng tuyệt đối nhưng không chứa vi sinh vật gây
bệnh, còn những vi sinh vật không gây bệnh và không sinh tổng hợp độc tố thì có thể vẫn còn
sống sót trong thực phẩm nhưng với số lượng rất hạn chế. “Thực phẩm vô trùng công nghiệp”
có thể bảo quản trong thời gian tối thiểu là 6 tháng trong những điều kiện xác định mà vẫn
không thay đổi các chỉ tiêu chất lượng về dinh dưỡng và cảm quan.
4.2. Các yếu tố ảnh hưởng
Hai thông số công nghệ quan trọng nhất trong quá trình thanh trùng và tiệt trùng nhiệt là nhiệt
độ và thời gian. Nếu nhiệt độ trong sản phẩm không đồng nhất trong quá trình thanh trùng /
tiệt trùng thì các nhà sản xuất sẽ quan tâm đến nhiệt độ tại tâm sản phẩm. Cần lưu ý là giá trị
nhiệt độ tại tâm sản phẩm không phải là một hằng số trong quá trình thanh trùng và tiệt trùng.
Các nhà sản xuất cần xác định một chế độ thanh trùng/ tiệt trùng hợp lý để chất lượng sản
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xlv
phẩm đảm bảo an toàn vệ sinh đồng thời giá trị dinh dưỡng và cảm quan của sản phẩm cũng
đạt yêu cầu. Việc lựa chọn chế độ thanh trùng/tiệt trùng sẽ phụ thuộc vào những yếu tố sau:
4.2.1. Hệ vi sinh vật trong thực phẩm
Mẫu thực phẩm trước khi đưa vào thanh trùng hoặc tiệt trùng luôn chứa một hệ vi sinh vật .
Các nhà sản xuất cần quan tâm đến các loài vi sinh vật bị nhiễm và mật độ của chúng trong
mẫu thực phẩm. Theo lý thuyết, nếu các loài vi sinh vật nhiễm thuộc nhóm ưa nhiệt thì chế độ
thanh trùng/ tiệt trùng cẩn phải “ nghiêm ngặt” thì mới tiêu diệt được chúng. Khả năng chịu
nhiệt của một loài vi sinh vật thường được đánh giá dựa trên giá trị “ thời gian phá hủy thập
phân”. Ví dụ như loài Clostridium thermosaccharolyticum có giá trị D121oC= 3- 4. Ngoài ra,
mật độ vi sinh vật trong mẫu ban đầu càng cao thì việc tăng nhiệt độ và thời gian xử lý là cần
thiết để đảm bảo sản phẩm có xác suất tái nhiễm thấp. Do đó, việc tuân thủ các quy phạm về
vệ sinh trong quy trình sản xuất là rất cần thiết để khống chế mật độ vi sinh vật trong mẫu
thực phẩm trước khi thực hiện quá trình thanh trùng/tiệt trùng luôn ở mức thấp nhất.
4.2.2. Trạng thái vật lý của thực phẩm
Thực phẩm lỏng có hệ số truyền nhiệt cao hơn thực phẩm rắn vì trong quá trình thanh trùng và
tiệt trùng sẽ xuất hiện các dòng đối lưu trong sản phẩm. Các chỉ tiêu như hàm lượng chất khô,
độ nhớt....sẽ ảnh hưởng đến hệ số truyền nhiệt của thực phẩm lỏng. Đối với thực phẩm rắn, sự
truyền nhiệt xảy ra chủ yếu là do sự dẫn nhiệt.
4.2.3. Thành phẩn hóa học của thực phẩm
Việc chọn chế độ thanh trùng/tiệt trùng sẽ phụ thuộc vào giá trị pH hay độ chua sản phẩm.
Những thực phẩm lỏng có giá trị pH cao như sữa tươi (pH ≥ 4,5) thì giá trị nhiệt độ xử lý
thường không thấp hơn 100oC để sản phẩm đạt được độ vô trùng công nghiệp. Ngược lại,
những sản phẩm có giá trị pH khá thấp (pH= 3,7-4,5) như nước ép từ nhóm trái cây có múi
hoặc pH thấp (pH<3,7 ) như một số loại rượu vang, rau trái dầm giấm...thì có thể thanh trùng
ở nhiệt độ thấp nhưng vẫn đảm bảo được vô trùng công nghiệp.
Trong số các thành phần hóa học của thực phẩm , cần lưu ý đến chất béo vì chúng có hệ số
dẫn nhiệt thấp.
4.2.4. Phương pháp thanh trùng và tiệt trùng
Các phương pháp thanh trùng và tiệt trùng nhiệt có thể được chia thành hai nhóm: xử lý sản
phẩm trong bao bì và xử lý sản phẩm ngoài bao bì.
Riêng phương pháp xử lý sản phẩm ngoài bao bì thường chỉ áp dụng cho nhóm thực phẩm
lỏng. Phương pháp này được sử dụng kết hợp với phương pháp rót sản phẩm vào bao bì vô
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xlvi
trùng trong điều kiện vô trùng. Tùy theo tính chất của sản phẩm và vốn đầu tư mà các nhà sản
xuất cần lựa chọn phương pháp thanh trùng/tiệt trùng phù hợp.
4.3. giá trị D, z của vi sinh vật chỉ thị.
Trị số D và trị số Z được ứng dụng rộng rãi trông công nghiệp chế biến thực phẩm. Cần xử lý
nhiệt để đủ mức diệt được vi khuẩn chỉ thị gây hư hỏng thực phẩm.
D là thời gian phá hủy thập phân (decimal reduction time). Nói cách khác D là khoảng thời
gian cần thiết để thực hiện quá trình thanh trùng tiệt trùng ở nhiệt độ T để tổng số tế bào vi
sinh vật trong mẫu thực phẩm khảo sát sẽ giảm đi 10 lần.
D có thể được tính theo công thức sau:
T
D
log 10 N 0 log 10 N1
Trong đó N0: là số tế bào vi sinh vật ban đầu
N1: số tế bào vi sinh vật sau quá trình thanh trùng.
T: là thời gian thực hiện quá trình thanh trùng.
Z là khoảng giá trị nhiệt độ cần tăng để thời gian phá hủy thập phân của loài vi sinh vật giảm
đi 10 lần
Z được tính dựa trên công thức sau:
t 2 t1
Z
D1
log 10 ( )
D2
4.4. xác định công thức thanh trùng:
4.4.1. cơ sở lý thuyết.
Công thức thanh trùng tổng quát :
𝐴−𝐵−𝐶
𝑇
Trong đó:
A: Thời gian nâng nhiệt độ, từ nhiệt độ ban đầu tới nhiệt độ thanh trùng cần thiết (phút)
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xlvii
B: Thời gian giữ nhiệt độ không đổi trong thiết bị thanh trùng (phút)
C: Thời gian hạ nhiệt từ nhiệt độ thanh trùng tới nhiệt độ có thể lấy sản phẩm ra (phút)
T: Nhiệt độ thanh trùng (0C)
Hình1.Đồ thị thanh trùng tổng quát.
Xác định thời gian hiệu quả thực tế
Quá trình thanh trùng nhằm làm vô hoạt hệ enzyme trong sản phẩm, tiêu diệt vi sinh vật có
hại, chống hư hỏng, đồng thời làm tăng tính cảm quan của sản phẩm thực phẩm.
Ở điều kiện nhiệt độ thanh trùng bình thường, có thể vô hoạt hệ enzyme một cách dễ dàng, tuy
nhiên các vi sinh vật lại bền với nhiệt và khó tiêu diệt hơn nhiều. Một số vi sinh vật có khả
năng chịu nhiệt cao, do đó muốn tiêu diệt được chúng, ta phải nâng cao nhiệt độ và phải duy
trì ở nhiệt độ đó trong một thời gian nhất định. Như vậy, nhiệt độ tiêu diệt càng cao thì thời
gian càng ngắn và ngược lại.
Khi nâng nhiệt độ hoặc kéo dài thời gian thanh trùng đều có tác dụng nhất định đối với thực
phẩm. Vì vậy, một sự kết hợp thích đáng giữa thời gian và nhiệt độ thanh trùng là rất quan
trọng để tiêu diệt vi sinh vật. Tương ứng ta có công thức:
Tc− Ta
τ = τ0 . 10 𝑧 (1)
𝑇𝑐−𝑇𝑎
Hay D = D0 . 10 𝑧 (2)
Với:
τ: Thời gian tiêu diệt cần xác định ở nhiệt độ nhất định nào đó Ta, phút.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xlviii
τ0: Thời gian tiêu diệt ở nhiệt độ chuẩn đã biết trước Tc, phút.
D: Thời gian cần thiết để số lượng vi sinh vật giảm xuống 10 lần ở nhiệt độ nhất định nào đó
Ta, phút.
Do: Thời gian cần thiết để số lượng vi sinh vật giảm xuống 10 lần ở nhiệt độ chuẩn đã biết
trước Tc, phút.
z: Hằng số bền nhiệt của vi sinh vật, oC
Ta có thể quy đổi mỗi khoảng thời gian tiêu diệt vi sinh vật ở nhiệt độ bất kì thành thời gian có
điều kiện ở nhiệt độ chuẩn bằng cách sử dụng công thức (1), ta có phương trình sau:
τ 𝑇𝑐− 𝑇𝑎
lgτo = 𝑧
(3)
Quy ước nhiệt độ chuẩn là 121,10C, do nhà bác học Boll (Mỹ) đề ra.
Công thức (3) được viết lại như sau:
𝑈 121,1−𝑇
lg 𝐹 = (4)
𝑧
Trong đó:
τ = U: Thời gian tiêu diệt cần xác định ở nhiệt độ nhất định nào đó T, phút.
τo = F: Thời gian tiêu diệt ở nhiệt độ chuẩn 121,10C, phút.
Từ công thức (4) ta có:
121,1−𝑇
𝑈
= 10 𝑧
𝐹
1
Hay: F = U . 121,1−𝑇
10 𝑧
Số F được quy ước gọi là thời gian hiệu quả thanh trùng.
Như vậy, để tính thời gian hiệu quả F ở 121,10C ta cần nhân thời gian tiêu diệt thực tế U với
1
biểu thức 121,1−𝑇 .
𝑒 𝑧
1
Gọi KF = 121,1−𝑇 thì KF chính là hệ số chuyển đổi thời gian thực tế U (thời gian tác dụng lên
10 𝑧
vi sinh vật ở nhiệt độ xác định bất kỳ T) thành thời gian F ở 121,10C có tác dụng tiêu diệt vi
sinh vật tương đương.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xlix
Suy ra: F = U.KF (5)
Với biểu thức (5), có thể tính được hệ số chuyển đổi cho nhiệt độ thanh trùng bất kì với độ
chính xác mà ta mong muốn, đồng thời có thể tính được thời gian hiệu quả không chỉ của một
khoảng thời gian U nào đó mà có thể áp dụng cho cả quá trình thanh trùng với các khoảng chia
nhỏ. Và sự phân tích trên cơ sở toán học của một chế độ thanh trùng xác định chính là ở đây:
sự thiết lập mối quan hệ giữa công thức thanh trùng (thể hiện các đặc điểm bên ngoài của chế
độ thanh trùng) và thời gian hiệu quả (xác định được theo công thức này) xác định mức độ tiêu
diệt vi sinh vật
Đồ thị hệ số chuyển đổi có dạng như hình 2.2
Hình 2.2 Đồ thị hệ số chuyển đổi KF trên lý thuyết
Theo đồ thị, phần diện tích giới hạn bởi đường cong hệ số chuyển đổi được tính bằng tích
𝑏
phân xác định dạng ∫𝑎 𝐾𝐹 . 𝑑 𝜏 chính là thời gian hiệu quả F của quá trình thanh trùng trong
khoảng thời gian từ a đến b.
𝑏 𝑏
Tức là: F = ∫𝑎 𝑑 𝐹 = ∫𝑎 𝐾𝐹 . 𝑑τ
Để xác định giá trị của tích phân này, người ta dùng phương pháp tích phân gần đúng: chia
khoảng thời gian từ a đến b thành n phần bằng nhau biểu thị bằng τp. Kẻ các đường thẳng
vuông góc trục hoành đi qua các điểm chia này, cắt đồ thị hệ số chuyển đổi tại các điểm khác
nhau và như vậy diện tích F bị chia nhỏ thành n phần, kí hiệu là f1, f2,…, fn. Căn cứ theo hình
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 l
vẽ có thể thấy mỗi phần diện tích nhỏ được tạo thành là một hình thang vuông. Tuy nhiên,
chấp nhận một sai số nhỏ, ta có thể xem các diện tích nhỏ fn trên có dạng hình chữ nhật.
𝑏
Như vậy: F = ∫𝑎 𝐾𝐹 . 𝑑τ = τp (Kf1 + Kf2 + … + Kfn)
𝑏
Hay: F = ∫𝑎 𝐾𝐹 . 𝑑τ ≈ 𝑑τ. ∑𝑛𝑖=1 𝐾𝑓𝑖 (6)
4.4.2. Xác định hiệu quả thanh trùng cần thiết:
Đây chính là thời gian hiệu quả thanh trùng tối thiểu cần phải đạt được theo lý thuyết, giá trị
này được tính theo công thức:
𝑁
F = D121,1 . log 𝑁𝑜 (7)
𝑐
Hay: F = n . D121,1 (8)
Trong đó:
D121,1: giá trị hằng số D ở 121,1oC.
No: hàm lượng vi sinh vật trong thực phẩm trước khi thanh trùng.
Nc: hàm lượng vi sinh vật trong thực phẩm sau khi thanh trùng.
Vì với một loài vi sinh vật xác định ở loại đồ hộp nhất định nào đó, giá trị D là hằng số nên có
thể dễ dàng thấy được thời gian hiệu quả F, vì vậy để tính thời gian hiệu quả cần thiết Fc ta
cần xác định được mức độ vô trùng cần thiết phải đạt được n.
Nếu cho rằng giá trị Nc phải thật nhỏ và có thể biểu diễn ở dạng lũy thừa với cơ số 10 và số
mũ là một số âm nào đó (Nc = 10-a), thì độ vô trùng là:
𝑁 0
n = lg 10−𝑎 = lg (No . 10a) = a + lgNo
Do đó thời gian hiệu quả cần thiết sẽ là:
F = D121,1.(a + lgNo) (9)
Người ta thường chọn Clostridium Botulinum là vi sinh vật chỉ thị vì chúng có khả năng sinh
độc tố gây ngộ độc mà không làm biến đổi, hư hỏng thực phẩm làm con người khó thể nhận
thấy được.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 li
Tuy nhiên, mỗi loại đồ hộp thực phẩm khác nhau đều có các vi sinh vật gây hư hỏng đặc trưng
khác nhau và khi tính thời gian hiệu quả cần thiết theo vi sinh vật gây hư hỏng đặc trưng,
người ta thấy rằng kết quả thu được cao hơn nhiều so với giá trị hiệu quả F cần thiết tính theo
Cl.botulinum mà nguyên nhân chính là do các vi sinh vật này có độ bền nhiệt cao hơn, vì vậy
người ta chấp nhận độ nhiễm khuẩn ban đầu No đối với các vi sinh vật gây hư hỏng đặc trưng
là 0,1 – 3 nha bào/ 1g thực phẩm.
Như vậy, trong công thức (9) độ nhiễm khuẩn ban đầu No phụ thuộc vào khối lượng thực
phẩm trong hộp G (tính bằng g) và mật độ vi sinh vật C (tế bào/g) trong sản phẩm lúc bắt đầu
thanh trùng. Do đó, công thức (9) có thể viết ở dạng tổng quát sau:
Fc = D.(a + lgCG)
Vì tỉ lệ đồ hộp hư hỏng do tất cả các loại vi sinh vật gây hư hỏng đặc trưng đều được chấp
nhận là 0,01% (nghĩa là Nc = 10-4 hay a = 4) nên thời gian hiệu quả thanh trùng cần thiết Fc
được viết lại như sau:
Fc = D.(4 + lgCG) (10)
4.4.3. Kiểm tra lại công thức thanh trùng được sử dụng:
Để kiểm tra công thức thanh trùng đang sử dụng có hiệu quả hay không, ta sẽ so sánh thời
gian hiệu quả thanh trùng thực tế Ftt với thời gian hiệu quả cần thiết Fc:
Nếu Ftt < Fc: chế độ thanh trùng chưa đủ, cần tăng thêm thời gian giữ nhiệt nếu vẫn muốn duy
trì nhiệt độ của chế độ hiện tại, hoặc tăng nhiệt độ thanh trùng.
Nếu Ftt = Fc: chế độ thanh trùng vừa đủ và không có dự trữ.
Nếu Ftt > Fc: chế độ thanh trùng là phù hợp.
Trên thực tế, người ta thường chọn lựa công thức thanh trùng sao cho luôn có một lượng dư
nhỏ Ftt > Fc để đảm bảo việc thanh trùng đạt được độ vô trùng cần thiết dù có những sai sót
nhỏ trong kiểm soát quá trình xảy ra. Tuy nhiên, Ftt không nên lớn hơn Fc quá nhiều vì sẽ dẫn
tới lãng phí nhiệt và làm giảm giá trị cảm quan cũng như dinh dưỡng của thực phẩm.
5. sơ lược về soup rau.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lii
5.1. giới thiệu chung.
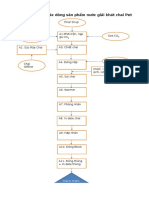
5.2. quy trình sản xuất
5.3. Nguyên liệu chính trong sản phẩm
5.3.1. Nấm rơm
Nấm rơm có tên khoa học Volvariella volvacea gồm nhiều loài khác nhau, có loại
màu xám trắng, có loại màu xám hay xám đen… kích thước đường kính “cây nấm”
lớn, nhỏ tùy thuộc từng loại. Ở các quốc gia vùng nhiệt đới rất thích hợp về nhiệt độ
để nấm rơm sinh trưởng và phát triển.
Nấm rơm
5.3.1.1. Đặc điểm hình thái của nấm
Bao gốc (volva): dài và cao lúc nhỏ, bao lấy tai nấm. Khi tai nấm trưởng thành, nó
chỉ còn lại phần trùm lấy phần gốc chân cuống nấm, bao nấm là hệ sợi tơ nấm chứa
sắc tố melanin tạo ra màu đen ở bao gốc . Độ đậm nhạt tùy thuộc vào ánh sáng. Ánh
sáng càng nhiều thì bao gốc càng đen.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 liii
Cấu tạo nấm rơm
Cuống nấm (stem): Là bó hệ sợi xốp, xếp theo kiểu vòng tròn đồng
tâm. Khi còn non thì mềm và giòn. Nhưng khi già xơ cứng và khó bẻ
gãy.
Mũ nấm (cap): Hình nón, cũng có melanin, nhưng nhạt dần từ trung tâm ra rìa mép.
5.3.1.2. Cách thu hái nấm
Kể từ lúc trồng đến khi hái hết đợt 1 khoảng 15-17 ngày. Nấm ra rộ vào ngày thứ 12
đến 15 Sau 7-8 ngày ra tiếp đợt 2 và hái trong 3-4 ngày thì kết thúc một đợt nuôi
trồng (tổng thời gian 25-30 ngày). Dọn vệ sinh sạch sẽ, tưới nước vôi để 3-4 ngày lại
trồng đợt tiếp. Hái nấm còn ở giai đoạn hình trứng (trước khi nấm nở dù ) là tốt nhất,
đảm bảo chất lượng và năng suất cao. Trường hợp nấm mọc tập trung thành cụm, ta có
thể tách những cây lớn hái trước, nếu khó tách thì hái cả cụm (cả to, nhỏ đều hái hết).
Một ngày, hái nấm 2-3 lần . Những ngày nắng nóng, nhiệt độ không khí cao, nấm
phát triển rất nhanh , vì vậy người hái nấm phải quan sát kỹ, khi nấm hơi nhọn đầu là
hái được rồi.
5.3.1.3. Thành phần hóa học:
Thành phần Hàm lượng
Nước (% khối lượng của nấm tươi) 91±0.64
Chất khô (% khối lượng của nấm tươi) 9 ± 0.36
Nito tổng ( % khối lượng chất khô) 6.5 ± 0.04
Protein thô ( % khối lượng chất khô) 28 ± 0.16
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 liv
Xơ thô ( % khối lượng chất khô) 9.8 ± 0.41
Tro ( % khối lượng chất khô) 10 ± 0.12
Glucid tổng ( % khối lượng hất khô) 50 ± 3.15
Thành phần khoáng Hàm lượng (mg/100g chất
khô)
Na 258± 2,2
K 1324 ± 2.5
P 1699 ± 2.57
Mg 57 ± 2.3
Ca 446 ± 19
Zn 68 ± 2.2
Fe 426 ± 2.4
Mn 5.2 ± 1.7
Cu 426 ± 0.42
Co Không có
Nấm rơm còn chứa 17 loại amino acid ( trong đó có 8 loại cơ thể rất cần thiết); lại có
chứa lượng lớn protein có tác dụng chống ung thư và các chất aminobenzoic acid, D-
mannitol và vitamin v.v…
Nấm rơm là loại thực phẩm bảo vệ sức khỏe có giá trị dinh dưỡng cao. 100g nấm rơm
tươi cung cấp 31 cal.
5.3.2. Cà rốt
5.3.2.1. Phân loại khoa học:
Tên khoa học: Daucus carota L. ssp.
sativus
Giới: Plantae
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lv
Ngành: Magnoliophyta
Lớp: Magnoliopsida
Phân lớp: Rosidae
Bộ: Apiales
Họ: Apiaceae
Chi: Daucus
Các loài cà rốt là các cây thân thảo sống hai năm, ít khi một năm hay lâu năm. Thân
đơn độc mọc thẳng đứng, rỗng ruột, khía dọc, phân cành, có lông mọc ngược. Các lá có
cuống; mọc cách, phiến lá xẻ lông chim 2-3 lần, các chét lá nhỏ và hẹp. Các tán hoa
mọc ở đầu cành hay nách lá, dạng kép lỏng lẻo; nhiều lá bắc, hình lông chim; nhiều tia,
trải rộng hay cong vào sau khi nở; nhiều lá bắc con, khía răng cưa hay nguyên mép;
các tán nhiều hoa. Các hoa trung tâm thường vô sinh với các cánh hoa màu tía và lớn.
Các răng nhỏ của đài hoa bị teo đi. Hoa tạp tính, màu trắng hay vàng, hình tim ngược,
với đỉnh cụp vào trong, các cánh bên ngoài của các hoa phía ngoài trong tán hoa lớn và
tỏa ra. Gốc trụ hình nón, vòi nhụy ngắn. Hoa thụ phấn nhờ các loại côn trùng.
Quả hình trứng, bị nén ở phần sống lưng, chứa 2 hạt dài 3-4 mm; các gân chính
hình chỉ, cứng; các gân phụ có cánh, các cánh với gai móc; các ống tinh dầu nhỏ với số
lượng là 1 tại các rãnh cắt phía dưới các gân thứ cấp và 2 trên chỗ nối. Mặt hạt hơi lõm
tới gần phẳng. Cuống lá noãn nguyên hay chẻ đôi ở đỉnh. Rễ củ to, dài, hình cọc, có
nhiều màu tùy theo từng chủng loại; các loại cà rốt thường gặp có màu trắng, vàng,
cam, đỏ, tím.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lvi
Hình 1.1: Các bộ phận của cây cà rốt
1. Thân ; 2. Hoa cà rốt ; 3. Rễ (củ) cà rốt
(http://dictionary.bachkhoatoanthu.gov.vn/default.aspx?param=1633aWQ9MzE0NzUmZ3Jvd
XBpZD0ma2luZD1zdGFydCZrZXl3b3JkPWM=&page=1; ngày 23/10/2008)
Cà rốt có nguồn gốc từ khu vực Bắc Phi, Tây Nam Á và châu Âu, nhưng hiện nay
được gieo trồng rộng khắp thế giới, chủ yếu là khu vực ôn đới; thích hợp với các vùng
thấp có khí hậu mát, có mưa mùa hè và đầu mùa thu. Hai chủng Nantes và Chantenay
của Pháp được trồng phổ biến trên thế giới và tương đối thích hợp với vùng nhiệt đới.
Ở Việt Nam cà rốt được nhập vào và trồng thí điểm trong những năm cuối thế kỉ
XIX do người Pháp đem từ châu Âu sang. Và hiện nay được trồng ở nhiều nơi như:
Lâm Đồng, các tỉnh miền Bắc, miền Trung, một số tỉnh thuộc miền Đông Nam Bộ.
5.3.2.2. Thành phần dinh dưỡng và công dụng:
(i) `Giá trị dinh dưỡng của cà rốt:
Cà rốt là một trong những loại rau trồng rộng rãi và lâu đời nhất trên thế giới. Trong
củ cà rốt có protein, lipid, carbonhydrat, một số vitamin B, C, E, đặc biệt là tiền
vitamin A; có 15 acid amin trong đó có 9 loại thiết yếu mà cơ thể người không tự sản
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lvii
xuất được; giàu muối khoáng Na, K, Ca, P, Mg, Fe, Zn, Cu,... Trong 100g cà rốt tươi
thường chứa 88,5% nước và cung cấp giá trị năng lượng là 48 calorie. Các thành phần
quan trọng khác bao gồm:
1g chất đạm
0,2g chất béo
9 g chất bột đường
24mg Phospho
2,4mg Natri
289mg Kali
80mg Canxi
24mg Magie
0,75mg Sắt
0,45mg Mangan
12400UI carotene
0,05mg vitamin B1
0,04mg vitamin B2
1,1mg vitamin PP
13mg vitamin C
(ii) Công dụng của cà rốt:
Cà rốt là một trong những loại rau quý nhất được các thầy thuốc trên thế giới đánh
giá cao về giá trị dinh dưỡng và chữa bệnh đối với con người. Người La Mã gọi cà rốt
là nữ hoàng của các loại rau. Cà rốt giàu đường và các loại vitamin cũng như năng
lượng. Các dạng đường tập trung ở lớp vỏ và thịt nạc của củ, phần lõi rất ít.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lviii
Hình 1.2: Phần thịt của củ cà rốt
(http://www.nutifood.com.vn/Default.aspx?pageid=146&mid=326&action=docdetailview&in
tDocId=2414&intSetItemId=297&breadcrumb=297; ngày 23/10/2008)
Đường trong cà rốt chủ yếu là đường đơn (như fructose, glucose) chiếm tới 50%
tổng lượng đường có trong củ, là loại đường dễ oxy hóa dưới tác dụng của enzyme
trong cơ thể; các loại đường như levulose và dextrose được hấp thụ trực tiếp.
Trong cà rốt có rất nhiều vitamin C, D, E và các vitamin nhóm B. Ngoài ra, nó còn
chứa β-carotene, sau khi vào cơ thể, chất này sẽ chuyển hóa dần thành vitamin A. Beta
carotene có cấu trúc hóa học và hoạt tính sinh học tương tự vitamin A nhưng ở người
nó được dự trữ ở khắp các mô còn vitamin A được dự trữ ở gan. So với vitamin A thì
carotene ít độc hại hơn, vì nó được chuyển dạng theo nhu cầu của cơ thể và ít bị phá
hủy hơn. Một số nhà khoa học đã khuyến cáo nên dùng carotene hơn là vitamin A.
Người ta thường sử dụng cà rốt dưới dạng tươi để ăn sống (làm gỏi, trộn dầu giấm)
hay xào, nấu canh, hầm thịt. Hoặc dùng cà rốt ép lấy dịch, phối hợp với các loại hoa
quả khác để làm nước giải khát hoặc nước dinh dưỡng.
Thịt củ, dịch (nước ép cà rốt) và hạt non còn được dùng để làm thuốc. Cà rốt có các
tính chất: bổ, giàu chất khoáng, làm tăng lượng hồng cầu, tăng sự miễn dịch tự nhiên,
là yếu tố sinh trưởng, kích thích sự tiết sữa, làm cho các mô và da trẻ lại. Nó còn giúp
lọc máu, làm loãng mật, trị ho, lợi tiểu, trị giun và liền sẹo.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lix
Cà rốt chứa nhiều pectin nên có tác dụng điều hòa nhu động ruột, hút các chất độc
trong ruột, tạo lớp băng bảo vệ niêm mạc ruột.
Các carotenoid rất tốt cho sự tăng trưởng của trẻ từ nhỏ cho đến khi dậy thì nếu
trong chế độ ăn có bổ sung cà rốt.
Ngoài ra, cà rốt còn có tác dụng phòng chống bệnh quáng gà, nhất là chứng khô mắt
dẫn đến mù lòa. Có lời khuyên người làm việc nhiều bằng mắt, nhất là vào ban đêm
nên ăn nhiều cà rốt.
Việc dùng cà rốt sống hay chín cũng có ý kiến trái ngược. Theo các chuyên gia Đại
học tổng hợp Arkansas (Mỹ) ăn cà rốt chín hàm lượng dinh dưỡng cao hơn so với cà
rốt sống (tăng 34%). Trong chế biến thực phẩm nên phối hợp với gan một số động vật
(gà, lợn) để có sự phối hợp 2 loại vitamin A: động vật và thực vật, tác dụng dược lý tốt
hơn (khi nấu nên dùng dầu thực vật vì vitamin A tan trong dầu...).
Cà rốt quý nhưng cũng không nên lạm dụng, dùng bừa bãi, tùy thích mà nên căn cứ
vào nhu cầu tối thiểu hằng ngày của beta carotene.
5.3.3. Phân bố, thời vụ:
5.3.3.1. Phân bố
Cà rốt cũng được trồng nhiều ở nước ta. Hiện nay, các vùng trồng rau đang trồng
phổ biến 2 loại cà rốt: một loại củ có màu đỏ tươi, một loại có màu đỏ ngả sang màu da
cam.
Loại vỏ đỏ (cà rốt đỏ) được nhập trồng từ lâu, chủ yếu là các giống Văn Đức
(miền Bắc) và Đà Lạt (miền Nam). Nó có củ to nhỏ không đều, lõi to, nhiều xơ,
hay phân nhánh, kém ngọt, khả năng thích ứng đất đai và thời tiết tốt hơn giống
ngoại nhập.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lx
Loại vỏ màu đỏ ngả màu da cam là cà rốt nhập của Pháp (cà rốt Tim-Tom) sinh
trưởng nhanh hơn loại trên; tỷ lệ củ trên 80%, da nhẵn, lõi nhỏ, ít bị phân nhánh
nhưng củ hơi ngắn, mập hơn, ăn ngon. Các giống ngoại nhập khác gồm có: NS,
Nans, Nataise Amelirec,… của Pháp; PS của Mỹ, giống 555 của Thái Lan…
Đây là các giống lai F1, ưu thế lớn nhất là năng suất cao, củ to, đều, ít xơ, ăn
ngọt, được thị trường ưa chuộng.
5.3.3.2. Thời vụ:
Vụ sớm: trên các chân đất cao, gieo hạt từ tháng 7, tháng 8; thu hoạch tháng 10,
tháng 12.
Vụ chính: gieo hạt tháng 9, tháng 10 để thu hoạch vào tháng 12, tháng 1. Đây là
thời vụ cho năng suất cao vì điều kiện nhiệt độ thích hợp cho toàn bộ thời gian
sinh trưởng và phát triển của cà rốt.
Ngoài ra cũng có thể trồng thêm vụ muộn: gieo hạt vào tháng 12, tháng 1 để thu
hoạch vào tháng 3, tháng 4.
Cà rốt được trồng phổ biến với giống địa phương (chủ yếu là giống Đà Lạt) có thời
gian sinh trưởng 95-100 ngày, kích thước 18-22cm x 2,5-3cm, màu đỏ nhạt, năng suất
trung bình 20-25 tấn/ha và các giống của Pháp như Nantaise, Seamllienee, Tim-Tom
có củ to, kích thước 22-25 x 3-3,5cm, có tiềm năng tăng mạnh sản lượng trong tương
lai.
Cà rốt sẵn sàng thu hoạch sau khi gieo hạt giống 90 ngày nhưng tiếp tục lớn lên và
mở rộng sau đó. Thu hoạch khi rễ có kích thước tốt nhưng vẫn còn mềm.Cà rốt có thể
được trữ trên đất trong suốt những tháng mùa đông. Nếu cà rốt lấy khỏi đất quá lâu
hoặc cho phép chín nẫu, rễ trở nên dai, nhiều gỗ và có thể gãy.
Vấn đề bảo quản cà rốt cũng như các loại rau củ khác tương đối khó vì đây là thực
phẩm tươi, rất dễ bị thối rữa, hư hỏng, nấm mốc, vi khuẩn dễ phát triển (do nước chiếm
gần 90%). Trong công nghệ chế biến thực phẩm hiện nay, người ta đòi hỏi càng cao về
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxi
việc bảo quản. Có rất nhiều cách để bảo quản thực phẩm, ở đây đối với cà rốt ta dùng
phương pháp sấy. Với phương pháp này sẽ bảo quản cà rốt được lâu hơn, dễ dàng trong
quá trình vận chuyển, ứng dụng nhiều trong quá trình chế biến các sản phẩm ăn liền.
Phần II. PHẦN III. PHƯƠNG PHÁP NGHIÊN CỨU
1. Quy trình sản xuất
Lá tươi
làm sạch
Xử lý thu dịch
Nước
Lọc Bã
Chất ổn định
Đường, nước Phối chế
Acid citric
Bài khí
Rót chai
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxii
thanh trùng
Sản
phẩm
Thuyết minh quy trình sản xuất :
1.1. Nguyên liệu:
Nguyên liệu được sử dụng là lá chùm ngây, đã đạt độ đồng nhất về độ già, có
hàm lượng giá trị dinh dưỡng cao.
Thực hiện: lá được thu mua về sẽ được phân loại về độ đồng nhất, và loại bỏ
cành để hạn chế ảnh hưởng của cành đến hiệu suất thu hồi sản phẩm.
1.2. Làm sạch:
Mục đích: loại bỏ những lá bị héo, dập nát, sâu, thối hay hư hỏng. Đồng
thời rửa sạch nguyên liệu nhằm hạn chế bụi bẩn và vi sinh vật.
Thực hiện: lá chùm ngây tươi sau khi mua về được chọn lọc thật kĩ, bỏ
đi những lá héo úa, dập nát hay sâu thối. Sau đó, tiến hành nhặt lá, bỏ cành, rửa
lá chùm ngây bằng nước muối rồi rửa lại với nước sạch nhiều lần nhằm loại bỏ
bụi bẩn và vi sinh vật rồi để ráo nước. Trong quá trình rửa cần lưu ý tránh làm
cho lá bị dập nát gây tổn thất các chất có trong lá.
1.3. Xử lý thu dịch:
Mục đích:
- giảm bớt mùi hăng tanh khó chịu của lá sống, đạt chỉ tiêu cảm quan
mùi tốt nhất.
- Bên cạnh đó còn tạo điều kiện thuận lợi cho quá trình thu dịch chiết
dễ dàng và đạt hiệu suất cao.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxiii
- Đồng thời quá trình xử lý thu dịch phải giữ được màu sắc của sản
phẩm, giúp sản phẩm không bị thay đổi màu trong các quá trình xử lý
sau.
Như vậy quá trình xử lý này phải đồng thời đạt được chỉ tiêu cảm
quan mùi, cảm quan màu tốt nhất và có hiệu suất thu hồi chất khô
không quá thấp để đảm bảo chất lượng của sản phẩm.
Thực hiện:
- Tiến hành xử lý nguyên liệu bằng cách chần trong môi trường kiềm
hoặc trong môi trường nước và kết hợp xử lý với ion kim loại tạo
phức.
- Xử lý bằng emzyme cenlulase, sau đó gia nhiệt lên cao để đảm bảo
giá trị cảm quan màu cho sản phẩm.
- Thực hiện quá trình lạnh đông.
1.4. Lọc
Mục đích: tách bỏ bã khỏi dịch chùm ngây sau quá trình xay nhuyễn.
Thực hiện: dịch chùm ngây thu được sẽ được tách bã bằng cách lọc qua vải
mùng 5 lớp. Đây là quá trình lọc thô, chỉ đủ để loại bỏ hết cặn bã vừa và lớn,
không cần lọc tinh tách những hạt keo vì như thế sẽ làm tổn thất các chất có
trong dịch chùm ngây
1.5. Phối chế:
Mục đích: tạo hương vị cũng như đảm bảo cấu trúc lơ lửng, đồng nhất và không
lắng cặn của các hạt keo trong dịch chùm ngây.
Thực hiện: sau khi khảo sát lượng đường, acid citric và chất ổn định với hàm
lượng thích hợp, tiến hành phối chế vào dịch chùm ngây, lưu ý khuấy đều tay
trong khi phối chế để đảm bảo dịch chùm ngây được đồng nhất.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxiv
Bên cạnh đó, có thể làm tăng hương vị nước chùm ngây bằng cách bổ sung
thêm hương vani vào để tạo mùi thơm, kích thích sự ngon miệng.
1.6. Bài khí – Rót chai:
Mục đích: tách các khí phân tán và hòa tan ra khỏi hỗn hợp dịch chùm
ngây nhằm chuẩn bị cho giai đoạn thanh trùng, tăng hiệu suất của quá trình
truyền nhiệt và hạn chế bọt khí còn sót lại trong chai có thể dẫn tới nổ chai khi
thanh trùng cũng như tạo độ chân không trong chai. Đồng thời nhằm hạn chế sự
phát triển của các vi sinh vật hiếu khí, hạn chế sự oxy hóa làm biến đổi mùi vị
và tổn thất các chất dinh dưỡng, đặc biệt là các loại vitamin.
Thực hiện: đun cách thủy hỗn hợp dịch chùm ngây sau khi phối trộn đến
85oC rồi rót vào chai ngay. Khi đun cần lưu ý không đun sôi hay đun quá lâu vì
sẽ làm cho sản phẩm có mùi nấu và khi rót chai cũng không nên rót quá đầy,
nên cách miệng chai khoảng từ 2 – 3 cm. Sau khi rót chai xong cần phải đóng
nắp và đem đi thanh trùng ngay, thời gian chờ thanh trùng không được quá 30
phút, nếu không nhiệt độ sản phẩm sẽ giảm gây ảnh hưởng đến chế độ thanh
trùng.
1.7. Thanh trùng:
Mục đích: tiêu diệt hầu hết các vi sinh vật, đồng thời kéo dài thời gian bảo quản
sản phẩm.
Thực hiện: sản phẩm sau khi rót chai sẽ được khảo sát, tính toán chế độ thanh
trùng dựa theo công thức thanh trùng nhằm đảm bảo chất lượng dinh dưỡng và
cảm quan của sản phẩm.
2. SƠ ĐỒ NGHIÊN CỨU.
Bảng 1.1: Sơ đồ nghiên cứu
Giai đoạn Thí nghiệm Yếu tố khảo sát Chỉ tiêu đánh
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxv
giá
1. Xử lý Khảo sát quá trình Thời gian Đánh giá cảm
thu dịch. chần kết hợp với ion Nồng độ quan màu.
kim loại tạo phức.
Khảo sát ảnh hưởng Thời gian
của độ acid kết hợp Nồng độ NaOH Đánh giá cảm
với ion kim loại tạo Nồng độ muối. quan màu.
phức trong quá trình
chần.
Khảo sát ảnh hưởng Nồng độ NaOH Đánh giá cảm
của độ acid trong Thời gian ngâm quan màu
quá trình chần kết Nồng độ muối.
hợp với ngâm ion
kim loại sau chần.
Khảo sát quá trình Nồng độ emzyme Đánh giá cảm
xử lý sơ bộ với Thời gian xử lý quan mùi
emzyme Cenllulase. Đánh giá cảm
quan màu
Hiệu suất thu
hồi
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxvi
2. Khảo sát Khảo sát bổ sung % dịch nấm Cảm quan vị
quá dịch nấm cô đặc vào Hàm lượng muối Cảm quan màu
trình sản phẩm sau thu
phối chế dịch
Khảo sát tính đồng Chất ổn định Cảm quan:
nhất của đơn chất Nồng độ chất ổn mouthfeel, độ
ổn định đến độ đồng định nhớt
nhất của sản phẩm. Độ lắng: quan
sát và OD.
Khảo sát kết hợp 2 Chất ổn định Cảm quan:
chất ổn định đến Nồng độ chất ổn mouthfeel, độ
tính đồng nhất của định nhớt
sản phẩm. Độ lắng: quan
sát và OD.
Khảo sát kết hợp 3 Chất ổn định Cảm quan:
chất ổn định đến Nồng độ chất ổn mouthfeel, độ
tính đồng nhất của định nhớt
sản phẩm. Độ lắng: quan
sát và OD.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxvii
3. Khảo sát Thực nghiệm D, z. Nhiệt độ Giá trị D và z.
quá Thời gian
trình Mật độ vi sinh
thanh vật sau thanh
trùng trùng.
Xác định công thức Nhiệt độ Xây dựng công
thanh trùng bằng Thời gian thức thanh
phương pháp toán trùng.
học tương ứng ở các
mốc thời gian khác
nhau.
Đánh giá cảm quan
toàn diện sản phẩm,
xây dựng công thức
hoàn thiện sản
phẩm.
2.1. Giai đoạn 1: Xử lý thu dịch.
2.1.1. Khảo sát quá trình chần kết hợp với ion kim loại.
Mục đích:
Giúp tăng khả năng giữ màu cho sản phẩm.
Bố trí thí nghiệm:
o Chọn các yếu tố ảnh hưởng:
Z1: Thời gian chần, phút.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxviii
Z2: Nồng độ ion kim loại tạo phức, ppm.
o Chọn các hàm mục tiêu:
Y: độ hấp phụ OD.
Phương trình biểu diễn mối quan hệ có dạng: Y = f (Z1 , Z2);
Chọn miền khảo sát:
Dựa vào các thí nghiệm khảo sát sơ bộ,chúng tôi chọn miền khảo sát của các
yếu tố là:
+ thời gian chần : 1-5 phút.
+ nồng độ ion kim loại tạo phức: ( VD: Cu2+ (CuCl2) 10 – 30ppm, Zn2+ (kẽm
acetat) 100- 150ppm, Mg2+ (MgCO3)1000-2000ppm).
Từ đó xây dựng điều kiện thí nghiệm theo bảng
Bảng 1.2: Điều kiện thí nghiệm chần kết hợp với ion kim loại
Các yếu tố ảnh hưởng
Z2: Nồng độ ion kim
Các mức
Z1: Thời gian chần loại tạo phức ( Cu2+,
Zn2+, Mg2+).
Mức trên (+1) 5 30, 150, 2000
Mức cơ sở (0) 3 20, 125, 1500
Mức dưới (-1) 1 10, 100, 1000
Khoảng biến thiên 2 10, 25, 500
Chọn phương án quy hoạch trực giao cấp I(TYT 2k) thực nghiệm yếu tố toàn phần 2
mức, 2 yếu tố ảnh hưởng. Phương trình hồi qui có dạng:
Y = b0 + b1x1 + b2x2 + b12x1x2
Trong đó:
x1: Nồng độ enzyme; x2: Thời gian xử lý
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxix
b0: Hệ số hồi qui.
b1, b2: Hệ số tuyến tính
b12: Hệ số tương tác đôi
o Tổ chức thí nghiệm trực giao cấp I:
Để nhanh chóng tiến tới miền tối ưu, chúng tôi tiến hành 7 thí nghiệm điều kiện
đã chọn ở bảng 2.1. Trong đó số thí nghiệm của phương án là 2k = 4, (k = 2), số thí
nghiệm ở tâm là 3.
Bảng 2.2: Kế hoạch bố trí thí nghiệm chần kết hợp với ion kim loại
Giá trị thực ( VD:
Biến mã Cu2+).
STT
Số thí
x1 x2 x1x2 x1 x2
nghiệm
1 + + + 5 30
trong
phương án 2 - + - 1 30
2k 3 + - - 5 10
4 - - + 1 10
5 0 0 0 3 20
Số thí
nghiệm ở 6 0 0 0 3 20
tâm 7 0 0 0 3 20
Tiến hành thí nghiệm:
Lá chùm ngây tươi sau khi rửa sạch sẽ được đem đi cân với lượng là 25g/mẫu.
=> 25g/nghiệm thức x 7 nghiệm thức = 175g.
Các nghiệm thức được chần ở nhiệt độ 1000C/ trong thời gian và nồng độ muối
đã được bố trí thí nghiệm ở bảng 2.2. Các mẫu sau chần sẽ được rửa lại với nước lạnh
50C.
Tiến hành đánh giá:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxx
Hàm mục tiêu chủ yếu của khảo sát trên là độ hấp phụ OD của sản phẩm.
vì thế chúng tôi tiến hành đo độ hấp phụ OD của mẫu sau quá trình xử lý thu
dịch và tiến hành gia nhiệt lên nhiệt độ cao để quan sát sự thay đổi màu của
sản phẩm và đo đo độ hấp phụ OD sau đun sôi. Đồng thời kết hợp với đánh
giá cảm quan các mẫu.
o Đánh giá cảm quan mẫu theo phương pháp cho điểm, chỉ tiêu màu dựa
theo bảng điểm sau TCVN 5050-90:
Bảng 1.4: Bảng cho điểm chỉ tiêu cảm quan màu
Điểm Màu
0
1
2
3
4
5
Ghi nhận lại kết quả đo OD, cảm quan màu cho từng mẫu.
Tiến hành xử lý số liệu theo phương pháp quy hoạch thực nghiệm:
Xây dựng mô tả toán học cho từng hàm mục tiêu:
Sau khi chọn phương trình hồi qui (*), các hệ số b1, b2, b3, b12 , b13, b23, được
tính theo số liệu thực nghiệm theo từng hàm mục tiêu.
Tính hệ số b:
Dựa vào công thức:
∑ni=1 Yi
𝑏0 =
N
n
∑ X ji Yi
i=1
bj =
N
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxi
n
∑ (X j . X l )i Yi
i=1
bjl =
N
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Sau đó, tính phương sai tái hiện theo công thức:
m
1
2
Sth = ̅̅̅0 )2
∑(Yu0 − Y
m−1
u=1
Với m là số thí nghiệm ở tâm phương án (m = 3)
Sự có nghĩa của hệ số hồi qui được kiểm định theo tiêu chuẩn Student (t)
|𝑏𝑗 |
𝑡𝑗 = (**)
𝑆𝑏𝑗
Trong đó: bj: là hệ số thứ j trong phương trình hồi quy.
𝑆𝑡ℎ
Sbj: Độ lệch quân phương của hệ số thứ j, với: 𝑆𝑏𝑗 =
√𝑁
Tra bảng tiêu chuẩn Student tp(f) ứng với xác suất tin cậy p và bậc tự do f,
f = N0-1 rồi so sánh với tj.
o Nếu tj>tp(f) thì hệ số bj có nghĩa.
o Nếu tj <tp(f) thì hệ số bj bị loại khỏi phương trình.
Sau đó viết lại phương trình hồi qui với các hệ số bj có nghĩa.
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
Sự phù hợp của phương trình hồi qui được kiểm định theo tiêu chuẩn
Fisher.
2
𝑆𝑑ư
F= 2
𝑆𝑡ℎ
Trong đó:
𝑁
1
2
𝑆𝑑ư = ̂𝑖 )2
∑(Yi − 𝑌
𝑁−𝐿
𝑖=1
Với: N: số thí nghiệm trong phương án
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxii
L: số hệ số ý nghĩa
Yi: giá trị thực nghiệm
̂𝑖 : giá trị tính theo phương trình hồi qui
𝑌
Nếu F tính được nhỏ hơn giá trị tra bảng F1-p (f1, f2) với mức ý nghĩa p,
f1=N-L, f2= N0 – 1 thì phương trình tương thích với thực nghiệm.
Tối ưu hóa hàm mục tiêu bằng phương pháp đơn hình đều.
Đối với quy hoạch đon hình để tìm điểm tối ưu ta cần phải:
- Xây dựng ma trận đơn hình
- Thực hiện dịch chuyển về điểm tối ưu, sử dụng quy luật đối xứng
điểm có giá trị xấu nhất tham số tối ưu.
- Xác định thời điểm đạt đến miền tối ưu. Quan trọng là biết chuyển từ
quy hoạch đơn hình sang quy hoạch thực nghiệm, dùng để mô tả miền
tối ưu.
Trong giai đoạn đầu, ma trận đơn hình đầu tiên được xây dựng từ nhân tố được
mã hóa. Khi đó tâm đơn hình chuyển đến gốc tọa độ, đỉnh xk+1 trên trúc xk vá
các đỉnh còn lại đối xứng với các trục tọa độ. Khi đó tọa độ các đỉnh đơn hình
bằng bán kính đường tròn hoặc siêu cầu nội và ngoại tiếp.
Trong trường hợp tổng quát, tọa độ các đỉnh của đơn hình ban đầu k nhân tố
được xác định theo các hàng của ma trận sau.
-r1 -r2 -r3 … -rk
R1 -r2 -r3 … -rk
0 R2 -r3 … -rk
0 0 R3 … -rk
--- --- --- --- ---
0 0 0 … Rk
Nếu chiều dài cạnh đơn hình bắng 1, thì bán kính hình cầu nội ngoại tiếp được
xác định theo công thức sau:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxiii
1 i
ri = ; Ri =
2i (i 2) 2(i 1)
Trong đó I = 1,2,3…k.
Theo bảng () ta có tọa độ được mã hóa của đon hình ban đầu khi k = 10. Nếu
k<10 thì tọa độ của mó có thể nhận theo bảng này nhưng chỉ lấy k cột đầu tiên
và k+1 hàng. Trong bảng này thì N tương ứng với số thí nghiệm trong loạt đầu
tiên.
Bảng 1.5 Tọa độ được mã hóa của đơn hình ban đầu
N x1 x2 x3 x4 x5 x6 x7 x8
1 -0.5 -0.289 -0.204 -0.158 -0.129 -0.109 -0.095 -0.067
2 0.5 -0.289 -0.204 -0.158 -0.129 -0.109 -0.095 -0.067
3 0 0.578 -0.204 -0.158 -0.129 -0.109 -0.095 -0.067
4 0 0 0.612 -0.158 -0.129 -0.109 -0.095 -0.067
5 0 0 0 0.632 -0.129 -0.109 -0.095 -0.067
6 0 0 0 0 0.645 -0.109 -0.095 -0.067
7 0 0 0 0 0 0.645 -0.095 -0.067
8 0 0 0 0 0 0 0 -0.067
9 0 0 0 0 0 0 0 0.674
Khi dịch chuyển về miền tối ưu tốt nhất nên sử dụng tỉ lệ tự nhiên các nhân tố. khi đó
tọa độ đơn hình ban đầu chuyển từ tỉ lệ mã hóa sang tự nhiên. Đối với mỗi nhân tố y
đưa ra mức cơ sở Xio và khoảng giá trị Xi, thì:
Xiu = X io + Xixiu
Trong đó: - xiu – giá trị mã hóa nhân tố thứ I trong thí nghiệm thứ u
Xiu- giá trị nhân tố thứ i trong thí nghiệm thứ u dạng tự nhiên.
Ta sử dụng đơn hình đều đối với nhân tố bất kỳ. Ở đây đơn hình được sử dụng
là quy hoạch đối với loạt thí nghiệm đầu tiên, ta đưa chúng về dạng các ma trận bình
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxiv
thường dưới dạng mã hóa các nhân tố dịch chuyển của đơn hình trong miền tối ưu thực
hiện theo quy tắc đối xứng. Khi đó đỉnh của đơn hình có giá trị xấu nhất của tham số
tối ưu được loại bỏ và thay bằng đỉnh mới, đối xứng qua cạch đối diện của đỉnh được
loại bỏ. tọa độ của đỉnh mới ở dạng tự nhiên.
2 k
X ik 2
k u 1
xiu X it
Trong đó: X ik 2 - tọa độ theo trục x đỉnh mới của đơn hình k nhân tố
k- số nhân tố.
X it - tọa độ đỉnh có giá trị xấu nhất tham số tối ưu.
X iu - tổng tọa độ (theo trục Xi ) các nhân tố ngoại trừ X it .
Sau khi đạt vị trí tối ưu ta có thể kiểm tra vị trí điểm tối ưu bằng cách sử dụng quy
hoạch thực nghiệm bậc 2.
2.1.2. Khảo sát ảnh hưởng của độ acid kết hợp với ion kim loại tạo
phức trong quá trình chần.
Mục đích: Sự thay đổi pH trong quá trình chần và các ion kim loại tạo
phức có ảnh đến việc giữ màu chlorophyll của sản phẩm, do đó chúng
tôi thay đổi giá trị pH cũng như nồng độ muối và thời gian xử lý để
giữ màu chlorophyll tốt nhất.
Bố trí thí nghiệm bằng phương án quy hoạch trực giao cấp I
Bố trí thí ngiệm:
- Chọn yếu tố ảnh hưởng:
Z1: Nồng độ NaOH, C%.
Z2: Thời gian chần, phút.
Z3: nồng độ ion kim loại tạo phức ( VD: Cu2+).
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxv
- Chọn hàm mục tiêu.
Y1: Chỉ tiêu cảm quan màu (Y1 Max)
Phương trình biểu diễn mối quan hệ có dạng:
Y1 = f (Z1 , Z2, Z3)
Chọn miền khảo sát:
Dựa vào các thí nghiệm khảo sát sơ bộ chúng tôi chọn miền khảo sát của
các yếu tố là:
o Nồng độ NaOH: 1% -2%.
o Thời gian chần trong khoảng 1 ÷ 5 phút.
o Nồng độ ion Cu2+: 10-30ppm. (Zn2+, Mg2+ tương tự như khảo sát
trên).
Bảng 1.2: Điều kiện thí nghiệm chần theo nhiệt độ và thời
gian.
Các yếu tố ảnh hưởng
Nồng độ ion kim loại
Các mức Z2: Thời gian
Z1: Nồng độ NaOH tạo phức VD: Cu2+
chần, phút
(ppm)
Mức trên (+1) 0,1% 5 30
Mức cơ sở (0) 0,0755% 3 20
Mức dưới (-1) 0,05% 1 10
Khoảng biến thiên 0,025% 2 10
Chọn phương án quy hoạch trực giao cấp I ( TYT- 2k) thực nghiệm yếu
tố toàn phần 2 mức, 3 yếu tố ảnh hưởng. phương trình hồi quy có dạng.
Y= b0 + b1x1 + b2x2 + b3x3 + b12x1x2 + b13x1x3 + b23x2x3
Trong đó :
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxvi
x1: Nồng độ NaOH : x2: thời gian chần: x3: nồng độ ion kim loại tạo phức
b0: hệ số hồi qui
b1, b2, b3: hệ số tuyến tính.
b12, b23, b13: hệ số tương tác đôi.
- Tổ chức thí nghiệm trực giao cấp I.
Để nhanh chóng tiến tới miền tối ưu, chúng tôi tiến hành 11 thí
nghiệm điều kiện đã chọn ở bảng 2.2. Trong đó số thí nghiệm của
phương án là 2k= 8, (k=3). Số thí nghiệm ở tâm là 3.
Bảng1.3: kế hoạch bố trí thí nghiệm chần.
Stt Theo giá trị mã hóa Theo giá trị thực
x0 x1 x2 x3 x1x2 x1x3 x2x3 x1 x2 x3
1 + + + + + + + 0,1% 5 30
2 + - - + + - - 0,05% 1 30
3 + + - + - + - 0,1% 1 30
4 + - + + - - + 0,05% 5 30
5 + + + - + - - 0,1% 5 10
6 + - - - + + + 0,05% 1 10
7 + + - - - - + 0,1% 1 10
8 + - + - - + - 0,05% 5 10
9 + 0 0 0 0 0 0 0,0755% 3 20
10 + 0 0 0 0 0 0 0,075% 3 20
11 + 0 0 0 0 0 0 0,075% 3 20
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxvii
Tiến hành thí nghiệm.
Lá chùm ngây tươi sau khi rửa sạch sẽ đem đi cân với lượng là 25g/ mẫu.
25g/ nghiệm thức X 11 nghiệm thức = 275g
Các mẫu sau khi chần theo bảng 1.3 sẽ được rửa lại bằng nước lạnh ở
nhiệt độ 50C, sau khi rửa xong mẫu sẽ được nghiền và ép thu dịch (có bổ sung
thêm nước vào với tỉ lệ 1:1 để dễ nghiền ép thu dịch).
Tiến hành đánh giá:
Hàm mục tiêu chủ yếu của khảo sát trên là độ hấp phụ OD của sản phẩm. vì thế
chúng tôi tiến hành đo OD của mẫu sau quá trình xử lý thu dịch và chúng tôi tiến hành
gia nhiệt lên nhiệt độ cao để quan sát sự thay đổi màu của sản phẩm và đo giá trị OD
sau đun sôi.
Nghi nhận lại kết quả đo OD cho từng mẫu rồi biện luận, viết phương trình hồi quy cho
từng yếu tố. sau đó tối ưu hóa Quy hoạch thực nghiệm bằng phương pháp đơn hình đều
như khảo sát trên.
2.1.3. Khảo sát ảnh hưởng của độ acid trong quá trình chần kết hợp với
ngâm ion kim loại sau chần
Mục đích: quá trình chần trong môi trường kiềm vừa giúp khả năng giữ màu
Chlorophyll đồng thời nó giúp phá vỡ tế bào trong quá trình chần để các ion có thể
khuếch tán vào trong tạo phức và góp phần giữ màu chlorophyll. Do thời gian chần
ngắn nên khả năng giữ màu và tạo phức của ion kim loại có thể kém vì thế chúng tôi
muốn tiến hành khảo sát sau quá trình chần sẽ ngâm với dung dịch ion kim loại tạo
phức nhằm góp phần giữ được dinh dưỡng của sản phẩm và giữ được màu xanh cho
sản phẩm.
Bố trí thí nghiệm bằng phương án quy hoạch trực giao cấp I
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxviii
Bố trí thí ngiệm:
- Chọn yếu tố ảnh hưởng:
Z1: Nồng độ NaOH, C%.
Z3: thời gian ngâm.
Z3: nồng độ ion kim loại tạo phức
- Chọn hàm mục tiêu.
Y: độ hấp phụ OD.
Phương trình biểu diễn mối quan hệ có dạng:
Y1= f (Z1 , Z2, Z3)
Chọn miền khảo sát:
Dựa vào các thí nghiệm khảo sát sơ bộ chúng tôi chọn miền khảo sát của
các yếu tố là:
o Nồng độ NaOH: 0.05% -0. 1%.
o Thời gian ngâm 30 -120 phút
o Nồng độ ion kim loại tạo phức ( VD: Zn2+ 100 -150ppm, Cu2+ và
Mg2+ như ở các khảo sát trên).
Bảng 1.9: Điều kiện thí nghiệm chần theo nhiệt độ và thời
gian.
Các yếu tố ảnh hưởng
Các mức Thời gian ngâm Nồng độ ion kim loại
Z1: Nồng độ NaOH
(phút) (ppm) VD: Zn2+
Mức trên (+1) 0,1% 120 150
Mức cơ sở (0) 0,075% 75 125
Mức dưới (-1) 0,05% 30 100
Khoảng biến thiên 0,025% 45 25
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxix
Chọn phương án quy hoạch trực giao cấp I ( TYT- 2k) thực nghiệm yếu
tố toàn phần 2 mức, 3 yếu tố ảnh hưởng. phương trình hồi quy có dạng.
Y= b0 + b1x1 + b2x2 + b3x3 + b12x1x2 + b13x1x3 + b23x2x3
Trong đó :
x1: Nồng độ NaOH : x2: thời ngâm: x3: nồng độ ion kim loại tạo phức
b0: hệ số hồi qui
b1, b2, b3: hệ số tuyến tính.
b12, b23, b13: hệ số tương tác đôi.
- Tổ chức thí nghiệm trực giao cấp I.
Để nhanh chóng tiến tới miền tối ưu, chúng tôi tiến hành 11 thí
nghiệm điều kiện đã chọn ở bảng 1.9. Trong đó số thí nghiệm của
phương án là 2k= 8, (k=3). Số thí nghiệm ở tâm là 3.
Bảng 2.0: kế hoạch bố trí thí nghiệm chần.
Stt Theo giá trị mã hóa Theo giá trị thực
x0 x1 x2 x3 x1x2 x1x3 x2x3 x1 x2 x3
1 + + + + + + + 0,1% 120 150
2 + - - + + - - 0,05% 30 150
3 + + - + - + - 0,1% 30 150
4 + - + + - - + 0,05% 120 150
5 + + + - + - - 0,1% 120 100
6 + - - - + + + 0,05% 30 100
7 + + - - - - + 0,1% 30 100
8 + - + - - + - 0,05% 120 100
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxx
9 + 0 0 0 0 0 0 0,075% 75 125
10 + 0 0 0 0 0 0 0,075% 75 125
11 + 0 0 0 0 0 0 0,075% 75 125
Tiến hành thí nghiệm:
Lá chùm ngây tươi sau khi rửa sạch sẽ đem đi cân với lượng là 25g/ mẫu.
25g/ nghiệm thức X 11 nghiệm thức = 275g
Lá chùm ngây sẽ được chần ở nhiệt độ 1000C/ 1 phút, sau đó sẽ được rửa
bằng nước lạnh 50C và sẽ tiến hành ngâm dung dịch có chứa ion kim loại tạo
phức. Sau quá trính ngâm ta sẽ tiến hành xay nhuyễn ( có bổ sung nước với tỉ lệ
1:1) và thu dịch.
Tiến hành đánh giá:
Hàm mục tiêu chủ yếu của khảo sát trên là giá trị OD của sản phẩm. vì thế chúng
tôi tiến hành đo OD của mẫu sau quá trình xử lý thu dịch và chúng tôi tiến hành gia
nhiệt lên nhiệt độ cao để quan sát sự thay đổi màu của sản phẩm và đo OD mẫu sau gia
nhiệt.
Tiến hành đánh giá cảm quan các mẫu theo bảng 1.4 như ở thí nghiệm đã khảo sát
ở trên.
Nghi nhận lại kết quả cảm quan màu cho từng mỗi mẫu rồi biện luận, viết phương
trình hồi quy cho từng yếu tố. sau đó tối ưu hóa Quy hoạch thực nghiệm.
2.1.4. Khảo sát quá trình chần kết hợp với ngâm acid citric
Bố trí thí nghiệm:
o Chọn các yếu tố ảnh hưởng:
Z1: thời gian ngâm, phút.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxxi
Z2: nồng độ ion kim loại tạo phức, ppm.
o Chọn các hàm mục tiêu:
Y: Màu (Y Max).
Phương trình biểu diễn mối quan hệ có dạng: Y = f (Z1 , Z2);
Chọn miền khảo sát:
Dựa vào các thí nghiệm khảo sát sơ bộ,chúng tôi chọn miền khảo sát của các
yếu tố là:
+ thời gian ngâm: 30-120 phút.
+ nồng độ ion kim loại tạo phức, VD: Cu2+ 10- 30ppm
Từ đó xây dựng điều kiện thí nghiệm theo bảng 2.5
Bảng 2.1: Điều kiện thí nghiệm xử lý với enzyme
pectinase
Các yếu tố ảnh hưởng
Các mức Z2: Nồng độ ion kim
Z1: Thời gian ngâm
loại
Mức trên (+1) 120 30
Mức cơ sở (0) 75 20
Mức dưới (-1) 30 10
Khoảng biến thiên 45 10
Chọn phương án quy hoạch trực giao cấp I(TYT 2k) thực nghiệm yếu tố toàn
phần 2 mức, 2 yếu tố ảnh hưởng. Phương trình hồi qui có dạng:
Y = b0 + b1x1 + b2x2 + b12x1x2
Trong đó:
x1: Nồng độ enzyme; x2: Thời gian xử lý
b0: Hệ số hồi qui.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxxii
b1, b2: Hệ số tuyến tính
b12: Hệ số tương tác đôi
o Tổ chức thí nghiệm trực giao cấp I:
Để nhanh chóng tiến tới miền tối ưu, chúng tôi tiến hành 7 thí nghiệm điều kiện
đã chọn ở bảng 2.1. Trong đó số thí nghiệm của phương án là 2k = 4, (k = 2), số thí
nghiệm ở tâm là 3.
Biến mã Giá trị thực
STT
Số thí x1 x2 x1x2 x1 x2
nghiệm 120 30
1 - - +
trong
2 - + - 30 10
phương án
2k 3 + - - 120 10
4 + + + 30 30
5 0 0 0 75 20
Số thí
nghiệm ở 6 0 0 0 75 20
tâm 7 0 0 0 75 20
Bảng 2.2: Kế hoạch bố trí thí nghiệm xử lý enzyme
Tiến hành thí nghiệm:
Lá chùm ngây tươi sau khi rửa sạch sẽ đem đi cân với lượng là 25g/ mẫu.
25g/ nghiệm thức X 11 nghiệm thức = 275g
Lá chùm ngây sẽ được chần ở nhiệt độ 1000C/ 1 phút, sau đó sẽ được rửa
bằng nước lạnh 50C và sẽ tiến hành ngâm dung dịch có chứa ion kim loại tạo
phức. Sau quá trính ngâm ta sẽ tiến hành xay nhuyễn ( có bổ sung nước với tỉ lệ
1:1) và thu dịch.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxxiii
Tiến hành đánh giá:
Hàm mục tiêu chủ yếu của khảo sát trên là giá trị OD của sản phẩm. vì thế chúng
tôi tiến hành đo OD của mẫu sau quá trình xử lý thu dịch và chúng tôi tiến hành gia
nhiệt lên nhiệt độ cao để quan sát sự thay đổi màu của sản phẩm và đo OD mẫu sau gia
nhiệt.
Tiến hành đánh giá cảm quan các mẫu theo bảng 1.4 như ở thí nghiệm đã khảo sát
ở trên.
Nghi nhận lại kết quả cảm quan màu cho từng mỗi mẫu rồi biện luận, viết phương
trình hồi quy cho từng yếu tố. sau đó tối ưu hóa Quy hoạch thực nghiệm.
2.1.5. Khảo sát xử lý sơ bộ với emzyme cenllulase.
Mục đích:
Giúp tăng hiệu suất thu hồi chất khô, giữ được giá trị dinh dưỡng cao cho sản
phẩm.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxxiv
Bố trí thí nghiệm:
o Chọn các yếu tố ảnh hưởng:
Z1: Nồng độ enzyme, %.
Z2: Thời gian xử lý, phút.
o Chọn các hàm mục tiêu:
Y1: hiệu suất thu hồi chất khô, % (Y1Max).
Y2: Màu (Y2 Max).
Y3: Mùi (Y3 Max).
Phương trình biểu diễn mối quan hệ có dạng: Y1 = f (Z1 , Z2); Y2 = (Z1, Z2); Y3 =
(Z1, Z2).
o Chọn miền khảo sát:
Dựa vào các thí nghiệm khảo sát sơ bộ,chúng tôi chọn miền khảo sát của các
yếu tố là:
+ Nồng độ enzyme: 0,1 – 1%
+ Thời gian xử lý: 30 phút – 2 giờ
Từ đó xây dựng điều kiện thí nghiệm theo bảng 2.5
Bảng 2.1: Điều kiện thí nghiệm xử lý với enzyme
pectinase
Các yếu tố ảnh hưởng
Các mức
Z1: Nồng độ enzyme , % Z2: Thời gian xử lý, phút
Mức trên (+1) 1 120
Mức cơ sở (0) 0,55 75
Mức dưới (-1) 0,1 30
Khoảng biến thiên 0,45 45
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxxv
Chọn phương án quy hoạch trực giao cấp I(TYT 2k) thực nghiệm yếu tố toàn
phần 2 mức, 2 yếu tố ảnh hưởng. Phương trình hồi qui có dạng:
Y = b0 + b1x1 + b2x2 + b12x1x2
Trong đó:
x1: Nồng độ enzyme; x2: Thời gian xử lý
b0: Hệ số hồi qui.
b1, b2: Hệ số tuyến tính
b12: Hệ số tương tác đôi
o Tổ chức thí nghiệm trực giao cấp I:
Để nhanh chóng tiến tới miền tối ưu, chúng tôi tiến hành 7 thí nghiệm điều kiện
đã chọn ở bảng 2.1. Trong đó số thí nghiệm của phương án là 2k = 4, (k = 2), số thí
nghiệm ở tâm là 3.
Biến mã Giá trị thực
Số thí STT
x1 x2 x1x2 x1 x2
nghiệm
trong 1 - - + 0,1 120
phương án 2 - + - 0,1 30
2k
3 + - - 1 120
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxxvi
4 + + + 1 30
5 0 0 0 0,55 75
Số thí
nghiệm ở 6 0 0 0 0,55 75
tâm 7 0 0 0 0,55 75
Bảng 2.2: Kế hoạch bố trí thí nghiệm xử lý enzyme
Tiến hành thí nghiệm:
Lá chùm ngây tươi sau khi rửa sạch sẽ được đem đi cân với lượng là 25g/mẫu.
=> 25g/nghiệm thức x 7 nghiệm thức = 175g
Trước khi xử lý với enzyme, tiến hành xay nhuyễn bằng máy xay sinh tố, có bổ
sung nước tỉ lệ 1:1 để quá trình xay nhuyễn được dễ dàng và thuận lợi. Thực hiện thí
nghiệm theo bảng 2.1. Trong quá trình xử lý, duy trì nhiệt độ ổn định từ 550C để tạo
điều kiện thuận lợi cho enzyme hoạt động. Sau khi xử lý, gia nhiệt mẫu lên 80oC để bất
hoạt enzyme rồi mới vắt lọc thu dịch.
Tiến hành đánh giá:
Tiến hành đo nồng độ chất khô, tính toán hiệu suất thu hồi chất khô và đánh giá
cảm quan các mẫu theo bảng 1.4 như ở thí nghiệm chần.
So sánh hiệu suất thu hối chất khô giữa emzyme cenlulase và emzyme
Pectinase.
Ghi nhận lại kết quả cảm quan màu, mùi cũng như hiệu suất thu hồi chất khô
cho từng mẫu rồi biện luận, viết phương trình hồi quy cho từng yếu tố. tôi ưu hóa thực
nghiệm bằng phương pháp
1 So sánh với mẫu đối chứng để chọn được quá trình xử lý phù hợp:
Mục đích:
Chọn được mẫu tối ưu nhất về đồng thời cả 3 chỉ tiêu cảm quan mùi, cảm quan
màu và hiệu suất thu hồi chất khô. Tuy nhiên mẫu có chỉ tiêu cảm quan màu tốt hơn sẽ
được ưu tiên chọn.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxxvii
Bố trí thí nghiệm:
Thí nghiệm gồm 1 yếu tố với 5 nghiệm thức là mẫu đối chứng, mẫu tối ưu của
độ acid kết hợp với ion kim loại tạo phức, mẫu tối ưu của quá trình chần kết hợp xử lý
với ion tạo phức sau chần và mẫu tối ưu của quá trình xử lý với enzyme Cenlulase,
mẫu lạnh đông.
Tiến hành thí nghiệm:
Lá chùm ngây tươi sau khi rửa sạch sẽ được đem đi cân với lượng là 25g/mẫu
=> 25g/nghiệm thức x 5 nghiệm thức = 125g
+ Mẫu đối chứng: sau khi cân và rửa sạch, tiến hành xay nghiền (có bổ sung
nước tỉ lệ 1:1) và lọc thu dịch.
+ mẫu tối ưu của quá trình chần kết hợp với ion kim loại tạo phức: đem 25g lá
chần ở nhiệt độ và thời gian tối ưu đã được khảo sát ở thí nghiệm trước, rồi cũng xay
nghiền có bổ sung thêm nước (tỉ lệ 1:1) rồi lọc thu dịch.
+ Mẫu tối ưu của nồng độ NaOH kết hợp với kim loại tạo phức: đem 25g lá
chần ở nhiệt độ và thời gian tối ưu đã được khảo sát ở thí nghiệm trước, rồi cũng xay
nghiền có bổ sung thêm nước (tỉ lệ 1:1) rồi lọc thu dịch.
+ Mẫu tối ưu của quá trình chần kết hợp xử lý với ion tạo phức sau chần và mẫu
tối ưu của quá trình xử lý với enzyme Cenlulase: đem cân 25g lá chần ở nhiệt độ
1000C/ 1 phút sau đó ta tiến hành ngâm trong dung dịch chứa ion kim loại tạo phức và
giá trị thời gian đã được khảo sát ở trên.
+ Mẫu xử lý enzyme tối ưu: đem 25g lá xay nghiền (có bổ sung nước tỉ lệ 1:1)
rồi bổ sung enzyme vào với nồng độ tối ưu đã được khảo sát. Duy trì hỗn hợp này ở
nhiệt độ 500C trong khoảng thời gian tối ưu cũng đã được khảo sát ở thí nghiệm trên.
Kết thúc quá trình xử lý enzyme, tiến hành nâng nhiệt độ của hỗn hợp lên 800C để bất
hoạt enzyme rồi mới đem lọc thu dịch.
Tiến hành đo nồng độ chất khô và hiệu suất thu hồi chất khô ở cả 3 mẫu tương
tự như các thí nghiệm trước.
Tiến hành đánh giá:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxxviii
Kết thúc quá trình tiến hành đánh giá cảm quan các mẫu theo bảng 2.3 và 2.4
như ở thí nghiệm chần.
Ghi nhận lại kết quả cảm quan màu, mùi cũng như hiệu suất thu hồi chất khô
cho từng mẫu rồi biện luận để chọn được mẫu tối ưu cho quá trình xử lý nguyên liệu
ban đầu.
1.2 khảo sát độ kết lắng của chất ổn định trong khoảng tối ưu.
1.2.1 khảo sát sơ bộ chất ổn định.
1.2.1.1khảo sát ảnh hưởng của đơn chất đến độ đồng nhất của
sản phẩm.
mục đích: khảo sát việc sử dụng đơn chất ổn định để đạt
được độ đồng nhất cho sản phẩm.
bố trí thì nghiệm:
dịch phối chế: 300ml
chất ổn định sử dụng: CMC, Pectin,Xanthan gum, Alginate,
Guar Gum, carrageenan.
Tiến hành bổ sung các chất ổn định với 4 mức nồng độ khác nhau vào dịch phối
chế theo bảng:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 lxxxix
Chất ổn định Xanthan Carrageenan Alginate Guar
CMC Pectin Gum
Nồng độ (%) gum
Tiến
0,1 C1 P1 X1 N1 A1 G1
h 0,2 C2 P2 X2 N2 A2 G2
à 0,3 C3 P3 X3 N3 A3 G3
n 0,4 C4 P4 X4 N4 A4 G4
h
thí nghiệm:
Pha dung dịch các chất ổn định có nồng độ 5%
Tiến hành phối chế mẫu bao gồm dịch cốt chùm ngây, đường và acid citric theo
công thức tối ưu đã khảo sát được, phần nước thêm vào cho đủ được trích ra một phần
để pha dung dịch chất ổn định 5%, tuy nhiên lượng nước này là không đáng kể nên ta
có thể phối dịch chất ổn định 5% đã pha sẵn vào dịch phối chế luôn theo bảng 2.11.
Do điều kiện phòng thí nghiệm, tiến hành đồng nhất mẫu tương đối bằng máy
xay sinh tố cầm tay trong 3 phút, bài khí, rót nóng ở 85 oC, rót nóng và thanh trùng theo
công thức tham khảo là 105oC trong 15 phút.
Các mẫu được đánh giá cảm quan về trạng thái độ nhớt và độ đặc, đồng thời
quan sát độ kết lắng trong vòng 1 tháng rối nghi lại kết quả.
1.2.1.2 khảo sát ảnh hưởng sự kết hợp 2 chất đến độ đồng nhất
của sản phẩm.
mục đích: khảo sát việc sử dụng kết hợp 2 chất ổn định để
đảm bảo độ đồng nhất cho sản phẩm.
bố trí thì nghiệm:
dịch phối chế: 300ml
chất ổn định sử dụng: CMC-Pectin,CMC- Xanthan gum,
Xanthan gum – Pectin, CMC-guar gum, Pectin –guar gum,
Xanthangum – Guar gum.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xc
Tiến hành bổ sung các chất ổn định với các mức nồng độ, 2 chất ồn định khác
nhau vào dịch phối chế theo bảng:
VD: CMC – Xanthan Gum
Nghiệm thức Chất ổn định
CMC (%) Xanthan Gum (%)
1 0.05 0.05
2 0.1 0.1
3 0.2 0.05
4 0.05 0.2
5 0.2 0.2
Các cặp chất ổn định khác cũng tiến hành bố trí như bảng trên.
Tiến hành thí nghiệm:
Pha dung dịch các chất ổn định có nồng độ 5%
Tiến hành phối chế mẫu bao gồm dịch cốt chùm ngây, đường theo công thức tối
ưu đã khảo sát được, phần nước thêm vào cho đủ được trích ra một phần để pha dung
dịch chất ổn định 5%, tuy nhiên lượng nước này là không đáng kể nên ta có thể phối
dịch chất ổn định 5% đã pha sẵn vào dịch phối chế luôn theo bảng 2.11.
Do điều kiện phòng thí nghiệm, tiến hành đồng nhất mẫu tương đối bằng máy
xay sinh tố cầm tay trong 3 phút, bài khí, rót nóng ở 85 oC, rót nóng và thanh trùng theo
công thức tham khảo là 105oC trong 15 phút.
Các mẫu được đánh giá cảm quan về trạng thái độ nhớt và độ đặc, đồng thời
quan sát độ kết lắng trong vòng 1 tháng rối nghi lại kết quả.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xci
1.2.1.3 khảo sát ảnh hưởng sự kết hợp 3 chất đến độ đồng nhất
của sản phẩm.
mục đích: khảo sát việc sử dụng kết hợp 3 chất ổn định để
đảm bảo độ đồng nhất cho sản phẩm.
bố trí thì nghiệm:
dịch phối chế: 300ml
chất ổn định sử dụng: CMC-Pectin – Xanthan gum, CMC-
carrageenan-xanthan gum, CMC-carrageenan – guar gum.
Tiến hành bổ sung các chất ổn định với các mức nồng độ, 2 chất ồn định khác
nhau vào dịch phối chế theo bảng:
VD: CMC – Carrageenan - Xanthan Gum
Nghiệm thức Chất ổn định
CMC (%) carrageenan Xanthan
gum
1 0.05 0.2 0.05
2 0.1 0.1 0.1
3 0.2 0.05 0.05
4 0.05 0.05 0.2
5 0.2 0.2 0.2
Các cặp chất ổn định khác cũng tiến hành bố trí như bảng trên.
Tiến hành thí nghiệm:
Pha dung dịch các chất ổn định có nồng độ 5%
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xcii
Tiến hành phối chế mẫu bao gồm dịch cốt chùm ngây, đường theo công thức tối
ưu đã khảo sát được, phần nước thêm vào cho đủ được trích ra một phần để pha dung
dịch chất ổn định 5%, tuy nhiên lượng nước này là không đáng kể nên ta có thể phối
dịch chất ổn định 5% đã pha sẵn vào dịch phối chế luôn theo bảng 2.11.
Do điều kiện phòng thí nghiệm, tiến hành đồng nhất mẫu tương đối bằng máy
xay sinh tố cầm tay trong 3 phút, bài khí, rót nóng ở 85 oC, rót nóng và thanh trùng theo
công thức tham khảo là 105oC trong 15 phút.
Các mẫu được đánh giá cảm quan về trạng thái độ nhớt và độ đặc ( bảng ) ,
đồng thời quan sát độ kết lắng trong vòng 1 tháng rồi nghi lại kết quả.
Bảng điểm cảm quan độ nhớt
Điểm Thang điểm cảm quan độ nhớt
1.2.2 Tối ưu hóa chất ổn định đến độ đồng nhất của sản phẩm
1.2.2.1: tối ưu hóa đơn chất.
Mục đích: quan sát được hiện tượng kết lắng của sản phẩm theo từng
ngày.
Bố trí thí nghiệm:
Trong quá trình khảo sát sơ bộ, tìm được chất ổn định vừa cho điểm cảm
quan độ nhớt và độ đặc ở mức chấp nhận được, đồng thời quan sát sự kết
lắng theo thời gian rồi chọn ra được nghiệm thức tốt nhất rồi ta thu hẹp
khoảng nồng độ lại, tiến hành quan sát sự kết lắng theo ngày.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xciii
Tiến hành thí nghiệm:
Tiến hành phối chế mẫu bao gồm dịch cốt chùm ngây, đường theo công
thức tối ưu đã khảo sát được, phần nước thêm vào cho đủ được trích ra một
phần để pha dung dịch chất ổn định 5%, tuy nhiên lượng nước này là không
đáng kể nên ta có thể phối dịch chất ổn định 5% đã pha sẵn vào dịch phối chế
luôn theo bảng 2.7.
Do điều kiện phòng thí nghiệm, tiến hành đồng nhất mẫu tương đối bằng
máy xay sinh tố cầm tay trong 3 phút, bài khí, rót nóng ở 85oC, rót nóng và
thanh trùng theo công thức tham khảo là 105oC trong 15 phút.
Các mẫu được theo dõi độ kết lắng theo ngày ( 15 ngày) bằng phương
pháp đo độ truyển suốt (OD) 630nm.
1.2.2.2tối ưu hóa sự kết hợp các chất ổn định.
Qua khảo sát sơ bộ ta tiến hành chọn cặp chất kết hợp tối ưu,
thu hẹp khoảng nồng độ từng cặp chất lại, rồi bố trí thí
nghiệm và xử lý số theo phương án quy hoạch thực nghiệm
Tiến hành thí nghiệm:
Tiến hành phối chế mẫu bao gồm dịch cốt chùm ngây, đường theo công
thức tối ưu đã khảo sát được, phần nước thêm vào cho đủ được trích ra một
phần để pha dung dịch chất ổn định 5%, tuy nhiên lượng nước này là không
đáng kể nên ta có thể phối dịch chất ổn định 5% đã pha sẵn vào dịch phối chế
luôn theo bảng 2.7.
Do điều kiện phòng thí nghiệm, tiến hành đồng nhất mẫu tương đối bằng
máy xay sinh tố cầm tay trong 3 phút, bài khí, rót nóng ở 85oC, rót nóng và
thanh trùng theo công thức tham khảo là 105oC trong 15 phút.
Các mẫu được theo dõi độ kết lắng theo ngày ( 15 ngày) bằng phương
pháp đo độ truyển suốt (OD) 630nm.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xciv
Nghi nhận lải kết quả đo OD và tiến hành xử lý số liệu theo phương án quy hoạch thực
nghiệm
Xây dựng mô tả toán học cho từng hàm mục tiêu:
Sau khi chọn phương trình hồi qui (*), các hệ số b1, b2, b3, b12 được tính theo số
liệu thực nghiệm theo từng hàm mục tiêu.
2 Tính hệ số b:
Dựa vào công thức:
∑ni=1 Yi
𝑏0 =
N
n
∑ X ji Yi
i=1
bj =
N
n
∑ (X j . X l )i Yi
i=1
bjl =
N
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Sau đó, tính phương sai tái hiện theo công thức:
m
2
1 ̅̅̅0 )2
Sth = ∑(Yu0 − Y
m−1
u=1
Với m là số thí nghiệm ở tâm phương án (m = 3)
Sự có nghĩa của hệ số hồi qui được kiểm định theo tiêu chuẩn Student (t)
|𝑏𝑗 |
𝑡𝑗 = (**)
𝑆𝑏𝑗
Trong đó: bj: là hệ số thứ j trong phương trình hồi quy.
𝑆𝑡ℎ
Sbj: Độ lệch quân phương của hệ số thứ j, với: 𝑆𝑏𝑗 =
√𝑁
Tra bảng tiêu chuẩn Student tp(f) ứng với xác suất tin cậy p và bậc tự do
f, f = N0-1 rồi so sánh với tj.
o Nếu tj>tp(f) thì hệ số bj có nghĩa.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xcv
o Nếu tj <tp(f) thì hệ số bj bị loại khỏi phương trình.
Sau đó viết lại phương trình hồi qui với các hệ số bj có nghĩa.
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
Sự phù hợp của phương trình hồi qui được kiểm định theo tiêu chuẩn
Fisher.
2
𝑆𝑑ư
F= 2
𝑆𝑡ℎ
Trong đó:
𝑁
1
2
𝑆𝑑ư = ̂𝑖 )2
∑(Yi − 𝑌
𝑁−𝐿
𝑖=1
Với: N: số thí nghiệm trong phương án
L: số hệ số ý nghĩa
Yi: giá trị thực nghiệm
̂𝑖 : giá trị tính theo phương trình hồi qui
𝑌
Nếu F tính được nhỏ hơn giá trị tra bảng F1-p (f1, f2) với mức ý nghĩa p,
f1=N-L, f2= N0 – 1 thì phương trình tương thích với thực nghiệm
2.2. Khảo sát khoảng tối ưu của chất ổn định dựa vào điểm cảm
quan.
Mục đích: khảo sát ảnh hưởng của chất ổn định đến điểm cảm quan
độ nhớt và độ đặc cho sản phẩm.
Bố trí thí nghiệm:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xcvi
% chất ổn định
0.15 % 0.2% 0.25% 0.3%
Chất ổn định
Xanthan Gum 0.15 0.2 0.25 0.3
Xanthan Gum - 0.1-0.05 0.1 – 0.1
CMC 0.05 -0.1
0.075 -0.075
Xanthan Gum -
pectin
Xanthan Gum -
Carrageenan-
CMC
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xcvii
4. Khảo sát quá trình thanh trùng.
4.1 Xác định các tham số trong việc xây dựng công thức thanh trùng bằng
phương pháp toánhọc (D, z) thông qua khảo sát thực nghiệm
Mục đích: Các hệ số D và z được sử dụng trong tính toán công thức thanh
trùng, thông thường người ta tìm giá trị D, z dựa vào các giá trị tương đồng,
tuy nhiên đôi khi những sản phẩm tương đồng này nó lại không phù hợp cho
lắm, nên để chính xác hơn thì việc xác định các giá trị D và z trong điều kiện
có thể thực hiện được là điều nên làm.
Cách tiến hành.
Mẫu nghiên cứu trước khi thực hiện quá trình thanh trùng ta đem
đi xác đinh mật độ của vi sinh vật chỉ thị ban đầu có trong sản
phẩm
Thực hiện thanh trùng nhiều mẫu ở các mốc nhiệt độ khác nhau.
Xác định mật độ vi sinh vật chỉ thị sau quá trình thanh trùng.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xcviii
Từ giá trị mật độ vi sinh vật trước và sau quá trình thanh trùng ta
T
sẽ dựa vào công thức( D ) để tình
log 10 N 0 log 10 N1
giá trị D và dựa vào đồ thị Log (Dt) để tìm ra giá trị Z của vi sinh
vật chỉ thị.
Cách đánh giá.
Mẫu sau xử lý nhiệt ờ các mốc nhiệt độ khác nhau sẽ được đem đi xác định số
vi sinh vật còng lại sau thanh trùng.
4.2 Xác định công thức thanh trùng bằng phương pháp toán học tương ứng
ở các mốc nhiệt độ khác nhau.
Mục đích: Khi ta xử lý nhiệt ở các nhiệt độ khác nhau thì bên cạnh việc tiêu
diệt vi sinh vật còn ảnh hưởng đến giá trị cảm quan của sản phẩm, chúng tôi
muốn có một công thức thanh trùng phù hợp để tiếp tục khảo sát các khía cạnh
khác của sản phẩm.
Cách tiến hành: các mẫu thí nghiệm sẽ sẽ được xử lý nhiệt ở các chế độ khác
nhau.
Tiến hành đánh giá: Các mẫu sau khi xử lý nhiệt sẽ được đánh giá cảm quan
toàn diện sản phẩm về màu, mùi và cấu trúc của sản phẩm để tìm ra công thức
thanh trùng tôi ưu.
4.3 Đánh giá cảm quan toàn diện sản phẩm, xây dựng công thức hoàn
thiện sản phẩm
Mục đích: Hiện nay một số công trình nghiên cứu dùng phương pháp đánh giá
cảm quan để đánh giá chất lượng sản phẩm, tuy nhiên những nghiên cứ này thực
hiện đánh giá cảm quan trước khi thanh trùng, đồng nghĩa với sản phẩm sau
thanh trùng có thể không đạt giá trị cảm quan như lúc đầu. Với đề tài này chúng
tôi tiến hành thanh trùng sản phẩm trước khi đánh giá cảm quan. Như vậy sản
phẩm sẽ đạt ATVSTP và cả giá trị cảm quan.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 xcix
Cách tiến hành: các mẫu thí nghiệm sẽ được đánh giá cảm quan trước quá trình
xử lý nhiệt, sau đó thực hiện quá trình xử lý nhiệt đồng thới đánh giá cảm quan
chất lượng sản phẩm sau quá trình xử lý nhiệt.
So sánh giá trị cảm quan, giá trị dinh dưỡng trước và sau quá trình thanh trùng.
Từ đó ta lựa chọn công thức thanh trùng vừa đảm bảo ATVSTP và đạt về giá trị
cảm quan.
Tiến hành đánh giá:
Đánh giá cảm quan toàn diện sản phẩm vế chỉ tiêu màu như bảng (1.4 ) chỉ tiêu
mùi ( bảng 3.3 ), chỉ tiêu trạng thái (bảng 2.8)
Bảng 3.3 bảng điểm cảm quan mùi
Điểm Mùi
0 Mùi lạ, mùi hư hỏng, khó chịu
1 Không mùi hoặc có mùi nấu
2 Nồng
3 Hơi nồng
4 Thoang thoảng
5 Dịu nhẹ đặc trưng, dễ chịu
5. Tiến hành đa dạng hóa sản phẩm.
5.1 tiến hành cải thiện mùi của sản phẩm:
Mục đích: Lá chùm ngây thường tạo mùi nồng và hăng trong sản phẩm, để tạo
mùi thơm dễ chịu nhưng vẫn giữ mùi đặc trưng của chùm ngây. Đồng thời giảm
thiểu mùi nấu (nếu có) sau quá trình thanh trùng sản phẩm.
Bố trí thí nghiệm:
Tiến hành bổ sung dịch đậu nành rang vào dịch phối chế theo bảng:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 c
Dịch đậu Dịch
Nghiệm Dịch cốt Nước cho vào
nành rang Đường
thức (ml) đủ 60ml
(ml) 50%
A1 20 2.5 12 25.5
A2 20 5 12 23
A3 20 7.5 12 20.5
A4 20 10 12 18
B1 25 2.5 12 20.5
B2 25 5 12 18
B3 25 7.5 12 15.5
B4 25 10 12 13
C1 30 2.5 12 15.5
C2 30 5 12 13
C3 30 7.5 12 10.5
C4 30 10 12 8
D1 35 2.5 12 10.5
D2 35 5 12 8
D3 35 7.5 12 5.5
D4 35 10 12 3
Tiến hành thí nghiệm:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 ci
Lá chùm ngây tươi sau khi rửa sạch sẽ được đem đi cân với lượng là 150g.
Chuẩn bị dịch cốt chùm ngây theo các thông số tối ưu đã khảo sát được.
Chuẩn bị dịch đường saccharose 50% như sau: cân 200gr đường và pha vào
200ml nước ấm khoảng 500C.
Chuẩn bị dịch đậu nành rang như sau: đậu nành rang ở nhiệt độ 130 0C/7,5 phút,
rồi sau đó trích ly với tỉ lệ nguyên liệu: dung môi là 1: 10 ở nhiệt độ 100 0C/15 phút.
Dịch đậu nành rang sẽ được lọc qua vải lọc.
Các mẫu thu được sau quá trình lọc được tiến hành phối chế theo bảng
Tiến hành đánh giá:
Các mẫu sau qáu trình phối chế sẽ được đánh giá cảm quan về mức độ ua thích
của mình đối với từng nghiệm thức với thang điểm 9.
Điểm
9
8
7
6
5
4
3
2
1
0
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cii
Ghi nhận lại kết quả cảm quan thị hiếu của 20 thành viên trong hội cảm quan rồi
dùng phần mềm Statgraphic plus 3.0 để xử lý thống kê. Biện luận kết quả để
chọn được mẫu tối ưu nhất.
6. Nghiên cứu chế biến soup chùm ngây.
Mục đích: góp phần đa dạng hóa dòng sản phẩm nước uồng trên thị trường việt nam, đồng thời cải
thiện màu sắc của sản phẩm và góp phần tăng giá trị dinh dưỡng cho sản phẩm.
6.1 khảo sát dịch cà rốt và dịch nấm bổ sung vào sản phẩm
Mục đích: góp phẩn làm tăng giá trị cảm quan và dinh dưỡng cho sản phẩm cho sản phẩm.
Bố tri thí nghiệm:
Tiến hành phối chế dịch chùm ngây, dịch nấm và dịch cà rốt với các mức độ khác nhau theo bảng
Mẫu Dịch cốt Dịch Dịch Nước cho vào
(25ml/mẫu) (ml) Cà rốt nấm đủ 100 ml
A1 50 25 25 0
A2 40 20 25 15
A3 30 15 25 35
A4 50 15 20 15
B1 40 20 20 20
B2 30 25 20 25
B3 50 25 15 10
B4 40 20 15 25
C1 30 15 15 40
Tiến hành thí nghiệm:
Lá chùm ngây sẽ được rửa sạch, chần và tiến hành thu dịch. Nầm sẽ được đun sôi trong thời gian 30
phút, xay nhuyễn và thu dịch. Cà rốt sẽ được đun sôi trong thời gian 30 phút và xay nhuyễn thu dịch
cà rốt.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 ciii
Thực hiện quá trình phối chế với các nghiệm thức ở bảng ( ). Cho 2 ml muối NaCl 20% vào trong
100ml dịch đã phối chế.
Tiến hành đánh giá:
Các mẫu sau quá trình phối chế sẽ được đánh giá cảm quan theo phương pháp cho điểm thị hiều với
thang điểm như sau:
Điểm
9
8
7
6
5
4
3
2
1
0
Ngh nhận lại kết quả cảm quan của 20 thành viên trong hội đồng đánh già cảm quan rồi dùng phần
mềm Statgraphic plus 3.0 để xử lý thống kê. Biện luận kết quả để chọn mẫu tối ưu nhất.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 civ
Phần III. BÁO CÁO KẾT QUẢ THÍ NGHIỆM
1. Khảo sát quá trình sơ chế
1.1. Khảo sát quá trình chần kết hợp với ion kim loại.
1.1.1. Khảo sát quá trình chần kết hợp với ion Cu2+.
Bảng 1.1 : kết qua đo độ hấp phụ Chlorophyll ở bước sóng 680nm.
Mẫu
Số thí nghiệm trong phương án 2k Tại tâm
1 2 3 4 5 6 7
Giá trị OD 8.8 10.4 9.8 11.10 10.4 10.3 10.1
Bảng 1.2: điểm cảm quan màu trước đun sôi
Mẫu
Điểm các thành
viên hội đồng
Số thí nghiệm trong phương án 2k Tại tâm
1 2 3 4 5 6 7
Thành viên 1 4 4 4 4.5 3.5 3.5 3
Thành viên 2 3.5 5 3.5 3 3.5 4 3.5
Thành viên 3 3.5 4.5 3 4 3 3.5 4.5
Thành viên 4 3 5 3.5 4.5 3.5 3 4
Thành viên 5 4 4.5 3.5 4.5 4 4 3
Điểm trung bình 3.6 4.6 3.5 4.1 3.5 3.6 3.6
Bảng 1.3: điểm cảm quan sau đun sôi.
Mẫu
Điểm các thành
viên hội đồng
Số thí nghiệm trong phương án 2k Tại tâm
1 2 3 4 5 6 7
Thành viên 1 2 4 1 4 4 5 4
Thành viên 2 2 4.5 1 4.5 3.5 4.5 5
Thành viên 3 2 5 1 4 3.5 4.5 4
Thành viên 4 2 5 1 4.5 4 4.5 4.5
Thành viên 5 1 5 1 4 3.5 4 4
Điểm trung bình 1.8 4.7 1 4.2 4.5 4.5 4.3
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cv
Hàm mục tiêu độ hấp phụ Chlorophyll.
Chọn phương trình hồi qui (*), các hệ số b1, b2, b3, b12 được tính theo số liệu thực
nghiệm hàm mục tiêu độ hấp phụ Chlorophyll (Y).
Tính hệ số b: theo phần đánh giá ở thí nghiệm trên ta có:
b0 b1 b2 b12
10.025 -0.725 -0.425 -0.075
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Kết quả các thí nghiệm ở tâm:
Bảng 1.4 kết quả thí nghiệm ở tâm
N0 𝑌𝑢0 ̅̅̅0
𝑌 ̅̅̅0
𝑌𝑢0 − 𝑌 ̅̅̅0 )2
(𝑌𝑢0 − 𝑌 ̅̅̅0 )2
∑(𝑌𝑢0 − 𝑌
1 10.4 0.133 0.0177
2 10.3 10.267 0.033 0.001 0.0465
3 10.1 -0.167 0.0278
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cvi
2 1 ̅̅̅0 2
Phương sai tái hiện:𝑆𝑡ℎ = ∑𝑚 0
𝑢=1(𝑌𝑢 − 𝑌 ) = 0.0233
𝑚−1
Trong đó m là số thí nghiệm ở tâm phương án (m = 3)
𝑆𝑡ℎ
Sbj: Độ lệch quân phương của hệ số thứ j, với: 𝑆𝑏𝑗 = =0.076 Tính các hệ số tjtheo
√𝑁
công thức (**),thu được kết quả sau:
t0 t1 t2 t12
131.26 9.49 5.56 0.98
Tra bảng tiêu chuẩn Student ta có tp(fth) = t0,05(2) = 4,3
Ta nhận thấy, các hệ số t0, t1, t2 đều lớn hơn t0,05(2) = 4,3 còn t12lại nhỏ hơn, do đó chỉ
có các hệ số b0, b1, b2 có nghĩa và phương trình hồi qui hoàn chỉnh như sau:
𝑌̂1 = 10.025 – 0.725 x1 - 0.425 x2
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
STT 𝑌̂1 Yi Yi − 𝑌̂1 (Yi − 𝑌̂1 )2
1
8.88 8.80 -0.075 0.0056250
2
10.33 10.40 0.075 0.0056250
3
9.73 9.80 0.075 0.0056250
4
11.18 11.10 -0.075 0.0056250
1
2
Phương sai dư: 𝑆𝑑ư = ∑𝑁 ̂ 2
𝑖=1(Yi − 𝑌1 ) = 0.01125
𝑁−𝐿
(N là số thí nghiệm, L là hệ số ý nghĩa)
Tiêu chuẩn Fisher:
2
𝑆𝑑ư
F= 2 = 0.49
𝑆𝑡ℎ
Tra bảng phân vị phân bố Fisher với P=0,05, f1 = N-L=2, f2 = N0 – 1 = 2, ta có: F1-p =
F0,95 (1,2) = 19.0
Vì F < F0,095(1,2) nên phương trình hồi qui tương thích với thực nghiệm.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cvii
Giữa các biến mã hóa (xi) và các giá trị biến thật (Zi) đã chọn để nghiên cứu ở các mức
nghiên cứu khác nhau được liên hệ với nhau qua các hệ thức sau:
Z j Z j0
Xi =
Z j
Trong đó:
- Zio: giá trị nghiên cứu tại tâm ( mức 0).
- Zj: khoảng biến thiên của biến nghiên cứu.
Z1 3 Z 20
Ta có các giá trị: x1= , x2 = 2
2 10
Vậy phương trình biến thực nhận được là:
Y= 11.9625 – 0.3625Z1 – 0.0425Z2
Tối ưu hóa quy hoạch thực nghiệm theo phương pháp đơn hình.
Để xác định tọa độ đỉnh của đơn hình ban đầu, Chúng tôi sử dụng bảng ( 1.5) với k cột
và k+1 hàng. Tính toán được tiến hành theo công thức
Xiu = Xio + Xixiu
Trong đó:
Xiu: giá trị mã hóa nhân tố thứ i trong thí nghiệm thứ u
Xiu: gía trị nhân tố thứ i trong thí nghiệm thứ u dạng tự nhiên.
Khi đó ma trận của đơn hình đều và kết quả đo OD được cho sau đây được cho sau
đây.
Bảng : 1.5 Thí nghiệm khởi đầu.
Số thí nghiệm X1 X2 Giá trị thực Y
X1 X2
1 -0.5 -0.289 2 1,7 9.4
2 0.5 -0.289 4 1,7 6.6
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cviii
3 0 0.578 3 2.6 10.2
Y là hàm mục tiêu giá trị OD thu được. Theo bảng trên ta có y2= min{ y1….y3} = 6.6
cách xa so với giá trị hấp phụ OD của mẫu tối ưu mà chúng tôi đã chọn ( OD = 10.5).
Ta bỏ đỉnh x2, thay nó theo ánh xạ phản chiếu được đỉnh x4 đối xứng với x2 qua diện
tạo bởi các điểm 1,3.
Tọa độ của thí nghiệm thứ 4 là:
X 14 1
X 24 2.6
Điểm mới thứ 4 cùng với điểm còn lại tạo nên một đơn hình 1,3,4 . Lập được bảng 1.6.
Bảng 1.6
Số thí nghiệm X1 X2 Y
1 2 1.7 9.4
3 3 2.6 10.2
4 1 2.6 9.87
Tương tự ta thu được bảng 1.7, 1.8.
Bảng 1.7
Số thí nghiệm X1 X2 Y
3 3 2.6 10.20
4 1 2.6 9.87
5 2 3.5 10.46
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cix
Bảng 1.8
Số thí nghiệm X1 X2 Y
3 3 2.6 10.20
5 2 3.5 10.46
6 4 3.5 10.13
Đến đây thuật toán dừng lại vì đã tới miền chứa giá trị cực đại, các giá trị thí nghiệm
xấp xỉ gần bằng nhau và bằng với mẫu tối ưu mà chúng tôi đã chọn ở trên.
1.1.2. Khảo sát quá trình chần kết hợp với ion Zn2+.
Bảng 2.1: kết qua đo độ hấp phụ Chlorophyll ở bước sóng 680nm
Mẫu
Điểm các thành
viên hội đồng
Số thí nghiệm trong phương án 2k Tại tâm
1 2 3 4 5 6 7
Giá trị OD 14 10.8 13.7 12 12.8 12.9 12.6
Bảng 2.2:kết quả đánh giá cảm quan màu trước khi đun sôi
Mẫu
Điểm các thành
viên hội đồng
Số thí nghiệm trong phương án 2k Tại tâm
1 2 3 4 5 6 7
Thành viên 1 3.5 4.5 3 4 5 4.5 4
Thành viên 2 4.5 4 4 4.5 4.5 4 5
Thành viên 3 4 4 4.5 5 4 4 4
Thành viên 4 4.5 4 3 4 4 4.5 5
Thành viên 5 4 5 3.5 4.5 5 5 4
Điểm trung bình 4.1 4.3 3.6 4.4 4.5 4.4 4.5
Bảng 2.3 điểm cảm quan sau đun sôi.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cx
Mẫu
Điểm các thành
viên hội đồng
Số thí nghiệm trong phương án 2k Tại tâm
1 2 3 4 5 6 7
Thành viên 1 2 4 1 5 4 5 4
Thành viên 2 2 4.5 1 5 3.5 4.5 5
Thành viên 3 2 4 1 5 3.5 4.5 4
Thành viên 4 2 4.5 1 5 4 4.5 3.5
Thành viên 5 1 4 1 4.5 3.5 3.5 4
Điểm trung bình 1.8 4.2 1 4.9 3.7 4.4 4.1
Hàm mục tiêu độ hấp phụ Chlorophyll.
Chọn phương trình hồi qui (*), các hệ số b1, b2, b3, b12 được tính theo số liệu thực
nghiệm hàm mục tiêu độ hấp phụ Chlorophyll (Y).
Tính hệ số b: theo phần đánh giá ở thí nghiệm trên ta có:
b0 b1 b2 b12
12.625 1.225 -0.225 0.375
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxi
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Kết quả các thí nghiệm ở tâm:
Bảng 1.4 kết quả thí nghiệm ở tâm
N0 𝑌𝑢0 ̅̅̅0
𝑌 ̅̅̅0
𝑌𝑢0 − 𝑌 ̅̅̅0 )2
(𝑌𝑢0 − 𝑌 ̅̅̅0 )2
∑(𝑌𝑢0 − 𝑌
1 12.8 0.0333 0.0011
2 12.9 12.767 0.1333 0.0178 0.0467
3 12.6 -0.1667 0.0278
2 1 ̅̅̅0 2
Phương sai tái hiện:𝑆𝑡ℎ = ∑𝑚 0
𝑢=1(𝑌𝑢 − 𝑌 ) = 0.0233
𝑚−1
Trong đó m là số thí nghiệm ở tâm phương án (m = 3)
𝑆𝑡ℎ
Sbj: Độ lệch quân phương của hệ số thứ j, với: 𝑆𝑏𝑗 = =0.076 Tính các hệ số tjtheo
√𝑁
công thức (**),thu được kết quả sau:
t0 t1 t2 t12
165.30 16.04 2.95 4.91
Tra bảng tiêu chuẩn Student ta có tp(fth) = t0,05(2) = 4,3
Ta nhận thấy, các hệ số t0, t1, t12 đều lớn hơn t0,05(2) = 4,3 còn t2lại nhỏ hơn, do đó chỉ
có các hệ số b0, b1, b12 có nghĩa và phương trình hồi qui hoàn chỉnh như sau:
𝑌̂1 = 12.625 +1.225 x1 + 0.375 x12
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxii
STT 𝑌̂1 Yi Yi − 𝑌̂1 (Yi − 𝑌̂1 )2
1
14.23 14.00 -0.225 0.0506250
2
11.03 10.80 -0.225 0.0506250
3
13.48 13.70 0.225 0.0506250
4
11.78 12.00 0.225 0.0506250
1
2
Phương sai dư: 𝑆𝑑ư = ∑𝑁 ̂ 2
𝑖=1(Yi − 𝑌1 ) = 0.10
𝑁−𝐿
(N là số thí nghiệm, L là hệ số ý nghĩa)
Tiêu chuẩn Fisher:
2
𝑆𝑑ư
F= 2 = 4.29
𝑆𝑡ℎ
Tra bảng phân vị phân bố Fisher với P=0,05, f1 = N-L=2, f2 = N0 – 1 = 2, ta có: F1-p =
F0,95 (1,2) = 19.0
Vì F < F0,095(1,2) nên phương trình hồi qui tương thích với thực nghiệm.
Z1 3 Z 20
Ta có các giá trị: x1= , x2 = 2
2 10
Vậy phương trình biến thực nhận được là:
Y= 14.74375 + 0.51875Z1 + 0.00075Z12
Tối ưu hóa QHTN bằng phương pháp đơn hình đều.
Để xác định tọa độ đỉnh của đơn hình ban đầu, Chúng tôi sử dụng bảng (2.4 ) với k cột
và k+1 hàng. Tính toán được tiến hành theo công thức
Xiu = Xio + Xixiu
Trong đó:
Xiu: giá trị mã hóa nhân tố thứ i trong thí nghiệm thứ u
Xiu: giá trị nhân tố thứ i trong thí nghiệm thứ u dạng tự nhiên.
Khi đó ma trận của đơn hình đều và kết quả điểm cảm quan màu được cho sau đây.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxiii
Bảng: 2.4 Thí nghiệm khởi đầu.
Số thí nghiệm X1 X2 Giá trị thực Y
X1 X2
1 -0.5 -0.289 2 118 9.16
2 0.5 -0.289 4 118 14.76
3 0 0.578 3 140 10.32
Y là hàm mục tiêu giá trị OD thu được. Theo bảng trên ta có y1= min{ y1….y3} = 9.16
và cách xa độ giá trị OD với mẫu tối ưu. Ta bỏ đỉnh x1, thay nó theo ánh xạ phản
chiếu được đỉnh x4 đối xứng với x1 qua diện tạo bởi các điểm 2,3..
Tọa độ của thí nghiệm thứ 4 là:
X 14 5
X 24 140
Điểm mới thứ 4 cùng với điểm còn lại tạo nên một đơn hình 1,3,4 . Lập được bảng 2.5
Bảng 2.5
Số thí nghiệm X1 X2 Y
2 4 118 14.76
3 3 140 10.32
4 5 140 9.43
Theo bảng trên ta có y1= max{ y1….y3} = 14.76 và cách xa độ hấp phụ OD với
mẫu tối ưu. Ta bỏ đỉnh x2, thay nó theo ánh xạ phản chiếu được đỉnh x5 đối xứng với x2
qua diện tạo bởi các điểm 3,4..Ta có bảng 2.6.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxiv
Bảng 2.6
Số thí nghiệm X1 X2 Y
3 3 140 10.32
4 5 140 9.43
5 4 162 10.09
Bảng 2.7
Số thí nghiệm X1 X2 Y
3 3 140 10.32
5 4 162 10.19
6 2 162 10.23
Đến đây thuật toán dừng lại vì đã tới miền chứa giá trị cực đại, các giá trị thí nghiệm
này xấp xỉ gần bằng giá trị tối ưu
1.1.3. Khảo sát quá trình chần kết hợp với Mg2+.
Bảng 3.1 : kết quả giá trị OD thu được
Mẫu
Giá trị OD
Số thí nghiệm trong phương án 2k Tại tâm
1 2 3 4 5 6 7
Giá trị trung bình 10.70 11.50 11.60 15.60 10.40 10.30 9.7
Bảng 3.2 : kết quả cảm quan màu trước đun sôi
Mẫu
Điểm các thành
viên hội đồng
Số thí nghiệm trong phương án 2k Tại tâm
1 2 3 4 5 6 7
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxv
Thành viên 1 3.5 3 3 5 4 4 4.5
Thành viên 2 4 3.5 3.5 4 5 4 4
Thành viên 3 4 3 3 4 4 5 4
Thành viên 4 3 3 4 4.5 4 4.5 5
Thành viên 5 4 3.5 3.5 4 4.5 4.5 4
Điểm trung bình 3.7 3.2 3.4 4.3 4.3 4.4 4.3
Bảng 3.3: kết quả cảm quan màu sau đun sôi
Mẫu
Điểm các thành
viên hội đồng
Số thí nghiệm trong phương án 2k Tại tâm
1 2 3 4 5 6 7
Thành viên 1 3 2.5 2 1.5 3 2.5 3
Thành viên 2 3.5 3 2 2 3.5 3 3
Thành viên 3 2.5 2 2.5 2 2.5 3 3
Thành viên 4 3.5 3 3 1.5 3 3 2.5
Thành viên 5 3 2.5 2 1 3 2.5 5
Điểm trung bình 3.1 2.6 2.3 1.6 3.0 2.8 2.9
Hàm mục tiêu giá trị OD
Chọn phương trình hồi qui (*), các hệ số b1, b2, b3, b12 được tính theo số liệu thực
nghiệm hàm mục tiêu giá trị OD(Y).
Tính hệ số b: theo phần đánh giá ở thí nghiệm trên, ta có:
b0 b1 b2 b12
12.35 -1.2 -1.25 0.8
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxvi
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Kết quả các thí nghiệm ở tâm:
N0 𝑌𝑢0 ̅̅̅0
𝑌 ̅̅̅0
𝑌𝑢0 − 𝑌 ̅̅̅0 )2
(𝑌𝑢0 − 𝑌 ̅̅̅0 )2
∑(𝑌𝑢0 − 𝑌
1 10.40 0.2667 0.071
2 10.30 10.133 0.1667 0.0277 0.28677
3 9.7 -0.4333 0.1877
2 1 ̅̅̅0 2
Phương sai tái hiện:𝑆𝑡ℎ = ∑𝑚 0
𝑢=1(𝑌𝑢 − 𝑌 ) = 0.143
𝑚−1
Trong đó m là số thí nghiệm ở tâm phương án (m = 3)
𝑆𝑡ℎ
Sbj: Độ lệch quân phương của hệ số thứ j, với: 𝑆𝑏𝑗 = =0.189 Tính các hệ số tj theo
√𝑁
công thức (**),thu được kết quả sau:
t0 t1 t2 t12
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxvii
65.24 6.34 6.03 4.23
Tra bảng tiêu chuẩn Student ta có tp(fth) = t0,05(2) = 4,3
Ta nhận thấy, các hệ số t0, t1, t2 đều lớn hơn t0,05(2) = 4,3 còn t12 lại nhỏ hơn, do đó chỉ
có các hệ số b0, b1,b2 có nghĩa và phương trình hồi qui hoàn chỉnh như sau:
𝑌̂1 = 12.35– 1.2 x1 – 6.03x2
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
STT 𝑌̂1 Yi Yi − 𝑌̂1 (Yi − 𝑌̂1 )2
1
9.90 10.70 0.800 0.6400000
2
12.30 11.50 -0.800 0.6400000
3
12.40 11.60 -0.800 0.6400000
4
14.80 15.60 0.800 0.6400000
1
2
Phương sai dư: 𝑆𝑑ư = ∑𝑁 ̂ 2
𝑖=1(Yi − 𝑌1 ) = 1.28
𝑁−𝐿
(N là số thí nghiệm, L là hệ số ý nghĩa)
Tiêu chuẩn Fisher:
2
𝑆𝑑ư
F= 2 = 8.98
𝑆𝑡ℎ
Tra bảng phân vị phân bố Fisher với P=0,05, f1 = N-L=1, f2 = N0 – 1 = 2, ta có: F1-p =
F0,95 (1,2) = 18,51.
Vì F < F0,095(1,2) nên phương trình hồi qui tương thích với thực nghiệm.
Z1 3 Z 1500
Ta có các giá trị: x1= , x2 = 2
2 500
Vậy phương trình biến thực nhận được là:
Y= 32.3 – 0.6Z1 – 0.01206 Z2
Tương tự như phương pháp tối ưu trên:
Để xác định tọa độ đỉnh của đơn hình ban đầu, Chúng tôi sử dụng bảng (2.4 ) với k cột
và k+1 hàng. Tính toán được tiến hành theo công thức
Xiu = Xio + Xixiu
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxviii
Trong đó:
Xiu: giá trị mã hóa nhân tố thứ i trong thí nghiệm thứ u
Xiu: giá trị nhân tố thứ i trong thí nghiệm thứ u dạng tự nhiên.
Khi đó ma trận của đơn hình đều và kết quả điểm cảm quan màu được cho sau đây.
Bảng : 3.4 Thí nghiệm khởi đầu.
Số thí nghiệm X1 X2 Giá trị thực Y
X1 X2
1 -0.5 -0.289 2 1200 10.40
2 0.5 -0.289 4 1200 9.6
3 0 0.578 3 1400 10.20
Y là hàm mục tiêu độ hấp phụ OD thu được. Theo bảng trên ta có y2= min{ y1….y3} =
9.6 và cách xa độ hấp phụ OD với mẫu tối ưu. Ta bỏ đỉnh x2, thay nó theo ánh xạ
phản chiếu được đỉnh x4 đối xứng với x2 qua diện tạo bởi các điểm 1,3..
Tọa độ của thí nghiệm thứ 4 là:
X 14 1
X 24 1400
Điểm mới thứ 4 cùng với điểm còn lại tạo nên một đơn hình 1,3,4 . Lập được bảng 3.5
Bảng 3.5
Số thí nghiệm X1 X2 Y
2 1200 10.40
3 3 1400 10.20
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxix
4 1 1400 10.08
Đến đây thuật toán dừng lại vì đã tới miền chứa giá trị cực đại, các giá trị thí nghiệm
này xấp xỉ gần bằng giá trị tối ưu.
1.2. Khảo sát quá trình chần trong môi trường kiềm kết hợp với ion
kim loại tạo phức.
1.2.1. Khảo sát quá trình chần trong môi trường kiềm kết hợp với ion
Cu2+.
Bảng 4.1: Kết quả giá trị OD
Mẫu
Giá trị OD
1 2 3 4 5 6 7 8 9 10 11
Giá trị trung bình 10.8 5.1 9.1 3.1 5.4 4.5 6 4.3 6.8 7.3 7.9
Bảng 4.2: Điểm cảm quan màu trước đun sôi
Điểm các thành Mẫu
viên hội đồng 1 2 3 4 5 6 7 8 9 10 11
Thành viên 1 2.5 4 3.5 4 3.5 3.5 4.5 2.5 4.5 5 5
Thành viên 2 2.5 4 4.5 3 3 4.5 4 2.5 4 4.5 4
Thành viên 3 2 5 3.5 3 2 3 5 3 4.5 4 5
Thành viên 4 2 4.5 5 3 3 3 4 3 5 5 4.5
Thành viên 5 2.5 5 4 4.5 3 4 3 4 5 4 4
Điểm trung bình 2.3 4.5 4.1 3 2.9 3.6 3.3 3.0 4.6 4.5 4.5
Bảng 4.3 : Điểm cảm quan màu sau đun sôi
Điểm các thành Mẫu
viên hội đồng 1 2 3 4 5 6 7 8 9 10 11
Thành viên 1 4 3 2 3 2 2 3 2.5 2.5 3 3
Thành viên 2 3.5 3.5 3.5 4 2 2 2 3 3 3 2
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxx
Thành viên 3 3 2.5 3.5 4 2 1.5 2 2 3 3 3
Thành viên 4 3.5 3 2.5 4 2.5 2 2.5 3 3.5 2.5 3
Thành viên 5 3 3.5 3 4 2 2 2 2.5 3 3 3
Điểm trung bình 3.5 3.1 2.7 3.8 2.1 1.9 2.3 2.6 3.0 2.9 2.8
Chọn phương trình hồi qui (*), các hệ số b1, b2, b3, b12 , b13, b23 được tính theo số liệu
thực nghiệm hàm mục tiêu độ hấp phụ OD.
Tính hệ số b:
b0 b1 b2 b3 b12 b13 b23
6.04 1.79 -0.14 0.98 0.41 1.14 0.06
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxi
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Kết quả các thí nghiệm ở tâm:
N0 𝑌𝑢0 ̅̅̅0
𝑌 ̅̅̅0
𝑌𝑢0 − 𝑌 ̅̅̅0 )2
(𝑌𝑢0 − 𝑌 ̅̅̅0 )2
∑(𝑌𝑢0 − 𝑌
1 6.8 -0.5333 0.2844
2 7.3 7.3333 -0.0333 0.0011 0.60667
3 7.9 0.5667 0.32111
2 1 ̅̅̅0 2
Phương sai tái hiện: 𝑆𝑡ℎ = ∑𝑚 0
𝑢=1(𝑌𝑢 − 𝑌 ) =0.30
𝑚−1
𝑆𝑡ℎ
Độ lệch quân phương của hệ số thứ j: 𝑆𝑏𝑗 = =0.195
√𝑁
Tính các hệ số tj thu được kết quả sau:
t0 t1 t2 t3 t12 t13 t23
31.005 9.18 0.706 5.07 2.12 5.84 0.32
Tra bảng tiêu chuẩn Stdent ta có tp(fth) = t0,05(2) = 4,3
So sánh tj với tp(f) . Trong đó: - tp(f) là chuẩn student tra bảng ứng với xác suất tin cậy
p và bậc tự do f, f = N0 – 1.
Như vậy, các hệ số t0, t1, t3, t13, đều lớn hơn t0,05(2) = 4,3 nên các hệ số này đều có
nghĩa.
Phương trình hồi qui có dạng như sau:
𝑌̂2 = 6.0375- 1.7875 x1+ 0.9875x3 +1.375x13
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
STT 𝑌̂2 Yi Yi − 𝑌̂2 (Yi − 𝑌̂2 )2
1
9.95 10.8 0.85 0.7225
2
4.1 5.1 1 1
3
9.95 9.1 -0.85 0.7225
4
4.1 3.1 -1 1
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxii
5
5.7 5.4 -0.3 0.09
6
4.4 4.5 0.1 0.01
7
5.7 6 0.3 0.09
8
4.4 4.3 -0.1 0.01
1 3.645
2
Phương sai dư:𝑆𝑑ư = ∑𝑁
𝑖=1(Yi − 𝑌̂2 )2 = = 0.91125
𝑁−𝐿 84
Tiêu chuẩn Fisher:
2 0.91125
𝑆𝑑ư
F= 2 = 3.0375
𝑆𝑡ℎ 0.30
Tra bảng phân vị phân bố Fisher với P=0,05, f1 = N-L=4, f2 = N0 – 1 = 2, ta có: F1-p =
F0,95 (3,2) = 19.3
Vì F >F0,95(3,2) nên phương trình hồi qui tương thích với thực nghiệm.
Z 1 0.075 Z 2 Z 20
Ta có các giá trị: x1= , x2 = 2 , x3= 3
0.025 1 10
Vậy phương trình biến thực nhận được là:
Y= 17.6375 – 181.15Z1 – 0.31375Z3 + 5.5 Z13
Tối ưu hóa hàm mục tiêu bằng phương pháp đơn hình.
Để xác định tọa độ đỉnh của đơn hình ban đầu, Chúng tôi sử dụng bảng (3.4 ) với k cột
và k+1 hàng. Tính toán được tiến hành theo công thức
Xiu = Xio + Xixiu
Trong đó:
Xiu: giá trị mã hóa nhân tố thứ i trong thí nghiệm thứ u
Xiu: giá tri nhân tố thứ i tronh thí nghiệm thứ u dạng tự nhiên.
Khi đó ma trận của đơn hình đều và kết quả độ hấp phụ Chlorophyll được cho sau đây.
Bảng 3.4 : thí nghiệm khởi đầu
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxiii
Số thí Gí trị mã hóa Gí trị thực Y
nghiệm
X1 X2 X3 X1 X2 X3
1 -0.5 -0.289 -0.204 0.0625 2.422 18 9.25
2 0.5 -0.289 -0.204 0.0875 2.422 18 5.2
3 0 0.578 -0.204 0.075 4.156 18 8.4
4 0 0 0.612 0.075 3 26 6.0
Y là hàm mục tiêu độ giá trị OD. Theo bảng trên ta có y2 = min{ y1….y4} = 5.2 xa với
độ hấp phụ của mẫu tối ưu nhất. Ta bỏ đỉnh x2, thay nó theo ánh xạ phản chiếu được
đỉnh x5 đối xứng với x2 qua diện tạo bởi các điểm 1, 3, 4.
Tọa độ của thí nghiệm thứ 5 là:
X 15 0.054%
X 25 3.96
X 35 23.33
Điểm mới thứ 5 cùng với điểm còn lại tạo nên một đơn hình 1, 3,4,5. Lập được bảng
2.9.
Bảng 2.9
Số thí nghiệm X1 X2 X3 Y
1 0.0625 2.422 18 9.25
3 0.075 4.156 18 8.4
4 0.075 3 26 6.0
5 0.054 3.96 23.33 7.13
Sau khi tiến hành thí nghiệm thứ 5, điểm kém nhất của đơn hình 1,3,4,5 là đỉnh X4 ta
loại đỉnh X4 thêm vào đỉnh X6 đối xứng với x4 qua diện 1, 3,5.
Tiến hành tương tự như bước trước ta nhận được tọa độ các điểm mới:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxiv
X 16 0.053
X 26 4
X 36 14
Nhận được giá trị Y6 và bảng 3.6.
Bảng 3.6
Số thí nghiệm X1 X2 X3 Y
1 0.0625 2.422 18 9.25
3 0.075 4.156 18 8.40
5 0.054 3.96 23.34 7.13
6 0.052 4 14 8.54
Nhận được giá trị Y7 và bảng 3.7.
Bảng 3.7
Số thí nghiệm X1 X2 X3 Y
1 0.0625 2.422 18 9.25
3 0.075 4.156 18 8.40
6 0.052 4 14 8.54
7 0.072 3.092 10 9.07
Bảng 3.8
Số thí nghiệm X1 X2 X3 Y
1 0.0625 2.422 18 9.25
6 0.052 4 14 8.54
7 0.072 3.092 10 9.07
8 0.05 2.18 10 9.14
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxv
Đến đây thuật toán dừng lại vì các nghiệm thức không có sự chênh lệch nhiều và nó
xoay quanh giá tri OD của mẫu tối ưu.
1.2.2. Khảo sát quá trình chần trong môi trường kiềm kết hợp với ion
Zn2+.
Bảng 4.1: Bảng điểm cảm quan về màu sau khi chần thu dịch
Điểm các thành viên Mẫu
hội đồng 1 2 3 4 5 6 7 8 9 10 11
Giá tri trung bình 7.2 7.3 10.8 10.3 6.4 9.5 9.8 5.2 9.4 8.9 8.5
Bảng 4.2: điểm cảm quan màu trước đun sôi
Điểm các thành Mẫu
viên hội đồng 1 2 3 4 5 6 7 8 9 10 11
Thành viên 1 2 4 4 3 2 4 3 4 4 4 4
Thành viên 2 2 4.5 4.5 2 1 4 4 4.5 4 4 4.5
Thành viên 3 3 3.5 5 3 1.5 4 4 3.5 5 5 5
Thành viên 4 2 4 4 2.5 2.5 3.5 3 4.5 4 4.5 4.5
Thành viên 5 2 4 4 2 2 4 4 4 4.5 5 4
Điểm trung 2.2 4.0 4.3 2.5 1.8 3.9 3.6 4.1 4.3 4.5 4.4
bình
Bảng 4.3: điểm cảm quan màu sau đun sôi
Điểm các thành Mẫu
viên hội đồng 1 2 3 4 5 6 7 8 9 10 11
Thành viên 1 2 3 3.5 2 1.5 3 3.5 3 3.5 3 3
Thành viên 2 3 4 3 3 1 3 3 2 3 4 3
Thành viên 3 2.5 3 3 3 1 2 2.5 2 3 3 3
Thành viên 4 2 3 2.5 2.5 2 3 3 3 3 3 3
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxvi
Thành viên 5 2 4 3 3 2 3 3 2.5 3 3 3.5
Điểm trung 2.3 3.4 3.0 2.7 1.5 2.8 3.0 2.5 3.1 3.2 3.1
bình
Chọn phương trình hồi qui (*), các hệ số b1, b2, b3, b12 , b13, b23 được tính theo số liệu
thực nghiệm hàm mục tiêu độ hấp phụ OD (Y).
Tính hệ số b:
b0 b1 b2 b3 b12 b13 b23
8.1325 0.2375 -1.0375 0.5875 -0.7125 -0.1375 0.8875
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Kết quả các thí nghiệm ở tâm:
N0 𝑌𝑢0 ̅̅̅0
𝑌 ̅̅̅0
𝑌𝑢0 − 𝑌 ̅̅̅0 )2
(𝑌𝑢0 − 𝑌 ̅̅̅0 )2
∑(𝑌𝑢0 − 𝑌
1 9.4 0.4667 0.2178
8.9333 0.40667
2 8.9 -0.0333 0.0011
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxvii
3 9.5 -0.4333 0.1878
2 1 ̅̅̅0 2
Phương sai tái hiện: 𝑆𝑡ℎ = ∑𝑚 0
𝑢=1(𝑌𝑢 − 𝑌 ) =0.2033
𝑚−1
𝑆𝑡ℎ
Độ lệch quân phương của hệ số thứ j: 𝑆𝑏𝑗 = =0.1594
√𝑁
Tính các hệ số tj thu được kết quả sau:
t0 t1 t2 t3 t12 t13 t23
52.14 1.49 6.51 3.68 4.47 0.86 5.57
Tra bảng tiêu chuẩn Student ta có tp(fth) = t0,05(2) = 4,3
So sánh tj với tp(f) . Trong đó: - tp(f) là chuẩn student tra bảng ứng với xác suất tin cậy
p và bậc tự do f, f = N0 – 1.
Như vậy, các hệ số t0, t2, t3,t12 , t23, đều lớn hơn t0,05(2) = 4,3 nên các hệ số này đều có
nghĩa.
Phương trình hồi qui có dạng như sau:
𝑌̂2 = 8.3125 – 1.0375x2 + 0.5875x3- 0.7125x12 + 5.57x23
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
STT 𝑌̂2 Yi Yi − 𝑌̂2 (Yi − 𝑌̂2 )2
1
8.0375 7.2 -0.8375 0.701406
2
8.3375 7.3 -1.0375 1.076406
3
9.7625 10.8 1.0375 1.076406
4
9.4625 10.3 0.8375 0.701406
5
5.0875 6.4 1.3125 1.722656
6
8.9375 9.5 0.5625 0.316406
7
10.3625 9.8 -0.5625 0.316406
8
6.5125 5.2 -1.3125 1.722656
1 7.63375
2
Phương sai dư:𝑆𝑑ư = ∑𝑁
𝑖=1(Yi − 𝑌̂2 )2 = = 2.54
𝑁−𝐿 85
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxviii
Tiêu chuẩn Fisher:
2 2.54
𝑆𝑑ư
F= 2 = 11.04
𝑆𝑡ℎ 0.2033
Tra bảng phân vị phân bố Fisher với P=0,05, f1 = N-L=3, f2 = N0 – 1 = 2, ta có: F1-p =
F0,95 (3,2) = 19.2.
Vì F < F0,95(3,2) nên phương trình hồi qui tương thích với thực nghiệm.
Z 1 0.075 Z 2 Z 125
Ta có các giá trị: x1= , x2 = 2 , x3= 3
0.025 1 25
Vậy phương trình biến thực nhận được là:
Y= 58.875 – 28.67375Z2 – 0.4456Z3 – 28.5Z12 + 0.2228Z13
Tối ưu hóa hàm mục tiêu bằng phương pháp đơn hình.
Để xác định tọa độ đỉnh của đơn hình ban đầu, Chúng tôi sử dụng bảng (4.4 ) với k cột
và k+1 hàng. Tính toán được tiến hành theo công thức
Xiu = Xio + Xixiu
Trong đó:
Xiu: giá trị mã hóa nhân tố thứ i trong thí nghiệm thứ u
Xiu: giá tri nhân tố thứ i trong thí nghiệm thứ u dạng tự nhiên.
Khi đó ma trận của đơn hình đều và kết quả giá trị OD được cho sau đây.
Bảng 4.4 thí nghiệm khởi đầu
Số thí Gía trị mã hóa Gía trị thực Y
nghiệm
X1 X2 X3 X1 X2 X3
1 -0.5 -0.289 -0.204 0.0625 2.422 120 9.43
2 0.5 -0.289 -0.204 0.0875 2.422 120 8.92
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxix
3 0 0.578 -0.204 0.075 4.156 120 12.64
4 0 0 0.612 0.075 3 140 10.21
Y là hàm mục tiêu giá trị OD thu được. Theo bảng trên ta có y3= max{ y1….y4} =
12.64 độ hấp phụ OD cao và có sự chênh lệch cao hơn so với mẫu tối ưu. Ta bỏ đỉnh
x3, thay nó theo ánh xạ phản chiếu được đỉnh x5 đối xứng với x3 qua diện tạo bởi các
điểm 1, 2, 4.
Tọa độ của thí nghiệm thứ 5 là:
X 15 0.075
X 25 1.07
X 35 133.33
Điểm mới thứ 5 cùng với điểm còn lại tạo nên một đơn hình 1,2,4,5. Lập được bảng
3.3.
Bảng 4.3
Số thí nghiệm X1 X2 X3 Y
1 0.0625 2.422 120 9.43
2 0.0875 2.422 120 8.92
4 0.075 3 140 10.21
5 0.075 1.07 133.33 9.56
Sau khi tiến hành thí nghiệm thứ 5, điểm cách xa của mẫu tối ưu của đơn hình 1,2,4,5
là đỉnh X2 ta loại đỉnh X2 thêm vào đỉnh X6 đối xứng với x2 qua diện 1, 4, 5.
Tiến hành tương tự như bước trước ta nhận được tạo độ các điểm mới:
X 16 0.054
X 26 1.906
X 36 142.22
Nhận được giá trị Y6 và bảng 4.4.
Bảng 4.4
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxx
Số thí nghiệm X1 X2 X3 Y
1 0.0625 2.422 120 9.43
4 0.075 3 140 10.21
5 0.075 1.07 133.33 9.56
6 0.054 1.906 142.22 10.09
Cứ tiến hành như vậy lần lượt ta có bảng đơn hình 4.5, 4.6, 4.7.
Bảng 4.5
Số thí nghiệm X1 X2 X3 Y
4 0.075 3 140 10.21
5 0.075 1.07 133.33 9.56
6 0.054 1.906 142.22 10.09
7 0.0735 1.562 157 10.12
Bảng 4.6
Số thí nghiệm X1 X2 X3 Y
4 0.075 3 140 10.21
6 0.054 1.906 142.22 10.09
7 0.0735 1.562 157 10.12
8 0.06 3.234 160 10.36
Đến đây thuật toán dừng lại vì đã tới miền chứa giá trị cực đại, các thí nghiệm đã sấp xỉ
gần bằng nhau và bằng với mẫu tối ưu.
1.2.3. Khảo sát quá trình chần trong môi trường kiềm kết hợp với ion
Mg2+.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxxi
Bảng 5.1: Bảng kết quả đánh giá cảm quan màu (trước khi đun sôi)
Điểm các thành Mẫu
viên hội đồng 1 2 3 4 5 6 7 8 9 10 11
Điểm trung bình
8.9 7.6 9.7 10.2 4.5 8.3 9.3 6.4 10.2 9.7 9.6
Bảng 5.2: điểm cảm quan trước gia nhiệt
Điểm các thành Mẫu
viên hội đồng 1 2 3 4 5 6 7 8 9 10 11
Thành viên 1 1 3.5 3 2.5 2 3 3 1.5 3 2 3
Thành viên 2 1 3.5 2.5 2 1.5 3 3 1.5 2 3 2
Thành viên 3 1.5 4 4 2 1 3 5 1.5 1.5 2.5 1.5
Thành viên 4 1.5 4.5 4 2 1 3 4 3 2.5 1.5 2.5
Thành viên 5 1.5 4 3.5 2.5 2.5 3.5 3.5 2 2 2 2.5
Điểm trung bình
1.3 3.9 3.4 2.2 1.6 3.1 3.7 1.9 2.2 2.2 2.3
Chọn phương trình hồi qui (*), các hệ số b1, b2, b3, b12 , b13, b23 được tính theo số liệu
thực nghiệm hàm mục tiêu giá trị OD (Y).
Tính hệ số b:
b0 b1 b2 b3 b12 b13 b23
8.1125 -0.0125 -0.6125 0.9875 -0.7875 0.2125 1.0625
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxxii
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Kết quả các thí nghiệm ở tâm:
N0 𝑌𝑢0 ̅̅̅0
𝑌 ̅̅̅0
𝑌𝑢0 − 𝑌 ̅̅̅0 )2
(𝑌𝑢0 − 𝑌 ̅̅̅0 )2
∑(𝑌𝑢0 − 𝑌
1 10.2 0.3667 0.13444
2 9.7 9.8333 -0.1333 0.01778 0.20667
3 9.6 -0.2333 0.0544
2 1 ̅̅̅0 2
Phương sai tái hiện: 𝑆𝑡ℎ = ∑𝑚 0
𝑢=1(𝑌𝑢 − 𝑌 ) =0.0.1033
𝑚−1
𝑆𝑡ℎ
Độ lệch quân phương của hệ số thứ j: 𝑆𝑏𝑗 = =0.113
√𝑁
Tính các hệ số tjthu được kết quả sau:
t0 t1 t2 t3 t12 t13 t23
71.3805 0.1099 5.39 8.69 6.93 1.87 9.35
Tra bảng tiêu chuẩn Student ta có tp(fth) = t0,05(2) = 4,3
So sánh tj với tp(f) . Trong đó: - tp(f) là chuẩn student tra bảng ứng với xác suất tin cậy
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxxiii
p và bậc tự do f, f = N0 – 1.
Như vậy, các hệ số t0, t2, t3,t12 ,t23, đều lớn hơn t0,05(2) = 4,3 nên các hệ số này đều có
nghĩa.
Phương trình hồi qui có dạng như sau:
𝑌̂2 = 8.1125 – 0.6125x2 + 0.9875x3 – 0.7875x12 + 1.0625x13
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
STT 𝑌̂2 Yi Yi − 𝑌̂2 (Yi − 𝑌̂2 )2
1
8.7625 8.9 0.1375 0.018906
2
7.8625 7.6 -0.2625 0.068906
3
9.4375 9.7 0.2625 0.068906
4
10.3375 10.2 -0.1375 0.018906
5
4.6625 4.5 -0.1625 0.026406
6
8.0125 8.3 0.2875 0.082656
7
9.5875 9.3 -0.2875 0.082656
8
6.2375 6.4 0.1625 0.026406
2
Phương sai dư:𝑆𝑑ư =
1
∑𝑁 ̂ 2 0.39375 0.13125
𝑖=1(Yi − 𝑌2 ) =
𝑁−𝐿 85
Tiêu chuẩn Fisher:
2 0.13125
𝑆𝑑ư
F= 2 = 1.27
𝑆𝑡ℎ 0.1033
Tra bảng phân vị phân bố Fisher với P=0,05, f1 = N-L=3, f2 = N0 – 1 = 2, ta có: F1-p =
F0,95 (3,2) = 19.2
Vì F < F0,95(3,2) nên phương trình hồi qui tương thích với thực nghiệm.
Z 1 0.075 Z 2 Z 1500
Ta có các giá trị: x1= , x2 = 2 , x3= 3
0.025 1 500
Vậy phương trình biến thực nhận được là:
Y= 21.6375 +1.75 Z2 +0.092375 Z3 + 0.085 Z13
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxxiv
Tương tự như phương pháp tối ưu trên. Ta có
Bảng 5.4 thí nghiệm khởi đầu
Số thí Giá trị mã hóa giá trị thực Y
nghiệm
X1 X2 X3 X1 X2 X3
1 -0.5 -0.289 -0.204 0.065 2.422 1200 10.7
2 0.5 -0.289 -0.204 0.0875 2.422 1200 9.9
3 0 0.578 -0.204 0.075 4.156 1200 7.8
4 0 0 0.612 0.075 3 1400 9.3
Y là hàm mục tiêu giá trị OD thu được. Theo bảng trên ta có y3= { y1….y4} = 7.83 . Ta
bỏ đỉnh x3, thay nó theo ánh xạ phản chiếu được đỉnh x5 đối xứng với x3 qua diện tạo
bởi các điểm 1,2,4.
Tọa độ của thí nghiệm thứ 5 là:
X 15 0.076
X 25 1.07
X 35 1333
Điểm mới thứ 5 cùng với điểm còn lại tạo nên một đơn hình 1,2,3,5 . Lập được bảng
5.5.
Bảng 5.5
Số thí nghiệm X1 X2 X3 Y
1 0.065 2.422 1200 10.7
2 0.0875 2.422 1200 9.9
4 0.075 3 1400 9.3
5 0.075 1.07 1333 9.5
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxxv
Y là hàm mục tiêu giá trị OD thu được. Theo bảng trên ta có y4= { y1….y4} =
9.3 . Ta bỏ đỉnh x4, thay nó theo ánh xạ phản chiếu được đỉnh x6 đối xứng với x4 qua
diện tạo bởi các điểm 1,2,5.
Bảng 5.6
Số thí nghiệm X1 X2 X3 Y
1 0.065 2.422 1200 10.7
2 0.0875 2.422 1200 9.9
5 0.075 1.07 1333 9.58
6 0.075 0.01 1088 9.42
Đến đây thuật toán dừng lại vì đã tới miền chứa giá trị cực đại, các thí nghiệm đã sấp xỉ
gần bằng nhau và nó gẩn bằng mẫu tối ưu.
1.3. Khảo sát quá trình chần trong môi trường kiểm kết hợp với
ngâm trong dung dịch ion kim loại tạo phức.
1.3.1. Khảo sát ngâm trong dung dịch Cu2+.
Bảng 6.1 : kết quả giá trị OD thu được
Điểm các Mẫu
thành viên hội 1 2 3 4 5 6 7 8 9 10 11
Giáđồng
trị trung 10.8 11.1 15.7 15.1 12.5 16.6 17.3 11.4 12.2 12.8 11.9
bình
Bảng 6.2: điểm đánh giá cảm quan màu trước đun sôi
Điểm các thành Mẫu
viên hội đồng 1 2 3 4 5 6 7 8 9 10 11
Thành viên 1 3 4 4.5 3 4 3.5 4 5 4 4 3.5
Thành viên 2 3 5 5 4.5 3 3 3 4 5 5 4
Thành viên 3 2 4.5 3.5 4 3 3 3 5 4.5 2.5 3.5
Thành viên 4 2 4.5 5 3 2 2.5 4 4.5 3.5 4 4
Thành viên 5 2.5 3.5 5 4 3.5 3 4 4.5 3 4 4
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxxvi
Điểm trung bình 2.5 4.3 4.6 3.7 3.1 3 3.6 4.6 4 3.9 3.8
Bảng 6.3: điểm đánh giá cảm quan màu sau đun sôi
Điểm các thành Mẫu
viên hội đồng 1 2 3 4 5 6 7 8 9 10 11
Thành viên 1 4 2 1 3 2 0 1 3 1 2.5 2.5
Thành viên 2 3 2 2 2 3 0 1 3 2 3 3
Thành viên 3 3 3 3 2 2 1 2 2 1 3.5 2.5
Thành viên 4 3.5 2 1 1 3 1 1 2.5 1.5 3 3
Thành viên 5 4 1.5 2 2.5 3 0 2.5 2 2.5 3 3
Điểm trung bình 3.5 2.1 1.8 2.1 2.6 0.4 1.5 2.5 1.6 3 2.8
Chọn phương trình hồi qui (*), các hệ số b1, b2, b3, b12 , b13, b23 được tính theo số liệu
thực nghiệm hàm mục tiêu giá trị OD thu được (Y).
Tính hệ số b:
b0 b1 b2 b3 b12 b13 b23
13.8125 0.2625 -1.3625 -0.6375 -1.0625 -0.1875 1.1375
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxxvii
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Kết quả các thí nghiệm ở tâm:
N0 𝑌𝑢0 ̅̅̅0
𝑌 ̅̅̅0
𝑌𝑢0 − 𝑌 ̅̅̅0 )2
(𝑌𝑢0 − 𝑌 ̅̅̅0 )2
∑(𝑌𝑢0 − 𝑌
1 12.2 -0.1 0.01
2 12.8 12.3 0.5 0.25 0.42
3 11.9 0.4 0.16
2 1 ̅̅̅0 2
Phương sai tái hiện: 𝑆𝑡ℎ = ∑𝑚 0
𝑢=1(𝑌𝑢 − 𝑌 ) =0.21
𝑚−1
𝑆𝑡ℎ
Độ lệch quân phương của hệ số thứ j: 𝑆𝑏𝑗 = =0.0162
√𝑁
Tính các hệ số tjthu được kết quả sau:
t0 t1 t2 t3 t12 t13 t23
85.25 1.62 8.41 3.93 6.56 1.16 7.02
Tra bảng tiêu chuẩn Student ta có tp(fth) = t0,05(2) = 4,3
So sánh tj với tp(f) . Trong đó: - tp(f) là chuẩn student tra bảng ứng với xác suất tin cậy
p và bậc tự do f, f = N0 – 1.
Như vậy, các hệ số t0, t2 ,t12, t23, đều lớn hơn t0,05(2) = 4,3 nên các hệ số này đều có
nghĩa.
Phương trình hồi qui có dạng như sau:
𝑌̂2 = 13.8125- 1.3625x2 – 1.0625x12 + 1.1375 x23
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
STT 𝑌̂2 Yi Yi − 𝑌̂2 (Yi − 𝑌̂2 )2
1
12.525 10.8 -1.725 2.975625
2
12.975 11.1 -1.875 3.515625
3
15.1 15.7 0.6 0.36
4
14.65 15.1 0.45 0.2025
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxxviii
5
10.25 12.5 2.25 5.0625
6
15.25 16.6 1.35 1.8225
7
17.375 17.3 -0.075 0.005625
8
12.375 11.4 -0.975 0.950625
1 14.90
2
Phương sai dư:𝑆𝑑ư = ∑𝑁
𝑖=1(Yi − 𝑌̂2 )2 = = 3.725
𝑁−𝐿 84
Tiêu chuẩn Fisher:
2 3.725
𝑆𝑑ư
F= 2 = 17.74
𝑆𝑡ℎ 0.21
Tra bảng phân vị phân bố Fisher với P=0,05, f1 = N-L=4, f2 = N0 – 1 = 2, ta có: F1-p =
F0,95 (3,2) = 19.3
Vì F < F0,95(3,2) nên phương trình hồi qui tương thích với thực nghiệm
Z 1 0.075 Z 75 Z 20
Ta có các giá trị: x1= , x2 = 2 , x3= 3
0.025 45 10
Vậy phương trình biến thực nhận được là:
Y= 14.5625 -0.01Z2 – 0.95Z12 + 2.5x 10 3 Z23
Tương tự như tối ưu như phương pháp trên. Ta có
Bảng 6.4 thí nghiệm khởi đầu
Số thí Gía trị mã hóa Gía trị thực Y
nghiệm
x1 x2 x3 x1 x2 x3
1 -0.5 -0.289 -0.204 0.065 62 18 11.2
2 0.5 -0.289 -0.204 0.0875 62 18 12.8
3 0 0.578 -0.204 0.075 62 18 12.4
4 0 0 0.612 0.075 101 26 10.2
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxxxix
Y là hàm mục tiêu giá trị OD thu được. Theo bảng trên ta có y2= { y1….y4} = 12.8 có
khoảng cách xa độ hấp phụ OD so với mẫu chuẩn nhất . Ta bỏ đỉnh x2, thay nó theo
ánh xạ phản chiếu được đỉnh x5 đối xứng với x2 qua diện tạo bởi các điểm 1,3,4.
Tọa độ của thí nghiệm thứ 5 là:
X 15 0.056
X 25 88
X 35 23.33
Bảng 6.5
Số thí nghiệm X1 X2 X3 Y
1 0.065 62 18 11.2
3 0.075 62 18 12.4
4 0.075 101 26 10.2
5 0.056 88 23.33 10.9
Y là hàm mục tiêu giá trị OD thu được. Theo bảng trên ta có y3= { y1….y4} = 12.4 có
khoảng cách xa độ hấp phụ OD so với mẫu chuẩn nhất . Ta bỏ đỉnh x3, thay nó theo
ánh xạ phản chiếu được đỉnh x6 đối xứng với x3 qua diện tạo bởi các điểm 1,4,5.
Tương tự ta có các bảng đơn hình sau:
Bảng 6.6
Số thí nghiệm X1 X2 X3 Y
1 0.065 62 18 11.2
4 0.075 101 26 10.2
5 0.056 88 23.33 10.7
6 0.056 105 27 9.95
Bảng 6.7
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxl
Số thí nghiệm X1 X2 X3 Y
4 0.075 101 26 10.2
5 0.056 88 23.33 10.7
6 0.056 105 27 9.95
7 0.06 134 32.88 9.86
1.3.2. Khảo sát ngâm trong dung dịch Zn2+
Bảng 7. 1: Bảng kết quả đánh giá cảm quan màu (trước khi đun sôi)
Điểm các Mẫu
thành viên 1 2 3 4 5 6 7 8 9 10 11
Điểm trung
hội đồng 9.8 13.5 13.3 10.5 9.3 11.6 11.4 8.9 11.2 10.7 11.6
bình
Bảng 7.2: kết quả cảm quan màu trước đun sôi
Điểm các thành Mẫu
viên hội đồng 1 2 3 4 5 6 7 8 9 10 11
Thành viên 1 5 4 2.5 4 4.5 4 3 4.5 3 3 3
Thành viên 2 3.5 3.5 2.5 4 3.5 4 3 4 3 3 3
Thành viên 3 4 3.5 1 4 2.5 4.5 2.5 3 3 3.5 4
Thành viên 4 2.5 4 2 3 3 4.5 4 3.5 3.5 3.5 2
Thành viên 5 4 4 2.5 4 3 4 3 3 3 2 3
Điểm trung 3.8 3.8 2.1 3.8 3.3 4.2 3.1 3.6 3.1 3.0 3.0
bình
Chọn phương trình hồi qui (*), các hệ số b1, b2, b3, b12 , b13, b23 được tính theo số liệu
thực nghiệm hàm mục tiêu giá trị OD (Y).
Tính hệ số b:
b0 b1 b2 b3 b12 b13 b23
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxli
11.075 -0.125 -1.375 0.7 -0.025 -0.1 -0.25
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Kết quả các thí nghiệm ở tâm:
N0 𝑌𝑢0 ̅̅̅0
𝑌 ̅̅̅0
𝑌𝑢0 − 𝑌 ̅̅̅0 )2
(𝑌𝑢0 − 𝑌 ̅̅̅0 )2
∑(𝑌𝑢0 − 𝑌
1 11.2 11.167 0.0333 0.001 0.407
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxlii
2 10.7 -0.4667 0.218
3 11.6 0.4333 0.188
2 1 ̅̅̅0 2
Phương sai tái hiện: 𝑆𝑡ℎ = ∑𝑚 0
𝑢=1(𝑌𝑢 − 𝑌 ) =0.203
𝑚−1
𝑆𝑡ℎ
Độ lệch quân phương của hệ số thứ j: 𝑆𝑏𝑗 = =0.16
√𝑁
Tính các hệ số tj thu được kết quả sau:
t0 t1 t2 t3 t12 t13 t23
69.47 0.78 8.62 4.39 0.16 0.63 1.57
Tra bảng tiêu chuẩn Student ta có tp(fth) = t0,05(2) = 4,3
So sánh tj với tp(f) . Trong đó: - tp(f) là chuẩn student tra bảng ứng với xác suất tin cậy
p và bậc tự do f, f = N0 – 1.
Như vậy, các hệ số t0, t1, t2, t3, đều lớn hơn t0,05(2) = 4,3 nên các hệ số này đều có
nghĩa.
Phương trình hồi qui có dạng như sau:
𝑌̂2 = 11.075 – 1.375x2 + 0,7x3
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
STT 𝑌̂2 Yi Yi − 𝑌̂2 (Yi − 𝑌̂2 )2
1
10.4 9.8 -0.6 0.36
2
13.15 13.5 0.35 0.1225
3
13.15 13.3 0.15 0.0225
4
10.4 10.5 0.1 0.01
5
9 9.3 0.3 0.09
6
11.75 11.6 -0.15 0.0225
7
11.75 11.4 -0.35 0.1225
8
9 9.2 0.2 0.04
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxliii
2
Phương sai dư:𝑆𝑑ư =
1
∑𝑁 ̂ 2 0.79 = 0.158
𝑖=1(Yi − 𝑌2 ) =
𝑁−𝐿 83
Tiêu chuẩn Fisher:
2 0.158
𝑆𝑑ư
F= 2 = 0.77
𝑆𝑡ℎ 0.2033
Tra bảng phân vị phân bố Fisher với P=0,05, f1 = N-L=5, f2 = N0 – 1 = 2, ta có: F1-p =
F0,95 (3,2) = 19.3
Vì F < F0,95(3,2) nên phương trình hồi qui tương thích với thực nghiệm
Z 1 0.075 Z 75 Z 125
Ta có các giá trị: x1= , x2 = 2 , x3= 3
0.025 45 25
Vậy phương trình biến thực nhận được là:
Y= 9.865 -0.03Z2 + 0.028Z3
Tương tự như phương pháp tối ưu trên. Ta có
Bảng 7.4: thí nghiệm khởi đầu.
Số thí Giá trị mã hóa Giá trị thực Y
nghiệm
X1 X2 X3 X1 X2 X3
1 -0.5 -0.289 -0.204 0.0625 62 120 11.5
2 0.5 -0.289 -0.204 0.0875 62 120 10.9
3 0 0.578 -0.204 0.075 62 120 11.3
4 0 0 0.612 0.075 101 140 10.6
Tương tự như các phương pháp đơn hình trên:
Bảng 7.5
Số thí nghiệm X1 X2 X3 Y
2 0.0875 62 120 10.9
4 0.075 101 140 11.3
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxliv
3 0.075 62 120 10.6
5 0.01 88 133.33 9.8
Bảng 7.6
Số thí nghiệm X1 X2 X3 Y
2 0.0875 62 120 10.9
3 0.075 62 120 10.6
5 0.1 88 133.33 9.8
6 0.1 40 108.88 10.1
1.3.3. khảo sát ngâm trong Mg2+.
Bảng 8.1: kết quả giá trị OD
Điểm các Mẫu
thành viên 1 2 3 4 5 6 7 8 9 10 11
Giá
hộitrịđồng
trung 13.6 19.1 18.4 23.2 17.2 16.7 15.2 17.5 16.6 15.4 16
bình
Bảng 8.2: điểm đánh giá cảm quan màu trước đun đun sôi
Điểm các thành Mẫu
viên hội đồng 1 2 3 4 5 6 7 8 9 10 11
Thành viên 1 5 4 2.5 4 4 3.5 3.5 3.5 4.5 4.5 4.5
Thành viên 2 4.5 3.5 2.5 4.5 4.5 3 3.5 3 4.5 5 4
Thành viên 3 5 4 3 3.5 4.5 3.5 4 3 5 4 5
Thành viên 4 4 3 2 4 4.5 3 2.5 3.5 3.5 5 4.5
Thành viên 5 4.5 4 2.5 3.5 4.5 3.5 3.5 2.5 4 4 4.5
Điểm trung bình 4.6 3.7 2.5 3.9 4.4 3.3 3.4 3.1 4.3 4.5 4.5
fdffdfbbinhbình
Chọn phương trình hồi qui (*), các hệ số b1, b2, b3, b12 , b13, b23 được tính theo số liệu
thực nghiệm hàm mục tiêu giá trị OD (Y).
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxlv
Tính hệ số b:
b0 b1 b2 b3 b12 b13 b23
17.6125 -1.5125 0.2625 0.9625 -0.9625 -1.0625 -0.4375
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Kết quả các thí nghiệm ở tâm:
N0 𝑌𝑢0 ̅̅̅0
𝑌 ̅̅̅0
𝑌𝑢0 − 𝑌 ̅̅̅0 )2
(𝑌𝑢0 − 𝑌 ̅̅̅0 )2
∑(𝑌𝑢0 − 𝑌
1 16.6 0.6 0.36
2 15.4 16 -0.6 0.36 0.72
3 16 0 0
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxlvi
2 1 ̅̅̅0 2
Phương sai tái hiện: 𝑆𝑡ℎ = ∑𝑚 0
𝑢=1(𝑌𝑢 − 𝑌 ) =0.30
𝑚−1
𝑆𝑡ℎ
Độ lệch quân phương của hệ số thứ j: 𝑆𝑏𝑗 = =0.21
√𝑁
Tính các hệ số tjthu được kết quả sau:
t0 t1 t2 t3 t12 t13 t23
83.02 7.13 1.24 4.54 4.54 5.01 2.06
Tra bảng tiêu chuẩn Student ta có tp(fth) = t0,05(2) = 4,3
So sánh tj với tp(f) . Trong đó: - tp(f) là chuẩn student tra bảng ứng với xác suất tin cậy
p và bậc tự do f, f = N0 – 1.
Như vậy, các hệ số t0, t1, t3,t12 , t13 đều lớn hơn t0,05(2) = 4,3 nên các hệ số này đều có
nghĩa.
Phương trình hồi qui có dạng như sau:
𝑌̂2 = 17.6125 – 1.5125 x1 + 0.9625 x3 - 0.9625x12 – 1.0625x13
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
STT 𝑌̂2 Yi Yi − 𝑌̂2 (Yi − 𝑌̂2 )2
1
15.0375 13.6 -1.4375 2.066406
2
20.1875 19.1 -1.0875 1.182656
3
16.9625 18.4 1.4375 2.066406
4
22.1125 23.2 1.0875 1.182656
5
15.2375 17.2 1.9625 3.851406
6
16.1375 16.7 0.5625 0.316406
7
17.1625 15.2 -1.9625 3.851406
8
18.0625 17.5 -0.5625 0.316406
2
Phương sai dư:𝑆𝑑ư =
1
∑𝑁 ̂ 2 14.83 = 4.94
𝑖=1(Yi − 𝑌2 ) =
𝑁−𝐿 85
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxlvii
Tiêu chuẩn Fisher:
2 4.94
𝑆𝑑ư
F= 2 = 13.72
𝑆𝑡ℎ 0.36
Tra bảng phân vị phân bố Fisher với P=0,05, f1 = N-L=3, f2 = N0 – 1 = 2, ta có: F1-p =
F0,95 (3,2) = 19.2
Vì F < F0,95(3,2) nên phương trình hồi qui tương thích với thực nghiệm.
Z 1 0.075 Z 75 Z 1500
Ta có các giá trị: x1= , x2 = 2 , x3= 3
0.025 45 500
Vậy phương trình biến thực nhận được là:
Y= 4.50125 + 136.41Z1 + 0.955Z3 – 0.85Z12 – 0.1655Z13
Tương tự như phương pháp tối ưu trên. Ta có
Bảng 8.4 thí nghiệm khởi đầu
Số thí Giá trị mã hóa Giá trị thực Y
nghiệm
X1 X2 X3 X1 X2 X3
1 -0.5 -0.289 -0.204 0.0625 62 1200 16.4
2 0.5 -0.289 -0.204 0.0875 62 1200 13.2
3 0 0.578 -0.204 0.075 62 1200 14.2
4 0 0 0.612 0075 101 1400 14.6
Cứ tiến hành như vậy lần lượt ta có bảng đơn hình 8.5, 8.6, 8.7.
Bảng 8.5
Số thí nghiệm X1 X2 X3 Y
2 0.0875 62 1200 13.2
3 0.075 62 1200 14.2
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxlviii
4 0.075 101 1400 14.6
5 0.1 88 1333 12.9
Bảng 8.6
Số thí nghiệm X1 X2 X3 Y
2 0.0875 62 1200 13.2
3 0.075 62 1200 14.2
5 0.1 88 1333 12.9
6 0.1 40.33 1088 12.3
Bảng 8.7
Số thí nghiệm X1 X2 X3 Y
2 0.0875 62 1200 13.2
5 0.1 88 1333 12.9
6 0.1 40.33 1088 12.3
7 0.117 65 1214 13.8
1.4. Khảo sát quá trình chần ngâm acid citric kết hợp với ion kim
loại tạo phức.
1.4.1. Ngâm acid citric kết hợp với Cu2+
Bảng 9.1: kết quả giá trị OD thu được
Điểm các thành viên Mẫu
hội đồng
1 2 3 4 5 6 7
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxlix
Trung bình 10.4 6.6 7.70 8.30 7.80 7.70 7.40
Hàm mục độ hấp phụ Chlorophyll.
Chọn phương trình hồi qui (*), các hệ số b1, b2, b3, b12 được tính theo số liệu thực
nghiệm hàm mục tiêu hiệu suất thu hồi chất khô (Y).
Tính hệ số b:theo phần đánh giá ở thí nghiệm trên, ta có:
b0 b1 b2 b12
8.25 0.8 0.25 1.1
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Kết quả các thí nghiệm ở tâm:
N0 𝑌𝑢0 ̅̅̅0
𝑌 ̅̅̅0
𝑌𝑢0 − 𝑌 ̅̅̅0 )2
(𝑌𝑢0 − 𝑌 ̅̅̅0 )2
∑(𝑌𝑢0 − 𝑌
1 7.0 7.367 -0.3667 0.1344 0.2467
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cl
2 7.7 0.333 0.111
3 7.4 0.0333 0.0011
2 1 ̅̅̅0 2
Phương sai tái hiện:𝑆𝑡ℎ = ∑𝑚 0
𝑢=1(𝑌𝑢 − 𝑌 ) =0.123
𝑚−1
Trong đó m là số thí nghiệm ở tâm phương án (m = 3)
𝑆𝑡ℎ
Sbj: Độ lệch quân phương của hệ số thứ j, với: 𝑆𝑏𝑗 = =0.176
√𝑁
Tính các hệ số tj, thu được kết quả sau:
t0 t1 t2 t12
46.98 4.56 1.42 6.26
Tra bảng tiêu chuẩn Student ta có tp(fth) = t0,05(2) = 4,3
Ta nhận thấy, các hệ số t0, t1, t12 đều lớn hơn t0,05(2) = 4,3 còn t2 lại nhỏ hơn, do đó chỉ
có các hệ số b0, b2 ,b12 có nghĩa và phương trình hồi qui hoàn chỉnh như sau:
𝑌̂1 = 8.25 + 0.8x2 + 1.1x12
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
STT 𝑌̂1 Yi Yi − 𝑌̂1 (Yi − 𝑌̂1 )2
1
10.15 10.40 0.250 0.0625000
2
6.35 6.60 0.250 0.0625000
3
7.95 7.70 -0.250 0.0625000
4
7.20 8.30 1.100 1.2100000
1
2
Phương sai dư: 𝑆𝑑ư = ∑𝑁 ̂ 2
𝑖=1(Yi − 𝑌1 ) =1.40
𝑁−𝐿
(N là số thí nghiệm, L là hệ số ý nghĩa)
Tiêu chuẩn Fisher:
2
𝑆𝑑ư
F= 2 = 11.38
𝑆𝑡ℎ
Tra bảng phân vị phân bố Fisher với P=0,05, f1 = N-L=1, f2 = N0 – 1 = 2, ta có: F1-p=
F0,95 (1,2) = 19
Vì F < F0,095(1,2) nên phương trình hồi qui tương thích với thực nghiệm.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cli
Z 1 75
Ta có các giá trị: x1= , x2 = Z 2 20
45 10
Vậy ta có phương trình biến thực là:
Y= 10.313 – 0.1037Z2 + 2.44x 10 3 Z12
Tối ưu bằng phương pháp đơn hình đều.
Bảng 9.4: thí nghiệm khởi đầu
Số thí nghiệm X1 X2 Giá trị thực Y
X1 X2
1 -0.5 -0.289 25 17 10.8
2 0.5 -0.289 55 17 10.1
3 0 0.578 40 26 9.5
Như tối ưu ở phương pháp trên. Ta có
Y là hàm mục tiêu giá trị OD thu được. Theo bảng trên ta có y3= { y1….y4} = 3.9 . Ta
bỏ đỉnh x3, thay nó theo ánh xạ phản chiếu được đỉnh x4 đối xứng với x3 qua diện tạo
bởi các điểm 1,2.
Tọa độ của thí nghiệm thứ 4 là:
X 14 40
X 24 8
Điểm mới thứ 4 cùng với điểm còn lại tạo nên một đơn hình 1,2,4 . Lập được bảng sau.
Bảng 9.5
Số thí nghiệm X1 X2 Y
2 25 17 10.8
3 40 26 10.1
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clii
5 40 8 9.2
1.4.2. Ngâm acid citric kết hợp với Zn2+.
Bảng 10.1: kết quả cảm quan
Điểm các thành viên Mẫu
hội đồng
1 2 3 4 5 6 7
Trung bình 7.2 6.70 5.60 10.40 5.90 6.70 6.30
Hàm mục độ hấp phụ Chlorophyll
Chọn phương trình hồi qui (*), các hệ số b1, b2, b3, b12 được tính theo số liệu thực
nghiệm hàm mục tiêu hiệu suất thu hồi chất khô (Y).
Tính hệ số b:theo phần đánh giá ở thí nghiệm chần, ta có:
b0 b1 b2 b12
7.475 -1.075 -0.525 1.325
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cliii
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cliv
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Kết quả các thí nghiệm ở tâm:
N0 𝑌𝑢0 ̅̅̅0
𝑌 ̅̅̅0
𝑌𝑢0 − 𝑌 ̅̅̅0 )2
(𝑌𝑢0 − 𝑌 ̅̅̅0 )2
∑(𝑌𝑢0 − 𝑌
1 5.9 -0.4 0.16
2 6.7 6.3 0.4 0.16 0.32
3 6.3 0 0
2 1 ̅̅̅0 2
Phương sai tái hiện:𝑆𝑡ℎ = ∑𝑚 0
𝑢=1(𝑌𝑢 − 𝑌 ) =0.16
𝑚−1
Trong đó m là số thí nghiệm ở tâm phương án (m = 3)
𝑆𝑡ℎ
Sbj: Độ lệch quân phương của hệ số thứ j, với: 𝑆𝑏𝑗 = =0.2
√𝑁
Tính các hệ số tj, thu được kết quả sau:
t0 t1 t2 t12
37.375 5.375 2.625 6.625
Tra bảng tiêu chuẩn Student ta có tp(fth) = t0,05(2) = 4,3
Ta nhận thấy, các hệ số t0, t1, t12 đều lớn hơn t0,05(2) = 4,3 còn t2lại nhỏ hơn, do đó chỉ
có các hệ số b0, b1 ,b12 có nghĩa và phương trình hồi qui hoàn chỉnh như sau:
𝑌̂1 = 7.475 – 1.075x1 + 1.325 x12
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
STT 𝑌̂1 Yi Yi − 𝑌̂1 (Yi − 𝑌̂1 )2
1
7.73 7.20 -0.525 0.2756250
2
7.23 6.70 -0.525 0.2756250
3
5.08 5.60 0.525 0.2756250
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clv
4
9.08 10.40 1.325 1.7556250
1
2
Phương sai dư: 𝑆𝑑ư = ∑𝑁 ̂ 2
𝑖=1(Yi − 𝑌1 ) =2.58
𝑁−𝐿
(N là số thí nghiệm, L là hệ số ý nghĩa)
Tiêu chuẩn Fisher:
2
𝑆𝑑ư
F= 2 = 16.125
𝑆𝑡ℎ
Tra bảng phân vị phân bố Fisher với P=0,05, f1 = N-L=1, f2 = N0 – 1 = 2, ta có: F1-p=
F0,95 (1,2) = 18,51.
Vì F < F0,095(1,2) nên phương trình hồi qui tương thích với thực nghiệm.
Z 1 75
Ta có các giá trị: x1= , x2 = Z 2 125
45 25
Vậy ta có phương trình biến thực là:
Y= 22.99 – 0.2065Z2 + 1.22 x 10 3 Z12
Tối ưu bằng phương pháp đơn hình đều.
Bảng 10.2 thí nghiệm khởi đầu
Số thí nghiệm X1 X2 Giá trị thực Y
X1 X2
1 -0.5 -0.289 25 120 11.2
2 0.5 -0.289 55 120 10.7
3 0 0.578 40 140 13.65
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clvi
Như tối ưu ở phương pháp trên. Ta có
Y là hàm mục tiêu giá trị OD thu được. Theo bảng trên ta có y3= { y1….y4} = 13.65 .
Ta bỏ đỉnh x3, thay nó theo ánh xạ phản chiếu được đỉnh x4 đối xứng với x3 qua diện
tạo bởi các điểm 1,2.
Tọa độ của thí nghiệm thứ 4 là:
X 14 40
X 24 100
Điểm mới thứ 4 cùng với điểm còn lại tạo nên một đơn hình 1,2,4 . Lập được bảng sau.
Bảng 10.3
Số thí nghiệm X1 X2 Y
2 25 120 11.2
3 40 140 10.7
5 40 100 10.1
Bảng 10.4
Số thí nghiệm X1 X2 Y
3 40 140 10.7
5 40 100 10.1
6 55 120 10.6
1.4.3. Ngâm acid citric kết hợp với Mg2+.
Bảng 10.1: kết quả giá trị OD thu được
Điểm các thành viên Mẫu
hội đồng
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clvii
1 2 3 4 5 6 7
Trung bình 6.10 9.10 6.70 8.30 7.3 6.8 7.1
Hàm mục tiêu độ hấp phụ Chlorophyll.
Chọn phương trình hồi qui (*), các hệ số b1, b2, b3, b12 được tính theo số liệu thực
nghiệm hàm mục tiêu giá trị OD (Y).
Tính hệ số b:theo phần đánh giá ở thí nghiệm chần, ta có:
b0 b1 b2 b12
7.65 -1.2 0.55 -0.3
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Kết quả các thí nghiệm ở tâm:
N0 𝑌𝑢0 ̅̅̅0
𝑌 ̅̅̅0
𝑌𝑢0 − 𝑌 ̅̅̅0 )2
(𝑌𝑢0 − 𝑌 ̅̅̅0 )2
∑(𝑌𝑢0 − 𝑌
1 7.3 0.2333 0.0544
2 6.8 7.0667 -0.2667 0.0711 0.1267
3 7.1 0.0333 0.0011
2 1 ̅̅̅0 2
Phương sai tái hiện:𝑆𝑡ℎ = ∑𝑚 0
𝑢=1(𝑌𝑢 − 𝑌 ) =0.063
𝑚−1
Trong đó m là số thí nghiệm ở tâm phương án (m = 3)
𝑆𝑡ℎ
Sbj: Độ lệch quân phương của hệ số thứ j, với: 𝑆𝑏𝑗 = =0.126
√𝑁
Tính các hệ số tj, thu được kết quả sau:
t0 t1 t2 t12
60.79 9.54 4.37 2.38
Tra bảng tiêu chuẩn Student ta có tp(fth) = t0,05(2) = 4,3
Ta nhận thấy, các hệ số t0, t1, t2 đều lớn hơn t0,05(2) = 4,3 còn t12 lại nhỏ hơn, do đó chỉ
có các hệ số b0, b1 ,b2 có nghĩa và phương trình hồi qui hoàn chỉnh như sau:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clviii
𝑌̂1 = 7.65– 1.2x1 + 0.55 x2
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
STT 𝑌̂1 Yi Yi − 𝑌̂1 (Yi − 𝑌̂1 )2
1
6.15 6.70 0.550 0.3025000
2
9.15 9.70 0.550 0.3025000
3
6.75 6.20 -0.550 0.3025000
4
8.30 8.00 -0.300 0.0900000
1
2
Phương sai dư: 𝑆𝑑ư = ∑𝑁 ̂ 2
𝑖=1(Yi − 𝑌1 ) =0.997
𝑁−𝐿
(N là số thí nghiệm, L là hệ số ý nghĩa)
Tiêu chuẩn Fisher:
2
𝑆𝑑ư
F= 2 = 15.82
𝑆𝑡ℎ
Tra bảng phân vị phân bố Fisher với P=0,05, f1 = N-L=1, f2 = N0 – 1 = 2, ta có: F1-p=
F0,95 (1,2) = 18,51.
Vì F < F0,095(1,2) nên phương trình hồi qui tương thích với thực nghiệm.
Z 1 75
Ta có các giá trị: x1= , x2 = Z 2 1500
45 500
Vậy ta có phương trình biến thực là:
Y= 4 – 0.267 Z2 + 1.1x 10 3 Z12
Tối ưu bằng phương pháp đơn hình đều.
Bảng 10.2 thí nghiệm khởi đầu
Số thí nghiệm X1 X2 Giá trị thực Y
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clix
X1 X2
1 -0.5 -0.289 25 1200 11.4
2 0.5 -0.289 55 1200 9.3
3 0 0.578 40 1400 12.7
Như tối ưu ở phương pháp trên. Ta có
Y là hàm mục tiêu giá trị OD thu được. Theo bảng trên ta có y3= { y1….y4} = 12.7
cách xa so với giá trị OD của mẫu tối ưu. Ta bỏ đỉnh x3, thay nó theo ánh xạ phản
chiếu được đỉnh x4 đối xứng với x3 qua diện tạo bởi các điểm 1,2.
Tọa độ của thí nghiệm thứ 4 là:
X 14 40
X 24 1000
Điểm mới thứ 4 cùng với điểm còn lại tạo nên một đơn hình 1,2,4 . Lập được bảng sau.
Bảng 10.3
Số thí nghiệm X1 X2 Y
2 25 1200 11.4
3 40 1400 9.3
5 40 1000 11.2
Bảng 10.4
Số thí nghiệm X1 X2 Y
2 25 1200 11.4
5 40 1000 11.2
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clx
6 25 800 10.2
1.5. Khảo sát quá trình xử lý emzyme cenlulase.
Khi xử lý nguyên liệu với enzyme, vì được tiến hành ở điều kiện nhiệt độ tương đối
cao là 50oC (điều kiện thuận lợi cho enzyme cenlulase hoạt động) trong thời gian tương
đối dài (từ 30 phút đến 2 giờ), sau đó phải trải qua giai đoạn gia nhiệt lên 80oC để bất
hoạt enzyme rồi mới thu hồi dịch chiết. Do đó chỉ tiêu cảm quan màu và mùi của dịch
chiết thu được là rất kém, đồng thời cấu trúc sản phẩm lắng rất nhanh so với phương
pháp chần ( chỉ 1h đã lắng gấn như hoàn toàn).
Bảng 11.1. hiệu xuất thu hồi chất khô của emzyme cenlulase.
Thí Giá trị thực Hiệu suất thu hồi
nghiệm Nồng độ emzyme Thời gian xử lý
1 0,55 75 32,95
2 0,55 75 32,34
3 1 120 36,19
4 0,55 75 32,74
5 0,1 120 32,38
6 0,3 30 12,79
7 1 30 30,02
Hàm mục tiêu hiệu suất thu hồi chất khô:
Chọn phương trình hồi qui (*), các hệ số b1, b2, b3, b12 được tính theo số liệu thực
nghiệm hàm mục tiêu hiệu suất thu hồi chất khô (Y1).
Tính hệ số b:theo phần đánh giá ở thí nghiệm chần, trang 44, ta có:
b0 b1 b2 b12
27.85 5.26 6.44 -3.36
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxi
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Kết quả các thí nghiệm ở tâm:
N0 𝑌𝑢0 ̅̅̅0
𝑌 ̅̅̅0
𝑌𝑢0 − 𝑌 ̅̅̅0 )2
(𝑌𝑢0 − 𝑌 ̅̅̅0 )2
∑(𝑌𝑢0 − 𝑌
1 33.95 1.94 3.764
2 31.34 32.68 -0.67 0.449 5.853
3 30.74 -1.27 1.613
2 1 ̅̅̅0 2
Phương sai tái hiện:𝑆𝑡ℎ = ∑𝑚 0
𝑢=1(𝑌𝑢 − 𝑌 ) = 2.193
𝑚−1
Trong đó m là số thí nghiệm ở tâm phương án (m = 3)
𝑆𝑡ℎ
Sbj: Độ lệch quân phương của hệ số thứ j, với: 𝑆𝑏𝑗 = =0.853
√𝑁
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxii
Tính các hệ số tjtheo công thức (**), trang 44, thu được kết quả sau:
t0 t1 t2 t12
179.71 33.95 41.56 21.65
Tra bảng tiêu chuẩn Student ta có tp(fth) = t0,05(2) = 4,3
Ta nhận thấy, các hệ số t0, t1, t2 đều lớn hơn t0,05(2) = 4,3 còn t12lại nhỏ hơn, do đó chỉ
có các hệ số b0, b1, b2 ,b12 có nghĩa và phương trình hồi qui hoàn chỉnh như sau:
𝑌̂1 = 27.85 + 5.26x1 + 6.44x2
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
STT 𝑌̂1 Yi Yi − 𝑌̂1 (Yi − 𝑌̂1 )2
1
16.15 12.79 -3.355 11.26
2
29.03 32.38 3.355 11.26
3
26.67 30.02 3.355 11.26
4
39.55 36.19 -3.355 11.26
1
2
Phương sai dư: 𝑆𝑑ư = ∑𝑁 ̂ 2
𝑖=1(Yi − 𝑌1 ) =15
𝑁−𝐿
(N là số thí nghiệm, L là hệ số ý nghĩa)
Tiêu chuẩn Fisher:
2
𝑆𝑑ư
F= 2 = 7.17
𝑆𝑡ℎ
Tra bảng phân vị phân bố Fisher với P=0,05, f1 = N-L=1, f2 = N0 – 1 = 2, ta có: F1-p =
F0,95 (1,2) = 18,51.
Vì F < F0,095(1,2) nên phương trình hồi qui tương thích với thực nghiệm.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxiii
BÁO CÁO KHẢO SÁT SƠ BỘ CHẤT ỔN ĐỊNH
I. Khảo sát đơn chất.
1. Carrgeenan.
Nồng độ Độ nhớt Điểm cảm quan
( mPa.s)
Độ nhớt Độ đặc
0.1 2.47 4.1 3.9
0.2 14.72 3.5 2.5
0.3 154.35 2.5 1.8
0.4 378.98 1.9 1.3
400 4.5
350 4.1 3.9 378.98 4
300 3.5 3.5
3
250
2.5 2.5 giá trị độ nhớt
200
1.9 2 DCQ độ nhớt
150 1.8
154.35 1.5 DCQ độ đặc
1.3
100 1
50 0.5
2.47 14.72
0 0
0.10% 0.20% 0.30% 0.40%
Hình 1.1 đồ thị biểu diễn độ nhớt, điểm cảm quan độ nhớt và độ đặc
Nhận xét: Khi khảo sát sử dụng Carrageenan, ta thấy :
+ Carrageenan chủ yếu tạo độ đặc cho sản phẩm.
+ Về độ nhớt: chỉ có nghiệm thức ở nồng độ 0.1 là chấp nhận và 0.2 ta tạm chấp nhận . còn 2
nghiệm thức 0.3 và 0.4 loại vì độ nhớt quá cao .
+ Về điểm cảm quan: nghiệm thức ở nồng độ 0.1 có điểm cảm quan cao nhất cả trước và sau
thanh trùng.
+ nhận xét về độ kết lắng:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxiv
Bảng 1: Sau 7 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.1% Các mẫu đồng nhất, có hiện tượng lắng cặn, chiều cao cột lắng 2.5cm.
0.2% Các mẫu đồng nhất, có hiện tượng kết lắng, chiều cao cột lắng là 1.3cm.
0.3% Sản phẩm đồng nhất, không có hiện tượng kết lắng, không bị lắng cặn.
0.4% Sản phẩm đồng nhất, không có hiện tượng kết lắng, không bị lắng cặn.
Bảng 2: Sau 14 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.1% Mẫu bị kết lắng hoàn toàn
0.2% Mẫu lắng với kích thước 5.6cm.
0.3% Có hiện tượng kết lắng, ciều cao cột lắng 3cm.
0.4% Sản phẩm đồng nhất, không bị lắng.
Bảng 3: Sau 21 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.1% Sản phẩm lắng hoàn toàn
0.2%
0.3%
0.4% Có hiện tượng kết lắng ít, chiều cao cột lắng 1cm.
Bảng 4: sau 1 tháng theo dõi.
Nồng độ Nhận xét về độ lắng
0.1% Sản phẩm lăng hoàn toàn
0.2%
0.3%
0.4%
Kết luận và kiến nghị: qua thời gian theo dõi chất ổn định carragenan đến ổn định cấu trúc
của nước rau, chúng tôi nhận thấy các mẫu đều bị kết lắng hoàn toàn sau 1 tháng bảo quản,
với nồng độ 0.4% thì có hiện tượng kết lắng ít, tuy nhiên ở 0.4% caragennan thì điểm cảm
quan độ nhớt và độ đặc rất thấp, vì thế chúng tôi không khảo sát lại chất ổn định này trong
phần tối ưu.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxv
2. Alginate.
Nồng độ Độ nhớt Điểm cảm quan
Trước thanh Sau thanh trùng
trùng
Độ nhớt Độ Độ nhớt Độ đặc
đặc
0.1 1.82 2.9 4.1 2.7 3.8
0.2 3.89 2.8 3.9 2.8 3.7
0.3 5.33 1.4 2.2 1.2 2.0
0.4 12.41 0.8 1.7 0.8 1.5
14 4.5
4.1 4
12 3.9
3.5
10
2.9 3
2.8
8 2.5 giá trị độ nhớt
2.2 DCQ độ nhớt
6 12.41 2
1.7 DCQ độ đặc
1.4 1.5
4
1
5.33 0.8
2 3.89 0.5
1.82
0 0
0.10% 0.20% 0.30% 0.40%
Hình 1.2: Đồ thị biểu diễn độ nhớt và điểm cảm quan
Nhận xét: khi sử dụng Alginate trong sản phẩm ta thấy:
+ về cảm quan: cảm quan độ nhớt của sản phẩm đạt giá trị rất thấp, sản phẩm hầu như rất
nhớt. nồng độ chấp nhận Aginate chì nồng độ 0.1%.
+ về độ kết lắng:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxvi
Bảng 1: Sau 7 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.1% Sản phẩm đống nhất, có hiện tượng lắng, chiều cao cột
kết lắng 2cm, hơi lắng cặn ở dưới.
0.2% Sản phẩm đồng nhất, có hiện tượng lắng, chiều cao
Cột kết lắng 1.3cm, hơi lắng cặn ở dưới.
0.3% Sản phẩm đồng nhất, không có hiện tượng lắng, tuy nhiên
hơi lắng cặn ở dưới.
0.4% Sản phẩm đống nhất, không kết lắng
Bảng 2: Sau 14 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.1% Hầu như cả 3 nồng độ đều bị lắng hoàn toàn.
0.2%
0.3%
0.4% Đồng nhất, không có hiện tượng kết lắng.
Bảng 3: Sau 21 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.1% Hầu như cả 3 nồng độ đều bị lắng hoàn toàn.
0.2%
0.3%
0.4% Sản phẩm lắng 3.8cm.
Bảng 4: sau 1 tháng theo dõi.
Nồng độ Nhận xét về độ lắng
0.1% Sản phẩm lăng hoàn toàn
0.2%
0.3%
0.4%
Kết luận và kiến nghị: qua thời gian theo dõi chất ổn định Alginate đến ổn định cấu trúc của
nước rau, chúng tôi nhận thấy các mẫu hầu như đều bị kết lắng hoàn toàn sau 1 tháng bảo
quản, vì thế chúng tôi không khảo sát lại chất ổn định này trong phần tối ưu.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxvii
3. Xantha Gum
Nồng độ Độ nhớt Điểm cảm quan
Độ nhớt Độ đặc
0.1 2.7 4.1 4.3
0.2 6.85 4.4 4.5
0.3 33.52 3.0 2.0
0.4 82.04 2.3 1.0
90 5
80
70 82.04 4
60 giá trị độ
50 3 nhớt
40 2 DCQ độ
30 nhớt
33.52
20 1
10 DCQ độ đặc
2.7 6.85
0 0
Hình 1.3: đồ thị biểu diễn giá trị độ nhớt và điểm cảm quan
Bảng 1: Sau 7 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.1%
0.2% Sản phẩm đồng nhất, không có hiện tượng kết lắng, không lắng cặn
0.3%
0.4%
Bảng 2: Sau 14 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.1% Sản phẩm đồng nhất, không có hiện tượng tách lớp, lắng cặn ở dưới.
0.2% Sản phẩm đồng nhất, không kết lắng.
0.3%
0.4%
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxviii
Bảng 3: Sau 21 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.1% Sản phẩm lắng cặn, có hiện tượng tách lớp, chiều cao cột kết lắng 2.3cm
0.2% Sản phẩm hơi lắng cặn
0.3% Sản phẩm không có hiện tượng kết lắng
0.4%
Bảng 4: sau 1 tháng theo dõi.
Nồng độ Nhận xét về độ lắng
0.1% Sản phẩm lắng ½ chai
0.2% Sản phẩm hơi lắng nhẹ
0.3% Không có hiện tượng kết lắng
0.4%
Kết luận và kiến nghị: qua thời gian theo dõi chất ổn định Xanthan gum đến ổn định cấu trúc
của nước rau, chúng tôi nhận thấy ở nồng độ 0.1% sau 1 tháng theo dõi thí bị lắng 2.6cm, và
các nồng độ còn lại không bị lắng hoặc lắng nhẹ. Với nồng độ 0.4% thì điểm cảm quan độ
nhớt và độ đặc thấp, do đó chúng tôi khảo sát lại chất ổn định này ở nồng độ từ 0.15 – 0.3%.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxix
4. Guar Gum.
Nồng độ Độ nhớt Điểm cảm quan
Trước thanh
trùng
Độ nhớt Độ đặc
0.1 1.94 4.0 4.2
0.2 4.35 4.5 4.7
0.3 15.70 3.1 3.8
0.4 17.30 2.7 2.3
20 5
17.3 4
15
15.7
3 giá trị độ nhớt
10
2 DCQ độ nhớt
5 DCQ độ đặc
1
1.94 4.35
0 0
0.10% 0.20% 0.30% 0.40%
Hình : đồ thị biểu diễn giá trị độ nhớt và điểm cảm quan
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxx
Bảng 1: Nhận xét độ kết lắng Sau 7 ngày theo dõi.
Nồng độ Nhận xét về độ lắng
0.1% Lắng hoàn toàn
0.2%
0.3%
0.4%
Nhận xét: Guar Gum là chất có khả năng lắng rất cao, nên chúng tôi không sử dụng chất ổn
định này cho quá trình khảo sát tối ưu.
5. CMC
Nồng độ Độ nhớt Điểm cảm quan
Độ nhớt Độ đặc
0.1 0.93 4.4 4.4
0.2 2.65 4.6 4.8
0.3 3.93 4.1 4.0
0.4 6.83 3.9 3.5
8 6
7
5
6.83
6
4
5
giá trị độ nhớt
4 3
DCQ độ nhớt
3.93
3 DCQ độ đặc
2
2 2.65
1
1
0.93
0 0
0.10% 0.20% 0.30% 0.40%
Hình 1.3: đồ thị biểu diễn giá trị độ nhớt và điểm cảm quan
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxi
Bảng 1: Sau 7 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.1% Sản phẩm lắng cặn, có hiện tượng tách lớp, chiều cao cột kết lắng 5cm
0.2% Sản phẩm hơi lắng cặn, chiều cao cột lắng là 2.8 cm.
0.3% Sản phẩm không có hiện tượng kết lắng.
0.4%
Bảng 2: Sau 14 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.1% Sản phẩm kết lắng hoàn toàn.
0.2%
0.3% Sản phẩm có hiện tượng kết lắng , chiều cao cột lắng là 4 cm.
0.4% Sản phẩm có hiện tượng kết lắng , chiều cao cột lắng là 2.3 cm.
Bảng 3: Sau 21 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.1% Sản phẩm kết lắng hoàn toàn.
0.2%
0.3% Sản phẩm không có hiện tượng kết lắng, lắng hơn ½ chai.
0.4%
Nhận xét: Tuy cả 4 nghiệm thức khảo sát CMC ở 4 nồng độ khác nhau đều cho điểm cảm
quan cao, nhưng ta phải khẳng định CMC là chất có khả năng lắng rất cao, chỉ sau 2 tuần
theo dõi thì CMC nồng độ 0.1 và 0.2 đã lắng hoàn toàn , còn CMC ở nồng độ 0.3 và 0.4 đều
lắng nhiều sau 3 tuần theo dõi .Do đó , chúng tôi không sử dụng chất ổn định này cho quá
trình khảo sát chất ổn định.
6. Pectin
Nồng độ Độ nhớt Điểm cảm quan
Độ nhớt Độ đặc
0.1 1.5 4.4 4.3
0.2 3.6 4.5 4.6
0.3 8.2 3.5 3.5
0.4 13.1 2.6 2.4
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxii
14 5
4.5
12 13.1
4
10 3.5
8 3
giá trị độ nhớt
8.2 2.5
DCQ độ nhớt
6 2
DCQ độ đặc
4 1.5
3.6 1
2
0.5
1.5
0 0
0.10% 0.20% 0.30% 0.40%
Hình 1.4: đồ thị biểu diễn giá trị độ nhớt và điểm cảm quan
Bảng 1: Sau 7 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.1% Sản phẩm kết lắng hoàn toàn.
0.2% Sản phẩm kết lắng nhiều, chiều cao cột lắng là 5cm.
0.3% Sản phẩm không có hiện tượng kết lắng.
0.4%
Bảng 1: Sau 14 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.1% Sản phẩm kết lắng hoàn toàn.
0.2%
0.3% Sản phẩm có hiện tượng kết lắng , chiều cao cột lắng là 4 cm.
0.4% Sản phẩm có hiện tượng kết lắng , chiều cao cột lắng là 3.3 cm.
Bảng 1: Sau 21 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.1% Sản phẩm kết lắng hoàn toàn.
0.2%
0.3%
0.4%
Nhận xét : sau 3 tuần theo dõi, các nghiệm thực khảo sát Pectin ở cả 4 nồng độ đều cho hiện
tượng kết lắng hoàn toàn. do đó, chúng tôi không sử dụng chất ổn định này cho quá trình khảo
sát chất ổn định tối ưu.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxiii
II . Kết hợp từng cặp chất.
1. CMC – Pectin.
Nồng độ Độ nhớt Điểm cảm quan
( CMC- Pectin) Trước thanh trùng
Độ nhớt Độ đặc
0.2-02 8.29 3.2 2.5
0.2-0.05 3.38 3.8 4.3
0.05-0.2 4.48 4.0 3.8
0.05-0.05 1.36 3.8 4.2
0.125-0.125 2.53 4.0 4.7
10 5
8 4
6 3
4 2
giá trị độ nhớt
2 1
0 0 ĐCQ độ nhớt
ĐCQ độ đặc
Nhận xét: khi sử dụng kết hợp 2 chất ổn định CMC và Pectin ta thấy.
+ nhận xét về độ kết lắng: khi kết hợp 2 chất ổn định Pectin và CMC ta có: khi hàm lượng
Pectin cao hơn CMC thì khả năng kết lắng theo thời gian của sản phẩm tăng lên.
Bảng 1: Sau 7 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.2-0.2 Sản phẩm đồng nhất, có hiện tượng kết lắng với chiều cao cột
lắng là 0.5cm, và có hiện tượng lắng cặn ở đáy.
0.2-0.05 Sản phẩm đồng nhất, có hiện tượng kết lắng, chiều cao
cột lắng 0.7cm.
0.05-0.2 Sản phẩm đồng nhấ, có hiện tượng kết lắng, chiếu cao cột
lắng là 1cm
0.05-0.05 Sản phẩm đồng nhất, có hiện tượng kết lắng, với chiều
cao cột lắng là 1,5cm.
0.125-0.125 Sản phẩm đồng nhất, có hiện tượng kết lắng, với chiều
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxiv
Cao cột lắng là 1cm.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxv
Bảng 2: Sau 14 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.2-0.2 Sản phẩm đồng nhất, có hiện tượng kết lắng với chiều cao cột
lắng là 3.0 cm, và có hiện tượng lắng cặn ở đáy.
0.2-0.05 Sản phẩm đồng nhất, có hiện tượng kết lắng, chiều cao
cột lắng 2.5cm cm.
0.05-0.2 Sản phẩm đồng nhất, có hiện tượng kết lắng, chiều cao cột
lắng là 4.7cm
0.05-0.05 Sản phẩm đồng nhất, có hiện tượng kết lắng, lắng hoàn
toàn.
0.125-0.125 Sản phẩm đồng nhất, có hiện tượng kết lắng, với chiều
Cao cột lắng là 5cm cm.
Bảng: sau 21 ngày theo dõi.
Nồng độ Nhận xét về độ lắng
0.2-0.2 Sản phẩm có độ lắng gần ½ của chai.
0.2-0.05 Độ lắng của sản phẩm không thay đổi nhiều so với 7 ngày
trước.
0.05-0.2 Sản phẩm hầu như lắng hoàn toàn.
0.05-0.05
0.125-0.125
Bảng: sau 1 tháng
Nồng độ Nhận xét về độ lắng
0.2-0.2 Sản phẩm hầu như lắng hoàn toàn
0.2-0.05
0.05-0.2
0.05-0.05
0.125-0.125
Kết luận và kiến nghị: khi khảo sát 2 chất ổn định CMC – Pectin chúng tôi nhận thấy khi kết
hợp nồng Pectin chiếm tỉ lệ cao thì làm cho độ nhớt của sản phẩm tăng, tuy nhiên thời gian
kết lắng nhanh hơn so với tỉ lệ CMC cao.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxvi
2. CMC – Xanthan Gum.
Nồng độ Độ nhớt Điểm cảm quan
( CMC- Xanthan
Gum). Độ Độ
nhớt đặc
0.2-0.2 17.43 2.6 2.5
0.2-0.05 3.33 4.7 4.5
0.05-0.2 11.02 4.2 4.0
0.05-0.05 1.63 4.3 4.3
0.125-0.125 4.27 4.8 4.3
20 6
18
16 5
14 4
12
10 3 giá trị độ nhớt
8
2 ĐCQ độ nhớt
6
4 ĐCQ độ đặc
1
2
0 0
Nhận xét về độ kết lắng trong suốt thời gian bảo quản:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxvii
Bảng 1: Sau 7 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.2-0.2 Sản phẩm đồng nhất, không có hiện tượng kết lắng, không bị
lắng cặn.
0.2-0.05 Sản phẩm đồng nhất, không có hiện tượng kết lắng, không bị
lắng cặn.
0.05-0.2 Sản phẩm đồng nhất, không có hiện tượng kết lắng, không bị
lắng cặn.
0.05-0.05 Sản phẩm đồng nhất, không có hiện tượng kết lắng, không bị
lắng cặn.
0.125-0.125 Sản phẩm đồng nhất, không có hiện tượng kết lắng, không bị
lắng cặn.
Bảng 2: Sau 14 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.2-0.2 Tất cả các mẫu không bị kết lắng, không bị lắng cặn trong
0.2-0.05 Quá trình bảo quản.
0.05-0.2
0.05-0.05
0.125-0.125
Bảng: sau 21 ngày theo dõi.
Nồng độ Tất cả các mẫu không bị kết lắng, không bị lắng cặn trong thời
0.2-0.2 gian bảo quản.
0.2-0.05
0.05-0.2
0.05-0.05
0.125-0.125
Nhận xét :qua khảo sát sơ bộ 2 chất ổn định CMC và Xanthan gum chúng tôi nhận thấy ờ các
nồng độ khác nhau khi kết hợp các chất này thì không bị kết lắng trong suốt thời gian bảo
quản. tuy nhiên do nồng độ 0.4 % ( 0.2%CMC – 0.2% Xanthagum) thì điểm cảm quan độ
nhớt và độ đặc của sản phẩm là rất thấp vì thế chúng tôi loại bỏ khoảng giá trị này. Đồng thời
ở mức 0.25% khi kết hợp với tỉ lệ của cả 2 chất thì có điểm cảm quan ở mức trung bình nên
chúng tôi tiến hành khảo sát lại sự kết hợp 2 chất ổn định này trong khoảng nồng độ 0.1% -
0.25%.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxviii
3. Pectin – Xanthan Gum.
Nồng độ Độ nhớt Điểm cảm quan
(Pectin–Xanthan Gum) Trước thanh trùng
Độ nhớt Độ đặc
0.2-02 24.3 2.5 2.3
0.2-0.05 12.8 4.3 4.7
0.05-0.2 21.8 4.2 4.2
0.05-0.05 3.9 4 3.8
0.125-0.125 8.61 4.7 4.5
30 5
25 4
20
3
15
2 giá trị độ nhớt
10
5 1 ĐCQ độ nhớt
0 0 ĐCQ độ đặc
Bảng 1: Sau 7 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.2-0.2 Đồng nhất,không có hiện tượng kết lắng, không bị lắng cặn
0.2-0.05 Đồng nhất, có hiện tượng kết lắng, chiều cao cột lắng là 1.3 cm.
0.05-0.2 Đồng nhất, không có hiện tượng kết lắng, không bị lắng cặn
0.05-0.05 Đồng nhất, có hiện tượng phân lớp, bị kết lắng, chiều cao cột lắng
4 cm.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxix
Bảng 2: Sau 14 ngày theo dõi
Nồng độ Nhận xét về độ lắng
0.2-0.2 Không thay đổi sau 14 ngày theo dõi
0.2-0.05 Đồng nhất, có hiện tượng kết lắng, chiều cao cột lắng là 3.7cm.
0.05-0.2 Đồng nhất, có hiện tượng kết lắng, chiều cao cột lắng là 2.4 cm.
0.05-0.05 Sản phẩm lắng hoàn toàn
Bảng: sau 21 ngày theo dõi.
Nồng độ Nhận xét về độ lắng
0.2-0.2 Sản phẩm đồng nhất, không thay đổi sau thời gian bảo quản
0.2-0.05 Sản phẩm lắng hoàn toàn
0.05-0.2 Sản phẩm lắng gần ½ chai
0.05-0.05 Sản phẩm lắng hoàn toàn
Nhận xét: qua khảo sát sơ bộ 2 chất ổn định Pectin và Xanthan gum chúng tôi nhận thấy ở tất
cả nồng độ khảo sát đều có hiên tượng kết lắng gần như hoàn toàn sau 21 ngày theo dõi, chỉ
duy nhất ở nghiệm thức 0.2-0.2 thì sản phẩm giữ được độ đồng nhất . Tuy nhiên ở nồng độ
0.2- 0.2 lại có điểm cảm quan tương đối thấp, do đó tất cả nghiệm thức trên khi khảo sát sự
kết hợp như Pectin và Xanthan Gum chúng ta đều không khảo sát tiếp.
4. Kết hợp CMC – Guar Gum.
Nồng độ Độ nhớt Điểm cảm quan
( Guar Gum- CMC) Trước thanh trùng
Độ nhớt Độ đặc
0.05Guar-0.05CMC 1.39 3.6 3.5
0.2Guar -0.05CMC 3.38 4.3 4.1
0.05Guar-0.2CMC 3.64 4.6 4.6
0.125Guar-0.125CMC 3.17 4.3 4.5
0.2Guar -0.2CMC 9.39 2.8 2.1
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxx
10 5
8 4
6 3
giá trị độ
4 2 nhớt
2 1
ĐCQ độ nhớt
0 0
ĐCQ độ đặc
Nhận xét khi sử dụng kết hợp Guar Gum và CMC:
- Guar Gum để lại mùi khó chịu cho sản phẩm
- Với nồng độ CMC cao làm tăng giá trị độ nhớt
- Sau 1 tuần bảo quản tất cả các mẫu đều lắng hoàn toàn.
Kết luận: do tất cả các mẫu đều bị lắng hoàn toàn sau 1 tuần bảo quản nên chúng tôi không
khảo sát lại 2 chất ổn định này.
5. Kết hợp Xathan Gum – Guar Gum.
Nồng độ Độ nhớt Điểm cảm quan
(Xanthan Gum-
Độ nhớt Độ đặc
0.05Guar-0.05X 1.57 4.3 4.1
0.2Guar- 0.05X 7.44 3.5 3.7
0.05Guar – 0.2X 10.41 2.1 2.4
0.125Guar-0.125X 7.35 3.0 2.8
0.2 Guar – 0.2X 21.89 1.8 1.4
25 5
4.5
20 4
3.5
15 3
2.5 giá trị độ
10 2 nhớt
1.5 ĐCQ độ nhớt
5 1
0.5
0 0 ĐCQ độ đặc
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxxi
Nhận xét:
- Khi sử dụng kết hợp giữa Xanthan Gum và Guar Gum thì chúng tối nhận thấy cho
điểm cảm quan về độ nhớt và độ đặc rất thấp.
- Giá trị độ nhớt cũng tăng lên đáng kể
- Sau 1 tuần bảo quản tất cả các mẫu nghiên cứu đều bị lắng hoàn toàn.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxxii
III . Kết hợp 3 chất:
1. CMC- Pectin- Xanthan Gum.
Nồng độ. Độ nhớt Điểm cảm quan
( CMC-Pectin-Xanthan Gum)
Độ Độ đặc
nhớt
0.1C-0.1P-0.1X 10.53 3.7 4.0
0.1C-0.03P-0.03X 4.69 4.0 4.0
0.03C-0.1P-0.03X 4.76 3.2 3.2
0.03C-0.03P-0.1X 6.71 3.5 3.8
0.065C-0.065P-0.065X 5.27 3.8 4.2
0.03C-0.03P-0.03X 2.28 3.8 3.7
12 4.5
4
10
3.5
8 3
2.5
6
10.53 2
4 1.5 giá trị độ nhớt
6.71
4.694.76 5.27 1
2 ĐCQ độ nhớt
2.28 0.5
0 0 ĐCQ độ đặc
Nhận xét về độ kết lắng:
Bảng 1:
Sau 1 tuần theo dõi
Thí nghiệm Nhận xét về độ kết lắng
(CMC-P-X)
0.1-0.1-0.1 Đồng nhất, không bị kết lắng, không lắng cặn
0.03-0.03-0.03 Đồng nhất, có hiện tượng lắng cặn.
0.1-0.03-0.03 Đồng nhất, không có hiện tượng kết lắng, không lắng cặn
0.03-0.1-0.03
0.03-0.03-0.1
0.065-0.065-
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxxiii
0.065
Sau 2 tuần theo dõi
Thí nghiệm Nhận xét về độ kết lắng
(CMC-P-X)
0.1-0.1-0.1 Đồng nhất, không bị kết lắng, không lắng cặn
0.03-0.03-0.03 Đồng nhất, có hiện tượng lắng cặn, tuy nhiên có hiện tượng kết lắng
nhẹ.
0.1-0.03-0.03 Đồng nhất, không bị kết lắng, không lắng cặn
0.03-0.1-0.03
0.03-0.03-0.1
0.065-0.065-0.065 Đồng nhất, không lắng cặn, tuy nhiên sản phẩm bị kết lắng nhẹ.
Sau 3 tuần theo dõi
Thí nghiệm Nhận xét về độ kết lắng
(CMC-P-X)
0.1-0.1-0.1 Có hiện tượng lắng nhẹ
0.03-0.03-0.03 Tất cả có hiện tượng lắng ít hoặc lắng hoàn toàn.
0.1-0.03-0.03
0.03-0.1-0.03
0.03-0.03-0.1
0.065-0.065-0.065
Nhận xét:
- Khi sử dụng 3 chất ổn định chúng tôi nhận thấy ĐCQ độ nhớt và độ đặc tương đối cao,
đồng thời sản phẩm ít bị lắng.
- Khi Xanthan Gum chiềm tỉ lệ cao thì nó làm tăng độ nhớt cho sản phẩm.
2. CMC- Carrageenan-Xanthan Gum
Nồng độ. Độ nhớt Điểm cảm quan
( CMC-Car-Xanthan Gum)
Độ nhớt Độ đặc
0.1C-0.1Car-0.1X 12.67 3.4 3.1
0.1C-0.03Car-0.03X 5.82 4.1 4.2
0.03C-0.1Car-0.03X 7.61 4.3 4.4
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxxiv
0.03C-0.03Car-0.1X 9.46 3.6 3.7
14 5
12 4.5
4
10 3.5
8 3
12.67 2.5
6 2
4 9.46 8.57 1.5
7.61 giá trị độ nhớt
5.82 1
2 3.4 0.5 ĐCQ độ nhớt
0 0
ĐCQ độ đặc
0.065C-0.065Car-0.065X 8.57 3.9 4.0
0.03C-0.03Car-0.03X 3.4 4.0 4.5
Hình: độ nhớt và điểm cảm quan độ nhớt
Nhận xét về độ kết lắng:
Bảng 1:
Sau 1 tuần theo dõi
Thí nghiệm Nhận xét về độ kết lắng
(CMC-Car-X)
0.1-0.1-0.1 Sản phẩm đồng nhất, không kết lắng, không bị lắng cặn.
0.03-0.03-0.03
0.1-0.03-0.03
0.03-0.1-0.03
0.03-0.03-0.1
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxxv
0.065-0.065-
0.065
Sau 2 tuần theo dõi
Thí nghiệm Nhận xét về độ kết lắng
(CMC-Car-X)
0.1-0.1-0.1 Đồng nhất, không bị kết lắng, không lắng cặn
0.03-0.03-0.03 Có hiện tượng kết lắng nhẹ.
0.1-0.03-0.03 Đồng nhất, không bị kết lắng, không lắng cặn
0.03-0.1-0.03
0.03-0.03-0.1
0.065-0.065-0.065
Sau 3 tuần theo dõi
Thí nghiệm Nhận xét về độ kết lắng
(CMC-Car-X)
0.1-0.1-0.1 Đồng nhất không bị kết lắng, không có hiện tượng lắng cặn
0.03-0.03-0.03 Lắng hoàn toàn.
0.1-0.03-0.03 Đồng nhất, có hiện tượng kết lắng nhẹ
0.03-0.1-0.03
0.03-0.03-0.1 Đồng nhất, có hiện tượng lắng cặn ít ở dưới.
0.065-0.065-0.065
Sau 1 tháng theo dõi
Thí nghiệm Nhận xét về độ kết lắng
(CMC-Car-X)
0.1-0.1-0.1 Đồng nhất không bị kết lắng, không có hiện tượng lắng cặn
0.03-0.03-0.03 Lắng hoàn toàn.
0.1-0.03-0.03 Có hiện tượng kết lắng nhẹ.
0.03-0.1-0.03
0.03-0.03-0.1
0.065-0.065-0.065
3. Guar Gum – CMC- Xanthan Gum
Nồng độ. Độ nhớt Điểm cảm quan
( Guar Gum-CMC-Xanthan
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxxvi
Gum) Độ Độ đặc
nhớt
0.1G-0.1C-0.1X 4.33 4.0 4.2
0.1G-0.03C-0.03X 1.56 4.0 4.0
0.03G-0.1C-0.03X 2.04 4.2 4.2
0.03G-0.03C-0.1X 2.49 4.3 4.5
0.065G-0.065C-0.065X 2.66 4.3 4.3
0.03G-0.03C-0.03X 1.97 3.8 3.8
5 4.6
4 4.4
4.2
3
4
2 4.33
3.8 giá trị độ nhớt
1 2.042.492.661.97
1.56 3.6 ĐCQ độ nhớt
0 3.4
ĐCQ độ đặc
Nhận xét:
- Khi sử dụng 3 chất ổn định chúng
tôi nhận thấy ĐCQ độ nhớt và độ
đặc cao, đồng thời sản phẩm ít bị lắng.
- Khi Xanthan Gum chiềm tỉ lệ cao thì nó làm tăng độ nhớt cho sản phẩm.
Nhận xét về độ kết lắng:
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxxvii
Bảng 1:
Sau 1 tuần theo dõi
Thí nghiệm Nhận xét về độ kết lắng
(CMC-P-X)
0.1-0.1-0.1 Đồng nhất, không bị kết lắng, không lắng cặn
0.03-0.03-0.03 Đồng nhất, có hiện tượng lắng cặn
0.1-0.03-0.03 Đồng nhất, không có hiện tượng kết lắng, không lắng cặn
0.03-0.1-0.03
0.03-0.03-0.1 Đồng nhất , tuy nhiên có hiện tượng lắng cặn nhẹ.
0.065-0.065-
0.065
Sau 2 tuần theo dõi
Thí nghiệm Nhận xét về độ kết lắng
(CMC-P-X)
0.1-0.1-0.1 Đồng nhất, không bị kết lắng, không lắng cặn
0.03-0.03-0.03 Đồng nhất, sản phẩm lắng hoàn toàn.
0.1-0.03-0.03 Sản phẩm đồng nhất , có hiện lắng cặn gần như hoàn toàn.
0.03-0.1-0.03
0.03-0.03-0.1
0.065-0.065-
0.065
KHẢO SÁT CHẤT ỔN ĐỊNH TRONG KHOẢNG TỐI ƯU ĐÃ CHỌN
1. Nghiên cứu ảnh hưởng của nồng độ Xanthan Gum đến trạng thái
ổn định của sản phẩm.
Tương tự như các bước tiến hành như trên, tiến hành khảo sát lại chất ổn định với khoảng
nồng độ 0.1-0.3%. Trạng thái ổn định của nước uống dinh dưỡng từ cây chùm ngây được thể
hiện qua 2 chỉ tiêu là độ truyền suốt (OD) và độ nhớt. thời gian khảo sát của mẫu thí nghiệm
là 15 ngày.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxxviii
Bảng : kết quả quan sát sự thay đổi OD theo ngày
Nồng độ Giá trị OD Độ
1 ngày 3 ngày 5 ngày 7 ngày 10 ngày 15 ngày OD nhớt
0.1 34.5 36.8 38.2 41.3 41.9 42.3 7.8 1.83
0.15 33.3 35 36.1 36.9 37.3 38.9 5.4 2.94
0.2 34.2 35.6 35.9 36.4 36 36.5 2.3 5.31
0.25 35.6 36.3 36.4 37.5 38 37.7 2.1 14.59
0.3 36.8 37.0 37.0 37.7 38.9 38.7 1.9 33.52
Kết quả sự thay đổi giá trị OD của các mẫu nước uống dinh dưỡng chùm ngây theo thời gian
tương ứng với các nồng độ Xanthan Gum được thể hiện ở đồ thị sau.
độ truyền
80 0,1%
75
70 0,15%
65
60 0,2%
55
50 0,3% 0,25%
45
40 0,2% 0,3%
35 0,1%
30
Đ/C
1 3 5 7 10 15
ngày ngày ngày ngày ngày ngày
ngày khảo sát
Chỉ số OD biểu đạt độ truyền suốt của nước uống dinh dưỡng từ cây chùm ngây, có ý nghĩa
cho biết mức độ lơ lửng của dịch cốt có trong sản phẩm. Tuy nhiên, sự chênh lệch OD càng
nhỏ thì hiệu quả ổn định của phụ gia sử dụng càng cao. Mặc khác,
cần đảm bảo được độ nhớt của sản phẩm cho phù hợp, không làm ảnh hưởng đến giá trị cảm
quan của sản phẩm.
Kết quả sự chênh lệch OD giữa ngày đầu và ngày thứ 15 cùng với độ nhớt của sản
phẩm ở các nồng độ Xanthan Gum khác nhau được thể hiện ở đồ thị 1.2 và 1.3.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 clxxxix
sự chênh lệch OD
50
sự chên lệch OD
42.4 40
30
1.9
2.1 20
2.3 5.4
0,3% 7.8 10
0,25% 0
0,2%
0,15% sự chênh lệch OD
0,1%
Đ/C
nồng độ Xanthan Gum
40
35
30
giá trị độ nhớt
25
20
15
10
5
0
0,1% 0,15% 0,2% 0,25% 0,3%
nồng độ Xanthan Gum
Nhận xét:
- Khi sử dụng nồng độ Xanthan Gum càng tăng thì độ nhớt của sản phẩm càng tăng.
- ở nồng độ 0.3% OD thấp nhất chứng tỏ tại nồng độ này hiệu quả ổn định trạng thái
sản phẩm là tốt nhất.
- tất cả các mẫu sản phẩm sau 15 ngày khảo sát hầu như không xuất hiện hiện tượng
tách lớp ở các nồng độ Xanthan Gum khác nhau.
2. Nghiên cứu ảnh hưởng của sự kết hợp Xanthan Gum đến quá trình
trạng thái của sản phẩm.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxc
Qua khảo sát sơ bộ chúng tôi chọn 2 yếu tố là:
- Z1: nồng độ Xanthan Gum, %.
- Z2: nồng độ CMC, %.
Ta thu được ma trận thực nghiệm với các biến mã như sau:
Số TN X0 X1 X2 Y1 ( OD) Y2 ( độ nhớt)
1 1 1 1 0.9 10.87
2 1 -1 1 2.9 3.83
3 1 1 -1 1.3 4.99
4 1 -1 -1 5.8 1.67
Kết quả sự chênh lệch OD giữa ngày đầu và ngày thứ 15 cùng với độ nhớt của sản phẩm ở
các nồng độ kết hợp giữa Xanthan Gum – CMC khác nhau được thể hiện ở đồ thị 1.2 và 1.3.
độ truyền suốt
80
75
70
65
60 0.15X-0.15CMC
55
50
45 0.05X -0.15CMC
40
35 0.15X-0.05CMC
30 0.05X-0.05CMC
1 ngày
3 ngày
0.15X-0.15CMC 0.05X-0.05CMC
5 ngày
7 ngày
10 ngày
15 ngày
Đ/C
ngày khảo sát
60
sự chêch lệch OD
40 42.4
20
0
0.9
2.9
1.3
5.8
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxci
12
10.87
10
8
độ nhớt
6
4.99
4 3.83
2 1.67
0.71 độ nhớt
0
nồng độ chất ổn định
Từ số liệu thực nghiệm, áp dụng các công thức trên ta xác định được giá trị b0, b1, b2, b12 được
tính theo số liệu thực nghiệm hàm mục tiêu đợ chêch lệch giá trị OD (Y).
Tính hệ số b: theo phần đánh giá ở thí nghiệm trên ta có:
b0 b1 b2 b12
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxcii
2.725 -1.625 -0.825 0.625
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Kết quả các thí nghiệm ở tâm:
Bảng 1.4 kết quả thí nghiệm ở tâm
N0 𝑌𝑢0 ̅̅̅0
𝑌 ̅̅̅0
𝑌𝑢0 − 𝑌 ̅̅̅0 )2
(𝑌𝑢0 − 𝑌 ̅̅̅0 )2
∑(𝑌𝑢0 − 𝑌
1 2.0 - 0.367 0.135
2 2.7 2.367 0.333 0.11 0.25
3 2.4 0.033 0.001
0.25
Phương sai tái hiện: S th2 0.125
2
Trong đó m là số thí nghiệm ở tâm phương án (m = 3)
S th
Sbj: Độ lệch quân phương của hệ số thứ j, với: S bj 0.176 Tính các hệ số
N
tjtheo công thức (**),thu được kết quả sau:
t0 t1 t2 t12
15.52 9.25 4.70 3.60
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxciii
Tra bảng tiêu chuẩn Student ta có tp(fth) = t0,05(2) = 4,3
Ta nhận thấy, các hệ số t0, t1, t2 đều lớn hơn t0,05(2) = 4,3 còn t12 lại nhỏ hơn, do đó chỉ
có các hệ số b0, b1, b2 có nghĩa và phương trình hồi qui hoàn chỉnh như sau:
𝑌̂1 = 2.725 – 1.625 x1 – 0.825x2
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
STT 𝑌̂1 Yi Yi − 𝑌̂1 (Yi − 𝑌̂1 )2
1
0.28 0.90 0.625 0.3906250
2
3.53 2.90 -0.625 0.3906250
3
1.93 1.30 -0.625 0.3906250
4
5.18 5.80 0.625 0.3906250
1
2
Phương sai dư: 𝑆𝑑ư = ∑𝑁 ̂ 2
𝑖=1(Yi − 𝑌1 ) =1.56
𝑁−𝐿
(N là số thí nghiệm, L là hệ số ý nghĩa)
Tiêu chuẩn Fisher:
2
𝑆𝑑ư
F= 2 = 12.48
𝑆𝑡ℎ
Tra bảng phân vị phân bố Fisher với P=0,05, f1 = N-L=1, f2 = N0 – 1 = 2, ta có: F1-p =
F0,95 (1,2) = 19.2
Vì F < F0,095(1,2) nên phương trình hồi qui tương thích với thực nghiệm.
3. Nghiên cứu ảnh hưởng của sự kết hợp Xanthan Gum- pectin đến
quá trình trạng thái của sản phẩm.
Qua khảo sát sơ bộ chúng tôi chọn 2 yếu tố là:
- Z1: nồng độ Xanthan Gum, %.
- Z2: nồng độ Pectin, %.
Ta thu được ma trận thực nghiệm với các biến mã như sau:
Số TN X0 X1 X2 Y1 ( OD) Y2 (độ nhớt)
1 1 1 1 2.5 11.02
2 1 -1 1 6.9 4.92
3 1 1 -1 4.7 5.17
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxciv
4 1 -1 -1 8.2 1.91
Kết quả sự chênh lệch OD giữa ngày đầu và ngày thứ 15 cùng với độ nhớt của sản phẩm ở
các nồng độ kết hợp giữa Xanthan Gum – Pectin khác nhau được thể hiện ở đồ thị 1.2 và 1.3.
độ truyền suốt (OD)
80
75
70
65
60 0.15X-0.15Pectin
55
50 0.05X -0.15Pectin
45
40 0.15X-0.05Pectin
35 Đ/C
30
0.15X-0.05Pectin 0.05X-0.05Pectin
1 ngày
3 ngày
0.15X-0.15Pectin
5 ngày
7 ngày
Đ/C
10 ngày
15 ngày
ngày khảo sát
45
40
35
sự chêch lệch OD
30
25
20
15
10
12
11.02 5
10 0
8
độ nhớt
6
4.92 5.17
4
2 1.91 độ nhớt
0.71
0
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxcv
nồng độ chất ổn định
Từ số liệu thực nghiệm, áp dụng các công thức trên ta xác định được giá trị b0, b1, b2, b12 được
tính theo số liệu thực nghiệm hàm mục tiêu đợ chêch lệch giá trị OD (Y).
Tính hệ số b: theo phần đánh giá ở thí nghiệm trên ta có:
b0 b1 b2 b12
5.575 -1.975 -0.875 -0.225
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Kết quả các thí nghiệm ở tâm:
Bảng 1.4 kết quả thí nghiệm ở tâm
N0 𝑌𝑢0 ̅̅̅0
𝑌 𝑌𝑢0 − 𝑌 ̅̅̅0 )2
̅̅̅0 (𝑌𝑢0 − 𝑌 ̅̅̅0 )2
∑(𝑌𝑢0 − 𝑌
1 5.1 0.04 0.0016
2 5.4 5.06 0.34 0.1156 0.25
3 4.7 -0.36 0.1296
0.25
S th2 0.125
Phương sai tái hiện: 2
Trong đó m là số thí nghiệm ở tâm phương án (m = 3)
S th
S bj 0.176
Sbj: Độ lệch quân phương của hệ số thứ j, với: N Tính các hệ số tjtheo công
thức (**),thu được kết quả sau:
t0 t1 t2 t12
31.75 11.25 4.98 1.28
Tra bảng tiêu chuẩn Student ta có tp(fth) = t0,05(2) = 4,3
Ta nhận thấy, các hệ số t0, t1, t2 đều lớn hơn t0,05(2) = 4,3 còn t12 lại nhỏ hơn, do đó chỉ có các
hệ số b0, b1, b2 có nghĩa và phương trình hồi qui hoàn chỉnh như sau:
𝑌̂1 = 5.575 – 1.975x1 – 0.875x2
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxcvi
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
STT 𝑌̂1 Yi Yi − 𝑌̂1 (Yi − 𝑌̂1 )2
1 2.73 2.50 -0.225 0.0506250
2 6.68 6.90 0.225 0.0506250
3 4.48 4.70 0.225 0.0506250
4 8.43 8.20 -0.225 0.0506250
1
Phương sai dư: 𝑆𝑑ư2
= ∑𝑁 (Y − 𝑌̂1 )2 =0.1025
𝑁−𝐿 𝑖=1 i
(N là số thí nghiệm, L là hệ số ý nghĩa)
Tiêu chuẩn Fisher:
2
𝑆𝑑ư
F= 2 = 0.82
𝑆𝑡ℎ
Tra bảng phân vị phân bố Fisher với P=0,05, f1 = N-L=1, f2 = N0 – 1 = 2, ta có: F1-p = F0,95
(1,2) = 19.2
Vì F < F0,095(1,2) nên phương trình hồi qui tương thích với thực nghiệm.
4. Nghiên cứu ảnh hưởng của sự kết hợp các yếu tố đến quá trình trạng thái của sản phẩm
Qua khảo sát sơ bộ ở trên khi kết hợp 3 chất ổn định chúng tôi nhận thấy sự kết hợp giữa
CMC - Car- Xanthan Gum là tối ưu nhất vì thế chúng tôi khảo sát lại sự kết hợp của 3 chất
này với khoảng giá trị chúng tôi đã thu hẹp lại.
- Z1: nồng độ CMC, %.
- Z2: nồng độ Carageenan, %.
- Z3: nồng độ Xanthan Gum. %.
Ta thu được ma trận thực nghiệm với các biến mã như sau:
Số TN X0 X1 X2 X3 Y1 (OD) Y2 ( độ nhớt)
1 1 1 1 1 2.0 8.58
2 1 -1 -1 1 4.4 3.98
3 1 1 -1 1 2.1 4.30
4 1 -1 1 1 2.3 10.95
5 1 1 1 -1 3.9 5.68
6 1 -1 -1 -1 9.7 1.91
7 1 1 -1 -1 5.2 3.31
8 1 -1 1 -1 6.1 2.18
Chọn phương trình hồi qui (*), các hệ số b1, b2, b3, b12 , b13, b23 được tính theo số liệu
thực nghiệm hàm mục tiêu sự chênh lệch giá trị OD.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxcvii
Tính hệ số b:
b0 b1 b2 b3 b12 b13 b23
4.4625 -1.625 -0.8875 -1.6725 0.5375 0.5125 0.3375
Kiểm định mức ý nghĩa của các hệ số b trong phương trình (*):
Để tính phương sai tái hiện, tiến hành thêm 3 thí nghiệm ở tâm.
Kết quả các thí nghiệm ở tâm:
N0 𝑌𝑢0 ̅̅̅0
𝑌 ̅̅̅0
𝑌𝑢0 − 𝑌 ̅̅̅0 )2
(𝑌𝑢0 − 𝑌 ̅̅̅0 )2
∑(𝑌𝑢0 − 𝑌
1 3.1 0.033 0.001
2 2.7 3.067 -0.367 0.135 0.246
3 3.4 0.333 0.110
2 1 ̅̅̅0 2
Phương sai tái hiện: 𝑆𝑡ℎ = ∑𝑚 0
𝑢=1(𝑌𝑢 − 𝑌 ) =0.123
𝑚−1
𝑆𝑡ℎ
Độ lệch quân phương của hệ số thứ j: 𝑆𝑏𝑗 = =0.124
√𝑁
Tính các hệ số tj thu được kết quả sau:
t0 t1 t2 t3 t12 t13 t23
35.94 9.36 7.15 14.19 4.33 4.13 2.72
Tra bảng tiêu chuẩn Stdent ta có tp(fth) = t0,05(2) = 4,3
So sánh tj với tp(f) . Trong đó: - tp(f) là chuẩn student tra bảng ứng với xác suất tin cậy
p và bậc tự do f, f = N0 – 1.
Như vậy, các hệ số t0, t1, t2, t3,t12 đều lớn hơn t0,05(2) = 4,3 nên các hệ số này đều có
nghĩa.
Phương trình hồi qui có dạng như sau:
𝑌̂2 = 4.4625- 1.1625 x1- 0.8875x2 - 1.7625x3 + 0.5375 x12
Kiểm định sự phù hợp của phương trình hồi qui với thực nghiệm:
STT 𝑌̂2 Yi Yi − 𝑌̂2 (Yi − 𝑌̂2 )2
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxcviii
1
1.1875 2 0.8125 0.660156
2
4.75 4.4 -0.35 0.1225
3
2.425 2.1 -0.325 0.105625
4
2.975 2.3 -0.675 0.455625
5
4.175 3.9 -0.275 0.075625
6
8.275 9.7 1.425 2.030625
7
5.95 5.2 -0.75 0.5625
8
6.5 6.1 -0.4 0.16
1 4.17
2
Phương sai dư:𝑆𝑑ư = ∑𝑁
𝑖=1(Yi − 𝑌̂2 )2 = = 1.39
𝑁−𝐿 85
Tiêu chuẩn Fisher:
2 1.39
𝑆𝑑ư
F= 2 = 11.30
𝑆𝑡ℎ 0.123
Tra bảng phân vị phân bố Fisher với P=0,05, f1 = N-L=3, f2 = N0 – 1 = 2, ta có: F1-p =
F0,95 (3,2) = 19.2
Vì F >F0,95(3,2) nên phương trình hồi qui tương thích với thực nghiệm.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cxcix
1.5.1.
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cc
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 cci
SVTH: Đào Ngọc Thủy Tiên – Mssv: 0853010931 ccii
You might also like
- Food - Additives (Phan The Dong)Document235 pagesFood - Additives (Phan The Dong)174711111No ratings yet
- Bài Giảng Môn Công Nghệ Đồ Hộp Thực PhẩmDocument132 pagesBài Giảng Môn Công Nghệ Đồ Hộp Thực PhẩmLong Vũ NguyễnNo ratings yet
- FSMA Allergen Management Workshop 30.06.2019 PDFDocument63 pagesFSMA Allergen Management Workshop 30.06.2019 PDFTrang Xuân ThùyNo ratings yet
- Lecture notes. QT Chất lượng. Ver 2021Document100 pagesLecture notes. QT Chất lượng. Ver 2021Nguyễn Nhật Phương ĐàiNo ratings yet
- Ke Hoach Kiem Soat Chat Luong Binh 20l ChuanDocument50 pagesKe Hoach Kiem Soat Chat Luong Binh 20l ChuanNhạc BáNo ratings yet
- Iso 9100 VietnamDocument40 pagesIso 9100 VietnamHoang TanNo ratings yet
- Bài 2 Các hoạt động quản lý chất lượng thực phẩmDocument124 pagesBài 2 Các hoạt động quản lý chất lượng thực phẩmNguyen Thi Huyen TrangNo ratings yet
- Ky Thuat Phoi Tron Thuc An Chan Nuoi PDFDocument24 pagesKy Thuat Phoi Tron Thuc An Chan Nuoi PDFNguyenNgocNo ratings yet
- TLHV KN Xay Dung Quy Trinh Chuan 2023 PDFDocument26 pagesTLHV KN Xay Dung Quy Trinh Chuan 2023 PDFHuy Nguyen DucNo ratings yet
- Cay NgheDocument40 pagesCay NgheNguyen JamesNo ratings yet
- công nghệ sản xuất tinh bột sắnDocument52 pagescông nghệ sản xuất tinh bột sắnĐắc ThiệnNo ratings yet
- Chương 5Document125 pagesChương 52 VinhthanhdraoNo ratings yet
- Chuong 5 To ChucDocument70 pagesChuong 5 To ChucmonkeyNo ratings yet
- BT8. Thong Tin Bang Van BanDocument3 pagesBT8. Thong Tin Bang Van BanTiên NguyễnNo ratings yet
- BPM - Chuong 3 Process Analysis Hide SlideDocument215 pagesBPM - Chuong 3 Process Analysis Hide SlideThương LưuNo ratings yet
- Halal List Tv1Document17 pagesHalal List Tv1Gấu NgốcNo ratings yet
- Uvtn - CV HandbookDocument48 pagesUvtn - CV HandbookMẬP CÁNo ratings yet
- Ngữ Pháp Tiếng Nhật MinnanoDocument148 pagesNgữ Pháp Tiếng Nhật MinnanoHiếu Vũ MinhNo ratings yet
- Ung Dung Ban Do Tu Duy Trong Hoc Tap - 1980 BooksDocument98 pagesUng Dung Ban Do Tu Duy Trong Hoc Tap - 1980 BookstoansanNo ratings yet
- Traceability in Food 1578518702Document89 pagesTraceability in Food 1578518702huong2286No ratings yet
- Đệm Hát Căn Bản Tập 2+3Document17 pagesĐệm Hát Căn Bản Tập 2+3Tuan DzungNo ratings yet
- Checklist Danh Gia Noi Bo 9001Document18 pagesChecklist Danh Gia Noi Bo 9001Như Luân LêNo ratings yet
- So Tay An Toan Thuc Pham Danh Cho Cac Co So Ho San Xuat Kinh Doanh Thuc PhamDocument216 pagesSo Tay An Toan Thuc Pham Danh Cho Cac Co So Ho San Xuat Kinh Doanh Thuc PhamHoàng Long Trường ThịnhNo ratings yet
- Nghiên Cứu, Xác Định Hàm Lượng Vitamin C Trong Lá Cây Chùm Ngây Bằng Phương Pháp Von Ampe Hòa Tan Chu Thị OanhDocument100 pagesNghiên Cứu, Xác Định Hàm Lượng Vitamin C Trong Lá Cây Chùm Ngây Bằng Phương Pháp Von Ampe Hòa Tan Chu Thị Oanhle100% (1)
- CHƯƠNG 3 - ĐÁNH GIÁ VÀ LỰA CHỌN NHÀ CUNG CẤPDocument41 pagesCHƯƠNG 3 - ĐÁNH GIÁ VÀ LỰA CHỌN NHÀ CUNG CẤPTrần Lê Gia HânNo ratings yet
- BM-QT-10-07 Checklist ISO 9K (Theo Thứ Tự)Document27 pagesBM-QT-10-07 Checklist ISO 9K (Theo Thứ Tự)Đại Hữu Tuấn MaiNo ratings yet
- TCVN Iso 9001 2015 PDFDocument76 pagesTCVN Iso 9001 2015 PDFThanh DêyNo ratings yet
- Trà Xanh Đóng ChaiDocument15 pagesTrà Xanh Đóng ChaiNguyễn Bùi Tuyết TrâmNo ratings yet
- Kna - QaqcDocument103 pagesKna - QaqcKiệt Lê TuấnNo ratings yet
- Công Nghệ Chế Biến Nước Giải Khát Và Rau QuảDocument615 pagesCông Nghệ Chế Biến Nước Giải Khát Và Rau QuảTuyền Nguyễn Trần ThanhNo ratings yet
- Tai Lieu Huong Dan Chi Tiet Ve Danh Gia Rui Ro 0 Moi NguyDocument57 pagesTai Lieu Huong Dan Chi Tiet Ve Danh Gia Rui Ro 0 Moi NguyDang Hoang DuNo ratings yet
- KẾ HOẠCH HACCP SẢN PHẨM MÌ ĂN LIỀNDocument2 pagesKẾ HOẠCH HACCP SẢN PHẨM MÌ ĂN LIỀNHiếu NguyễnNo ratings yet
- Xây Dựng HACCP Kiểm Soát Quy Trình Sx Bún KhôDocument38 pagesXây Dựng HACCP Kiểm Soát Quy Trình Sx Bún KhôLuận HàNo ratings yet
- HACCP Sa Chua AnDocument12 pagesHACCP Sa Chua Annhi tranNo ratings yet
- Hinh Thanh y Tuong KDDocument72 pagesHinh Thanh y Tuong KDNguyễn Trọng Luận PH 1 6 6 7 4No ratings yet
- 4a PDFDocument107 pages4a PDF24 Yến Nhi 23 Đông Nhi 6HNo ratings yet
- DANH SÁCH CÁC CHẤT HARAM VÀ HALALDocument31 pagesDANH SÁCH CÁC CHẤT HARAM VÀ HALALChanlyislam83% (6)
- Chương 4Document42 pagesChương 42 VinhthanhdraoNo ratings yet
- Qui Pham San Xuat GMPDocument54 pagesQui Pham San Xuat GMPTrúcNo ratings yet
- Giáo Trình Guitar Đêm Hát K20 Hoàn ThànhDocument44 pagesGiáo Trình Guitar Đêm Hát K20 Hoàn Thànhnguyenminhhien2122No ratings yet
- Chương 4 Công Cụ Kiểm Soát Chất LượngDocument74 pagesChương 4 Công Cụ Kiểm Soát Chất LượngTín ĐứcNo ratings yet
- Khoi Su KD-Ke Hoach KDDocument40 pagesKhoi Su KD-Ke Hoach KDNguyễn Trọng Luận PH 1 6 6 7 4No ratings yet
- Quy Trình Lên Men Rư UDocument22 pagesQuy Trình Lên Men Rư UNam NguyenHoang100% (1)
- 16dtpa3 - 1 - BidricoDocument107 pages16dtpa3 - 1 - BidricoYến Oanh BùiNo ratings yet
- QT Bảo Trì, Sửa Chữa Thiết Bị, Cơ Sở Hạ TầngDocument5 pagesQT Bảo Trì, Sửa Chữa Thiết Bị, Cơ Sở Hạ TầngDungNo ratings yet
- Goc - GT Modun 04 - SX Thuc An Chan NuoiDocument141 pagesGoc - GT Modun 04 - SX Thuc An Chan NuoiPhạm ChúcNo ratings yet
- Đ Án HACCp 30.7.2022Document319 pagesĐ Án HACCp 30.7.2022Tấn ThànhNo ratings yet
- Chương Quality ManagementDocument87 pagesChương Quality ManagementNgọc HânNo ratings yet
- Recall TraceabilityDocument55 pagesRecall TraceabilityHoàng Nguyễn VănNo ratings yet
- FSSC 22000 V5.1 - Haccp 2020Document87 pagesFSSC 22000 V5.1 - Haccp 2020Thao VuongNo ratings yet
- R&D SpecialistDocument134 pagesR&D SpecialistHoàng DiệpNo ratings yet
- Phân Tích Mối Quan Hệ Chi Phí - Khối Lượng - Lợi NhuậnDocument25 pagesPhân Tích Mối Quan Hệ Chi Phí - Khối Lượng - Lợi NhuậnThiên LongNo ratings yet
- Chùm NgâyDocument19 pagesChùm NgâyChinh VuNo ratings yet
- Mẫu khóa luậnDocument84 pagesMẫu khóa luậnKiệt LêNo ratings yet
- Bộ câu trả lời Đào tạo Sản phẩmDocument19 pagesBộ câu trả lời Đào tạo Sản phẩmHien NguyenNo ratings yet
- BAOCAODocument48 pagesBAOCAOVăn minh Lộc NguyễnNo ratings yet
- Báo cáo thí nghiệm thực phẩm 2Document27 pagesBáo cáo thí nghiệm thực phẩm 2Duong le DaiNo ratings yet
- NHÓM 1 TIỂU LUẬN HẠT ĐẬU NÀNH VÀ VAI TRÒ ĐỐI VỚI SỨC KHỎE CON NGƯỜIDocument21 pagesNHÓM 1 TIỂU LUẬN HẠT ĐẬU NÀNH VÀ VAI TRÒ ĐỐI VỚI SỨC KHỎE CON NGƯỜIQuoc Anh PhamNo ratings yet
- HOẠT CHẤT CÓ HOẠT TÍNH SINH HỌC VÀ DƯỢC TÍNH CỦA NẤM BÀO NGƯDocument14 pagesHOẠT CHẤT CÓ HOẠT TÍNH SINH HỌC VÀ DƯỢC TÍNH CỦA NẤM BÀO NGƯLe Van KiemNo ratings yet