Professional Documents
Culture Documents
أهم ما جاء في 4
Uploaded by
zaki48Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
أهم ما جاء في 4
Uploaded by
zaki48Copyright:
Available Formats
األستاذ :بوزيان زكرياء السنة الثالثة تقني رياضي – علوم تجريبية ثانوية العقيد عثمان
المجـــال :التطورات الرتيبة
الوحدة الرابعة :تطور جملة كيميائية نحو حالة التوازن
المدة 2 :سا الموضوع :المحاليل المائية
.1مكتسبات قبلية:
.1-1تعريف برونشتد لألحماض واألسس:
-الحمض :هو كل فرد كيميائي ،شارديا أو جزيئيا كان ،قادر على التخلي عن بروتون 𝐻+أو أكثر.
مثال𝐶𝐻3 𝐶𝑂𝑂𝐻 → 𝐶𝐻3 𝐶𝑂𝑂− + 𝐻+ :
-األساس :هو كل فرد كيميائي ،شارديا أو جزيئيا كان ،قادر على تثبيت بروتون 𝐻+أو أكثر.
مثال𝑁𝐻3 + 𝐻 + → 𝑁𝐻4 + :
.2-1الثنائية (أساس/حمض):
في كل تفاعل يتخلى فيه حمض 𝐻𝐴 عن بروتون ،𝐻 +نحصل على أساس مرافق 𝐴−وفق املعادلة𝐴𝐻 → 𝐻+ + 𝐴− : -
في كل تفاعل يثبت فيه أساس 𝐴−بروتون ،𝐻 +نحصل على حمض مرافق 𝐻𝐴وفق املعادلة𝐴− + 𝐻 + → 𝐴𝐻 : -
تسمى الثنائية ) (𝐴𝐻/𝐴−بالثنائية حمض – أساس. -
.3-1التفاعل حمض أساس:
تتدخل في التفاعل حمض أساس ثنائيان ) (𝐴𝐻1 /𝐴1و ) (𝐴𝐻2 /𝐴2بحيث:
− −
- +
AH 1 = A 1 + H
- +
A2 + H = AH 2
- -
AH 1 + A 2 = A 1 + AH 2
pH .2املحاليل املائية:
.1-2مفهوم الـ 𝑯𝒑:
تتعلق الخواص الحمضية أو األساسية ملحلول مائي بتركيزه بشوارد الهيدرونيوم 𝐻3 𝑂+والذي يمكن أن يتغير ضمن مجال واسع يتراوح
بين 𝐿 1 𝑚𝑜𝑙/إلى 𝐿.10−14 𝑚𝑜𝑙/
من أجل تسهيل دراسة املحاليل املائية من الناحية تم إدخال سلم لوغاريتمي للتعبير عن العالقة بين الـ pHوتركيز املحلول بشوارد
الهيدرونيوم.
من أجل املحاليل املائية املمددة ،يعرف 𝐻𝑝 املحلول بالعالقة التالية𝑝𝐻 = − log[𝐻3𝑂 + ] :
حيث [𝐻3 𝑂+] :هو التركيز املولي بشوارد الهيدرونيوم مقدر بـ 𝐿.𝑚𝑜𝑙/
.2-2قياس الـ 𝑯𝒑:
-يمكن الحصول على قيمة تقريبية لـ 𝐻𝑝 محلول باستعمال ورق الـ 𝐻𝑝 حيث تجرى مطابقة لون الورقة بعد غمسها في املحلول مع
األلوان العيارية لعلبة ورق الـ 𝐻𝑝.
-بخصوص القياسات الدقيقة لقيمة الـ 𝐻𝑝 ،يتطلب استعمال جهاز قياس الـ 𝐻𝑝.
.3محلول حمض ي ومحلول أساس ي:
.1-3الحمض القوي والحمض الضعيف:
نقول عن الحمض 𝐻𝐴 تركيزه 𝑎𝐶 أنه حمض قوي إذا تشرد في املاء كليا بحيث عند التوازن يكون[𝐴𝐻]0 = 𝐶𝑎 = [𝐻3 𝑂+ ] : -
+ −
𝐴 𝐴𝐻 + 𝐻2 𝑂 → 𝐻3 𝑂 +
1
www.dzphysique.com اﻟﻤﻮﻗﻊ اﻟﺮﺳﻤﻲ ﻟﻸﺳﺘﺎذ ﺑﻮزﻳﺎن زﻛﺮﻳﺎء
نقول عن الحمض 𝐻𝐴 تركيزه 𝑎𝐶 أنه حمض ضعيف إذا تشرد جزئيا في املاء بحيث عند التوازن يكون[𝐴𝐻]0 = 𝐶𝑎 > [𝐻3 𝑂+ ] : -
+ −
𝐴 𝐴𝐻 + 𝐻2 𝑂 = 𝐻3 𝑂 +
.2-3األساس القوي واألساس الضعيف:
نقول عن أساس 𝐵 أنه أساس قوي إذا تشرد في املاء كليا بحيث عند التوازن يكون[𝐵]0 = [𝑂𝐻− ] : -
+ −
𝐻𝑂 𝐵 + 𝐻2 𝑂 → 𝐵𝐻 +
نقول عن أساس 𝐵 أنه أساس ضعيف إذا تشرد جزئيا في املاء بحيث عند التوازن يكون[𝐵]0 > [𝑂𝐻− ] : -
𝐵 + 𝐻2 𝑂 = 𝐵𝐻 + + 𝑂𝐻 −
2
www.dzphysique.com اﻟﻤﻮﻗﻊ اﻟﺮﺳﻤﻲ ﻟﻸﺳﺘﺎذ ﺑﻮزﻳﺎن زﻛﺮﻳﺎء
األستاذ :بوزيان زكرياء السنة الثالثة تقني رياضي – علوم تجريبية ثانوية العقيد عثمان
المجـــال :التطورات الرتيبة
الوحدة الرابعة :تطور جملة كيميائية نحو حالة التوازن
المدة 4 :سا الموضوع :تطور جملة كيميائية إلى حالة توازن
.4نسبة التقدم:
في اللحظة 𝑡 من التفاعل الكيميائي أين يكون التقدم 𝑥 ،تعرف نسبة التقدم في هذه اللحظة والتي يرمز لها بـ .τ
𝑥
=τ
𝑥𝑎𝑚𝑥
في نهاية التفاعل تكون عبارة نسبة التقدم النهائي 𝑓𝑥 كما يلي:
𝑓𝑥
= 𝑓τ
𝑥𝑎𝑚𝑥
بحيث 𝜏 محصور بين 0و .1
.5التفاعل التام وغيرالتام (محدود):
.1-2تفاعل تام:
نشاط :01
نحضر محلول لكلور الهيدروجين بحل 𝐋𝐦 𝟎𝟒𝟐 من غاز الهيدروجين في 𝑳𝟏 من املاء املقطر ،فنتحصل على محلول ذو تركيز
𝑳 𝟎, 𝟎𝟏 𝒎𝒐𝒍/نقيس 𝐇𝐩 املحلول الناتج فنجد 𝟎 .𝐩𝐇 = 𝟐,
نأخذ في شروط التجربة الحجم املولي 𝒍𝒐𝒎.𝑽𝑴 = 𝟐𝟒 𝑳/
.1اكتب معادلة التفاعل املنمذج النحالل الحمض 𝐥𝐂𝐇 في املاء.
-معادلة التفاعل:
𝐻𝐶𝑙 + 𝐻2 𝑂 = 𝐻3 𝑂+ + 𝐶𝑙 −
.2مثل جدول تقدم هذا التفاعل ،ثم أوجد قيمة التقدم األعظمي 𝒙𝒂𝒎𝒙.
جدول تقدم التفاعل: -
الحالة التقدم HCl + = H 2O H 3O
+
+ Cl
-
ابتدائية 0 10-2 0 0
بوفرة
وسطية x 10-2-x x x
نهائية xf 10-2-xf xf xf
باعتبار التفاعل تام لدينا:
−2
10 − 𝑥𝑚𝑎𝑥 = 0
ومنه:
𝑙𝑜𝑚 𝑥𝑚𝑎𝑥 = 10−2
.3اوجد مقدارالتقدم النهائي 𝒇𝒙 ،وكذا نسبة التقدم النهائي.
-مقدار التقدم النهائي 𝑓𝑥:
نعلم أن:
𝑓] 𝑝𝐻 = − log[𝐻3 𝑂+
ومنه:
𝑓] [𝐻3 𝑂+ = 10 𝐻𝑝− −2
𝐿= 10 𝑚𝑜𝑙/
من جدول التقدم:
𝑓𝑥
= 𝑓] [𝐻3 𝑂+
𝑉
إذن:
3
www.dzphysique.com اﻟﻤﻮﻗﻊ اﻟﺮﺳﻤﻲ ﻟﻸﺳﺘﺎذ ﺑﻮزﻳﺎن زﻛﺮﻳﺎء
𝑙𝑜𝑚 𝑥𝑓 = 𝑉. [𝐻3 𝑂+ ]𝑓 = 10−2
ومنه:
𝒍𝒐𝒎 𝟐𝒙𝒇 = 𝟏𝟎−
حساب نسبة التقدم النهائي: -
𝑓𝑥 10−2
= 𝑓τ = =1
𝑥𝑎𝑚𝑥 10−2
ومنه:
𝟏 = 𝒇𝛕
.4إذا علمت أن كلور الهيدروجين هو حمض قوي وأن انحالله في املاء تام ،ماذا يمكن قوله في هذا النوع من التفاعالت عن
التقدم النهائي 𝒇𝒙 والتقدم األعظمي 𝒙𝒂𝒎𝒙 من جهة ونسبة التقدم النهائي 𝒇𝝉 من حهة أخرى.
-نستنتج في التفاعل التام يكون:
𝟏 = 𝒇𝛕 𝒙𝒂𝒎𝒙 = 𝒇𝒙
.2-2تفاعل غيرتام (محدود):
نشاط :02
حضرنا محلول حمض اإليثانويك 𝐇𝐎𝐎𝐂 𝟑𝐇𝐂تركيزه املولي 𝑳 𝑪 = 𝟏𝟎−𝟑 𝒎𝒐𝒍/وحجمه 𝐋𝐦 𝟎𝟎𝟏 = 𝐕 وعندما قمنا بقياس
𝐇𝐩 املحلول الناتج عند الدرجة 𝐂 𝟐𝟓°وجدنا 𝟗 .𝐩𝐇 = 𝟑,
.1أكتب معادلة التفاعل املنمذج النحالل حمض اإليثانويك في املاء.
-معادلة التفاعل:
𝐶𝐻3 𝐶𝑂𝑂𝐻 + 𝐻2 𝑂 = 𝐶𝐻3 𝐶𝑂𝑂− + 𝐻3 𝑂+
.2مثل جدول تقدم هذا التفاعل ،ثم أوجد قيمة التقدم األعظمي 𝒙𝒂𝒎𝒙.
-جدول تقدم التفاعل:
الحالة التقدم CH3COOH + H 2O = CH 3COO + H 3O
- +
ابتدائية 0 10-4 0 0
بوفرة
وسطية x 10-4-x x x
نهائية xf 10-4-xf xf xf
باعتبار التفاعل تام لدينا:
−4
10 − 𝑥𝑚𝑎𝑥 = 0
ومنه:
𝒍𝒐𝒎 𝟒𝒙𝒎𝒂𝒙 = 𝟏𝟎−
.3اوجد مقدارالتقدم النهائي 𝒇𝒙 ،وكذا نسبة التقدم النهائي.
-مقدار التقدم النهائي 𝑓𝑥:
نعلم أن:
𝑓] 𝑝𝐻 = − log[𝐻3 𝑂+
ومنه:
𝑓] [𝐻3 𝑂+ = 10 𝐻𝑝−
𝐿= 1,25 × 10 𝑚𝑜𝑙/ −4
من جدول التقدم:
𝑓𝑥
= 𝑓] [𝐻3 𝑂+
𝑉
إذن:
𝑙𝑜𝑚 𝑥𝑓 = 𝑉. [𝐻3 𝑂+ ]𝑓 = 0,1 × 1,25 × 10−4
4
www.dzphysique.com اﻟﻤﻮﻗﻊ اﻟﺮﺳﻤﻲ ﻟﻸﺳﺘﺎذ ﺑﻮزﻳﺎن زﻛﺮﻳﺎء
ومنه:
𝒍𝒐𝒎 𝟓𝒙𝒇 = 𝟏, 𝟐𝟓 × 𝟏𝟎−
حساب نسبة التقدم النهائي: -
𝑓𝑥 −5
1,25 × 10
= 𝑓τ = = 0,125
𝑥𝑎𝑚𝑥 10−4
ومنه:
𝟓𝟐𝟏 𝛕𝒇 = 𝟎,
.4إذا علمت أن اإليثانويك هو حمض ضعيف وأن انحالله في املاء غير تام ،ماذا يمكن قوله في هذا النوع من التفاعالت عن
التقدم النهائي 𝒇𝒙 والتقدم األعظمي 𝒙𝒂𝒎𝒙 من جهة ونسبة التقدم النهائي 𝒇𝝉 من حهة أخرى.
-نستنتج في التفاعل غير التام يكون:
𝟏 < 𝒇𝛕 𝒙𝒂𝒎𝒙 < 𝒇𝒙
.6مفهوم حالة التوازن لجملة كيميائية:
نشاط :03
حضر بيشرين يحتويان محلول حمض اإليثانويك تركيزه املولي 𝑳 𝑪 = 𝟏𝟎−𝟐 𝒎𝒐𝒍/وذو 𝟒 𝐩𝐇 = 𝟑,مثال.
-نضيف إلى البيشراألول بعض قطرات حمض اإليثانويك ،تجد قيمة الـ 𝐇𝐩 أصبحت 𝟓𝟖 .𝟐,
-نضيف إلى البيشرالثاني بلورات إيثانوات الصوديوم 𝐚𝐍𝐎𝐎𝐂 𝟑𝐇𝐂 ،تجد قيمة الـ𝐇𝐩 أصبحت 𝟔𝟐 .𝟓,
.1ماذا تالحظ؟
-املالحظات:
• عند إضافة الحمض للبيشر األول تنقص قيمة الـ. pH
• عند إضافة امللح للبيشر الثاني تزداد قيمة الـ. pH
.2فسرماذا تالحظ؟
1 -التفسير:
- +
CH3COOH + H2O CH3COO + H3O
2
• عند إضافة الحمض تتناقص قيمة الـ pHدليل على تزايد في قيمة ] ،[H3O+إذن الجملة تطورت في االتجاه )( (1جهة تشكل
.)H3 O+
• عند إضافة امللح تزداد قيمة الـ pHدليل على تناقص في قيمة ] ،[H3O+إذن الجملة تطورت في االتجاه )( (2جهة تشكل
.)CH3 COOH
.3ماذا تسنتج؟
-النتيجة:
• يمكن للتفاعل الكيميائي أن يحدث في االتجاهين .إذن هذا التفاعل هو تفاعل عكوس.
• إذا كان التفاعل عكوس فهو حتما سيكون غير تام ألن األنواع الكيميائية الناتجة تتفاعل بعدما تتشكل ،وهذا ما يجعل
املتفاعالت ال تختفي كليا.
• في الحالة النهائية لتفاعل غير تام ،تكون املتفاعالت والنواتج متواجدة بكميات ثابتة ،فنقول إنها في حالة توازن.
5
www.dzphysique.com اﻟﻤﻮﻗﻊ اﻟﺮﺳﻤﻲ ﻟﻸﺳﺘﺎذ ﺑﻮزﻳﺎن زﻛﺮﻳﺎء
.7كسرالتفاعل:
1
a+ b cC+dD ليكن تفاعل الذي يؤدي إلى توازن كيميائي:
2
كسر التفاعل في أي لحظة 𝑡 يعرف كما يلي:
𝒕𝒅]𝑫[ [𝑪]𝒄𝒕 .
= )𝒕 ( 𝒓 𝑸
𝒕𝒃]𝑩[ [𝑨]𝒂𝒕 .
مثال:01
2-
1
- 2-
] [𝐼 − ]2 . [𝑆2 𝑂6 2−
I2(aq) + )2S2O3 (aq 2I (aq) + )S4O6 (aq = 𝑟𝑄 2
] [𝐼2 ]. [𝑆2 𝑂3 2−
2
مثال:02
1
)CH3COOH(aq) + H2O(l
-
CH3COO (aq) + H3O
+ ] [𝐶𝐻3 𝐶𝑂𝑂− ] . [𝐻3 𝑂 +
)(aq = 𝑟𝑄
2 ]𝐻𝑂𝑂𝐶 [𝐶𝐻3
1 مثال:03
2+ -
)Cu(OH)2(s Cu (aq) + )2OH (aq 𝑄𝑟 = [𝐶𝑢2+ ] . [𝑂𝐻 − ]2
2
مالحظة:
نالحظ بأن:
1
= 𝑄1
𝑄2
بحيث :𝑄1 :كسر التفاعل لالتجاه . 1
:𝑄2كسر التفاعل لالتجاه .2
.8ثابت التوازن 𝑲:
ثابت التوازن 𝐾 لتفاعل معين هو القيمة )𝑞𝑒( 𝑟𝑄 التي يأخذها كسر التفاعل عند درجة حرارة معينة عندما يتم بلوغ حالة التوازن.
𝑓𝑑]𝐷[ [𝐶]𝑐𝑓 .
= )𝑓( 𝑟𝑄 = 𝐾
𝑓𝑏]𝐵[ [𝐴]𝑎𝑓 .
.9تأثيرالحالة االبتدائية لجملة على حالة التوازن:
.1-6النسبة النهائية للتقدم والحالة االبتدائية:
)CH3COOH (aq) + H 2O(l CH3COO
- +
)(aq) + H 3O (aq
لدينا معادلة التفاعل التالية:
عبارة نسبة التقدم النهائي:
𝑓𝑥
= 𝑓τ
𝑥𝑎𝑚𝑥
ومنه:
𝑓] [𝐻3 𝑂+
= 𝑓τ
𝐶
تتعلق نسبة التقدم النهائي لتحول كيميائي معين بالحالة االبتدائية للجملة الكيميائية. -
.2-6النسبة النهائية للتقدم وثابت التوازن الكيميائي:
نعتبر التفاعل بين الحمض 𝐻𝑂𝑂𝐶 𝐶𝐻3و𝑂 𝐻2وفق املعادلة التالية:
- +
)CH3COOH (aq) + H 2O(l CH3COO )(aq) + H 3O (aq
6
www.dzphysique.com اﻟﻤﻮﻗﻊ اﻟﺮﺳﻤﻲ ﻟﻸﺳﺘﺎذ ﺑﻮزﻳﺎن زﻛﺮﻳﺎء
نمثل جدول تقدم التفاعل:
الحالة التقدم CH3COOH + H 2O = CH 3COO + H 3O
- +
ابتدائية 0 C.V 0 0
بوفرة
وسطية x C.V-x x x
نهائية xf C.V-xf xf xf
بحيث𝑥𝑚𝑎𝑥 = 𝐶. 𝑉 :
نعلم أن:
𝑓𝑥
= 𝑓τ
𝑥𝑎𝑚𝑥
ومنه:
𝑥𝑎𝑚𝑥 𝑥𝑓 = τ𝑓 .
إذن:
𝑉 𝑥𝑓 = τ𝑓 . 𝐶.
ونعلم أن عند نهاية التفاعل:
)+
𝑂 𝑛𝑓 (𝐻3 𝑓𝑥 =
إذن:
𝑉 𝑛𝑓 (𝐻3 𝑂+ ) = τ𝑓 . 𝐶.
منه:
)[𝐻3 𝑂 + ] = τ𝑓 . 𝐶 … . (1
ولدينا أيضا:
)[𝐶𝐻3 𝐶𝑂𝑂− ] = τ𝑓 . 𝐶 … . (2
من جدول التقدم لدينا أيضا:
𝑓𝑥 𝑛𝑓 (𝐶𝐻3 𝐶𝑂𝑂𝐻) = 𝐶. 𝑉 −
منه:
𝑉 𝑛𝑓 (𝐶𝐻3 𝐶𝑂𝑂𝐻) = 𝐶. 𝑉 − τ𝑓 . 𝐶.
إذن:
)[𝐶𝐻3 𝐶𝑂𝑂𝐻] = (1 − τ𝑓 ). 𝐶 … . (3
عبارة ثابت التوازن:
𝐶 [𝐶𝐻3 𝐶𝑂𝑂 − ]. [𝐻3 𝑂+ ] τ𝑓 . 𝐶. τ𝑓 .
=𝐾 =
]𝐻𝑂𝑂𝐶 [𝐶𝐻3 𝐶 (1 − τ𝑓 ).
𝐶 τ𝑓 2 .
=𝐾
) 𝑓(1 − τ
كلما كان ثابت التوازن 𝐾 مرتفعا كلما كانت نسبة التقدم النهائي أكبر.
• إذا كام 𝐾 > 104فإنه يمكن اعتبار أن التحول املدروس تام.
7
www.dzphysique.com اﻟﻤﻮﻗﻊ اﻟﺮﺳﻤﻲ ﻟﻸﺳﺘﺎذ ﺑﻮزﻳﺎن زﻛﺮﻳﺎء
األستاذ :بوزيان زكرياء السنة الثالثة تقني رياضي – علوم تجريبية ثانوية العقيد عثمان
المجـــال :التطورات الرتيبة
الوحدة الرابعة :تطور جملة كيميائية نحو حالة التوازن
المدة 2 :سا الموضوع :التحوالت المرفقة بالتفاعل حمض – أساس
.10املحاليل املائية:
.1-1التفكك الذاتي للماء:
يتفكك املاء املقطر ذاتيا إلى شوارد الهيدرونيوم 𝐻3 𝑂+وشوارد الهيدروكسيد 𝑂𝐻−وفق املعادلة التالية:
+ -
)H2O (l) + H 2O (l H3O (aq) + OH )(aq
.2-1الجداء الشاردي للماء:
يلعب املاء دورا مضاعفا حيث يسلك سلوك الحمض وسلوك األساس وذلك باملشاركة في الثنائيتين )𝑂.(𝐻2 𝑂/𝑂𝐻− ) ،(𝐻3 𝑂+ /𝐻2
يؤدي التفكك الذاتي للماء إلى التوازن الكيميائي ،ويمثل ثابت التوازن 𝑒𝐾 الذي يسمى "الجداء الشاردي للماء" املعرف بالعالقة التالية:
] 𝐾𝑒 = [𝐻3 𝑂+ ]. [𝑂𝐻 −
عند درجة حرارة 25°Cلدينا𝐾𝑒 = 10−14 :
.11سلم الـ: pH
تتغير قيمة الـ pHللمحاليل املائية عمليا ضمن املجال ] ،[14 − 0وحسب قيم الـ pHيمكن تصنيف املحاليل املائية إلى ثالثة أصناف:
.1-2املحلول املائي املعتدل:
يكون املحلول املائي معتدال إذا كان:
𝑂 [𝐻3 ]+ ] [𝑂𝐻 −
=
في هذه الحالة ،نكتب الجداء الشاردي للماء بالشكل:
𝐾𝑒 = [𝐻3 𝑂+ ]2
أي:
] −log 𝐾𝑒 = −2 log[𝐻3 𝑂+
إذن:
1
𝑒𝐾𝑝 = 𝐻𝑝
2
𝟕 = 𝑯𝒑
.2-2املحلول املائي الحمض ي:
يكون املحلول املائي حمضيا إذا كان:
] [𝐻3 𝑂+ ] > [𝑂𝐻 −
بضرب طرفي املتراجحة السابقة ] [𝐻3 𝑂+في ينتج:
] [𝐻3 𝑂 + ]2 > [𝐻3 𝑂+ ]. [𝑂𝐻 −
𝑒𝐾 > [𝐻3 𝑂 + ]2
ومنه:
+ ]2
𝑂 −log[𝐻3 𝑒𝐾 < − log
إذن:
1
𝑒𝐾𝑝 < 𝐻𝑝
2
𝟕 < 𝑯𝒑
.3-2املحلول املائي األساس ي:
يكون املحلول املائي أساسيا إذا كان:
] [𝐻3 𝑂+ ] < [𝑂𝐻 −
بضرب طرفي املتراجحة السابقة ] [𝐻3 𝑂+في ينتج:
] [𝐻3 𝑂 + ]2 < [𝐻3 𝑂+ ]. [𝑂𝐻 −
8
www.dzphysique.com اﻟﻤﻮﻗﻊ اﻟﺮﺳﻤﻲ ﻟﻸﺳﺘﺎذ ﺑﻮزﻳﺎن زﻛﺮﻳﺎء
𝑒𝐾 < [𝐻3 𝑂+ ]2
ومنه:
+ ]2
𝑂 −log[𝐻3 𝑒𝐾 > − log
إذن:
1
𝑒𝐾𝑝 > 𝐻𝑝
2
𝟕 > 𝑯𝒑
.12ثابت الحموضة للثنائية (أساس/حمض):
.1-3تعريف :تتميز الثنائية (أساس/حمض) يسمى بثابت الحموضة 𝑎 Kحيث:
] [𝐴− ]. [𝐻3 𝑂+
= 𝑎𝐾
]𝐻𝐴[
بالعالقة: يعرف الـ 𝑎 pK
𝑎𝐾 𝑝𝐾𝑎 = − log
𝑎𝐾𝑝𝐾𝑎 = 10−
ثابت الحموضة ال يتعلق إال بدرجة الحرارة.
.2-3العالقة بين الـ𝑯𝒑 والـ𝒂𝑲𝒑 :
] [𝐴− ]. [𝐻3 𝑂 +
= 𝑎𝐾
]𝐻𝐴[
]𝐻𝐴[ 𝐾𝑎 .
= ] [𝐻3 𝑂+
] [𝐴−
ومنه:
]𝐻𝐴[ 𝐾𝑎 .
− log[𝐻3 𝑂+ ] = − log
] [𝐴−
] [𝐴−
𝑝𝐻 = − log 𝐾𝑎 + log
]𝐻𝐴[
إذن:
] [𝐴−
𝑝𝐻 = 𝑝𝐾𝑎 + log
]𝐻𝐴[
مالحظة:
• يكون الحمض أقوى كلما كانت قيمة 𝑎 Kأكبر وبالتالي قيمة الـ 𝑎 pKاملوافقة أصغر.
] [𝐻3 𝑂+
= 𝑓𝜏
𝐶
2
𝐶𝜏 .
𝜏 { 𝐾𝑎 = 1 −
يكون األساس أقوى كلما كانت قيمة 𝑎 Kأصغر وبالتالي قيمة الـ 𝑎 pKاملوافقة أكبر. •
] [𝑂𝐻 −
= 𝑓𝜏
{ 𝐶
𝑒𝐾 (1 − 𝜏).
= 𝑎𝐾
𝐶 𝜏 2.
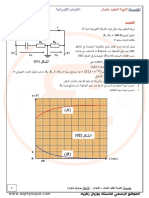
.3-3مجاالت تغلب الصفة الحمضية أو األساسية لثنائية (أساس/حمض):
من العالقة:
] [𝐴−
𝑝𝐻 = 𝑝𝐾𝑎 + log
]𝐻𝐴[
][𝐴− ][𝐴−
]𝐻𝐴[ ← log [𝐴𝐻] = 0ومنه ال وجود لصفة غالبة. الحالة األولى 𝑝𝐻 = 𝑝𝐾𝑎 :يعني أن = 1
][𝐴− ] [𝐴−
log [𝐴𝐻] > 0ومنه الصفة األساسية هي الغالبة. الحالة الثانية 𝑝𝐻 > 𝑝𝐾𝑎 :يعني أن ← [𝐴𝐻] > 1
9
www.dzphysique.com اﻟﻤﻮﻗﻊ اﻟﺮﺳﻤﻲ ﻟﻸﺳﺘﺎذ ﺑﻮزﻳﺎن زﻛﺮﻳﺎء
][𝐴− ] [𝐴−
log [𝐴𝐻] < 0ومنه الصفة الحمضية هي الغالبة. الحالة الثالثة 𝑝𝐻 < 𝑝𝐾𝑎 :يعني أن ← [𝐴𝐻] < 1
]𝐻𝐴[ < ] [𝐴− ]𝐻𝐴[ = ] [𝐴− ]𝐻𝐴[ > ] [𝐴−
pH
حمضي 𝑎𝐾𝑝 = 𝐻𝑝 أساسي
مخطط توزيع الصفة الغالبة:
%
100 –
HA A
80 الغالب الغالب
𝐴 60 pH < pK 𝐴 pH > pK
40
20
𝑯𝒑
0
𝑨𝑲𝒑
.13تطبيقات على الكواشف امللونة:
الكاشف امللون هو عبارة عن ثنائية أساس/حمض )(𝐻𝐼𝑛/𝐼𝑛−حيث يكون للصيغة الحمضية والصيغة األساسية لونين مختلفين.
)HIn (aq) + H 2O (l H O
+
+ In
- معادلة تفاعل الكاشف امللون مع املاء:
3 )(aq )(aq
إن ثابت الحموضة املرفق بهذه املعادلة هو:
] [𝐼𝑛− ]. [𝐻3 𝑂+
= 𝑖𝑎𝐾
]𝑛𝐼𝐻[
ومنه:
] [𝐼𝑛 −
𝑝𝐻 = 𝑝𝐾𝑎𝑖 + log
]𝑛𝐼𝐻[
][𝐼𝑛−
إن لون املحلول يتعلق بالنسبة ]𝑛𝐼𝐻[ وبالتالي بقيمة الـ(𝑝𝐾𝑎𝑖 − 1 < 𝑝𝐻 < 𝑝𝐾𝑎𝑖 + 1) . pH
10
www.dzphysique.com اﻟﻤﻮﻗﻊ اﻟﺮﺳﻤﻲ ﻟﻸﺳﺘﺎذ ﺑﻮزﻳﺎن زﻛﺮﻳﺎء
األستاذ :بوزيان زكرياء السنة الثالثة تقني رياضي – علوم تجريبية ثانوية العقيد عثمان
المجـــال :التطورات الرتيبة
الوحدة الرابعة :تطور جملة كيميائية نحو حالة التوازن
المدة 3 :سا الموضوع :المعايرة حمض – أساس
.14مفهوم املعايرة:
تهدف معايرة نوع كيميائي في محلول إلى تعيين تركيزه املولي .يتم تحقيق املعايرة ،عندما نقوم بمفاعلة هذا النوع الكيميائي ،الذي نسميه
ُ ُ
املتفاعل امل َع َاير ،مع نوع كيميائي آخر نسميه امل َع ِاير والذي يكون تركيزه املولي معلوم.
.15املعايرة الـ pHمترية:
تكتب معادلة تفاعل املعايرة لحمض 𝐻𝐴 في محلول بواسطة األساس 𝐵 بالشكل التالي:
- +
)AH (aq) + B (aq A )(aq) + BH (aq
يستعمل في املعايرة الـ pHمترية التركيب التجريبي املبين في الشكل املقابل:
الخطوات املتبعة في التجربة:
ُ
نضع في بيشر حجما معينا 𝐴 Vمن املحلول الحمض ي امل َع َاير ذي التركيز املولي 𝐴 Cاملجهول. -
نغمر مسبار الـ pHمتر في املحلول. -
َ ُ
نمأل السحاحة املدرجة حتى التدريجة الصفر باملحلول األساس ي املع ِاير ذي التركيز املولي 𝐵 Cاملعلوم. -
نسكب تدريجيا املحلول األساس ي على املحلول الحمض ي مع الرج املستمر بواسطة املخالط املغناطيس ي بغرض الحصول على خليط -
متجانس.
نسجل قيمة الـ pHبعد كل إضافة للحجم 𝐵 Vمن األساس. -
نرسم بعد ذلك منحنى املعايرة ) 𝐵 pH = f(Vالذي يمثل تغيرات pHاملزيج بداللة الحجم املضاف 𝐵 Vمن املحلول األساس ي. -
سحاحة
حامل
املعاير
ِ املحلول
القط قياس الـ 𝑯𝒑
بيشر جهاز قياس الـ 𝑯𝒑 متر
َ
املعاير املحلول
قضيب مغناطيس ي خالط مغناطيس ي
.16كيفية تعيين نقطة التكافؤ على منحنى املعايرة:
الطريقة األولى( :طريقة املماسين املتوازيين)
-نرسم املماسين للمنحنى البياني ،املتوازيين والواقعين من جهة وأخرى بالنسبة للمنطقة التي تحدث فيها القفزة الكبيرة للـ. pH
نرسم بعد ذلك املستقيم املوازي للمماسين والواقع على نفس البعد بينهما. -
نعين نقطة التكافؤ Eعند تقاطع هذا املستقيم مع املنحنى البياني ).pH = f(V -
11
www.dzphysique.com اﻟﻤﻮﻗﻊ اﻟﺮﺳﻤﻲ ﻟﻸﺳﺘﺎذ ﺑﻮزﻳﺎن زﻛﺮﻳﺎء
الطريقة الثانية( :رسم منحنى املشتقة)
𝐻𝑝𝑑
= )𝑉(.g 𝑉𝑑
في حالة متابعة املعايرة عن طريق برمجيات اإلعالم اآللي نعين نقطة التكافؤ من النهاية العظمى للمنحنى
الطريقة الثالثة( :الطريقة اللونية)
ُ
تعتمد على إضافة بضع قطرات من كاشف ملون إلى املحلول امل َع َاير ،يحصل التكافؤ عندما يتغير لون الكاشف.
𝑯𝒑
𝑬 نقطة التكافؤ
𝑬𝑯𝒑
) 𝑩𝑽(𝒇 = 𝑯𝒑 𝑯𝒑𝒅
= )𝑽(𝐠
𝑽𝒅
)𝑳𝒎( 𝒃𝑽
𝑬𝑽
.17أمثلة عن املعايرة الـ pHمترية:
.1-4معايرة حمض كلورالهيدروجين بواسطة محلول الصود:
تجربة :01
نضع في بيشر حجما 𝑳𝒎 𝟎𝟐 = 𝒂𝐕 من محلول حمض كلور املاء تركيزه مجهول ونضيف إليه حجما 𝑳𝒎 𝟎𝟑 = 𝒖𝒂𝒆𝐕 من املاء
املقطر ،ثم نسكب تدريجيا بواسطة سحاحة محلول هيدروكسيد الصوديوم تركيزه 𝑳 ،𝐂𝒃 = 𝟎, 𝟎𝟏 𝒎𝒐𝒍/باستخدام جهاز
الـ𝑶𝑨𝑿𝑬 نتحصل على املنحنى البياني ) 𝑩𝑽(𝒇 = 𝑯𝒑.
.1أكتب معادلة تفاعل املعايرة.
-معادلة تفاعل املعايرة:
)𝑙(𝑂 𝐻3 𝑂+ (𝑎𝑞) + 𝑂𝐻 − (𝑎𝑞) = 2𝐻2
.2حدد نقطة التكافؤ𝐄 ثم أحسب 𝑨𝐂.
تحديد نقطة التكافؤ Eوحساب 𝐴:C -
4
12
www.dzphysique.com اﻟﻤﻮﻗﻊ اﻟﺮﺳﻤﻲ ﻟﻸﺳﺘﺎذ ﺑﻮزﻳﺎن زﻛﺮﻳﺎء
• حساب 𝐴:C
لدينا عن نقطة التكافؤ:
𝑞𝑒𝐵𝑉 𝐶𝐴 . 𝑉𝐴 = 𝐶𝐵 .
𝐶𝐵 . 𝑉𝐵𝑒𝑞 10−2 × 20
= 𝐴𝐶 = = 10−2
𝐴𝑉 20
إذن:
𝑳𝑪𝑨 = 𝟏𝟎−𝟐 𝒎𝒐𝒍/
.3ما هو الكاشف املناسب لهذه املعايرة؟ علل.
تحديد الكاشف امللون: -
الكاشف املالئم لهذه املعايرة هو أزرق برومتيمول ألن 𝐸 pHلهذه املعايرة ينتمي إلى مجال تغيره اللوني.
.2-4معايرة حمض الخل بواسطة محلول هيدروكسيد الصوديوم:
تجربة :02
نضع في بيشرحجما 𝑳𝒎 𝟓 = 𝒂𝐕 من محلول حمض الخل تركيزه مجهول ونضيف إليه حجما 𝑳𝒎 𝟓𝟒 = 𝒖𝒂𝒆𝐕 من املاء املقطر،
ثم نسكب تدريجيا بواسطة سحاحة محلول هيدروكسيد الصوديوم تركيزه 𝑳 ، 𝐂𝒃 = 𝟎, 𝟎𝟏 𝒎𝒐𝒍/باستخدام جهاز الـ𝐎𝐀𝐗𝐄
نتحصل على املنحنى البياني ) 𝒃𝐕(𝐟 = 𝐇𝐩.
.1أكتب معادلة تفاعل املعايرة.
-معادلة تفاعل املعايرة:
)𝑙(𝑂 𝐶𝐻3 𝐶𝑂𝑂𝐻(𝑎𝑞) + 𝑂𝐻 − (𝑎𝑞) = 𝐶𝐻3 𝐶𝑂𝑂− (𝑎𝑞) + 𝐻2
.2حدد نقطة التكافؤ𝐄 ثم أحسب 𝒂𝐂.
-تحديد نقطة التكافؤ Eوحساب 𝐴:C
4
• حساب 𝐴:C
لدينا عن نقطة التكافؤ:
𝑞𝑒𝐵𝑉 𝐶𝐴 . 𝑉𝐴 = 𝐶𝐵 .
𝐶𝐵 . 𝑉𝐵𝑒𝑞 10−2 × 20
= 𝐴𝐶 = = 10−2
𝐴𝑉 20
إذن:
𝑳𝑪𝑨 = 𝟏𝟎−𝟐 𝒎𝒐𝒍/
13
www.dzphysique.com اﻟﻤﻮﻗﻊ اﻟﺮﺳﻤﻲ ﻟﻸﺳﺘﺎذ ﺑﻮزﻳﺎن زﻛﺮﻳﺎء
.3استنتج من البيان قيمة الـ𝒂 𝐊𝐩 للثنائية ) .(𝐂𝐇𝟑 𝐂𝐎𝐎𝐇/𝐂𝐇𝟑 𝐂𝐎𝐎−
-استنتاج قيمة 𝑎:pK
من البيان نجد أن pK 𝑎 = 4,8
.4ما هو الكاشف املناسب لهذه املعايرة؟ علل.
-تحديد الكاشف امللون:
الكاشف املالئم لهذه املعايرة هو الفينول فتالين ألن 𝐸 pHلهذه املعايرة ينتمي إلى مجال تغيره اللوني.
14
www.dzphysique.com اﻟﻤﻮﻗﻊ اﻟﺮﺳﻤﻲ ﻟﻸﺳﺘﺎذ ﺑﻮزﻳﺎن زﻛﺮﻳﺎء
You might also like
- الدرس 01Document2 pagesالدرس 01zaki48No ratings yet
- تعيين كمية المادة عن طريق المعايرةDocument8 pagesتعيين كمية المادة عن طريق المعايرةbdjabir17No ratings yet
- ملخص الوحدة 4Document2 pagesملخص الوحدة 4kader bouchikhiNo ratings yet
- Almondjid - 3-04Document46 pagesAlmondjid - 3-04AMIRAFORTASNo ratings yet
- Altholat Alkimiaiia Alti THDTH Fi Mnhiin Aldrs 2Document7 pagesAltholat Alkimiaiia Alti THDTH Fi Mnhiin Aldrs 2Kasper KasparovNo ratings yet
- همظنملا ليلاحملا Buffer SolutionsDocument33 pagesهمظنملا ليلاحملا Buffer SolutionsjngpgsgqrnNo ratings yet
- Guezouri Chapitre 4 PDFDocument10 pagesGuezouri Chapitre 4 PDFDouns ALNo ratings yet
- 3-04-1 - تطور جملة كيميائية نحو حالة التوازنDocument72 pages3-04-1 - تطور جملة كيميائية نحو حالة التوازنZaki LaidouneNo ratings yet
- ملخص شامل أحماض وأسسDocument9 pagesملخص شامل أحماض وأسسfleur2narcisseNo ratings yet
- 3AS U04 - E3 - Cour-Exe 01Document19 pages3AS U04 - E3 - Cour-Exe 01yacinesatNo ratings yet
- ملخص الوحدة 04Document20 pagesملخص الوحدة 04abdelrahimdzzeNo ratings yet
- Dzexams Docs 3as 904821Document2 pagesDzexams Docs 3as 904821ặděɱ ɱěžĥŏud-أدمہ مہزهودNo ratings yet
- G12A Sem2 Unit5 الدرس الثالثDocument22 pagesG12A Sem2 Unit5 الدرس الثالثmr MeetNo ratings yet
- Dzexams Docs 3as 907342Document21 pagesDzexams Docs 3as 907342maadzha14No ratings yet
- التفاعل بين المحاليل الحمضية الحمضية و المحاليل الأساسيةDocument9 pagesالتفاعل بين المحاليل الحمضية الحمضية و المحاليل الأساسيةChahine OffNo ratings yet
- bch101 - Part 1 0Document238 pagesbch101 - Part 1 0ابن الحكيميNo ratings yet
- Publication 3 27706 350Document57 pagesPublication 3 27706 350Elsayed ElazazyNo ratings yet
- تمارين المعايرة الحمضية القاعديةDocument4 pagesتمارين المعايرة الحمضية القاعديةAzul AzulNo ratings yet
- RevFinal2020 Doc3 PDFDocument4 pagesRevFinal2020 Doc3 PDFIvan CrowNo ratings yet
- Altfaalat HMDH Qaada Aldrs 1Document3 pagesAltfaalat HMDH Qaada Aldrs 1SLAMTI AnassNo ratings yet
- ملخصات العلوم الفيزيائية 2 ثانويDocument6 pagesملخصات العلوم الفيزيائية 2 ثانويAs benNo ratings yet
- Dzexams Docs 3as 904821Document3 pagesDzexams Docs 3as 904821wwaassiim2006No ratings yet
- Physics2as-Resume Chimie BensaidDocument6 pagesPhysics2as-Resume Chimie BensaidMohamed BensoulaNo ratings yet
- ملخص دروس الكمياء 2 ثانوي إعدد الأستاذ نصر الله بن سعيد PDFDocument6 pagesملخص دروس الكمياء 2 ثانوي إعدد الأستاذ نصر الله بن سعيد PDFHalimi Abdellah Takieddine100% (1)
- التحولات الكيميائية التي تحدث في المنحيينDocument3 pagesالتحولات الكيميائية التي تحدث في المنحيينOmar ait taleb aliNo ratings yet
- ملخص تعيين كمية المادة بواسطة المعايرة حمض - أساس للأستاذ التيجاني دهامDocument3 pagesملخص تعيين كمية المادة بواسطة المعايرة حمض - أساس للأستاذ التيجاني دهامАсма МилыйNo ratings yet
- (H) Ka (Acid)Document28 pages(H) Ka (Acid)Elsayed ElazazyNo ratings yet
- سلسلة تمارين بالحلولالمعايرة جزء01 كريم سنيDocument10 pagesسلسلة تمارين بالحلولالمعايرة جزء01 كريم سنيTarakk KaziNo ratings yet
- Keem 315 Qui Fs Module 1Document7 pagesKeem 315 Qui Fs Module 1darkactinoliteNo ratings yet
- تقويم تشخيصي 2 باكDocument2 pagesتقويم تشخيصي 2 باكAliNo ratings yet
- مفهوم التقدم لتفاعل كيميائي وحصيلة المادةDocument5 pagesمفهوم التقدم لتفاعل كيميائي وحصيلة المادةAICHA MERABETNo ratings yet
- Transformations Chimiques S'effectuant Dans Les Deux SensDocument5 pagesTransformations Chimiques S'effectuant Dans Les Deux SensHarakat ElhoucineNo ratings yet
- درس التفاعلات حمض قاعدة أولى باك النموذج 1Document3 pagesدرس التفاعلات حمض قاعدة أولى باك النموذج 1Oussama NigrouNo ratings yet
- Dzexams Docs 2as 906571Document4 pagesDzexams Docs 2as 906571houdahmdoudaNo ratings yet
- المكثف 2021Document79 pagesالمكثف 2021Batool Al-kharabshehNo ratings yet
- 2 - Evolution Dun Systeme Vers Un Etat DequilibreDocument62 pages2 - Evolution Dun Systeme Vers Un Etat Dequilibrezybras100% (2)
- لقطة شاشة 2023-02-16 في 1.37.26 صDocument14 pagesلقطة شاشة 2023-02-16 في 1.37.26 صmizare29gNo ratings yet
- Exc3b 2bac PDFDocument2 pagesExc3b 2bac PDFAbdelmoghit IdhsaineNo ratings yet
- (H) Ka (Acid)Document8 pages(H) Ka (Acid)Elsayed ElazazyNo ratings yet
- C3-التحولات التي تحدث في المنحيين PDFDocument7 pagesC3-التحولات التي تحدث في المنحيين PDFHarakat ElhoucineNo ratings yet
- تطور جملة كيميائية نحو حالة التوازنDocument28 pagesتطور جملة كيميائية نحو حالة التوازن3adiloNo ratings yet
- BBL 22Document12 pagesBBL 22al maktabaNo ratings yet
- UntitledDocument72 pagesUntitledمحمد طاهرNo ratings yet
- - نماذج احيائي منهج عربي 4Document4 pages- نماذج احيائي منهج عربي 4hassanghfran283No ratings yet
- ملخص شامل في الكيمياءDocument7 pagesملخص شامل في الكيمياءbekhaddachimaNo ratings yet
- ملخص السنة الثانية #مجال #المادة وتحولاتهاDocument6 pagesملخص السنة الثانية #مجال #المادة وتحولاتهاtouhami messiidNo ratings yet
- Résumé U04 3asDocument4 pagesRésumé U04 3asBàlkis ReiNaNo ratings yet
- Physics 2se20 2trim1Document4 pagesPhysics 2se20 2trim1noureddine SILININo ratings yet
- تصحيح 2016Document8 pagesتصحيح 2016Tarik SouimdiNo ratings yet
- تمارين الأحماض و الأسس 2016 2017Document3 pagesتمارين الأحماض و الأسس 2016 2017khalil75No ratings yet
- في الاحماض والقواعد 2Document39 pagesفي الاحماض والقواعد 2رهف موسىNo ratings yet
- CourU4Ter NeddineGDocument11 pagesCourU4Ter NeddineGrachidguessoum4No ratings yet
- Altholat Alkimiaiia Alti THDTH Fi Mnhiin Mlkhs Aldrs 3 PDFDocument3 pagesAltholat Alkimiaiia Alti THDTH Fi Mnhiin Mlkhs Aldrs 3 PDFmemez phosphateNo ratings yet
- وحدة444444Document1 pageوحدة444444Houssem HassouNo ratings yet
- الاختبار بالحلgDocument13 pagesالاختبار بالحلgاستاذك في الفيزياءNo ratings yet
- ch2 6-Les Réactions Acido-Basiques ActivitéDocument2 pagesch2 6-Les Réactions Acido-Basiques ActivitéRachid SadNo ratings yet
- حل كهرباء 2Document2 pagesحل كهرباء 2zaki48No ratings yet
- تمرين كهرباء 6Document2 pagesتمرين كهرباء 6zaki48No ratings yet
- حل كهرباء 1Document3 pagesحل كهرباء 1zaki48No ratings yet
- تمرين كهرباء 7Document1 pageتمرين كهرباء 7zaki48No ratings yet
- تمرين كهرباء 2 PDFDocument2 pagesتمرين كهرباء 2 PDFzaki48No ratings yet
- حل ميكانيك 2Document2 pagesحل ميكانيك 2zaki48No ratings yet
- حل ميكانيك 6Document2 pagesحل ميكانيك 6zaki48No ratings yet
- تمرين دمج كيمياء 3Document2 pagesتمرين دمج كيمياء 3zaki48No ratings yet
- حدود ميكانيك نيوتنDocument7 pagesحدود ميكانيك نيوتنzaki48No ratings yet
- الواجب المنزلي رقم 04Document1 pageالواجب المنزلي رقم 04zaki48No ratings yet
- بطاقة التلميذ رقم 08Document2 pagesبطاقة التلميذ رقم 08zaki48No ratings yet
- تمرين جملة كيميائية 3Document1 pageتمرين جملة كيميائية 3zaki48No ratings yet
- تمرين كهرباء 1 PDFDocument1 pageتمرين كهرباء 1 PDFzaki48No ratings yet