Professional Documents
Culture Documents
8 Αλκάλια
8 Αλκάλια
Uploaded by
chris09 xgames0 ratings0% found this document useful (0 votes)
11 views1 pageCopyright
© © All Rights Reserved
Available Formats
PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
11 views1 page8 Αλκάλια
8 Αλκάλια
Uploaded by
chris09 xgamesCopyright:
© All Rights Reserved
Available Formats
Download as PDF, TXT or read online from Scribd
You are on page 1of 1
ΑΝΑΚΕΦΑΛΑΙΩΣΗ
Αλκάλια ονομάζονται τα χημικά στοιχεία της 1 ης ομάδας του περιοδικού πίνακα,
εκτός από το υδρογόνου.
Είναι πολύ δραστικά στοιχεία, για αυτό δεν συναντώνται ελεύθερα στη φύση, αλλά
βρίσκονται μόνο σε χημικές ενώσεις.
Η δραστικότητα των αλκαλίων αυξάνεται με την αύξηση του ατομικού αριθμού.
Φυσικές ιδιότητες των αλκαλίων
o Έχουν αργυρόλευκο χρώμα και μεταλλική λάμψη
o Είναι μαλακά και κόβονται εύκολα με μαχαίρι
o Έχουν σχετικά μικρή πυκνότητα
o Έχουν χαμηλά σημεία τήξης (εύτηκτα μέταλλα).
Χημικές ιδιότητες των αλκαλίων
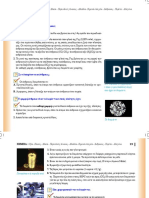
o Οξειδώνονται εύκολα από το οξυγόνο του αέρα για αυτό και φυλάσσονται σε
δοχείο με πετρέλαιο ή υγρή παραφίνη.
αλκάλιο + οξυγόνο οξείδιο αλκαλίου
o Αντιδρούν με το νερό. Κατά την αντίδραση ελευθερώνεται αέριο υδρογόνο και
προκύπτουν βασικά διαλύματα εξαιτίας της παραγωγής ανιόντων υδροξυλίου
(ΟΗ-).
αλκάλιο + νερό βάση + υδρογόνο
H ανίχνευση των κατιόντων αλκαλίων στις χημικές τους ενώσεις γίνεται με την
πυροχημική μέθοδο.
o Τα Li+ χρωματίζουν τη φλόγα του λύχνου κόκκινη, τα Νa+ κίτρινη και τα Κ+
ιώδες.
Ο βιολογικός ρόλος του νατρίου και του καλίου είναι πολύ σημαντικός, είναι στοιχεία
απαραίτητα για τη ζωή.
You might also like
- 8 ΑλκάλιαDocument1 page8 Αλκάλιαchris09 xgamesNo ratings yet
- Σελιδες 127 - 138Document12 pagesΣελιδες 127 - 138GorjahAngelNo ratings yet
- 2.2 ΤΑ ΑΛΚΑΛΙΑ - ΘΕΩΡΙΑDocument3 pages2.2 ΤΑ ΑΛΚΑΛΙΑ - ΘΕΩΡΙΑValia100% (2)
- ΑΛΚΑΛΙΑ ΜΕΤΑΛΛΑDocument1 pageΑΛΚΑΛΙΑ ΜΕΤΑΛΛΑgeogeorgousisNo ratings yet
- ΕΠΑΝΑΛΗΠΤΙΚΟ ΦΥΛΛΑΔΙΟ ΘΕΩΡΙΑΣ ΧΗΜΕΙΑ Γ ΓΥΜΝΑΣΙΟΥ (ΚΑΛΟ) 2015 PDFDocument15 pagesΕΠΑΝΑΛΗΠΤΙΚΟ ΦΥΛΛΑΔΙΟ ΘΕΩΡΙΑΣ ΧΗΜΕΙΑ Γ ΓΥΜΝΑΣΙΟΥ (ΚΑΛΟ) 2015 PDFOrfanos Lefteris100% (1)
- ΕΠΑΝΑΛΗΠΤΙΚΟ ΦΥΛΛΑΔΙΟ ΘΕΩΡΙΑΣ ΧΗΜΕΙΑ Γ ΓΥΜΝΑΣΙΟΥ (ΚΑΛΟ) 2015 PDFDocument15 pagesΕΠΑΝΑΛΗΠΤΙΚΟ ΦΥΛΛΑΔΙΟ ΘΕΩΡΙΑΣ ΧΗΜΕΙΑ Γ ΓΥΜΝΑΣΙΟΥ (ΚΑΛΟ) 2015 PDFOrfanos LefterisNo ratings yet
- ΕΠΑΝΑΛΙΟΥ ΚΑΛΟ 2015Document15 pagesΕΠΑΝΑΛΙΟΥ ΚΑΛΟ 2015ZaaraveerNo ratings yet
- ΧΗΜΕΙΑΣ Γ ΓΥΜΝΑΣΙΟΥDocument5 pagesΧΗΜΕΙΑΣ Γ ΓΥΜΝΑΣΙΟΥGIANNARASNo ratings yet
- 13. αλκοόλες-φαινόλεςDocument57 pages13. αλκοόλες-φαινόλεςLakis TriantafillouNo ratings yet
- Σελιδες 98 - 126Document29 pagesΣελιδες 98 - 126GorjahAngelNo ratings yet
- Φύλλο εργασίας «Τα αλκάλια - Ασκήσεις»Document2 pagesΦύλλο εργασίας «Τα αλκάλια - Ασκήσεις»Vagelis egialosNo ratings yet
- 1 138Document138 pages1 138PMNNo ratings yet
- χημεια οξεα βασεις αλαταDocument7 pagesχημεια οξεα βασεις αλαταΤατιάνα ΑλεξάκηNo ratings yet
- 7 ΆλαταDocument1 page7 Άλαταchris09 xgamesNo ratings yet
- Χημεία Β' Λυκειου 1.5 ΑλκένιαDocument3 pagesΧημεία Β' Λυκειου 1.5 ΑλκένιαDimitris OikonomouNo ratings yet
- ΟξειδοαναγωγήDocument8 pagesΟξειδοαναγωγήNikos Galanis100% (4)
- FarmakologiaDocument39 pagesFarmakologialeipsosNo ratings yet
- Ο ΑΝΘΡΑΚΑΣDocument8 pagesΟ ΑΝΘΡΑΚΑΣgivasila100% (1)
- ΑΛΚΑΛΙΑ ΑΝΘΡΑΚΑΣ ΠΥΡΙΤΙΟ Γ ΓΥΜΝΑΣΙΟΥDocument15 pagesΑΛΚΑΛΙΑ ΑΝΘΡΑΚΑΣ ΠΥΡΙΤΙΟ Γ ΓΥΜΝΑΣΙΟΥVasso ExarhouNo ratings yet
- ΑΛΚΑΛΙΑ-ΑΝΘΡΑΚΑΣ-ΠΥΡΙΤΙΟ Γ ΓΥΜΝΑΣΙΟΥDocument15 pagesΑΛΚΑΛΙΑ-ΑΝΘΡΑΚΑΣ-ΠΥΡΙΤΙΟ Γ ΓΥΜΝΑΣΙΟΥVasso ExarhouNo ratings yet
- ΤΑ ΑΛΚΑΛΙΑDocument2 pagesΤΑ ΑΛΚΑΛΙΑchris09 xgamesNo ratings yet
- Lecture 11Document31 pagesLecture 11mirtoNo ratings yet
- Γενική Χημεία ΜΑΚΡΗΣ ΔΗΜΗΤΡΙΟΣ Πανεπιστήμιο ΘεσσαλίαςDocument199 pagesΓενική Χημεία ΜΑΚΡΗΣ ΔΗΜΗΤΡΙΟΣ Πανεπιστήμιο ΘεσσαλίαςmpiliasNo ratings yet
- ΠΥΡΙΤΙΟ - ΚΕΡΑΜΙΚΗDocument10 pagesΠΥΡΙΤΙΟ - ΚΕΡΑΜΙΚΗμαρια γκαρNo ratings yet
- Ximeia-G-Gimnasiou Dorean-VoithimaDocument50 pagesXimeia-G-Gimnasiou Dorean-VoithimaStavros PapandreouNo ratings yet
- Xhmeia G-Gymnasioy Taexeiola GR PDFDocument0 pagesXhmeia G-Gymnasioy Taexeiola GR PDFManolis FounargiotakisNo ratings yet
- Theory B Gym ChemDocument11 pagesTheory B Gym ChemAnastasiaVlachouNo ratings yet
- οξειδοαναγωγηDocument27 pagesοξειδοαναγωγηThanasisKoufoNo ratings yet
- 2020-ΧΗΜΕΙΑ Γ ΓΥΜΝΑΣΙΟΥDocument81 pages2020-ΧΗΜΕΙΑ Γ ΓΥΜΝΑΣΙΟΥAlexNo ratings yet
- πειραματα χημειασDocument10 pagesπειραματα χημειασ21filipposNo ratings yet
- ΤΟ ΧΗΜΙΚΟ ΣΤΟΙΧΕΙΟ ΛΙΘΙΟDocument18 pagesΤΟ ΧΗΜΙΚΟ ΣΤΟΙΧΕΙΟ ΛΙΘΙΟparotidouNo ratings yet
- Εργαστηριακή αναφορά 3Document10 pagesΕργαστηριακή αναφορά 3kosmas ArapidisNo ratings yet
- ΧΡΗΣΗ ΧΡΩΣΤΙΚΩΝ ΟΞΕΙΔΙΩΝ ΓΙΑ ΧΡΩΜΑΤΙΣΜΟ ΚΕΡΑΜΙΚΩΝ ΥΑΛΩΜΑΤΩΝ ΔΙΑΦΟΡΕΤΙΚΩΝ ΣΥΝΘΕΣΕΩΝDocument61 pagesΧΡΗΣΗ ΧΡΩΣΤΙΚΩΝ ΟΞΕΙΔΙΩΝ ΓΙΑ ΧΡΩΜΑΤΙΣΜΟ ΚΕΡΑΜΙΚΩΝ ΥΑΛΩΜΑΤΩΝ ΔΙΑΦΟΡΕΤΙΚΩΝ ΣΥΝΘΕΣΕΩΝKaterina AntonNo ratings yet
- 1. Τι ονομάζονται οξέα; ΑΠΑΝΤΗΣΗ Οξέα ονομάζονται οι ενώσεις οι οποίες, όταν διαλύονται στο νερό, δίνουν κατιόντα υδρογόνου (Η) .Document32 pages1. Τι ονομάζονται οξέα; ΑΠΑΝΤΗΣΗ Οξέα ονομάζονται οι ενώσεις οι οποίες, όταν διαλύονται στο νερό, δίνουν κατιόντα υδρογόνου (Η) .AnastasiaVlachouNo ratings yet
- ΧΗΜΕΙΑΓΓΥΜΝΒDocument4 pagesΧΗΜΕΙΑΓΓΥΜΝΒvlachoelipNo ratings yet
- ΑΝΤΙΔΡΑΣΕΙΣ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣDocument29 pagesΑΝΤΙΔΡΑΣΕΙΣ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣKonstantina Sykoudi100% (1)
- αλκάνια- αλκένια- αλκίνιαDocument41 pagesαλκάνια- αλκένια- αλκίνιαgeorgiaNo ratings yet
- ΦΥΛΛΑΔΙΟ Β ΛΥΚΕΙΟΥDocument41 pagesΦΥΛΛΑΔΙΟ Β ΛΥΚΕΙΟΥVasso ExarhouNo ratings yet
- Το χημικό στοιχείο ΑρσενικόDocument11 pagesΤο χημικό στοιχείο ΑρσενικόparotidouNo ratings yet
- 3ΑΝΤΙΔΡΑΣΕΙΣ ΥΠΟΚΑΤΑΣΤΑΣΗΣ +ασκησεις PDFDocument24 pages3ΑΝΤΙΔΡΑΣΕΙΣ ΥΠΟΚΑΤΑΣΤΑΣΗΣ +ασκησεις PDFΠερί ΕπιστήμηςNo ratings yet
- ΟΞΕΑDocument10 pagesΟΞΕΑsotas27No ratings yet
- ΑΝΤΙΔΡΑΣΕΙΣ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣDocument27 pagesΑΝΤΙΔΡΑΣΕΙΣ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣKonstantina Sykoudi100% (1)
- Η ΑΠΛΗ ΑΝΤΙΚΑΤΑΣΤΑΣΗDocument17 pagesΗ ΑΠΛΗ ΑΝΤΙΚΑΤΑΣΤΑΣΗgivasila100% (1)
- Οξέα Βάσεις Άλατα ΟνοματολογίαDocument26 pagesΟξέα Βάσεις Άλατα Ονοματολογίαmarylovecatgacha72No ratings yet
- Η Χημική Ένωση Του Μήνα - Μάιος2011-Ιούλιος2013Document256 pagesΗ Χημική Ένωση Του Μήνα - Μάιος2011-Ιούλιος2013Κωνσταντίνος ΔημογέρονταςNo ratings yet
- νιοβιο PDFDocument29 pagesνιοβιο PDFLakis Takis PapasNo ratings yet
- Α ΛΥΚΕΙΟΥ-ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ ΔΙΠΛΗΣ ΑΝΤΙΚΑΤΑΣΤΑΣΗΣDocument6 pagesΑ ΛΥΚΕΙΟΥ-ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ ΔΙΠΛΗΣ ΑΝΤΙΚΑΤΑΣΤΑΣΗΣchemerica2No ratings yet
- Ονοματολογία Οργανικών Ενώσεων - 1Document9 pagesΟνοματολογία Οργανικών Ενώσεων - 1Άννα ΠαπαδάκουNo ratings yet
- ΥδατάνθρακεςDocument6 pagesΥδατάνθρακεςNasiaDeligianniNo ratings yet
- Γραφή χημικών τύπωνDocument8 pagesΓραφή χημικών τύπωνΜΗΛΙΑΡΑ ΚΑΤΕΡΙΝΑNo ratings yet
- VF Xhmikh Texnologia Erwthseis ProodouDocument13 pagesVF Xhmikh Texnologia Erwthseis ProodousofNo ratings yet
- οξεα-βασεις -εξουδετερωσηDocument5 pagesοξεα-βασεις -εξουδετερωσηGiannis PantelopoulosNo ratings yet
- ΚΕΦΑΛΑΙΟ 4Document3 pagesΚΕΦΑΛΑΙΟ 4IoannaGkoutsoulaNo ratings yet
- Αριθμός Οξείδωσης- Γραφή Χημικών ΤύπωνDocument7 pagesΑριθμός Οξείδωσης- Γραφή Χημικών Τύπωνavranes316No ratings yet
- ΥΛΗ ΓΙΑ ΔΙΑΓΩΝΙΣΜΑ Α ΤΕΤΡΑΜΗΝΟΥ ΣΤΗ ΧΗΜΕΙΑ Γ ΓΥΜΝΑΣΙΟΥDocument2 pagesΥΛΗ ΓΙΑ ΔΙΑΓΩΝΙΣΜΑ Α ΤΕΤΡΑΜΗΝΟΥ ΣΤΗ ΧΗΜΕΙΑ Γ ΓΥΜΝΑΣΙΟΥchris09 xgames100% (1)
- ΦΥΣΙΚΗ ΧΗΜΕΙΑ γγυμν Ε 13 03 2022Document5 pagesΦΥΣΙΚΗ ΧΗΜΕΙΑ γγυμν Ε 13 03 2022chris09 xgamesNo ratings yet
- _ΑΡΧΑΙΑ_αγυμν_Ε_20_03_2022Document3 pages_ΑΡΧΑΙΑ_αγυμν_Ε_20_03_2022chris09 xgamesNo ratings yet
- _ΦΥΣΙΚΗ_ΧΗΜΕΙΑ_βγυμν_Ε_05_03_2023 (5)Document2 pages_ΦΥΣΙΚΗ_ΧΗΜΕΙΑ_βγυμν_Ε_05_03_2023 (5)chris09 xgamesNo ratings yet
- ΦΥΣΙΚΗ ΧΗΜΕΙΑ γ2γυμν Ε 18 04 2023Document4 pagesΦΥΣΙΚΗ ΧΗΜΕΙΑ γ2γυμν Ε 18 04 2023chris09 xgamesNo ratings yet
- ΦΥΣΙΚΗ Γ 18 04 2023Document6 pagesΦΥΣΙΚΗ Γ 18 04 2023chris09 xgamesNo ratings yet
- Δ ΦDocument1 pageΔ Φchris09 xgamesNo ratings yet
- CivicsDocument7 pagesCivicschris09 xgamesNo ratings yet
- ΜΑΘΗΜΑΤΙΚΑ β2γυμν 05 12 2021Document1 pageΜΑΘΗΜΑΤΙΚΑ β2γυμν 05 12 2021chris09 xgamesNo ratings yet
- 9 ΠΕΙΡΑΜΑΤΑ ΣΤΑΤΙΚΟΥ ΗΛΕΚΤΡΙΣΜΟΥDocument11 pages9 ΠΕΙΡΑΜΑΤΑ ΣΤΑΤΙΚΟΥ ΗΛΕΚΤΡΙΣΜΟΥchris09 xgamesNo ratings yet
- ΙΣΤΟΡΙΑ Γ 20042023Document5 pagesΙΣΤΟΡΙΑ Γ 20042023chris09 xgamesNo ratings yet
- ΦΥΣΙΚΗDocument4 pagesΦΥΣΙΚΗchris09 xgamesNo ratings yet
- ΑσκησηDocument1 pageΑσκησηchris09 xgamesNo ratings yet
- Ν.ΕΛ. ΓΛΩΣΣΑ - ΤΟ ΡΗΜΑDocument5 pagesΝ.ΕΛ. ΓΛΩΣΣΑ - ΤΟ ΡΗΜΑchris09 xgamesNo ratings yet
- ΑΓΝΩΣΤΟ Γ 07 05 2023Document2 pagesΑΓΝΩΣΤΟ Γ 07 05 2023chris09 xgamesNo ratings yet
- ΒΙΟΛΟΓΙΑ Γ 07 05 2023Document5 pagesΒΙΟΛΟΓΙΑ Γ 07 05 2023chris09 xgamesNo ratings yet
- ΒΙΟΛΟΓΙΑ Γ 02 04 2023Document5 pagesΒΙΟΛΟΓΙΑ Γ 02 04 2023chris09 xgamesNo ratings yet
- ΜΑΘΗΜΑΤΙΚΑ Γ 02 04 2023Document3 pagesΜΑΘΗΜΑΤΙΚΑ Γ 02 04 2023chris09 xgamesNo ratings yet
- ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ Β ΤΕΤΡΑΜΗΝΟΥDocument4 pagesΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ Β ΤΕΤΡΑΜΗΝΟΥchris09 xgamesNo ratings yet
- ΒΙΟΛΟΓΙΑ Β 18 04 2023Document3 pagesΒΙΟΛΟΓΙΑ Β 18 04 2023chris09 xgamesNo ratings yet
- ΑΟΔΕ Ν 20 4 2023 ΘΕΜΑΤΑ Γ ΕΠΑΛ ΣΥΣΤΗΜΑDocument3 pagesΑΟΔΕ Ν 20 4 2023 ΘΕΜΑΤΑ Γ ΕΠΑΛ ΣΥΣΤΗΜΑchris09 xgamesNo ratings yet
- ΒΙΟΛΟΓΙΑ Β 03 01 2023Document4 pagesΒΙΟΛΟΓΙΑ Β 03 01 2023chris09 xgamesNo ratings yet
- ΥΓΙΕΙΝΗ ΜΙΚΡΟΒΙΟΛΟΓΙΑ Γ ΕΠΑΛ 20 04 2023Document4 pagesΥΓΙΕΙΝΗ ΜΙΚΡΟΒΙΟΛΟΓΙΑ Γ ΕΠΑΛ 20 04 2023chris09 xgamesNo ratings yet
- ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣDocument2 pagesΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣchris09 xgamesNo ratings yet
- ΔΙΑΓΩΝΙΣΜΑ ΤΕΧΝΟΛΟΓΙΑΣDocument4 pagesΔΙΑΓΩΝΙΣΜΑ ΤΕΧΝΟΛΟΓΙΑΣchris09 xgamesNo ratings yet
- Vaccination CertificateDocument1 pageVaccination Certificatechris09 xgamesNo ratings yet
- ΠΡΑΚΤΙΚΟ ΑΝΔΡΕΑΔΗΣDocument5 pagesΠΡΑΚΤΙΚΟ ΑΝΔΡΕΑΔΗΣchris09 xgamesNo ratings yet
- ΒΙΟΛΟΓΙΑ Β 03 01 2023Document3 pagesΒΙΟΛΟΓΙΑ Β 03 01 2023chris09 xgamesNo ratings yet
- ΕπταπύργιοDocument3 pagesΕπταπύργιοchris09 xgamesNo ratings yet
- ΠΡΑΚΤΙΚΟ ΠΑΠΑΡΗDocument5 pagesΠΡΑΚΤΙΚΟ ΠΑΠΑΡΗchris09 xgamesNo ratings yet