Professional Documents
Culture Documents
דיאגרמות פאזה
Uploaded by
Shikma SassonOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
דיאגרמות פאזה
Uploaded by
Shikma SassonCopyright:
Available Formats
פרק – 7דיאגרמת פאזות
דיאגרמת פאזות Phase diagrams
פאזות ודיאגרמת פאזות
סגסוגת ) – (Alloyחומר המציג תכונות של חומר מתכתי והמורכב ממספר אלמנטים .ישנם שני סוגים
של סגסוגות:
א .סגסוגות חד פאזות.
ב .סגסוגות רב פאזות.
פאזה היא חלק מהחומר ,הנמצא במצב פיזי הומוגני עם עצמו ,כך שניתן להפריד אותו מחלקים אחרים של
החומר הנמצאים בפאזות שונות .לדוגמא :למים 3פאזות :קרח ,מים וקיטור.
לפאזה 3מאפיינים:
א .מבנה קבוע ,או צורת סידור אטומים קבועה.
ב .בערך אותה קומפוזיציה ואותן תכונות בכל הפאזה.
ג .משטח גבול ברור בין הפאזה לפאזות הסובבות אותה.
מסיסות ותמיסות מוצקים )(Solubility and Solid Solutions
מסיסות אינסופית – ניקח מים ואלכוהול שכל אחד מהם הוא פאזה שונה .נערבב אותם ביחד ונקבל רק
פאזה אחת .בכל ריכוז שהוא של אחד המרכיבים ,תמיד נקבל פאזה אחת .כלומר ,מים ואלכוהול מסיסים
אחד כלפי השני ויש בניהם מסיסות אינסופית.
נערבב ניקל נוזלי עם נחושת נוזלית ושוב נקבל פאזה אחת .כשנקרר את התמיסה עד שתתמצק נקבל
סגסוגת מוצקה בפאזה אחת .בתוך הסגסוגת ,אטומים של הניקל והנחושת מפוזרים רנדומלית ואין גבול
ברור בניהן .זוהי אינה תערובת מכיוון שהמאפיינים האישיים של כל אחד מהמרכיבים אינם נשמרים אלא
כל המאפיינים מתמוססים ויוצרים מאפיינים חדשים של החומר החדש.
מסיסות מוגבלת – אם נכניס מלח למים הוא יתמוסס ונקבל פאזה אחת – מי מלח .אך אם נוסיף עוד הרבה
מלח ,חלק ממנו ישקע לקרקעית ונקבל שתי פאזות – מי מלח ,ומלח .לכן ,למלח מסיסות מוגבלת במים.
במקרים מסוימים ,על ידי העלאת הטמפרטורה נוכל להעלות את המסיסות של החומרים.
עמוד 1מתוך 28
פרק – 7דיאגרמת פאזות
תנאים למסיסות מוצקים אינסופית
על מנת שלסגסוגת כלשהי תהיה מסיסות אינסופית חייבים להתקיים מספר תנאים הנקראים חוקי
.Hume-Rotheryהתנאים הם:
.1מקדם הגודל ) – (Size factorעל האטומים של החומרים המרכיבים את הסגסוגת להיות בערך
באותו הגודל עם סטייה אפשרית של עד ,15%על מנת להקטין את הלחץ על הסריג בשל
המרווחים הבין אטומיים השונים.
.2מבנה הגבישים ) – (Crystal structureלשני החומרים צריך להיות מבנה קריסטלוגרפי זהה או
שבנקודה מסוימת יהיה מעבר מפאזה אחת לפאזה שנייה עם מבנה קריסטלוגרפי שונה.
.3מספר אלקטרונים ברמה אחרונה ) – (Valenceלשני החומרים חייב להיות אותו מספר
אלקטרונים ברמה האחרונה ,מכיוון שמספר שונה מעודד יצירת תרכובות.
.4אלקטרונגטיביות )) – (Electronegativityזוהי תכונה של אטומים .חומר בעל אלקטרונגטיביות
גבוהה הוא חומר הוא חומר שקולט אלקטרונים בקלות ועל ידי כך הופך לאניון( .על המרכיבים
של התמיסה להיות בעלי אלקטרונגטיביות זהה פחות או יותר .הבדל גדול באלקטרונגטיביות
גורם להיווצרות תרכובות.
עמוד 2מתוך 28
פרק – 7דיאגרמת פאזות
חיזוק תמיסות מוצקים Solid Solution Strengthening
בחומרים מתכתיים ,אחד האפקטים החשובים של היווצרות תמיסות מוצקות הוא חיזוק התמיסה המוצקה.
חיזוק זה נובע מעמידות גבוהה יותר לתנועת נקעים בחומר.
רמת חיזוק התמיסה המוצקה – מושפעת על ידי שני גורמים .קודם כל ,הפרש גדול בין קטרי האטומים
המרכיבים את התמיסה תורם לחיזוק על ידי כך שהוא גורם לעיוות גדול יותר במבנה הקריסטלוגרפי
ומקשה על תנועת נקעים .שנית ,ככל שמוסיפים יותר חומר לתמיסה ,התמיסה מתחזקת .לדוגמא :אם
נוסיף לכסף 30%בריליום ,התמיסה הנוצרת תהיה חזקה מתמיסת כסף שבה 10%בריליום.
-Yield strengthהכוח שניתן
להפעיל על חומר לפני שהוא
מאבד את היכולת לחזור
לצורה המקורית שלו.
השפעת חיזוק התמיסה המוצקה על מאפייני החומר – האפקטים על תכונותיו של חומר מתכתי הם:
.1החוזק והקשיחות של הסגסוגת גדלים.
.2בד"כ הגמישות של הסגסוגת נמוכה יותר מזו של המרכיבים אותה.
.3המוליכות החשמלית של הסגסוגת נמוכה בהרבה מזו של מתכת טהורה .למרות זאת ,בסגסוגות
המוליכות החשמלית הנמוכה היא יותר יציבה מזו שבמתכות טהורות בטמפרטורות שונות.
.4ההתנגדות להחלשות של התמיסה המוצקה בטמפרטורות גבוהות גבוהה יותר.
עמוד 3מתוך 28
פרק – 7דיאגרמת פאזות
גרף קירור של מתכת טהורה – בתנאי שיווי משקל ,לכל המתכות ישנה נקודת קיפאון או נקודת היתוך
מוגדרת .גרף קירור של מתכת כזו יראה כך:
Liquid
phase Solid
Temp phase
Freezing point
Time
הקו האופקי נובע מכך שכל אנרגית החום מושקעת בשינוי הפאזה ,ולכן עד שלא כל החומר יעבור פאזה
הטמפרטורה שלו לא תשתנה.
גרף קירור של תמיסה מוצקה –
– Soluteהחלק הקטן בתמיסה.
– Solventהחלק הגדול בתמיסה.
מכיוון שלכל חומר בתמיסה יש נקודת היתוך שונה ,ההתקשות של התמיסה עשויה להתחיל בטמפרטורה
גבוהה או נמוכה יותר מזו של ה .solvent-בד"כ לתמיסות מוצקים יש טווח טמפרטורות מסוים בו
מתרחשת סולידיפיקציה.
Liquid
phase
Temp
Phase change start temperature
Phase change finish temperature
Solid
phase
Time
עמוד 4מתוך 28
פרק – 7דיאגרמת פאזות
חוק הפאזה Phase Rule
חוק הפאזה של גיבס ) (Gibbs' Phase lawמתאר את הקשר בין מספר המרכיבים למספר הפאזות
במערכת נתונה ,ואת התנאים שעשויים להשתנות ללא תלות בתנאים האחרים )לחץ ,טמפרטורה(...
F =2+C −P
כאשר:
= Cמספר המרכיבים שהם עצמאים כימית ,כלומר ,מספר היסודות או התרכובות הדרושים על מנת
להגדיר את המערכת .לדוגמא :מים H 2 Oנחשבים מערכת של מרכיב אחד ,מכיוון שהריכוזים של H
ושל Oב H 2 O -לא יכולים להשתנות כל אחד בנפרד.
= Fמספר דרגות חופש או מספר המשתנים )כמו לחץ ,טמפרטורה או קומפוזיציה( שיכולים להשתנות
לבד מבלי להשפיע על מספר הפאזות בשיווי משקל.
= Pמספר הפאזות במערכת.
= 2הקבוע 2מציין שגם הטמפרטורה וגם הלחץ יכולים להשתנות ללא תלות בשאר המשתנים במערכת.
הערות:
א .החוק מניח שהמערכת נמצאת בשיווי משקל.
ב .חומר לא חייב להיות באחת משלושת הפאזות המוכרות – מוצק ,נוזל וגז .יסוד כמו ברזל יכול
להתקיים גם במבנה FCCוגם במבנה .BCCשני מצבים אלה הם מוצקים אך נחשבים פאזות
שונות ,שיהיו יציבות בטמפרטורות ובלחצים שונים זה מזה.
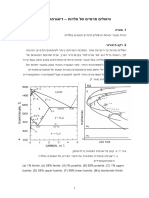
נראה כיצד החוק הנ"ל בא לידי ביטוי על ידי הגרף הבא:
זוהי דיאגרמת פאזות של מגנזיום ,כלומר 1=Cמכיוון שיש רק מרכיב אחד במערכת והוא המגנזיום.
הקווים מפרידים בין הפאזות השונות .ניתן לראות שבטמפרטורות מסוימות ותחת לחצים שונים המגנזיום
יכול להתקיים בפאזה אחת ,שתי פאזות חופפות ,ואפילו שלוש פאזות.
חשוב לשים לב שהחיתוך בין הקווים בדיאגרמה לבין קו האטמוספרה האחת נותן למעשה את טמפרטורת
ההיתוך והאידוי של המגנזיום.
נניח שיש לנו לחץ וטמפרטורה כמו בנקודה .Aכל המגנזיום כרגע נוזלי .מספר הפאזות הוא ) 1נוזל( חוק
הפאזות אומר לנו שיש לנו 2דרגות חופש:
2 + C = F + P ⇒ 2 +1 = F +1 ⇒ F = 2
עמוד 5מתוך 28
פרק – 7דיאגרמת פאזות
הכוונה בדרגות חופש היא שבמסגרת הגבולות ,אנחנו יכולים לשנות את הטמפרטורה ,הלחץ ,או שניהם
ביחד ,ועדיין להימצא בסביבה הנוזלית בדיאגרמה.
נסתכל על נקודה C .Bעדיין שווה ל P .1-לעומת זאת שווה ל 2-מכיוון ששתי פאזות יכולות להתקיים
בתנאים אלה .לפי חוק הפאזות:
2 + C = F + P ⇒ 2 +1 = F + 2 ⇒ F = 1
יש לנו דרגת חופש אחת בלבד ,כלומר ,אם נשנה את הטמפרטורה ,נהיה חייבים לשנות את הלחץ על מנת
להישאר במצב הגבול כך שעדיין יהיו לנו שתי פאזות.
נסתכל על נקודה C .Xעדיין שווה ל .1-ישנן 3פאזות בנקודה זו ולכן:
2 + C = F + P ⇒ 2 +1 = F + 3 ⇒ F = 0
אין דרגות חופש = אין משתנים חופשיים = אם נשנה את אחד המשתנים לא נימצא יותר במצב שיכולים
להתקיים בו שלושת הפאזות .הנקודה Xנקראת נקודה משולשת ).(Triple point
דיאגרמת פאזות
הדרך הטובה ביותר לתאר שינויי פאזה בסגסוגות הן דיאגרמות הפאזות .בדיאגרמות אלה ציר Xמתאר
את ההרכב של הסגסוגת וציר Yמתאר את הטמפרטורה )בד"כ(.
דיאגרמת פאזות בינארית היא דיאגרמה המתארת תמיסה המורכבת משני מרכיבים.
הרכב הסגסוגת מצויר כך שבצד שמאל של הציר יש 100%מחומר אחד ובצד ימין של הציר 100%
מהחומר השני.
כאשר רושמים Cu-20%Alהכוונה היא שיש Cu 80%ו.Al 20%-
לפעמים ,לתמיסה עם מרכיבים באחוז מסוים יש טמפרטורת קיפאון אחת )ולא טווח טמפרטורות( כמו
ליסוד טהור .נקודה זו נקראת נקודה אוטקטית ).(Eutectic point
ניתן למצוא נקודה זו על ידי ביצוע ניסויים ומדידת טמפרטורת הקיפאון בתמיסות שונות.
הקו המפריד בין אזור שכולו נוזל לבין אזור שחלקו נוזל וחלקו מוצק ,או שכולו מוצק,
נקרא . Liquidus line
הקו המפריד בין אזור שכולו מוצק לבין אזור שחלקו מוצק וחלקו נוזל ,או שכולו נוזל נקרא סולידוס
.Solidus line,
הקו המפריד בין שני אזורים מוצקים בעלי פאזות שונות נקרא סולבוס.Solvus line ,
בדומה לדרך בה אלמנט אחד יכול להתמוסס לתוך אלמנט אחר בתמיסה נוזלית ,אלמנט אחד יכול
להתמוסס בתוך אלמנט אחר כאשר שניהם במצב מוצק .יכולת זו מוגבלת לאחוז קטן מהמשקל של
התמיסה ומשתנה בטמפרטורות שונות.
בגרף שלמטה נציין את היכולת של אלמנט אחד להתמוסס בתוך אלמנט אחר ועדיין לשמור על מצב מוצק
על ידי :
= αהתמוססות של מרכיב Bבתוך Aכש A-הוא המרכיב הגדול.
= βהתמוססות של מרכיב Aבתוך Bכש B-הוא המרכיב הגדול.
ובמילים אחרות α ,היא תמיסה מוצקה שבה כמות מצומצמת של אטומי Bבתוך סריג של אטומי .A
המבנה הקריסטלוגרפי של αזהה למבנה הקריסטלוגרפי של Aהטהור.
בגרף ,האזור שנמצא מתחת לקו האוטקטי ומחוץ לאזור של התמיסה המוצקה הוא תרכובת מוצקה של
שני האלמנטים המרכיבים.
עמוד 6מתוך 28
פרק – 7דיאגרמת פאזות
נקודת היתוך נקודת היתוך
של מרכיב A של מרכיב B
Temp Liquid
Liquidus
β + liquid
α + liquid
α
β
solvus eutectic point
eutectic line
α+β
100% Composition 100%
A B
הדיאגרמה הבאה היא דיאגרמת פאזות בינארית של :Ni-Cu
בכדי להגדיר מצב של מערכת הנמצאת בשיווי משקל ,הכרחי להגדיר שלושה משתנים בלתי תלויים:
טמפרטורה ,לחץ וקומפוזיציה.
כאשר הלחץ קבוע ,הדיאגרמה מראה את השינויים המבניים של התמיסה בשל שינויי טמפרטורה וריכוז.
דיאגרמת פאזות מראה את מערכות היחסים בין המשתנים תחת תנאי שיווי משקל ,כלומר ,במצב שאין
שינוי עם הזמן .שיווי משקל כזה ניתן להשיג על ידי חימום וקירור איטיים ביותר ,כך שאם החל שינוי
פאזה ,יהיה מספיק זמן לכל החומר להשתנות.
עמוד 7מתוך 28
פרק – 7דיאגרמת פאזות
דוגמא
מצא:
א .מסיסות Snבעופרת ) (Pbמוצקה בטמפרטורה של 100מעלות צלזיוס.
ב .המסיסות המקסימלית של עופרת ב Sn-מוצק.
ג .הכמות של βהנוצרת כאשר סגסוגת Pb-10% Snמקוררת ל 0-מעלות צלזיוס.
ד .המסות של Snהנמצאות בפאזות αו.β-
ה .מסת העופרת המצויה בפאזות αו .β-הנח שהכמות הכוללת של הסגסוגת Pb-10% Snהיא 100
גרם.
פתרון
א .קו ה 100-מעלות צלזיוס חותך את קו הסולבוס בריכוז .Sn 5%לכן ,מסיסות Snבעופרת
בטמפרטורה של 100מעלות צלזיוס היא .5%
ב .את המסיסות המקסימלית של Pbב Sn-ניתן למצוא מהצד העשיר ב Sn-שבדיאגרמה .המסיסות
המקסימלית מתרחשת בטמפרטורה האוטקטית של 183מעלות צלזיוס והיא .Sn 97.5%
ג .ב 0-מעלות ,סגסוגת ה Sn 10%-נמצאת באזור של פאזה .β+αנצייר קו מקשר בקו ה 0-מעלות
ובעזרת חוק המנוף נמצא ש:
10 − 2
= %β × 100 = 8.2%
100 − 2
%α = 100 − 8.2 = 91.8% מכך ניתן גם לנחש ש:
ד .שים לב ש 100-גרמים של סגסוגת יכילו 10גרם Snו 90-גרם .Pbשני המרכיבים מחולקים לשתי
הפאזות הקיימות .β+αמסת Snבתוך αהיא) = 1.836 g :הכמות של פאזת . 2% Sn × 91.8 g (α
מכיוון ש Sn-מופיע בשתי הפאזות נחשב את נוכחותו בפאזת :β
(10 − 1.836) g = 8.164 g
ה .כעת נחשב את מסת העופרת בשתי הפאזות .המסה בפאזת αשווה ל. 91.8 g − 1.836 g = 89.964 g -
מכיוון שאנו יודעים את המסה הכוללת של העופרת ) 90גרם( ואת המסה שלה בפאזת αקל לחשב
שבפאזה βיש לנו . 90 g − 89.964 g = 0.036 g
עמוד 8מתוך 28
פרק – 7דיאגרמת פאזות
הרכב של כל פאזה – בדיאגרמה שבעמוד הבא משורטט קו מקשר – .Tie lineזהו קו אופקי שמשתמשים
בו בדיאגרמת פאזה בינארית על מנת לגלות את הקומפוזיציה של סגסוגת הנמצאת בשתי פאזות במקביל.
על מנת למצוא את הקומפוזיציה נבחר את הטמפרטורה שאנו רוצים לבדוק בה ונצייר קו אופקי בין
הסולידוס לליקווידוס .באזור זה ישנן שתי פאזות של החומר .נקודת המגע בין הקו שלנו לסולידוס
ולליקווידוס מגדירה את הקומפוזיציה של כל פאזה.
Temp L
α+L
Tie line
CL CS
α
CL
CS
Composition
ניתן להבין זאת על ידי הדוגמא הבאה:
קבע את ההרכב של כל פאזה בסגסוגת Cu-40% Niהנמצאת ב.1300C, 1270C, 1250C, 1200C -
העזר בדיאגרמה הנתונה למטה!
פתרון
הקו האנכי ב 40% Ni-שבדיאגרמה מציין את ההרכב הכללי של הסגסוגת:
.1עבור 1300מעלות צלזיוס :ישנה רק פאזה נוזלית שחייבת להכיל 40%ניקל.
.2עבור 1270מעלות צלזיוס :ישנן שתי פאזות .נצייר tie lineבטמפרטורה זו ונראה שהוא פוגש את
הליקווידוס ב ,37% -כלומר ,בפאזה הנוזלית ריכוז הניקל הוא .37%כמו כן ,ניתן לראות שהקו
פוגש את הסולידוס ב – ,50%כלומר ,ריכוז הניקל בפאזה המוצקה הוא .50%
.3עבור 1250מעלות צלזיוס :שוב ישנן שתי פאזות .ה tie line-מראה שיש ריכוז של 32%ניקל
בפאזה הנוזלית ו 45%-ניקל בפאזה המוצקה.
.4עבור 1200מעלות צלזיוס :ישנה פאזה אחת מוצקה המכילה 40%ניקל.
עמוד 9מתוך 28
פרק – 7דיאגרמת פאזות
בדרך כלל נרצה לדעת את האחוז המשקלי ) (Weight percent = Wt%של שני החומרים המרכיבים
את הסגסוגת .מדי פעם נרצה לדעת את האחוז האטומי ) (Atomic percent = At%של שני המרכיבים.
נשתמש בשתי הנוסחאות הבאות על מנת להמיר בין היחידות:
⎛ ⎤ ⎡ wt % Ni ⎞
⎜ ⎢ ⎥ ⎟
⎜ ⎣ M ⎦ Ni ⎟
⎜ = at % Ni ⎟ × 100
⎜ ⎡ wt % Ni wt % Cu ⎤ ⎟
⎜⎢ M + ⎟⎥
⎣⎝ Ni M Cu ⎠⎦
⎛ ⎤ ⎡ at % Ni ⎞
⎜ ⎢ ⎥ ⎟
⎜ ⎣ M ⎦ Ni ⎟
⎜ = wt % Ni ⎟ × 100
⎜ ⎡ at % Ni at % Cu ⎤ ⎟
⎜⎢ M + ⎟⎥
⎣⎝ Ni M Cu ⎠⎦
כאשר M Niו M Cu -הם המשקלים המולקולרים של שני האלמנטים ,וכאשר הנוסחאות משתמשות
בניקל וכרום כמשתנים אך למעשה ניתן להציב כל אלמנט במקומם.
כמות של כל פאזה )חוק המנוף( – The Lever ruleנשתמש בחוק כאשר אנו רוצים לדעת את הכמויות
היחסיות של כל פאזה בסגסוגת .החוק מוגדר על ידי הנוסחה:
Lever length opposite the phase which we want to calculate
= Phase percent × 100
total length of tie line
עמוד 10מתוך 28
פרק – 7דיאגרמת פאזות
הדוגמה הבאה תבהיר את החוק ושימושו:
מצא את הכמות של כל פאזה ב Cu-40% Ni-בטמפרטורות .1300C, 1270C, 1250C, 1200C
השתמש בדיאגרמה המצורפת:
פתרון
.1עבור 1300מעלות צלזיוס :ישנה רק פאזה אחת נוזלית ,כלומר 100%נוזל.
.2עבור 1270מעלות צלזיוס :נסתכל על ה Tie line-בטמפרטורה 1270מעלות .ניתן לראות שהוא
חוצה את הליקווידוס ב 37%-ואת הסולידוס ב .50%-אנו רוצים לדעת את כמות הנוזל .נגדיר את ציר
ה"מנוף" כאחוז הנתון של הסגסוגת ) .( 40%נמדוד את האורך של זרוע המנוף שבכיוון המנוגד לחלק
הנוזלי ,כלומר .10 = 50-40נחלק את התוצאה באורך המנוף כולו ונכפיל ב .100-כך נקבל את כמות
50 − 40
= % Liquid × 100 = 77% הפאזה הנוזלית:
50 − 37
40 − 37
= %α × 100 = 23%
50 − 37
45 − 40
= % Liquid × 100 = 38% .3עבור 1250מעלות צלזיוס:
45 − 32
40 − 32
= %α × 100 = 62%
45 − 32
.4עבור 1200מעלות צלזיוס :יש רק פאזה אחת ,כלומר.α 100% ,
עמוד 11מתוך 28
פרק – 7דיאגרמת פאזות
התמצקות של סגסוגת תמיסה מוצקת
כאשר סגסוגת כמו ה Cu-40% Ni-מותכת ומתקררת ,התמצקות דורשת גם נוקלאציה וגם גידול.
נוקלאציה הטרוגנית מאפשרת מעט קירור יתר ) (Undercoolingאו בכלל לא ,ולכן התמצקות מתחילה
כאשר הנוזל מגיע לטמפרטורת הליקווידוס .מדיאגרמת הפאזה שלמטה ניתן לראות לפי הקו המקשר
שלמוצק הראשון שנוצר ישנו הרכב של .Cu-52% Ni
שני תנאים צריכים להתקיים על מנת לאפשר את גידול המוצק .קודם כל ,יש להיפטר מהחום המיותר
שנוצר בתהליך ההתמצקות .שנית ,חייבת להתקיים דיפוזיה כל הזמן ,בין הנוזל למוצק ובין המוצקים
הנוצרים על מנת שנקבל סגסוגת שוות ריכוז .ניתן להשיג זאת על ידי קירור איטי ביותר של הנוזל ומתן
זמן להתמצקות.
החום יוצא מהסגסוגת הנוצרת בקשת רחבה של טמפרטורות ולכן בגרף הקירור של הסגסוגת ישנו שיפוע
באזור ההתמצקות )במצב אידיאלי היינו מצפים לראות קו מאוזן( .ניתן לראות זאת בדיאגרמה הבאה:
עמוד 12מתוך 28
פרק – 7דיאגרמת פאזות
תרכובות בין-מתכתיות Intermetallic Compounds
תרכובת בין מתכתית מורכבת משני אלמנטים מתכתיים או יותר ,היוצרים פאזה חדשה,מבנה
קריסטלוגרפי ,ותכונות ייחודיות .בד"כ חומרים אלה הם קשים מאוד ופריכים ) .(brittleמבחינת תכונות,
חומרים אלה דומים לחומרים קרמיים.
תרכובות בין מתכתיות סטוכיומטריות הן תרכובות בעלות קומפוזיציה קבועה ,כלומר ,היחס הסטוכיומטרי
שלהן נשאר קבוע )מספר אטומים מסוג אחד קבוע ביחס למספר אטומים מסוג אחר( .בדיאגרמת פאזות
נסמן תרכובת כזו בקו אנכי עבה.
תרכובות בין מתכתיות לא סטוכיומטריות הן תרכובות בהן היחס הסטוכיומטרי יכול להשתנות.
עמוד 13מתוך 28
פרק – 7דיאגרמת פאזות
דיאגרמת פאזות אוטקטית
סגסוגת היפואוטקטית היא סגסוגת שההרכב שלה יהיה בין הקצה השמאלי של הקו המקשר המתאר את
הריאקציה האוטקטית ובין הקומפוזיציה האוטקטית )הרכב הסגסוגת בנקודה האוטקטית(.
נסתכל על דיאגרמת פאזה של :Pb-30% Sn
בקומפוזיציה שהגדרנו ,סגסוגת זו היא היפואוטקטית .כאשר סגסוגת היפואוטקטית המכילה בין 19%
לבין Sn 61.9%מתקררת ,הנוזל מתחיל להתמצק כאשר הוא מגיע לטמפרטורת הליקווידוס
) 260מעלות במקרה שלנו( ,ובנקודה זו יש לנו במוצק αבערך 12%גרעיני Snמוצקים .המוצק αגדל
עד שהטמפרטורה יורדת לטמפרטורת הקו האוטקטי ) 184מעלות( ואם נצייר את ה Tie line-נראה
שהמוצק αמכיל ,Sn 19%והנוזל הנותר מכיל .Sn 61.9%נשים לב שכעת הנוזל נמצא בריכוז
האוטקטי ולכן ברגע שנקרר אותו אל 183מעלות ,כל הנוזל הנותר יתמצק ויוצר לנו מוצק מעורב של α
ו .β-ההתמצקות מסתיימת כאשר הסגסוגת חוצה את הקו האוטקטי.
דוגמא
עבור סגסוגת ,Pb-30% Snמצא אילו פאזות קיימות ,כמויותיהן ,וההרכבים שלהן ב,200C ,300C-
.0C ,182C ,184C
פתרון
כמות הרכב פאזות טמפרטורה )(C
L=100% L: 30% Sn L 300
30 − 18
=L × 100 = 32%
55 − 18 L: 55% Sn
α +L 200
55 − 30 α: 18% Sn
=α × 100 = 68%
55 − 18
עמוד 14מתוך 28
פרק – 7דיאגרמת פאזות
30 − 19
=L × 100 = 26%
61.9 − 19 L: 61.9% Sn
α +L 184
61.9 − 30 α: 19% Sn
=α × 100 = 74%
61.9 − 19
97.5 − 30
=α × 100 = 86%
97.5 − 19 α: 19% Sn
α+β 182
30 − 19 β: 97.5% Sn
=β × 100 = 14%
97.5 − 19
100 − 30
=α × 100 = 71%
100 − 2 α: 2% Sn
α+β 0
30 − 2 β: 100% Sn
=β × 100 = 29%
100 − 2
הערה :כל התוצאות עוגלו לשם הנוחות!!!
סגסוגת היפראוטקטית היא סגסוגת שההרכב שלה יהיה בין הקצה הימני של הקו המקשר המתאר את
הריאקציה האוטקטית ובין הנקודה המתארת את ההרכב האוטקטי .בדיאגרמה שלמעלה ,הכוונה היא
לאזור שבין נקודת ה 61.9%-לבין נקודת ריכוז ה.97.5%-
נסתכל על גרף קירור של סגסוגת היפואוטקטית ונזכור שבנקודה האוטקטית ,הטמפרטורה לא משתנה עד
שלא כל הנוזל הנותר התמצק!
עמוד 15מתוך 28
פרק – 7דיאגרמת פאזות
דיאגרמות פאזות המכילות ריאקציות תלת פאזיות
Phase Diagrams Containing Three Phase Reactions
מערכות בינאריות רבות יוצרות דיאגרמות פאזות יותר מסובכות מאלו שהתעסקנו איתן עד כה .בטבלה
הבאה מתוארות חמש ריאקציות כאלה.
ניתן לזהות כל אחת מחמש הריאקציות בדיאגרמת פאזות על ידי התהליך הבא:
.1מצא קו אופקי בדיאגרמה .הקו הזה ,המראה נוכחות של ריאקציה תלת פאזית ,מיצג את
הטמפרטורה שבה מתרחשת הריאקציה תחת תנאי שיווי משקל.
.2מצא שלוש נקודות מיוחדות על קו אופקי .שתי נקודות הקצה פלוס נקודה אחת בניהן .הנקודה
האחרונה ,מייצגת את ההרכב שבו הריאקציה התלת פאזית תתרחש.
.3הבט בדיוק מעל לנקודה שבין שתי נקודות הקצה וזהה את הפאזה או הפאזות שם .רשום את
הריאקציה שבין הפאזות שמעל לנקודה לבין הפאזות שמתחת לנקודה .השווה את הריאקציה
שרשמת לאלה שבטבלה הנ"ל.
עמוד 16מתוך 28
פרק – 7דיאגרמת פאזות
זהה את הריאקציות התלת פאזיות שבדיאגרמה הבינארית הבאה:
פתרון
אנו מוצאים קווים אופקיים ב.1150C, 920C, 750C, 450C, 300C -
:1150Cהנק' שבין שני קצות הקטע נמצאת ב L+δ .B 15%-הם הפאזות מעל לנקודה γ ,היא הפאזה
מתחתיה .הריאקציה היא δ + L → γ :ולפי הטבלה ריאקציה פריטקטית .Peritecic
L1 → γ + L2מונוטקטית A monotectic :920Cהריאקציה הזו מתרחשת ב.B 40%-
L2 → γ + βאוטקטית A eutectic :750Cהריאקציה הזו מתרחשת ב.B 70%-
γ → α + βאוטקטויד A eutectoid :450Cהריאקציה הזו מתרחשת ב.B 20%-
α + β → µפריטקטויד A peritectoid :300Cהריאקציה הזו מתרחשת ב.B 50%-
הריאקציות האוטקטית ,הפריטקטית והמונוטקטית הן חלק מתהליך ההתמצקות.
דיאגרמת פאזות של סגסוגת מונוטקטית מכילה מין "כיפה" או "גבעה" ) (miscibility gapבה מתקיימות
שתי פאזות נוזליות.
הריאקציות הפריטקטויד והאאוטקטויד הן ריאקציות המתרחשות במצב מוצק לגמרי.
כל אחת מחמש הריאקציות הללו מתרחשת בטמפרטורה ובקומפוזיציה מסוימת יחידה.
לפי חוק הפאזה ,בריאקציה תלת פאזית אין דרגות חופש מכיוון שהלחץ קבוע ומכיוון ששלוש פאזות
מעורבות בריאקציה:
1 + C = F + P ⇒ F =1 + C − P ⇒ 1 + 2 − 3 = 0
⇑
⎤מספר המרכיבים = ⎡C = 2
לחץ קבוע = ⎢1 ⎥
⎢ ⎥
⎦⎥ פאזות מעורבות = ⎢⎣ P = 3
עמוד 17מתוך 28
פרק – 7דיאגרמת פאזות
שיטות ניסוי לבניית דיאגרמות פאזות
ישנן מספר שיטות ניסוייות שדרכן אוספים את המידע הדרוש לבניית דיאגרמות פאזות:
.1שיטות מטלוגרפיות – מחממים דגימות של סגסוגת מסוימת לטמפרטורות שונות ,ממתינים עד
שיוצר מצב שיווי משקל ,ואז מקררים אותן במהירות על מנת לשמור על המבנה שהיה להן
בטמפרטורה הגבוהה .לאחר מכן בוחנים את התוצאות תחת מיקרוסקופ.
קשה ליישם שיטה זו לגבי מתכות בטמפרטורות גבוהות מכיוון שגם דגימות שקוררו במהירות
מאבדות את המבנה הקודם שלהן ואז דרוש ניסיון רב על מנת לתרגם את המבנה המיקרוסקופי
בצורה נכונה.
.2דיפרקצית קרני – Xבשיטה זו מודדים את מידות הסריג ,ומציינים שינוי פאזה כאשר ישנו
שינוי במבנה ובמידות הסריג ,או כאשר נוצר מבנה קריסטלוגרפי חדש.
שיטה זו מדויקת מאוד ומשמשת להבחנה בשינויים במסיסות מוצקים המשתנה עם הטמפרטורה.
.3ניתוח טרמי – שיטה זו נפוצה ביותר .היא מסתמכת על המידע הנובע מדיאגרמות קירור.
בשיטה זו מתיכים סגסוגות בריכוזים שונים ומודדים את הטמפרטורה של הסגסוגת בזמנים
שונים של הקירור.
בונים דיאגרמת קירור לכל ריכוז ומוציאים ממנה את הטמפרטורות בהן התחילו והסתיימו שינויי
פאזה .אז ,משתמשים בטמפרטורות אלה לבניית דיאגרמת פאזות של הסגסוגת.
דיאגרמות פאזות של שלושה מרכיבים Ternary Phase Diagrams
עד עכשיו התעסקנו עם מערכות בינאריות .מערכות סגסוגת רבות מורכבות משלושה אלמנטים או יותר.
כאשר יש לנו סגסוגת המורכבת משלושה אלמנטים היא נקראת סגסוגת טרנרית .עבור מערכת טרנרית
הנמצאת תחת לחץ קבוע מקסימום 4פאזות יתקיימו יחדיו ,ובנקודה זו לא יהיו דרגות חופש .דיאגרמת
פאזות של מערכת כזו היא תלת מימדית.
להלן דוגמא של דיאגרמה כזו .שים לב שישנן שתי נקודות אוטקטיות ועוד אחת מוסתרת מאחור.
קשה להשתמש בדיאגרמות התלת-מימדיות ולכן יש לנו שתי דרכים אחרות להציג את הדיאגרמה:
– Liquidos Plotנעביר את טמפרטורות הליקווידוס של שלושת המרכיבים .1
לדיאגרמה משולשת כקווים איזוטרמיים .בעזרת קווים אלה נמצא את הפאזה
הראשונה אליה יתקרר הנוזל.
– Isothermal Plotהוא מפה משולשת המראה את הפאזות הקיימות בחומר .2
בטמפרטורות מסוימות.
עמוד 18מתוך 28
פרק – 7דיאגרמת פאזות
עמוד 19מתוך 28
פרק – 7דיאגרמת פאזות
באמצעות הדיאגרמות המשולשות שבעמוד הקודם מצא את טמפרטורת הליקווידוס ,הפאזה הראשונה
הנוצרת במהלך ההתמצקות ,ואת הפאזות בטמפרטורת החדר של החומרים הבאים:
נקודה A ,C 10% ,B 10% :Xבשיווי משקל
נקודה A ,C 60% ,B 10% :Yבשיווי משקל
נקודה A ,C 40% ,B 40% :Zבשיווי משקל
פתרון
ההרכב 10% B-10% C balance Aמצוי בדיאגרמה בנקודה .Xמהאיזוטרם באזור זה נסיק
שטמפרטורת הליקווידוס היא 400מעלות צלזיוס .הפאזה הראשונה לפי הדיאגרמה היא .αלפי
הדיאגרמה התחתונה ,המבנה הסופי הוא כולו .α
ההרכב 10% B-60% C balance Aמצוי בדיאגרמה בנקודה .Yלפי הערכת האיזוטרמים באזור,
טמפרטורת הליקווידוס היא בערך 270מעלות צלזיוס .הפאזה הראשית הנוצרת באזור זה של הדיאגרמה
היא γוהפאזות בטמפרטורת החדר הן αו.γ-
ההרכב 40% B-40% C balance Aמצוי בדיאגרמה בנקודה .Zטמפרטורת הליקווידוס היא 350
מעלות צלזיוס ,והנקודה נמצאת באזור של הפאזה .βהפאזות בטמפרטורת החדר הן β ,αו.γ-
הקשחת סגסוגות על ידי מעבר גבול המסיסות
Alloys Strengthened by Exceeding the Solubility Limit
משקעים רציפים ) – (Coherent Precipitateכבר אמרנו שאם יוצרו בסגסוגת משקעים
) (precipitatesעצמאיים ,הם יחזקו את הסגסוגת על ידי כך שימנעו תנועת נקעים .ייתכן שהם לא ייצרו
הפרעה מספיק גדולה במבנה הסריג ולכן לא ימנעו את תנועת הנקעים ולא יתרמו לחיזוק הסגסוגת בצורה
משמעותית .על מנת להפריע לתנועת הנקעים ,המשקעים חייבים להימצא בדרכם של הנקעים.
כאשר נוצר משקע רציף האטומים שבמבנה הסריגי שלו נקשרים לאטומים שבמבנה הסריגי של הסגסוגת,
ובכך גורמים להפרעה לטווח ארוך הרבה יותר במבנה הסריגי של הסגסוגת .במצב זה ,מספיק שהנקע
עובר קרוב למשקע על מנת שזה האחרון יפריע לתנועתו.
ניתן להבין זאת מהתמונה הבאה:
עמוד 20מתוך 28
פרק – 7דיאגרמת פאזות
זיקון או הקשחת משקעים Age or Precipitation Hardenincg
זיקון ) (Age Hardeningאו הקשחת משקעים ) (Precipitation Hardeningנוצר בעקבות סדרה של
מעברי פאזה שבסופם נוצר נתך שבו מפוזרים ננו -משקעים רציפים )(Nano Coherent precipitates
באופן אחיד וחזק יותר.
Microstructural Evolution in Age or Precipitation Hardening
על מנת להבין כיצד נוצרים המשקעים ומה המגבלות שלהם ניעזר בחלק מדיאגרמת פאזות של
:Al-Cu
ישנם שלושה שלבים בתהליך הקשחת זיקון:
.1טיפול המסה ) – (Solution treatmentקודם כל מחממים את הסגסוגת אל מעל לטמפרטורת
הסולבוס ומחזיקים אותה כזו עד שתמיסה מוצקה הומוגנית של αנוצרת .צעד זה מביא
להיעלמות הפאזה θומקטין את כל ההפרדות המיקרוכימיות )(Microchemical segregation
שהיו בסגסוגת המקורית.
.2צינון ,חיסום ) – (Quenchכעת ,מקררים את הסגסוגת במהירות .לאטומים אין זמן לעשות
דיפוזיה לאתרי נוקלאציה אפשריים ולכן לא נוצרת פאזת .θלאחר התהליך ,המבנה הוא תמיסה
מוצקה סופר-רוויה ) α ss (Supersaturated solid solutionהמכיל כמות גדולה של נחושת.
.3זיקון ) – (Ageמחממים את הסגסוגת הנמצאת במצב α ssאל מתחת לטמפרטורת הסולבוס.
בטמפרטורה כזו ,האטומים יכולים לבצע דיפוזיה רק למרחקים קצרים מאוד .מכיוון שהסגסוגת
לא נמצאת במצב שיווי משקל ,אטומי הנחושת מבצעים דיפוזיה למספר עצום של אתרי
נוקלאציה וגדלים משקעים .אם נחזיק את הסגסוגת מספיק זמן בטמפרטורה זו ,נגיע למבנה שיווי
המשקל .θ+αלמרות שנוצר מבנה בעל שתי פאזות ,מבנה זה שונה מזה שהיינו מגיעים אליו אם
היינו מקררים את הסגסוגת באיטיות.
עמוד 21מתוך 28
פרק – 7דיאגרמת פאזות
השפעות של טמפרטורת הזיקון והזמן
תכונות סגסוגת שעברה טיפול Agingתלויות בטמפרטורה בה חוממה ובמשך זמן החימום .נסתכל
בדיאגרמה הבאה המדגימה כיצד תלוי חוזק הסגסוגת בשני המשתנים הנ"ל:
לפי הדיאגרמה ,אם נחמם את הסגסוגת )זו שהשתמשנו בה בעמוד הקודם( ל 260-מעלות צלזיוס ,נשיג
חוזק מרבי של הסגסוגת בתוך פחות מ 0.1-שעה ) 6דקות( .אם נמשיך את החימום נקבל זיקון יתר
והסגסוגת תיחלש.
לעומת זאת ,אם נחמם את הסגסוגת פחות )לטמפרטורה של 190מעלות צלזיוס( ונמתין יותר זמן )שעה
אחת( נקבל סגסוגת חזקה יותר מזו שהיינו מקבלים בחימום של 260מעלות צלזיוס.
מהדיאגרמה ניתן לראות שככל שנשתמש בטמפרטורות נמוכות יותר ,נקבל סגסוגת חזקה יותר.
שנית ,ואת זה לא ניתן לראות בדיאגרמה ,סגסוגת שטופלה בטמפרטורה נמוכה יותר תשמור על החוזק
המקסימלי שלה לאורך זמן גדול יותר מסגסוגת שטופלה בטמפרטורה גבוהה.
שלישית ,ככל שניתן יותר זמן לדיפוזיה להתבצע ,נקבל סגסוגת יותר אחידה בתכונותיה .אם נחמם גוש
סגסוגת למשך זמן קצר ,החלק החיצוני שלה יתחמם ותתבצע בו הדיפוזיה ,אך החלק הפנימי לא יספיק
להתחמם ולא תתבצע בו דיפוזיה.
סגסוגות ברזליות Ferrous Alloys
חומרים אלה ,המבוססים על סגסוגות ברזל-פחמן הם החומרים שנעשה בהם השימוש המקיף ביותר
ברחבי העולם.
דיאגרמת הפאזות של סגסוגות אלה מסובכת מאוד ומכיוון שאנו מעוניינים רק בפלדות שבה נפשט אותה
מעט .בעמוד הבא מצוירת דיאגרמת הפאזה עד ריכוז של 7%פחמן.
עמוד 22מתוך 28
פרק – 7דיאגרמת פאזות
δ+ L γ = Austenite
1539 α = Ferrite L
1493 oC
δ = Delta iron CM begins
δ+γ γ +L CM =Cementite
to solidiffy
1400 Primary
0.51 % austenite
0.16 % begins to
Tempo γ
Austenite solidify
in liquid
C
1130 Austenite solid solution of 1147 oC L + Fe3C
carbon in gamma iron Austenite
Ledeburite Fe3C
910 910 oC
and γ+ Fe3C
cementite
Cementite
Austenite to and
723 α+γ 723 oC pearlite ledeburite
Pearlite Eutectoid α + Fe3C ,
Cementite,pearlite
and point and transformed
Ferrite ledeburite
Pearlite
210 and Cementite
0.16 % 0.50 % 0.83 % 1% 2% 3% 4% 6%
Hypo-eutectoid Hyper-eutectoid
Steel White Cast Iron
Weight percent carbon
ניתן לחלק את הטבלה ל .2-עד C 2%אלה הן פלדות ומעבר לכך יש לנו יציקות ברזל לבנות.
עד ריכוז C 6.7%יש לנו סגסוגות עתירות פחמן ,בין C 6.7%ועד ל C 100%-יש לנו סגסוגות דלות
פחמן ) = C 100%גרפיט( הברזל הטהור שבצד השמאלי של הדיאגרמה עובר במהלך החימום 3
מעברים אלוטרופיים:
בין 0ל 910-מעלות צלזיוס יש לו מבנה BCCהנקרא .α iron
בין 910-1400מעלות צלזיוס יש לו מבנה FCCהנקרא .γ iron
בין 1400מעלות לבין נקודת ההיתוך הוא שוב בעל מבנה BCCהנקרא .δ ferritr
כמו כן ,עד בין 0-0.8%פחמן ,הפלדה נקראת היפו-אוטקטואידית ובין 0.8%-2%פחמן ,היא נקראת
היפר-אוטקטואידית .פלדה בעלת ריכוז של 0.8%פחמן נקראת פלדה אוטקטואידית או פלדה פריטית.
נסתכל על הפאזות והמבנים שלהן:
.1צמנטיט ) – (Cementiteשם נוסף לקרביד הברזל ) . ( Fe3Cריכוז הפחמן בו .6.7%יש לו
מבנה אורתורומבי והוא חומר קשה ופריך.
.2אוסטניט ) – (Austeniteתמיסה מוצקה חדירה המורכבת מפחמן בתוך γFeובעלת מבנה .FCC
פאזה זו יציבה בטמפרטורות גבוהות אבל מטה-יציבה )שואפת
לשנות פאזה( בטמפ' נמוכות .אוסטניט היא פאזה רכה וגמישה.
.3פריט ) – (Ferriteתמיסה מוצקה חדירה המורכבת מפחמן בתוך αFeובעלת מבנה .BCC
עמוד 23מתוך 28
פרק – 7דיאגרמת פאזות
לפריט המבנה הרך ביותר מבין כל המבנים בדיאגרמת הברזל –
צמנטיט .מכיוון שלפריט יש מסיסות נמוכה עבור פחמן ,במהלך יצירת הפריט מאוסטניט כל
הפחמן מועף החוצה ויוצר צבירי פחמן.
פרליט ) – (Pearliteכאשר מקררים סגסוגת פחמן בריכוז 8%במצב אוסטניטי ,מתפרק .4
האוסטניט בטמפרטורה האוטקטואידית לתערובת של שתי פאזות :פריט וצמנטיט .פאזות אלה
מונחות זו ליד זו במבנה שכבות הנקרא מבנה שכבתי )למלרי( .המבנה הזה בפלדה נקרא פרליט.
לפרליט ריכוז פחמן של .0.83%זהו חומר די רך.
– Delta Iron – γFeיכול להתקיים עם הברזל המותך כאשר ריכוז הפחמן הוא עד ,0.5%עם .5
האוסטניט עד ריכוז של 0.18%פחמן ,ולבד עד ריכוז של 0.1%פחמן .יש לו מבנה BCCוהוא
מגנטי.
לדבוריט ) – (Ledeburiteזוהי תערובת של אוסטניט וצמנטיט .לדבוריט מכיל 4.3%פחמן .6
והוא קיים כאשר ישנו ריכוז של יותר מ 2%-פחמן בתמיסה הכללית ,ריכוז המייצג את ההפרדה
בין פלדות לברזל יצוק.
באייניט ) – (Bainiteהפריט במבנה זה מופיע כמבנה נוצתי ,כאשר בתוך כל גרעין נוצתי כזה .7
מופיעים חלקיקים קטנים מאוד של צמנטיט .מבנה זה קשה ופריך יותר מהפרליט .באייניט יכול
להיווצר בשתי צורות :בקירור מ 550-מעלות ל 400-מעלות ,ובקירור מ 400-מעלות ל240-
מעלות .פאזה זו נוצרת בכמות מועטה מאוד בסגסוגות פלדה .מנגנון ההיווצרות שלו כולל שינוי
הסריג של אוסטניט למבנה סריגי של פריט ,הפצה מחדש של הפחמן ,ויצירת משקעים של
קרביד.
מרטנסיט ) – (Martensiteנוצר מאוסטניט בחיסום )קירור מהיר( בלבד ,התלוי בטמפרטורה .8
ובריכוז הפחמן בתמיסה .מרטנסיט נוצר על ידי עיוות של מבנה ה FCC-של אוסטניט והפיכתו
למבנה .(Body Centered Tetragonal) BCT
ניתן למצוא פלייט מרטנסיט ) (Plate Martensiteבפלדות עשירות בפחמן או נטולות פחמן
לגמרי .גבישי המרטנסיט בנויים בצורה של פלטות דקות שאינן מקבילות אחת לשכנתה.
לאוו מרטנסיט ) (Lath Martensiteניתן למצוא בפלדות עם כמות ממוצעת או נמוכה של פחמן.
גבישי המרטנסיט הזה נראים כמו פלטות המחוברות אחת לשנייה ובעלות אוריינטציה דומה זו
לזו.
מרטנסיט היא פאזה מאוד חזקה אבל פריכה ,המקבלת את החוזק שלה מהמבנה הסריגי שלה.
הריאקציה האוטקטואידית
תזכורת :ריאקציה אוטקטואידית היא ריאקצית מצב מוצק שבה פאזה מוצקה הופכת לשתי פאזות מוצקות
אחרות:
S1 → S 2 + S3
תמיסות מוצקות – במהלך חימום ,עובר הברזל שני מעברים אלוטרופיים .מיד לאחר ההתמצקות לברזל
מבנה BCCהנקרא .δ ferriteבהמשך הקירור ,הברזל משתנה למבנה FCCהנקרא "אוסטניט"
עמוד 24מתוך 28
פרק – 7דיאגרמת פאזות
או .γ ironלבסוף חוזר הברזל למבנה BCCהנקרא "פריט" או . α ferriteשלושת המבנים הללו הם
בעלי חדירויות של אטומי פחמן בתוך הברזל.
מכיוון שה"חורים" במבנה FCCגדולים מאלה שבמבנה ,BCCניתן להחדיר יותר אטומי פחמן למבנה
.FCCלכן ,המסיסות המרבית באוסטניט היא 2.11%פחמן ,ובברזל עם מבנה BCCהיא הרבה יותר
נמוכה ,באזור 0.0218%פחמן עבור ,αו 0.09%-פחמן עבור .δהתמיסות המוצקות של פחמן בברזל הם
רכות וגמישות יחסית ,אבל חזקות מברזל טהור בשל חיזוק התמיסה המוצקה הנובע מנוכחות הפחמן.
תרכובות – תרכובת סטוכיומטרית בשם צמנטיט ) , ( Fe3Cנוצרת כאשר עוברים את המסיסות המרבית
של הפחמן בברזל .הצמנטיט מכיל 6.67%פחמן ,הוא מאוד חזק ופריך )כמו חומרים קרמיים( .שליטה
בגודל ,במבנה ובצורה של הצמנטיט מקנה לנו שליטה על תכונות הפלדה.
הריאקציה האוטקטואידית – אם אנו מחממים סגסוגת המכילה הרכב אוטקטואידי של 0.77%פחמן אל
מעל 727מעלות צלזיוס ,נקבל מבנה המכיל רק גרעיני אוסטניט .כאשר האוסטניט מתקרר תתרחש
הריאקציה האוטקטואידית:
) γ (0.77%C ) → α (0.0218%C ) + Fe3C (6.67%C
כמו בריאקציה אוטקטית ,לשנתי הפאזות שנוצרות יש קומפוזיציות שונות ,ולכן אטומים חייבים לבצע
דיפוזיה במהלך הריאקציה .רוב הפחמן שבאוסטניט עושה דיפוזיה לצמנטיט ,ורוב אטומי הברזל עושים
דיפוזיה לפריט .ההפצה מחדש של האטומים היא קלה ביותר כאשר מרחקי הדיפוזיה קצרים ,כמו במקרה
זה שפריט וצמנטיט גדלים כמו למלות או פלטות ,אחד על גבי השני.
דוגמא
חשב את כמות הפריט וכמות הצמנטיט הנוכחים בפרליט.
עמוד 25מתוך 28
פרק – 7דיאגרמת פאזות
פתרון
מכיוון שבפרליט חייב להימצא 0.77%פחמן ,בעזרת חוק המנוף נקבל:
6.67 − 0.77
= %α × 100 = 88.7%
6.67 − 0.0218
0.77 − 0.0218
= % Fe3C × 100 = 11.3%
6.67 − 0.0218
מיקרומרכיבים ראשיים ) – (Primary Microconstituentsפלדות היפואוטקטואידיות מכילות פחות מ-
0.77%פחמן ,ופלדות היפראוטקטואידיות מכילות יותר מכך .פריט הוא המיקרו-מרכיב הראשי או
המרכיב הפרו-אוטקטואידי בסגסוגות היפואוטקטואידיות ,וצמנטיט הוא המיקרו-מרכיב הראשי בפלדות
היפראוטקטואידיות.
אם נחמם סגסוגת היפואוטקטואידית המכילה 0.6%פחמן אל מעל 750מעלות צלזיוס ,רק אוסטניט
יישאר במיקרו מבנה .התמונה שבעמוד הבא מדגימה מה קורה כאשר נקרר את האוסטניט.
מיד מתחת ל 750-מעלות צלזיוס ,פריט יבצע נוקלאציה ויגדל ,בד"כ בגבולות הגרעין של האוסטניט.
הפריט ימשיך לגדול עד שהטמפרטורה תרד ל 727-מעלות צלזיוס .האוסטניט שנשאר עד עתה מוקף
הפריט וההרכב שלו השתנה מ 0.6%-פחמן ל 0.77%-פחמן המשך קירור אל מתחת ל 727-מעלות
צלזיוס יגרום לכל האוסטניט שנשאר להפוך לפרליט על ידי ריאקציה אוטקטואידית .המבנה מכיל כעת
שתי פאזות – פריט וצמנטיט – המאורגנים כשני מיקרו-מרכיבים – פריט ופרליט .המיקרו-מבנה הסופי
מכיל איים של פרליט המוקפים ב"ים" מוצק של פריט.
בסגסוגות היפראוטקטואידיות ,הפאזה הראשית היא צמנטיט ,הנוצר בגבולות הגרעין של האוסטניט.
לאחר שהאוסטניט מתקרר ועובר את הריאקציה האוטקטואידית ,הפלדה מכילה צמנטיט פריך המוקף איים
של פרליט.
עמוד 26מתוך 28
פרק – 7דיאגרמת פאזות
דיאגרמת TTT
דיאגרמת (Time-Tempetature-Transformation) TTTהיא דיאגרמה המתארת את הזמן הדרוש
בכל טמפרטורה למעבר פאזה כלשהי )מתחילתו ועד לסופו( הדיאגרמה מניחה שהטמפרטורה נשארת
קבועה בכל התהליך .דיאגרמה זו מאפשרת לנו להעריך את המבנה ,התכונות וטיפול החום הדרוש
בפלדות שונות .הציון (Start) Sליד כל פאזה מציין את נקודת ההתחלה של מעבר הפאזה .הציון F
) (Finishמציין את סוף התהליך.
עמוד 27מתוך 28
פרק – 7דיאגרמת פאזות
עמוד 28מתוך 28
You might also like
- תרגול 4Document18 pagesתרגול 4api-26922789No ratings yet
- דף סיכום הנדסת חומריםDocument1 pageדף סיכום הנדסת חומריםapi-26922789No ratings yet
- קבוצה 6 דוח נגיפהDocument13 pagesקבוצה 6 דוח נגיפהYaniv ZilevitzNo ratings yet
- סכום סמסטר א'Document9 pagesסכום סמסטר א'api-3801666100% (1)
- נוסחאות חומרים - לילךDocument1 pageנוסחאות חומרים - לילךLEVNo ratings yet
- כימיה פיסיקלית סיכום כלליDocument54 pagesכימיה פיסיקלית סיכום כללינגה מואפיק100% (1)
- הרצאה 1Document17 pagesהרצאה 1MichaelNo ratings yet
- Crystallography PDFDocument78 pagesCrystallography PDFViswa NathanNo ratings yet
- תרגול 1Document2 pagesתרגול 1api-26922789No ratings yet
- הרצאה 11Document17 pagesהרצאה 11MichaelNo ratings yet
- Summaries 2 F 150001840037Document16 pagesSummaries 2 F 150001840037Yuval EizikNo ratings yet
- הכנה למבחן בתורת החומריםDocument17 pagesהכנה למבחן בתורת החומריםapi-2692278950% (2)
- תורת החומרים 1 סמס ב מועד BDocument4 pagesתורת החומרים 1 סמס ב מועד Bapi-26922789No ratings yet
- הרצאה 8Document16 pagesהרצאה 8Michael100% (1)
- כימיה בסיסית הנדסת מכונות בן גוריוןDocument98 pagesכימיה בסיסית הנדסת מכונות בן גוריוןLior GoldbergNo ratings yet
- הרצאה 6Document15 pagesהרצאה 6MichaelNo ratings yet
- תורת החומרים 1 סמס א מועד בDocument5 pagesתורת החומרים 1 סמס א מועד בapi-26922789No ratings yet
- הרצאה 9Document23 pagesהרצאה 9Michael100% (1)
- בוחן חלק 2 - חומריםDocument4 pagesבוחן חלק 2 - חומריםhomarimNo ratings yet
- הרצאה 10Document22 pagesהרצאה 10Michael100% (1)
- Intro 5Document8 pagesIntro 5api-26922789No ratings yet
- תורת החומרים 1 סמס א מועד אDocument5 pagesתורת החומרים 1 סמס א מועד אapi-26922789No ratings yet
- תרגול 5Document3 pagesתרגול 5api-26922789No ratings yet
- הרצאה 4Document17 pagesהרצאה 4MichaelNo ratings yet
- מבנה מולקולות קוטביותDocument36 pagesמבנה מולקולות קוטביותmikafain100% (1)
- הרצאה 12Document21 pagesהרצאה 12MichaelNo ratings yet
- פתרון מועד א - 2016 - 2017Document10 pagesפתרון מועד א - 2016 - 2017mayah sabarNo ratings yet
- Appendix Tensile TestingDocument11 pagesAppendix Tensile TestingAgam SigawiNo ratings yet
- TipulimTemiimPladot OldDocument22 pagesTipulimTemiimPladot OldEden Ben HamoNo ratings yet
- פתרונות פרק 02Document9 pagesפתרונות פרק 02api-26922789No ratings yet
- הרצאה 2Document15 pagesהרצאה 2MichaelNo ratings yet
- בוחן מתיחהDocument7 pagesבוחן מתיחהapi-3708873No ratings yet
- Lecture 2Document39 pagesLecture 2tmoney5151No ratings yet
- Ceramics Excercise4 SinteringDocument2 pagesCeramics Excercise4 SinteringerezNo ratings yet
- קריסטלוגרפיהDocument14 pagesקריסטלוגרפיהapi-26922789No ratings yet
- הרצאה 7Document20 pagesהרצאה 7Michael100% (3)
- כימיה כללית ואנליטית סיכומונהDocument20 pagesכימיה כללית ואנליטית סיכומונהמירי צבריNo ratings yet
- Hozek Homarim VeilerDocument37 pagesHozek Homarim VeilererezNo ratings yet
- בוחן קשיותDocument1 pageבוחן קשיותapi-3708873No ratings yet
- הרצאה 3Document18 pagesהרצאה 3MichaelNo ratings yet
- מבוא לחשמל ואלקטרוניקהDocument18 pagesמבוא לחשמל ואלקטרוניקהMoshe ZioniNo ratings yet
- קטלוג פלדותDocument32 pagesקטלוג פלדותeleyahobNo ratings yet
- Mechanical DocumentDocument16 pagesMechanical DocumentFELIXENGIPLASCOMNo ratings yet
- חוזק חומרים 1Document59 pagesחוזק חומרים 1David_TouitoNo ratings yet
- סיכוםDocument30 pagesסיכוםapi-3704690100% (3)
- כימיה כללית - 26.10.06Document3 pagesכימיה כללית - 26.10.06api-3738386No ratings yet
- תרגול קריסטופולוגיה חשובDocument10 pagesתרגול קריסטופולוגיה חשובapi-26922789No ratings yet
- תרמודינמיקה - עבודה אנרגיה ואנתלפיהDocument5 pagesתרמודינמיקה - עבודה אנרגיה ואנתלפיהRonit MelnikNo ratings yet
- תמיסות חומרים יונייםDocument19 pagesתמיסות חומרים יונייםBecky AverbuchNo ratings yet
- תרגילים פתורים בחוזק חומרים 1Document120 pagesתרגילים פתורים בחוזק חומרים 1FELIXENGIPLASCOM100% (1)
- תרגול 2Document5 pagesתרגול 2api-26922789No ratings yet
- כימיה פיזיקאלית סיכום קצרDocument10 pagesכימיה פיזיקאלית סיכום קצרמירי צבריNo ratings yet
- בוחן חיסוםDocument1 pageבוחן חיסוםapi-3708873No ratings yet
- Mendellevs TableDocument28 pagesMendellevs Tableתמיר רבינוביץNo ratings yet
- בדיקת קושיותDocument16 pagesבדיקת קושיותTzvi TemplemanNo ratings yet
- פרק 8 אבלינהDocument17 pagesפרק 8 אבלינהG GNo ratings yet
- תרגיל כיתה 10- קשרים בין מולקולריים ומעברי פאזהDocument7 pagesתרגיל כיתה 10- קשרים בין מולקולריים ומעברי פאזהתומר וולקNo ratings yet
- 10Document34 pages10api-38391090% (1)
- מצבי צבירהDocument2 pagesמצבי צבירהטל מרוםNo ratings yet
- מבחן פיזיקה ז2Document5 pagesמבחן פיזיקה ז2alikhalilaseelNo ratings yet
- תרגול 5Document3 pagesתרגול 5api-26922789No ratings yet
- תרגול קריסטופולוגיה חשובDocument10 pagesתרגול קריסטופולוגיה חשובapi-26922789No ratings yet
- תרגול 1Document2 pagesתרגול 1api-26922789No ratings yet
- Intro 5Document8 pagesIntro 5api-26922789No ratings yet
- תורת החומרים 1 סמס ב מועד BDocument4 pagesתורת החומרים 1 סמס ב מועד Bapi-26922789No ratings yet
- קריסטלוגרפיהDocument14 pagesקריסטלוגרפיהapi-26922789No ratings yet
- תורת החומרים 1 סמס א מועד בDocument5 pagesתורת החומרים 1 סמס א מועד בapi-26922789No ratings yet
- תרגול 2Document5 pagesתרגול 2api-26922789No ratings yet
- הכנה למבחן בתורת החומריםDocument17 pagesהכנה למבחן בתורת החומריםapi-2692278950% (2)
- פתרונות פרק 02Document9 pagesפתרונות פרק 02api-26922789No ratings yet
- תורת החומרים 1 סמס ב מועד אDocument5 pagesתורת החומרים 1 סמס ב מועד אapi-26922789No ratings yet
- תרגול 5Document3 pagesתרגול 5api-26922789No ratings yet
- תורת החומרים 1 סמס א מועד אDocument5 pagesתורת החומרים 1 סמס א מועד אapi-26922789No ratings yet
- חומר לימוד טובDocument10 pagesחומר לימוד טובapi-26922789No ratings yet
- הצעה לעבודת גמר בחומריםDocument1 pageהצעה לעבודת גמר בחומריםapi-26922789No ratings yet
- חומר למבחן בחומרים קשריםDocument7 pagesחומר למבחן בחומרים קשריםapi-26922789No ratings yet
- Intro 5Document8 pagesIntro 5api-26922789No ratings yet
- א מבואDocument4 pagesא מבואapi-26922789No ratings yet
- לקחת סיכוןDocument13 pagesלקחת סיכוןapi-26922789No ratings yet
- תרגול 2Document5 pagesתרגול 2api-26922789No ratings yet
- תרגול 1Document2 pagesתרגול 1api-26922789No ratings yet