Professional Documents
Culture Documents
265613793 Nghien cứu quy trinh sản xuất mứt ổi đong PDF
265613793 Nghien cứu quy trinh sản xuất mứt ổi đong PDF
Uploaded by
Khải PhanOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
265613793 Nghien cứu quy trinh sản xuất mứt ổi đong PDF
265613793 Nghien cứu quy trinh sản xuất mứt ổi đong PDF
Uploaded by
Khải PhanCopyright:
Available Formats
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.
S Nguyễn Lệ Hà
MỞ ĐẦU
Trong những loại quả ở Việt Nam, trái ổi là loại khá phổ biến vì điều kiện nước
ta rất thích hợp cho việc sinh trưởng và phát triển của cây ổi. Trái ổi không chỉ ăn tươi mà
còn dùng làm nguyên liệu để chế biến các sản phẩm như nước ổi, mứt ổi, ngâm chua
ngọt…các sản phẩm này được làm từ trái ổi Xá lỵ có mùi thơm rất đặc trưng, vị chua
ngọt hài hòa và rất được ưa chuộng.
Tuy nhiên các sản phẩm từ ổi và công nghệ chế biến từ trái ổi Xá lỵ này trên thị
trường Việt Nam hiện nay chưa được phổ biến rộng rãi.
Với sự phát triển của kinh tế vườn, cây ổi chiếm một diện tích khá đáng kể
nhưng trái ổi được sử dụng mới chỉ dừng lại ở dạng quả tươi, chưa có giá trị kinh tế
cao, đặc biệt trong thời gian thu hoạch, nếu ổi tiêu thụ không hết sẽ làm thiệt hại kinh tế
của các nhà làm vườn vì trái ổi Xá Lỵ rất dễ chín và bị hỏng sau thu hoạch nếu không tiêu
thụ kịp thời.
Với mục đích đa dạng hóa sản phẩm để tạo ra sản phẩm vừa tiện lợi, vừa kinh tế và có
chất lượng cao đối với người tiêu dùng. Trong khuôn khổ Đồ Án này và với sự đồng ý của
giáo viên hướng dẫn, em xin được trình bày đề tài “Nghiên cứu quy trình sản xuất mứt ổi
đông”
SVTH: Đỗ Nguyễn Nam Hoa Trang 1
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
CHƯƠNG I: TỔNG QUAN NGUYÊN LIỆU
1.1 Tìm hiểu về nguyên liệu ổi
1.1.1 Nguồn gốc và phân loại
Ổi có tên khoa học: Psidium gayava, thuộc họ Myrtaceate (họ Sim).
Ổi có nguồn gốc ở vùng nhiệt đới châu Mỹ (Brazil hoặc đảo Antille) du nhập vào Việt Nam
do người Tây Ban Nha mang sang Ấn Độ, Philippin và sau đó phổ biến ở tất cả các xứ nóng.
Không chỉ phát triển tốt ở các nước nhiệt đới mà cả ở một số vùng á nhiệt đới như các nước xung
quanh Địa Trung Hải, phía nam nước Pháp, Florida, California (Mỹ) đều trồng ổi khá phổ biến.
Ổi còn có tên là thạch lựu cầu, phan thạch lựu. Người pháp gọi là Goyavier. Người Anh gọi là
Guava, Ý gọi là Peraindiana, Đức gọi là Guajave.
Việt Nam đâu đâu ổi cũng mọc, ở đồng bằng cũng như miền núi, trừ những núi cao. Miền Nam
cũng như miền Bắc, không hiếm những rừng ổi, rặng ổi hoàn toàn không được chăm sóc và mùa
mưa tháng 8 có nơi quả chín nhanh và nhiều đến độ hái không kịp, làm thức ăn cho chim chóc và
rụng đầy mặt đất. Khoảng năm 1950, ổi Xá lỵ được xem là một món quà quen thuộc, rẻ tiền, và
đặc sắc của người dân miền Tây.
Ở Việt Nam, ổi được trồng ở cả hai miền Nam và Bắc. Tuy nhiên, chỉ ở Miền Nam ổi mới
được trồng tập trung và quy hoạch thành từng vùng lớn như ở đồng bằng sông Cửu Long. Có
nhiều loại ổi tồn tại trong sản xuất ở nước ta cũng như trên thế giới. Tuy nhiên sự mô tả một cách
có hệ thống những giống này chưa được thực hiện đầy
đủ. Hiện nay có một số loại ổi phổ biến sau:
- Ổi Xá lỵ:
Cây mọc khỏe nhưng không cao, lá to, tán thưa, thịt
quả dày, ít hạt, khi chín thịt quả mềm trái mềm, ngon,
giòn, ngọt, tỷ lệ hạt trong trái thấp.
Giống ổi này có nguồn gốc từ Indonesia di thực vào
nước ta từ lâu.
Cây tăng trưởng nhanh, mau ra trái, cây chiết bắt đầu Hình 1.1: Ổi Xá lỵ
cho ra trái sau 8 tháng trồng. Ổi Xá lỵ cho trái quanh năm, trái nặng 165-250g, dạng tròn hay
dạng hình trứng, màu xanh nhạt hay màu vàng khi trái chín.
SVTH: Đỗ Nguyễn Nam Hoa Trang 2
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
- Ổi Bo Thái Bình:
Cây cao 3- 4m, quả to (trọng lượng trung bình 100-200g/quả), cùi dày, ruột nhỏ, ít hạt, thịt
quả giòn và thơm. Đây là giống ổi rất thích hợp cho mục đích ăn tươi và chế biến đóng hộp.
Hình 1.2: Ổi Bo
- Ổi Trâu:
Thường được nhân giống bằng hạt, do đó ổi có
nhiều hình dạng. Trái dài hình tròn hay hình quả lê,
vỏ xám đậm, trái nặng 100-150g, thịt trái màu hồng
khi chín, có vị chua ngọt và tương đối ít hạt.
- Ổi Sẻ:
Trái nhỏ, nặng 50-70g, trái tròn, thịt trái màu
hồng, tỷ lệ hạt trong trái cao, trái có vị chua ngọt.
Hình 1.3: Ổi Trâu - Ổi Đào:
Đây là các giống ổi ruột có màu đỏ. Quả có hình cầu, cùi dày,
ruột bé có màu hồng đào, ít hạt. Thịt quả mềm, khi chín có mùi
thơm hấp dẫn.
- Ổi Mỡ:
Quả có hình tròn, nhỏ, trọng lượng quả từ 40 – 50g/quả, thịt
quả dày, mịn, màu trắng, ruột bé, ít hạt. Khi chín, vỏ có màu vàng
Hình 1.4: Ổi Mỡ
trắng, thịt quả có mùi thơm mạnh.
SVTH: Đỗ Nguyễn Nam Hoa Trang 3
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Bảng 1.1: Đặc điểm một số giống ổi trên thế giới
STT Vị trí địa lý Giống ổi Đặc điểm
1 Hawaii Hồng Kông Prink Trái không lớn, ruột dày, ít hột, ngọt
Beaumont Trái khá lớn, ruột trắng, hơi chua
2 California Pertuier Trái khá lớn, ruột vàng, ngọt, ngon
3 India Lucknon 49 Trái khá lớn, ruột trắng, dày, ngọt
Beaumont Trái khá lớn, ruột trắng, hơi chua
4 Trinidad Centeno Polific Trái khá lớn, ruột trắng, ngon
1.1.2 Đặc điểm
Cây ổi là loại cây mọc như bụi, nhiều chồi có thân cong queo, đầy vỏ tróc, cao từ 3-10 m,
đường kính thân tối đa 30 cm. Cành nhỏ có cạnh vuông, lá mọc đối, hình bầu dục, có cuống
ngắn, phiến lá có lông mịn ở mặt dưới, hoa màu trắng, mọc ra từ kẽ lá. Hoa ổi màu trắng, thỉnh
thoảng có phơn phớt hồng, thơm dịu, mọc đơn chiếc hay từng khóm ở nách lá vừa mới mọc
xong. Trái to nhỏ khoảng 3-10 cm, tròn, hình bầu dục hay hình quả lê. Vỏ vàng nhưng ruột màu
trắng, vàng, hồng hay đỏ. Trái ổi nặng từ 30-40g đến 500-600g, tùy theo giống ổi mà chứa nhiều
hạt hay ít. Cần khoảng 100 ngày từ khi hoa nở đến khi trái chín. Ở vùng khí hậu có mưa nắng rõ
rệt thì chỉ có một mùa ổi chín nhưng ở vùng xích đạo mưa nắng quanh năm thì có đến hai mùa ổi
chín.
Thân cây: Thân cây chắc, khỏe, ngắn vì phân cành sớm. Thân nhẵn nhụi rất ít bị sâu đục, vỏ
già có thể tróc ra từng mảng phía dưới lại có một lượt vỏ mới cũng nhẵn, màu xám, hơi xanh.
Cây trưởng thành nhanh, cây có thể cao tới 10m, thân đâm nhiều nhánh, thấp gần mặt đất và
thường tạo nhiều chồi rễ mọc ở gần thân. Thân nhánh non có cạnh, vỏ sần sùi màu xanh. Thân
nhánh già hình tròn, trơn láng, vỏ màu vàng hơi nâu đỏ và tróc ra khi già.
Lá: Lá nguyên mọc đối dài từ 5- 15 cm, rộng 3-6,5cm, màu xanh đậm và nhẵn ở mặt trên, hơi
uốn cong và có màu xanh đục, ở mặt dưới thường có lông. Phiến lá hình trứng hay hình bầu dục,
hơi nhọn ở đầu. Gân lá khắc sâu lên ở mặt trên và nổi gồ lên ở mặt dưới. Lá có nhiều tinh dầu
thơm.
Hoa: Hoa ổi lưỡng tính, đơn độc hay thành chùm 2-3 hoa, có màu trắng, thỉnh thoảng có
phơn phớt hồng, thơm dịu, ít khi ở đầu cành mà thường mọc ở nách lá trên chồi non. Cuống hoa
SVTH: Đỗ Nguyễn Nam Hoa Trang 4
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
mảnh khảnh, đài hoa dài từ1-1,5cm, màu xanh vàng, chia 4-5 thùy khi hoa nở và không rụng
trong lúc trái phát triển. Hoa ổi có 4-5 cánh, hình bầu dục, màu trắng, bầu noãn màu xanh, có 4-5
buồng và có nhiều hạt. Hoa ổi thụ phấn vào buổi sáng, kéo dài khoảng 2 giờ, thường tự thụ phấn,
tuy nhiên vẫn có thể tự thụ phấn chéo được do thu hút ong và côn trùng đến hút mật. Tỷ lê thụ
phấn chéo trên cây ổi tùy thuộc vào giống. Ổi có thể trổ hoa quanh năm trong điều kiện khí hậu
ấm áp.Tuy nhiên sự phân hóa mầm hoa mạnh ở nhứng chồi phát triển đầu tiên trong mùa so với
các chồi mọc sau.
Trái: Trái ổi có hình tròn, trứng hay quả lê, luôn còn dấu vết của đài hoa. Kích thước trái thay
đổi tùy giống, dài 5-12cm, nặng 30-600g tùy giống. Vỏ trái cứng, gồ ghề hay trơn láng, màu xanh
đậm, xanh nhạt hay vàng. Thịt trái có màu trắng, vàng, hồng hay đỏ, ngọt hay chua, có mùi thơm
và mềm khi trái chín.
Hạt: Hạt nằm lẫn trong thịt trái, nhỏ, hình thận, cứng, có màu vàng nhạt hay màu nâu vàng.
Các hạt xếp thành hàng và tập trung ở phần giữa của thịt trái. Hạt ổi vẫn có khả năng nảy mầm
tốt sau khi đi qua bộ phận tiêu hóa của người và động vật.
Điều kiện sinh thái:
Ở vùng nhiệt đới có thể trồng ổi ở độ cao 0 – 1200m so với mặt nước biển.
Ổi chịu được khí hậu sa mạc cũng như khí hậu nhiều mưa và mọc bình thường, không cần
tưới nước nếu lượng mưa giới hạn từ 1000 – 4000mm. Dưới 1000mm và nhiệt độ cao thì phải
tưới, nếu không cây sẽ còi cọc.
Ổi là một trong những cây ăn quả chịu nước ngập lâu nhất, hơn những cây ăn quả khác như
đu đủ, chuối, dứa, mít, vải, nhãn, cam, bưởi,..
Ổi trồng được ở nhiều loại đất, pH thích hợp từ 4,5 đến 8,2. Muốn đạt sản lượng cao chất
lượng tốt phải chọn đất tốt, sâu và phải bón phân đủ và hợp lý. Ổi không sợ gió nhưng giống quả
to lá to khi bị bão bị rách lá, sẽ rụng quả. Vậy nên chọn chỗ khuất gió hoặc trồng hàng rào chắn
gió.
1.1.3 Thành phần hóa học
Thành phần dinh dưỡng của quả ổi: trong thịt quả có chứa một hàm lượng vitamin C gấp 3 –
4 lần so với cam và một lượng chất xơ rất cao, do đó năng lượng do chúng cung cấp thấp so với
trọng lượng (55KJ/100g thịt quả). Ngoài ra, thịt quả còn chứa một số chất có hoạt tính sinh học
quan trọng tự nhiên rất cần thiết cho sự phát triển của cơ thể như vitamin niacin, axit pantothenic,
SVTH: Đỗ Nguyễn Nam Hoa Trang 5
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
thiamin, riboflavin và vitamin A cùng với các khoáng chất như photpho, canxi, sắt, magiê và
protein.
Ổi là loại quả có hàm lượng nước chiếm tỷ lệ tương đối cao (82 – 85%). Hàm lượng glucid
trong ổi ở mức thấp (7,1 – 7,9%), trong đó hàm lượng đường ở mức trung bình đối với một số
loại quả thông thường (6 – 9%), phần còn lại là glucoza và fructoza với tỷ lệ tương đương nhau.
Lượng axit hữu cơ trong ổi không đáng kể (0,2 – 0,3%), trong đó chủ yếu là axit citric. Ngoài
ra còn có các axit malic, fumaric, glycollic tạo cho ổi có vị hơi chua dịu.
Các nghiên cứu cho thấy có khoảng 154 hợp chất bay hơi đã được tìm thấy trong quả ổi tạo ra
hương thơm hấp dẫn mà chủ yếu là các hợp chất của carbonyl, este của rượu thơm, cồn,
hydrocarbon và hỗn hợp các chất bay hơi khác. Một trong số chúng là methyl benzoat,
pphenylethyl axetat, cinnamyl axetat, hexanon và β-ionon, đặc biệt cinnamyl axetat là một trong
những hợp chất bay hơi chính tạo nên hương thơm đặc trưng cho ổi. Ngoài các thành phần có giá
trị dinh dưỡng, trong quả ổi có chứa một lượng pectin đáng kể (chiếm khoảng 1,0 – 1,5%).
SVTH: Đỗ Nguyễn Nam Hoa Trang 6
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Bảng 1.2: Thành phần hóa học trong 100g trái ổi
Thành phần hóa học Đơn vị Trong 100g thịt trái
Nước g 84,10
Năng lượng Kcal 51,00
Protein g 0,82
Lipit tổng g 0,60
Glucid tổng g 9,88
Pectin g 3,40
Tro g 0,60
Chất khoáng
Ca mg 20,00
Fe mg 0,31
Mg mg 10,00
P mg 25,00
K mg 284,00
Na mg 3,00
Zn mg 0,23
Cu mg 0,10
Mn mg 0,14
Se mcg 0,06
Vitamin
Vitamin C mg 183.50
Thiamin mg 0,50
Riboflavin mg 0,50
Niacin mg 1,20
Pantothenic acid mg 0,15
Vitamin B6 mg 0,14
Vitamin A IU 792,00
Vitamin E Mg ATE 1,12
Bảng1.3: Hàm lượng acid ascorbic trong một số giống ổi
Hàm lượng acid ascorbic
Vị trí địa lý Giống ổi
(mg/100g)
Florida Red Cattley 29,10
Florida Yellow Cattley 39,10
Florida Common Cattley 23-486
Hawaii Red Cattley, White Cattley 25-50
Hawaii Common 96,306
California Common 50-352
Puerto Rico Common 50-442
Ấn Độ Country 299
SVTH: Đỗ Nguyễn Nam Hoa Trang 7
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Ấn Độ Hill 11-19
Australia Large Yellow 110
1.1.4 Giá trị dinh dưỡng
Ổi là một trong số loại trái cây có giá trị dinh dưỡng cao nhất. PGS.TS Trần Đình Toán,
Trưởng khoa dinh dưỡng bệnh viện Hữu Nghị cho biết trái ổi chứa ít chất béo bão hoà,
cholesterol và natri nhưng chứa nhiều chất xơ ăn kiêng, vitamin C, A, kẽm, kali và mangan.
Loại quả bình dị này mang lại nhiều lợi ích cho sức khỏe của con người:
Giảm nguy cơ ung thư: ít ai biết được rằng lượng vitamin C hiện diện trong ổi cao gấp
bốn lần so với cam. Vitamin C, là một chất chống oxy hóa hiệu nghiệm, giúp bảo vệ các tế
bào không bị hư hại bởi các gốc tự do. Lượng chất chống oxy hóa trong cơ thể quá cao không
chỉ gây tổn hại cho các màng tế bào mà còn góp phần làm phát triển bệnh tim cũng như ung
thư.
Giảm nguy cơ tiểu đường: chất xơ là một trong những chất được quan tâm nhiều nhất vì
chúng có khả năng ngăn ngừa được nhiều căn bệnh bao gồm cả tiểu đường bằng cách làm
chậm quá trình hấp thụ đường của cơ thể.
Tăng cường thị lực: do ổi là nguồn cung cấp vitamin A khá tốt.
Điều chỉnh huyết áp: ổi chứa nhiều kali, kali hoạt động như một nhân tố quan trọng trong
việc điều chỉnh mức huyết áp bằng cách hủy bỏ vai trò của natri, vốn là nguyên nhân gây ra
sự mất cân bằng và ổn định của mức huyết áp.
Giúp tuyến giáp khỏe: ổi có khá nhiều đồng, có vai trò trong quá trình trao đổi chất diễn
ra ở tuyến giáp, đặc biệt là sự sản xuất và hấp thu hormone.
Giúp cơ thể sử dụng những dưỡng chất then chốt: Mangan là một trong những chất dinh
dưỡng chủ yếu của cơ thể, đóng vai trò là một cơ quan hoạt hóa enzyme, bao gồm các
enzyme chịu trách nhiệm sử dụng một số dưỡng chất then chốt như biotin, thiamin và axit
ascorbic. Ổi chính là loại trái cây chứa nhiều mangan.
SVTH: Đỗ Nguyễn Nam Hoa Trang 8
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Thư giãn thần kinh và cơ bắp: ổi chứa magiê nên ăn vài quả ổi chính là cách để làm cho
hệ thần kinh và các cơ được thư giãn.
Giúp não luôn khỏe: Các vitamin nhóm B đóng vai trò thiết yếu trong chức năng hoạt
động của não. Ổi lại giàu vitamin B3 và B6. Vitamin B3, hay còn gọi là niacin, có tác dụng
kích thích chức năng của não và đẩy mạnh sự lưu thông của máu. Trong khi đó, vitamin B6
(pyridoxine), là một chất dinh dưỡng quan trọng đối với sự hoạt động của não và hệ thần
kinh.
Đẹp da: Ăn ổi thường xuyên chính là một thói quen tốt, giúp bổ sung thêm vitamin E cho
da. Nhờ khả năng chống oxy hóa, vitamin E sẽ duy trì sự khỏe mạnh cho da.
Ổi chín có tác dụng bổ dưỡng, kiện tỳ, trợ tiêu hóa, thường dùng trong các trường hợp táo
bón, ăn uống không tiêu, xuất huyết, đái tháo đường, PGS.TS Trần Đình Toán còn cho biết
thêm các chất dinh dưỡng trong ổi như vitamin C, carotenoids có tác dụng bồi dưỡng hệ tiêu
hóa. Ổi còn kiêm chức năng hỗ trợ ruột và dạ dày trong trường hợp những bộ phận này bị
viêm nhiễm. Ổi cũng giàu chất xơ, do đó ăn ổi sẽ giúp ruột giữ nước, làm sạch hệ tiêu hóa và
các dịch bài tiết.
Đây cũng là loại trái cây còn giúp làm giảm cholesterol trong máu, ngăn ngừa quá trình
làm máu trở nên đặc, vì vậy làm tăng tính linh động của máu, giúp máu lưu thông trong cơ
thể dễ dàng hơn.
Lưu ý khi ăn ổi lượng vitamin C trong ổi lại tập trung chủ yếu ở phần gần lớp vỏ. Vì vậy,
nên rửa thật sạch ổi và ăn cả vỏ để có thể tận dụng được hết lượng vitamin có trong ổi. Khi ăn
ổi chín, cũng nên bỏ hạt ổi vì hạt ổi khó tiêu, gây trở ngại cho hệ tiêu hóa.
1.1.5 Thu hoạch và bảo quản
Trồng từ hạt, ổi được thu hoạch sau khoảng 4 năm. Trồng bằng cành chiết chỉ cần 2 năm, có
thể ít hơn. Quả chín thì màu xanh lạt đi, sau chuyển vàng, vỏ quả nhẵn, nắn thì mềm hơn. Trẻ em
thường bấm bằng móng tay, móng cắm phập vào là quả sắp chín. Không để trên cây lâu được vì
chín nhanh, chim đến mổ.
SVTH: Đỗ Nguyễn Nam Hoa Trang 9
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Từ hoa đến quả chỉ cần hơn 3 tháng. Ở miền Bắc, ổi thường chín vào giữa mùa hè lúc này
mưa nhiều chất lượng kém, ở miền Nam điều khiển bằng đốn tỉa, tưới bón có thể chín vào cuối
năm, mùa khô chất lượng tốt hơn khi chín vào mùa mưa. Tuy nhiên có thể có ổi chín quanh năm.
Vào năm thứ 3 – 5 năng suất có thể đạt 20 tấn/ha, vào năm thứ 6 - 7: có thể hơn 50 tấn/ha.
Hình 1.5: Bao ổi
Ổi rất mau chín, thu hoạch xong nên bán cho nhanh và để trong nhà chỉ giữ được vài ngày ở
nhiệt độ bình thường. Xử lý bằng một số hóa chất như GA3 có thể giữ được lâu hơn.
Ở phòng lạnh: độ nhiệt 5 – 15 oC độ ẩm không khí 85 – 90% có thể bảo quản được 3 – 4 tuần
lễ.
Quả ổi đã chín thường mềm, rất dễ bị dập nát do va chạm, do đó nên thu hoạch khi quả còn
ương. Thu hoạch quả bằng tay hay các công cụ thủ công (rọ, xuộc). Đựng ổi vào trong các hộp
hoặc thùng lót giấy, hạn chế va chạm cơ học khi vận chuyển.
1.1.6 Tình hình sản xuất ổi
Ổi là một loại thực vật khỏe, có thể thích nghi với các điều kiện khí hậu từ ẩm đến khô,
ngoài ra chúng còn có khả năng sinh trưởng và phát triển ở những vùng lạnh và có tuyết rơi.
Vì vậy, sản lượng ổi là rất lớn và được trồng ở rất nhiều nước trên thế giới.
Ấn Độ: Ổi được trồng phổ biến với diện tích khoảng 1,5 triệu ha và hàng năm cho sản
lượng khoảng 1,8 triệu tấn.
SVTH: Đỗ Nguyễn Nam Hoa Trang 10
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Hawaii: Đây là nơi trồng ổi lớn nhất thế giới. Năm 1996, sản lượng thu hoạch đạt 7 triệu
tấn, năm 1999 sản lượng đạt 4,8 triệu tấn. Năm 2000, sản lượng có sự gia tăng đáng kể, tăng
48,6% so với năm 1999 và đạt 7,2 triệu tấn. Phần lớn lượng ổi thu hoạch được dùng cho chế
biến và chỉ một lượng nhỏ được dùng để ăn tươi.
Malaysia: Đây là một trong những nước sản xuất ổi lớn nhất trên thế giới. Năm 1990, sản
lượng ổi của Malaysia chỉ đạt 25.200 tấn, nhưng đến năm 1995 sản lượng thu hoạch là 79.500
tấn/năm.
Ở Việt Nam: hiện nay ổi đang được trồng và phát triển thành một cây mang tính chất
thương mại. Tại Miền Bắc, ổi được trồng tập trung tại các vùng Gia Lộc, Tứ Kỳ, Thanh Hà
của tỉnh Hải Dương, Chương Mỹ, Quốc Oai, Hoài Đức của Hà Tây và Đông Dư, Gia Lâm,
Hà Nội.
Các tỉnh phía Nam ổi hiện đang được xếp vào loại trái cây có thế mạnh ở Đồng bằng sông
Cửu Long. Diện tích ổi tăng theo từng năm và thị trường tiêu thụ cũng rộng mở. Tuy nhiên,
do nhà vườn vẫn áp dụng phương pháp canh tác cũ nên chất lượng, mẫu mã chưa đáp ứng
được yêu cầu của thị trường. Chính vì vậy, áp dụng tiến bộ kỹ thuật vào sản xuất là việc cần
làm ngay. Cùng với nhiều loại cây ăn trái khác, ổi đã thực sự trở thành nông sản hàng hoá ở
Đồng Bằng Sông Cửu Long từ nhiều năm nay.
Sản lượng ổi không chỉ đáp ứng nhu cầu trong vùng mà còn được tiêu thụ ở nhiều tỉnh thành
trong nước, trong đó TP.Hồ Chí Minh là thị trường lớn nhất. Với 1.197ha (sản lượng 27,525 tấn),
Tiền Giang trở thành địa phương có diện tích ổi lớn nhất vùng, với nhiều giống khác nhau: ổi sẻ,
ổi bom, ổi xá lỵ, ổi Đài Loan, ổi không hạt Thái Lan,... Hiện ở Đồng Bằng Sông Cửu Long, giống
ổi xá lỵ được trồng nhiều nhất nhờ ưu điểm trái to, da hơi trắng vàng và láng, ít hạt, thịt dày, giòn,
vị chua ngọt. ổi xá lỵ nghệ cho năng suất cao, đối với những vườn 2 - 4 tuổi, nếu được chăm sóc
tốt, có thể đạt năng suất 20-60 tấn/ha/năm, từ 5 năm tuổi trở đi đạt 70 tấn/ha/năm.
Giống ổi không hạt đang được nhiều nhà vườn nhân rộng. Giống ổi Xá lỵ sần tuy giá bán ở mức
trung bình khá, nhưng trái khá ngon, hương vị đậm đà và có thị trường tiêu thụ khá bền. Cũng
như nhiều loại nông sản hàng hoá khác, trái ổi chịu sự lên xuống về giá theo mùa vụ. Các tháng
mùa nắng (từ tháng 12 đến tháng 4 năm sau - ở Nam Bộ), giá thường cao hơn các tháng mùa mưa
SVTH: Đỗ Nguyễn Nam Hoa Trang 11
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
(tháng 6 đến tháng 10). Tháng mùa nắng thường xảy ra tình trạng ổi không đủ đáp ứng nhu cầu
thị trường, do vậy giá khá cao.
1.1.7 Một số sản phẩm từ ổi trên thị trường
Trên thế giới, các sản phẩm từ ổi đã được sản xuất nhiều nhưng chủ yếu là nước ép ổi, tiếp
đến là các sản phẩm đóng hộp khác như mứt ổi. Chúng là một trong những mặt hàng chế biến từ
ổi được các thị trường lớn như Mỹ, Canada, Anh...ưa chuộng. Ở Việt Nam, quả ổi đang được chế
biến thành nước quả và đã có một số nhà máy chế biến như Nhà máy xuất khẩu Đồng Giao, Công
ty sữa Vinamilk...nhưng công suất còn hạn chế. Các sản phẩm được sản xuất hiện có trên thị
trường chủ yếu ở dạng Nectar và được chế biến từ puree nhập khẩu của nước ngoài.
Việt Nam có một điều kiện sinh thái rất đa dạng và phong phú nên có tiềm năng phát triển về
cây ăn quả trong đó có quả ổi với nhiều chủng loại có hương vị và màu sắc độc đáo. Đây thực sự
là nguồn nguyên liệu quý báu, tạo điều kiện thuận lợi cho sự phát triển của ngành công nghiệp
sản xuất ở nước ta.
Một số sản phẩm từ ổi trên thị trường:
Puree ổi:
Ổi được nghiền, chà, thanh trùng, bảo quản để sử dụng trong sản xuất nectar, nước trái cây
hỗn hợp, sirô, nước quả, mứt đông. Sau khi sản xuất có thể bảo quản bằng cách lạnh đông.
Hình 1.6: Puree ổi
Nectar ổi:
Sản phẩm là dạng dịch ổi có lẫn thịt. Nước ổi đục sản xuất ở Pradesh (Ấn Độ) chứa 55- 60%
thịt quả, ở các sản phẩm khác tỷ lệ này có thể lên đến 85%. Ổi được rửa sạch, gọt vỏ, cắt miếng,
qua chà và rây, thêm acid ascorbic 0,01%. Sau đó được thanh trùng và làm lạnh ở nhiệt độ phòng.
SVTH: Đỗ Nguyễn Nam Hoa Trang 12
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Hình 1.7: Nectar ổi
Trà ổi:
Trà ổi được chế biến từ trái và lá ổi tươi.
Hình 1.8: Trà ổi
Khai thác pectin từ ổi:
Ổi là một nguyên liệu giàu pectin. Pectin là một loại hợp chất tự nhiên giúp cho quá trình
đông tụ và keo cứng thực phẩm. Kanechiro và Sherman vào năm 1946 đã tách được pectin từ thịt
quả ổi bằng cách: đun sôi 20-30 phút nguyên liệu ổi được thái nhỏ với một lượng nước bằng khối
lượng ổi. Hỗn hợp được đem lọc. Nước lọc thu được nhằm để trích ly pectin từ lượng thịt quả ổi
mới cho đến khi đạt 8,5% chất khô và khoảng 1,2% pectin. Dịch trích ly được cô đặc bằng
phương pháp chân không đến nồng độ 20%.
Mứt ổi:
Mứt quả là các sản phẩm chế biến từ quả tươi hoặc từ quả bán chế phẩm (purê quả, nước quả,
quả sunfit hoá) nấu với đường đến độ khô 65-70%. Ngoài hàm lượng đường có sẵn trong quả
người ta còn bổ sung thêm một lượng đường khá lớn.
SVTH: Đỗ Nguyễn Nam Hoa Trang 13
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Hình 1.9: Mứt ổi
1.2 Tìm hiểu về nguyên liệu phụ và phụ gia
1.2.1 Đường
Cấu tạo:
Được sản xuất chủ yếu từ mía và củ cải đường. Saccharose là một saccharide có công
thức C12H22O11 (M=342), tinh thể màu trắng dễ tan trong nước và có độ tan tăng theo nhiệt độ.
Khối lượng riêng d=1,5879g/cm3. Saccharose được cấu tạo từ hai đường đơn là α-glucose và
β-fructose. Có công thức cấu tạo:
Hình 1.10: Đường
Saccaroza là đường để hòa tan trong nước.
Chỉ tiêu cảm quan của đường tinh luyện
Hình dạng: tinh thể tương đối đồng đều, tơi khô, không vón cục.
Mùi vị: tinh thể đường cũng như dung dịch đường trong nước cất có vị ngọt, không có mùi
lạ, vị lạ.
Màu sắc: tất cả tinh thể đều trắng óng ánh. Khi pha trong nước cất dung dịch đường trong
suốt.
Chỉ tiêu chất lượng hóa lý của đường tinh luyện
SVTH: Đỗ Nguyễn Nam Hoa Trang 14
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Hàm lượng Saccharose 99,8 % chất khô
Độ ẩm 0,05 % khối lượng
Hàm lượng đường khử 0,03 % khối lượng
Hàm lượng tro 0,03 % khối lượng
Độ màu 1,2 % (độ Stame oST)
1.2.2 Acid citric
Cấu tạo:
Công thức phân tử: C6H8O7.H2O
Acid citric là chất kết tinh bán trong suốt, không màu hoặc dạng bột kết tinh màu trắng,
không hôi vị rất chua.
Có trong hầu hết các loại quả, đặc biệt quả citrus (acid
chanh)
Vị chua thanh, dễ chịu, nếu sử dụng nồng độ cao sẽ gây vị
chát.
Không màu, không mùi.
Vai trò: Hình 1.11: Acid citric
Điều chỉnh pH
Hòa tan pectin
Tạo thành dạng đông tụ (gel hóa)
Thúc đẩy thủy phân saccharose thành glucose và fructose
1.2.3 Pectin
Pectin là một tác nhân làm đông có nguồn gốc thực vật. Chúng là polysaccharide có nhiều
ở quả, củ, thân, lá, tập trung nhiều nhất ở vỏ quả: vỏ cam chứa 4,7%, vỏ chanh chứa 7%, vỏ bưởi.
Cấu tạo:
Pectin là các polysaccharide, mạch thẳng, gồm các phân tử acid D-galacturonic C 6H10O7, liên
kết với nhau bằng liên kết 1,4- glucoside. Trong đó một số gốc acid có chứa nhóm thế methoxyl
(-OCH3). Chiều dài của chuỗi acid polygalacturonic có thể biến đổi từ vài đơn vị tới hàng trăm
đơn vị acid galacturonic. Phân tử lượng của các loại pectin tách từ các nguồn nguyên liệu khác
nhau thay đổi trong giới hạn rộng tùy theo số phân tử acid galacturonic, thường vào khoảng
SVTH: Đỗ Nguyễn Nam Hoa Trang 15
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
10.000 – 100.000 Da. Trong các hợp chất dạng glucid, so về chiều dài phân tử thì pectin cao hơn
tinh bột nhưng thấp hơn cellulose.
Phân loại:
Theo nhóm methoxyl có trong phân tử:
o HMP (High Methoxyl Pectin): Nhóm có chỉ số methoxyl cao (HMP): MI >7%, trong phân
tử pectin có trên 50% các nhóm acid bị ester hóa (DE > 50%).
o LMP (Low Methoxyl Pectin): Nhóm có chỉ số methoxyl thấp: MI < 7%, khoảng từ 3 – 5%,
trong phân tử pectin có dưới 50% các nhóm acid bị ester hóa (DE ≤ 50%).
Theo khả năng hòa tan trong nước
o Pectin không hòa tan (protopectin): chủ yếu trong trái cây non, là dạng pectin không hòa tan,
chúng tạo cho quả độ cứng.
o Pectin hòa tan (methoxyl polygalaturonic): Là dạng kết hợp của pectin với araban
polysaccharide ở thành tế bào. Khi hoa quả chín, lượng protopectin giảm vì bị thủy phân
thành pectin dưới tác dụng của enzym protopectinase, pectin này tan được trong nước.
Cơ chế tạo gel:
Các pectin và acid pectinic có các nhóm hydroxyl (-OH) nên có khả năng hydrat hóa cao.
Các phân tử pectin mang điện tích âm nên chúng có khả năng đẩy lẫn nhau, do đó làm dãn
mạch và làm tăng độ nhớt của dung dịch. Vì vậy khi làm giảm độ tích điện và độ hydrat hóa sẽ
làm cho các phân tử pectin xích lại gần nhau, và tương tác với nhau tạo thành một mạng lưới ba
chiều rắn chứa pha lỏng bên trong.
Khả năng tạo gel phụ thuộc chủ yếu vào 2 yếu tố: chiều dài của chuỗi pectin và mức độ
methoxyl hóa.
o Chiều dài của phân tử quyết định độ cứng của gel: Nếu phân tử pectin quá ngắn thì nó sẽ
không tạo gel mặc dù sử dụng với liều lượng cao. Nếu phân tử pectin quá dài thì gel tạo
thành rất cứng.
o Mức độ methoxyl hóa quy định cơ chế tạo gel: Khả năng keo hóa của pectin phụ thuộc tương đối
vào mức độ hiện diện của các nhóm methoxyl. Tùy thuộc vào chỉ số methoxyl cao (>7%) hoặc
thấp (3 – 5%) ở phân tử pectin mà các kiểu kết hợp giữa chúng sẽ khác nhau trong việc tạo gel
như đã trình bày ở trên.
HMP (high methyoxyl pectin): tạo gel bằng liên kết hydro:
- Điều kiện tạo gel: Hàm lượng chất khô từ 65 ÷ 70%, pH = 2,8 ÷ 3,2; [Pectin]= 0,5 ÷ 1%
SVTH: Đỗ Nguyễn Nam Hoa Trang 16
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
- Đường có khả năng hút ẩm, vì vậy nó giảm mức độ hydrat hóa của phân tử pectin trong dung
dịch
- pH acid trung hòa bớt các gốc COO-, làm giảm độ tích điện của các phân tử. Vì vậy các phân tử
có thể tiến lại gần nhau để tạo thành liên kết nội phân tử và tạo gel. Liên kết hydro được tạo
thành giữa các phân tử pectin có thể hydroxyl – hydroxyl, carboxyl – carboxyl, hoặc hydroxyl –
carboxyl. Kiểu liên kết này không bền do đó các gel tạo thành sẽ mềm dẻo bởi tính linh động của
các phân tử trong khối gel.
- Cấu trúc gel phụ thuộc vào hàm lượng đường, hàm lượng acid, hàm lượng pectin, loại pectin và
nhiệt độ. Lượng đường thêm vào pectin có khoảng 30 ÷ 50% sacharose, ngăn cản sự kết tinh của
đường sacharose.
- Tuy nhiên cũng không nên dung quá nhiều acid vì pH quá thấp sẽ gây ra hiện tượng nghịch đảo
một lượng lớn sacharose gây kết tinh glucose và hóa gel nhanh tạo các vón cục. Khi dung lượng
pectin vượt quá lượng thích hợp sẽ gây ra gel quá cứng do đó khi dung 1 nguyên liệu có chư
nhiều pectin cần tiến hành phân giái bớt chúng bằng cách đun lâu hơn.
- Khi sử dụng 1 lượng cố định bất cứ 1 lượng pectin nào pH, nhiệt độ càng giảm và hàm lượng
đường càng cao thì gel tạo thành càng nhanh
LMP (low methyoxyl pectin): tạo gel bằng liên kết Ca2+:
- Điều kiện tao gel: khi có mặt Ca2+, ngay cả ở nồng độ < 0,1%, không cần đường và acid.
- Ở LMP, tỉ lệ các nhóm COO- cao, do đó các liên kết giữa các phân tử pectin sẽ được tạo thành
qua cầu nối là các ion hóa trị (II), đặt biệt là Ca2+
- Cấu trúc của gel phụ thuộc vào nồng độ Ca2+.
- Đặc điểm của gel đàn hồi
Hình 1.12: Cấu tạo của High Methoxyl pectin
Hình 1.13: Cấu tạo của Low Methoxyl pectin
SVTH: Đỗ Nguyễn Nam Hoa Trang 17
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Bảng 1.4: Ảnh hưởng của chỉ số DE của pectin lên sự tao gel
Điều kiện tạo gel
DE Tốc độ tạo gel
pH Đường (%) Ion hóa trị (II)
>70 2,8 ÷ 3,4 65 Không Nhanh
50 ÷ 70 2,8 ÷ 3,4 65 Không Chậm
<50 2,5 ÷ 6,5 0 Có Nhanh
Ảnh hưởng của đường và acid lên khả năng tạo gel của pectin:
Đường và acid là hai tác nhân đồng tạo gel của HMP, sự có mặt và nồng độ của chúng có ảnh
hưởng rất lớn đến khả năng tạo gel của HMP. Trong khi đó, cả hai nhân tố này (đường và acid)
lại ít có ảnh hưởng đến khả năng tạo gel của LMP. Tuy nhiên, cũng có ý kiến cho rằng, ngay cả
trong qúa trình tạo gel của LMP thì việc bổ sung thêm đường sẽ làm tăng độ bền của cấu trúc gel
cũng như tạo sự đồng nhất cho sản phẩm (Axelos và Thibault, 1991). Sau đây là những ảnh
hưởng của đường và acid đến quá trình tạo gel của HMP.
- Đường:
o Trong dung dịch nước, pectin ở trạng thái hòa tan là do có sự tạo thành liên kết hydro
giữa nhóm OH- của mạch phân tử pectin và H+ của phân tử nước. Khi có sự có mặt của
đường, đường đóng vai trò của chất hydrate hóa, ngậm mất phần nước đang liên kết với
pectin. Khi đó pectin trở nên không hòa tan. Cộng với tác động của ion H + từ lượng acid
sử dụng để tạo đông, H+ làm trung hòa điện tích của các gốc COO- trên mạch phân tử
pectin, tạo gốc -COOH. Vì thế sợi pectin không còn đẩy nhau mà tiến lại gần nhau từ đó
hình thành nên cấu trúc khung mạng.
o Lượng đường trong hỗn hợp pectin – đường – acid thường phải lớn hơn 50% thì mới có
khả năng tạo gel. Thông thường người ta tạo hỗn hợp có 65% đường để tiến hành tạo
đông. Nếu hàm lượng đường dùng cao hơn, sự kết tinh đường có thể xảy ra trên bề mặt
hạt keo, hoặc ngay trong hệ keo. Để có thể khắc phục hiện tượng này, như đã trình bày ở
trên, ta có thể thay thế một phần đường saccharose bằng các loại đường khác nhằm tránh
hiện tượng kết tinh đường. Với pectin chất lượng càng tốt thì thì lượng pectin dùng để gel
hóa cùng một lượng đường càng ít.
- Acid:
o Pectin chỉ có thể tạo gel trong môi trường acid có pH < 4.
SVTH: Đỗ Nguyễn Nam Hoa Trang 18
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
o Trong môi trường có ion H+, các phân tử pectin tích điện âm sẽ bị trung hòa và khi ở dạng
trung hòa điện thì dễ đông tụ hơn. Hơn nữa, ion H + sẽ thay thế các ion kim loại (nếu có)
trong nhóm cacboxyl của phân tử pectin và chuyển dạng muối pectat (không tạo đông)
thành dạng pectin (có tạo đông).
o Acid sử dụng để tạo đông cần có mức độ phân ly cao hơn acid pectic để acid này có thể
ngăn cản sự phân ly của acid pectic, và giữ cho chúng ở dạng trung hòa điện tích.
o Nồng độ ion H+ càng lớn thì khả năng tạo gel của dung dịch pectin sẽ càng cao. Cần duy
trì độ pH thấp để khi đun nấu sẽ gây ra quá trình nghịch đảo đường saccharose (30 – 50%
đường thêm vào pectin) để ngăn cản sự kết tinh của đường saccharose.
o Cũng không nên dùng quá nhiều acid, vì pH quá thấp sẽ gây ra sự nghịch đảo một lượng
lớn saccharose từ đó gây kết tinh glucose và hóa gel nhanh tạo nên các vón cục. Thường
dùng độ pH từ 3 đến 3,5.
o Mức độ tạo gel chỉ tăng đến một giới hạn nào đó của nồng độ acid rồi sẽ ngừng lại bởi vì
ở ngưỡng nồng độ đó toàn bộ gốc COO - của phân tử pectin đã được trung hòa điện tích.
Nên dù có tăng thêm ion H+ cũng không thể tăng thêm khả năng tạo gel. Nồng độ acid để
tạo gel dung dịch pectin phụ thuộc mức độ methoxyl của pectin cũng như hàm lượng
pectin trong dung dịch. Khi hàm lượng pectin sử dụng tăng khoảng 0,05 – 0,1% thì pH
của dung dịch có thể tăng lên 1 đơn vị.
o Nếu phải sử dụng pectin có khả năng đông tụ yếu thì nên tăng nồng độ acid lên. Nhưng
việc tăng nồng độ này lại dễ làm tăng lượng đường nghịch đảo và làm tăng tính háo nước
của sản phẩm.
1.3 Bao bì thủy tinh
Trong sản xuất đồ hộp thường sử dụng 2 nhóm bao bì:
Bao bì gián tiếp: để đựng các đồ hộp thành phẩm, tạo thành các kiện hàng.
Bao bì trực tiếp: tiếp xúc với thực phẩm, cùng với thực phẩm tạo thành một đơn vị sản phẩm
hàng hóa hoàn chỉnh và thường được gọi là bao bì đồ hộp đối với sản phẩm mứt quả đông ta
dùng bao bì thủy tinh. Bao bì thủy tinh bền vững về mặt hóa học, hình thức đẹp nhưng nặng, dễ
vỡ và truyền nhiệt kém.
SVTH: Đỗ Nguyễn Nam Hoa Trang 19
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Hình1.14: Bao bì thủy tinh
Yêu cầu bao bì thực phẩm:
o Không gây ngộ độc cho thực phẩm, không làm cho thực phẩm biến đổi chất lượng,
mùi vị , màu sắc.
o Chịu được nhiệt độ và áp suất cao
o Bền đối với tác dụng của thực phẩm
o Truyền nhiệt tốt, chắc chắn, nhẹ
o Dễ gia công, rẻ
o Dễ dàng trong sử dụng, vận chuyển và bảo quản
Trước khi sử dụng bao bì phải được kiểm tra lại phẩm chất và rửa sạch.
Các loại bao bì thủy tinh thường nhiễm bẩn và khó rửa sạch hơn bao bì kim loại, phải rửa kỹ
bằng hóa chất. Các dung dịch kiềm ( NaOH, KOH, Na 2CO3) thường làm cho thủy tinh bị mờ vì
tạo nên mặt thủy tinh các hợp chất Calxi carbonat. Dung dịch hỗn hợp của NaOH 3%, Na 3PO4
1% và Na2SiO3 không làm mờ thủy tinh. Để sát trùng lọ thủy tinh dùng hóa chất có chứa Cl 2 với
hàm lượng hoạt động 100mg/l. Sau khi rửa hóa chất, sát trùng, rửa lại bằng nước nóng hay nước
lã sạch, sấy khô hoặc để ráo.
1.4 Tổng quan về sản phẩm mứt quả
1.4.1 Tổng quan về mứt quả
Mứt quả là các sản phẩm chế biến từ quả tươi hoặc từ quả bán chế phẩm (purê quả, nước quả,
quả sunfit hoá) nấu với đường đến độ khô 65-70%. Ngoài hàm lượng đường có sẵn trong quả
người ta còn bổ sung thêm một lượng đường khá lớn.
SVTH: Đỗ Nguyễn Nam Hoa Trang 20
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Đường cho vào mứt quả không chỉ để tăng vị ngọt mà còn để bảo quản sản phẩm. Tế bào vi
sinh vật ở trạng thái co nguyên sinh nên bị ngừng hoạt động. Vì vậy nhiều loại mứt nấu xong có
thể không cần thanh trùng. Một số loại mứt khác có độ khô thấp hơn cần phải thanh trùng với
thời gian ngắn, chủ yếu để diệt nấm men, nấm mốc, chủ yếu để diệt nấm men, nấm mốc. Mứt quả
có hàm lượng acid cao cũng làm ức chế hoạt động của vi sinh vật.
Mứt đặc trưng ở vị ngọt và màu sắc. Mỗi loại mứt có hương thơm và vị ngọt khác nhau. Kể
tên mứt thì rất đa dạng và thú vị. Việt Nam là đất nước quanh năm hoa trái, có bao nhiêu loại quả
thì có thể chế biến thành bấy nhiêu loại mứt. Không chỉ thơm ngon, tinh khiết mà nhiều loại mứt
còn có công dụng rất tốt cho sức khoẻ.
Mứt quả được chế biến ở nhiều dạng, có thể phân loại thành các dạng sau:
Theo trạng thái cấu trúc sản phẩm:
Mứt đông:
Mứt đông là các sản phẩm chế biến từ quả tươi hoặc từ quả bán chế phẩm (puree quả, nước
quả, quả sunfit hoá) nấu với đường đến độ khô 60-65%, có bổ sung pectin hay agar để tạo gel
đông. Sản phẩm mứt nổi bật là vị ngọt, thơm đặc trưng của quả. Ngoài hàm lượng đường khá lớn
của quả, người ta còn bổ sung thêm một lượng khá lớn đường tinh khiết. Có 3 dạng:
Jelly:
- Mứt được chế biến từ nước quả trong suốt.
- Nếu nước quả sunfit hoá, trước khi nấu mứt phải khử SO 2 bằng cách đun nóng để hàm
lượng SO2 trong sản phẩm không quá 0,025%. Tùy theo độ nhớt của nước quả và độ đông của
sản phẩm mà người ta pha hoặc không pha thêm pectin.
Jam:
- Mứt đông chế biến từ puree quả, có thể dùng riêng một chủng loại hoặc hỗn hợp nhiều
loại quả, có thể dùng puree quả tươi hay puree quả bán chế phẩm.
Marmalade:
- Mứt miếng đông chế biến từ quả (tươi, sunfit hoá hay lạnh đông) để nguyên hay cắt
miếng, nấu với đường, có pha hoặc không pha thêm acid thực phẩm và pectin.
Mứt rim:
SVTH: Đỗ Nguyễn Nam Hoa Trang 21
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Chế biến từ quả tươi nguyên trái hoặc cắt miếng nấu với nước đường sao cho không bị nát.
Nước đường trong sản phẩm cần đặc sánh nhưng không đông cần tách khỏi quả. Đặc điểm có lớp
siro đường xung quanh sản phẩm, không tạo gel đông. Hàm lượng chất khô khoảng 65 - 70%.
Mứt dẻo:
Được chế biến từ quả hoặc dạng miếng, có thể dùng riêng một chủng loại hoặc hỗn hợp nhiều
loại quả. Đặc điểm của sản phẩm là mềm, hơi nước, không có lớp siro đường xung quanh. Hàm
lượng chất khô khoảng 70 - 75%.
Mứt khô:
Được chế biến từ quả hoặc dạng miếng nấu với nước đường và được sấy tới độ khô 75 - 80%,
mặt ngoài miếng mứt, đường có thể tạo thành một màng trắng đục (gọi là lớp vỏ đường).
Theo trạng thái nguyên liệu:
Mứt nhuyễn/nhừ:
Nguyên liệu: Nghiền, chà, ép quả (Jam, confiture)
Tận dụng nguyên liệu không đạt tiêu chuẩn, phần vụn của quá trình khác
Mứt miếng:
Nguyên liệu: Dạng miếng hay thỏi cắt từ trái cây nguyên liệu.
Mứt nguyên trái:
Nguyên liệu: Nguyên trái, giữ được hình dạng trái
Các loại trái nhỏ (tầm ruột, tắc, mơ…)
1.4.2 Nguyên tắc bảo quản sản phẩm mứt đông
Khử trùng kỹ lưỡng là yêu cầu kỹ thuật cần thiết để có thể giữ mứt được lâu. Rửa sạch
các dụng cụ chế biến thật kỹ, các lọ đựng mứt và cả nắp lọ cần được thanh trùng.
Bảo quản mứt ở những nơi thoáng mát, tránh xa chỗ ẩm ướt và có ánh nắng mặt trời.
Tránh đảo trộn, lắc đảo sản phẩm. Khi đã mở nắp lọ, cần cho mứt vào tủ lạnh để bảo quản.
- Trong quá trình bảo quản mứt đông có các hiện tượng:
o Thoái hóa cấu trúc (vữa):
SVTH: Đỗ Nguyễn Nam Hoa Trang 22
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Nước và cái tách rời không còn ở trạng thái đồng nhất. các yếu tố ảnh hưởng đến hiện
tượng vữa là độ acid của sản phẩm, độ tạp chất và các tác động cơ học đến sản phẩm.
Nguyên nhân:
Do bảo quản mứt ở nhiệt độ cao làm thành phần pectin bị phân hủy nhanh.
Do di chuyển, xáo động cơ học của hệ keo làm mứt vữa.
Chất tạo đông có chất lượng kém, khả năng giữ nước kém.
Hậu quả: phần cái và nước trong mứt tách rời nhau ảnh hưởng đến cấu trúc của sản phẩm.
Biện pháp: tránh đảo trộn, lắc đảo sản phẩm.
o Mốc:
Nguyên nhân: do nhiễm vi sinh vật (nấm mốc, nấm men, vi khuẩn).
Hậu quả: mứt có mùi hôi, vị chua, nhớt bề mặt, cấu trúc bị phá vỡ.
Biện pháp: cần chọn bao bì thích hợp, sử dụng gói hút ẩm.
1.4.3 Một số sản phẩm mứt quả trên thị trường
SVTH: Đỗ Nguyễn Nam Hoa Trang 23
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Hình1.15: Một số sản phẩm mứt quả
SVTH: Đỗ Nguyễn Nam Hoa Trang 24
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
1.4.4 Một số quy trình mứt đông từ nguyên liệu khác
Dâu
Rửa
Phân loại
Rửa
Acid citric, đường RE
Chà
Phối trộn
Bã
Pectin: Nước
Cô đặc
Rót nóng
Làm nguội, tạo đông
Jam dâu
Sơ đồ 1.1: Quy trình sản xuất mứt Jam dâu
SVTH: Đỗ Nguyễn Nam Hoa Trang 25
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Sơ đồ 1.2: Quy trình sản xuất mứt Jelly táo
SVTH: Đỗ Nguyễn Nam Hoa Trang 26
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Xử lí enzym (nếu cần)
Bao bì
SVTH: Đỗ Nguyễn Nam Hoa Trang 27
Bã
Tạp chất
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Enzymm
Pectin
Sơ đồ 1.3: Quy trình sản xuất mứt Marmalade cam
SVTH: Đỗ Nguyễn Nam Hoa Trang 28
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
CHƯƠNG II: ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU
2.1 Địa điểm nghiên cứu
Phòng thí nghiệm công nghệ thực phẩm của trường Đại học Kỹ Thuật Công Nghệ Tp Hồ Chí
Minh.
2.2 Nguyên liệu
2.2.1 Nguyên liệu ổi Xá lỵ Hạt
Nguyên liệu ổi dùng nghiên cứu trong đề tài này là ổi xá lỵ sử dụng cho nghiên cứu sản xuất
mứt ổi đông được mua tại chợ Thanh Đa, quận Bình Thạnh, Thành phố Hồ Chí Minh.
Ổi xá lỵ được sử dụng cho nguyên cứu là giống ổi được trồng tại Tiền Giang. Ổi xá lỵ sử
dụng cho nghiên cứu chọn có đặc điểm như sau:
Ổi xá lỵ mới chín tới, da vàng bóng, ruột màu hồng tươi, có trong lượng từ 120 -170g/ quà.
Tạp chất
Hình 2.1: Ổi xá lỵ
2.2.2 Đường
Đường giúp tạo gel tốt, tăng hương vị, kéo dài thời gian bảo quản và nâng cao giá trị dinh
dưỡng cho sản phẩm.
Đường dùng cho thí nghiệm là đường tinh luyện RE (Extra Refined Sugar) của công ty Cổ
phần Biên Hoà, địa chỉ tại khu công nghiệp Biên Hòa 1, tỉnh Đồng Nai, đạt các chỉ tiêu chất
lượng như sau:
2.2.3 Acid citric
SVTH: Đỗ Nguyễn Nam Hoa Trang 29
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Sử dụng acid citric của phòng thí nghiệm trường Đại học Kỹ thuật công nghệ TP Hồ Chí
Minh, xuất xứ Trung Quốc, có độ tinh khiết 99,5%.
2.2.4 Pectin
Sử dụng loại pectin của phòng thí nghiệm trường Đại học Kỹ thuật công nghệ TP Hồ Chí
Minh để nghiên cứu.
2.2.5 Nước
Nước sử dụng cho nghiên cứu gồm 2 loại nước: nước cất và nước máy.
Nước cất được lấy từ máy nước cất trong phòng thí nghiệm, sử dụng nước cất cho các quá
trình phân tích và kiểm nghiệm.
Nước máy được sử dụng cho các quá trình rửa nguyên liệu, chần, thanh trùng và vệ sinh các
dụng cụ, máy móc thiết bị…
Nước máy sử dụng phải đạt được các chỉ tiêu chất lượng như sau:
Bảng 2.1: Tiêu chuẩn chất lượng nước dùng trong công nghiệp thực phẩm
Chỉ tiêu Tiêu chuẩn
Chỉ tiêu vật lý
Mùi vị Không
Độ trong (ống Dienert) 100ml
Màu sắc (thang màu Coban) 50
Chỉ tiêu hóa học
pH 6,0 – 7,8
Cao 50 – 100 mg/l
MgO 50 mg/l
Fe2O3 0,3 mg/l
MnO 0,2 mg/l
BO43- 1,2 – 2,5 mg/l
SO42- 0,5 mg/l
NH4 - 0,1 – 0,3 mg/l
NO2- Không
NO3- Không
Pb 0,1 mg/l
As 0,05 mg/l
Cu 2,0 mg/l
Zn 5,0 mg/l
F 0,3 - 0,5 mg/l
Chỉ tiêu vi sinh
Tổng số vi sinh vật hiếu khí < 100 cfu/ml
Chỉ số Coli ( số Coli/1l nước ) <20
Chuẩn số Coli ( số ml nước có 1 >50
SVTH: Đỗ Nguyễn Nam Hoa Trang 30
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Coli )
Vi sinh vật gây bệnh Không có
2.2.6 Bao bì và nắp
Sử dụng bao bì thủy tinh có chiều cao là 9 cm đường kính 5cm và nắp là nắp sắt tây.
2.3 Các thiết bị và dụng cụ sử dụng trong nghiên cứu
Khúc xạ kế pH kế
Cân phân tích Nhiệt kế
Nồi sử dụng cho bếp điện từ Bếp điện từ
Cốc thủy tinh Muỗng inox
Burret Thau rổ
Pipette…
2.4 Bố trí thí nghiệm
2.4.1 Khảo sát một số chỉ tiêu hóa học của ổi xá lỵ nguyên liệu
2.4.1.1 Xác định hàm lượng chất khô hòa tan
Dụng cụ bao gồm: Brix kế của phòng thí nghiệm
Đũa khuấy
Khăn giấy
Bình tia nước cất
Cách tiến hành: nghiền nhuyễn nguyên liệu, lấy nước và cho một giọt dung dịch lên mặt kính
của Brix kế, đậy nắp kính lại. Quan sát và đọc kết quả bằng vạch phân chia vùng sáng tối trên
thang đo. Có thể hướng kính về phía ánh sáng để thấy được rõ hơn vùng phân chia. Sau đó rửa
mặt kính bằng nước cất và dùng khăn giấy lau sạch nhẹ nhàng.
2.4.1.2 Xác định pH
Dụng cụ: máy đo pH của phòng thí nghiệm.
Cách tiến hành:
Nghiền nhuyễn nguyên liệu, lấy nước
Rửa sạch điện cực bằng nước cất, dùng giấy mềm thấm khô đầu điện cực.
Đặt điện cực vào dung dịch cần đo, bấm nút Start.
Chờ cho màn hình hiện lên dấu hiệu báo chỉ số pH không thay đổi nữa thì ghi nhận kết
quả. Sau đó nhấn Stop.
SVTH: Đỗ Nguyễn Nam Hoa Trang 31
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Lấy điện cực ra khỏi dung dịch cần đo, tráng rửa điện cực bằng nước cất, thấm khô bằng
giấy mềm.
2.4.1.3 Xác định lượng độ ẩm nguyên liệu
Nguyên tắc: Mẫu được sấy ở nhiệt độ 105oC đến khối lượng không đổi. Hàm lượng nước
được tính toán dựa trên khối lượng mất đi của quả trong quá trình sấy.
Dụng cụ bao gồm: Tủ sấy có điều chỉnh nhiệt độ
Cốc sứ
Bình hút ẩm
Cân kỹ thuật 3 số lẻ
Cách tiến hành:
Sấy cốc sứ trong tủ sấy ở 105 oC trong 1 giờ, sau đó để nguội trong bình hút ẩm và cân.
Đặt cốc vào tủ sấy, sấy tiếp 30 phút, sau làm nguội trong bình hút ẩm và cân lại. Sấy và cân cốc
tới khối lượng không đổi.
Cân mỗi mẫu 2g. Sấy ở 105oC trong tủ sấy thời gian 1 giờ 30 phút, sau đó để nguội trong
bình hút ẩm và cân. Đặt cốc lại vào tủ sấy, sấy tiếp 30 phút, sau làm nguội trong bình hút ẩm và
cân lại, sấy đến khối lượng không đổi, chênh lệch giữa 2 lần cân không quá 0,5%. Cân lại và tính
lượng nước có trong mẫu ( % khối lượng).
Lượng ẩm được tính theo công thức:
G 1−G 2
(
X = 1−
G )
x 100
X: phần trăm ẩm
G1: Khối lượng cốc và mẫu đã sấy đến khối lượng không đổi (g)
G2: Khối lượng cốc đựng mẫu đã sấy ở 105oC đến khối lượng không đổi (g).
G: Khối lượng mẫu phân tích (g)
2.4.1.4 Xác định lượng tro
Nguyên tắc: Dùng nhiêt độ cao (550 - 600oC) nung cháy hoàn toàn các chất hữu cơ, phần
còn lại sau khi nung chính là tổng số tro có trong thực phẩm cần xác định.
Dụng cụ bao gồm: Cốc sứ - Bếp điện
Cân kỹ thuật 3 số lẻ
Bình hút ẩm
Tủ sấy có điều chỉnh nhiệt độ
SVTH: Đỗ Nguyễn Nam Hoa Trang 32
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Lò nung (550-600oC).
Cách tiến hành:
Nung cốc sứ ở nhiệt độ 600oC trong vòng 1 giờ hạ nhiệt độ chén sứ từ từ bằng cách cho
vào tủ sấy ở 120oC, để nguội rồi mới cho vào bình hút ẩm.
Cân khối lượng cốc sứ, ta được m1 (g)
Khối lượng mẫu đem làm thí nghiệm m (g)
Đun cốc sứ có mẫu trên bếp điện cho tới khi mẫu cháy thành than rồi mới cho vào lò nung
ở nhiệt độ 600oC cho đến khi thấy mẫu cháy trắng hoàn toàn
Hạ nhiệt độ cốc sứ tương tự nhu trên rồi đem cân cốc sứ có chứa tro, ta được m2(g).
Tính kết quả:
Độ tro của nguyên liệu tính theo công thức:
X= ( m2−m1
m ) x 100
X: độ tro của nguyên liệu
m1: Khối lượng cốc đã sấy ở 550-600oC đến khối lượng không đổi (g).
m2: Khối lượng của cốc và tro trắng sau khi nung đến khối lượng không đổi (g).
m: Khối lượng của mẫu (g)
2.4.1.5 Xác định hàm lượng acid toàn phần
Nguyên tắc:
Dựa trên phản ứng trung hòa các acid có trong mẫu bằng dung dịch kiềm NaOH 0,1 N với
chất chỉ thị bromothymol xanh. Từ lượng dịch kiềm tiêu hao, tính được lượng acid tổng số có
trong mẫu (không tính lượng acid carbonic và SO2 tự do và liên kết có trong mẫu).
Dụng cụ bao gồm: Bình tam giác
Pipet
Hóa chất: Dung dịch NaOH chuẩn 0.1N
Chỉ thị Bromothymol xanh 1% trong cồn.
Cách tiến hành:
Xử lý mẫu:
Cân 5g mẫu, nghiền nhỏ, thêm nước cất vừa đủ 50ml, lắc đều. Sau đó để lắng lấy phần
dịch trong để định lượng.
SVTH: Đỗ Nguyễn Nam Hoa Trang 33
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Hút 10ml dung dịch cần chuẩn. Thêm vào 2 – 3 giọt bromothymol xanh. Chuẩn bằng
dung dịch NaOH 0.1N cho đến khi dung dịch xuất hiện màu xanh khá rõ.
Kết quả:
Hàm lượng acid trong dung dịch được tính theo g/l acid citric:
0,0064 x V NaOH x 1000
X=
10
= 0,64 x V NaOH (g/l)
Trong đó:
X: lượng acid quy về acid citric (g/l).
0.0064: gam acid citric ứng với 1 ml dung dịch NaOH 0.1N.
VNaOH : thể tích dung dịch NaOH 0.1N dùng để định phân (ml).
10 (ml): thể tích dung dịch hút định phân.
2.4.1.6 Xác định hàm lượng Vitamin C
Ngyên tắc:
Acid ascorbic là một hợp chất không no có chứa nhóm Endiol dễ bị oxi hóa khử thuận
nghịch, bị phá hủy nhanh dưới tác dụng của các chất oxy hóa và bền trong môi trường acid.
Vì vậy có thể định lượng acid Ascorbic bằng phương pháp chuẩn độ iod với các
phương trình phản ứng sau:
KIO3 + 5KI + 6HCl 3I2 + 6KCl + 3H2O
C7H8O6 + I2 C7H6O6 + 2 HI
KIO3 + 5KI + 6HCl + C6H8O7 3 C6H6O6 + 6 KCl + 2 HI
Dụng cụ bao gồm: Bình định mức 100ml
Pipette 10ml,
Burette 25ml,
Erlen 50ml.
Cối chày sứ
Hóa chất: HCl 1%
KIO3/KI 0,001N
Hồ tinh bột 1%
Cách tiến hành:
SVTH: Đỗ Nguyễn Nam Hoa Trang 34
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Cân 10g mẫu nguyên liệu, nghiền nhỏ trong dung dịch 10 ml HCl 1%. Chuyển dịch vào
bình định mức 100 ml, trích ly và định mức đến vạch bằng dung dịch HCl 1%. Lắc trộn đều,
sau đó lọc lấy phần dịch trong có chứa vitamin C đem đi phân tích.
Lấy 10ml dịch từ bình định mức cho vào erlen, thêm 5 giọt hồ tinh bột và đem định
phân bằng KIO3/KI 0,001N tới khi xuất hiện màu xanh.
Tiến hành song song các mẫu kiểm chứng: thay dịch chiết Vitamin C bằng dung dịch
10 ml HCl 1%, 5 giọt hồ tinh bột đem đem định phân bằng KIO3/KI 0,001N
Tính kết quả:
Hàm lượng Vitamin trong mẫu thí nghiệm được tính theo công thức:
( a−b ) x 0,088 x 100 100
x= x
10 m
Trong đó: x: hàm lượng Vitamin C,mg%
a – số ml KIO3/KI 0,001N dùng định phân dịch chiết Vitamin C
b – số ml KIO3/KI 0,001N dùng định phân mẫu kiểm chứng: 6ml
100: thể tích bình định mức, ml
0,088- số mg axit ascorbic ứng với 1ml dung dịch KIO3/KI 0,001N.
m- khối lượng mẫu nguyên liệu, 10g.
2.4.1.7 Xác định hàm lượng pectin
Nguyên tắc: Dựa trên cơ sở thu nhận muối canxi pectat ở dạng kết tủa.
Dụng cụ bao gồm: Bình tam giác
Giấy lọc
Tủ sấy
Hóa chất: Dung dịch CaCl2 1N
Dung dịch NaOH 0,1 N
Dung dịch axit acetic CH3COOH 0,1N
Dung dịch AgNO3 1%.
Cách tiến hành:
Lấy 20 ml dịch quả cho vào bình tam giác 250ml, cho thêm dung dịch NaOH 0,1N để hỗn
hợp trong 7h hoặc qua đêm để xà phòng hóa hoàn toàn pectin thành axit pectic. Sau đó cho thêm
vào 50ml dung dịch CH3COOH 0,1N và để yên 5 phút, thêm 50 ml dung dịch CaCl 2 1N và để
1giờ (kết tủa pectin bằng ion Ca2+).
SVTH: Đỗ Nguyễn Nam Hoa Trang 35
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Đun sôi 5 phút và lọc qua giấy lọc đã được sấy khô đến khối lượng không đổi.
Rửa kết tủa canxi pectat bằng nước cất nóng cho đến khi không còn ion Clo nữa (thử
nước rửa bằng dung dịch bạc nitrat 1% không có kết tủa trắng).
Sau khi rửa xong cho giấy lọc có kết tủa vào chén cân và sấy ở 105 oC cho đến khối lượng
không đổi.
Tính kết quả:
Hàm lượng của canxi pectat bằng hiệu của khối lượng giấy lọc có kết tủa và giấy lọc
không.
Hàm lượng pectin (P) tính theo công thức sau:
m x 0,92 x 1000
P= g/l
V
Trong đó: m: khối lượngcủa kết tủa canxi pectat (g)
V : ml dịch quả mang đi phân tích
0,92: hệ số tính chuyển đã trừ hàm lượng canxi trong kết tủa ( nghĩa là pectin chiếm 92%
trọng lượng Canxi pectat).
2.4.2 Thí nghiệm thăm dò
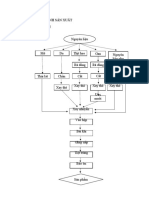
2.4.2.1 Quy trình công nghệ nghiên cứu dự kiến
SVTH: Đỗ Nguyễn Nam Hoa Trang 36
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Ổi xá lỵ
Lựa chọn Phần hư hỏng
Nước Rửa
Nước thải
Xử lý, cắt nhỏ
Núm, cuống
Chần
Pectin Chà Bã chà
Đường, acid citric
Nước Ngâm Phối trộn
Gia nhiệt
Lọ thủy tinh Rót lọ
Thanh trùng
Làm nguội Công đoạn cần
khảo sát
Jam ổi
Sơ đồ 2.1 Quy trình sản xuất dự kiến
SVTH: Đỗ Nguyễn Nam Hoa Trang 37
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
2.4.2.2 Thuyết minh quy trình
Lựa chọn nguyên liệu:
Chọn quả ổi chín mềm, màu sắc tươi đẹp, không dập úng. Chọn quả có kích thước, khối
lượng gần tương đương nhau để thuận lợi cho các quá trình tiếp theo.
Rửa sạch:
Quả mua về tùy theo độ nhiễm bẩn mà ta có thể rửa một hoặc nhiều lần để loại bổ các tạp
chất cơ học như bụi bặm, đất cát và làm giảm lượng vi sinh vật bám trên vỏ nguyên liệu. Nước
rửa sử dụng nước thủy cục, đạt tiêu chuẩn nước sạch của Bộ y tế.
Nguyên liệu sau khi rửa phải sạch, không bị dập nát. Nếu hư tổn quá nhiều, chất dinh dưỡng
rất dễ bị tổn thất làm mất giá tri dinh dưỡng của sản phẩm.
Xử lý, cắt nhỏ:
Cắt bỏ phần có giá trị dinh dưỡng thấp hay không có giá trị dinh dưỡng, không sử dụng được:
cuống và núm của quả ổi.
Cắt nhỏ trái ổi ra kích thước 2cm x 3cm chuẩn bị cho quá trình chần.
Chần:
Quá trình này được thực hiện nhằm mục đích đuổi bớt khí có trong nguyên liệu, đình chỉ các
quá trình sinh hóa của nguyên liệu và tiêu diệt vi sinh vật để hạn chế những biến đổi xảy ra trong
quá trình chế biến. Khử hoạt tính các enzym có trong thịt quả, ngăn chặn các quá trình oxy hóa
sau này làm ảnh hưởng đến màu sắc sản phẩm. Ngoài ra trong quá trình chần, dưới tác dụng của
nhiệt độ cao, thành phần protopectin không tan tồn tại trong thành tế bào sẽ chuyển thành dạng
pectin hòa tan trong dịch tế bào.
Chà:
Mục đích của quá trình chà là để thu hồi thịt quả ở dạng nhuyễn (puree) có kích thước nhỏ và
đồng nhất. Mặt khác có tác dụng loại bỏ các thành phần không có giá trị dinh dưỡng hay có giá
trị dinh dưỡng thấp như hạt, xơ ra khỏi nguyên liệu. Dùng loại rây có đường kính 0,5mm x 0,5
mm, sau đó tiến hành chà nhanh tay để tránh quá trình oxi hóa và nhiễm vi sinh vật vào nguyên
liệu.
Phối trộn:
Dịch quả trộn với đường saccharose dạng tinh thể. Tính toán lượng đường cho vào dịch nước
quả – đường hàm lượng chất khô thích hợp. Bổ sung thêm acid citric chỉnh pH dịch quả theo tỷ lệ
nhất định tạo điều kiện cho quá trình thủy phân protopectin thành pectin.
SVTH: Đỗ Nguyễn Nam Hoa Trang 38
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Pectin được bổ sung vào hỗn hợp dưới dạng past. Việc chuẩn bị pectin được thực hiện như
sau: pectin, nước theo tỷ lệ 1:19 sau đó để yên hỗn hợp đó trong vòng 24 tiếng tạo điều kiện cho
pectin trương nở hoàn toàn.
Gia nhiệt:
Là quá trình nâng cao nồng độ chất khô của sản phẩm bằng phương pháp bay hơi nước.
Mục đích là tách bớt một phần nước có trong puree làm cho sản phẩm có giá trị dinh dưỡng
cao.
Để quá trình tạo gel xảy ra, ngoài pH acid hỗn hợp cần đạt đến một độ khô thích hợp nên sau
khi phối trộn cần nâng cao nồng độ chất khô bằng cách cô đặc hỗn hợp. Ngoài ra quá trình gia
nhiệt còn diệt men và vi sinh vật có lẫn trong trong dung dịch, giúp thanh trùng dịch quả, vô hoạt
được enzym pectinase làm cho sản phẩm không bị đục, tránh sự hư hỏng của sản phẩm làm tăng
thời gian bảo quản sản phẩm.
Rót lọ:
Mứt đông thường được đựng trong bao bì thủy tinh. Khi rót nóng, lọ cần phải rửa sạch, vô
trùng bằng hơi nước và rót sản phẩm ngay để tránh nhiễm bẩn lại. Sau khi rót xong phải được
đóng nắp và quá trình rót nóng còn giúp quá trình bài khí xảy ra giúp đuổi bớt không khí có trong
bao bì.
Thanh trùng:
Mục đích: Sử dụng nhiệt độ thanh trùng để tiêu diệt vi sinh vật nhằm để bảo quản sản phẩm
được lâu hơn.
Làm nguội:
Sau khi rót sản phẩm vào bao bì, để yên sản phẩm trong vòng 24 giờ, tránh lắc đảo mạnh sản
phẩm để tạo sự ổn định cho quá trình tạo đông.
2.4.3 Khảo sát ảnh hưởng quá trình chần đến hiệu suất thu bột thịt quả ổi
Mục đích khảo sát: Ảnh hưởng của chần để có hiệu suất trong quá trình chà là cao nhất, tìm
ra thời gian chần phù hợp cho nguyên liệu.
Chỉ tiêu theo dõi: Đánh giá cảm quan của sản phẩm, hiệu suất thu dịch quả sau quá trình chà,
màu, mùi vị để chọn ra thời gian chần thích hợp nhất cho sản phẩm.
Yếu tố thí nghiệm: Thời gian chần ổi
Các nghiệm thức: Thời gian chần ổi 0; 2,5 phút; 5 phút; 7,5 phút; 10 phút
Các thông số cố định: Khối lượng ổi xá lỵ, nhiệt độ chần 90oC.
SVTH: Đỗ Nguyễn Nam Hoa Trang 39
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Cách tiến hành thí nghiệm:
Ổi được cắt miếng nhỏ, kích thước 2cm x 3cm, chia làm 5 mẫu, mỗi mẫu thực hiện 3 lần, mỗi
lần 200g tiến hành chần ở nhiệt độ 90oC với tỷ lệ nước 1:1 lần lượt với thời gian là 0; 2,5 phút; 5
phút; 7,5 phút; 10 phút. Nấu sôi đến 90oC sau đó cho ổi đã cắt vào, tiếp tục nấu cho nước đến
90oC thì giữ nhiệt độ với lẩn lượt thời gian là 0; 2,5 phút; 5 phút; 7,5 phút; 10 phút. rồi cho vào
máy xay Panasonic MJ – M176P xay với tốc độ nhỏ nhất trong 5 giây sau đó tiến hành chà qua
rây và xác định hiệu suất thu hồi dịch quả.
Sơ đồ bố trí thíỔi
nghiệm
xá lỵ đã cắt miếng nhỏ, kích thước 2cm x 3cm
Chần ở 90oC
0 2,5 phút 5 phút 7,5 phút 10 phút
Chà Bã
Xác định hiệu suất chà
Lựa chọn chế độ chần
Sơ đồ 2.2: Bố trí thí nghiệm khảo sát ảnh hưởng quá trình chần
đến hiệu suất thu bột thịt quả ổi
SVTH: Đỗ Nguyễn Nam Hoa Trang 40
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
2.4.4 Thí nghiệm thăm dò – công thức phối trộn:
Lượng dịch quả 200g; pH=2.8; lượng đường 200g
Pectin =1,5g; Acid citric=1,4g
2.4.5 Khảo sát tỉ lệ đường bổ sung
Mục đích khảo sát: Tìm ra hàm lượng đường bổ sung phù hợp ảnh hưởng đến mùi vị, cấu trúc
của sản phẩm.
Chỉ tiêu theo dõi: Đánh giá cảm quan của sản phẩm, màu sắc, mùi vị, cấu trúc sản phẩm để
chọn ra tỉ lệ đường thích hợp nhất cho sản phẩm.
Yếu tố thí nghiệm: hàm lượng đường bổ sung
Các nghiệm thức: lượng đường bổ sung lần lượt là 160g, 180g, 200g, 220g, 240g.
Các thông số cố định: Khối lượng ổi xá lỵ, nồng độ chất khô của dịch puree ổi, pH
của dịch puree ổi
Cách tiến hành thí nghiệm:
Ổi sau khi được chà qua rây, chia thành 5 mẫu, gia nhiệt đạt độ khô 10% tiến hành phối trộn
đường lần lượt là 160g, 180g, 200g, 220g, 240g. Sau đó đưa các mẫu vể pH=2,8, tiến hành gia
nhiệt và đưa về nồng độ chất khô 65%. Cuối cùng cho pectin vào tạo đông. Rót lọ, làm nguội tiến
hành đánh giá cảm quan sản phẩm.
200g dịch quả (puree quả)
Sơ đồ bố trí thí nghiệm
Bổ sung đường,acid, pectin với lượng đường
160g 180g 200g 220g 240g
Phối trộn, gia nhiệt
Rót lọ, thanh trùng, làm nguội
Đánh giá cảm quan sản phẩm
Xác định tỷ lệ thích hợp
SVTH: Đỗ Nguyễn Nam Hoa Trang 41
Sơ đồ 2.3: Bố trí thí nghiệm khảo sát lượng đường bổ sung
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
2.4.6 Khảo sát hàm lượng acid citric bổ sung
Mục đích khảo sát: Tìm ra hàm lượng acid citric bổ sung phù hợp ảnh hưởng đến vị, cấu trúc
của sản phẩm.
Chỉ tiêu theo dõi: Cấu trúc của sản phẩm.
Yếu tố thí nghiệm: hàm lượng acid citric bổ sung vào dịch quả.
Các nghiệm thức: hàm lượng acid citric bổ sung lần lượt là 1g; 1,2g; 1,4g; 1,6g; 1,8g. Thông
số cố định: Khối lượng ổi xá lỵ, nồng độ chất khô của dịch puree ổi, lượng đường
Cách tiến hành thí nghiệm:
Ổi sau khi được chà qua rây, tiến hành phối trộn đường theo tỉ lệ. Sau đó chia thành 5 mẫu
bổ sung acid citric vào lần lượt là 1g; 1,2g; 1,4g; 1,6g; 1,8g. Tiến hành gia nhiệt và đưa về
nồng độ chất khô 65%. Cuối cùng cho pectin vào tạo đông. Rót lọ, thanh trùng, làm nguội rồi
tiến hành đánh giá cảm quan sản phẩm.
Sơ đồ bố trí thí nghiệm
200g dịch quả đã bổ sung đường
Bổ sung pectin
Bổ sung acid citric
1g 1,2g 1,4g 1,6g 1,8g
Khuấy đều, gia nhiệt
Rót lọ, thanh trùng, làm nguội
Đo pH, đánh giá cảm quan về vị sản phẩm
Xác định lượng thích hợp
Sơ đồ 2.4: Bố trí thí nghiệm khảo sát hàm lượng acid citric bổ sung
SVTH: Đỗ Nguyễn Nam Hoa Trang 42
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
2.4.7 Khảo sát hàm lượng pectin bổ sung
Mục đích khảo sát: Tìm ra hàm lượng pectin ảnh hưởng đến cấu trúc của sản phẩm.
Chỉ tiêu theo dõi: Cấu trúc của sản phẩm.
Yếu tố thí nghiệm: Tỷ lệ pectin bổ sung vào dịch quả.
Các nghiệm thức: Tỷ lệ pectin 1g; 1,5g; 2g; 2,5g;
Thông số cố định: Khối lượng puree quả: đường, nồng độ chất khô của dịch puree ổi, pH của
dịch puree ổi.
Cách tiến hành thí nghiệm:
Ổi xá lỵ đã bổ sung đường, acid citric, khuấy đều. Chia thành 3 mẫu bổ sung pectin theo tỉ lệ
lần lượt: 1g; 1,5g; 2g; 2,5g;. Tiếp đó khuấy đều, gia nhiệt sau đó rót lọ và thanh trùng, làm nguội.
Tiến hành nhận xét khả năng tạo đông sản phẩm.
Sơ đồ bố trí thí nghiệm
Ổi xá lỵ đã bổ sung đường, acid citric, khuấy đều và gia nhiệt
Bổ sung pectin
1g 1,5g 2g 2,5g
Khuấy đều, gia nhiệt
Rót lọ - làm nguội
Nhận xét khả năng tạo đông, lựa chọn tỉ lệ pectin thích hợp
Sơ đồ 2.5: Bố trí thí nghiệm khảo sát hàm lượng pectin bổ sung
SVTH: Đỗ Nguyễn Nam Hoa Trang 43
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
2.4.8 Kiểm tra chế độ thanh trùng
Mục đích: Xác định công thức thanh trùng phù hợp để đảm bảo rằng trong đồ hộp không tồn
tại các vi sinh vật có thể gây hư hỏng thực phẩm và các loại tạo độc tố hoặc có thể còn sống sót
các vi sinh vật không có khả năng phát triển hay gây hư hỏng đồ hộp ở điều kiện bình thường.
Công thức thanh trùng đề nghị
Thanh trùng sản phẩm
Đo nhiệt độ tâm hộp
Xác định thời gian hiệu quả cần thiết Att
Vẽ đồ thị hiệu chỉnh công thức thanh trùng
Xác định công thức thanh trùng mới
Thanh trùng sản phẩm
Sơ đồ 2.6: Bố trí thí nghiệm kiểm tra công thức thanh trùng
Kết
2.4.9 Đánh giá cảm quan luận
bằng côngpháp
phương thứccho
thanh
điểmtrùng
Các tính chất cảm quan của thực phẩm (màu sắc, mùi, vị, cấu trúc) chiếm vị trí rất quan trọng
đối chất lượng của một sản phẩm thực phẩm do đó ta dùng phương pháp phân tích cảm quan để
đánh giá cảm quan chất lượng của sản phẩm cuối và cũng áp dụng phương pháp phân tích cảm
quan xuyên suốt trong quá trình thí nghiệm.
2.5 Các phương pháp sử dụng trong nghiên cứu
2.4.1 Phương pháp xác định các chỉ tiêu hóa học của nguyên liệu và sản phẩm
SVTH: Đỗ Nguyễn Nam Hoa Trang 44
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Xác định hàm lượng chất khô hòa tan: được xác định bằng khúc xạ kế cầm tay, nhãn hiệu
ATAGON-1
Xác định pH: được xác định bằng máy đo pH hiệu Oakion
2.4.2 Phương pháp phân tích các chỉ tiêu vi sinh của sản phẩm
Xác định Escherichia Coli theo AOAC 966.25-2005
Xác định tổng số nấm mốc – nấm men theo ISO 21527-2:2010
Xác định Clostridium Perfringens theo AOAC 976.30-2010
Tiêu chuẩn mứt đông không có vi sinh gây bệnh
2.4.3 Phương pháp đánh giá cảm quan cho từng thí nghiệm và sản phẩm cuối
2.5.3.1 Lựa chọn phép thử
Đánh giá cảm quan là phương pháp khoa học không thể thiếu trong việc đánh giá
chất lượng thực phẩm
Đánh giá cảm quan cho từng thí nghiệm
Sử dụng phép thử cho điểm thị hiếu.
Phép thử cho điểm dùng để xác định xem mức độ ưa thích của người thử đối với sản
phẩm.
Trong phép thử cho điểm này người thử sẽ nhận được đồng thời tất cả các mẫu thử
cần đánh giá. Sau khi nếm thử, người thử sẽ đánh giá mức độ ưa thích của mình đối với sản phẩm
bằng thang điểm đã được định nghĩa trước thông qua các thuật ngữ mô tả mức độ hài lòng và ưa
thích:
1: Không thích
2: Không thích cũng không ghét
3: Tương đối thích
4: Thích
5: Rất thích
Trong đó thang điểm hay thuật ngữ mô tả mức độ ưa thích do người tiến hành thí
nghiệm lựa chọn.
Đánh giá cảm quan cho sản phẩm cuối
Sử dụng phép thử cho điểm theo TCVN 3215-1979 để kiểm tra tất cả các chỉ tiêu cảm
quan (màu sắc, mùi, vị, cấu trúc…) của sản phẩm cuối.
SVTH: Đỗ Nguyễn Nam Hoa Trang 45
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Khi đánh giá tất cả các chỉ tiêu của sản phẩm cuối, ta dùng hệ điểm 20 xây dựng trên
một thang điểm thống nhất là 6 bậc 5 điểm (từ 0 đến 5).
Trong đó có 5 trong 6 bậc đánh giá (bằng chữ số 5 đến 1) ở dạng điểm chưa có trọng
lượng đối với mức độ khuyết tật của từng chỉ tiêu cảm quan.
Bậc đánh giá bằng 0 để biểu thị khuyết tật ứng với sản phẩm “bị hỏng” và không sử
dụng được nữa.
Ở điểm 5 sản phẩm coi như không có khuyết tật nào trong tính chất đang xét, sản
phẩm có tính chất đặc trưng và rõ rệt cho chỉ tiêu đó.
Bảng điểm đánh giá cảm quan cho sản phẩm mứt ổi đông được xây dựng như sau:
Bảng 2.2 Bảng điểm đánh giá cảm quan
Điểm
Hệ số
chưa có
STT Tên chỉ tiêu quan Các đặc tính cảm quan
trọng
trọng
lượng
Màu đỏ đặc trưng của sản phẩm 5
Màu đỏ nhạt, ít đặc trưng, không tươi 4
Màu đỏ sáng không bị sẫm màu 3
1 Màu sắc 1.0
Màu sắc không đặc trưng hơi sẫm màu 2
Sản phẩm bị biến màu (màu sẫm mạnh) 1
Sản phẩm bị đen, hư hỏng 0
Bề mặt phẳng, đồng nhất, cấu trúc gel mềm,
5
độ đong tốt, không bọt
Trạng thái cấu Cấu trúc tương đối, hơi bỡ hay hơi cứng 4
2 1.5 Xuất hiện bọt, cấu trúc gel hơi bỡ hay hơi
trúc 3
cứng
Bề mặt không phẳng hay nhiều bọt 2
SVTH: Đỗ Nguyễn Nam Hoa Trang 46
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Cấu trúc xấu, có độ chảy 1
Có hiện tượng tách lớp, không đong, có vật lạ 0
Mùi ổi xá lỵ rất đặc trưng, không có mùi lạ 5
Giữ được mùi thơm của ổi xá lỵ 4
Mùi thơm nhẹ của ổi xá lỵ, ít đặc trưng 3
3 Mùi 0.7
Không có mùi thơm của ổi, có mùi nấu nhẹ 2
Mùi lạ không thể chấp nhận 1
Mùi của sản phẩm hư hỏng 0
Vị hài hòa, đặc trưng của sản phẩm hấp dẫn 5
Vị hài hòa đặc trưng của sản phẩm 4
Vị kém hài hòa 3
4 Vị 0.8
Vị không hài hòa 2
Vị lạ không thể chấp nhận 1
Vị của sản phẩm hư hỏng 0
Hệ số quan trọng của mỗi chỉ tiêu cảm quan căn cứ vào đặc điểm và tính chất quan trọng của
chỉ tiêu đó đối với chất lượng sản phẩm
Bảng 2.3 Hệ số quan trọng của các chỉ tiêu
Chỉ tiêu Hệ số quan trọng
Trạng thái cấu trúc 1.5
Màu sắc 1.0
Mùi 0.8
SVTH: Đỗ Nguyễn Nam Hoa Trang 47
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Vị 0.7
Điểm cảm quan chung = điểm trạng thái cấu trúc x 1.5 + điểm màu sắc x
1.0 + điểm mùi x 0.8 + điểm vị x 0.7
Điểm cảm quan chung bằng tổng điểm cảm quan có trọng lượng của các chỉ tiêu đánh giá.
Căn cứ vào điểm cảm quan chung sẽ phân cấp chất lượng sản phẩm như sau (TCVN 3215-1979)
Bảng 2.4 Đánh giá chất lượng sản phẩm theo điểm chung
Yêu cầu về điểm trung bình chưa có
Danh hiệu chất lượng Điểm chung
trọng lượng đối với các chỉ tiêu
Loại tốt Phòng thí18.6
nghiệm
20.0 phân tích
Cáccảm quan
chỉ tiêu quan trọng nhất 4.8
Loại khá 18.5 TRẢ LỜI
15.2PHIẾU Các chỉ tiêu quan trọng nhất 3.8
Loại trung bình Phép thử
11.2 cho điểm thị
15.1 Mỗihiếu
chỉ tiêu 2.8
Loại kém (không đạt mức
Họ và tên:……….Ngày thử: ………..
chất lượng quy định trong
Giới tính: ………. 7.2 11.1 Mỗi chỉ tiêu 1.8
tiêu chuẩn nhưng còn khả
năng bán được)
Bạn nhận được
Loạicác mẫu(không
rất kém mứt ổi
có đông
khả đã được mã hóa có ký hiệu …,…, .., và ….
Bạn hãy nếm thử vàbán
năng định lượng
được nhưngmức
sau độ ứa thích của mình đối với mỗi mẫu theo thang điểm sau:
4.0 7.1 Mỗi chỉ tiêu 1.0
Không thích: 1Thích: 4 thích hợp còn
khi tái chế
Không thích không ghét:
sử dụng 2Rất thích: 5
được)
Loại hỏng
Tương đối thích: 3 (không còn sử
0 3.9 Mỗi chỉ tiêu 1.0
dụng được)
Chú ý dùng nước và bánh mì thanh vị sau mỗi lần thử
2.5.3.2 Lập hội đồng đánh giá cảm quan
Trả lời:
Gồm 10 thành viên đã được học qua bộ môn đánh giá cảm quan sản phẩm thực phẩm
2.5.3.3 Lập phiếu đánh giá cảm quan
Mẫu phiếu đánh giá cảm quan chung cho các thí nghiệm
Nhận xét: ……………………………………………………………….
SVTH: Đỗ Nguyễn Nam Hoa Trang 48
Hình 2.1 Phiếu đánh giá cảm quan cho các thí nghiệm
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Phòng thí nghiệm phân tích cảm quan
PHIẾU CHO ĐIỂM
Phép thử cho điểm chất lượng (TCVN 3215:1979)
Họ và tên:……….Ngày thử: ………..
Sản phẩm: Mứt ổi đôngChữ ký: ………….
Trả lời:
Nhận xét: ……………………………………………………………….
Mẫu phiếu cho điểm theo TCVN3215:1979
SVTH: Đỗ Nguyễn Nam Hoa Trang 49
Hình 2.2 Phiếu cho điểm theo TCVN 3215:1979
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
1 Chuẩn bị mẫu và dụng cụ đánh giá cảm quan
Mẫu thử được giữ ở nhiệt độ phòng thử 2 giờ trước khi đánh giá cảm quan và được chuẩn bị
cho từng thí nghiệm riêng biệt, lau sạch và ghi mã số trên bao bì mẫu thử.
Dụng cụ chuẩn bị cho mỗi người thử gồm: khay / đĩa tráng men trắng, dụng cụ mở hộp, và
muỗng bằng inox.
Dùng bánh mì lạt và nước trắng không mùi để thanh vị, khăn lau miệng.
2.5.3.5 Tiến hành thử
Mỗi thành viên 1 lọ sản phẩm
Xác định màu:
Cầm lọ sản phẩm lên, xoay nhẹ quan sát màu sắc, ghi nhận và cho điểm.
Xác định mùi:
Mỗi người tự mở lọ. Trước hết mở khoảng 1/3 miệng lọ, ngửi mùi sản phẩm, ghi nhận và cho
điểm.
Xác định vị, trạng thái cấu trúc:
SVTH: Đỗ Nguyễn Nam Hoa Trang 50
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Cho một ít mẫu lên đầu lưỡi, ngậm miếng mứt trong miệng, chắp miệng, đưa về cuối lưỡi
nhai và nuốt, ghi nhận trạng thái cấu trúc bên trong và mùi vị cho điểm..
2.6 Các phương pháp xử lý số liệu
Mỗi thí nghiệm trong đồ án này được thực hiện 3 lần, mỗi lần từ 3 mẫu trở lên. Kết quả thí
nghiệm trình bày trong đồ án được xử lý thống kê và loại bỏ sai số thô (nếu có) trên phần mềm
SG-Plus for win 3.0 và phần mềm Microsoft Excel 2007.
SVTH: Đỗ Nguyễn Nam Hoa Trang 51
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
CHƯƠNG III: KẾT QUẢ VÀ THẢO LUẬN
3.1 Khảo sát thành phần nguyên liệu
Chất lượng nguyên liệu là một trong những yếu tố quan trọng quyết định đến chất lượng sản
phẩm cuối cùng. Vì vậy việc khảo sát các thông số hóa học của nguyên liệu được coi là quan
trọng để đánh giá giá trị sử dụng của nguyên liệu, dễ dàng kiểm soát nguyên liệu trong quá trình
sản xuất. Trong quá trình khảo sát thành phần hóa lý của nguyên liệu, ứng với mỗi chỉ tiêu, tiến
hành thí nghiệm 3 lần, kết quả phân tích một số chỉ tiêu hóa học của nguyên liệu ổi xá lỵ được
trình bày trong bảng 3.1 sau:
Bảng 3.1 Chỉ tiêu hóa học của nguyên liệu ổi xá lỵ
Chỉ tiêu Đơn vị Giá trị
o
Chất khô hòa tan Bx 6,1
pH 4,23
Độ ẩm % 86,68
Tro % 0,58
Độ Acid g/l 0,29
Vitamin C mg/100g 200,35
Pectin g/l 1,42
Kết quả các số liệu trong bảng 3.1 cho thấy:
Ổi là loại trái có hàm lượng vitamin C cao, đạt đến 200,35 mg/100g thịt quả, cao hơn một
số loại trái như cam, bưởi (50-60mg/100g thịt quả)
Qua khảo sát một số thông số hóa học của nguyên liệu ổi Xá lỵ không chỉ cung cấp dưỡng
chất có giá tri cao mà nó còn chứa một lượng lớn chất xơ hòa tan (pectin) giúp cho quá trình
tiêu hóa được tốt hơn.
Trong khi tiến hành thí nghiệm, lựa chọn nguyên liệu là một quá trình quan trọng nó sẽ ảnh
hưởng đến những thí nghiệm và sản phẩm sau này, vì vậy ổi xá lỵ được chọn làm nguyên liệu
những quả lỵ mới chín tới, da vàng bóng, ruột màu hồng tươi, không bị sâu bệnh, không bị dập
nát hoặc hư hỏng ảnh hưởng đến mùi vị sản phẩm sẽ giúp sản phẩm có hượng vị và màu sắc đặc
trưng.
3.2 Nhận xét tính chất cảm quan của sản phẩm sau thí nghiệm thăm dò
SVTH: Đỗ Nguyễn Nam Hoa Trang 52
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Sản phẩm sau khi được thực hiện theo quy trình công nghệ dự kiến được bảo quản trong vài
ngày sau đó tiến hành đánh giá cảm quan sản phẩm:
Bảng 3.2 Kết quả nhận xét sản phẩm mứt ổi xá lỵ sau thí nghiệm thăm dò
Tính chất Mô tả
Mùi Mùi thơm nhẹ của ổi xá lỵ
Vị Vị chua chưa hài hòa. Không mùi vị lạ.
Màu sắc Màu đỏ sáng của sản phẩm.
Cấu trúc Cấu trúc chưa đồng nhất
Sản phẩm mứt ổi đông đòi hỏi phải có mùi thơm đặc trưng của ổi xá lỵ; kết quả đánh giá cảm
quan về tính chất mùi của sản phẩm cho thấy mùi ổi đặc trưng của sản phẩm là chưa đủ chỉ
thoang thoảng nhẹ.
Tóm lại, qua kết quả đánh giá cảm quan sản phẩm thí nghiệm thăm dò thì các thí nghiệm sẽ
được tiến hành bao gồm:
Khảo sát quá trình chần
Khảo sát tỷ lệ đường bổ sung
Khảo sát tỷ lệ acid citric bổ sung
Khảo sát tỷ lệ pectin bổ sung
Thiết lập và kiểm tra lại công thức thanh trùng
3.3 Xác định ảnh hưởng quá trình chần đến hiệu suất thu bột thịt quả ổi
Chần làm cho vi sinh vật bị tiêu diệt vì vậy quá trình chần làm tăng chất lượng sản phẩm và
rút ngắn thời gian thanh trùng. Trong quá trình chần dưới tác dụng của nhiệt độ cao thành phần
protopectin không tan tồn tại trong thành tế bào sẽ chuyển thành dạng pectin hòa tan trong dịch tế
bào.
Ổi được cắt miếng nhỏ, kích thước 2cm x 3cm, chia làm 5 mẫu, mỗi mẫu thực hiện 3 lần, mỗi
lần 200g tiến hành chần ở nhiệt độ 90 oC bổ sung nước tỉ lệ 1:1 lần lượt với thời gian l à 0; 2,5
SVTH: Đỗ Nguyễn Nam Hoa Trang 53
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
phút; 5 phút; 7,5 phút; 10 phút, rồi cho vào máy xay Panasonic MJ – M176P xay với tốc độ nhỏ
nhất trong 5 giây sau đó tiến hành chà qua rây và xác định hiệu suất thu hồi dịch quả.
Bảng 3.3 Ảnh hưởng nhiệt độ chần đến sản phẩm
Hiệu suất Hiệu suất chà
Khối lượng Khối lượng
Thời gian chà (%) trung bình Nhận xét
đem chần sau chà
(%)
165,20g 104,02g 62,97 Màu hồng
0 155.70g 103,98g 66,78 65,57 nhạt,có mùi
159,50g 106,80g 66,96 thơm ổi xá lỵ
151,30g 110,53g 73,05 Màu đỏ sáng,
2,5 phút 155,78g 103,00g 66,11 71,06 mùi thơm ổi xá
159,10g 117,77g 74,02 lỵ
167,82g 122,73g 73,13 Màu đỏ sáng,
5 phút 165,40g 126,43g 76,44 74,9 mùi thơm đặc
169,8g 127,69g 75,20 trưng ổi xá lỵ
168,6g 118,02g 70,00
Màu đỏ đậm,
7,5 phút 163,24g 118,96g 72,87 69,9
mùi thơm nhẹ
162,33 108,59g 66,90
142,90g 101,42g 70,97
Màu đỏ sẫm, mùi
10 phút 157,70g 108,05g 68,52 69,32
nấu
155,4g 106,38g 68,46
SVTH: Đỗ Nguyễn Nam Hoa Trang 54
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
76 74.9
74
72 71.06
69.9
70 69.32
68
66 65.57
64
62
60
0 2.5 phut 5 phut 7.5 phut 10 phut
thời gian
Từ kết quả trên nhìn hình cho thấy chần ở thời gian 5 phút cho tỷ lệ thu hồi puree cao nhất và
có màu sắc, mùi thơm đặc trưng của ổi xá lỵ
3.4 Xác định đường bổ sung
Sau khi tiến hành thí nghiệm theo sơ đồ sản phẩm được bảo quản 3 ngày rồi sau đó được
đánh giá cảm quan theo phương pháp cho điểm.
Sau đó phép thử được tiến hành với 10 người thử và mỗi người sẽ nhận được một phiếu trả
lời kèm theo các mẫu thử và được hướng dẫn cách thức đánh giá cảm quan
Và kết quả đánh giá được tập hợp trong bảng sau:
Bảng 3.4 Kết quả tổng điểm đánh giá cảm quan
Mẫu
Người thử
1 2 3 4 5
1 2 2 3 3 2
2 2 3 5 4 3
3 1 3 4 4 3
4 1 1 5 4 4
5 2 4 4 3 3
6 2 2 5 3 2
SVTH: Đỗ Nguyễn Nam Hoa Trang 55
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
7 1 3 5 4 4
8 2 3 4 3 3
9 2 1 3 3 2
10 1 2 4 3 3
Tổng 16 24 42 34 30
Trung bình 1.6 2.4 4.2 3.4 3.0
Bảng 3.5: Kết quả cảm quan khi thay đổi lượng đường
Thí nghiệm Lượng đường Nhận xét Điểm
1 160 Vị chưa ngọt 1,6
2 180 Vị chưa ngọt 2,4
3 200 Vị ngọt vừa 4,2
4 220 Vị ngọt đậm 3,4
5 240 Vị rất ngọt 3,0
4.5 4.2
4
3.4
3.5
3
3
2.4
2.5
Điểm TBCCTL 2 1.6
1.5
1
0.5
0
160 180 200 220 240
Lượng đường
Hình 3.1: Biểu đồ kết quả cảm quan khi thay đổi lượng đường
SVTH: Đỗ Nguyễn Nam Hoa Trang 56
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Đường cho vào có tác dụng tạo vị ngọt cho sản phẩm mứt, vừa có tạo gel vừa có tác dụng bảo
quản. Do đường trong mứt gây ra hiện tượng teo nguyên sinh, tạo áp suất thẩm thấu lớn.
Đường giúp tạo gel tốt, tăng vị ngọt cho sản phẩm, kéo dài thời gian bảo quản và nâng cao
giá trị dinh dưỡng cho sản phẩm.
Qua bảng trên mẫu 1 là mẫ được đáng giá thấp nhất.
Mẫu 3 là mẫu có độ ưa thích cao nhất, mẫu này có vị ngọt vừa phải, tạo vị đặt trưng cho sản
phẩm, màu sắc đẹp và có mùi thơm ổi vì vậy mẫu này được các bạn đánh giá là cao nhất.
3.5 Xác định hàm lượng acid citric bổ sung
Sau khi tiến hành thí nghiệm theo sơ đồ 2.1 sản phẩm được bảo quản 3 ngày rồi sau đó được
đánh giá cảm quan theo phương pháp cho điểm. Các mẫu sẽ được mã hóa theo bảng sau
Sau đó phép thử được tiến hành với 10 người thử và mỗi người sẽ nhận được một phiếu trả
lời kèm theo các mẫu thử và được hướng dẫn cách thức đánh giá cảm quan
Và kết quả đánh giá được tập hợp trong bảng sau:
Bảng 3.6 Kết quả tổng điểm đánh giá cảm quan
Mẫu
Người thử
1 2 3 4 5
1 1 2 4 3 3
2 2 3 5 5 3
3 1 2 3 4 2
4 2 3 4 3 4
5 3 4 5 5 3
6 2 2 4 3 4
7 2 3 5 3 3
8 2 1 4 4 3
9 3 2 3 4 4
10 2 3 4 4 3
SVTH: Đỗ Nguyễn Nam Hoa Trang 57
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Tổng 20 25 41 38 32
Trung bình 2.0 2.5 4.1 3.8 3.2
Bảng 3.7: Kết quả cảm quan khi thay đổi lượng acid citric
Thí Lượng acid citric pH Nhận xét Điểm
nghiệm
1 1 3,54 Vị ngọt đậm 2,0
2 1,2 3,33 Vị ngọt đậm 2,5
3 1,4 3,30 Vị ngọt vừa 4,1
4 1,6 2,87 Vị ngọt, chua vừa 3,8
hài hòa
5 1,8 2,62 Vị ngọt, chua hài 3,2
hòa
4.5 4.1
4 3.8
3.5 3.2
3
2.5
2.5
2
Điểm TBCCTL 2
1.5
1
0.5
0
1 1.2 1.4 1.6 1.8
lượng acid citric
Hình 3.2: Biểu đồ kết quả cảm quan khi thay đổi lượng acid citric
Acid citric được cho vào mứt vào tạo vị vừ thay đổi pH môi trường tạo điều kiện thuận lợi
cho quá trình tạo gel. Thêm vào đó acid citric là môi trường để thủy phân đường sacaroza thành
đường chuyển hóa làm tăng vị ngọt
SVTH: Đỗ Nguyễn Nam Hoa Trang 58
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Ở đây lượng acid citric cho vào mới dùng để phối trộn với nguyên liệu sau khi cô đặc cùng
với lượng đường cố định chưa bổ sung pectin nên cần lấy lượng acid citric cho vào tạo pH thấp.
Trong thực tế mẫu 1,2 ,5 được đánh giá thấp về mức độ ưa thích.Qua bảng cảm quan ở trên
nên ta chọn thí nghiệm 4 với pH= 2,87 thích hợp môi trường tạo cấu trúc cho mứt, màu sắc đẹp
và có mùi thơm ổi so với mẩu 3.
3.6 Xác định hàm lượng pectin bổ sung
Sau khi tiến hành thí nghiệm theo sơ đồ 2.1 sản phẩm được bảo quản 3 ngày rồi sau đó được
đánh giá cảm quan theo phương pháp cho điểm.
Sau đó phép thử được tiến hành với 10 người thử và mỗi người sẽ nhận được một phiếu trả
lời kèm theo các mẫu thử và được hướng dẫn cách thức đánh giá cảm quan
Và kết quả đánh giá được tập hợp trong bảng sau:
Bảng 3.8 Kết quả tổng điểm đánh giá cảm quan
Mẫu
Người thử
1 2 3 4
1 1 4 5 2
2 2 5 4 3
3 1 3 4 3
4 2 4 5 3
5 3 5 4 3
6 2 4 5 3
7 2 5 5 2
8 2 4 5 3
9 3 3 5 3
10 2 4 5 5
Tổng 20 41 47 33
Trung bình 2.0 4.1 4.7 3.3
Bảng 3.9: Kết quả cảm quan khi thay đổi lượng pectin
SVTH: Đỗ Nguyễn Nam Hoa Trang 59
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Thí Lượng pectin pH sản phẩm Nhận xét Điểm
nghiệm
1 1 3,05 Sản phẩm đông kém 2,0
2 1,5 3,16 Sản phẩm đông 4,1
không tốt
3 2 3,32 Sản phẩm đông tốt, 4,7
bề mặt láng min
4 2,5 3,40 Sản phẩm đông 3,3
nhanh, cứng
5 4.7
4.5 4.1
4
3.5 3.3
3
2.5
Điểm TBCCTL 2
2
1.5
1
0.5
0
1 1.5 2 2.5
lượng pectin
Hình 3.3: Biểu đồ kết quả cảm quan khi thay đổi lượng pectin
Dựa vào đặc điểm cấu trúc tạo gel của mứt đông từ quá trình làm thí nghiệm, qui ước chia
thành các mức sau.
Mức 1 : Chưa đông, cấu trúc gel chưa hình thành, vẫn ở trạng thái lỏng, nhiều bọt, phân bố
không đều.
Mức 2 : Đông nhưng cấu trúc vẫn còn bỡ, mềm nhiều bọt, phân bố không đều.
Mức 3 : Cấu trúc gel tốt , đông bề mặt láng mịn, không phân pha dễ trét lên bánh mì đều.
SVTH: Đỗ Nguyễn Nam Hoa Trang 60
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Mức 4 : Đông hơi cứng, bề mặt gel láng, mịn, nhưng hơi khó trét bánh mì
Mức 5: đông cứng, bề mặt láng mịn, khó trét lên bánh mì
Dựa vào đặc điểm cấu trúc tạo gel của mứt đông có cấu trúc tương ứng mức 3 qua qúa trình làm
thí nghiệm kết quả trên cho thấy pectin sử dụng 2g cho sản phẩm có chất lượng tốt hơn cả vì cấu
trúc gel tốt, đông, bề mặt láng mịn, không phân pha dễ trét lên bánh mì đều, màu sắc đẹp và mùi
thơm ổi.
3.7 Xác định chế độ thanh trùng
Sản phẩm mứt ổi đông có lượng đường cao không chỉ tăng độ ngọt độ dinh dưỡng mà còn có
tác dụng bảo quản. vì vậy có nhiều loại mứt quả xong khi nấu xong không cần thanh trùng, thanh
trùngchỉ diệt nấm men nấm mốc trên bề mặt sản phẩm vì vậy thí nghiệm chọn nhiệt độ thanh
trùng là 90oC – công thức thanh trùng thăm dò. Các bước thiết lập công thức thanh trùng được
thực hiện theo mục 2.4.7 và kết quả thu được:
Bảng 3.10 Nhiệt độ thiết bị, tâm hộp và hệ số chuyển đổi K A của chế độ thanh trùng hiện
tại
Nhiệt độ Nhiệt độ
Thời gian KA
thiết bị tâm hộp
0 40 40 0.00219
3 45.5 40.5 0.00234
6 72 42.5 0.00316
9 76 44.9 0.00457
12 82 48.6 0.00813
15 90 53.7 0.0178
18 90 58.8 0.0389
21 90 63.9 0.085
24 90 68.1 0.162
27 84 72.6 0.323
SVTH: Đỗ Nguyễn Nam Hoa Trang 61
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
30 73.5 73.7 0.38
33 66.7 72.8 0.331
36 62 71.3 0.284
39 58.9 69.4 0.1995
42 55.9 67.3 0/144
45 52.3 65 0.1
48 48.9 62.9 0.072
51 45.8 60 0.0464
2,204944
∑ KA
Thời gian hiệu quả thực tế Att :
A tt =U . ∑ K A =3 . 2,2662=6.614832
Thời gian hiệu quả cần thiết AC:( tra bảng thanh trùng tính sẵn)
AC=10 phút quy ước
Sau khi có được kết quả thời gian hiệu quả thực tế của chế độ thanh trùng hiện tại ta sẽ so
sánh với thời gian hiệu cần thiết và thấy rằng chế độ thanh trùng hiện tại còn thiếu, cần phải hiệu
chỉnh bằng cách tăng thêm thời gian giữ nhiệt để đạt mức cần thiết. Việc hiệu chỉnh chế độ thanh
trùng đươc thực hiện như sau:
Vẽ đồ thị gia nhiệt của thiết bị, tâm hộp và hệ số chuyển đổi K A trên nền kẻ ô ly như hình
3.4. Sau đó tính diện tích giới hạn bởi đường cong hệ số chuyển đổi K A bằng cách đếm số ô
vuông trên hình. Kết quả ta đếm được 7 ô vuông lớn.
Vì thời gian hiệu quả cần thiết là 10 phút quy ước lớn gấp 1.51 lần so với hiệu quả thực tế (10
: 6.61432) cho nên ta sẽ vẽ lại đường cong KA sao cho phần diện tích giới hạn bởi đường cong KA
và trục hoành có diện tích lớn gấp 1.51 lần so với diện tích cũ, tức là 11 ô vuông lớn.
Tuy nhiên cần lưu ý là đồ thị mới được vẽ sao cho có dạng tương tự đồ thị cũ, nghĩa là nhánh
trái của đồ thị mới trùng với nhánh trái đồ thị cũ nhưng ở đỉnh đồ thị sẽ cao hơn một chút; nhánh
phải của đồ thị mới thì vẽ song song với đồ thị cũ; điểm kết thúc của nhánh trái và bắt đầu của
SVTH: Đỗ Nguyễn Nam Hoa Trang 62
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
nhánh phải được vẽ sao cho đảm bảo diện tích giới hạn bởi đường cong là 11.51 ô vuông lớn (có
thể lớn hơn 11 ô một chút).
Từ đường cong KA mới sẽ suy ra được các điểm nhiệt độ mới của tâm hộp bằng cách tra bảng
hoặc giống lên trên đồ thị. Đồ thị biểu diễn nhiệt độ tâm hộp cũng vẽ trùng khớp với đồ thị cũ
nhưng kéo dài thêm thời gian nâng nhiệt. Khoảng cách giữa đường gia nhiệt mới và cũ là khoảng
thời gian cần giữ nhiệt của thiết bị thanh trùng.
Dựa vào hình 3.4, ta xác định được thời gian cần giữ nhiệt thêm của thiết bị thanh trùng là 5
phút .
Hình 3.4:Đồ thị hiệu chỉnh công thức thanh trùng
Và công thanh trùng mới là :
15−15−25
90o C
Để kiểm tra tính đúng đắn của công thanh trùng mới thiết lập ta tiến hành tương tự và kết quả
thu được ở bảng
Bảng 3.11 Nhiệt độ thiết bị, tâm hộp và hệ số chuyển đổi KA của chế độ thanh trùng mới
hiệu chỉnh
SVTH: Đỗ Nguyễn Nam Hoa Trang 63
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Nhiệt độ Nhiệt độ
Thời gian KA’
thiết bị ‘ tâm hộp ‘
SVTH: Đỗ Nguyễn Nam Hoa Trang 64
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
0 40 40 0.00219
3 45.5 40.5 0.00234
6 72 42.5 0.00316
9 76 44.9 0.00457
12 82 48.6 0.00813
15 90 53.7 0.0178
18 90 58.8 0.0389
21 90 63.9 0.085
24 90 68.1 0.162
27 84 72.6 0.323
30 84.7 76.5 0.589
33 79.5 77.6 0.691
36 75.8 76.8 0.617
39 71.2 74.3 0.4169
42 66.9 70.9 0.2511
45 62.3 67.3 0.1584
48 48.9 64.4 0.1
51 78.9 61.7 0.0602
54 54.8 58 0.0341
3.56479
∑ KA
Thời gian hiệu quả thực tế Att :
A tt =U . ∑ K A =3 . 3.56479=10.69437
Thời gian hiệu quả cần thiết AC:( tra bảng thanh trùng tính sẵn)
SVTH: Đỗ Nguyễn Nam Hoa Trang 65
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
AC=10 phút quy ước
Như vậy sau khi hiệu chỉnh ta có thời gian hiệu quả thực tế (A tt ) của chế độ thanh trùng mới
là 10.69437 phút quy ước 10 phút quy ước một chút, để đảm bảo độ vô trùng cần thiết khi
có những sai sót nhỏ trong quá trình thanh trùng.
15−15−25
Cho nên ta quyết định chọn công thức cho chế độ thanh trùng mới.
90o C
3.8 Sơ bộ đánh giá chất lượng sản phẩm
Sản phẩm được đánh giá cảm quan bằng phương pháp cho điểm theo TCVN 3215:1979 với 10
người cảm quan để sơ bộ đánh giá chất lượng sản phẩm. Kết quả cho điểm của sản phẩm được
trình bày ở bảng
Bảng 3.12 Điểm đánh giá cảm quan của sản phẩm mứt ổi đông
Chỉ tiêu chất lượng
Điểm các thành
Trạng thái cấu
viên Mùi Vị Màu sắc
trúc
1 4 5 4 3
2 4 4 3 4
3 4 3 4 5
4 4 4 4 3
5 4 4 4 4
6 3 4 5 4
7 4 3 3 5
8 4 4 4 4
9 3 3 4 4
10 4 4 3 3
Tổng số điểm 38 38 38 39
Điểm trung bình
chưa có trọng 3.8 3.8 3.8 3.9
lượng
Hệ số quan trọng 0.7 0.8 1.0 1.5
Điểm có trọng
2.66 3.04 3.8 5.85
lượng
Điểm chung 15.35
SVTH: Đỗ Nguyễn Nam Hoa Trang 66
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Dựa vào bảng phân hạng sản phẩm thực phẩm của TCVN 3215:1979 thì sản phẩm mứt ổi đông
đạt loại khá với điểm chung đạt 15.35 và mỗi chỉ tiêu quan trọng đều có điểm trung bình chưa có
trọng lượng 3.8.
Hình 3.4: sản phẩm mứt ổi đông
3.9 Hoạch toán sơ bộ giá thành sản phẩm:
Sơ bộ tính toán giá thành cho 1 hộp sản phẩm mứt ổi đông như sau:
Bảng: Hoạch tính sơ bộ giá thành sản phẩm:
Nguyên vật liệu Số lượng Đơn giá Thành tiền
Ổi 200g 20000/kg 4000
Đường 200g 21000/kg 4000
Acid citric 1,6g 29000/kg 46,4
Pectin 2g 50000/kg 75
Lọ thủy tinh 1 5000/lọ 5000
Chi phí khác 5000
(điện, nước, nhân
công, khấu hao tài
sản..)
Tổng cộng 18121.4
SVTH: Đỗ Nguyễn Nam Hoa Trang 67
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Từ bảng trên cho thấy để chế biến sơ bộ 1 hộp sản phẩm mứ ổi đông thì chi phí sơ bộ là
18121.4 vnđ. Nếu đưa vào sản xuất với quy mô lớn thì có thể giảm chi phí mua nguyên vật liệu
do mua số lượng lớn thì giá thành sản phẩm có thể thấp hơn.
SVTH: Đỗ Nguyễn Nam Hoa Trang 68
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
CHƯƠNG IV: KẾT LUẬN VÀ KIẾN NGHỊ
4.1 Kết luận
Dựa vào những kết quả thu được của quá trình thử nghiệm chế biến mứt ổi đông cho phép ta
có kết luận sau đây:
Để thu được hiệu suất chà cao nhất ta tiến ta chần 90 oC trong thời gian 5 phút thì ta có
hiệu suất thu hồi dịch quả là cao nhất.
Tỷ lệ phối chế:
Thành phần Hàm lượng (g) Hàm lượng (%)
Ổi 200 49.55
Đường 200 49.55
Pectin 2 0.5
Acid citric 1.6 0.4
15−15−25
Công thức thanh trùng o
90 C
Trong đó 15 phút gia nhiệt
15 phút giữ nhiệt
25 phút hạ nhiệt
Nhiệt độ thanh trùng 90oC
Qua phân tích thành phần hóa học, vi sinh vật trong sản phẩm sau một tháng bảo ôn ta
nhận thấy sản phẩm có chất lượng tốt và đảm bảo vệ sinh an toàn thực phẩm và có thể
bảo quản ở điều kiện bình thường.
Qua đánh giá cảm quan của các bạn thì đây là một sản phẩm loại khá nó đáp ứng các đòi
hỏi khắc khe của người tiêu dùng nhưng vẫn còn một số vấn đề cần giải quyết.
Đã xây dựng được quy trình công nghệ sản xuất thử sản phẫm mứt ổi đông:
SVTH: Đỗ Nguyễn Nam Hoa Trang 69
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Ổi xá lỵ
Lựa chọn
Nước Rửa
Xử lý, cắt nhỏ Cắt nhỏ 2x3cm
Chần 90oC trong 5 phút
2g Pectin
Chà
200g Đường,
Nước Ngâm Phối trộn
1,6g acid citric
Gia nhiệt 85oC trong 20 phút
Lọ thủy tinh Rót lọ
Thanh trùng 15−15−25
o
90 C
Làm nguội
Jam ổi
Sơ đồ 2.1 Quy trình sản xuất thử
SVTH: Đỗ Nguyễn Nam Hoa Trang 70
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
4.2 Kiến nghị
Sau 3 tháng thực hiện đồ án tại phòng thí nghiệm công nghệ - Khoa công nghệ thực phẩm
trường Đại Học Kỹ Thuật Công Nghệ Tp.Hồ Chí Minh, do thời gian nghiên cứu có hạn cho nên
còn một số thông số của quá trình chưa được khảo sát, nếu có điều kiện cần nghiên cứu thêm vấn
đề sau:
Để thanh trùng, dưới tác dụng của nhiệt độ cao thì các thành phần hóa học của nguyên liệu
ban đầu bị biến đổi, vì vậy cần nghiên cứu sâu hơn về sự biến đổi của các thành phần trong sản
phầm khi thanh trùng.
Để đảm bảo độ vô trùng cần thiết cho sản phẩm ta dùng t o=90oC để thanh trùng, dưới tác
dụng của nhiệt độ cao thì các thành phần hóa học của nguyên liệu ban đầu bị biến đổi, vì vậy cần
nghiên cứu sâu hơn về sự biến đổi của các thành phần trong sản phầm khi thanh trùng.
SVTH: Đỗ Nguyễn Nam Hoa Trang 71
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
TÀI LIỆU THAM KHẢO
[1.] Đống Thị Anh Đào (2011). Kỹ thuật bao bì thực phẩm. NXB Đại Học Quốc Gia TP Hồ Chí
Minh.
[2.] Đỗ Ngọc An, Huỳnh Lý, Ngô Bích Nga, Nguyễn Văn Trung (1973). Cây ăn quả nhiệt đới.
NXB khoa học kỹ thuật HN
[3.] Hà Duyên Tư (2006). Kỹ thuật phân tích cảm quan thực phẩm. NXB Khoa Học Và Kỹ
Thuật.
[4.] Lê Ngọc Tú (2000). Hóa sinh công nghiệp, NXB Khoa học - Kỹ Thuật,
[5.] Ngô Thị Hồng Thư (1989). Kiểm nghiệm thực phẩm bằng phương pháp cảm quan. NXB Đại
Học Quốc Gia TP Hồ Chí Minh.
[6.] Nguyễn Trọng Cẩn, Nguyễn Lệ Hà (2001). Công nghệ sản xuất đồ hộp rau quả. Đại học
Nha Trang.
[7.] Nguyễn Trọng Cẩn, Nguyễn Lệ Hà (2009). Nguyên lý sản xuất đồ hộp thực phẩm. NXB
Khoa Học Và Kỹ Thuật.
[8.] Tôn Nữ Minh Nguyệt (2010). Bài giảng Công nghệ chế biến rau trái
[9.] Trần Bích Lam (2006). Thí nghiệm phân tích thực phẩm. NXB Đại Học Quốc Gia TP Hồ
Chí Minh.
[10.] Trần Bích Lam, Tôn Nữ Minh Nguyệt, Đinh Trần Nhật Thu (2009). Thí nghiệm hóa sinh
thực phẩm, Nhà xuất bản Đại Học Quốc Gia TP. HCM
[11.] Tiêu chuẩn quốc gia. TCVN 3215:1979. Hà Nội 2008.
[12.] TS. Nguyễn Ngọc Ẩn (1978). Kỹ thuật trồng và chăm sóc vườn cây. NXB Nông nghiệp
[13.] Võ Văn Chi (1978). Phân loại thực vật. NXB ĐH, Hà Nội.
[14.] Vũ Công Hậu (1980). Trồng cây ăn quả ở Việt Nam. NXB Nông Nghiệp,Tp. HCM
SVTH: Đỗ Nguyễn Nam Hoa Trang 72
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
PHỤ LỤC
Phụ lục 1: Kết quả phân tích ANOVA so sánh tỷ lệ đường bổ sung
Analysis Summary
Dependent variable: DIEM
Factor: MAU
Number of observations: 50
Number of levels: 5
The StatAdvisor
---------------
This procedure performs a one-way analysis of variance for DIEM.
It constructs various tests and graphs to compare the mean values of
DIEM for the 5 different levels of MAU. The F-test in the ANOVA table
will test whether there are any significant differences amongst the
means. If there are, the Multiple Range Tests will tell you which
means are significantly different from which others. If you are
worried about the presence of outliers, choose the Kruskal-Wallis Test
which compares medians instead of means. The various plots will help
you judge the practical significance of the results, as well as allow
you to look for possible violations of the assumptions underlying the
analysis of variance.
ANOVA Table for DIEM by MAU
Analysis of Variance
-----------------------------------------------------------------------------
Source Sum of Squares Df Mean Square F-Ratio P-Value
-----------------------------------------------------------------------------
Between groups 38.8 4 9.7 18.42 0.0000
SVTH: Đỗ Nguyễn Nam Hoa Trang 73
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Within groups 23.7 45 0.526667
-----------------------------------------------------------------------------
Total (Corr.) 62.5 49
The StatAdvisor
---------------
The ANOVA table decomposes the variance of DIEM into two
components: a between-group component and a within-group component.
The F-ratio, which in this case equals 18.4177, is a ratio of the
between-group estimate to the within-group estimate. Since the
P-value of the F-test is less than 0.05, there is a statistically
significant difference between the mean DIEM from one level of MAU to
another at the 95.0% confidence level. To determine which means are
significantly different from which others, select Multiple Range Tests
from the list of Tabular Options.
Table of Means for DIEM by MAU
with 95.0 percent LSD intervals
--------------------------------------------------------------------------------
Stnd. error
MAU Count Mean (pooled s) Lower limit Upper limit
--------------------------------------------------------------------------------
1 10 1.6 0.229492 1.27316 1.92684
2 10 2.4 0.229492 2.07316 2.72684
3 10 4.2 0.229492 3.87316 4.52684
4 10 3.4 0.229492 3.07316 3.72684
5 10 2.9 0.229492 2.57316 3.22684
--------------------------------------------------------------------------------
Total 50 2.9
The StatAdvisor
---------------
SVTH: Đỗ Nguyễn Nam Hoa Trang 74
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
This table shows the mean DIEM for each level of MAU. It also
shows the standard error of each mean, which is a measure of its
sampling variability. The standard error is formed by dividing the
pooled standard deviation by the square root of the number of
observations at each level. The table also displays an interval
around each mean. The intervals currently displayed are based on
Fisher's least significant difference (LSD) procedure. They are
constructed in such a way that if two means are the same, their
intervals will overlap 95.0% of the time. You can display the
intervals graphically by selecting Means Plot from the list of
Graphical Options. In the Multiple Range Tests, these intervals are
used to determine which means are significantly different from which
others.
Multiple Range Tests for DIEM by MAU
--------------------------------------------------------------------------------
Method: 95.0 percent LSD
MAU Count Mean Homogeneous Groups
--------------------------------------------------------------------------------
1 10 1.6 X
2 10 2.4 X
5 10 2.9 XX
4 10 3.4 X
3 10 4.2 X
--------------------------------------------------------------------------------
Contrast Difference +/- Limits
--------------------------------------------------------------------------------
1-2 *-0.8 0.653681
1-3 *-2.6 0.653681
1-4 *-1.8 0.653681
1-5 *-1.3 0.653681
2-3 *-1.8 0.653681
2-4 *-1.0 0.653681
SVTH: Đỗ Nguyễn Nam Hoa Trang 75
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
2-5 -0.5 0.653681
3-4 *0.8 0.653681
3-5 *1.3 0.653681
4-5 0.5 0.653681
--------------------------------------------------------------------------------
* denotes a statistically significant difference.
The StatAdvisor
---------------
This table applies a multiple comparison procedure to determine
which means are significantly different from which others. The bottom
half of the output shows the estimated difference between each pair of
means. An asterisk has been placed next to 8 pairs, indicating that
these pairs show statistically significant differences at the 95.0%
confidence level. At the top of the page, 4 homogenous groups are
identified using columns of X's. Within each column, the levels
containing X's form a group of means within which there are no
statistically significant differences. The method currently being
used to discriminate among the means is Fisher's least significant
difference (LSD) procedure. With this method, there is a 5.0% risk of
calling each pair of means significantly different when the actual
difference equals 0.
SVTH: Đỗ Nguyễn Nam Hoa Trang 76
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
Phụ lục 2: Kết quả phân tích ANOVA so sánh tỷ lệ acid citric bổ sung
Analysis Summary
Dependent variable: DIEM
Factor: MAU
Number of observations: 50
Number of levels: 5
The StatAdvisor
---------------
This procedure performs a one-way analysis of variance for DIEM.
It constructs various tests and graphs to compare the mean values of
DIEM for the 5 different levels of MAU. The F-test in the ANOVA table
will test whether there are any significant differences amongst the
means. If there are, the Multiple Range Tests will tell you which
means are significantly different from which others. If you are
worried about the presence of outliers, choose the Kruskal-Wallis Test
which compares medians instead of means. The various plots will help
you judge the practical significance of the results, as well as allow
you to look for possible violations of the assumptions underlying the
analysis of variance.
ANOVA Table for DIEM by MAU
Analysis of Variance
-----------------------------------------------------------------------------
Source Sum of Squares Df Mean Square F-Ratio P-Value
-----------------------------------------------------------------------------
Between groups 30.68 4 7.67 14.03 0.0000
Within groups 24.6 45 0.546667
-----------------------------------------------------------------------------
Total (Corr.) 55.28 49
SVTH: Đỗ Nguyễn Nam Hoa Trang 77
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
The StatAdvisor
---------------
The ANOVA table decomposes the variance of DIEM into two
components: a between-group component and a within-group component.
The F-ratio, which in this case equals 14.0305, is a ratio of the
between-group estimate to the within-group estimate. Since the
P-value of the F-test is less than 0.05, there is a statistically
significant difference between the mean DIEM from one level of MAU to
another at the 95.0% confidence level. To determine which means are
significantly different from which others, select Multiple Range Tests
from the list of Tabular Options.
Table of Means for DIEM by MAU
with 95.0 percent LSD intervals
--------------------------------------------------------------------------------
Stnd. error
MAU Count Mean (pooled s) Lower limit Upper limit
--------------------------------------------------------------------------------
1 10 2.0 0.233809 1.66701 2.33299
2 10 2.5 0.233809 2.16701 2.83299
3 10 4.1 0.233809 3.76701 4.43299
4 10 3.8 0.233809 3.46701 4.13299
5 10 3.2 0.233809 2.86701 3.53299
--------------------------------------------------------------------------------
Total 50 3.12
The StatAdvisor
---------------
This table shows the mean DIEM for each level of MAU. It also
shows the standard error of each mean, which is a measure of its
sampling variability. The standard error is formed by dividing the
SVTH: Đỗ Nguyễn Nam Hoa Trang 78
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
pooled standard deviation by the square root of the number of
observations at each level. The table also displays an interval
around each mean. The intervals currently displayed are based on
Fisher's least significant difference (LSD) procedure. They are
constructed in such a way that if two means are the same, their
intervals will overlap 95.0% of the time. You can display the
intervals graphically by selecting Means Plot from the list of
Graphical Options. In the Multiple Range Tests, these intervals are
used to determine which means are significantly different from which
others.
Multiple Range Tests for DIEM by MAU
--------------------------------------------------------------------------------
Method: 95.0 percent LSD
MAU Count Mean Homogeneous Groups
--------------------------------------------------------------------------------
1 10 2.0 X
2 10 2.5 X
5 10 3.2 X
4 10 3.8 XX
3 10 4.1 X
--------------------------------------------------------------------------------
Contrast Difference +/- Limits
--------------------------------------------------------------------------------
1-2 -0.5 0.665977
1-3 *-2.1 0.665977
1-4 *-1.8 0.665977
1-5 *-1.2 0.665977
2-3 *-1.6 0.665977
2-4 *-1.3 0.665977
2-5 *-0.7 0.665977
3-4 0.3 0.665977
3-5 *0.9 0.665977
SVTH: Đỗ Nguyễn Nam Hoa Trang 79
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
4-5 0.6 0.665977
--------------------------------------------------------------------------------
* denotes a statistically significant difference.
The StatAdvisor
---------------
This table applies a multiple comparison procedure to determine
which means are significantly different from which others. The bottom
half of the output shows the estimated difference between each pair of
means. An asterisk has been placed next to 7 pairs, indicating that
these pairs show statistically significant differences at the 95.0%
confidence level. At the top of the page, 3 homogenous groups are
identified using columns of X's. Within each column, the levels
containing X's form a group of means within which there are no
statistically significant differences. The method currently being
used to discriminate among the means is Fisher's least significant
difference (LSD) procedure. With this method, there is a 5.0% risk of
calling each pair of means significantly different when the actual
difference equals 0.
Phụ lục 3: Kết quả phân tích ANOVA so sánh tỷ lệ pectin bổ sung
Analysis Summary
Dependent variable: DIEM
Factor: MAU
Number of observations: 40
Number of levels: 4
The StatAdvisor
---------------
SVTH: Đỗ Nguyễn Nam Hoa Trang 80
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
This procedure performs a one-way analysis of variance for DIEM.
It constructs various tests and graphs to compare the mean values of
DIEM for the 4 different levels of MAU. The F-test in the ANOVA table
will test whether there are any significant differences amongst the
means. If there are, the Multiple Range Tests will tell you which
means are significantly different from which others. If you are
worried about the presence of outliers, choose the Kruskal-Wallis Test
which compares medians instead of means. The various plots will help
you judge the practical significance of the results, as well as allow
you to look for possible violations of the assumptions underlying the
analysis of variance.
ANOVA Table for DIEM by MAU
Analysis of Variance
-----------------------------------------------------------------------------
Source Sum of Squares Df Mean Square F-Ratio P-Value
-----------------------------------------------------------------------------
Between groups 45.475 3 15.1583 33.07 0.0000
Within groups 16.5 36 0.458333
-----------------------------------------------------------------------------
Total (Corr.) 61.975 39
The StatAdvisor
---------------
The ANOVA table decomposes the variance of DIEM into two
components: a between-group component and a within-group component.
The F-ratio, which in this case equals 33.0727, is a ratio of the
between-group estimate to the within-group estimate. Since the
P-value of the F-test is less than 0.05, there is a statistically
significant difference between the mean DIEM from one level of MAU to
another at the 95.0% confidence level. To determine which means are
significantly different from which others, select Multiple Range Tests
SVTH: Đỗ Nguyễn Nam Hoa Trang 81
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
from the list of Tabular Options.
Table of Means for DIEM by MAU
with 95.0 percent LSD intervals
--------------------------------------------------------------------------------
Stnd. error
MAU Count Mean (pooled s) Lower limit Upper limit
--------------------------------------------------------------------------------
1 10 2.0 0.214087 1.69298 2.30702
2 10 4.1 0.214087 3.79298 4.40702
3 10 4.8 0.214087 4.49298 5.10702
4 10 3.0 0.214087 2.69298 3.30702
--------------------------------------------------------------------------------
Total 40 3.475
The StatAdvisor
---------------
This table shows the mean DIEM for each level of MAU. It also
shows the standard error of each mean, which is a measure of its
sampling variability. The standard error is formed by dividing the
pooled standard deviation by the square root of the number of
observations at each level. The table also displays an interval
around each mean. The intervals currently displayed are based on
Fisher's least significant difference (LSD) procedure. They are
constructed in such a way that if two means are the same, their
intervals will overlap 95.0% of the time. You can display the
intervals graphically by selecting Means Plot from the list of
Graphical Options. In the Multiple Range Tests, these intervals are
used to determine which means are significantly different from which
others.
Multiple Range Tests for DIEM by MAU
SVTH: Đỗ Nguyễn Nam Hoa Trang 82
Nghiên cứu quy trình sản xuất mứt ổi đông GVHD: T.S Nguyễn Lệ Hà
--------------------------------------------------------------------------------
Method: 95.0 percent LSD
MAU Count Mean Homogeneous Groups
--------------------------------------------------------------------------------
1 10 2.0 X
4 10 3.0 X
2 10 4.1 X
3 10 4.8 X
--------------------------------------------------------------------------------
Contrast Difference +/- Limits
--------------------------------------------------------------------------------
1-2 *-2.1 0.614037
1-3 *-2.8 0.614037
1-4 *-1.0 0.614037
2-3 *-0.7 0.614037
2-4 *1.1 0.614037
3-4 *1.8 0.614037
--------------------------------------------------------------------------------
* denotes a statistically significant difference.
The StatAdvisor
---------------
This table applies a multiple comparison procedure to determine
which means are significantly different from which others. The bottom
half of the output shows the estimated difference between each pair of
means. An asterisk has been placed next to 6 pairs, indicating that
these pairs show statistically significant differences at the 95.0%
confidence level. At the top of the page, 4 homogenous groups are
identified using columns of X's. Within each column, the levels
containing X's form a group of means within which there are no
statistically significant differences. The method currently being
used to discriminate among the means is Fisher's least significant
SVTH: Đỗ Nguyễn Nam Hoa Trang 83
You might also like
- CHIÊN - Báo CáoDocument21 pagesCHIÊN - Báo CáoDung PhamNo ratings yet
- Tiểu luận VANG DỨADocument15 pagesTiểu luận VANG DỨATrịnh HuyềnNo ratings yet
- Quy trình chế biến thanh long sấy dẻoDocument22 pagesQuy trình chế biến thanh long sấy dẻoTrúcNo ratings yet
- Tempeh Miso ShoyuDocument64 pagesTempeh Miso ShoyuThu ThủyNo ratings yet
- ĐỘC TỐ HỌC THỰC PHẨMDocument18 pagesĐỘC TỐ HỌC THỰC PHẨMHậu HuỳnhNo ratings yet
- (123doc) - Do-Hop-Xoai-Nuoc-DuongDocument63 pages(123doc) - Do-Hop-Xoai-Nuoc-DuongMỹ LyNo ratings yet
- Bai Luan Cuoi Ky-CNCBRQ-HC18TP-Cao Dang KhoaDocument32 pagesBai Luan Cuoi Ky-CNCBRQ-HC18TP-Cao Dang KhoaKhoa CaoNo ratings yet
- Thực tập sấy nhóm 2Document27 pagesThực tập sấy nhóm 2Quang TríNo ratings yet
- Ruou Vang Bup GiamDocument20 pagesRuou Vang Bup GiamHưng TrịnhNo ratings yet
- NẤM MEN VÀ NẤM MỐCDocument37 pagesNẤM MEN VÀ NẤM MỐCNgân ChâuNo ratings yet
- Quá Trình Ép ĐùnDocument32 pagesQuá Trình Ép ĐùnNgọc NguyễnNo ratings yet
- Quy trình sản xuất sữa bắpDocument10 pagesQuy trình sản xuất sữa bắpNgọc NguyễnNo ratings yet
- TỔNG QUAN VỀ SẢN PHẨM GIÒ LỤADocument10 pagesTỔNG QUAN VỀ SẢN PHẨM GIÒ LỤAminh_ly_2No ratings yet
- (123doc) - Thiet-Ke-Phan-Xuong-San-Xuat-Nuoc-Chanh-Day-Nang-Suat-30-Tan-San-PhamngayDocument58 pages(123doc) - Thiet-Ke-Phan-Xuong-San-Xuat-Nuoc-Chanh-Day-Nang-Suat-30-Tan-San-PhamngayUranium PlatinumNo ratings yet
- Bài phúc trình báo cáo thực tập công nghệ len men thực phẩmDocument17 pagesBài phúc trình báo cáo thực tập công nghệ len men thực phẩmTran Thi Thao Nguyen B1703279No ratings yet
- Sản Xuất Nước Giải Khát Lên Men Từ Dịch Chiết Đài Hoa Bụp Giấm Hibiscus Sabdariffa L.Document55 pagesSản Xuất Nước Giải Khát Lên Men Từ Dịch Chiết Đài Hoa Bụp Giấm Hibiscus Sabdariffa L.Tieu Ngoc LyNo ratings yet
- Bài Thu Ho CHDocument10 pagesBài Thu Ho CHnguyenthianhthu12a4qt100% (1)
- TINH BỘT NGHỆDocument5 pagesTINH BỘT NGHỆThùy DươngNo ratings yet
- CHƯƠNG 1,2 Rau quả muối chuaDocument19 pagesCHƯƠNG 1,2 Rau quả muối chuaDuy PhạmNo ratings yet
- Banh Bong Lan Cong Nghiep 2312Document59 pagesBanh Bong Lan Cong Nghiep 2312ThanhNo ratings yet
- đồ hộp nước quảDocument29 pagesđồ hộp nước quảVương NguyênNo ratings yet
- Báo cáo thực tập CNCB trà, cà phê, chocolateDocument106 pagesBáo cáo thực tập CNCB trà, cà phê, chocolateHuỳnh Điệp TrầnNo ratings yet
- Tieu Luan Bao Quan Thuc PhamDocument47 pagesTieu Luan Bao Quan Thuc PhamnhanluanproNo ratings yet
- Quy Trinh Dinh Tinh SalmonellaDocument54 pagesQuy Trinh Dinh Tinh SalmonellaHoàng AnNo ratings yet
- Quá Trình Lên Men MalolacticDocument4 pagesQuá Trình Lên Men MalolacticHoàng Ngọc LinhNo ratings yet
- Tiểu Luận an Toàn Thực PhẩmDocument30 pagesTiểu Luận an Toàn Thực PhẩmPhạm Huyền TrangNo ratings yet
- Bánh PH NG TômDocument2 pagesBánh PH NG Tômtrandainghia1987No ratings yet
- BÀI 1 Lương TH CDocument23 pagesBÀI 1 Lương TH CCao Trọng HiếuNo ratings yet
- Báo Cáo Lên Men - Nhóm 4 - K18 ĐT - L P CDocument14 pagesBáo Cáo Lên Men - Nhóm 4 - K18 ĐT - L P CUyen NguyenNo ratings yet
- Chế Biến Rau QuảDocument13 pagesChế Biến Rau QuảNhật GiangNo ratings yet
- ĐỒ ÁN - Tổng Quan Công Nghệ Sản Xuất NECTAR XOÀIDocument36 pagesĐỒ ÁN - Tổng Quan Công Nghệ Sản Xuất NECTAR XOÀITrang LưuNo ratings yet
- HACCP-VSATTP-nhóm 14Document60 pagesHACCP-VSATTP-nhóm 14Tai PhuongNo ratings yet
- Cong Nghe Do Hop Thuc PhamDocument62 pagesCong Nghe Do Hop Thuc PhamlthcNo ratings yet
- Đề Cương Sinh Tố Từ Múi Mít - Nguyễn Thị Mai LinhDocument28 pagesĐề Cương Sinh Tố Từ Múi Mít - Nguyễn Thị Mai LinhTrịnh Phương ThảoNo ratings yet
- ĐỀ CƯƠNG KẸO DẺODocument11 pagesĐỀ CƯƠNG KẸO DẺOHồ Trúc LinhNo ratings yet
- Bao Quan Rau Qua Bang Hoa ChatDocument31 pagesBao Quan Rau Qua Bang Hoa ChatLan NhiNo ratings yet
- CÔNG NGHỆ SẢN XUẤT BÁNH MACARONDocument34 pagesCÔNG NGHỆ SẢN XUẤT BÁNH MACARONNguyễn GiangNo ratings yet
- Đề cương Bồ câu đóng hộpDocument17 pagesĐề cương Bồ câu đóng hộpHồ Đắc HuânNo ratings yet
- Bài 3 Tôm Đông L NHDocument20 pagesBài 3 Tôm Đông L NHThanh HùngNo ratings yet
- Chương IDocument49 pagesChương IĐặngThảo100% (1)
- QUY TRÌNH SẢN XUẤT CHÈ XANHDocument24 pagesQUY TRÌNH SẢN XUẤT CHÈ XANHÁnh Linh100% (1)
- Giáo Trình Sản Xuất Quả Ngâm Nước Đường Đống Hộp - MĐ03 - Chế Biến Rau Quả - 957694Document102 pagesGiáo Trình Sản Xuất Quả Ngâm Nước Đường Đống Hộp - MĐ03 - Chế Biến Rau Quả - 957694Chi Lan Tôn NữNo ratings yet
- CNVSTP - T 3 - Nhóm T6C1 PDFDocument31 pagesCNVSTP - T 3 - Nhóm T6C1 PDFĐinh Đăng TườngNo ratings yet
- chế biến nghiên cứu mứt bí đỏDocument59 pageschế biến nghiên cứu mứt bí đỏHoàng NguyễnNo ratings yet
- Chương 3 Quy Trình Sản XuấtDocument15 pagesChương 3 Quy Trình Sản XuấtDao Thi Lan AnhNo ratings yet
- Tổng Quan Về Cà ChuaDocument5 pagesTổng Quan Về Cà ChuaKiều DiễmNo ratings yet
- Luận văn - Cách thức nghiên cứu chất màu họ Anthocyanin - 686571Document68 pagesLuận văn - Cách thức nghiên cứu chất màu họ Anthocyanin - 686571Nguyen Thi Thuy Duong B1606703100% (1)
- (New) Nước Thanh Long-Khóm. INDocument92 pages(New) Nước Thanh Long-Khóm. INThuấn NguyễnNo ratings yet
- 2.1.3.Men giống: Hình. Mối quan hệ cộng sinh của hai chủng vi khuẩn trong sữa chuaDocument3 pages2.1.3.Men giống: Hình. Mối quan hệ cộng sinh của hai chủng vi khuẩn trong sữa chuaNguyen Hong Xuan MaiNo ratings yet
- Quy trình sản xuất tương cà quy mô công nghiệpDocument14 pagesQuy trình sản xuất tương cà quy mô công nghiệpNguyễn Thị Thanh TuyếtNo ratings yet
- Báo Cáo Thực Hành: Môn Học: Công Nghệ Chế Biến Sữa Và Các Sản Phẩm Từ SữaDocument10 pagesBáo Cáo Thực Hành: Môn Học: Công Nghệ Chế Biến Sữa Và Các Sản Phẩm Từ SữaNguyễn Phương Lệ HàNo ratings yet
- ĐỒ ÁN - Công nghệ sản xuất đồ hộp thịt bò hầmDocument48 pagesĐỒ ÁN - Công nghệ sản xuất đồ hộp thịt bò hầmthuong hoangNo ratings yet
- Quy trình sản xuất cà phêDocument9 pagesQuy trình sản xuất cà phêviet nguyenNo ratings yet
- Lên Men TempehDocument16 pagesLên Men TempehHải Linh VũNo ratings yet
- Bài Báo Cáo Quá Trình Công Nghệ Sản Xuất Phô Mai MozzarellaDocument16 pagesBài Báo Cáo Quá Trình Công Nghệ Sản Xuất Phô Mai MozzarellaGia My LưuNo ratings yet
- bí đao và các sản phẩm từ bí đaoDocument36 pagesbí đao và các sản phẩm từ bí đaoQuach Bao Linh100% (1)
- Nhom 27 Loc MembraneDocument31 pagesNhom 27 Loc MembranePham KhoaNo ratings yet
- Quy trình sản xuất chuốiDocument3 pagesQuy trình sản xuất chuốiTrung NguyenNo ratings yet
- Quy trình sản xuất nước giải khát có gas theo GMPDocument7 pagesQuy trình sản xuất nước giải khát có gas theo GMPThanh ThảoNo ratings yet
- Đề Tài Snack Khoai TâyDocument20 pagesĐề Tài Snack Khoai TâyTieu Ngoc LyNo ratings yet