Professional Documents
Culture Documents
Bài 3.Trạng thái dừng và cơ chế phản ứng phức tạp
Bài 3.Trạng thái dừng và cơ chế phản ứng phức tạp
Uploaded by
Hương Nguyễn0 ratings0% found this document useful (0 votes)
3 views10 pagesOriginal Title
Bài 3.Trạng thái dừng và cơ chế phản ứng phức tạp - Copy
Copyright
© © All Rights Reserved
Available Formats
PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
3 views10 pagesBài 3.Trạng thái dừng và cơ chế phản ứng phức tạp
Bài 3.Trạng thái dừng và cơ chế phản ứng phức tạp
Uploaded by
Hương NguyễnCopyright:
© All Rights Reserved
Available Formats
Download as PDF, TXT or read online from Scribd
You are on page 1of 10
CƠ CHẾ PHẢN ỨNG
VÀ CÁC PHƯƠNG PHÁP GẦN ĐÚNG
1. Khái niệm và một số lưu ý về cơ chế phản ứng
2. Phương pháp giả trạng thái dừng
CƠ CHẾ PHẢN ỨNG
• Là chuỗi các bước sơ cấp được giả định của phản ứng
• chỉ là một giả thuyết để giải thích những hiện tượng quan sát
được. Không thể chứng minh là đúng, mà chỉ có thể nói là có phù
hợp với dữ kiện thực nghiệm hay không.
• Các bước sơ cấp thường có các chất trung gian, hiếm khi có thể
cô lập hay thậm chí là phát hiện được.
• mọi chất trung gian xuất hiện phải bị mất đi trong một bước nào
đó, để cuối cùng nó không có mặt trong phương trình phản ứng
tổng
• phải phù hợp với hệ thức tỉ lượng trong phương trình phản ứng
tổng (tức là nếu ta cộng các bước trong cơ chế lại thì phải được
tổng là phương trình phản ứng đã cân bằng)
PHƯƠNG PHÁP XẤP XỈ TRẠNG THÁI DỪNG
(QUASI-) STEADY-STATE APPROXIMATION
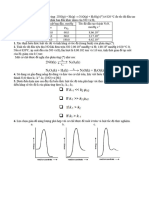
Sau giai đoạn cảm ứng
(induction period), nồng độ các
chất trung gian rất nhỏ và gần
như không thay đổi trong phần
lớn quá trình phản ứng.
𝑑[𝐼]
≈0
𝑑𝑡
Example 1: SN1 mechanism
Kết quả thực nghiệm:
– Tốc độ không phụ thuộc
nồng độ nucleophile X-
(v=k[Ph2CHCl])
– Tốc độ không phụ thuộc
bản chất nucleophile
d[Ph 2 CH ]
va v a v b k a [Ph 2CHCl] k a [Ph 2CH ][Cl ] k b [[Ph 2CH ][X ] 0
dt
k a [Ph 2CHCl] k a [Ph 2CH ][Cl ] k b [Ph 2CH ][X ] [Ph 2CH ] k a [Cl ] k b [X ]
k a [Ph 2CHCl]
[Ph 2CH ]
k a [Cl ] k b [X ]
d[Ph 2CH ] k a [Ph 2CHCl]
v k b [Ph 2CH ][X ] k b
[X ]
dt k a [Cl ] k b [X ]
Nếu kb>>k-a: v k k a [Ph 2CHCl] [X ] k [Ph CHCl]
b a 2
k b [X ]
RÚT PHƯƠNG TRÌNH TỐC ĐỘ TỪ CƠ CHẾ PHẢN ỨNG
BẰNG CÁCH DÙNG PHƯƠNG PHÁP TRẠNG THÁI DỪNG
DERIVE A REACTION RATE LAW ACCORDING TO A GIVEN
MECHANISM USING STEADY STATE APPROXIMATION
1. Xác định các chất trung gian (có trong cơ chế nhưng không có
trong phản ứng tổng)
2. Viết biểu thức tốc độ biến đổi nồng độ từng chất trung gian
trong tất cả các bước và cho bằng 0
3. Rút ra biểu thức tính nồng độ chất trung gian theo tác chất và
sản phẩm.
4. Viết biểu thức tốc độ phản ứng theo một trong các tác chất/sản
phẩm. Nên chọn chất xuất hiện trong ít bước trung gian để biểu
thức được đơn giản.
Example 2:Lindemann-Hinshelwood
mechanism
• cyclo-C3H6→CH3CH=CH2 v = k[cyclo-C3H6]
EXERCISE 1
• Derive the rate law for the decomposition of
ozone in the reaction 2 O3(g)→3 O2(g) on the
basis of the (incomplete) mechanism:
O3→O2 + O ka
O2 + O→O3 ka ′
O + O3→O2 + O2 kb
Answer: 2kakb[O3]2/(ka′[O2] + kb[O3])]
EXERCISE 2
ẢNH HƯỞNG CỦA NHIỆT ĐỘ ĐẾN
(HẰNG SỐ) TỐC ĐỘ PHẢN ỨNG
• Phương trình Arrhenius:
Ví dụ
You might also like
- Bài 3.Trạng Thái Dừng Và Cơ Chế Phản Ứng Phức TạpDocument10 pagesBài 3.Trạng Thái Dừng Và Cơ Chế Phản Ứng Phức TạpLe Nguyen Thu HaNo ratings yet
- Bài 3.Trạng thái dừng và cơ chế phản ứng phức tạpDocument10 pagesBài 3.Trạng thái dừng và cơ chế phản ứng phức tạp22130010No ratings yet
- Slide TH Hóa Phân Tích 1Document49 pagesSlide TH Hóa Phân Tích 102 - Trương Tấn Anh D20No ratings yet
- Chương 2 - P1Document28 pagesChương 2 - P1Linh Nguyễn Thị HồngNo ratings yet
- Chương 5 - Tốc Độ Phản Ứng Hóa HọcDocument39 pagesChương 5 - Tốc Độ Phản Ứng Hóa Họcphuckaduc1234No ratings yet
- Bài 1.Động học phản ứng một chiều đơn giản (Autosaved)Document15 pagesBài 1.Động học phản ứng một chiều đơn giản (Autosaved)Dao Khanh ChiNo ratings yet
- Chuong 1 Mở đầuDocument52 pagesChuong 1 Mở đầuThảo NguyênNo ratings yet
- động học hoa lýDocument96 pagesđộng học hoa lýtomNo ratings yet
- 1. Bài 1.Động học phản ứng một chiều đơn giản (Autosaved) -đã gộpDocument66 pages1. Bài 1.Động học phản ứng một chiều đơn giản (Autosaved) -đã gộp22128058No ratings yet
- Ôn tập ĐHXTDocument30 pagesÔn tập ĐHXThungdiep27012002No ratings yet
- Chương 5 - Tốc Độ Phản Ứng Hóa HọcDocument39 pagesChương 5 - Tốc Độ Phản Ứng Hóa HọcDŨNG TRƯƠNG ANHNo ratings yet
- Gioi Thieu Va Dong Hoa HocDocument53 pagesGioi Thieu Va Dong Hoa HocPhước Tạ BìnhNo ratings yet
- Chuyên đề Nhiệt động lực học 2018 PDFDocument40 pagesChuyên đề Nhiệt động lực học 2018 PDFduy Nguyễn100% (1)
- BG Hoa Huu Co 2 C. ThoDocument101 pagesBG Hoa Huu Co 2 C. ThoLọ LemNo ratings yet
- Bai 4. Xúc TácDocument23 pagesBai 4. Xúc TácHương NguyễnNo ratings yet
- Câu Hỏi Ôn Tập Ktra Tt Hóa Lý Dược 2023-2024Document17 pagesCâu Hỏi Ôn Tập Ktra Tt Hóa Lý Dược 2023-2024Quỳnh Anh Phạm NguyễnNo ratings yet
- Một số phương pháp tách trong kiểm nghiệmDocument46 pagesMột số phương pháp tách trong kiểm nghiệmLương VămNo ratings yet
- Bài 5- Phương pháp phân tích thể tích-bản inDocument53 pagesBài 5- Phương pháp phân tích thể tích-bản inHuy 11 Nguyễn ĐứcNo ratings yet
- Thí Nghiệm Hóa Lý Kỹ ThuậtDocument38 pagesThí Nghiệm Hóa Lý Kỹ Thuậtmai anhNo ratings yet
- Chuong 8 Dan Xuat HalogenDocument39 pagesChuong 8 Dan Xuat HalogenMinh Quang TrầnNo ratings yet
- Ch1. Nguyên Lý 1 NĐLHDocument38 pagesCh1. Nguyên Lý 1 NĐLHTHUẬN NGUYỄN MINHNo ratings yet
- Thực Hanh Phan Tich Hoa Lý Chuẩn Độ Điện ThếDocument29 pagesThực Hanh Phan Tich Hoa Lý Chuẩn Độ Điện ThếLam NguyễnNo ratings yet
- Chương 8. Động Hoá Học: 1 Genaral Chemistry Ths. Nguy N Th HoàiDocument28 pagesChương 8. Động Hoá Học: 1 Genaral Chemistry Ths. Nguy N Th HoàiSong NgưNo ratings yet
- 06-Toc Do Phan UngDocument12 pages06-Toc Do Phan UngVĩnh Tân TrầnNo ratings yet
- Ôn Thi HoáDocument69 pagesÔn Thi Hoáminhkhoivts1No ratings yet
- 6. Tính toán trong dược động họcDocument13 pages6. Tính toán trong dược động họcPhan LinhNo ratings yet
- Chương 2Document21 pagesChương 2Trần Minh ĐạtNo ratings yet
- 04.1-Hieu Ung Nhiet Cua Cac Qua Trinh Hoa Hoc 211Document30 pages04.1-Hieu Ung Nhiet Cua Cac Qua Trinh Hoa Hoc 211Vĩnh Tân TrầnNo ratings yet
- Hóa Lí - 2023-TNLDocument365 pagesHóa Lí - 2023-TNLthành táNo ratings yet
- Bai Giang CH3220 Chương 8 Dan Xuat Halogen PDFDocument44 pagesBai Giang CH3220 Chương 8 Dan Xuat Halogen PDFMinhAnhNo ratings yet
- Chương 2Document21 pagesChương 2ngoaitienkhongcogiNo ratings yet
- Động hóa học - XuânDocument63 pagesĐộng hóa học - XuânThư PhạmNo ratings yet
- Nhom QG - Buoi 2 - HSDocument4 pagesNhom QG - Buoi 2 - HSKiên TrầnNo ratings yet
- CHUONG 4 Phần 4A Tốc Độ Pu Và Định Luật Tốc ĐộDocument33 pagesCHUONG 4 Phần 4A Tốc Độ Pu Và Định Luật Tốc Độ22130010No ratings yet
- Chuong 3-Bai 8Document34 pagesChuong 3-Bai 8Ha Khanh Linh NguyenNo ratings yet
- Chapter 1 PDFDocument30 pagesChapter 1 PDFBùi Quang HuyNo ratings yet
- Phương pháp mô phỏng CFDDocument12 pages Phương pháp mô phỏng CFDDuy Dương PhướcNo ratings yet
- Chap 1Document84 pagesChap 1Van Nguyen Phuong NganNo ratings yet
- 2. HIỆU ỨNG - CƠ CHẾ PHẢN ỨNGDocument55 pages2. HIỆU ỨNG - CƠ CHẾ PHẢN ỨNGTâm Phạm CôngNo ratings yet
- ĐỀ CƯƠNG LÝ SINHDocument14 pagesĐỀ CƯƠNG LÝ SINHTruc NguyenNo ratings yet
- Chuong 1.3 Co Che Phan Ung - 45Document27 pagesChuong 1.3 Co Che Phan Ung - 45TrucNo ratings yet
- (123doc) - Bai-Tap-Nong-Do-Dung-Va-Co-Che-Phan-UngDocument26 pages(123doc) - Bai-Tap-Nong-Do-Dung-Va-Co-Che-Phan-UngKiên PhạmNo ratings yet
- Bai 4. Xúc TácDocument23 pagesBai 4. Xúc TácHoàng Nhựt NguyễnNo ratings yet
- Ôn Tập Thi Cuối Kỳ - Hóa Đại Cương - Updated 19-12-2023Document70 pagesÔn Tập Thi Cuối Kỳ - Hóa Đại Cương - Updated 19-12-2023quang.trandanh05No ratings yet
- Mô Hình Hóa Nhóm 7 2Document48 pagesMô Hình Hóa Nhóm 7 2SANG TRƯƠNG TẤNNo ratings yet
- 1 THUYẾT CẤU TẠO HÓA HỌCDocument13 pages1 THUYẾT CẤU TẠO HÓA HỌChpktcn0% (1)
- Bu I 3 Hóa Lý 1Document31 pagesBu I 3 Hóa Lý 1Nhàn Trần ThịNo ratings yet
- Ky 1. Hoa Dai Cuong Vo Co - 123.new Da NenDocument121 pagesKy 1. Hoa Dai Cuong Vo Co - 123.new Da NenThai NgoNo ratings yet
- Cau Hoi On TapDocument13 pagesCau Hoi On TapNanNo ratings yet
- Nhiet DongDocument35 pagesNhiet DongĐức Cường NguyễnNo ratings yet
- Bài Giảng Chương 2 - Động Học Của Phản Ứng - fullDocument64 pagesBài Giảng Chương 2 - Động Học Của Phản Ứng - fullThành NguyễnNo ratings yet
- Bai Giang Hoa Hoc PFIEV-Chuong 5Document18 pagesBai Giang Hoa Hoc PFIEV-Chuong 5Sang TrầnNo ratings yet
- BÀI 5 PHẢN ỨNG BẬC 1Document3 pagesBÀI 5 PHẢN ỨNG BẬC 1Nguyễn Đức Tín100% (1)
- Co Che Phan UngDocument22 pagesCo Che Phan UngKaka Ricardo100% (2)
- Chương 4 - Động Hóa HọcDocument33 pagesChương 4 - Động Hóa Họcnguyenhophutrong03No ratings yet
- Chuong 1aDocument47 pagesChuong 1aPhương LanNo ratings yet
- CHƯƠNG 4+5 Nhiệt động hóa họcDocument68 pagesCHƯƠNG 4+5 Nhiệt động hóa họctonvu0310No ratings yet
- CHE 203-Hoa Huu Co - 2021F-Lecture Slides-7Document32 pagesCHE 203-Hoa Huu Co - 2021F-Lecture Slides-7Minh Nhật Võ ThịNo ratings yet
- Chương 1 - 2020Document49 pagesChương 1 - 2020Trần Thuý QuỳnhNo ratings yet
- Quá trình truyền khối hoàn chỉnh lý thuyêtDocument10 pagesQuá trình truyền khối hoàn chỉnh lý thuyêtHương NguyễnNo ratings yet
- 04CLC - UTExMC - Nhóm 1 - Nguyễn Cẩm Hương + 22128032Document1 page04CLC - UTExMC - Nhóm 1 - Nguyễn Cẩm Hương + 22128032Hương NguyễnNo ratings yet
- Cách tổ chức kiểm tra TN Hóa Phân Tích (chính thức)Document5 pagesCách tổ chức kiểm tra TN Hóa Phân Tích (chính thức)Hương NguyễnNo ratings yet
- BAOCAOBAI4HOALYDocument9 pagesBAOCAOBAI4HOALYHương NguyễnNo ratings yet
- Bài chuẩn bị 7Document4 pagesBài chuẩn bị 7Hương NguyễnNo ratings yet
- Bài 3 WWWDocument19 pagesBài 3 WWWHương NguyễnNo ratings yet
- Báo Cáo Hóa Lí Bài 4 - DDDDDDDDDDDocument7 pagesBáo Cáo Hóa Lí Bài 4 - DDDDDDDDDDHương NguyễnNo ratings yet
- Bai 4. Xúc TácDocument23 pagesBai 4. Xúc TácHương NguyễnNo ratings yet
- Báo Cáo TN Update 2023Document47 pagesBáo Cáo TN Update 2023Hương NguyễnNo ratings yet