Professional Documents
Culture Documents
Báo Cáo Bài 1 Và 2 Nhóm 2 1
Uploaded by
Lê PhươnggOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Báo Cáo Bài 1 Và 2 Nhóm 2 1
Uploaded by
Lê PhươnggCopyright:
Available Formats
Nhóm: 2 Lưu Thị Huỳnh Mai 2004180034
Nguyễn Ngọc Phương Anh 2004180284
BÁO CÁO BÀI 1 VÀ 2
1. Sơ đồ quá trình thực nghiệm:
Pha 250 mL dd H2C2O4 0,1N Hiệu chuẩn NaOH Pha 1 lít HCl 0,1N
Pha 1 lít NaOH 0,1N bằng H2C2O4 Pha 1 lít CH3COOH 0,1N
(từ không màu sang hồng nhạt)
Chuẩn độ với 10mL HCl, 10mL CH3COOH bằng dd chuẩn
NaOH bằng phương pháp máy pH, chuẩn độ độ dẫn, máy chuẩn
độ độ dẫn tự động.
2. Kiểm tra nồng độ của NaOH:
- Khối lượng H2C2O4.2H2O: 1,5929 (g) Vbđm = 250 (mL)
- Nồng độ H2C2O4: 0,1005(N)
- Thể tích H2C2O4: 5 (mL)
- Kết quả phân tích:
Lần thí nghiệm 1 2 3
VNaOH (mL) 5 5 5,1
CNaOH (N) 0,1005 0,1005 0,09853
Nồng độ NaOH
0,09984 ± 0,02521
(có kèm sai số theo Student với độ tin cây p = 95(%))
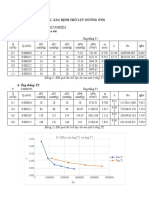
3. Số liệu thực nghiệm phương pháp độ dẫn:
Dung dịch HCl:
VNaOH Độ dẫn VNaOH Độ dẫn VNaOH Độ dẫn
Stt Stt Stt
(mL) (mS hoặc µS) (mL) (mS hoặc µS) (mL) (mS hoặc µS)
1. 0 2780 11. 9,5 861 21. 17,1 2060
2. 1 2560 12. 9,7 886 22. 18,1 2190
3. 2 2320 13. 9,9 896 23. 19,1 2330
4. 3 2090 14. 10,1 924 24. 20,1 2470
5. 4 1862 15. 11,1 1041 25. 21,1 2600
6. 5 1643 16. 12,1 1193 26. 22,1 2730
7. 6 1422 17. 13,1 1491 27. 23,1 2860
8. 7 1209 18. 14,1 1641 28.
9. 8 998 19. 15,1 1781 29.
10. 9 795 20. 16,1 1918 30.
Kết quả đồ thị:
Nhóm: 2 Lưu Thị Huỳnh Mai 2004180034
Nguyễn Ngọc Phương Anh 2004180284
V(NaOH) mL
3500
3000
2500
2000
1500
1000
500
0
0 5 10 15 20 25
Đồ thị phương pháp độ dẫn
Kết quả Vtđ: Vtđ = 9 mL
Dung dịch CH3COOH:
VNaOH Độ dẫn VNaOH Độ dẫn VNaOH Độ dẫn
Stt Stt Stt
(mL) (mS hoặc µS) (mL) (mS hoặc µS) (mL) (mS hoặc µS)
1. 0 139,8 11. 6 348 21. 8,9 490
2. 1 125,6 12. 6,5 372 22. 9,1 500
3. 2 152,6 13. 7 396 23. 9,3 509
4. 2,5 174,4 14. 7,5 419 24. 9,5 518
5. 3 201 15. 7,7 431 25. 9,7 526
6. 3,5 225 16. 7,9 441 26. 9,9 539
7. 4 249 17. 8,1 449 27. 10,1 550
8. 4,5 277 18. 8,3 458 28. 10,3 559
9. 5 299 19. 8,5 472 29. 10,5 568
10. 5,5 323 20. 8,7 479 30. 10,7 578
31. 10,9 590 41. 16,9 1329
32. 11,1 607 42. 17,9 1446
33. 11,3 636 43. 18,9 1569
34. 11,5 651 44. 19,9 1699
35. 11,7 681 45. 20,9 1809
36. 11,9 706 46. 21,9 2040
37. 12,9 832 47. 22,9 2150
38. 13,9 967 48. 23,9 2280
39. 14,9 1082 49.
40. 15,9 1205 50.
Kết quả đồ thị:
Nhóm: 2 Lưu Thị Huỳnh Mai 2004180034
Nguyễn Ngọc Phương Anh 2004180284
V(NaOH) mL
2500
2000
1500
1000
500
0
0 5 10 15 20 25 30
Đồ thị phương pháp độ dẫn
Kết quả Vtđ: Vtđ = 10,7 (mL)
4. Số liệu thực nghiệm phương pháp chuẩn độ bằng máy pH:
Dung dịch HCl:
VNaOH VNaOH VNaOH
Stt pH Stt pH Stt pH
(mL) (mL) (mL)
1. 0 2,11 11. 9,5 9,954 21. 17,1 11,307
2. 1 2,180 12. 9,7 9,999 22. 18,1 11,351
3. 2 2,239 13. 9,9 10,124 23. 19,1 11,393
4. 3 2,389 14. 10,1 10,499 24. 20,1 11,428
5. 4 2,487 15. 11,1 10,685 25. 21,1 11,461
6. 5 2,617 16. 12,1 10,965 26. 22,1 11,493
7. 6 2,789 17. 13,1 11,060 27. 23,1
8. 7 3,083 18. 14,1 11,135 28.
9. 8 4,860 19. 15,1 11,204 29.
10. 9 9,848 20. 16,1 11,261 30.
Kết quả đồ thị:
Nhóm: 2 Lưu Thị Huỳnh Mai 2004180034
Nguyễn Ngọc Phương Anh 2004180284
V(NaOH) mL
14
12
10
0
0 5 10 15 20 25
Đồ thị phương pháp chuẩn độ bằng máy pH
Kết quả Vtđ: Vtđ = 9 (mL)
Dung dịch CH3COOH:
VNaOH VNaOH VNaOH
Stt pH Stt pH Stt pH
(mL) (mL) (mL)
1. 0 3,36 11. 6 4,69 21. 8,9 5,29
2. 1 3,72 12. 6,5 4,77 22. 9,1 5,34
3. 2 3,97 13. 7 4,86 23. 9,3 5,41
4. 2,5 4,08 14. 7,5 4,94 24. 9,5 5,48
5. 3 4,19 15. 7,7 5 25. 9,7 5,55
6. 3,5 4,28 16. 7,9 5,04 26. 9,9 5,69
7. 4 2,37 17. 8,1 5,08 27. 10,1 5,83
8. 4,5 4,46 18. 8,3 5,11 28. 10,3 5,97
9. 5 4,53 19. 8,5 5,18 29. 10,5 6,17
10. 5,5 4,61 20. 8,7 5,23 30. 10,7 6,54
31. 10,9 8,06 41. 16,9 10,98
32. 11,1 9,17 42. 17,9 11,06
33. 11,3 9,64 43. 18,9 11,13
34. 11,5 9,79 44. 19,9 11,20
35. 11,7 9,97 45. 20,9 11,26
36. 11,9 10,08 46. 21,9 11,33
37. 12,9 10,42 47. 22,9 11,37
38. 13,9 10,64 48. 23,9 11,41
39. 14,9 10,78 49.
40. 15,9 10,89 50.
Kết quả đồ thị:
Nhóm: 2 Lưu Thị Huỳnh Mai 2004180034
Nguyễn Ngọc Phương Anh 2004180284
V(NaOH) mL
12
10
0
0 5 10 15 20 25 30
Đồ thị phương pháp chuẩn độ bằng máy pH
Kết quả Vtđ: Vtđ = 10,1 (mL)
5. Số liệu thực nghiệm phương pháp chuẩn độ bằng máy chuẩn độ điện thế:
Dung dịch HCl:
Dung dịch CH3COOH:
VNaOH VNaOH VNaOH
Stt pH Stt pH Stt pH
(mL) (mL) (mL)
1. 0,01 2,98 11. 5,12 9,16 21. 8,15 10,43
2. 1,01 3,22 12. 5,14 9,25 22. 9,05 10,56
3. 2,00 3,85 13. 5,26 9,37 23. 9,89 10,63
4. 3,10 4,16 14. 5,42 9,49 24. 9,98 10,66
5. 4,10 4,38 15. 5,66 9,64 25.
6. 5,02 6,65 16. 5,86 9,87 26.
7. 5,03 8,92 17. 6,13 9,87 27.
8. 5,04 8,96 18. 6,77 10,06 28.
9. 5,06 8,98 19. 7,12 10,27 29.
10. 5,10 9,01 20. 7,89 10,34 30.
Kết quả đồ thị:
Nhóm: 2 Lưu Thị Huỳnh Mai 2004180034
Nguyễn Ngọc Phương Anh 2004180284
12
10
0
0 2 4 6 8 10 12
250
200
150
100
50
0
0 2 4 6 8 10 12
Đồ thị phương pháp độ dẫn
Kết quả Vtđ:
6. Kiểm tra mẫu thử:
- Nồng độ NaOH (có kèm sai số theo Student với độ tin cậy p = 95(%)): 0,09984 ±
0,02521.
- Thể tích xác định: 10 (mL)
- Kết quả phân tích HCl:
Máy chuẩn
Máy chuẩn
độ điện thế
Phương pháp Độ dẫn Máy pH độ điện thế
(KQ trên
(đồ thị)
máy)
VNaOH (mL) 9 9
CN (HCl) 0,08986 0,08986
P (g/L) 3,279744 3,279744
- Kết quả phân tích CH3COOH:
Nhóm: 2 Lưu Thị Huỳnh Mai 2004180034
Nguyễn Ngọc Phương Anh 2004180284
Máy chuẩn
Máy chuẩn
độ điện thế
Phương pháp Độ dẫn Máy pH độ điện thế
(KQ trên
(đồ thị)
máy)
VNaOH (mL) 10,7 10,1
CN (CH3COOH) 0,1068 0,1008
P (g/L) 6,409728 6,050304
Nhận xét:
Từ kết quả trên có thể thấy, độ chua có trong HCl ít hơn trong CH 3COOH và khi đo
bằng hai phương pháp máy pH và độ dẫn thì ở HCL sai số không đáng kể gần như bằng nhau.
Còn ở CH3COOH thì có sai số nhưng không quá lớn không vượt quá 5%.
7. Trả lời câu hỏi:
a. Nêu cấu tạo điện cực đo độ dẫn và điện cực pH?
- Đầu điện cực: cho phép thâm nhập vào nước, đất,... và đo trực tiếp đo độ dẫn điện của
các dung dịch.
- Thân điện cực: tùy thuộc vào từng model mà thân điện cực đo độ dẫn điện được làm
bằng chất liệu: thủy tinh, nhựa,...
b. Tại sao phải hiệu chuẩn pH, cách thực hiện?
- Vì hiệu chuẩn pH giúp khắc phục được những thay đổi đặc điểm hiện tại của máy đo
pH và cảm biến pH mà nó đang sử dụng. Sau 1 thời gian sử dụng, kể cả đối với các điện cực
ổn định nhất cũng sẽ diễn ra sự thay đổi của bởi sự lão hóa và phủ điện cực pH. Việc thực
hiện hiệu chuẩn sẽ bù cho mọi sự khác biệt trong các hành vi của điện cực giữa lý thuyết và
thực tế.
- Hiệu chuẩn máy đo pH giúp giảm trôi, tăng độ chính xác cho các phép đo. Một vấn đề
rất phổ biến khi thực hiện phép đo với máy đo pH là đo lường trôi dạt làm giảm tính chính
xác của kết quả đo. Nếu không thực hiện hiệu chuẩn cho máy đo pH, máy sẽ thực hiện các
phép đo không đúng và trả về kết quả không chính xác.
- Hiệu chuẩn giúp giải quyết các vấn đề liên quan đến sự khác biệt về mẫu. Các mẫu
của cùng 1 chất có thể có các đặc tính khác nhau; việc hiệu chuẩn máy đo pH sẽ ngăn ngừa
các vấn đề như: sự khác biệt về cường độ ion, các vấn đề khác liên quan đến màng tế bào,...
c. Các lưu ý khi sử dụng điện cực pH:
- Nếu máy thực hiện hiệu chuẩn thành công: máy sẽ hiện kết quả hiệu chuẩn và hướng
dẫn bước tiếp theo (nếu cần).
- Nếu máy không thể nhận biết được pH của dung dịch đệm, nó sẽ thông báo lỗi
“WRONG” trên màn hình.
- Đối với các máy đo pH có hiệu chuẩn tự động máy sẽ tự nhận diện được loại pH phù
hợp và điều chỉnh đồng hồ đúng với giá trị pH của dung dịch đệm; đối với các máy hiệu
chuẩn bằng tay, bạn hãy dùng tua vít đính kèm máy để vặn đồng hồ về đúng giá trị pH của
dung dịch đệm.
d. Tại sao hiệu chuẩn NaOH, nếu nguyên tắc, viết PTPU quá trình hiệu chuẩn:
- Hiệu chuẩn NaOH, vì dung dịch NaOH không bền trong không khí, nồng độ bị thay
đổi theo thời gian do hấp thụ khí CO2 tạo ra Na2CO3.
Nhóm: 2 Lưu Thị Huỳnh Mai 2004180034
Nguyễn Ngọc Phương Anh 2004180284
- Nguyên tắc: axit H2C2O4 có các hằng số phân li như sau: K1 = 5,9.10 , K2 = 6,4.10-5 rất
-2
gần nhau nên khi chuẩn độ NaOH bằng H2C2O4 sẽ trung hòa cả 2 nấc.
- PTPU:
2NaOH + H2C2O4 Na2C2O4 + 2H2O
You might also like
- Bài 11 Nhóm 3Document5 pagesBài 11 Nhóm 3Dang Bich Duyen B2101408No ratings yet
- Baibaocao 3Document6 pagesBaibaocao 3Thư MaiNo ratings yet
- Bài 24-hptDocument6 pagesBài 24-hptLê Vũ Khánh QuyênNo ratings yet
- Bài 3-thhptncDocument6 pagesBài 3-thhptncThư MaiNo ratings yet
- Bài 3Document5 pagesBài 3Dương HoàngNo ratings yet
- Báo Cáo Hóa LýDocument15 pagesBáo Cáo Hóa Lýhuytvg163No ratings yet
- Bai 3-Báo Cáo Thực Hành Phân Tích Điện HóaDocument8 pagesBai 3-Báo Cáo Thực Hành Phân Tích Điện Hóadee deeNo ratings yet
- HoaptDocument4 pagesHoaptĐỗ Quang MinhNo ratings yet
- Baibaocao 4Document9 pagesBaibaocao 4Thư MaiNo ratings yet
- BÁO CÁO TH KTTP - BÀI LỌC KHUNG BẢNDocument8 pagesBÁO CÁO TH KTTP - BÀI LỌC KHUNG BẢNVũ Phan Ánh VyNo ratings yet
- BÀI 3 Hóa Phân Tích Nâng CaoDocument9 pagesBÀI 3 Hóa Phân Tích Nâng CaoTrang Ú NguyễnNo ratings yet
- HPT - Bài Tập Chuẩn Độ - Đáp ÁnDocument10 pagesHPT - Bài Tập Chuẩn Độ - Đáp ÁnNguyễn Bùi Giang0% (1)
- BÁO CÁO THÍ NGHIỆM SỨC BỀN- VẬT LIỆU XÂY DỰNGDocument45 pagesBÁO CÁO THÍ NGHIỆM SỨC BỀN- VẬT LIỆU XÂY DỰNGAnh KiệtNo ratings yet
- So Lieu Dau VaoDocument4 pagesSo Lieu Dau VaoNgoVietCuongNo ratings yet
- IR SpectrumDocument19 pagesIR SpectrumlinhhdngNo ratings yet
- Bai 3 P KaDocument3 pagesBai 3 P KaQuỳnh Trần Thúy0% (1)
- Báo Cáo TH C Hành Hóa Phân Tích 2 Bài 4Document6 pagesBáo Cáo TH C Hành Hóa Phân Tích 2 Bài 4Phạm Thị Ngọc BíchNo ratings yet
- Deadline Acid BazoDocument18 pagesDeadline Acid BazoMai Gia ThảoNo ratings yet
- 14 - Trần Thị Len - 646926 - 01-03 - PTTP - Bài 03Document3 pages14 - Trần Thị Len - 646926 - 01-03 - PTTP - Bài 03Linh NguyễnNo ratings yet
- Đề Thi Cuối KỳDocument2 pagesĐề Thi Cuối KỳQuốc KhánhNo ratings yet
- Báo Cáo Bài TH y Phân Ester-Nhóm 4-Lo3Document6 pagesBáo Cáo Bài TH y Phân Ester-Nhóm 4-Lo3Võ Nhật ThanhNo ratings yet
- Thủy Phân Ester Bằng Phương Pháp Đo Độ Dẫn: Họ tên các thành viên trong nhómDocument5 pagesThủy Phân Ester Bằng Phương Pháp Đo Độ Dẫn: Họ tên các thành viên trong nhómMinh Hiếu CaoNo ratings yet
- BÁO CÁO THÍ NGHIỆM BÀI 7Document13 pagesBÁO CÁO THÍ NGHIỆM BÀI 7phamtrucvy2003No ratings yet
- Xác Định Pka Bằng Phương Pháp Đường Cong Chuẩn Độ: Tiểu nhóm: 14 - 21DS111 Thành viên: Nguyễn Văn Hoàng DũngDocument25 pagesXác Định Pka Bằng Phương Pháp Đường Cong Chuẩn Độ: Tiểu nhóm: 14 - 21DS111 Thành viên: Nguyễn Văn Hoàng DũngHoàng DũngNo ratings yet
- Bài 4Document12 pagesBài 4Bùi Thành PhướcNo ratings yet
- PHÚC TRÌNH TRUYỀN NHIỆTDocument15 pagesPHÚC TRÌNH TRUYỀN NHIỆTThiên Trân Võ NguyễnNo ratings yet
- ĐẠI HỌC QUỐC GIA THÀNH PHỐ HỒ CHÍ MINHDocument37 pagesĐẠI HỌC QUỐC GIA THÀNH PHỐ HỒ CHÍ MINHNguyễn Thái HoàngNo ratings yet
- Bai Tap Enzyme Vitamin HormoneDocument6 pagesBai Tap Enzyme Vitamin Hormonelinh HuynhnhatNo ratings yet
- UntitledDocument10 pagesUntitledĐào Huỳnh Tấn PhúcNo ratings yet
- Phúc trình TT. Hóa PT2 nhóm 5 chiều 4 (bài chung)Document19 pagesPhúc trình TT. Hóa PT2 nhóm 5 chiều 4 (bài chung)giaobui0310No ratings yet
- Iii. Xử Lý Kết Quả Thí NghiệmDocument15 pagesIii. Xử Lý Kết Quả Thí NghiệmTrần Thiên ThưNo ratings yet
- Bai6 21247194 DươngKhảiMinh 21247219 HuỳnhNhậtMinhNhưDocument8 pagesBai6 21247194 DươngKhảiMinh 21247219 HuỳnhNhậtMinhNhưDương MinhNo ratings yet
- Bài 3 Hóa LúDocument11 pagesBài 3 Hóa LúĐức Mạnh ĐoànNo ratings yet
- Bài số 2 - Tiểu nhóm 1 - Nhóm 4Document3 pagesBài số 2 - Tiểu nhóm 1 - Nhóm 4PHẠM VIỆT QUYÊNNo ratings yet
- Bài 2Document18 pagesBài 2ppthao1100No ratings yet
- Bài giảng Chuẩn độ kết tủa 20211105Document46 pagesBài giảng Chuẩn độ kết tủa 20211105Cá Viên Chiên0% (1)
- bảng tínhDocument4 pagesbảng tínhbiledeptrai123No ratings yet
- CUNG CẤP ĐIỆNDocument67 pagesCUNG CẤP ĐIỆNKhoa LêNo ratings yet
- Đề CDocument2 pagesĐề Csonvipli098No ratings yet
- (LinksVIP.Net) TN Cơ Lưu Chất 1 2 3B 5A 6Document10 pages(LinksVIP.Net) TN Cơ Lưu Chất 1 2 3B 5A 6Thông Nguyễn GgNo ratings yet
- BÀI 1 Truyen NhietDocument4 pagesBÀI 1 Truyen NhietHue LeNo ratings yet
- Bai3 Nhom1 TranThanhNhan NguyenThiThuyDungDocument23 pagesBai3 Nhom1 TranThanhNhan NguyenThiThuyDungThùy Dung Nguyễn ThịNo ratings yet
- Bài 5Document7 pagesBài 5Dinh Duc Huy100% (2)
- TRẦN PHƯƠNG THẢO 20190383Document13 pagesTRẦN PHƯƠNG THẢO 20190383Hiraeth JeyNo ratings yet
- Bài 6Document10 pagesBài 6thaothanhle96No ratings yet
- Ôn Thi CKDocument59 pagesÔn Thi CKduy dsfdsNo ratings yet
- Bài Tập Dựng Đường Chuẩn Và Vẽ Đồ ThịDocument8 pagesBài Tập Dựng Đường Chuẩn Và Vẽ Đồ Thịquangvinh151103No ratings yet
- BÀI TẬP THỐNG KÊ ỨNG DỤNGDocument17 pagesBÀI TẬP THỐNG KÊ ỨNG DỤNGKim LeNo ratings yet
- Bài 4 - Chưng Cất - Phần Báo CáoDocument14 pagesBài 4 - Chưng Cất - Phần Báo CáoPhan LianieNo ratings yet
- Báo Cáo Hóa Lý Bài 6 Lần 6 Nhóm 5Document16 pagesBáo Cáo Hóa Lý Bài 6 Lần 6 Nhóm 5nhiphamhoang2003No ratings yet
- Bài 3 - nhóm N.M.ThuậnDocument13 pagesBài 3 - nhóm N.M.ThuậnDinh Duc HuyNo ratings yet
- Trần Thị Thanh Trang-Đề 2-Lớp AH20A3BDocument10 pagesTrần Thị Thanh Trang-Đề 2-Lớp AH20A3BTrang TrầnNo ratings yet
- đg hấp phụ bth4Document6 pagesđg hấp phụ bth4Linh LinhNo ratings yet
- Điểm Qúa TrìnhDocument1 pageĐiểm Qúa TrìnhHải Minh Nguyễn KhoaNo ratings yet
- Báo Cáo CSĐKTĐDocument20 pagesBáo Cáo CSĐKTĐPhùng AnNo ratings yet
- Tháng Số lượng: Trung bình trượt w=3 0 0 54 54Document22 pagesTháng Số lượng: Trung bình trượt w=3 0 0 54 54Thúy Cao Ngọc ThanhNo ratings yet
- Bài tập truyền nhiệt Phần 1Document15 pagesBài tập truyền nhiệt Phần 1Phúc NguyễnNo ratings yet
- Bài tập excel 2Document6 pagesBài tập excel 2huhuhuh huhuhNo ratings yet